Изобретение относится к биохимии, в частности к применению известного антибиотика брунеомицина /стрептонигрина, 5-амино-6-(7-амино-5,8-дигидро-6-метокси-5,8-диоксохинолин-2-ил)-4-(2-гидрокси-3,4-диметоксифенил)-3-метил-пиридин-2-карбоновой кислоты/ и его известных производных общей формулы I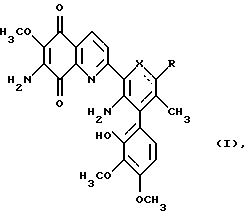
где, если 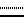 - простая связь, то Х=NH и R=O или =NН, и если
- простая связь, то Х=NH и R=O или =NН, и если 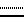 - двойная связь, то Х=N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы C(O)NHR1, где R1= Н, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил)оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибиторов NO-зависимой активации растворимой формы гуанилатциклазы (рГЦ).
- двойная связь, то Х=N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы C(O)NHR1, где R1= Н, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил)оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибиторов NO-зависимой активации растворимой формы гуанилатциклазы (рГЦ).
Изобретение может быть использовано в биохимии для изучения регуляторных эффектов оксида азота и механизма действия рГЦ.
Гуанилатциклаза /КФ 4.6.1.2. ; гуанозин-5'-трифосфат-пирофосфатлиаза (циклизующая)/ является ферментом, катализирующим биосинтез гуанозин-3', 5'-циклофосфата (цГМФ) - универсального регулятора внутриклеточного метаболизма (Hobbs, A. J. "Soluble guanylate cyclase: the forgotten sibling" Trends in Pharm. Sci. , 1997, v. l8, 12, р. 487-491 [1]). ГЦ существует в двух формах - мембранной и растворимой и играет ключевую роль в регуляции таких физиологических процессов, как сокращение и расслабление гладких мышц кровеносных сосудов и агрегация тромбоцитов. Основным эндогенным активатором рГЦ является оксид азота, который в результате взаимодействия с атомом железа гема, входящего в состав фермента, образует комплекс нитрозил-гем. Известны также соединения, способные активировать рГЦ по гем-независимому механизму: например, протопорфирин IX, ионы Mn2+, арахидоновая кислота и др.
В настоящее время для изучения возможного участия рГЦ в различных физиологических процессах применяют ингибиторы данного фермента, в частности 3,7-бис(диметиламино)фенотиазинийхлорид (метиленовый синий), 6-(фениламино)-5,8-хинолиндион (LY 83583) и 1Н-[1,2,4]-оксадиазоло[4,3-а]хиноксалин-1-он (ОДХ) [1]. Данные соединения являются ингибиторами NO-зависимой активации рГЦ и частично влияют на базальную активность фермента. Кроме того, в аэробных условиях они способствуют образованию супероксид-аниона (кроме ОДХ), а также действуют на другие биологические объекты.
Известен бис(N,N-диметиламид)азодикарбоновой кислоты (диамид) формулы II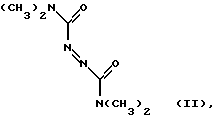
оказывающий ингибирующее действие на базальную и NО-зависимую активность рГЦ (Craven, P.A., DeRubertis, F.R. "Effects of thiol inhibition on hepatic guanylate cyclase activity. Evidence for the involvement of vicinal dithiols in the supression of basal and agoniststimulated activity" Biochim. Biophys. Acta 1978, v. 524, p. 231-244).
Основным недостатком данного соединения является низкая эффективность ингибирующего действия на рГЦ (IC50=0,5-20 мМ).
Известно ингибирование базальной активности рГЦ макроциклическими производными азофуразана, в частности циклическим тетрамером азофуразана формулы III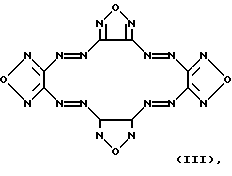
(патент РФ 2151799, кл. С 12 N 9/99, 9/88, 1999).
Данное соединение практически не влияет на гемзависимую активацию рГЦ под действием нитропруссида натрия.
Известно снижение базальной и NO-зависимой активностей рГЦ под действием ингибиторов цитохром Р-450-содержащих монооксигеназ, в частности метирапона (2-метил-1,2-бис(пиридил-3)-1-пропанона) формулы IV и 2,3,5-триметил-6-(12-гидроксидодека-5,10-диинил)-1,4-бензохинона (АА 861) формулы V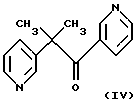
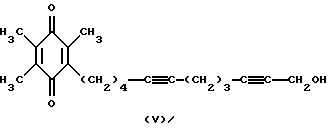
(Forstermann, U. , Alheid, U., et al. "Mechanisms of action of lipoxygenase and cytochrome P-450-mono-oxygenase inhibitors in blocking endothelium-dependent vasodilatation" Br. J. Pharm., 1988, v. 93, p. 569-578).
Недостатками данных соединений являются неспецифичность и низкая эффективность ингибирующего действия на фермент (IС50=0,1-3 мМ).
Известно применение антибиотика брунеомицина вышеуказанной общей формулы I, где X=N и R=C(O)OH, в качестве средства для лечения онкологических заболеваний (Машковский М. Д. Лекарственные средства, т. 2, Харьков, "Торсинг", 1997, стр. 470). Показано также, что данное соединение в отличие от доксорубицина оказывает слабое активирующее действие на базальную активность рГЦ (Levey, G. S. , Levey, В.A., et al. "Selective inhibition of rat and human cardiac guanylate cyclase in vitro by doxorubicin (Adriamycin): possible link to anthracycline cardiotoxicity" J. Mol. Cell. Cardiol. 1979, v. 11, 6, p. 591-599). Кроме этого известно, что производные брунеомицина общей формулы I, где R имеет указанные значения, обладают цитотоксическим действием на опухолевые клетки (Толстиков В. В., Козлова Н.В. и др. Получение амидов и эфиров антибиотика брунеомицина и изучение его цитотоксической и антиретровирусной активности. Хим-фарм. ж. 1990, т. 24, 2, с. 130-132 [7]; Tolstikov, V. V. , Holpne Kozlova, N.V., et al. "Amides of antibiotic streptonigrin and aminodicarboxylic acids or amino sugars: synthesis and biological evaluation" J. Antib. 1992, v. 45, 6, p. 1020-1025 [8]; Tolstikov, V.V., Preobrazhenskaya, M.N., et al. "Chemical modification of antibiotic streptonigrin; synthesis and properties of 2'-decarboxy-2'-aminostreptonigrin (streptonigrone-2'-imine)" J. Antib. 1992, v. 45, 6, p. 1002-1004 [9]; Miyasaka, Т., Hibino, S., et al. "Synthesis of novel streptonigrin 2-amide derivatives with 3,3'-(phenylphosphoryl)bis(l, 3-thiazolidine-2- thione)" J. Chem. Soc. , Perkin Trans. I, 1986, 3, р. 479-482 [10]; патенты Японии 61280490 (C 07 D 471/04), оп. 1985 [11]; 61280490 (C 07 D 471/04), оп. 1987 [12]).
Способность данных соединений ингибировать NО-зависимую активацию рГЦ до настоящего времени не изучена.
Наиболее близким к брунеомицину и его производным общей формулы I по действию и структуре в ряду полициклических соединений, содержащих хиноидный фрагмент, является противоопухолевый антибиотик доксорубицин (адриамицин) формулы VI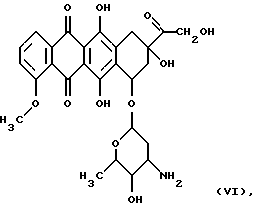
ингибирующий базальную и NO-зависимую активности рГЦ (Lehotai, D.C., Levey, В.А., et.al. "Inhibition of cardiac guanylate cyclase by doxorubicin and some of its analogs: possible relationship to cadiotoxicity" Cancer Treat. Rep. 1982, v. 66, 2, p. 311-316; Vesely, D.L., Levey, G.S., "Inhibition of nitroso chemical carcinogen activation of rat hepatic cyclase by anticancer reagent" Oncology. 1979, v. 36, 3, р. 122-126 - прототип).
Недостатком данного соединения является низкая эффективность ингибирующего действия на рГЦ (IС50=0,26-1 мМ).
Цель изобретения - поиск и выявление новых ингибиторов NO-зависимой активации рГЦ, обладающих более выраженными ингибирующими свойствами.
Указанная цель достигается применением известных соединений - брунеомицина и его производных общей формулы I, где Х и R имеют вышеуказанные значения, в качестве новых ингибиторов NO-зависимой активации рГЦ.
Согласно данному изобретению предпочтительно применение брунеомицина общей формулы I, где  - двойная связь, Х=N и R=C(O)OH, в качестве нового ингибитора NO-зависимой активации рГЦ.
- двойная связь, Х=N и R=C(O)OH, в качестве нового ингибитора NO-зависимой активации рГЦ.
Производные брунеомицина общей формулы I, где X=N и R имеет вышеуказанные значения, получены известным способом при взаимодействии соответствующих гидрокси- или аминопроизводных с брунеомицином в присутствии конденсирующего реагента (напр., 3,3'-(фенилфосфорил)бис(1,3-тиазолидин-2-тиона)) или с реакционноспособным производным брунеомицина (напр., его хлорангидридом или N-гидроксисукцинимидным эфиром) в присутствии основания в среде безводного органического растворителя (напр., ацетонитрила), при необходимости, при повышенной температуре, с последующим выделением целевого продукта в свободном виде или в виде соли [7, 8, 10-12]. Производное брунеомицина общей формулы I, где Х=NH и R=NH, было получено из амида брунеомицина известным способом, основанным на реакции Шмидта [9].
Изобретение иллюстрируется следующим примером.
Пример 1. Ингибирующее действие брунеомицина и его производных общей формулы I на NO-зависимую активацию частично очищенной рГЦ из тромбоцитов человека.
Препарат фермента получали центрифугированием (10500 g) тромбоцитов человека, выделенных из венозной крови доноров известным способом.
Активность фермента определяли по количеству образовавшегося цГМФ известным иммуноферментным способом с использованием наборов реактивов для количественного определения цГМФ АО "Биоиммуноген" (РФ).
Инкубационная смесь для определения активности (общий объем пробы 150 мкл) приготавливалась при 0-4oС и содержала 50 мМ Трис-НСl (рН 7,6), 1 мМ ГТФ, 4 мМ MgCl2, 4 мМ креатинфосфат, 20 мкг (50 ед/мг) креатинфосфокиназы, 10 мМ теофиллин и полученный ферментный препарат (10-20 мкг белка). При определении ингибирующего действия в среду инкубации вносили изучаемое соединение в виде раствора в водном диметилсульфоксиде (ДМСО). Концентрация соединения в пробе составляла 1•10-7-1•10-4 М, ДМСО - 0,2 об.%. Контрольная проба показала отсутствие влияния ДМСО в указанной концентрации на базальную активность рГЦ. Через 10 мин. в инкубационную смесь добавляли расчетное количество нитропруссида натрия (ННП) для достижения его концентрации в пробе, равной 100 мМ. Пробы инкубировали в термостате при 37oС в течение 15 минут. Реакцию останавливали перенесением проб на 2 мин в кипящую водяную баню с последующим охлаждением в водяной бане. После отделения денатурированного белка центрифугированием (10 мин при 1500 g) в полученном супернатанте определяли количество образовавшегося цГМФ вышеуказанным способом. Определение белка проводили по способу Лоури, в качестве стандарта использовали бычий сывороточный альбумин. Для оценки степени ингибирования NO-зависимой (под действием ННП) активации рГЦ соединениями общей формулы I проводили сравнение полученных данных с удельной активностью фермента в тех же условиях в отсутствие указанных веществ (фермент в 15,9 раз активировался 0,1 мМ ННП в присутствии 0,5 мМ дитиотреитола).
Брунеомицин и его производные общей формулы I в концентрации 1-100 мкМ оказывали ингибирующее действие на NO-зависимую активацию частично очищенной рГЦ из тромбоцитов человека, вызываемую ННП. Так, концентрация брунеомицина, при которой наблюдалось снижение активирующего эффекта ННП на 50% (IС50), составляла 4,2 мкМ. При этом базальная активность фермента (в отсутствие ННП) незначительно повышалась (на 20-24%). Наиболее близкий структурный аналог - доксорубицин в вышеописанных условиях ингибировал NO-зависимую активацию рГЦ на 26% в концентрации 10 мкМ.
Таким образом, брунеомицин и его производные общей формулы I являются новыми эффективными ингибиторами NO-зависимой активации рГЦ и расширяют ассортимент модуляторов активности данного фермента.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР NO-ЗАВИСИМОЙ АКТИВАЦИИ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 2001 |
|
RU2189392C1 |
| ИНГИБИТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 2001 |
|
RU2196175C2 |
| ИНГИБИТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1999 |
|
RU2151799C1 |
| ИНГИБИТОР NO-ЗАВИСИМОЙ АКТИВАЦИИ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 2001 |
|
RU2218399C2 |
| ПРОИЗВОДНЫЕ 1,4,2,5-ДИОКСАДИАЗИНА | 2001 |
|
RU2212409C1 |
| СПЕЦИФИЧЕСКИЙ РЕГУЛЯТОР АКТИВНОСТИ НУКЛЕОТИД-ЗАВИСИМЫХ ФЕРМЕНТОВ | 1997 |
|
RU2130490C1 |
| КОМПЛЕКСЫ ВКЛЮЧЕНИЯ ПРОИЗВОДНЫХ 1,2,5-ОКСАДИАЗОЛ-2-ОКСИДА С ПОЛИЦИКЛИЧЕСКИМИ ПРОИЗВОДНЫМИ ГЛЮКОПИРАНОЗЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2186782C1 |
| ДОНОР ОКСИДА АЗОТА И АКТИВАТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1998 |
|
RU2139932C1 |
| ПРОИЗВОДНЫЕ 1,2,5-ОКСАДИАЗОЛО-[3,4-D]-ПИРИДАЗИН-5,6-ДИОКСИДА В КАЧЕСТВЕ АКТИВАТОРОВ РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ И СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1997 |
|
RU2165256C2 |
| ДОНОР ОКСИДА АЗОТА, АКТИВИРУЮЩИЙ РАСТВОРИМУЮ ФОРМУ ГУАНИЛАТЦИКЛАЗЫ, ИНГИБИРУЮЩИЙ АГРЕГАЦИЮ ТРОМБОЦИТОВ И ОБЛАДАЮЩИЙ СПАЗМОЛИТИЧЕСКИМ И СОСУДОРАСШИРЯЮЩИМ ДЕЙСТВИЕМ | 2001 |
|
RU2208438C1 |
Изобретение относится к биохимии, в частности к применению известного антибиотика брунеомицина /стрептонигрина, 5-амино-6-(7-амино-5,8-дигидро-6-метокси-5,8-диоксохинолин-2-ил)-4-(2-гидрокси-3,4-диметоксифенил)-3-метилпиридин-2-карбоновой кислоты/ и его известных производных общей формулы, где, если  - простая связь, то Х=NH и R=O или =NH, и, если
- простая связь, то Х=NH и R=O или =NH, и, если  - двойная связь, то Х=N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы С(О)NHR1, где R1=H, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил) оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы (рГЦ). Изобретение может быть использовано в биохимии для изучения регуляторных эффектов оксида азота и механизма действия рГЦ. Брунеомицин и его производные общей формулы I в концентрации 1-100 мкМ оказывают ингибирующее действие на NO-зависимую активацию рГЦ из тромбоцитов человека, вызываемую нитропруссидом натрия. Концентрация брунеомицина, при которой наблюдалось снижение активирующего эффекта ННП на 50% (LC50), составляет 4,2 мкМ. Наиболее близкий структурный аналог доксорубицин в тех же условиях ингибировал активацию рГЦ на 26% в концентрации 10 мкМ. 1 з.п. ф-лы.
- двойная связь, то Х=N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы С(О)NHR1, где R1=H, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил) оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы (рГЦ). Изобретение может быть использовано в биохимии для изучения регуляторных эффектов оксида азота и механизма действия рГЦ. Брунеомицин и его производные общей формулы I в концентрации 1-100 мкМ оказывают ингибирующее действие на NO-зависимую активацию рГЦ из тромбоцитов человека, вызываемую нитропруссидом натрия. Концентрация брунеомицина, при которой наблюдалось снижение активирующего эффекта ННП на 50% (LC50), составляет 4,2 мкМ. Наиболее близкий структурный аналог доксорубицин в тех же условиях ингибировал активацию рГЦ на 26% в концентрации 10 мкМ. 1 з.п. ф-лы.
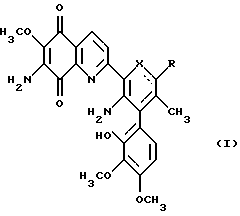
где, если 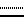 - простая связь, то Х= NH и R= = O или = NH, и, если
- простая связь, то Х= NH и R= = O или = NH, и, если 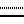 - двойная связь, то Х= N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы С(О)NHR1, где R1= H, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил)оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы.
- двойная связь, то Х= N и R - карбоксил, (низший алкил)оксикарбонил, [бис(низший алкил)амино] этоксикарбонил или группа общей формулы С(О)NHR1, где R1= H, NH2, NHC(O)NH2, NHC(S)NH2, незамещенный низший алкил, низший алкил, содержащий в качестве заместителя гидроксильную, карбоксильную или (низший алкил)оксикарбонильную группу, или β-D-гексопиранозил, и их биохимически приемлемых солей в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы.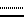 - двойная связь, Х= N и R= C(O)OH, в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы.
- двойная связь, Х= N и R= C(O)OH, в качестве ингибитора NO-зависимой активации растворимой формы гуанилатциклазы.
| LEHOTAI D.C., LEVEY B.А., et | |||
| al | |||
| Inhibition of cardiac guanylate cyclase by doxorubicin and some of its analogs:possible relationship to cadiotoxicity | |||
| Cancer Treat | |||
| Rep | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| Способ приготовления массы для карандашей | 1921 |
|
SU311A1 |
| VESELY D.L., LEVEY G.S | |||
| Inhibition of nitroso chemical carcinogen activation of rat hepatic cyclase by anticancer reagent | |||
| Oncolоgy | |||
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
| Схема обмотки ротора для пуска в ход индукционного двигателя без помощи реостата, с применением принципа противосоединения обмоток при трогании двигателя с места | 1922 |
|
SU122A1 |
| ТОЛСТИКОВ В.В., КОЗЛОВА Н.В | |||
| и др | |||
| Получение амидов и эфиров антибиотика брунеомицина и изучение его цитотоксической и антиретровирусной активности | |||
| Химико-фармацевтический журнал | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
| ИНГИБИТОР РАСТВОРИМОЙ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ | 1999 |
|
RU2151799C1 |
Авторы
Даты
2002-09-10—Публикация
2001-01-16—Подача