Изобретение относится к липосомам, содержащим новые пептидные антигены, которые принимают участие в регуляции иммунитета человека против вируса гепатита В ("HBV"), более конкретно к группам пептидов, соответствующих эпитопам антигенов, полученных из белка Х HBV, которые индуцируют цитотоксические Т-лимфоциты ("CTL") против вирусов, или иммунологической толерантности к вирусам, и рН-чувствительным липосомам, содержащим указанные группы пептидов, для индуцирования клеточного иммунитета таким образом, чтобы осуществлялась выработка CTL специфических в отношении этого вируса.
Описание уровня техники
Когда организм человека инфицирован HBV, в нем происходят различные физиологические реакции для удаления вируса. Среди этих реакций одна из наиболее важных состоит в разрушении и удалении инфицированных клеток, что, в конце концов, приводит к выздоровлению от вирусной инфекции. Разрушение инфицированных клеток осуществляется клетками другого типа, которые обладают цитотоксичностью, и которые носят название CTL. Для проявления цитотоксичности CTL должны прежде всего распознать некоторые пептиды, полученные из вторгшихся вирусных белков. Обычно вирусные белки синтезируются внутри инфицированных клеток, а затем они превращаются в короткие пептиды, содержащие от 8 до 15 аминокислот, в результате внутриклеточной деградации. Если некоторые из образовавшихся таким образом пептидов появляются на клеточной поверхности в объединенной форме с молекулой внутриклеточного главного комплекса гистосовместимости ("МНС"), CTL распознает их, чтобы разрушить инфицированные клетки. С другой стороны, МНС подразделены на класс I и класс II, и было известно, что МНС класса I играют более важную роль в индуцировании CTL по сравнению с CTL класса II. Однако сообщалось, что сайты белков (пептидов), распознаваемые CTL, ограничены только теми, которые содержат специфичные аминокислотные последовательности среди всех пептидов, которые образуются при разрушении вирусных белков (см.: Fremont, D. et al., Science, 257:919-926 (1992); Matsumura, M. et al., Science, 257:929-934 (1992)).
Соответственно выяснение аминокислотных последовательностей этих специфичных сайтов позволит химическим способом синтезировать и получить пептиды, соответствующие этим аминокислотным последовательностям, и такое использование этих пептидов позволит искусственным образом индуцировать CTL, специфически распознающие вирус гепатита в организме человека, или регулировать другие иммунные реакции, такие как иммуносупрессия, что приведет к эффективной профилактике и лечению заболеваний, вызываемых вирусом гепатита.
Зная это, многие исследователи предпринимали попытки найти аминокислотные последовательности пептидов, распознаваемых CTL, среди пептидов, образующихся в результате разрушения протеинов вируса гепатита. В результате было обнаружено несколько специфичных аминокислотных последовательностей, и ожидалось, что в дальнейшем будет обнаружено еще несколько последовательностей. Кроме того, чтобы использовать такие пептиды для профилактики и лечения связанных с гепатитом заболеваний, необходимо, чтобы одновременно использовалось как можно больше пептидов, и их эффективность могла бы меняться в зависимости от типа пептидов. Поэтому раскрытие аминокислотных последовательностей таких пептидов имеет очень важное значение.
Пептиды для профилактики и лечения гепатита В, достоверно распознаваемые CTL, происходят главным образом из белка S (поверхностного антигена) и белка С (ядерного) HBV. Однако о пептидах, полученных из белка X, одного из антигенных белков HBV, до сих пор не сообщалось, несмотря на то, что ряд исследований с использованием трансгенных мышей четко показал, что белок Х непосредственно связан с HBV-ассоциированной злокачественной опухолью печени (см: Hoyhne et al, EMBO J., 9:1137-1145 (1990); Kim et al., Nature, 351:317-320 (1991)).
С другой стороны, если фосфолипиды диспергированы в воде, полярные головные группы ориентируются к воде, а гидрофобные хвосты собираются за счет гидрофобных взаимодействий, спонтанно образуя сферические замкнутые двухслойные пузырьки, так называемые "липосомы". Такие липосомы широко используются в качестве носителей в системах доставки лекарств, а также в моделирующих исследованиях биологических мембран (см: Lee, J.w. and Kim, H., Arch. Biochem. Biophys., 297:354(1992); Hahn, K.H. and Kim, H., J. Biochem., 110: 635(1991); Yun, C. H. and Kim, H., J. Biochem., 105:406(1989); Kim, J. and Kim, H. , Biochemistry, 25:7867(1986); Kim, J. and Kim, H., 15 Korean Biochem. J., 18:403 (1985)).
Недавно сообщалось, что липосомы можно использовать в области иммунологии, что ускоряет исследования липосом в качестве носителей вакцин или адъювантов (см: Rooijen, N.V., Vaccine, 11:1170 (1993). Обычно, если липосомы вводят внутривенно, их легко захватывают макрофаги ("МО"), которые в большом количестве присутствуют в крови, что играет важную роль в процессинге липосомного антигена, а также в иммунологическом процессинге антигена.
Кроме того, недавно были разработаны способы индуцирования CTL реакции специфической в отношении некоторых белков или пептидов с использованием рН-чувствительных липосом (см.: Readdy, R. et al., J. Immunol. Methods, 141: 157(1991); Zhou, F. et al., J. Immnunol. Methods, 145:143(1991); Nair, S. et al. , J. Exp. Med., 175: 609(1992); Harding, C.V. et al., J. Immunol. 147: 2860(1991); Zhou, F. and Huang, L., Vaccine, 11:1139(1993)), и рН-чувствительные липосомы были широко использованы в качестве носителей и систем адъювантов белка или пептидного антигена для получения субъединичной вакцины. В этой связи авторы настоящего изобретения раскрыли способ получения рН-чувствительной липосомы, которая позволяет обеспечить селективный транспорт противобластомных лекарственных средств (см: Choi, M.J. et al., J. Biochem., 112:694 (1992)).
Сущность изобретения
В соответствии с настоящим изобретением предложен ряд пептидов, специфически распознаваемых CTL, среди пептидов, полученных из белка Х HBV. Предложены также рН-чувствительные липосомы, содержащие пептидные антигены, полученные из белка Х HBV. Авторы настоящего изобретения обнаружили, что эти липосомы можно использовать для создания предполагаемых терапевтических агентов для профилактики и лечения HBV-связанных заболеваний за счет индуцирования клеточного иммунитета таким образом, чтобы могли вырабатываться CTL, специфичные в отношении пептидных антигенов HBV.
Поэтому основной целью изобретения является создание пептидных антигенов, полученных из белка Х HBV, которые могут распознаваться CTL и демонстрируют цитотоксичность в отношении вируса.
Другой целью изобретения является создание рН-чувствительных липосом, включающих указанные пептидные антигены, которые могут индуцировать клеточный иммунитет.
Краткое описание чертежей
Вышеуказанные и другие объекты и признаки настоящего изобретения станут более очевидны из следующего описания, приведенного вместе с сопровождающими чертежами, где:
Фиг. 1 представляет график, демонстрирующий изменение количества молекул МНС класса I, экспрессированных на поверхности Т2-клетки, что представлено как интенсивность флуоресценции. Фиг.2 представляет график, демонстрирующий цитотоксичность CTL в отношении Т2-клеток.
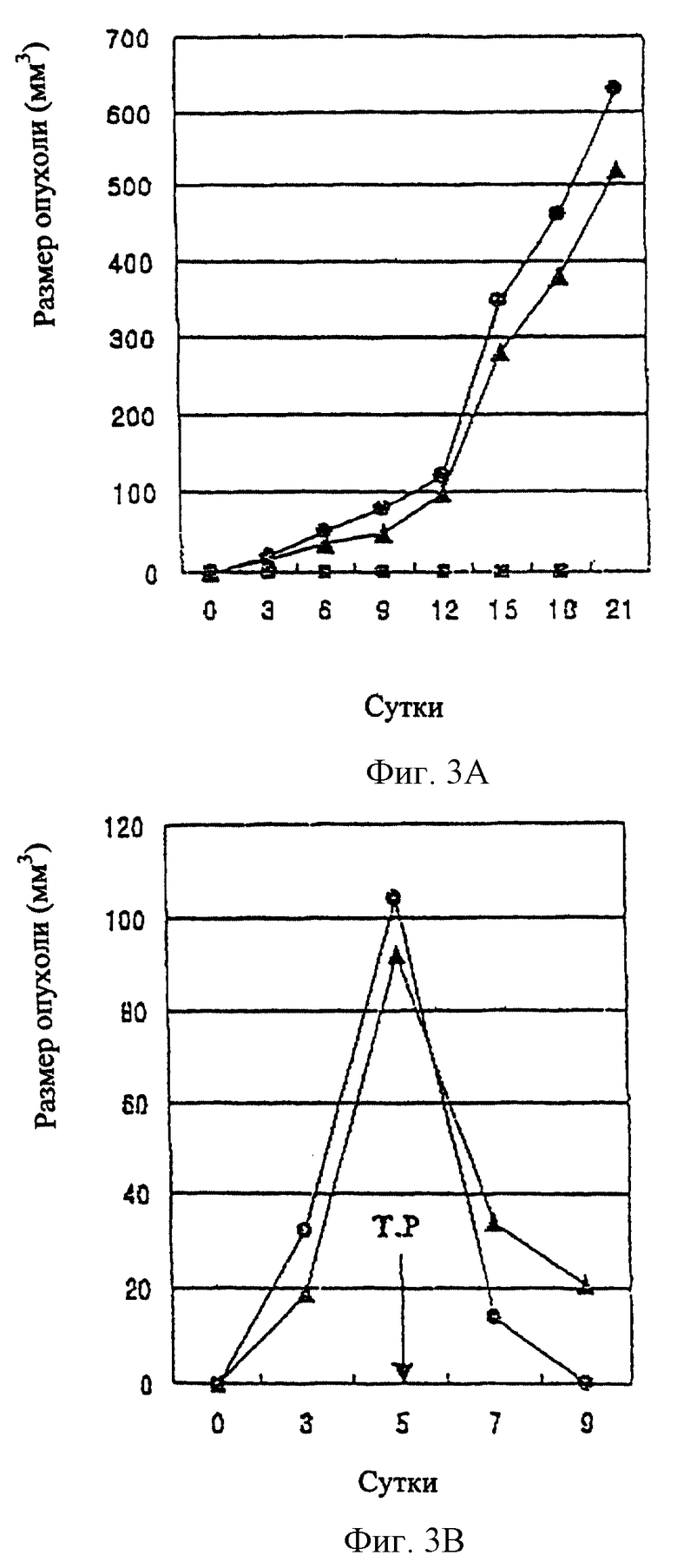
Фиг.3А представляет график, демонстрирующий образование опухолей у мышей nude, зараженных гепатоцеллюлярной карциномой человека.
Фиг. 3В представляет график, демонстрирующий регрессирование опухоли у мышей nude после лечения CTL, стимулированными пептидными антигенами, полученными из белка Х HBV.
Подробное описание изобретения
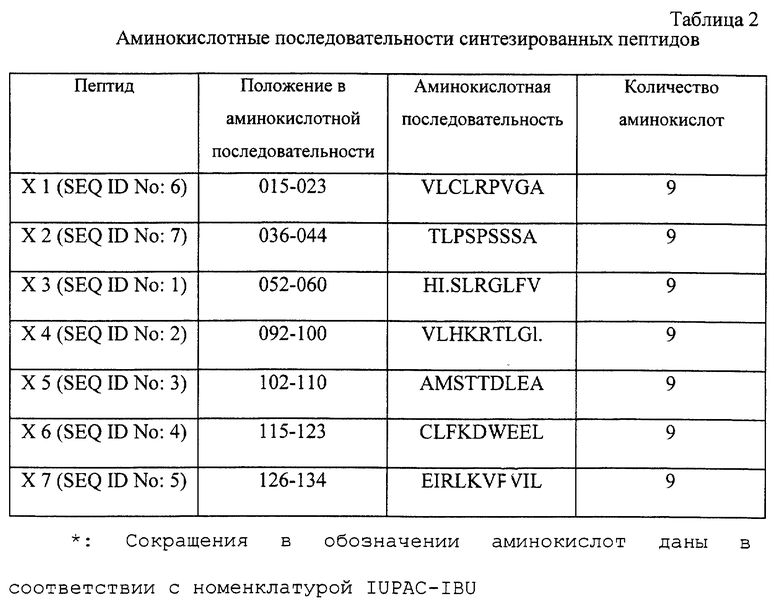
На основании открытия того факта, что пептиды, связывающиеся с молекулами МНС класса I, имеют специфичные аминокислотные последовательности, пептиды, обладающие потенциальными возможностями связывания с молекулами МНС класса I, были секвенированы в полных аминокислотных последовательностях белка Х HBV. То есть, так как пептиды, которые могут связываться с HLA-A2, человеческой молекулой МНС класса I, содержат лейцин, валин или изолейцин у С-концов и во втором положении с N-концов (см.: Matsumura, М. et al., Science, 257: 929-934 (1992)), аминокислотные последовательности, удовлетворяющие указанным условиям, были скринированы из полных аминокислотных последовательностей белка Х HBV, и пептиды, которые обладают потенциалом связывания с HLA-A2 молекулой, т.е. пептидные антигены, которые могут индуцировать ответ CTL за счет связывания с человеческой молекулой МНС класса I, были отобраны из пептидов, образующихся при деградации антигенного белка Х HBV, на основании трехмерной структуры, молекулы (см. таблицу 1 далее). Затем были химически синтезированы пептиды в соответствии с определенными таким образом аминокислотными последовательностями. Аминокислотные последовательности пептидов, полученных из HBV Х белка, т.е. Х3, Х4, Х5, Х6 и Х7, представлены далее в таблице 1.
Настоящее изобретение охватывает не только описанные выше пептиды, состоящие из 9 аминокислот, но также и пептиды, к которым добавлены от 1 до 5 аминокислот с N- или С-концов указанных пептидов, а также их функциональные эквиваленты. В настоящем изобретении термин "функциональные эквиваленты" используют для обозначения всех пептидов, замещенных 1 или 2 аминокислотами среди аминокислотных последовательностей указанных пептидов. Например, такие замещения включают такие комбинации, как Gly, Ala; Val, Ile, Leu; Asp, Glu; Asn, Gln; Ser, Thr; Lys, Arg; и Phe, Туr.
Для получения рН-чувствительных липосом, включающих пептидные антигены, полученные из белка X HBV, фосфатидилэтаноламин-β-олеоил-γ-пальмитоил (POPE) и холестерингемисукцинат (СНОН) смешивают в молярном отношении от 6:4 до 8: 2, более предпочтительно 7: 3, или POPE, фосфатидилэтаноламин (РЕ) и СНОН смешивают в молярном отношении от 3:3:4 до 4:4:2, более предпочтительно 3,5: 3,5: 3, для получения в итоге тонкой мембраны фосфолипидов. Затем полученные таким образом липосомы добавляют к буферному раствору, содержащему указанные пептидные антигены, полученные из белка Х HBV. В этой связи липосомы, включающие пептидные антигены, полученные из белка Х HBV, приготавливают, смешивая 1 или более из типов пептидных антигенов с фосфолипидом в молярном отношении от 1:5 до 1:25, более предпочтительно 1:20. Кроме того, рН-чувствительные липосомы, полученные в соответствии с настоящим изобретением, могут включать далее вплоть до 1 мольного % монофосфориллипида А в качестве фосфолипида.
Липосомы настоящего изобретения инкапсулируют пептидные антигены, индуцирующие CTL реакцию у человека, и рН-чувствительные липосомы, которые используются в качестве носителей пептидов, также могут индуцировать CTL реакцию, специфическую в отношении вируса, из которого получены инкапсулированные пептиды. Естественно, четко показано, что рН-чувствительные липосомы, включающие указанные пептиды, могут индуцировать клеточный иммунитет у человека.
При описании аминокислотных последовательностей пептидов настоящего изобретения используются следующие однобуквенные символы в соответствии со стандартами IUPAC-IUB:
Аминокислота - Символ
Аланин - А
Аргинин - R
Аспарагин - N
Аспарагиновая кислота - D
Цистеин - С
Глутамин - Q
Глутаминовая кислота - Е
Глицин - G
Гистидин - Н
Изолейцин - I
Лейцин - L
Лизин - К
Метионин - М
Фенилаланин - F
Пролин - Р
Серин - S
Треонин - Т
Триптофан - W
Тирозин - Y
Валин - V
Далее настоящее изобретение иллюстрируется примерами, которые не следует рассматривать как ограничивающие объем изобретения.
Пример 1. Определение пептидов, обладающих потенциалом связывания с молекулами МНС белка Х
Так как пептиды, которые могут связываться с HLA-A2, человеческой молекулой МРС класса I, содержат лейцин, валин или изолейцин с С-концов, и во втором положении от N-концов (см.: Matsumura, М. et al., Science, 257:929-934 (1992)), аминокислотные последовательности, удовлетворяющие указанным условиям, вначале скринируют из полных аминокислотных последовательностей белка Х HBV, и в итоге отбирают пептиды, обладающие потенциальными возможностями связывания с HLA-A2 молекулами, учитывая трехмерную структуру молекулы (см. таблицу 1). Затем осуществляют химический синтез пептидов известными специалистам способами на основании определенных таким образом аминокислотных последовательностей.
Пример 2. Синтез пептидов и определение их связывания с молекулами МНС
Семь различных пептидов, включая пептиды, указанные ранее в таблице 1, которые были получены из белка Х HBV, были синтезированы химическим способом и растворены в фосфатно-буферном растворе (здесь и далее именуемом "PBS"). Для исследования возможности связывания этих пептидов с молекулами МНС класса I, связанными с индуцированном CTL, каждый из пептидов добавляют к Т2 клеточной линии в концентрации 100, 64, 32, 16, 8, 2 и 1 мкг/мл соответственно и оставляют взаимодействовать при 37oС в течение 4 часов. Затем клетки промывают PBS для удаления непрореагировавших пептидов, добавляют ВВ7.2 антитело против HLA-2A.1, молекул МНС класса I, и оставляют реагировать при 4oС в течение 1 часа. Клетки снова промывают PBS, добавляют флуоресцинизотиоцианат (FITC), конъюгированный с антителом к мышиному иммуноглобулину, и реакции позволяют протекать при 4oС в течение 1 часа. Затем определяют флуоресценцию клеток с помощью флюороцитометра (FACScan, BECTON DICKINSON), и полученные результаты представлены на фиг.1 далее.
Как видно на фиг.1, было обнаружено 5 пептидов, таких как Х3, Х4, Х5, Х6 и Х7, которые успешно связываются с молекулами МНС класса I на поверхности Т2 клеток. Пептиды, использованные в этих экспериментах, охарактеризованы в таблице 2.
Клеточная линия Т2, используемая в этом примере, имеет нарушение в схеме внутриклеточного транспорта пептидов, и не позволяет осуществить правильное связывание молекулы МНС класса I с пептидом с образованием нестабильной молекулярной структуры, что приводит к низкой экспрессии молекул МНС во время культивирования при 37oС, нормальной температуре для роста. Однако, если клетки Т2 культивируют в среде, содержащей пептиды, которые могут связываться с молекулами МНС, эти пептиды связываются с молекулами МНС на поверхности Т2-клеток, повышая стабильность молекул МНС, что приводит к усилению экспрессии молекул МНС. Зная это, связывание специфических пептидов с молекулами МНС на поверхности Т2-клеток можно анализировать, определяя степень связывания ВВ7.2 антител с клеточной поверхностью.
Пример 3: Определение распознавания пептида CTL
Связывание определенного пептида с молекулой МНС не может доказать распознавание пептида CTL. Соответственно следующий эксперимент был проведен для исследования того, действительно ли пептиды, используемые для определения связывания с молекулами МНС в примере 2, распознаются CTL, которые могут распознавать HBV в организме человека.
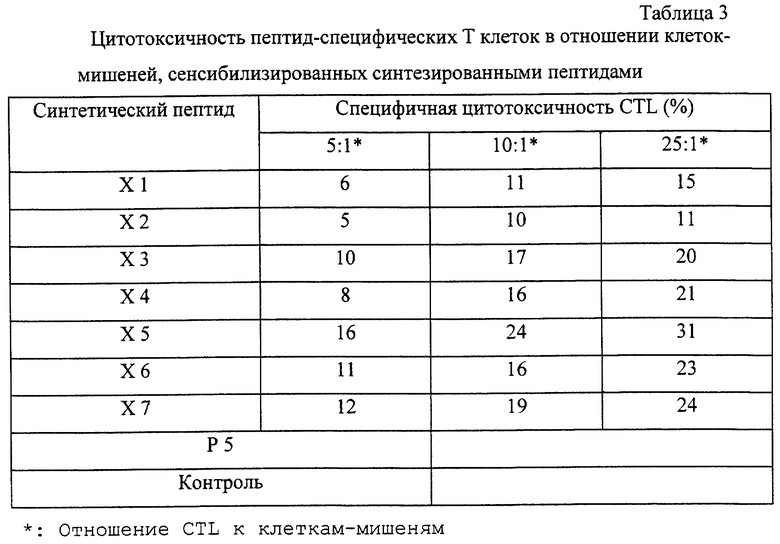
То есть отбирают кровь, положительную в отношении анти-HBV антител (величина, полученная с помощью ELISA: 1,0 или более), у обычных доноров и центрифугируют для сбора клеток крови. Указанные пептиды добавляют в концентрации 10 мкг/мл к лейкоцитам, которые остались после удаления красных кровяных клеток (эритроцитов) из клеток крови, и инкубируют при 37oС в СO2 инкубаторе, в котором поддерживается концентрация 5% СO2. Через 2 суток культивирования 10 ед интерлейкина-2 добавляют к культуральной среде и клетки продолжают культивировать еще 3 суток. Затем клетки крови с одинаковыми МНС инактивируют митомицином С и добавляют к культуральной среде в качестве стимулирующих клеток. И пептиды, и интерлейкин-2 добавляют к среде, и клетки продолжают культивировать в течение 7 суток. Затем определяют, распознают ли клетки крови и разрушают ли Т2 клетки, содержащие определенный пептид на своей поверхности, полученные результаты представлены в таблице 3 и на фиг.2 соответственно.
Разрушение Т2-клеток культивируемыми клетками крови определяют следующим образом: 100 мкг/мл пептида добавляют к Т2 клеткам и оставляют реагировать при 37oС в течение 3 часов. Затем клетки тщательно промывают для удаления непрореагировавших пептидов, добавляют радиоактивный хромат натрия (Сr51) и оставляют реагировать при 37oС на 2 часа в СO2 инкубаторе. Затем их тщательно промывают RPMI средой для удаления непрореагировавшего хромата, смешивают с клетками крови, промытыми PBS, в определенном соотношении и оставляют реагировать при 37oС в течение 4 часов в СО2 инкубаторе. Полученную среду собирают и определяют интенсивность гамма лучей для определения цитотоксичности клеток крови в отношении Т2 клеток, т.е. клеток-мишеней. Как видно из таблицы 3, было обнаружено, что Х3, Х4, Х6, Х7 и Р5 распознаются культивируемыми клетками крови, причем Р5 представляет известный пептид, играющий роль позитивного контроля (см: Nayersina, R. Et al., J. Immunol., 150: 4659-4671 (1993)), что свидетельствует о пригодности экспериментальных методик, использованных в этом примере.
Пример 4: Получение рН-чувствительных липосом, содержащих пептидные антигены
Фосфолипид, содержащий РОРЕ/СНОН (7: 3 молярное отношение) или РОРЕ/РЕ/СНОН (3,5:3,5:3 молярное отношение) добавляют в стеклянный сосуд и растворяют в органическом растворителе. Затем сосуд заполняют газообразным азотом для образования липидной тонкой пленки в сосуде. Затем к липидной пленке добавляют буфер (рН 8,0), содержащий пептиды, которые должны быть инкапсулированы, для достаточного увлажнения, и интенсивно перемешивают для получения многослойных пузырьков ("MLV"), из которых получают маленькие однослойные пузырьки ("SUV") в результате обработки ультразвуком. Полученные таким образом SUV инкубируют при комнатной температуре в течение от 2 до 12 часов и быстрое замораживание SUV с помощью жидкого азота и медленное оттаивание при комнатной температуре повторяют 3-4 раза для получения липосом, включающих пептиды. Таким образом в итоге получают липосомы в результате смешивания пептидов и фосфолипидов в молярном отношении 1:20. В этой связи используемыми пептидами являются пептидные антигены, которые получают из белка Х HBV, и которые могут индуцировать CTL реакцию за счет связывания с молекулами МНС класса I (см. таблицу 1).
Физическую стабильность и рН-чувствительность полученных таким образом липосом исследуют следующим образом, что показало слабое разрушение липосом при обработке этанолом и очень малое уменьшение содержания липосом по сравнению с обычными рН-чувствительными липосомами:
(1) Определение физической стабильности
Физическую стабильность полученных таким образом липосом определяют, измеряя изменение мутности раствора при добавлении к нему этанола. Так как обработка этанолом разрушает липосомы, что приводит к уменьшению мутности, стабильность липосом определяют, измеряя изменение поглощения на 400 нм. В результате было обнаружено, что липосомы, содержащие пептиды настоящего изобретения, обладают более высокой физической стабильностью, нежели обычные рН-чувствительные липосомы.
(2) Определение рН-чувствительности
12,5 мМ динатриевой соли 8-аминонафталин-1,3,6-трисульфоновой кислоты (ANTS), 45 мМ параксилол-бис(пиридиний)бромида (DPX), 68 мМ NaCl и 10 мМ буферированного раствора HEPES (рН 8,0) инкапсулируют в липосомы, содержащие пептиды, a FNTA и DPX, которые оказались не инкапсулированы, удаляют, используя колонку Sephadex G-50 (1•20 см) для сбора только липосомного раствора. Концентрацию фосфолипидов в липосомах определяют по методу Vaskovsky (см: Vaskovsky, V.E., Kostetsky, E.Y. and Vasendin, I.M., J. Chromatogr., 114:129 (1975)).
В этом эксперименте для определения рН-чувствительности интенсивность флуоресценции прошедшего через колонку липосомного раствора, принимают за "0% рассеяния", а интенсивность флуоресценции липосомного потока, разрушенного Triton X-100, принимают за "100% рассеяния". Концентрации липосом (по 30 мкМ) добавляют к 2 мл буферного раствора с соответствующими значениями рН (7,5, 6,9, 5,9, 5,4, 4,9 и 4,5), и оставляют выстаиваться при 37oС в течение 30 минут. Затем определяют рН-чувствительность, измеряя флуоресценцию. При этом флуоресценцию измеряют, используя возбуждающее излучение с длиной волны 360 нм и измеряя эмиссию на длине волны 545 нм с помощью спектрофлюориметра (FP-777, JASCJ, Japan).
В результате оказалось, что липосомы, которые содержат пептиды настоящего изобретения, демонстрируют меньшее уменьшение содержания липосом (примерно 20%) по сравнению с обычными рН-чувствительными липосомами, которые используют в качестве контроля (примерно 80%).
Пример 5: Индуцирование клеточного иммунитета рН-чувствительными липосомами, содержащими пептиды
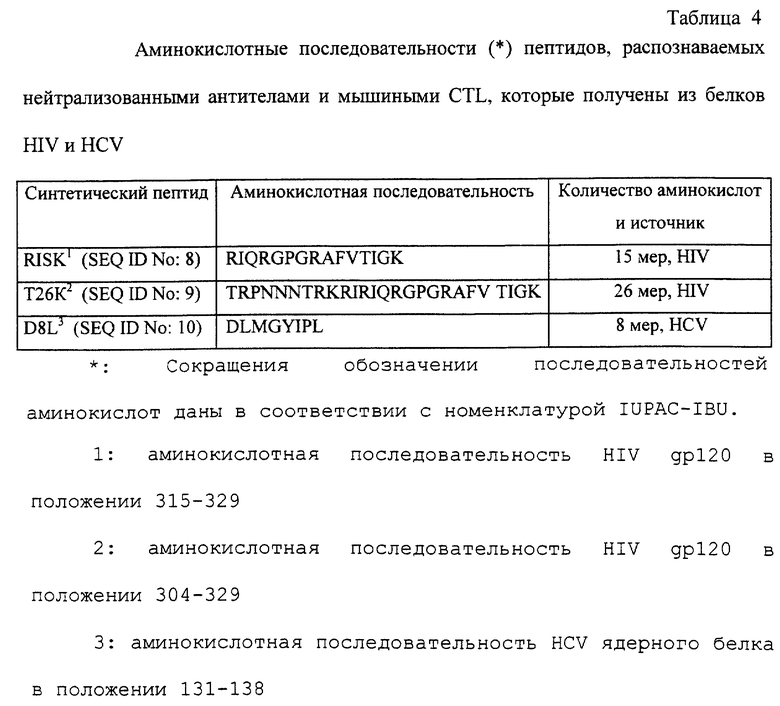
Для определения того, могут ли рН-чувствительные липосомы в качестве носителя пептидов индуцировать CTL реакцию, специфическую в отношении вируса, из которого эти пептиды получены, получают рН-чувствительные липосомы, в которых инкапсулированы синтетические пептиды, и проводят исследования цитотоксичности серийным способом. Так как клеточный иммунитет пептидов, которые могут связывать HLA-А2, человеческие молекулы МНС класса I, должен быть исследован, используя организм человека, осуществляют косвенный эксперимент с использованием пептидов, полученных из белков HBV и HCV, которые могут связывать мышиные молекулы МНС класса I (см. таблицу 4). Для этого получают рН-чувствительные липосомы, включающие пептиды, используя композицию фосфолипидов, содержащую РОРЕ/СНОН (7:3 молярное отношение). Затем осуществляют иммунизацию мышей липосомами и определяют цитотоксичность Т-лимфоцитов после распознавания клеток-мишеней, меченных Cr51.
В случае HIV мышей штамма Balb/C иммунизуют рН-чувствительными липосомами, включающими R15K или Т26К, и через 4 недели после бустерной иммунизации иссекают селезенку и гомогенизируют в 2 мл клеточной культуральной среды RPMI, используя гомогенизатор. 2 мл полученного таким образом гомогената добавляют к 2 мл фиколла и центрифугируют при 1500 об/мин в течение 30 минут. Т-лимфоциты, расположенные между фиколлом и клеточной культуральной средой, выделяют, добавляют к 15 мл клеточной культуральной среды RPMI-10, центрифугируют при 1000 об/мин и трижды промывают RPMI-10 средой. Т-лимфоциты разбавляют до клеточной концентрации 5 х 106/мл в 24-луночном планшете и иммунизированный пептидный антиген добавляют до конечной концентрации 2 мкМ. Затем клетки культивируют при 37oС в течение 3 дней в СO2 инкубаторе, содержащем 5% СО2, и используют в качестве эффекторных клеток. В случае HCV пятинедельных мышей штамма C57BL/6 иммунизируют липосомами, содержащими пептидный антиген D8L и Т-лимфоциты выделяют таким же образом, что и описан выше, и используют в качестве эффекторных клеток. С другой стороны, р815 клетки (АТСС TIB64) у которых МНС класса I такие же, что и у мышей Balb/C, используют в качестве клеток-мишеней в случае HIV, и RMA клетки (см.: Hosken, N.A. and Bevan, M.J., J.Exp. Med., 175:719 (1992)) или EL4 клетки (АТСС TIB39), у которых МНС класса I такие же, что и у мышей штамма C57BL/6, используют в качестве их клеток-мишеней в случае HCV.
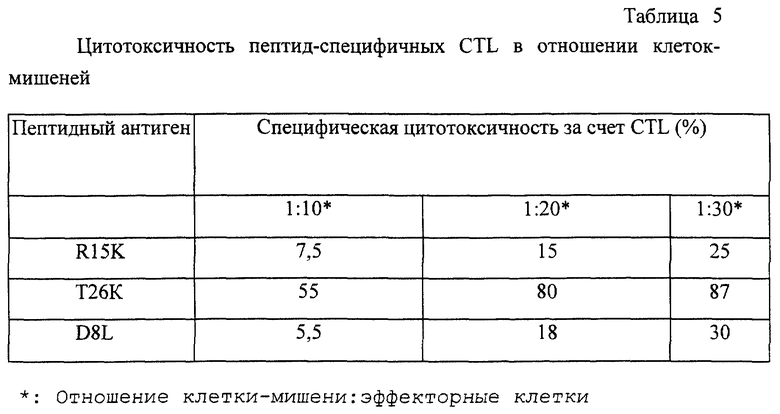
100 мкМ иммунизованного пептида добавляют к соответствующим клеткам-мишеням, оставляют реагировать при 37oС в течение 16 часов и дважды промывают клеточной культуральной средой RPMI. Затем к клеткам добавляют радиоактивный хромат натрия (Сr51) и оставляют реагировать при 37oС в течение 2 часов в СO2 инкубаторе. После реакции клетки тщательно промывают клеточной культуральной средой RPMI для удаления непрореагировавшего хромата натрия, смешивают с эффекторными клетками, промытыми фосфатно-буферным раствором, в различных отношениях, представленных в таблице 5, и оставляют реагировать при 37oС в течение 4 часов в CO2 инкубаторе. Полученную среду собирают и измеряют интенсивность гамма-лучей для определения цитотоксичности эффекторных клеток в отношении клеток-мишеней (см. таблицу 5).
Как видно из таблицы 5, оказалось, что эффекторные клетки, выделенные из селезенок мышей, иммунизованных R15K, Т26К и D8L пептидными антигенами, могут распознавать и уничтожать клетки-мишени. Более того, было обнаружено, что если мышей иммунизировать пептидными антигенами, индуцирующими CTL реакцию, используя рН-чувствительные липосомы, можно индуцировать клеточный иммунитет, выражающийся в продукции CTL, специфичных в отношении вируса.
На непрямых экспериментах по индуцированию клеточного иммунитета, которые проводили с использованием рН-чувствительных липосом, содержащих пептиды, полученные из белков HIV и HCV, было четко показано, что: липосомы, содержащие пептидные антигены, полученные из белка Х HBV, могут индуцировать клеточный иммунитет, который, в свою очередь, индуцирует ответ CTL, так как пептидные антигены, полученные из белка Х HBV, могут индуцировать ответ CTL реакцию у человека (см. пример 3), и рН-чувствительные липосомы, содержащие эти пептиды, также могут индуцировать ответ CTL реакцию, специфическую в отношении вируса, из которого эти пептиды получены.
Пример 6: Уничтожение гепатоцеллюлярной карциномы человека НВх-специфичными Т-клетками
Уничтожение опухоли CTL, которые были стимулированы пептидными антигенами, полученными из белка Х HBV (т.е. пептидом НВх) исследуют следующим образом. Клетки гепатокарциномы человека подкожно вводят мышам nude штамма Ва1Ь/С в различном количестве клеток от 1•107 до 2•107, и на голых мышах проводят тест на образование опухоли. Через 3 суток опухоли уже можно определять, а через 5 суток адоптивно переносят CTL, стимулированные пептидом Нвх в хвостовую вену мышей, у которых образовались опухоли, в количестве 1,5х 108 клеток (см. фиг.3А). В результате показано, что размеры опухоли начинают уменьшаться на 2 сутки после обработки, и опухоли полностью исчезают после обработки (см фиг.3В). На фиг 3А и 3В значки (-•-) и  представляют вводимые дозы 2•107 и 1•106 соответственно, а Т.Р. представляют моменты обработки CTL.
представляют вводимые дозы 2•107 и 1•106 соответственно, а Т.Р. представляют моменты обработки CTL.
Как было четко проиллюстрировано выше, в настоящем изобретении предложены рН-чувствительные липосомы, которые включают группы пептидов, соответствующих эпитопам антигенов, полученных из белка Х HBV, которые индуцируют CTL против вируса или иммунологической толерантности к вирусу, таким образом, что можно индуцировать клеточный иммунитет против HBV. Так как пептидные антигены, полученные из белка Х а, такие как Х3, Х4, Х5, Х6 и Х7, активируют CTL, которые могут распознавать HBV антигены, присутствующие в организме человека, и также могут распознаваться CTL, указанные рН-чувствительные липосомы, включающие пептидные антигены, полученные из белка Х HBV, можно использовать для создания потенциальных терапевтических средств для профилактики и лечения HBV-ассоциированных заболеваний.
Список последовательностей приведен в конце описания.








Изобретение относится к липосомам, включающим новые пептидные антигены, которые принимают участие в регулировании иммунитета человека против вируса гепатита В, более конкретно к группам пептидов, соответствующих эпитопам антигенов, полученных из балка Х НВV. Пептидные антигены индуцируют цитотоксические Т-лимфоциты против вируса гепатита В или иммунологической толерантности в отношении вируса. рН-чувствительные липосомы включают пептидные антигены для индуцирования клеточного иммунитета таким образом, чтобы могли вырабатываться СТL, специфичные в отношении вируса. Так как пептидные антигены, полученные из белка Х, такие как Х3, Х4, Х5, Х6 и Х7, активируют СТL, которые могут распознавать антигены НВV, присутствующие в организме человека, и могут также распознаваться СТL, указанные липосомы можно использовать для создания потенциальных лекарственных средств для профилактики и лечения НВV-ассоциированных заболеваний. 6 с. и 6 з.п. ф-лы, 3 ил., 5 табл.
| WO 9527788 А1, 19.10.1995 | |||
| JP 5105699, 27.04.1993 | |||
| US 4935235 А, 19.06.1990. |
Авторы
Даты
2002-09-27—Публикация
1998-01-19—Подача