Изобретение относится к медицине и может быть использовано при получении лечебных средств, имеющих противоишемическую активность, при профилактике и лечении ишемической болезни сердца.
Препараты, отличающиеся биологической активностью и используемые для профилактики и лечения ишемической болезни сердца, применяются как в виде таблеток, капсул, порошков, так и в виде инъекций, причем часто инъекционная форма препарата в силу наиболее сильного и активного влияния на ишемическое повреждение миокарда является предпочтительным.
В настоящее время известно, что аденозин-5-трифосфаты металлов, в частности натрия, биометаллов, имеют свойство достаточно эффективно защищать миокард от ишемического повреждения (п. СССР 755201 и др.).
Однако существуют определенные проблемы, связанные с получением их инъекционной формы необходимой активности.
Наиболее близким к заявляемому объекту является инъекционная форма противоишемического препарата, содержащего в качестве активного компонента (субстанции) динатриевую соль аденозин-5-трифосфата (Na2ATF), и изотонический раствор. Концентрация активного компонента составляет 1% (Машковский М.Д. . Лекарственные средства, Минск, "Белорусь", ч.2, 1988, с.125).
Известное средство имеет мембрано-стабилизирующее, энергосберегающее действие и в значительно меньшей степени проявляет противоишемическую активность. При лечении ишемической болезни известное средство в инъекционной форме используют в комплексе с другими препаратами. Однако следует отметить, что средство-прототип не исчерпывает все возможности защиты миокарда от ишемического повреждения, что свидетельствует о его недостаточной биологической активности. При растворении Na2ATF в воде рН раствора составляет 4,0-4,5, что влечет за собой дальнейшее подщелачивание раствора до рН 7,0-7,4.
В процессе стерилизации и сохранения известного препарата в инъекционной форме происходит заметное уменьшение ATF за счет его гидролиза до адениннуклеотидов и неорганического фосфора, что в конечном результате приводит к некоторой потере активности лекарственной формы.
Задачей настоящего изобретения является создание инъекционной формы препарата, обладающего противоишемическим действием, путем соединения наиболее активной субстанции и соответствующих добавок, в результате чего достигается высокое лечебно-профилактическое действие инъекционной формы препарата и увеличивается срок ее хранения.
Поставленная задача решается тем, что инъекционная форма препарата, проявляющего противоишемическую активность, на основе аденозин-5'-трифосфата, в изотоническом растворе, согласно изобретению в качестве источника аденозин-5-трифосфата содержит трикалиевую соль аденозин-5-трифосфатогистидинатомагний (II) октагидрат и дополнительно содержит фармацевтически приемлимую органическую или неорганическую кислоту, или ее кислую соль в количестве, необходимом для достижения рН 7,0-7,4, при следующем соотношении компонентов на 1000 изотонического раствора:
- трикалиевая соль аденозин-5-трифосфатогистидинатомагний (II) октагидрат 10-20 г
- фармацевтически приемлимая органическая или неорганическая кислота или ее кислая соль в количестве, необходимом для достижения рН 7,0-7,4
Авторами настоящего изобретения предложено использовать в качестве активного компонента близкое по химической природе к (Na2ATF) соединение такой формулы K2Mg(His(ATF), называемое далее ATF-лонг, и в котором His-анион гистидина, ATF-анион аденозин-5'-трифосфат. Однако совокупность лигандов и биологически активных металлов - калия, магния значительно расширила спектр действия на ишемическое повреждение миокарда, тем самым определив наиболее высокую эффективность указанного координационного соединения.
Соединение ATF-лонг является новым, состав и строение которого подтверждены данными элементного анализа, термогравиметрией, ИК- и электронной спектроскопией в УФ-области.
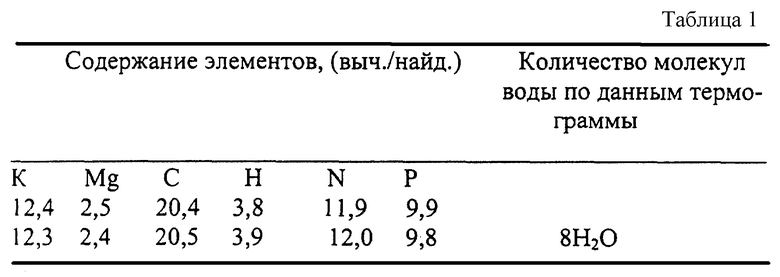
Данные элементного анализа и термогравиметрии координационного соединения ATF-лонг (см. табл.1).
Строение указанного соединения представлено ниже.
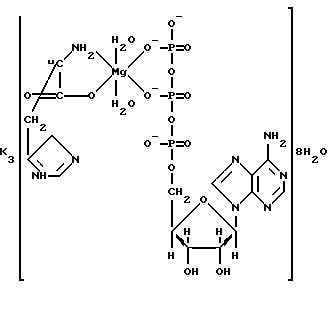
Исследование токсичности вышеприведенного соединения показало, что ЛД50= 850 мг/кг.
Противоишемическая активность ATF-лонг была исследована на экспериментальной модели острой ишемии миокарда, воспроизводимой на изолированных, перфузируемых по Лангендорфу сердцах крыс. Адекватная перфузия и период стабилизации сердец длилась 30-40 мин, затем перфузионную линию переключали на раствор, содержащий 0,3 г исследуемого соединения. Через 20 мин перфузии сердец указанным раствором воспроизводили ограничение объема коронарной перфузии на 80%. Период ишемии длился 60 мин.
Уже в период адекватной перфузии добавление ATF-лонг приводит к изменениям некоторых показателей ионного и энергетического обмена сердечной мышцы, которые в целом указывают на умеренную стимуляцию окислительно-восстановительных процессов (увеличение активности α-кетоглутаратдегидрогеназы на 15%, сукцинатдегидрогеназы на 7%), повышение функции ионтранспортных свойств мембран (прирост активности Na+, К+-АТФ-азы на 17%, Са2+-связывающей способности мембраны на 9% по сравнению с адекватной перфузией). Имеет место увеличение энергетического потенциала сердца на этапе адекватной перфузии под влиянием рассматриваемого координационного соединения, о чем свидетельствует увеличение содержания АТФ и гликогена соответственно на 16 и 10% по сравнению с контролем. В этих условиях происходит увеличение внутриклеточного содержания калия и магния на 12 и 15% и уменьшение натрия на 85 по сравнению с контролем.
Острая ишемия миокарда длительностью 60 мин приводила к угнетению окислительных процессов в миокарде, уменьшению энергетических субстратов - АТФ и гликогена на 55 и 60% по сравнению с контролем. Изменение биоэнергетики сердечных клеток сопровождалось нарушением липидной структуры их мембран (убыль фосфолипидов на 37%, накопление жирных на 27%), ионтранспортных свойств мембран (ингибирование Na+, К+-АТФ-азы на 36%, Са2+-связывающая способность мембраны снижалась на 28%). Одновременно с этим увеличивалась проницаемость мембран для ионов кальция на 85%. Период ишемии сопровождался резкой активацией анаэробного гликолиза и развитием ацидоза в ткани миокарда, на что указывало увеличение концентрации молочной кислоты в оттекающей от сердца перфузионной жидкости к 60-й минуте ишемии до 320% исходной величины. В сердечных клетках происходило перераспределение электролитов в сторону уменьшения калия и магния соответственно на 20 и 24% и увеличение натрия и кальция соответственно на 17 и 23% по сравнению с контролем.
В случае лечебно-профилактического применения ATF-лонг значительно выражена степень защиты сердечных клеток от ишемического воздействия. Под воздействием исследуемого соединения пониженная активность Na+, К+-АТФ-азы повышалась на 33% по сравнению с ишемией. Наиболее выражена нормализация фосфолипидного и жирнокислотного состава мембран, сопровождающаяся снижением проницаемости мембран для ионов кальция до 128% контрольного уровня. Наиболее выраженной была активация окислительных ферментов под влиянием данного соединения, в частности до 95 и 98% контрольного уровня достигала активность сукцинатдегидрогеназы и α-кетоглутаратдегидрогеназы соответственно. При этом в наименьшей степени выражен ацидоз в миокарде до 165% по сравнению с контролем. Вышеописанные изменения сопровождались повышением содержания энергетических субстратов в сердце, а именно - до 89% контроля, АТФ до 83% контроля. При введении ATF-лонг наблюдалась более адекватная коррекция внутриклеточных электролитов.
Таким образом, по большинству изученных показателей ATF-лонг проявляет высокую противоишемическую активность.
Авторами настоящего изобретения были выявлены соответствующие дополнительные компоненты, которым присуща роль буфера, что в свою очередь позволяет повысить гидролитическую стабильность активного противоишемического вещества. Эти компоненты, представляющие собой органические кислоты, или неорганические кислоты, или их кислые соли, хорошо сочетаются с ATF-лонг и обеспечивают рН инъекционного раствора концентрацией 1-2% в диапазоне 7,0-7,4.
Указанные добавки не снизили биологической активности препарата и не ухудшили его свойства.
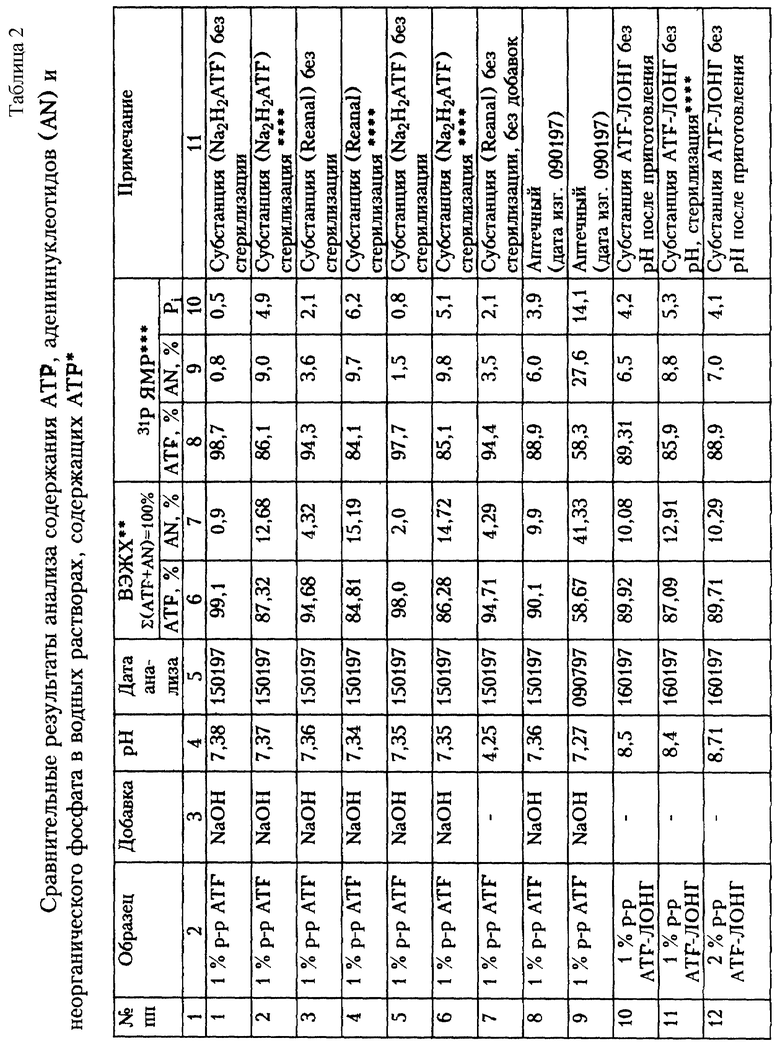
Как видно из данных табл. 2, в коммерческих препаратах (субстанциях) содержание ATF составляет от 99 до 95 ( 1, 3, 5). В результате стерилизации согласно ВФС 42У (на 1%-ный раствор ATF для инъекций) 1%-ный раствор динатриевой соли ATF при рН 7,0-7,4 (доводится раствором NaOH согласно ВФС) в течение 30 мин в запаянных ампулах ( 2, 4, 6) около 10% ATF гидролизует до адениннуклетидов и неорганического фосфата. То же самое происходит при приготовлении лекарственной формы в заводских условиях ( 9).
При растворении субстанции ATF-ЛОНГ в воде и получении 1%-ного раствора ( 10) или 2%-ного раствора ( 12) рН составляет соответственно 8,5 и 8,7. При стерилизации таких растворов в течение 30 мин потери ATF составляют всего несколько процентов ( 1, 13). Поэтому для приготовления инъекционной формы ATF-ЛОНГ 2%-ного раствора (рН 7,0-7,4) необходима частичная нейтрализация кислотой. При нейтрализации, например, фосфорной кислотой содержание ATF в растворе практически не изменяется ( 14), а при стерилизации уменьшается всего на 5% ( 15) в отличие от динатриевой соли ATF.
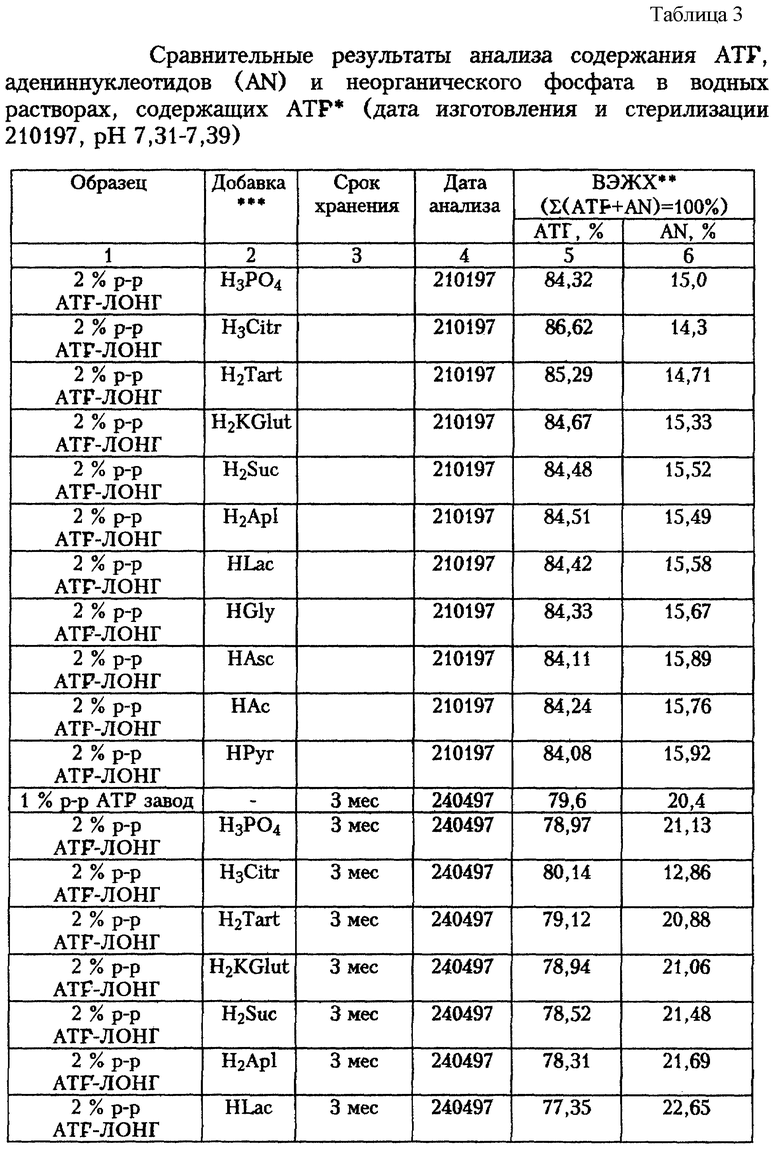
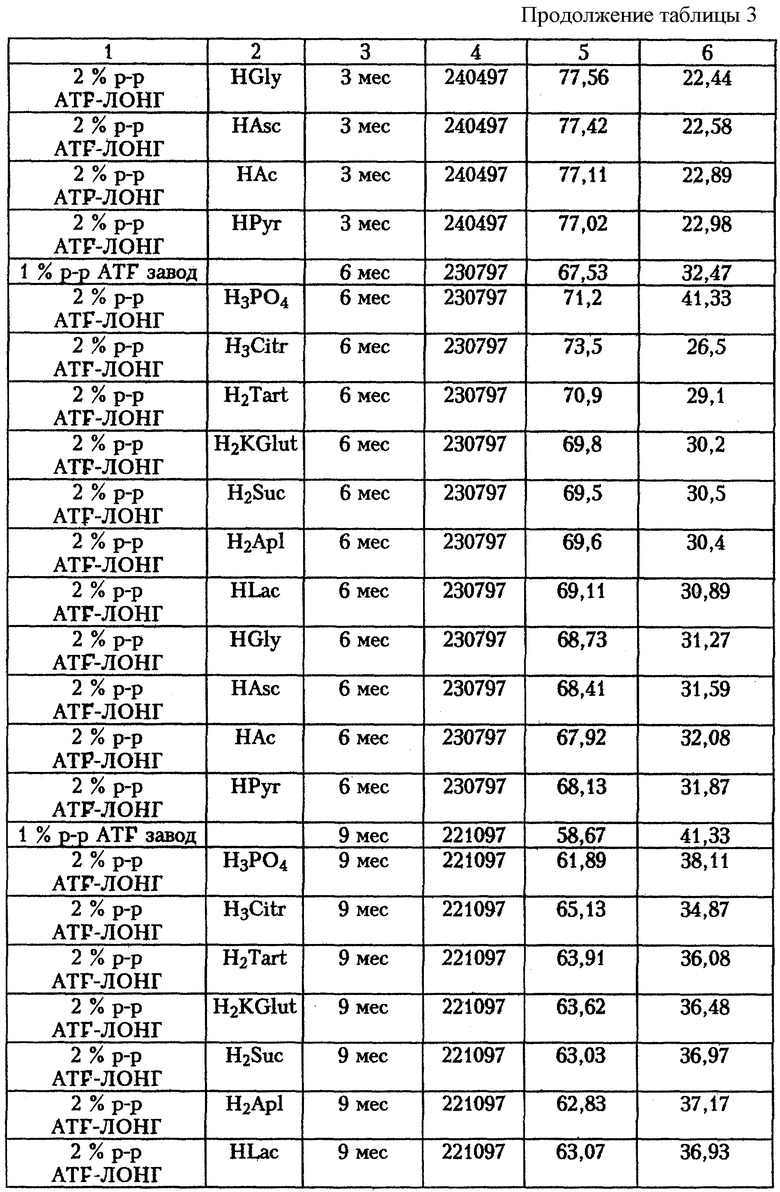
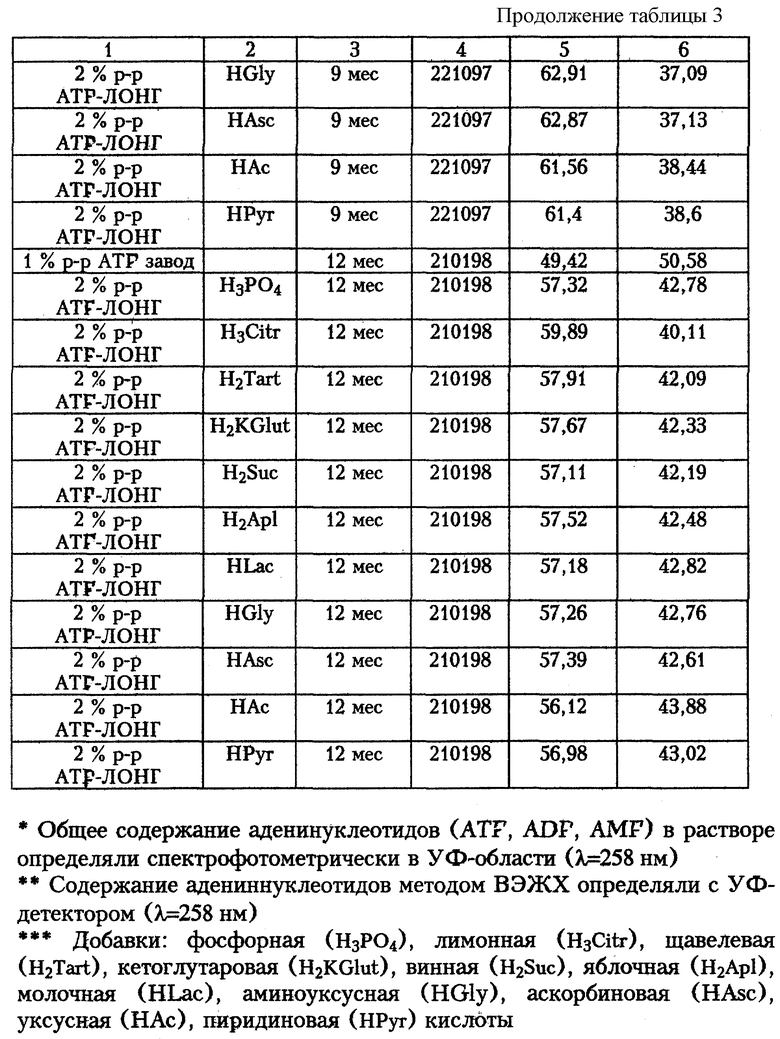
Был испытан ряд органических трехосновных, двухосновных и одноосновных кислот в качестве добавки для нейтрализации раствора ATF-ЛОНГ и получения 2%-ного раствора ATF-ЛОНГ для инъекций с рН 7,0-7,4. Результаты приведены в табл.3.
Как видно из данных, приведенных в таблице 3, все испытанные добавки пригодны для получения инъекционной формы ATF-ЛОНГ, поскольку в процессе стерилизации приготовленных с использованием добавок растворов содержание ATF в растворе изменяется всего на несколько процентов по сравнению с содержанием ATF в исходной субстанции ATF-ЛОНГ и близки к соответствующим величинам для динатриевой соли ATF (табл. 2).
Благодаря введению добавок кислот или их кислых солей (например, ортофосфорной кислоты или ее кислых солей, лимонной или ее кислых солей, яблочной, винной, янтарной и др.) достигается оптимизация рН раствора для инъекций (рН 7,0-7,4). Эти буферирующие и комплексующие добавки ингибируют процессы гидролиза ATF как при комнатной температуре, так и в условиях стерилизации.
Наилучшие результаты получены для растворов, содержащих в качестве добавки лимонную и винную кислоты.
Важнейшим преимуществом лимонной кислоты является не только то, что необходимое количество для доведения рН минимальны (поскольку она является трехосновной кислотой с достаточно низким рК) и после стерилизации препарат содержит наибольшее количество ATF, но и то, что цитрат, как известно, является достаточно эффективным антикоагулятором и дезагрегантом крови и поэтому предотвращает сгусткообразование. Поэтому с точки зрения практического применения добавка лимонной кислоты представляет наибольший интерес.
В процессе хранения полученных растворов субстанции ATF-ЛОНГ (табл. 3) скорость уменьшения содержания в них АТА меньше по сравнению с 1%-ным раствором динатриевой соли.
Сравнительное изучение хранения 1%-ного раствора Na2ATF и предложенных инъекционных растворов показало, что в предложенных растворах ATF дольше сохраняется в исходном виде, что открывает возможность увеличения срока годности предлагаемой инъекционной формы по сравнению с 1%-ным раствором Na2ATF.
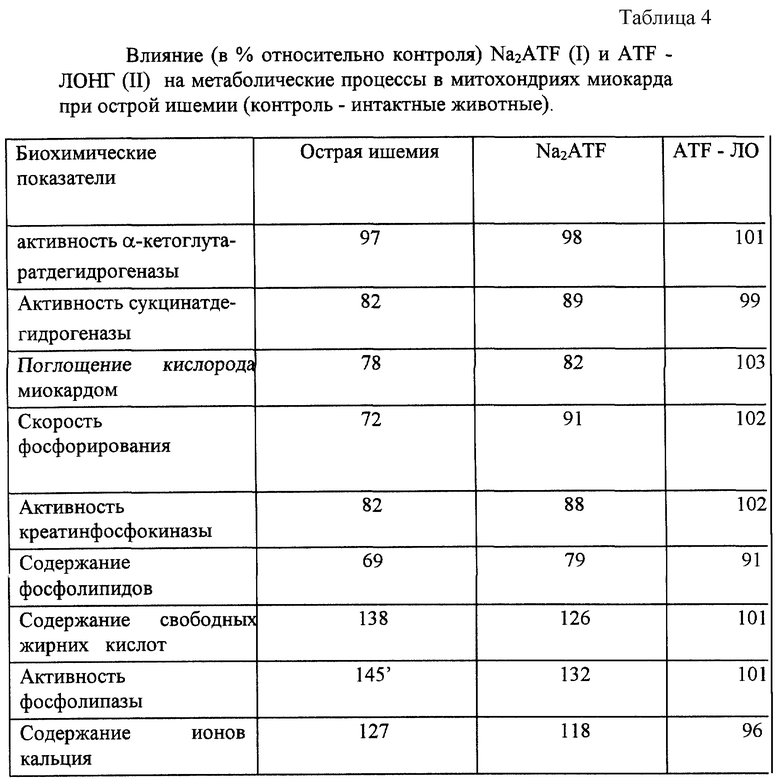
Учитывая то обстоятельство, что в субстанции препарата ATF-ЛОНГ содержание ATF (в том числе адениннуклеотидов) составляет около 46%, а в 2%-ном растворе препарата ATF-ЛОНГ содержание ATF приблизительно такое же, как и в 1%-ном растворе динатриевой соли ATF. Вместе с тем, результаты многочисленных биологических испытаний показали, что ATF-ЛОНГ значительно более эффективен (табл. 4, 5). Даже при введении в одинаковой дозе (0,3 мг/кг массы животных) динатриевой соли ATF и ATF-ЛОНГ (в этом случае содержание ATF в растворе ATF-ЛОНГ в два раза меньше, чем в растворе динатриевой соли ATF) биологические эффекты в случае ATF-ЛОНГ были значительно выше.
В табл. 4 приведены некоторые сравнительные данные для растворов Na2ATF (1%-ный раствор для инъекций) и ATF-ЛОНГ (1%-ный раствор с добавкой цитрата, рН 7,37).
Из приведенных данных видно, что инъекционный раствор ATF-ЛОНГ проявляет ярко выраженный энергосберегающий а также мембраностабилизирующий эффект.
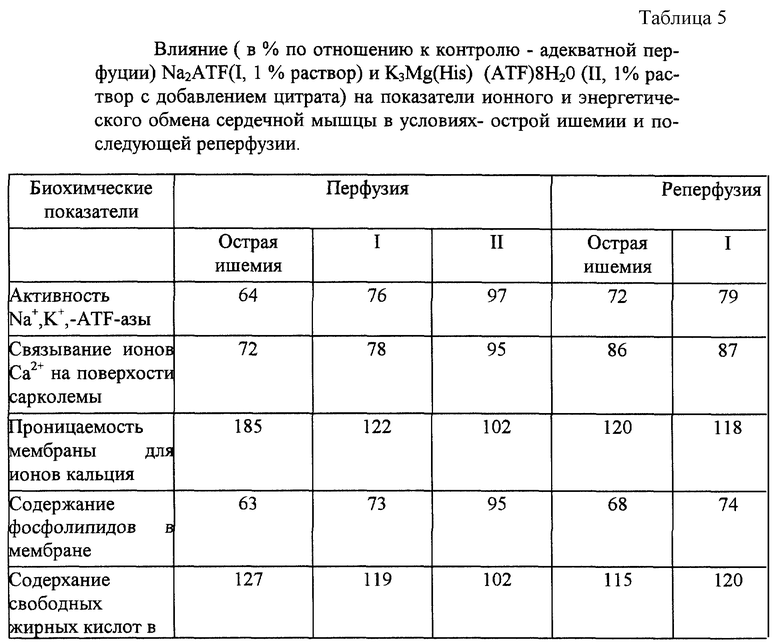
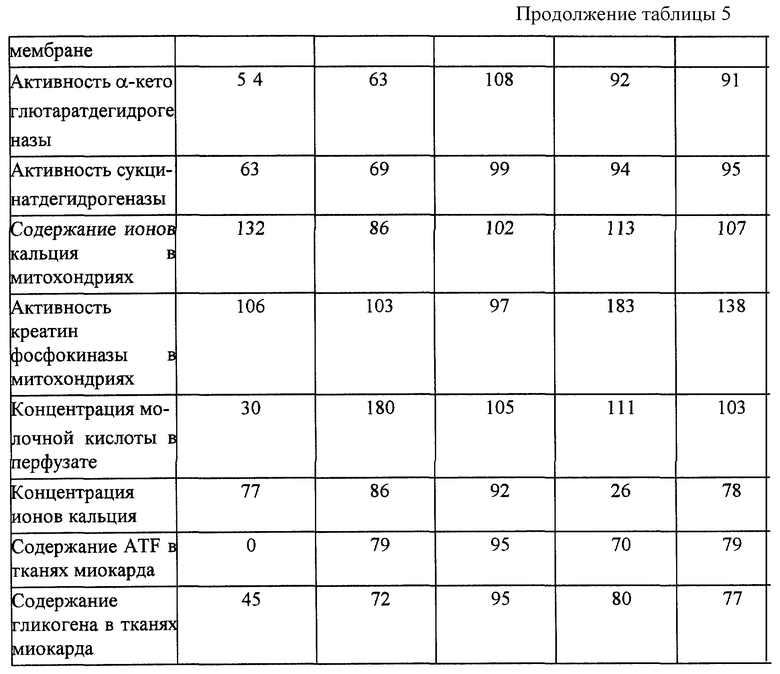
Предварительное введение в перфузионную жидкость ATF-ЛОНГ также предупреждает возникновение или снижает степень выраженности сдвигов энергетического или ионного метаболизма миокарда в условиях ишемии и гипоксии (табл. 5). Это проявляется, например, в предупреждении снижения уровня фосфолипидов мембран (на 35% от контроля) и накоплении в них свободных жирных кислот (102% от контроля), что можно оценить как мембраностабилизирующий эффект. Соответствующие показатели при введении Na2ATF составляют 73 и 119%. При этом проницаемость мембран для ионов кальция в случае ATF-ЛОНГ очевидно не отличается от контроля (в случае Na2ATF она на 22% выше контроля). Благодаря сохранению липидного слоя мембран при введении ATF-ЛОНГ на постоянном уровне (97% от контроля) поддерживается активность мембраносвязанного фермента Na+, К+, ATF-азы сарколемы (для Na2ATF этот показатель составляет всего 76%). Под влиянием ATF-ЛОНГ внешняя мембрана кардиомиоцита сохраняет способность связывать ионы кальция (95%), то есть улучшаются процессы энергообеспечения ионного транспорта в клетках. В случае Na2ATF этот показатель на 22% ниже контроля. Состав ATF и гликона в сердечной мышце при введении ATF-ЛОНГ составляет соответственно 90 и 95% от исходного уровня, что выше, чем в случае Na2ATF (79 и 72% соответственно). Благодаря полученным эффектам Na2ATF-ЛОНГ в период постишемической реперфузии протекает более эффективно и показатели энергетического и ионного метаболизма сердца до 30 секунд в основном нормализуются и, вероятно, не отличаются от исходных величин (табл. 5). При этом отмечается незначительный выход КФК в перфузионную жидкость и снижение в ней концентрации ионов кальция, что указывает на сохранение барьерных свойств мембран и меньшую степень их поражения в условиях реперфузии.
Из данных, приведенных в табл. 4 и 5, видно, что инъекционный раствор ATF-ЛОНГ (1 и 2%) обладает выраженным антиишемическим действием, которое значительно больше по сравнению с 1% раствором Na2ATF для инъекций.
Изобретение поясняется примером конкретного выполнения.
Пример
10 г ATF-ЛОНГ поместили в 1 л изотонического раствора (9 г NaCl в 1 л дистиллированной воды), после чего добавили лимонной кислоты в количестве 0,8 г, в результате чего раствор приобрел рН 7,2. Затем полученный раствор поместили в ампулы по 0,2 мл, ампулы запаяли и провели их стерилизацию.
Свойства полученного препарата подтверждаются данными, приведенными в табл.2-5.
Таким образом, предложенная инъекционная форма препарата, обладающего противишемической активностью, проявляет высокие лечебные и профилактические свойства, отличается высокими биохимическими показателями, необходимой стабильностью и, соответственно, повышенными в несколько раз сроками хранения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАЛИЕВЫЕ СОЛИ РАЗНОЛИГАНДНЫХ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ МАГНИЯ С ГИСТИДИНОМ, АДЕНОЗИН-5'-ТРИФОСФАТОМ И КРЕАТИНФОСФАТОМ, ПРОЯВЛЯЮЩИЕ ЗАЩИТНОЕ ДЕЙСТВИЕ НА МИОКАРД ОТ ИШЕМИЧЕСКОГО ПОВРЕЖДЕНИЯ | 1997 |
|
RU2144922C1 |
| ПРОИЗВОДНЫЕ β- ГИДРОКСИЭТИЛАМИНИЙНИКОТИНАТА, ПРОЯВЛЯЮЩИЕ ПРОТИВОИШЕМИЧЕСКУЮ АКТИВНОСТЬ | 1993 |
|
RU2124502C1 |
| КОМПОЗИЦИЯ УБИХИНОЛА ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2016 |
|
RU2635993C1 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 1994 |
|
RU2118161C1 |
| ВОДНЫЙ РАСТВОР НИТРОГЛИЦЕРИНА ДЛЯ ИНФУЗИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1993 |
|
RU2092158C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИКОРРОЗИОННОГО ПИГМЕНТА НА ОСНОВЕ ТРИФОСФАТА АЛЮМИНИЯ | 1995 |
|
RU2102420C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИШЕМИИ МОЗГА | 1994 |
|
RU2108095C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМОГО ЛИОФИЛИЗАТА 4-(3-ОКСО-3-ЭТОКСИПРОПАНОИЛ)АМИНО)БЕНЗОЙНОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЙ АНТИИШЕМИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2602665C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИФИДУМБАКТЕРИНА КОНЦЕНТРИРОВАННОГО | 1993 |
|
RU2072856C1 |
| ИНЪЕКЦИОННАЯ ФОРМА ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ (ВАРИАНТЫ) ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ НЕРВНОЙ СИСТЕМЫ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2010 |
|
RU2448706C2 |

Препарат изготовлен на основе аденозин-5'-трифосфата в изотоническом растворе. В качестве источника аденозин-5'-трифосфата препарат содержит трикалиевую соль аденозин-5'-трифосфатогистидинатомагний (II) октагидрат в количестве 10-20 г на 1000 мл изотонического раствора. Препарат дополнительно содержит фармацевтически приемлемую органическую или неорганическую кислоту или ее кислую соль в количестве, необходимом для достижения рН 7,0-7,4. Предпочтительно в качестве фармацевтически приемлемой органической кислоты препарат содержит лимонную кислоту в количестве 0,6-1,2 г на 1000 мл изотонического раствора. Препарат в виде инъекционной формы обеспечивает высокое лечебно-профилактическое действие и имеет увеличенный срок хранения. 1 з.п.ф-лы, 5 табл.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - Минск: Беларусь, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| SU 755201, 07.08.1980 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| UA 96124897, 29.08.1999 | |||
| RU 97119808 A1, 27.08.1999 | |||
| КАЛИЕВЫЕ СОЛИ РАЗНОЛИГАНДНЫХ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ МАГНИЯ С ГИСТИДИНОМ, АДЕНОЗИН-5'-ТРИФОСФАТОМ И КРЕАТИНФОСФАТОМ, ПРОЯВЛЯЮЩИЕ ЗАЩИТНОЕ ДЕЙСТВИЕ НА МИОКАРД ОТ ИШЕМИЧЕСКОГО ПОВРЕЖДЕНИЯ | 1997 |
|
RU2144922C1 |
Авторы
Даты
2002-10-10—Публикация
1999-03-18—Подача