Изобретение относится к медицине, а именно к онкологии, и может найти применение при лечении злокачественных заболеваний.
В общей структуре заболеваемости злокачественными новообразованиями лимфогранулематоз (ЛГМ) занимает шестое место с преобладанием среди мужчин по сравнению с женщинами в 1,5 раза [М.Л. Гершанович, в кн.: Клиническая онкология для семейного врача. С.-Пб., 1995]. Из всех заболевших ЛГМ около 50% случаев приходятся на возрастной период между 20 и 40 годами, т.е. на наиболее трудоспособный возраст. При современных методах лучевого и химиолучевого лечения порядка 80% больных ЛГМ потенциально излечимы. В связи с этим, наряду со стремлением к увеличению продолжительности жизни, повышенное внимание должно уделяться и обеспечению высокого качества жизни больных ЛГМ. Главными факторами, влияющими на ухудшение качества жизни больных ЛГМ после проведенного лучевого лечения, являются ранние и поздние лучевые осложнения (пульмониты, пневмофиброзы, миелиты, перикардиты, вторые опухоли) со стороны критических нормальных тканей, которыми при ЛГМ являются легкие, спинной мозг, сердце. Риск радиационных повреждений может повышаться при комбинации облучения органов грудной клетки с полихимиотерапией.
Одним из основных методов лечения больных ЛГМ является крупнопольная лучевая терапия, которая в большинстве онкорадиологических центров осуществляется режимом стандартного ежедневного облучения (1,8-2 Гр/5 раз в неделю) до суммарной очаговой дозы (СОД) 40-45 Гр на манифестированные лимфатические узлы [Виноградов В. М., Ритила А., В кн.: Лимфогранулематоз. Под ред. Л.П. Симбирцева, Л. Холсти. М.: Медицина, 1985, с. 198; Kaplan H. Hodgkin's Disease. Harvard University Press, Cambridge, 1980]. Эта методика лучевой терапии позволила увеличить 5-летнюю выживаемость больных ЛГМ до 70-75% [Kaplan H. In: Cancer. A Comprehensive Treatise. Ed. F.F. Becker. Plenum Press, New York etc., 1977. - Vol. 6. - P. 29]. При этом в 13-50% случаев диагностировались лучевые пульмониты, а в 37,6-95% случаев локальный пневмофиброз, степень тяжести которого обычно не указывается [Канаев С.В. и др. Вопр. онкол. - 1986. - 5.-С.50; Байсоголов и др. Мед. радиол. - 1983. - 10. - С. 22; Frija J. et al. Eur. J. Radiol. - 1988. - V. 8. - P. 18-23].
Наиболее близким к предлагаемому является способ крупнопольной лучевой терапии с ускоренным мультифракционированием дозы, используемый в Центральном научно-исследовательском рентгенорадиологическом институте (ЦНИРРИ, Санкт-Петербург): облучение двумя фракциями в день с интервалом между фракциями 3-4 ч разовой очаговой дозой 1,35 Гр на средостение и СОД 40-44 Гр [Ильин Н. В., Оптимизация методов лучевой терапии лимфогранулематоза. Автореф. дисс. С-Пб., 1993; Ильин Н.В. и др. В кн.: Медицинская физика-97. Новые технологии в радиационной онкологии. Тез.докл. -Обнинск, 1997.-С. 48]. Значения разовой дозы и интервала между фракциями выбраны эмпирически. Этот режим дозного фракционирования у больных ЛГМ показал хорошую терапевтическую эффективность в отношении снижения частоты рецидивов с 19,7% до 11,8%; пульмонитов с 48,7% до 19,6%, и хотя общая частота легочных фиброзов составляла 90-95%, но частота тяжелых легочных фиброзов (3-й степени поражения), приводящих к инвалидизации больного, снизилась до 3,9% по сравнению с 11,4% при стандартном фракционировании [Коврыжкина Т.А. и др., Мед.радиология, 1997, 3, с. 59-63].
Технический результат настоящего изобретения состоит в снижении числа лучевых осложнений за счет оптимизации разовой очаговой дозы и уменьшения дозных нагрузок на критические ткани.
Этот результат достигается проведением химио- и/или лучевой терапии ускоренным мультифракционированием (МФ) двумя фракциями в день на средостение, при котором интервал между фракциями составляет 4 часа, разовая доза на средостение 1,2 Гр, суммарная очаговая доза 30-36 Гр.
Занимаясь профессионально в течение многих лет лечением больных ЛГМ посредством лучевой терапии и наблюдая у них тяжелые лучевые осложнения, мы попробовали изменить условия проведения лучевого лечения. На основании радиобиологических параметров, а именно времени половинной репарации T1/2 внутриклеточных лучевых повреждений основных критических (дозно-лимитирующих) нормальных органов, которыми при лечении больных лимфогранулематозом являются спинной мозг и легкое, и на основании выбранного нами интервала между фракциями (t= 4 ч) мы предложили формулу расчета разовой очаговой дозы (d) на средостение: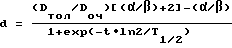
где Dтол - толерантная доза для спинного мозга и легких при стандартном режиме фракционирования, Гр;
Doч - суммарная поглощенная доза в очаге при стандартном режиме фракционирования, Гр;
(α/β) - радиобиологический параметр, характеризующий зависимость лучевой толерантности ткани от дозы за фракцию, Гр;
t - длительность интервала между фракциями, ч;
Т1/2 - время половинной репарации внутриклеточных повреждений критической ткани, ч.
В результате количественного анализа многочисленных клинических и экспериментальных данных по лучевым пульмонитам и миелитам с использованием метода математической оптимизации нами были определены значения Т1/2=0,5 ч для клеток легочной паренхимы и T1/2=3,0 ч для клеток спинного мозга, которые отличаются от известных значений, полученных на лабораторных животных (соответственно 1,5 ч и 1,0 ч) [Thames H.D., Hendry J.H. Fractionation in Radiotherapy. London, 1987].
Современные клинические данные свидетельствуют о том, что оптимальным значением суммарной очаговой дозы (Dоч) при крупнопольной технике облучения стандартным курсом лучевой терапии ЛГМ является величина 35 Гр [Mendenhall N. P. Cancer. - 1999. - Vol. l7. - Р. 47]. Используя формализацию линейно-квадратичной модели с коррекцией на скорость репарации внутриклеточных повреждений (T1/2) при интервале между фракциями t=4 ч нами установлены значения d, которые позволяют проводить лучевую терапию больных ЛГМ, не превышая толерантность легких и спинного мозга. Значения α/β, равные 3,07 Гр и 1,7 Гр соответственно для радиационных повреждений легких и спинного мозга и Dтол= 30-32 Гр, взяты из литературы [Ang K.K. et al. Radiation Research 1895-1995. Congress Proceeding. 1995. - Vol. 2. - P. 874; Dubray В. et al. Radiother. Oncol. -1995.Vol.36.-P.211]. Полагая в приведенной формуле Dоч=35 Гр, Dтол= 32 Гр, T1/2=0,5 ч и 3,0 ч и показатели α/β, приведенные выше, находим d= l, 2 Гр при интервале между фракциями 4 ч для курса ускоренного мультифракционирования.
Сущность способа поясняется примерами.
Пример 1.
Больная Д. , 51 год, история болезни 452, поступила в клинику ЦНИРРИ 16.02.2000 г. с диагнозом: лимфома, жалобы на увеличение надключичных лимфатических узлов. Из анамнеза выявлено, что больная сама обнаружила увеличение лимфоузлов на шее справа около года назад, узлы медленно росли. Биопсия увеличенных лимфоузлов была произведена 2.02.2000 г. в Санкт-Петербургском НИИ фтизиопульмонологии. Пересмотр препаратов в ЦНИРРИ КМ-133 245-248 - лимфогранулематоз, нодулярный склероз.
При поступлении больной - состояние удовлетворительное. Кожа обычной окраски, определяются увеличенные лимфоузлы на шее справа размером 2•3 см, рубец после биопсии. Щитовидная железа не увеличена, узлов нет. Пульс 74 ритм, АД 120/80 мм. Тоны сердца ясные, чистые, отеков нет, дыхание везикулярное, хрипов нет. Язык чистый, миндалины не увеличены, живот мягкий, безболезненный. Печень и селезенка не увеличены.
При обследовании больной выполнены рентгенотомография грудной клетки, компьютерная томография живота, сцинтиграфия печени и селезенки, скелета, лимфосцинтиграфия, общий и биохимический анализ крови, анализ мочи, ультразвуковое исследование органов живота и забрюшинного пространства. Выявлено увеличение лимфоузлов в правой надключичной области и умеренное увеличение лимфоузлов средостения. На основании проведенного исследования установлен диагноз: лимфогранулематоз, нодулярный склероз, клиническое стадирование II А.
Лечение начато с 29.02.2000 г. с крупнопольной лучевой терапии, облучение лимфоколлекторов выше диафрагмы (мантиевидное облучение) на линейном ускорителе электронов SL-75-5 в тормозном режиме с граничной энергией 6 МэВ по методике мультифракционирования, разовой дозой на средостение 1,2 Гр два раза в день, интервал 4 часа. Лечение продолжалось в течение 13 дней. Суммарная очаговая доза составила на средостение 36 Гр. Лечение перенесла хорошо, тошноты и рвоты не было.
При выписке: достигнута полная клиническая ремиссия - лимфатические узлы не определяются, лучевых легочных осложнений не выявлено, цитопении нет.
К настоящему времени (16.05.2000) больная находится в ремиссии, увеличенных лимфатических узлов не определяется, лучевых легочных и иных осложнений нет.
Пример 2.
Больная Я., 20 лет, 299 впервые поступила в клинику ЦНИРРИ 1.02.2000 г. с диагнозом лимфогранулематоз. Из анамнеза известно, что больная сама обнаружила увеличение лимфоузлов на шее. Биопсия лимфоузла в правой надключичной области к-4148-50 от 16.06.99 г. в МСЧ 70: лимфогранулематоз, нодулярный склероз, клиническое стадирование II А. В больнице 31 (в июле 1999 г.) получила 2 цикла полихимиотерапии COPP-ABVD (полный регресс периферических лимфоузлов после 1 курса).
При поступлении в ЦНИРРИ - состояние удовлетворительное. Кожа обычной окраски, рубец в правой надключичной области после биопсии. Щитовидная железа не увеличена, узлов нет. Пульс 84' ритм, АД 110/80 мм. Тоны сердца ясные, чистые, отеков нет, дыхание везикулярное, хрипов нет. Язык чистый, миндалины не увеличены, живот мягкий, безболезненный. Печень и селезенка не увеличены.
При обследовании выполнены рентгенотомография грудной клетки, компьютерная томография живота, сцинтиграфия печени и селезенки, скелета, лимфосцинтиграфия, общий и биохимический анализ крови, анализ мочи, ультразвуковое исследование органов живота и забрюшинного пространства. Выявлено поражение лимфоузлов в правой надключичной области и лимфоузлов средостения.
Диагноз: Лимфогранулематоз, нодулярный склероз, клиническое стадирование IIA.
Лечение начато 14.02.2000 г. с крупнопольной лучевой терапии, облучение лимфоколлекторов выше диафрагмы (мантиевидное облучение) на линейном ускорителе электронов SL-75-5 в тормозном режиме с граничной энергией 6 МэВ по методике мультифракционирования разовой дозой 1,2 Гр два раза в день, интервал 4 часа. Лечение продолжалось в течение 14 дней. Подведена суммарная очаговая доза на средостение, равная 33,6 Гр. Лечение перенесла хорошо, тошноты и рвоты не было.
При выписке: достигнута полная клиническая ремиссия - лимфатические узлы не определяются, лучевых легочных осложнений не выявлено, цитопении нет.
На контрольных осмотрах (20.03., 24.04. и 22.05.2000) увеличенные лимфатические узлы не определялись, лучевые легочные и иные осложнения не выявлены. Больная находится в ремисси.
Пример 3.
Больной О. , 19 лет, история болезни 86, поступил в клинику ЦНИРРИ 10.01.2000 г. с диагнозом лимфогранулематоз. Из анамнеза известно, что в ноябре 1999 г. больной заметил ассиметрию в области шеи. Биопсия увеличенных лимфоузлов была произведена 17.12.1999 г. в г.Тихвин Ленинградской области, по месту жительства. При поступлении больного: состояние удовлетворительное. Кожа обычной окраски, определяется увеличенный лимфоузел в правой надключичной области размером 6 см в диаметре, рубец после биопсии. Сердечные тоны ритмичные, звучные. Щитовидная железа не увеличена, узлов нет. Пульс 66 ритм, АД 120/80 мм. Тоны сердца ясные, чистые, отеков нет, дыхание везикулярное, хрипов нет. Язык чистый, миндалины не увеличены, живот мягкий, безболезненный. Печень и селезенка не увеличены.
При обследовании в ЦНИРРИ: рентгенотомография грудной клетки, компьютерная томография живота, сцинтиграфия печени и селезенки, скелета, лимфосцинтиграфия, общий и биохимический анализ крови, анализ мочи, ультразвуковое исследование органов живота и забрюшинного пространства, выявлены поражение правых шейно-надключичных, подмышечных лимфоузлов, лимфоузлов средостения, тимуса, паратрахеальных и подвздошных, забрюшинных лимфоузлов. Пересмотр препаратов: КМ 131786-89 от 28.12.99 - лимфогранулематоз, нодулярный склероз.
Диагноз: Лимфогранулематоз, нодулярный склероз, клиническое стадирование IIIА (12.99).
Лечение начато с 17.01.2000 г. с крупнопольной лучевой терапии, облучение лимфоколлекторов выше диафрагмы (мантиевидное облучение) на линейном ускорителе электронов SL-75-5 в тормозном режиме с граничной энергией 6 МэВ по методике мультифракционирования разовой дозой 1,2 Гр два раза в день, интервал 4 часа. Лечение продолжалось в течение 13 дней. Подведена суммарная очаговая доза на средостение 31,2 Гр. Лечение перенес хорошо, тошноты и рвоты не было.
При выписке: достигнута клиническая ремиссия, цитопении нет. Лучевые легочные осложнений не выявлены. Явка через месяц для проведения химиотерапии.
20.03.2000 - больной госпитализирован повторно. Проведено два курса полихимиотерапии (COPP/ABVD). Лечение перенес удовлетворительно. Патологических изменений со стороны легких не выявлено, цитопении нет.
На контрольном осмотре 24.04.2000: увеличенных лимфатических узлов не определяется, лучевых легочных и иных осложнений не выявлено. До настоящего времени (16.05.2000) больной находится в ремиссии.
К настоящему времени предлагаемым способом проведено лечение 11 больных ЛГМ II А - III А стадий. Все больные находятся в клинической ремиссии. Ни у одного из них до настоящего времени (в течение 5 месяцев) не выявлены лучевые осложнения. Поскольку ранние лучевые реакции проявляются, как правило, во время или в ближайщие сроки после окончания лучевого лечения, а в предлагаемом способе они не обнаружены (на наш взгляд, ввиду более низкой дозной нагрузки), можно надеяться на то, что и в более поздние сроки лучевые осложнения не появятся, или если появятся, то у меньшего числа пациентов.
Основными преимуществами предлагаемого способа по сравнению с известными являются:
1. Способ сокращает длительность курса лучевой терапии, что снижает вероятность репопуляции опухолевых клеток, которая возможна при длительном фракционированном облучении больных ЛГМ, что предупреждает возможность рецидивирования опухоли.
2. Способ снижает выраженность и частоту лучевых легочных повреждений, а именно острых пульмонитов, т. е. ранних лучевых повреждений и, благодаря снижению дозной нагрузки на легкие, позволяет надеяться на уменьшение числа локальных пневмофиброзов.
3. Снижение дозовых нагрузок на нормальные ткани позволяет в дальнейшем без перерыва проводить химиотерапию с меньшей опасностью для пациента в отношении усиления токсических эффектов от лучевого компонента, в то время как в известных способах комбинированного лечения нередко приходится прерывать курс химиотерапии.
Способ разработан сотрудниками НИИ онкологии и ЦНИРРИ и прошел клиническую апробацию в отделении лучевой терапии системных заболеваний и лучевой патологии ЦНИРРИ у 11 больных с положительным результатом.
Способ может быть использован в медицине, а именно в онкологии. Проводят химио- и/или лучевую терапию. Лучевое лечение осуществляют ускоренным мультифракционированием двумя фракциями в день с интервалом между фракциями 4 ч, разовой дозой на средостение 1,2 Гр до суммарной очаговой дозы 30-36 Гр. Способ позволяет уменьшить частоту ранних лучевых легочных осложений без опасности возникновения тяжелых побочных эффектов.
Способ лечения лимфогранулематоза посредством химио- и/или лучевой терапии, причем лучевую терапию осуществляют ускоренным мультифракционированием двумя фракциями в день на средостение, отличающийся тем, что мультифракционирование проводят с интервалом между фракциями 4 ч, разовой очаговой дозой на средостение 1,2 Гр до суммарной очаговой дозы 30-36 Гр.
| ИЛЬИН Н.В | |||
| Оптимизация методов лучевой терапии лимфогранулематоза | |||
| Автореф | |||
| дисс | |||
| - С.-Пб | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| RU 2062102 С1, 20.06.1996 | |||
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМИ ФОРМАМИ РАКА | 1994 |
|
RU2098154C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ПОЛОСТИ РТА | 1997 |
|
RU2128060C1 |
Авторы
Даты
2002-10-20—Публикация
2000-05-29—Подача