Изобретение относится к симметрическим производным триазина, к получению этих соединений, а также к их использованию для защиты органических материалов от вредных воздействий ультрафиолетового излучения.
O-алкилированные о-гидроксифенилтриазины (ГФТ), содержащие по крайней мере одну о-гидроксильную группу или по крайней мере два алкоксифенил-заместителя, известны, например, из заявки на Европейский патент 0743309 в качестве косметических абсорберов ультрафиолетового излучения, имеющих хорошие спектральные свойства и хорошие свойства для технического применения. Однако получение таких производных триазина, которые происходят из несимметрической основной структуры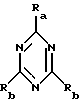
требует проведения многоэтапных процессов синтеза.
В вышеприведенной формуле каждый Ra и Rb обозначает реакционноспособный радикал, в частности фенильный радикал, который является одно- или многозамещенным при помощи гидроксильных групп.
К симметрическим производным триазина, которые могут быть получены из симметрической основной структуры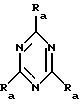
можно легко получить доступ в простых однократных процессах.
Такие "основные структуры триазина" могут быть получены, например, тримеризацией соответствующих соединений бензонитрила или, начиная с цианурхлорида, путем реакции Гриньяра или алкилирования Фриделя-Крафтса. Последующая этерификация свободных групп ОН дает возможность получить желательные производные триазина в процессе двухэтапной реакции.
В соответствии с этим настоящее изобретение относится к симметрическим производным триазина формулы
где R1 и R2 - одинаковые и обозначают водород или С1-С5-алкил; R3 - C1-C12-aлкокси.
C1-C12-алкил или С1-С12-алкокси обозначает прямоцепочечный или разветвленный радикал алкила, обычно метил, этил, н-пропил, изопропил, втор-бутил, трет-бутил, амил, изоамил или трет-амил, гептил, октил, изооктил, нонил, децил, ундецил или додецил, либо метокси, этокси, пропокси, бутокси, пентилокси, гексилокси, гептилокси, октилокси, нонилокси, децилокси, ундецилокси или додецилокси.
Особенно предпочтительны соединения формулы (1), в которых R3 обозначает С5-С12-алкокси, a R1 и R2 имеют значения, приведенные в формуле (1).
Производные триазина в соответствии с настоящим изобретением могут быть использованы в качестве отдельных соединений или в качестве смесей различных отдельных соединений друг с другом.
Новые симметрические производные триазина формулы (1) могут, в частности, также быть использованы в виде смесей с соединениями триазина формулы (4)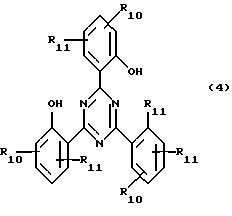
где R10 обозначает водород, С6-С12-алкил или С2-С6-алкенил, а R11 обозначает С1-С12-алкокси.
С2-С6-Алкенил обозначает, например, аллил, металлил, изопропенил, 2-бутенил, 3-бутенил, изобутенил, н-пента-2,4-диенил или 3-метил-бут-2-енил.
Новые производные триазина формулы (1) можно получить различными способами. В реакции Гриньяра, например, 1 моль цианурхлорида подвергают взаимодействию с 3 молями соответствующего соединения фенилмагний бромида, которое в зависимости от значения R1, R2 и R3 в формуле (1), может содержать радикал алкила и/или одну или несколько свободных групп гидроксила. Способы получения этого промежуточного соединения известны и описаны, между прочим, в заявке на Европейский патент 0557559.
Данное промежуточное соединение также получают путем алкилирования Фриделя-Крафтса цианурхлорида с соответствующим соединением фенила формулы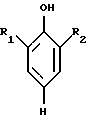
где R1 и R2 - водород или C1-C5 алкил, в присутствии кислоты Льюиса, предпочтительно алюминий хлорида.
В соответствии с работой A. Ninagawa, M. Kawazoe, H. Matsuda, Makromol. Chem. 180 (1979), 2123, это промежуточное соединение также получают циклотримеризацией соединения бензонитрила формулы
где R1 и R2 - водород или C1-C5 алкил.
Конечные продукты, соответствующие формуле (1), получают на второй стадии реакции этерификацией свободных гидроксильных групп промежуточных соединений, полученных на первой стадии реакции, алкилирующим агентом НаlR3, где R3 - С1-С12-алкокси, в соответствии с традиционными способами.
Другой предмет настоящего изобретения относится к способам получения новых производных триазина.
Симметрические производные триазина формулы (1) или смеси этих соединений с соединениями триазина формулы (4), а также соединениями формулы (5)
где Аr обозначает радикал формулы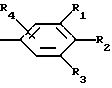
R1 обозначает водород, гидрокси, С1-С12-алкил или С1-С12-алкокси;
R2 обозначает гидрокси, С1-С12-алкокси; или бензилокси;
R3 обозначает гидрокси, С1-С12-алкил или С1-С12-алкокси; и
R4 обозначает водород или С1-С12-алкокси; или
R1 и R2 вместе с радикалом фенила обозначают гетероциклическое пятичленное кольцо, которое конденсировано бензолом, предпочтительно радикалом формулы (5а),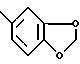
особенно пригодны в качестве фильтров ультрафиолетового излучения, то есть для защиты чувствительных к ультрафиолету органических материалов, в особенности кожи и волос людей и животных, от вредных воздействий ультрафиолетового излучения.
Характерными примерами соединений формулы (5) являются

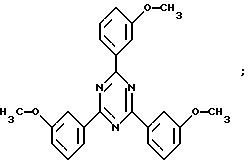

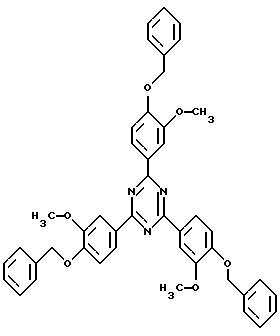
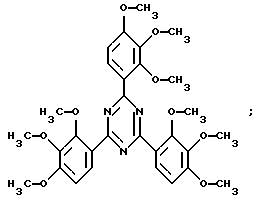

В соответствии с этим данные соединения пригодны в качестве стабилизаторов света в косметических, фармацевтических и ветеринарных препаратах. Они могут быть получены в растворенной форме или, если они являются лишь умеренно растворимыми или нерастворимыми, они могут быть введены в препараты в измельченном виде со средним размером частиц в диапазоне от 0,02 до 2, предпочтительно от 0,05 до 1,5 и наиболее предпочтительно от 0,1 до 1,0 мкм.
Помимо новых абсорберов ультрафиолетового света, косметические составы могут также содержать одно или более одного из числа других соединений, защищающих от ультрафиолетового излучения и входящих в следующие классы веществ:
1) производные пара-аминобензойной кислоты, обычно 2-этилгексил 4-диметиламинобензоат;
2) производные салициловой кислоты, обычно 2-этилгексил салицилат;
3) производные бензофенона, обычно 2-гидрокси-4-метоксибензофенон и производные его 5-сульфокислоты;
4) производные дибензоилметана, обычно 1-(4-трет-бутилфенил)-3-(4-метоксифенил)пропан-1,3-дион;
5) дифенилакрилаты, обычно 2-этилгексил-2-циано-3,3-дифенилакрилат и 3-(бензофуранил)-2-цианоакрилат;
6) 3-имидазол-4-ил-акриловая кислота и 3-имидазол-4-ил-акрилат;
7) производные бензофурана, предпочтительно производные 2-(пара-аминофенил)бензофурана, раскрытые в заявке на европейский патент 582189; патенте США 5338539; патенте США 5518713 и в заявке на европейский патент 613893;
8) полимерные абсорберы ультрафиолетового света, такие как производные бензилиденмалоната, описанные, между прочим, в заявке на европейский патент 709080;
9) производные коричной кислоты, обычно 2-этилгексил 4-метоксициннамат или изоамилат, либо производные коричной кислоты, раскрытые, между прочим, в патенте США 5601811 и заявке на патент РСТ WO 97/00851;
10) производные камфоры, обычно 3-(4'-метил)-бензилиденборнана-2-он, 3-бензилиденборнан-2-он, N-[2(и 4)-2-оксиборн-3'-илиденметил) бензил]акриламидный полимер, 3-(4'-триметиламмоний)бензилиденборнан-2-онеметилсульфат, 3,3'-(1,4-фенилендиметин)-бис-(7,7 -диметил-2-оксо-бицикло- [2,2,1] -гептан-1-метансульфокислота) и ее соли, 3-(4'-сульфо)-бензилиденборнан-2-он и его соли;
11) производные трианилино-втор-триазина, 2,4,6-трианилин-(пара-карбо-2'-этил-1'-окси)-1,3,5-триазины, а также абсорберы ультрафиолетового света, раскрытые в патенте США 5332568, в заявке на европейский патент 517104, в заявке на европейский патент 507691, в заявке на патент РСТ WO 93/17002 и в заявке на европейский патент 570838;
12) производные 2-гидроксифенилбензотриазола;
13) 2-фенилбензимидазол-5-сульфокислота и ее соли;
14) ментил-орто-аминобензоат;
15) TiO2 (c различными покрытиями), ZnO и слюда.
Абсорберы ультрафиолетового света, описанные в работе "Sunscreens", Eds. N. J. Lowe, N. A. Shaath, Marcel Dekker, Inc., New York and Basel, Cosmetics & Toiletries (107) 50 et seq. (1992), также могут быть использованы в качестве дополнительных защитных средств от ультрафиолетового излучения в предлагаемых составах.
Косметические составы также могут использоваться вместе с известными антиокислителями, такими как витамин Е, каротиноиды или пространственно-затрудненные амиды, служащие светостабилизаторами для полимеров.
Новые косметические составы обычно содержат от 0,1 до 25, предпочтительно от 0,5 до 10% по массе, на основе общей массы композиции, абсорбера ультрафиолетового излучения формулы (1) или (5) или смеси абсорберов ультрафиолетового излучения формулы (1) и формулы (4), а также косметически совместимое вспомогательное вещество.
Косметические составы могут быть получены за счет физического смешивания абсорбера (абсорберов) ультрафиолетового излучения со вспомогательной добавкой традиционными способами, например путем простого смешивания отдельных компонентов.
Косметические составы могут быть приготовлены в виде эмульсии типа вода в масле или масло в воде, в виде лосьона типа масло в спирте, в виде ячеистой (пористой) дисперсии ионогенного или неионогенного амфифильного липида, в виде геля, твердого шаровидного препарата или в виде аэрозольного состава.
В качестве эмульсии типа вода в масле или масло в воде косметически совместимое вспомогательное вещество предпочтительно содержит от 5 до 50% масляной фазы, от 5 до 20% эмульгатора и от 30 до 90% воды. Масляная фаза может содержать любое масло, пригодное для косметических составов, например одно или несколько углеводородных масел, парафин, натуральное масло, силиконовое масло, сложный эфир жирной кислоты или жирный спирт. Предпочтительными моно- или полиолями являются этанол, изопропанол, пропиленгликоль, гексиленгликоль, глицерин и сорбит.
Косметические составы для волос могут присутствовать
- в виде шампуня, лосьона, геля или эмульсии для промывки, до или после лечения шампунем, до или после крашения или удаления красителя, до или после процесса перманента или распрямления волос;
- в виде лосьона, пены или геля для укладки или лечения волос;
- в виде лосьона или геля для прически или завивки волос;
- в виде лака для волос;
- в виде композиции для перманента или распрямления волос, для крашения или удаления красителя.
Что касается волос, то есть возможность использовать, например, следующие косметические составы:
a1) спонтанно эмульгирующие исходные составы, содержащие абсорбер ультрафиолетового излучения, эскиолеат сорбитана и С10-оксоспирт ПЭГ-6, который нагружен водой и любым соединением четвертичного аммония, таким как 4% минкамидопропилдиметил-2-гидроксиэтил аммония хлорид или Quaternium 80;
a2) спонтанно эмульгирующие исходные составы, содержащие абсорбер ультрафиолетового излучения, трибутил цитрат и моноолеат сорбитана ПЭГ-20, который нагружен водой и любым соединением четвертичного аммония, таким как 4% минкамидопропилдиметил-2-гидроксиэтил аммония хлорид или Quaternium 80;
b) кватернизованно-легированные растворы абсорбера ультрафиолетового излучения в бутил тригликоле и трибутил цитрате;
c) дисперсии измельченных до микронного размера частиц абсорберов ультрафиолетового излучения, полученных известными методами (осаждением из растворов или смесей растворов, измельчением), имеющие средний диаметр 0,05-1,0 мкм (например, Plantaren), а также четвертичное соединение (например, минкамидопропилдиметил-2-гидроксиэтил аммония хлорид) в водной формуле;
d) смеси растворов абсорбера ультрафиолетового излучения с н-алкилпирролидоном.
Составы для косметического применения, используемые в соответствии с настоящим изобретением для защиты кожи или волос, также могут содержать другие компоненты, например смягчающие вещества, стабилизаторы эмульсии, увлажнители кожи, ускорители загара, загустители, такие как ксантан, средства для удержания влаги, такие как глицерин, консерванты, ароматики и красители.
Новые косметические составы для кожи или волос отличаются превосходной защитой человеческой кожи и волос от вредных воздействий солнечного света.
Следующие не ограничивающие объем изобретения Примеры иллюстрируют изобретение более подробно. Проценты даны по массе.
Пример 1: Получение 2,4,6-трис(4-2 -этилгексилоксифенил) -(1,3,5)-триазина
Основную структуру формулы
получают путем циклотримеризации п-гидроксибензонитрила. Для этого 5,0 г (42 ммоль) п-гидроксибензонитрила медленно добавляют к 10 мл хлорсульфоновой кислоты, охлаждают до 0oС и выдерживают в течение 5 часов. В реакционную смесь добавляют ледяную воду, отфильтровывают, промывают горячей водой и рекристаллизуют из водного раствора метанола. Выход соединения (101а) 62%.
5,36 г соединения формулы (101а) растворяют в 50 мл диметилформамида (ДМФ) с последующим добавлением в смесь 6,53 г мелкоизмельченного карбоната калия при температуре 100-105oС. Эту смесь перемешивают в течение 30 минут, после чего 8,23 г 3-(хлорметил)гептана, растворенного в 10 мл ДМФ, добавляют по каплям в течение 30 минут при температуре 100-105oС. Температуру смеси медленно повышают до 135oС в течение 6 часов. После охлаждения до температуры 100oС добавляют 50 мл толуола и осажденные соли удаляют фильтрацией. Фильтрат концентрируют до сухости упариванием и остаток берут с 50 мл толуола и 100 мл воды, подкисляют и экстрагируют встряхиванием. Высушенную органическую фазу концентрируют упариванием. Сырой продукт (около 7 г) очищают колоночной хроматографией (силикагель, циклогексан/толуол 7:3). Выход: 4,8 г бесцветного масла (46% от теоретического), характеризующегося 13С NMR (90 MHz, СDСl3): δ = 11,54; 14,50; 23,47; 24,27; 29,52; 30,93; 39,77; 71,11; 114,79; 129,11; 131,13; 163,43; 171,02.
Пример 2: Получение 2,4,6-трис(3,5 -диметил-4-(2- этилгексилоксифенил)- (1,3,5)-триазина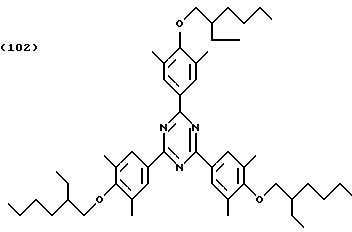
Основную структуру формулы
получают следующим образом: смесь из 18,5 г цианурхлорида и 40 г АlСl3, растворенных в 700 г тетрахлорэтилена, перемешивают в течение 40 мин при комнатной температуре. 73 г 2,6-диметилфенола добавляют к этой смеси (молярное отношение цианурхлорида к 2,6-диметилфенолу 1:3). Реакция протекает при перемешивании при комнатной температуре в течение следующих 93 часов. Плотный продукт реакции отделяют фильтрацией и промывают 100 г 2 N HCl. Этот продукт очищают путем рекристаллизации из 100 г горячего диметилформамида. Перекристаллизованный продукт имеет точку плавления 311-315oС.
6,62 г соединения формулы (102а) растворяют в 70 мл диметилформамида (ДМФ) с последующим добавлением в смесь 6,53 г мелкоизмельченного карбоната калия при температуре 100-105oС. Эту смесь перемешивают в течение 30 минут, после чего 11,65 г 3-(хлорметил)гептана, растворенного в 10 мл ДМФ, добавляют по каплям в течение 60 минут при температуре 100-105oС. Температуру смеси поддерживают на уровне 100-105oС в течение 3 часов. После охлаждения до температуры 100oС добавляют 50 мл толуола и осажденные соли удаляют фильтрацией. Фильтрат концентрируют до сухости упариванием и в остаток добавляют 100 мл толуола и 100 мл воды, подкисляют и экстрагируют встряхиванием. Органическую фазу промывают водой до нейтральности, отделяют, сушат и концентрируют упариванием. Сырой продукт (около 10 г) очищают колоночной хроматографией (силикагель, циклогексан/толуол 65:35). Выход: 4,7 г бесцветных кристаллов, температура плавления 83-84oС (40% от теоретического).
Пример 3:
Соединения формулы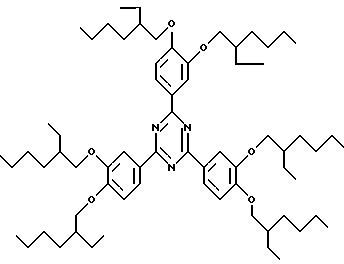
получают по аналогии с методикой примера 1.
Примеры применения
Пример 4: Получение эмульсии типа масло в воде
Состав (отдельные компоненты имеют названия в соответствии с рекомендациями Ассоциации производителей косметических, парфюмерных и туалетных изделий):
(a1) цетеарет 6 (и) стеариловый спирт - 2,0%
(a2) цетеарет 25 - 2,0%
(а3) цетеариловый спирт - 5,0%
(а4) каприловый/каприновый триглицерид - 5,0%
(a5) цетеарил октанат - 10,0%
(а6) вазелин - 5,0%
(а7) соединение формулы (101) - 4,0%
(b1) пропиленгликоль - 3,0%
(b2) карбопол 934 - 0,2%
(b3) Н2O - 63,53%
(с) триэтаноламин - 0,27%
Компоненты (a1)-(a7) (=фаза А) и (b1)-(b3) (=фаза В) нагревают до температуры 75-80oС. Затем фазу В добавляют в фазу А и гомогенизируют. Затем добавляют компонент (с) (=фаза С) и вновь гомогенизируют.
Коэффициенты защиты от солнечного света определяют в соответствии с методом, описанным Diffey и Robson, J. Soc. Cosmet. Chem. 40, 127-133 (1989), с использованием анализатора SPF коэффициента защиты от солнечного света (Optometrix, SPF 290).
Эта эмульсия типа масло в воде имеет коэффициент защиты от солнечного света, равный 4.
Пример 5: Получение крема от солнечного загара
Состав (отдельные компоненты имеют названия в соответствии с рекомендациями Ассоциации производителей косметических, парфюмерных и туалетных изделий):
Фаза А:
(a1) диметикон - 2,0%
(а2) изопропил миристат - 9,0%
(а3) стеариловый спирт - 10,0%
(a4) стеариновая кислота - 4,0%
(a5) соединение формулы (102) - 4,0%
(a6) измельченный до микронных размеров 2,4-бис(фенил)-6-(2-гидрокси-4-метоксифенил)-(1,3,5-триазин) (0,25 мкм) - 3,2%
(b1) триэтаноламин - 1,2%
(b2) карбомер 934 (1%) - 5,0%
(b3) Н2O - 61,6%
Компоненты (a1)-(a6) (= фаза А) гомогенизируют отдельно и очень тщательно, после чего, как компоненты (b1)-(b3) (= фаза В), нагревают отдельно до температуры 75-80oС. Затем фазу В добавляют в фазу А при энергичном перемешивании. Перемешивая, смесь охлаждают.
Коэффициент защиты от солнечного света этого крема составляет 11.
Описываются симметричные производные триазина общей формулы I, где R1 и R2 - одинаковые и означают водород или С1-С5-алкил; R3 - С1-С12-алкокси, и два способа их получения. Соединения I обладают защитными свойствами от ультрафиолетового излучения. 3 с. и 1 з.п.ф-лы.


где R1 и R2 - одинаковые и означают водород или C1-С5 алкил,
R3-C1-С12 алкокси.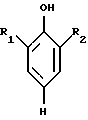
где R1 и R2 имеют приведенные в п.1 значения,
в условиях реакции алкилирования Фриделя-Крафтса в присутствии кислоты Льюиса с последующей этерификацией свободных гидроксильных групп алкилирующим агентом НаlR3, где R3 имеет указанные в п.1 значения.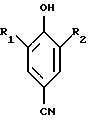
где R1 и R2 имеют приведенные в п.1 значения,
с последующей этерификацией свободных гидроксильных групп алкилирующим агентом НаlR3, где R3 имеет указанные в п.1 значения.
| Прибор для измерения подачи основы на основязальной машине | 1974 |
|
SU539101A1 |
| Теплообменник | 1978 |
|
SU659877A1 |
| US 3932402 А, 13.01.1976 | |||
| Устройство для считывания графической информации | 1975 |
|
SU542212A1 |
| ЕР 0743309 А, 20.11.1996 | |||
| ГИДРОКСИФЕНИЛТРИАЗИНЫ | 1993 |
|
RU2125049C1 |
| Способ определения блокировки колес транспортного средства | 1974 |
|
SU654469A1 |
| Растровый электронный микроскоп | 1976 |
|
SU693483A1 |
| Устройство для измерения скорости движения автомобиля | 1979 |
|
SU775698A2 |
Авторы
Даты
2002-10-20—Публикация
1997-11-10—Подача