Фторолефиновые соединения, которые полезны в качестве пестицидных средств, описаны в WO 94/06741 и GB 2288803-А. В указанных заявках на патент описаны также способы получения фторолефиновых соединений. Однако эти способы не вполне удовлетворительны, потому что они требуют применения реактивов Гриньяра, соединений щелочных металлов и катализаторов на основе переходных металлов. Кроме того, эти способы дают фторолефины с относительно низкими выходами.
Поэтому задачей настоящего изобретения является предоставление нового, эффективного и экономичного способа получения пестицидных фторолефинов, который не требовал бы использования реактивов Гриньяра, соединений щелочных металлов и катализаторов на основе переходных металлов.
Задачей настоящего изобретения является также предоставление промежуточных соединений, полезных для получения пестицидных фторолефинов.
Другие задачи и преимущества настоящего изобретения будут очевидны специалистам в данной области техники из следующего далее описания и прилагаемых пунктов формулы изобретения.
В соответствии с настоящим изобретением предлагается способ получения пестицидного фторолефинового соединения, имеющего структурную формулу I: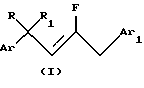
где R представляет водород или C1-C4 алкил, и
R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или
1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или
бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп,
бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена,C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
и конфигурация групп ArCRR1- и CH2Ar1 у двойной связи является преимущественно взаимно транс-конфигурацией,
который (способ) включает
а) фторирование 4-арил-3-оксо-2-(замещенный бензил) бутаноата, имеющего структурную формулу II: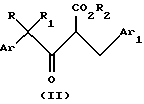
где R2 представляет C1-C6 алкил и Ar, Ar1, R и R1 имеют значения, определенные выше, в присутствии первого основания с образованием 4-арил-2-фтор-3-оксо-2-(замещенный бензил) бутаноата, имеющего структурную формулу III: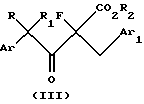
где Ar, Ar1, R, r1 и R2 имеют значения, определенные выше;
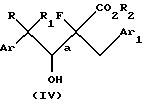
b) восстановление соединения формулы III с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутаноата, имеющего структурную формулу IV:
где Ar, Ar1, R, R1 и R2 имеют значения, определенные выше, и конфигурация групп ArCRR1CH (ОН) - и -CF(CO2R2)CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущественно R,S или S,R или их смесь;
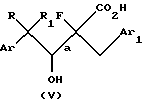
с) омыление соединения формулы IV с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутановой кислоты, имеющей структурную формулу V: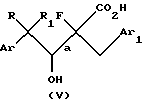
где Ar, Ar1, R и R1 имеют значения, определенные выше, и конфигурация групп ArCRR1CH (ОН)- и -CF (CO2H) CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущество R, S или S, R или их смесь; и
d) осуществление взаимодействия соединения формулы V с сульфонилгалогенидом и вторым основанием.
Настоящее изобретение охватывает также промежуточные соединения формул III, IV и V.
Предпочтительный вариант осуществления настоящего изобретения включает
a) фторирование соединения формулы II, по крайней мере, примерно одним молярным эквивалентом фторирующего агента в присутствии, по крайней мере, примерно одного молярного эквивалента первого основания, предпочтительно в температурном интервале примерно от -15 до 100oС, в присутствии первого растворителя с образованием 4-арил-2-фтор-3-оксо-2-(замещенный бензил)бутаноата формулы III;
b) восстановление соединения формулы III, по крайней мере, примерно одним молярным эквивалентом восстанавливающего агента, предпочтительно в температурном интервале примерно от -50oС до 80oС, в присутствии второго растворителя с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутаноата формулы IV;
c) омыление соединения формулы IV путем осуществления его взаимодействия с, по крайней мере, примерно одним молярным эквивалентом первого основания, а затем с, по крайней мере, примерно одним молярным эквивалентом кислоты, предпочтительно в температурном интервале примерно от -15 до 80oС, в присутствии третьего растворителя с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутановой кислоты формулы V; и
d) осуществление взаимодействия соединения формулы V с, по крайней мере, примерно одним молярным эквивалентом сульфонилгалогенида и, по крайней мере, примерно одним молярным эквивалентом второго основания, предпочтительно в температурном интервале примерно от 0 до 130oС, необязательно в присутствии четвертого растворителя.
Настоящее изобретение также включает 4-арил-2-фтор-3-оксо-2-(замещенный бензил)бутаноаты, 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутаноаты и 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутановые кислоты, которые используют в способе по настоящему изобретению. Указанные соединения представлены структурными формулами соответственно III, IV и V: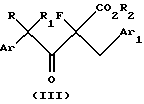
где R представляет водород или C1-C4 алкил, и
R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или
1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкокси-групп или C1-C4 галогеналкоксигрупп;
Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или
бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп,
бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или
бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп; и
R2 представляет C1-C4 алкил; и и их оптические изомеры и диастереомеры.
Примерами упомянутого выше галогена являются фтор, хлор, бром и иод. Термины "C1-C4 галогеналкил" и "C1-C4 галогеналкокси" определяются как C1-C4 алкильная группа и C1-C4 алкоксигруппа, замещенные одним или несколькими атомами галогена соответственно.
Полученные соединения формулы I могут быть выделены путем разбавления реакционной смеси водой и экстрагирования продукта подходящим экстракционным растворителем. Для выделения можно использовать традиционные экстракционные растворители, такие, как эфир, этилацетат, толуол, метиленхлорид и аналогичные.
Преимуществом является то, что необычный способ по настоящему изобретению дает пестицидные фторолефины с относительно высоким выходом. Кроме того, в способе по настоящему изобретению не используют неэкономичные реагенты, требуемые известными способами.
Фторирующие агенты, подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими) фтор, диэтиламиносератрифторид, 1-фтор-4-гидрокси-1,4-диазониабицикло [2,2,2]октан бис(тетрафторборат), N-фторпиридиний-пиридин гептафтордиборат, N-фторбензолсульфонимид, N-фтор-3,3-диметил-2,3-дигидро-1,2-бензотиазол-1,1-диоксид, N-фтор-оксатиазинондиоксид и аналогичные и их смеси. Предпочтительным фторирующим агентом является N-фтор-3,3-диметил-2,3-дигидро-1,2-бензотиазол-1,1-диоксид.
Восстанавливающие агенты, подходящие для использования в настоящем изобретении, дают соединения формулы IV, в которых конфигурация групп ArCRR1CH (ОН) - и CF(CO2R2)CH2Ar1 представляет собой преимущественно R,S или S,R или их смесь. Восстанавливающие агенты, которые могут быть использованы в настоящем изобретении, включают (но не ограничиваются ими) ферментные восстанавливающие системы, одноклеточные микроорганизмы, борогидриды, такие, как борогидрид натрия, цианоборогидрид натрия, борогидрид цинка и аналогичные, замещенные гидриды алюминия, такие, как три-трет-бутоксиалюминийгидрид лития и аналогичные комплексы C1-C6 алкоксида с C1-C6 спиртом, такие как комплекс изопропоксида алюминия с изопропанолом и аналогичные, и водород в присутствии катализатора на основе благородного металла. Предпочтительными восстанавливающими агентами являются борогидриды.
Основания, подходящие для использования на стадии омыления в способе по настоящему изобретению, включают (но не ограничиваются ими) карбонаты щелочных металлов, такие, как карбонат натрия и карбонат калия, карбонаты щелочноземельных металлов, такие, как карбонат кальция, гидроксиды щелочных металлов, такие, как гидроксид натрия и гидроксид калия, гидроксиды щелочноземельных металлов, такие, как гидроксид кальция, C1-C6 алкоксиды щелочных металлов, такие, как этоксид натрия и трет-бутоксид калия, C1-C6 алкоксиды щелочноземельных металлов, карбонат таллия (I), C1-C6 алкоксиды таллия (I) и гидроксид таллия (I) и их смеси, причем предпочтительными являются гидроксиды щелочных металлов. Кислоты, подходящие для использования в настоящем изобретении, включают неорганические кислоты, такие, как хлороводородная кислота, бромоводородная кислота, серная кислота и аналогичные, и сильные органические кислоты, такие, как трифторуксусная кислота и тому подобные, и их смеси, причем предпочтительными являются неорганические кислоты.
Сульфонилгалогениды, подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими) алкилсульфонилхлориды, такие, как метансульфонилхлорид и тому подобные, и арилсульфонилхлориды, такие, как п-толуолсульфонилхлорид, бензолсульфонилхлорид и тому подобные, и их смеси.
Первые основания, подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими) C1-C6 алкоксиды щелочных металлов, такие, как этоксид натрия и трет-бутоксид калия, гидриды щелочных металлов, такие, как гидрид натрия, гидроксиды щелочных металлов, такие, как гидроксид натрия и гидроксид калия, гидроксиды щелочноземельных металлов, такие, как гидроксид кальция, алкиллитиевые соединения, такие, как н-бутиллитий и втор-бутиллитий, ариллитие-вые соединения, такие, как фениллитий, C1-C6 алкоксиды щелочноземельных металлов, C1-C6 алкоксиды таллия (I) и гидроксид таллия (I), и их смеси. Предпочтительные первые основания включают C1-C6 алкоксиды щелочных металлов и гидриды щелочных металлов. Вторые основания, подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими) третичные амины, такие, как три(C1-C4 алкил)амины, пиридин и замещенные пиридины, причем предпочтительным является пиридин.
Первые растворители, подходящие для использования на стадии фторирования в способе по настоящему изобретению, включают (но не ограничиваются ими) простые эфиры, такие, как тетрагидрофуран, диоксан и тому подобные, ароматические углеводороды, такие, как толуол, бензол, ксилолы, мезитилен и тому подобные, галогенированные ароматические углеводороды, такие, как хлорбензол, фторбензол и тому подобные,и амиды карбоновых кислот, такие, как N,N-диметилформамид и тому подобные, и их смеси. Предпочтительные первые растворители включают простые эфиры, причем более предпочтительным является тетрагидрофуран.
Вторые и третьи растворители (которые могут быть одинаковыми или разными), подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими)C1-C4 спирты, такие, как метанол, этанол и тому подобные, и простые эфиры, такие, как тетрагидрофуран, диоксан и тому подобные, и их смеси. Предпочтительные вторые и третьи растворители включают C1-C4 спирты, причем более предпочтительным является метанол.
Четвертые растворители, подходящие для использования в настоящем изобретении, включают (но не ограничиваются ими) ароматические углеводороды, такие, как толуол, бензол, ксилолы, мезитилен и тому подобные, галогенированные ароматические углеводороды, такие, как хлорбензол, фторбензол и тому подобные, простые эфиры, такие, как тетрагидрофуран, диоксан и тому подобные, амиды карбоновых кислот, такие, как N,N-диметилформамид и тому подобные, галогенированные алифатические углеводороды, такие, как хлороформ, тетрахлорид углерода и тому подобные,и ацетонитрил и их смеси.
Настоящее изобретение включает также новые соединения, представленные формулами II, III, IV и V, где Ar, Ar1, R, R1и R2 имеют значения, определенные выше, при условии, что в соединениях формулы II R отличен от водорода.
Исходные 4-арил-3-оксобутаноаты формулы II могут быть получены, как показано на технологической схеме I, приведенной в конце описания, путем осуществления взаимодействия 4-арил-3-оксобутаноата формулы VI с основанием и замещенным бензилгалогенидом формулы VII.
Предпочтительными фторолефиновыми соединениями формулы I, которые могут быть получены способом по настоящему изобретению, являются соединения, в которых
R представляет водород и R1 представляет изопропил или циклопропил, или R и R1 представляют метил , или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-С4 алкильных групп, C1-С4 галогеналкильных групп, C1-С4 алкоксигрупп или C1-С4 галогеналкоксигрупп; и
Ar1 представляет 3-феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-С4 алкильных групп, C1-С4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-С4 галогеналкоксигрупп,
3-бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена,C1-С4 алкильных групп, C1-С4 галогеналкильных групп, C1-С4 алкоксигрупп или C1-С4 галогеналкоксигрупп,
3-бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена,C1-С4 алкильных групп, C1-С4 галогеналкильных групп, C1-С4 алкоксигрупп или C1-С4 галогеналкоксигрупп, или 3-бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-С4 алкильных групп, C1-С4 галогеналкильных групп, C1-С4 алкоксигрупп или C1-С4 галогеналкоксигрупп.
Способ по настоящему изобретению особенно полезен для получения пестицидных фторолефинов формулы I, в которой
R представляет водород и R1 представляет изопропил или циклопропил, или R и R1 представляют метил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет 4-хлорфенил, 4-фторфенил, 4-(трифторметокси)фенил или 4-этоксифенил; и
Ar1 представляет 4-фтор-3-феноксифенил или 3-феноксифенил.
Предпочтительными исходными соединениями формулы II по настоящему изобретению являются соединения, в которых R2 представляет C1-С4 алкил.
Чтобы облегчить дальнейшее понимание настоящего изобретения, представлены следующие далее примеры, прежде всего с целью иллюстрации более конкретных его деталей. Не следует считать, что эти примеры ограничивают объем настоящего изобретения, определенный прилагаемой формулой изобретения.
ПРИМЕР 1
Получениеэтил1-(п-хлорфенил)-α-фтор-β-оксо-α-(м-феноксибензил)циклопропанпропионата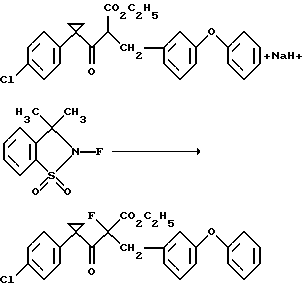
Дисперсию (60%) гидрида натрия в масле (0,17 г, 4,3 ммоль) промывают гексанами, сушат и диспергируют в тетрагидрофуране. Полученную смесь охлаждают на водяной бане со льдом, обрабатывают раствором этил 1- (п-хлорфенил) -β-оксо-α-(м-феноксибензил)циклопропанпропионата (1,72 г, 3,84 ммоль) в тетрагидрофуране, перемешивают при 0oС в течение 4 ч, обрабатывают раствором N-фтор-3,3-диметил-2,3-дигидро- 1,2-бензотиазол-1,1-диоксида (1,10 г, 5,12 ммоль) в тетрагидрофуране, перемешивают при 0oС в течение 90 мин, перемешивают при комнатной температуре в течение одного часа, охлаждают на водяной бане со льдом, гасят 10 мл рассола и разбавляют этилацетатом и водой. Органическую фазу отделяют, промывают последовательно водой и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением остатка. Хрома-тография остатка с использованием силикагеля и раствора гексаны/этилацетат (19:1) дает указанный в заголовке продукт в виде бесцветного масла (1,25 г, 70%), который идентифицируют методом ЯМР-спектроскопии.
ПРИМЕР 2
Получениеэтил1-(п-хлорфенил)-α-фтор-β-гидрокси-α-(м-феноксибензил)циклопропанпропионата, отношение [R,S и S,R] к [R,R и S,S] равно 9:1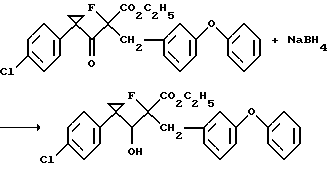
Борогидрид натрия (20 мг, 0,53 ммоль) добавляют к раствору этил 1-(п-хлорфенил)-α-фтор-β-оксо-α-(м-феноксибензил)циклопропанпропионата (214 мг, 0,46 ммоль) в метаноле при 0oС. Реакционную смесь перемешивают при 0oС в течение 20 мин, обрабатывают водой (2 мл) и концентрируют в вакууме с получением остатка. Раствор остатка в этилацетате промывают последовательно водой и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением указанного в заголовке продукта в виде бесцветной смолы (224 мг, 100%), который, как было установлено путем ЯМР-спектроскопии, имеет отношение [R,S и S,R] к [R,R и S,S], равное 9:1.
ПРИМЕР 3
Получение1-(п-хлорфенил)-α-фтор-β-гидрокси-α-(м-феноксибензил)циклопропанпропионовой кислоты, отношение [R, S и S,R] к [R,R и S,S] равно 9:1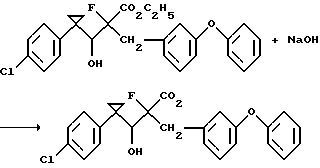
Раствор гидроксида натрия (3 мл 1 М раствора) добавляют к раствору этил 1-(п-хлорфенил)-α-фтор-β-гидрокси-α- (м-феноксибензил)циклопропанпропионата (224 мг, 0,48 ммоль) с отношением [R,S и S,R] к [R,R и S,S], равным 9:1, в метаноле при 0oС. Реакционную смесь перемешивают при комнатной температуре в течение ночи, подкисляют до рН 1 концентрированной хлороводородной кислотой и концентрируют в вакууме с получением остатка. Раствор остатка в этилацетате промывают последовательно водой и рассолом, сушат над безводным сульфатом натрия, концентрируют в вакууме, разбавляют диэтиловым эфиром и гексанами и концентрируют в вакууме с получением указанного в заголовке продукта в виде белого пенообразного вещества (210 мг, 100%), который идентифицируют путем ЯМР-спектрометрии.
ПРИМЕР 4
Получение 1 -(п-хлорфенил)-1 -[2-фтор-3 -(м-феноксифенил) пропенил]циклопропана, отношение Z к Е равно 9:1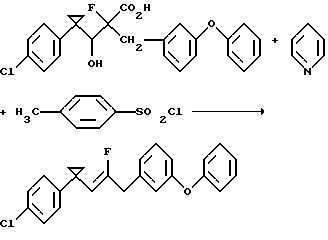
К раствору 1-(п-хлорфенил)-α-фтор-β-гидрокси-α- (м-феноксибензил)циклопропанпропионовой кислоты (20 мг, 0,05 ммоль), имеющей отношение [R, S и S,R] к [R,R и S,S], равное 9:1, в пиридине (2 мл) добавляют п-толуолсульфонилхлорид (19,07 мг, 0,10 ммоль). Реакционную смесь нагревают до 60oС и выливают в воду. Водную смесь экстрагируют диэтиловым эфиром. Органические экстракты объединяют, промывают последовательно 2 н. хлороводородной кислотой, водой, 10% раствором бикарбоната натрия и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением указанного в заголовке продукта в виде бесцветного масла (18 мг, 100%), который, как было установлено путем ЯМР-спектрометрии, имеет отношение Z к Е, равное 9:1.
ПРИМЕР 5
Получение этил 1-(п-хлорфенил)-β-гидроксициклопропанпропионата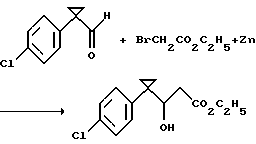
Смесь цинковой пыли (4,0 г, 61,2 ммоль), этилбромацетата (6,5 мл, 58,3 ммоль) и 1-(п-хлорфенил)циклопропанкарбоксальдегида (10,0 г, 55,4 ммоль) в толуоле перемешивают при 70oС в течение 45 мин, охлаждают на водяной бане со льдом, обрабатывают 100 мл 10% серной кислоты, перемешивают при комнатной температуре в течение одного часа и разбавляют этилацетатом. Органическую фазу отделяют, промывают последовательно 10% серной кислотой, водой, 10% раствором бикарбоната натрия и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением масла. Хроматография масла с использованием силикагеля и градиентной смеси гексаны/этилацетат от 9:1 до 7: 3 дает указанный в заголовке продукт в виде бесцветного масла (11,3 г, 76%), который идентифицируют путем ЯМР-спектроскопии.
ПРИМЕР 6
Получение этил 1-(п-хлорфенил)-β-оксоциклопропанпропионата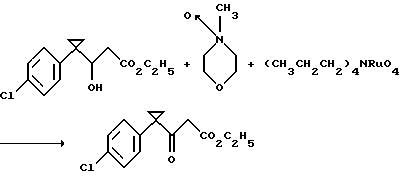
Раствор этил 1-(п-хлорфенил)-β- гидроксициклопропанпропионата (7,9 г, 29,4 ммоль) и N-оксида 4-метилморфолина (14,0 г, 120 ммоль) в ацетонитриле, содержащий 30 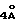 молекулярных сит, перемешивают при комнатной температуре в течение 20 мин, обрабатывают тетрапропиламмонийперрутенатом (0,8 г, 2,3 ммоль), перемешивают два часа, поддерживая температуру реакционной смеси при комнатной температуре с помощью водяной бани со льдом, разбавляют диэтиловым эфиром, фильтруют через диатомовую землю и концентрируют в вакууме с получением остатка. Раствор остатка в диэтиловом эфире промывают последовательно водой, 5% серной кислотой, водой и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением темного масла. Хроматография масла с использованием силикагеля и градиентной смеси этилацетат/гексаны с отношением от 1:19 до 3:17 дает указанный в заголовке продукт в виде бледно-желтого масла (4,3 г, 55%), который идентифицируют путем ЯМР-спектрометрии.
молекулярных сит, перемешивают при комнатной температуре в течение 20 мин, обрабатывают тетрапропиламмонийперрутенатом (0,8 г, 2,3 ммоль), перемешивают два часа, поддерживая температуру реакционной смеси при комнатной температуре с помощью водяной бани со льдом, разбавляют диэтиловым эфиром, фильтруют через диатомовую землю и концентрируют в вакууме с получением остатка. Раствор остатка в диэтиловом эфире промывают последовательно водой, 5% серной кислотой, водой и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением темного масла. Хроматография масла с использованием силикагеля и градиентной смеси этилацетат/гексаны с отношением от 1:19 до 3:17 дает указанный в заголовке продукт в виде бледно-желтого масла (4,3 г, 55%), который идентифицируют путем ЯМР-спектрометрии.
ПРИМЕР 7
Получение этил 1-(п-хлорфенил)-β-оксо-α-(м-феноксибензил) циклопропанпропионата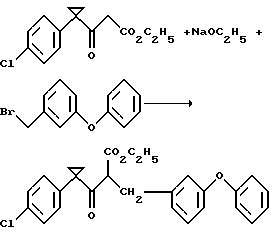
Смесь натрия (0,31 г, 13,5 ммоль) в этаноле (90 мл) перемешивают при комнатной температуре до тех пор, пока не растворится натрий. Полученный раствор нагревают до 70oС, обрабатывают по каплям раствором этил 1-(п-хлорфенил)-β- оксо-циклопропанпропионата (3,4 г, 12,8 ммоль) в этаноле, перемешивают при 70oС в течение одного часа, обрабатывают по каплям раствором α-бром-м-толилфенилового эфира (4,0 г, 15,2 ммоль) в этаноле, перемешивают при нагревании с обратным холодильником в течение ночи, перемешивают при комнатной температуре два дня и концентрируют в вакууме с получением остатка. Раствор остатка в этилацетате промывают последовательно водой, 10% раствором бикарбоната натрия и рассолом, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением масла. Хроматография масла с использованием силикагеля и раствора гексаны/этилацетат с отношением 19:1 дает указанный в заголовке продукт в виде бесцветного масла (5,24 г, 92%), который идентифицируют путем ЯМР-спектрометрии.
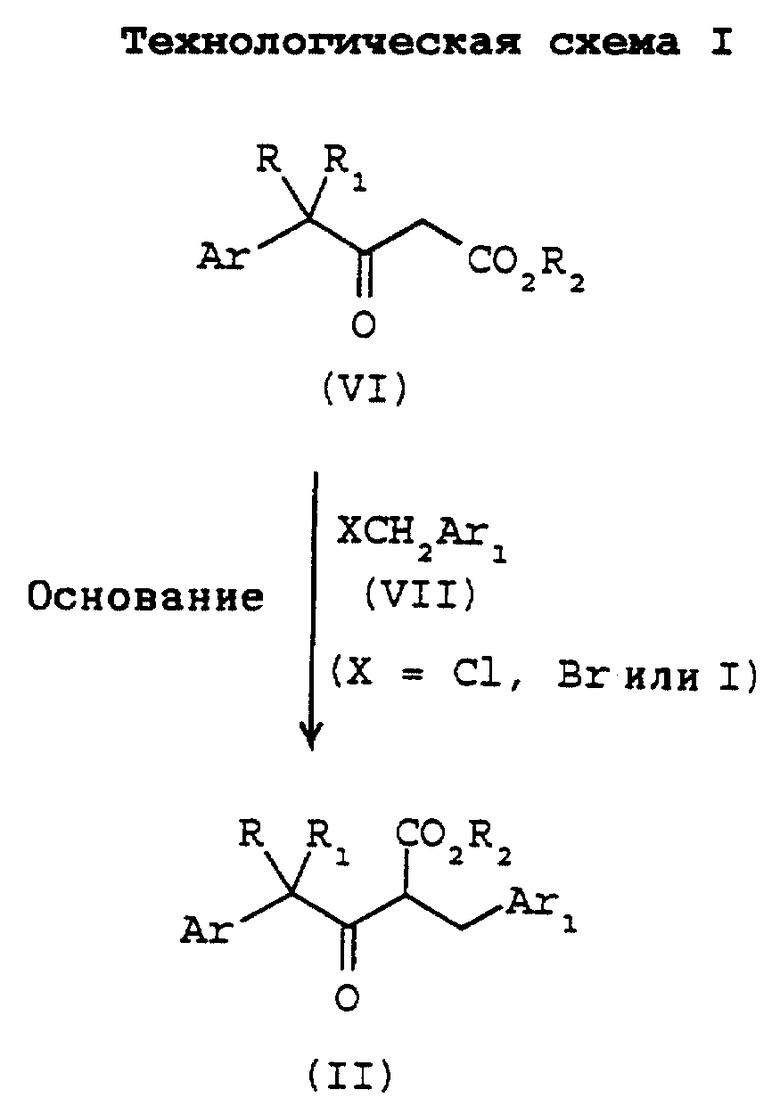
Изобретение относится к способу получения пестицидного фторолефинового соединения общей формулы I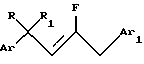
где R представляет водород или C1-C4 алкил, и R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу; Аr представляет фенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или 1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкокси-групп или C1-C4 галогеналкоксигрупп; Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бифенил, бензилфенил или бензоилфенил, необязательно замещенные одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, конфигурация групп ArCRR1- и -СН2Аr1 у двойной связи является преимущественно взаимно транс-конфигурацией, способ включает фторирование 4-арил-3-оксо-2-(замещенный бензил)бутаноата формулы II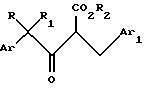
где R2 =C1-C6 алкил, значения остальных радикалов указаны выше, в присутствии первого основания с образованием 4-арил-2-фтор-3-оксо-2-(замещенный бензил)бутаноата формулы III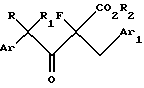
последнее восстанавливают, полученный 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутаноат формулы IV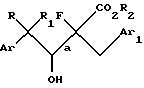
конфигурация групп ArCRR1CH(OH) - и -CF(CO2R2)CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущественно R, S и S, R или их смесь, омыляют с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутановой кислоты, имеющей структурную формулу V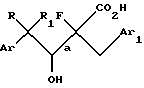
и конфигурация групп ArCRR1CH(OH)- и -CF(CO2H)CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущественно R, S и S, R или их смесь; и осуществляют взаимодействие соединения формулы V с сульфогалогенидом и вторым основанием, причем первое основание выбирают из группы, состоящей из гидроксида щелочного, щелочноземельного металла, C1-C6 алкоксида щелочного или щелочноземельного металла, C1-C6 алкоксида таллия (I), гидроксида таллия (I), гидрида щелочного металла, алкилметил и ариллития, а второе основание представляет собой третичный амин, выбранный из группы, состоящей из три(C1-C4-алкил)амина, пиридина и замещенного пиридина; а также новым промежуточным соединением, имеющим структурные формулы II, III, IV и V. Предлагаемый способ эффективен, экономичен, не требует использования реактивов Гриньяра, соединений щелочных металлов и катализаторов на основе переходных металлов. 3 с. и 12 з.п. ф-лы.
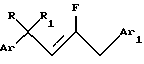
где R представляет водород или C1-C4 алкил;
R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или 1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
конфигурация групп ArCRR1- и -CH2Ar1 у двойной связи является преимущественно взаимно транс-конфигурацией, который (способ) включает
а) фторирование 4-арил-3-оксо-2-(замещенный бензил)бутаноата, имеющего структурную формулу II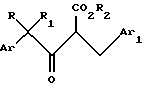
где R2 представляет C1-C6 алкил и Аr, Ar1, R и R1 имеют значения, определенные выше, в присутствии первого основания с образованием 4-арил-2-фтор-3-оксо-2-(замещенный бензил)бутаноата, имеющего структурную формулу III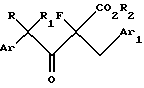
где Ar, Ar1, R, R1 и R2 имеют значения, определенные выше,
b) восстановление соединения формулы III с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутаноата, имеющего структурную формулу IV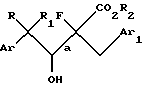
где Аr, Ar1, R, R1 и R2 имеют значения, определенные выше, и конфигурация групп ArCRR1CH(OH) - и -CF(CO2R2)CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущественно R, S и S, R или их смесь;
с) омыление соединения формулы IV с образованием 4-арил-2-фтор-3-гидрокси-2-(замещенный бензил)бутановой кислоты, имеющей структурную формулу V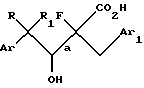
где Аr, Ar1, R и R1 имеют значения, определенные выше/и конфигурация групп ArCRR1CH(OH)- и -CF(CO2H)CH2Ar1, присоединенных к связи, обозначенной "а", представляет собой преимущественно R, S и S, R или их смесь;
d) осуществление взаимодействия соединения формулы V с сульфонилгалогенидом и вторым основанием.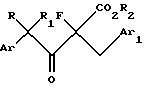
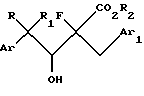
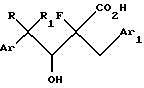
где R представляет водород или C1-C4 алкил;
R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4галогеналкоксигрупп, или 1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп или бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
R2 представляет C1-C6 алкил;
и его оптические изомеры и диастереомеры.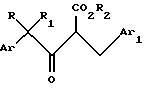
где R представляет C1-C4 алкил;
R1 представляет C1-C4 алкил, C1-C4 галогеналкил или циклопропил, или R и R1, взятые вместе с углеродным атомом, к которому они присоединены, образуют циклопропильную группу;
Аr представляет фенил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или 1- или 2-нафтил, необязательно замещенный одной-тремя группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
Ar1 представляет феноксифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бифенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, бензилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп, или бензоилфенил, необязательно замещенный одной-пятью группами, независимо выбранными из атомов галогена, C1-C4 алкильных групп, C1-C4 галогеналкильных групп, C1-C4 алкоксигрупп или C1-C4 галогеналкоксигрупп;
R2 представляет C1-C6 алкил,
и его оптические изомеры.
| 1-(4-Этилфенокси)-3-метил-5-изопропокси-2-пентен, обладающий инсектицидной активностью | 1982 |
|
SU1058101A1 |
| Инсектицидное средство | 1986 |
|
SU1470172A3 |
| US 4975451 А, 04.12.1990 | |||
| Экономайзер | 0 |
|
SU94A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
Авторы
Даты
2002-11-20—Публикация
1998-06-18—Подача