Изобретение относится к фармацевтическим соединениям, называемым в данном патентном описании как "конденсированные пирроло[2,3-с]карбазол-6-оны". Кроме того, раскрываются способы получения этих соединений и способы их использования.
Человеческий гамма-интерферон (IFN-γ) представляет природный человеческий иммунорегуляторный белок. Установлено, что он является средством, эффективным при лечении опухолей и вирусных инфекций у людей. Точный механизм, с помощью которого IFN-γ ингибирует вирус и рост опухоли in vivo, остается неизвестным. Очевидно, что IFN-γ работает, по крайней мере, по одному из двух механизмов: (1) действуя непосредственно на клетку, инфицированную вирусом, и клетку опухоли и/или (2), сначала активируя клетки иммунной системы, которые затем разрушают инфицированную вирусом клетку или клетку опухоли [Interferons and other Regulatory Cytokines, E. De Maeyer and J. De Maeyer-Guignard, John Wiley & Sons, New York (1988)].
Одно из проявлений стимулированной иммунной системы заключается в усиленной экспрессии на поверхности иммунных клеток белков главного комплекса гистосовместимости (МНС). МНС состоит из генов класса I, II и III, которые кодируют соответствующие белки класса I, II и III. Белки класса I и II находятся на поверхности клеток и вовлекаются в контролирование иммунного ответа, в то время как белки класса III появляются в сыворотке и не вовлекаются в контролирование иммунного ответа. Белки класса I и II (находятся) на антиген представляющих клетках, например моноцитах. Лимфоциты В, дендритные клетки, представляют чужеродные антигены Т лимфоцитов с последующей деструкцией клетки, содержащей чужеродный антиген. Усиленная экспрессия белков класса I и II необходима для иммунной системы, чтобы спасти животное с инфицированными вирусом клетками и повысить продуцирование специфических антител. IFN-γ является одним из основных регуляторов иммунного ответа благодаря своей способности усиливать экспрессию белков класса I и II МНС. Примером полезности МНС I повышения с помощью IFN-γ является увеличение белков класса I на инфицированных вирусом клетках (вирусинфицированных клетках). Вирусинфицированная клетка представляет синтезированные на ее клеточной поверхности вирусные антигены рецептору Т клетки на цитотоксических Т клетках (CD4 клетках) с последующей деструкцией инфицированной вирусом клетки с помощью цитотоксической Т клетки.
Примером полезности МНС II повышения с помощью IFN-γ является увеличение белков класса II на моноцитах. Моноциты могут переваривать вторгающиеся (поражающие) микроорганизмы и белки класса II на поверхности моноцитов, представляющие пептиды, полученные из вторгающегося микроорганизма. Эти пептиды, удерживаемые белками класса II, присутствуют на рецептор Т клетки на клетках Т-хелперах (CD8) с последующей секрецией лимфокинов CD8 клеткой. Секретированные лимфокины вызывают пролиферацию антитела, синтезирующего В лимфоциты, которые синтезируют большие количества антител против вторгающегося микроорганизма.
Из вышеприведенных примеров можно видеть, что соединение, которое усиливает IFN-γ индукцию МНС молекул, можно было бы использовать в комбинации с IFN-γ для лечения инфекций, вызванных микроорганизмами. Такое соединение позволит уменьшить дозу IFN-γ, с успехом обеспечивая такое же терапевтическое действие, как в случае только одного IFN-γ, но с меньшими побочными действиями, сопутствующими IFN-γ.
Имеются, по крайней мере, три сообщения о соединениях, которые потенцируют IFN-γ-индуцированную МНС экспрессию [Coutinho, G.C., Dudrieu-Trautmann, О. , Strosberg, A. D. and Couraud, P. O. , Catecholamines Stimulate the IFN-γ-induced Class II MHC Expression on Bovine Brain Capillary Endothelial Cells, J. Immunol. 147, 2525-2529 (1991); Zhu, J., Mix, E., Olsson, Т. и Link, H. , "Influence of Ion Channel Modulation of in Vitro Interferon-γ Induced MHC Class I и II Expression on Macrophages", Immunopharmacology и Immunotoxicology, 17, 109-136 (1995); Mothes, Т., Bendix, U., Pfannschmidt. С. и Lehmann. I., "Effect of Gliadin and Other Food Peptides on Expression of MHC Class II Molecules by HT-29 Cells", Gut, 36, 548-552 (1995)].
Сущность изобретения
Здесь раскрыт новый класс соединений, представленный формулами I и II, который мы называем как конденсированные пирроло[2,3-с]карбазол-6-оны.
ФОРМУЛА I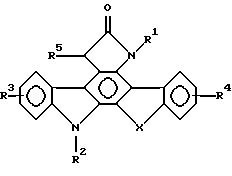
ФОРМУЛА II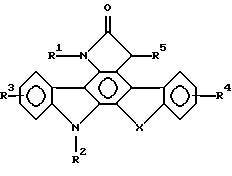
Составляющие заместители определены ниже. Предпочтительные способы получения этих соединений раскрыты ниже.
Нами установлено, что наши соединения конденсированные пирроло[2,3-с]карбазол-6-оны (нумерация, обозначенная для К-252а и К-252с, предложена Moody et. al, J. Org. Chem., 1992, 57, 2105) потенцируют активность человеческого IFN-γ в индуцировании экспрессии МНС на поверхности рецептивных (восприимчивых) клеток. Соединения данного изобретения демонстрируют способность усиливать эффективность иммунной системы, и это, в свою очередь, с успехом обеспечивает усиление ингибирования роста вируса и/или опухоли. Нами также установлено, что конденсированные пирроло[2,3-с]карбазол-6-оновые соединения данного изобретения полезны для потенцирования, предпочтительно, нейротрофин-3 (NT-3) активности.
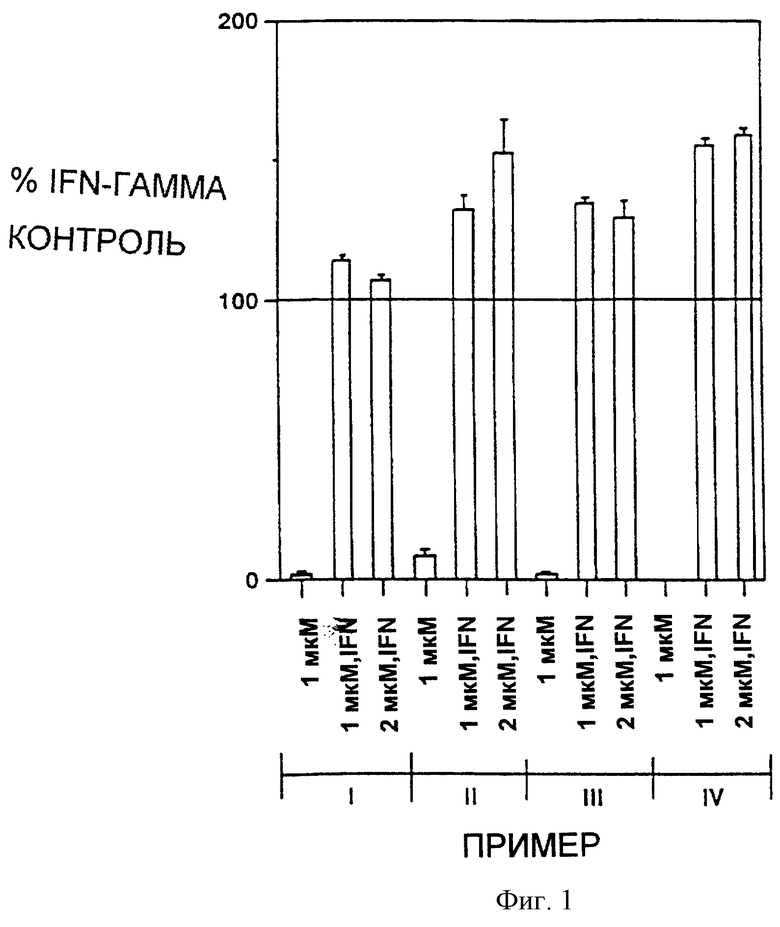
Фигура 1 представляет гистограмму, показывающую повышение IFN-γ-индуцированной экспрессии HLA-DR МНС II молекулы с помощью пирроло[2,3-с]-карбазол-6-онов данного изобретения.
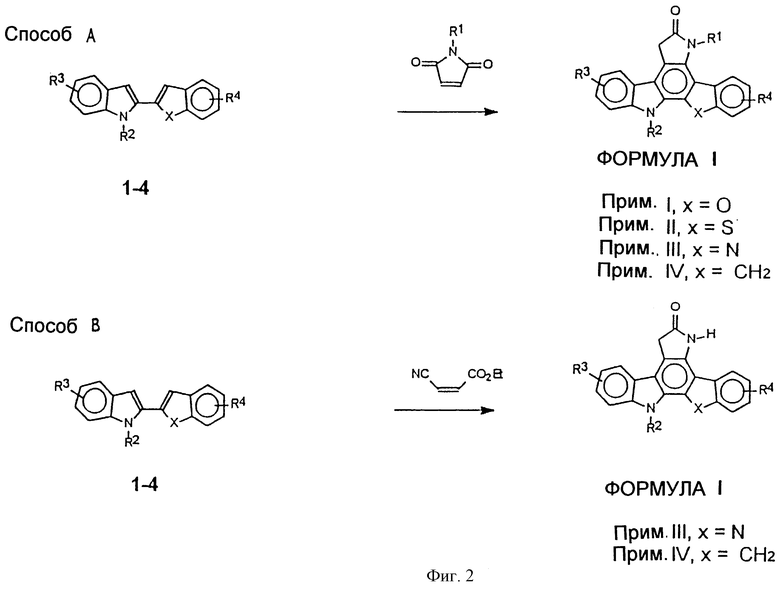
Фигура 2 представляет в общих чертах схему химического синтеза пирроло[2,3-с]карбазол-6-онов формулы I, раздел V (A)-(D).
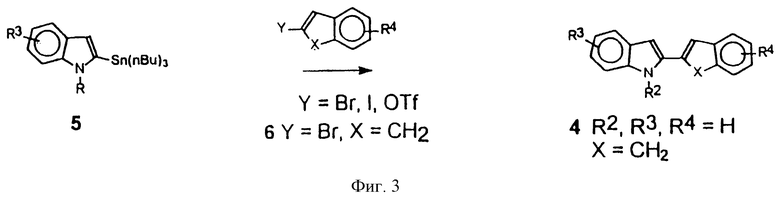
Фигура 3 представляет схему, показывающую синтез промежуточных продуктов для пирроло[2,3-с]карбазол-6-онов.
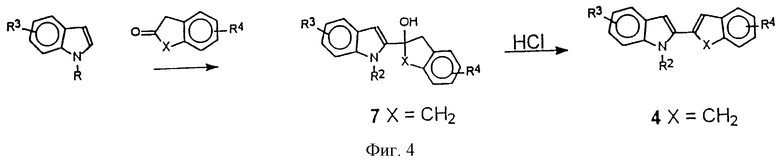
Фигура 4 представляет схему альтернативного синтеза промежуточных для пирроло[2,3-с]карбазол-6-онов.
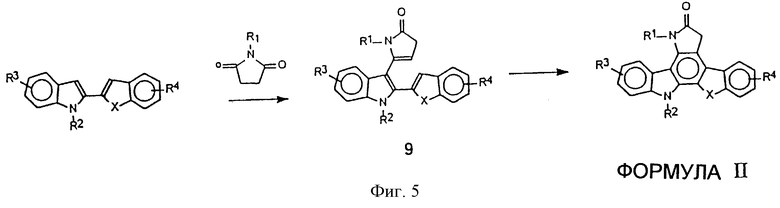
Фигура 5 представляет схему, показывающую синтез пирроло[2,3-с]карбазол-6-онов формулы II.
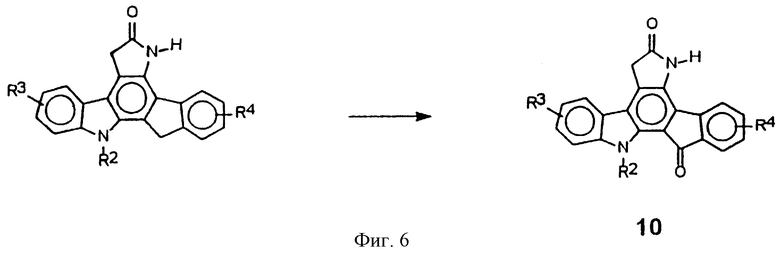
Фигура 6 представляет схему, показывающую синтез пирроло[2,3-с]карбазол-6-онов, в которых Х представляет С=О из соответствующих соединений, в которых Х представляет СН2.
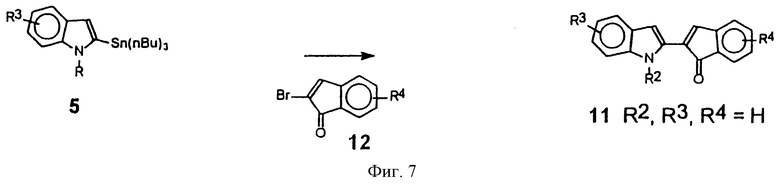
Фигура 7 представляет схему, показывающую синтез пирроло[2,3-с]карбазол-6-она из промежуточного продукта 11.
II. Конденсированные пирроло[2,3-с]карбазол-6-оны
Новые соединения данного изобретения, которые называются как конденсированные пирроло[2,3-с]карбазол-6-оновые производные, представлены следующими формулами: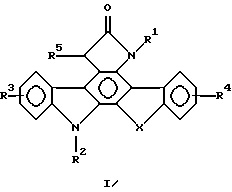
и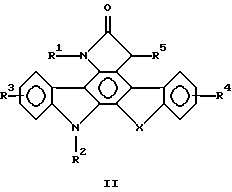
где:
a) R1 выбран из группы, состоящей из Н, алкила с 1-4 углеродами, арила, арилалкила, гетероарила, гетероарилалкила; C(= O)R9, где R9 представляет алкил с 1-4 углеродами или арил; (CH2)nOR9, где n представляет целое число 1-4; OR10, где R10 представляет Н или алкил с 1-4 углеродами; (СН2)nОR14, где R14 представляет остаток аминокислоты после удаления гидроксила карбоксильной группы; OR14, NR7R8; (СН2)nNR7R8 и O(СН2)nNR7R8; и либо
(1) R7 и R8 независимо представляют Н или алкил с 1-4 углеродами; или
(2) R7 и R8 соединены вместе с образованием связывающей группы общей формулы -(СН2)2-Х1(СН2)2-, где X1 представляет О, S или СН2;
b) R2 выбран из группы, состоящей из Н, SO2R9, CO2R9, C(=O)R9, алкила с 1-8 углеродами, алкенила с 1-8 углеродами, алкинила с 1-8 углеродами и моносахарида с 5-7 углеродами, в котором каждая гидроксильная группа указанного моносахарида независимо выбрана из группы, состоящей из незамещенного гидроксила и фрагмента заменяющего указанную гидроксильную группу, выбранного из Н, алкила с 1-4 углеродами, алкилкарбонилокси с 2-5 углеродами и алкокси с 1-4 углеродами; где либо
1) каждый алкил с 1-8 углеродами, алкенил с 1-8 углеродами или алкинил с 1-8 углеродами является незамещенным; либо
2) каждый алкил с 1-8 углеродами, алкенил с 1-8 углеродами или алкинил с 1-8 углеродами независимо замещен 1-3 группами, выбранными из группы, состоящей из арила с 6-10 углеродами, гетероарила, F, Cl, Br, I, CN, NO2, ОН, OR9, O(CH2)nNR7R8, OCOR9, OCONHR9, O-тетрагидропиранила, NH2, NR7R8, NR10COR9, NR10CO2R9, NR10CONR7R8, NHC(= NH)NH2, NR10S02R9; S(O)yR11, где R11 представляет Н, алкил с 1-4 углеродами, арил с 6-10 углеродами или гетероарил, и y равен 1 или 2; SR11, CO2R9, CONR7R8, CHO, COR9, CH2OR7, CH2OR9, CH= NNR11R12, CH=NOR11, CH=NR9, CH=NNHCH(N=NH)NH2; SO2NRl2R13, где либо
(la) R12 и R13 независимо представляют Н, алкил с 1-4 углеродами, арил с 6-10 углеродами или гетероарил; либо
(2а) R12 и R13 соединены вместе с образованием -(СН2)2-Х1-(СН2)2 связывающей группы;
PO(OR11)2, NHR14, NR10R14, OR14 и моносахарида с 5-7 углеродами, в котором каждая гидроксильная группа указанного моносахарида независимо выбрана из группы, состоящей из незамещенного гидроксила и фрагмента, заменяющего указанную гидроксильную группу, выбранного из Н, алкила с 1-4 углеродами, алкилкарбонилокси с 2-5 углеродами и алкокси с 1-4 углеродами;
с) каждый R3 и R4 независимо выбран из группы, состоящей из Н, арила с 6-10 углеродами, гетероарила, F, Cl, Br, I, CN, СF3, NO2, ОН, OR9 О(CH2)nNR7R8, OCOR9, OCONHR9, NH2, (СН2)nОR9, (CH2)nOR10, (CH2)nOR14, OR14, NHR14, NR7R8, NR7(CH2)nNR7R8, NR10COR9, NR10CONR7R8, SR11, S(О)yR11,
CO2R9, COR9, CONR7R8, CHO, CH= NOR11, CH=NR9, CH=NNR11R12, (CH2)nSR9, (CH2)nS(О)yR9; CH2SR15, где R15 представляет алкил с 1-4 углеродами; CH2S(О)yR14, (CH2)nNR7R8, (CH2)nNHR14, алкила с 1-8 углеродами, алкенила с 1-8 углеродами и алкинила с 1-8 углеродами; и либо
1) каждый алкил с 1-8 углеродами, алкенил с 1-8 углеродами или алкинил с 1-8 углеродами является незамещенным, либо
2) каждый алкил с 1-8 углеродами, алкенил с 1-8 углеродами или алкинил с 1-8 углеродами является независимо замещенным, как описано выше в b)2);
d) R5 выбран из группы, состоящей из алкила с 1-8 углеродами, алкенила с 1-8 углеродами и алкинила с 1-8 углеродами, и либо
1) каждая алкильная, алкенильная или алкинильная группа является незамещенной; или
2) каждая алкильная, алкенильная или алкинильная группа является замещенной 1-3 группами, выбранными из группы, состоящей из F, Cl, Br, I, CN, СF3, NO2, ОН, OR9, О(СН2)nNR7R8, OCOR9, OCONHR9, NH2, (CH2)nOR9, (CH2)nOR14,
NR7R8, NR7(CH2)nNR7R8, NR10COR9, NR10CONR7R8, SR11, S(О)yR11, CО2R9, COR9, CONR7R8, CHO, CH=NOR11, CH=NR9, CH=NNR11R12, (CH2)nSR9, (CH2)nS(О)yR9, CH2SR15, CH2S(О)yR14, (CH2)nNR7R8 и (CH2)nNHR14;
e) X выбран из группы, состоящей из -N-, -О-, -S-, -S(=О)-, -S(=О)2-, алкилена с 1-3 углеродами, -С(=О)-, -С(R2)=C(R2)-, -C(R2)2-, -СН=СН-, -СН(ОН)-СН(ОН)-, -C(=NOR11)-, -С(OR11)(R11)- -C(=О)CH(R15)-, -CH(R15)C(=О)-, -CH2-Z-, -Z-CH2-, -CH2ZCH2-, где Z выбран из группы, состоящей из -С(OR11)(R11)-; О, S, С(=О), и NR11; и алкилена с 1-3 углеродами, замещенного группой, выбранной из группы, состоящей из одной R5 группы-заместителя, SR10, OR10, OR14, R15, фенила, нафтила и арилалкила с 7-14 углеродами.
Используемый здесь термин "арил" означает моноциклические и полициклические ароматические группы, включающие, например, фенильные, нафтильные, бифенильные и ксилильные группы. Арильные группы могут быть незамещены или замещены, например, алкильными группами и галогенами. Галогены включают фтор, хлор, бром и иод. Предпочтительными являются арильные группы, которые содержат 6-10 углеродов. Фенильные и нафтильные группы особенно предпочтительны.
Используемый здесь термин "гетероарил" означает арильную часть, которая содержит, по крайней мере, один основной атом азота и 0-4 гетероатомов, выбранных из О, S и N. Примеры гетероарильных групп включают пирролил, пиранил, тиопиранил, фурил, имидазолил, пиридил, тиазолил, триазинил, фталимидо, индолил, пиринил и бензотиазолил.
Используемый здесь со ссылкой на определение R14 термин "аминокислота" означает молекулу, содержащую как аминогруппу, так и карбоксильную группу. Он включает "α-аминокислоту", которая имеет свое обычное значение как карбоновая кислота, которая несет аминофункциональность на углероде, соседнем к карбоксильной группе. α-Аминокислоты могут быть природного происхождения или неприродного происхождения. Аминокислоты также включают "дипептиды", которые определены здесь как две аминокислоты, которые соединены пептидной связью. Таким образом, составляющие дипептидов не ограничиваются α-аминокислотами и могут быть любой молекулой, содержащей как аминогруппу, так и карбоксильную группу. Предпочтительными являются α-аминокислоты, дипептиды, такие как лизил-β-аланин, и аминоалкановые (alkanoic) кислоты с 2-8 углеродами, например 3-диметиламиномасляная кислота.
Предпочтительные "алкильные", "алкенильные" и "алкинильные" группы содержат 1-4 углеродных атомов.
Предпочтительные R1 группы включают Н, алкил с 1-4 углеродами, замещенный или незамещенный фенил, OR10 и О(СН2)nNR7R8. Предпочтительные фенильные заместители включают алкил с 1-4 углеродами и галоген. Наиболее предпочтителен Н.
Предпочтительные R2 группы включают Н, C(=О)R9, алкил с 1-8 углеродами и алкил с 1-8 углеродами, замещенный одной OR9, ОН, OCOR9, NR7R8, NH2, NR10COR9 или NR10R14 группой. Наиболее предпочтителен Н.
Предпочтительные R3 и R4 группы включают Н, галоген, CN, ОН, OR9, OR14, NH2, NR7R8, (CH2)nOR10, (CH2)nOR14, COR9, NR10COR9, NHR14 и (СН2)nNR7R8. Наиболее предпочтителен Н.
Предпочтительные R5 группы включают Н и алкил с 1-4 углеродами. Наиболее предпочтителен Н.
Предпочтительные Х группы включают -N-, -О-, -S-, алкилен с 1-3 углеродами, -С= О-, -CH2-Z- и -Z-СН2-. Наиболее предпочтительными являются -N-, -О-, -S- и -СН2- группы.
III. Применения конденсированных пирроло[2,3-с]карбазол-6-онов
Предлагаемые нами конденсированные пирроло[2,3-с]карбазол-6-оны проявили целый ряд (a panoply) важных функциональных активностей, которые находят применение в ряде областей (settings), включая как область научно-исследовательской работы, так и терапевтическую область. Для легкости представления и для того, чтобы не ограничивать диапазон применений, для которых эти соединения могут быть охарактеризованы, предпочтительные активности конденсированных пирроло[2,3-с] карбазол-6-онов могут быть обычно описаны следующим образом:
А. Усиление IFN-γ индукции МНС молекул;
В. Потенцирование функции и/или выживаемости клеток, чувствительных к трофическому фактору.
Усиление IFN-γ индукции МНС молекул может быть предпочтительно установлено, используя клеточную линию моноцитов человека, которая отвечает на IFN-γ; особенно предпочтительная клеточная линия доступна от the American Type Culture Collection (ATCC), называемая ТНР-1, под инвентарным номером (accession number) ATCC TIB-202. IFN-γ, как известно, индуцирует экспрессию трех МНС II гетеродимеров. HLA-DP, HLA-DQ и HLA-DR; в ТНР-клетках. Потенцирование функции и/или выживаемости клеток, чувствительных к трофическому фактору, например клеток нервного происхождения (рода, относящегося к нервным клеткам), может быть предпочтительно установлено, используя анализ культивированной холин ацетилтрансферазы ("ChAT") спинного мозга (a cultured spinal cord choline acetyltransferase ("ChAT") assay).
Используемый здесь термин "потенцирование" при использовании его для модификации терминов "функция" и "выживаемость" означает положительное изменение или изменение. Потенцирование, которое является положительным, может здесь также называться как "увеличение" или "усиление".
Используемые здесь термины "увеличение" или "усиление", будучи использованными для модификации терминов "функция" и "выживаемость", означают, что присутствие конденсированного пирроло[2,3-с]карбазол-6-она оказывает сравнительно более высокое действие на функцию и/или выживаемость клетки, чувствительной к трофическому фактору, или, в случае IFN-γ, на индукцию МНС молекул, чем на сравнительную клетку, не представленную конденсированным пирроло[2,3-с]карбазол-6-оном.
Используемый здесь термин "нейрон", "клетка, относящаяся к нервным клеткам", "нейронная клетка" включает, но не ограничивается гетерогенную популяцию нейронных типов, имеющих сингулярные или множественные трансмиттеры и/или сингулярные или множественные функции; предпочтительно нейроны являются холинергическими нейронами. Используемый здесь термин "холинергический нейрон" означает нейроны центральной нервной системы (ЦНС, CNS) и периферической нервной системы (ПНС, PNS), чьим нейротрансмиттером является ацетилхолин; иллюстративными примерами являются нейроны базального переднего мозга и спинного мозга.
Используемый здесь термин "трофический фактор" представляет молекулу, которая прямо или косвенно (непрямо) влияет на выживаемость или функцию клетки, чувствительной к трофическому фактору. Примеры трофических факторов включают цилиарный нейротрофический фактор (Ciliary Neurotrophic Factor) (CNTF), основной фактор роста фибробласта (basic Fibroblast Growth Factor) (bFGF), инсулиновый и инсулиноподобный факторы роста (insulin and insulin-like growth factors) (например, IGF-I, IGF-II, IGF-III), интерфероны, интерлейкины, цитокины, и нейротрофины, включая фактор роста нерва (Nerve Growth Factor) (NGF), Нейротрофин-3 (NT-3), Нейротрофин-4/5 (NT-4/5) и нейротрофиновый фактор, полученный из мозга (Brain Derived Neurotrophic Factor) (BDNF).
Используемый здесь термин "клетка, чувствительная к трофическому фактору", представляет клетку, которая включают рецептор, с которым трофический фактор может специфически связываться; примеры включают нейроны (например, холинергические нейроны) и ненейронные клетки (например, моноциты и неопластические клетки).
Используемый здесь термины "активность трофического фактора" и "активность, индуцированная трофическим фактором" определяются как любой ответ, который прямо или косвенно (непрямо) является следствием связывания трофического фактора (например, NT-3) с клеткой, включающей рецептор трофического фактора.
Используемый здесь в выражениях "активность трофического фактора" и "активность, индуцированная трофическим фактором", термин "трофический фактор" включает как эндогенный, так и экзогенный трофические факторы, где "эндогенный" относится к трофическому фактору, уже присутствующему, а "экзогенный" относится к трофическому фактору, добавляемому к системе. По определению, "активность, индуцированная трофическим фактором", включает активность, индуцированную (1) эндогенными трофическими факторами; (2) экзогенными трофическими факторами и (3) комбинацией эндогенных и экзогенных трофических факторов.
А. Усиление IFN-γ индукции МНС молекул
Соединения изобретения могут быть использованы для повышения IFN-γ индукции МНС молекул. Указанный IFN-γ эффективен при лечении вирусных инфекций и некоторых опухолей. Однако из-за побочных действий, ограничивающих его дозу, применение IFN-γ ограничено. В иммунокомпромиссной ситуации, например у пациента с подтвержденной вирусной инфекцией, повышение IFN-γ опосредованного иммунного ответа было бы полезным при условии, что IFN-γ индуцирует экспрессию МНС молекул. Поэтому соединения данного изобретения, которые повышают способность эндогенного IFN-γ или экзогенно введенного IFN-γ индуцировать МНС экспрессию, являются полезными.
Как детально описано в разделе V ниже, способность конденсированного пирроло[2,3-с] карбазол-6-она повышать IFN-γ МНС молекул предпочтительно оценивают, используя ТНР-1 клеточную линию. Эта клеточная линия подтверждает экспрессию МНС II гетеродимера HLA-DR. Сравнение экспрессии HLA-DR в присутствии IFN-γ и IFN-γ плюс одно или несколько конденсированных пирроло[2,3-с] карбазол-6-онов данного изобретения обеспечивает быстрый и эффективный способ определения усиления IFN-γ индукции МНС молекул и может быть оценено.
Соединения данного изобретения могут быть использованы для разработки in vitro моделей повышения экспрессии МНС молекул, функции, идентификации или для скрининга других синтетических соединений, которые имеют активности, сходные с активностями конденсированных пирроло[2,3-с]карбазол-6-онов. Соединения могут быть использованы в круге исследований, направленных на исследование, очистку и определение молекулярных мишеней, связанных с функциональными ответами. Например, путем радиомечения конденсированного пирроло[2,3-с] карбазол-6-она, связанного со специфической клеточной функцией (например, HLA-DR индукция), мишень (как таковая, объективно существующая), с которой связывается конденсированный пирроло[2,3-с]карбазол-6-он, может быть идентифицирована, выделена и очищена для идентификации (определения характеристик). В следующем примере конденсированный пирроло[2,3-с]карбазол-6-он может быть использован в качестве скринирующего инструмента для обнаружения средств, которые имеют маргинальную активность, но при комбинировании с, по крайней мере, одним раскрытым конденсированным пирроло[2,3-с]карбазол-6-оном способны усилить IFN-γ индукцию МНС молекул. Поскольку предлагаемые конденсированные пирроло[2,3-с]карбазол-6-оны используют для усиления IFN-γ индукции МНС молекул, предлагаемые соединения с успехом могут быть предложены для использования в качестве терапевтических средств. Такое усиление имеет значение для иммунокомпромиссного пациента.
В. Потенцирование функции и/или выживания клеток, чувствительных к трофическому фактору.
Конденсированные пирроло[2,3-с]карбазол-6-оны данного изобретения могут быть использованы для усиления функции и/или выживания клеток нейронного происхождения. Конденсированные пирроло[2,3-с]карбазол-6-оны могут быть использованы индивидуально или с другими конденсированными пирроло[2,3-с]карбазол-6-онами, или в комбинации с другими полезными молекулами, такими как индолкарбазолами, которые также имеют способность потенцировать функцию и/или выживание указанной клетки. В ситуациях, когда конденсированный пирроло[2,3-с] карбазол-6-он, как полагают, усиливает биологическую активность, например нейротрофическую активность, экзогенные нейротрофины, такие как NT-3, могут быть использованы в сочетании с конденсированным пирроло[2,3-с] карбазол-6-оном.
Ряд неврологических нарушений характеризуются нейронными клетками, которые погибают, повреждаются с функциональным нарушением, подвергаются аксонной дегенерации при риске отмирания, и т.д. Эти расстройства включают, но не ограничиваются: болезнь Альцгеймера; расстройства двигательного нейрона (например, боковой амиотрофический склероз); болезнь Паркинсона; цереброваскулярные нарушения (например, рассеянный склероз, периферические невропатии (например, невропатии, затрагивающие DRG нейроны при периферической нейропатии, ассоциированной с химиотерапией); расстройства, вызванные возбудительными (excitatory) аминокислотами; расстройства, связанные с повреждениями при сотрясении головного мозга или спинного мозга или проникающими внутрь повреждениями головного мозга или спинного мозга.
Как описано в разделе V ниже, способность конденсированного пирроло[2,3-с] карбазол-6-она усиливать функцию и/или выживание клеток нейронного происхождения может быть определена, используя анализ ChAT активности базального головного мозга. ChAT катализирует синтез ацетилхолина-нейротрансмиттера и ее считают ферментативным маркером для функционального холинергического нейрона. Функциональный нейрон также способен к выживанию. Повышение нейротрофина, такого как NT-3, может быть определено путем сравнения функциональной активности нейротрофина в присутствии или отсутствии конденсированного пирроло[2,3-с]карбазол-6-она.
Фармацевтически приемлемые соли конденсированных пирроло[2,3-с]карбазол-6-онов также охватываются объемом данного изобретения. Используемый здесь термин "фармацевтически приемлемые соли" означает соль присоединения неорганической кислоты, такую как гидрохлорид, сульфат, и фосфат, или соль присоединения органической кислоты, такую как ацетат, малеат, фумарат, тартрат и цитрат. Примерами фармацевтически приемлемых солей металла являются соли щелочных металлов, такие как соль натрия и соль калия, соли щелочноземельных металлов, такие как соль магния и соль кальция, соль алюминия и соль цинка. Примерами фармацевтически приемлемых солей аммония являются соль аммония и соль тетраметиламмония. Примерами фармацевтически приемлемых солей присоединения органических аминов являются соли с морфолином и пиперидином. Примерами фармацевтически приемлемых солей присоединения аминокислот являются соли с лизином, глицином и фенилаланином.
Предлагаемые здесь соединения могут быть составлены в фармацевтические композиции путем смешения с фармацевтически приемлемыми нетоксичными эксципиентами и носителями. Такие композиции можно получить для использования при парентеральном введении, в частности, в форме жидких растворов или суспензий; или оральном введении, в частности, в форме таблеток или капсул; или для применения интраназально, в частности, в форме порошков, капель для носа или аэрозолей; или применения дермально при помощи, например, трансдермальных повязок.
Композицию обычно применяют в единичной лекарственной форме и ее можно приготовить любым из способов, известных в фармацевтической области, например, описанных в Remington's Pharmaceutical Sciences (Mack Pub. Co., Easton, PA, 1980). Составы для парентерального применения могут содержать в качестве стандартных наполнителей стерильную воду или физиологический раствор, полиалкиленовые гликоли, такие как полиэтиленгликоль, масла и масла растительного происхождения, гидрированные нафталины и т.п. В частности, биосовместимый, биодеградируемый лактидный полимер, лактид/гликолид сополимер или полиоксиэтилен-полиоксипропиленовые сополимеры могут быть полезными наполнителями для контролируемого высвобождения активных соединений. К другим потенциально полезным системам для парентеральной доставки этих активных соединений относятся частицы этилен-винилацетатного сополимера, осмотические насосы, имплантируемые системы инфузии и липосомы. Составы для введения путем ингаляции содержат в качестве наполнителей, например, лактозу, или могут представлять собой водные растворы, содержащие, например, полиоксиэтилен-9-лауриловый эфир, гликохолат и дезоксихолат, или представлять масляные растворы для введения в форме капель для носа, или могут быть в виде геля, подлежащего применению интраназально. Составы для парентерального применения могут также включать гликохолат для щечного (внутриротового) введения, салицилат для ректального введения или лимонную кислоту для вагинального введения. Составы для трансдермальных повязок предпочтительно представляют собой липофильные эмульсии.
Соединения данного изобретения могут использоваться как самостоятельное активное средство в фармацевтической композиции. Альтернативно их можно использовать в комбинации с другими активными ингредиентами, например синтетический IFN-γ и/или другими факторами роста, которые облегчают потенцирование NT-3, такими как факторы, раскрываемые в US Patent No. 5468872 и International Publication No. WO 95/07911 (publication date: March 23, 1995).
Концентрации соединений данного изобретения в терапевтической композиции могут варьироваться. Концентрация обычно зависит от факторов, таких как суммарная доза лекарственного средства, подлежащего введению, химических характеристик (например, гидрофобность) применяемых соединений и пути введения. Соединения данного изобретения обычно применяют в водном физиологическом буферном растворе, содержащем приблизительно 0,1-10 мас.%/об. соединения для парентерального применения. Диапазон типичной дозы составляет приблизительно от 1 мкг/кг до 1 г/кг веса тела в день; предпочтительный диапазон дозы составляет приблизительно от 0,01 мг/кг до 100 мг/кг веса тела в день. Предпочтительная дозировка лекарственного средства, подлежащего применению, по-видимому, зависит от переменных, таких как тип и степень прогрессирования болезни или расстройства, общего состояния здоровья конкретного пациента, относительной биологической эффективности выбранного соединения и состава соединения-наполнителя и пути его введения.
IV. Общее описание способов синтеза
Для получения производных конденсированного пирроло[2,3-с]карбазол-6-она данного изобретения используют два пути синтеза. В способе А (фиг.2) производное 2-(арил) или 2-(гетероарил)индола (1-4), которое является либо незамещенным, либо замещенным при углеродах 4-7 (включительно) индольного кольца (R3), или замещенным или незамещенным в (гетеро)арил положении (R4), подвергают взаимодействию с малеимидом в присутствии катализатора, такого как трифторуксусная кислота (TFA, ТФК) с получением производных конденсированного пирролокарбазол-6-она формулы I (примеры I-IV). Для осуществления реакции могут быть также использованы дополнительные катализаторы-кислоты Льюиса, такие как SnCl4, А1С13, EtAlCl2 или Et2AlCl. Реакцию можно также проводить в растворителе, таком как ТФК, толуол, СН2С12 или 1,2-дихлорэтан.
Биарил индольные промежуточные 2,2'-бииндол 1 (X=N, R2, R3, R4=H), 2-(2-фурил)индол 2 (Х=0, R2, R3, R4=H) и 2-(бензотиенил) индол 3 (X=S, R2, R3, R4= H) можно получить, используя стандартные опубликованные методики (Hudkins, R.L., et al., J. Org. Chem., 1995, 60, 6218) (фиг.2). Производные 2(2-Инденил) индола 4 (фиг.3) (X=CH2, R2, R3, R4=H) или 2-(2-инденил)индола, замещенные R3 или R4 группой, можно получить взаимодействием 1-карбокси-2-(трибутилстаннил)индола 5 или 1-карбокси-2-(трибутилстаннил)индола, замещенного R3 группой (Hudkins, R.L. et al., J. Org. Chem., 1995, 60, 6218), с 2-броминденом 6 (J. Org. Chem., 1982, 47, 705) или 2-броминденом, замещенным R4 группой. Альтернативно производные 2-(2-инденил) индола 4 (X=СН2, R2, R3, R4= H) или 2-(2-инденил)индола, замещенные R3 или R4 группой, можно получить взаимодействием lH-индола или его производного, содержащего R3 группу, защищенного в виде литий индол-1-карбоксилатного интермедиата (Tetrahedron Lett. 26: 5935 (1985)), затем обрабатывают сильным основанием, таким как т-BuLi, затем алкилируют соответствующим 2-инданоном или 2-инданонпроизводным, замещенным R4 группой, получая соответствующий третичный спирт 7 (фиг.4). Полученный третичный спирт 7 обрабатывают разбавленной кислотой (например, 2N НС1 в ацетоне), получая соответствующий 2-(2-инденил)индол 4 (US Patent 5475110). Используя другие бензоциклоалкан-2-оны, такие как 2-тетралон, в последовательности реакций, представленной на фигуре 4, можно получить 2-(2-(3,4-дигидронафтил)индол 8 (X=CH2CH2, R2, R3, R4=H) (пат. США 5475110). Можно использовать метод катализируемого палладием перекрестного сочетания (Stille реакция) для получения других производных, например, где Х на фигуре 3 имеет 1-3 углерода (включительно), путем сочетания 2-(трифторметансульфоната)- или 2-иодо- или 2-бромвинилпроизводного соответствующего циклического кетона с 1-карбокси-2-трибутилстаннилиндолом, получая 2-(2-бензоциклоалкенил)индолы.
Описанное ранее исходное производное IH-индола превращают в производное 1-замещенного индола (R2 не Н) при помощи стандартной методологии, например путем обработки IH-индола основанием и алкилирующим агентом, получая 1-замещенный индол. В этих примерах производное индола может быть непосредственно обработано сильным основанием (например, т-BuLi, втор-BuLi, н-BuLi, литий диизопропиламид) с последующим алкилированием производным 2-инданона, получая соответствующий третичный спирт 7, который включает R2 заместители в положении один индольного кольца. Производное 2-(арил)- или 2-(гетероарил)индола (1-3), 2-(2-инденил)индол 4 или 2-(2-(1,2-дигидронафтил)индол 8 могут быть превращены в интермедиаты, которые содержат R2 заместители в положении один индольного кольца по способу, описанному выше для производных индола.
Соединения общих формул I и II, которые содержат R1 группы, не = Н, можно получить исходя из соответствующего R1 замещенного малеимида (фиг.2, способ А). Соединения общих формул I и II, в которых R1 представляет водород, можно алкилировать в присутствии основания (например, гидриды, алкоксиды, гидроксиды щелочных или щелочноземельных металлов или литийорганические соединения) обработкой R1L, где L представляет отщепляемую группу, такую как галоген, мезилат или тозилат, с получением производного конденсированного пирролокарбазол-6-она, которое имеет R1 группу, связанную с азотом лактама. Соединения общих формул I и II, в которых R5 является водородом, можно превратить в производные, где одна или две R5 группы могут быть введены путем обработки производного конденсированного пирролокарбазол-6-она одним эквивалентом или избытком сильного основания (например, гидриды, алкоксиды, гидроксиды щелочных или щелочноземельных металлов или литийорганические соединения) с R5L, где L представляет отщепляемую группу, такую как галоген, или путем конденсации с R5 содержащим кетоном или производным альдегидкарбонила, получая производное конденсированного пирролокарбазол-6-она, которое имеет одну или две R5 группы. Производные от реакций кетон- или альдегидной конденсации обычно дают винильные производные при R5.
Производные индола получают, используя стандартную методологию (US Patent 3976639; US Patent 3732245; The Chemistry of Heterocyclic Compounds. Indoles Parts One and Two; Houlihan Ed., Wiley-Interscience (1972)). Производные 2-инданона можно получить, используя ранее описанные способы (смотри US Patent 4192888; US Patent 4128666; J. Am. Chem. Soc. 89:4524 (1967); Tetrahedron Lett. 43:3789 (1974); Сhem. Ber. 122:1791 (1989); Can. J. Chem. 60: 2678 (1982); Helvetica Chimica Acta 70:1791 (1987). Chem. Pharm. Bull. 33: 3336 (1985); J. Org. Chem. 55: 4835 (1990); Tetrahedron 45:1441 (1989); Synthesis 818 (1981)).
В способе В (фиг.2) производное 2-(гетероарил)индола (1-3) или производное 2-(арил)индола, такое как 2-(2-инденил)индол 4, подвергают взаимодействию с этил цис-β-цианоакрилатом в присутствии катализатора, такого как SiCl4, А1С13, EtAlCl2, Et2AlCl или ТФК, в СН2Cl2, С2Н4С12 или толуола в качестве растворителя, получая соединения 6-оксокарбазола формулы I изобретения.
Соединения формулы II получают, как показано на фиг.5. Присоединение 2-(арил)- или 2-(гетероарил)индолилцинкреагентов (Tetrahedron Lett., 1994, 35, 793; Tetrahedron Lett. , 1994, 35, 7123; Tetrahedron Lett., 1993, 35, 5955: Tetrahedron Lett., 1993, 34, 6245) к сукцинимиду или производному R1 замещенного сукцинимида с помощью реакции Реформатского (Reformatzsky) (Synthesis, 1975, 685) с последующей дегидратацией обычно дает соединения общей структуры 9. Палладий-катализируемое раскрытие кольца (US Patent 5475110; Tetrahedron Lett. , 1993, 34, 8361) обычно дает соединения пирроло[2,3-с]карбазола формулы II.
Соединения, в которых Х=(С=О) (общая структура 10), получают окислением производных общей формулы I (или II), где Х=СН2, используя стандартные окисляющие реагенты (например, SeO2, СrО3, Na2CrО7 или МnО2) (фиг.6). Альтернативно 2-(2-инденил)индол 4 можно окислить в 2-(2-(1-оксоинденил)индол и использовать для получения соединений формулы I или II, где Х=(С=О), способом, представленном на фигурах 2 и 5. Альтернативно 2-(2-(1-оксоинденил)) индол 11 можно получить, используя методологию палладий-катализируемого перекрестного связывания (сочетания) (фиг.3), путем связывания (сочетания) 1-карбокси-2-трибутилстаннилиндола 5 или его производных с 2-(трифторметансульфонил)оксиинден-1-оном или 2-броминден-1-оном 12 (фиг.7) (J. Org. Chem. , 1994, 59, 3453) или одним из его производных. Соединения общей структуры 10 (X=(С=О)) могут подвергаться ряду реакций олефинирования присоединения и конденсации, известных специалистам в области органического синтеза, с получением производных, например, таких как, но не ограничиваясь ими, Х=(С=С(R2)2), C(R2)2, С(OR11)R11). Производные конденсированного пирролокарбазол-6-она, где Х представляет S(=О) или S(=О)2, могут быть получены окислением X=S производных способом, аналогичным Х=(С=О).
ПРИМЕРЫ
V. Конкретное описание способов синтеза
Нижеследующие примеры представлены для иллюстрации и их не следует рассматривать как ограничивающие каким-либо образом объем данного изобретения.
А. Пример I: 5Н,7Н,13Н-Бензофурано[2,3-а]пирроло[2,3-с]карбазол-6(6Н)он (X=О; R1, R2, R3, R4, R5=Н)
Смесь 2-(2-бензофурил)индола 2 (250 мг; 1,0 ммоль) и малеимида (110 мг; 1,2 ммоль) в трифторуксусной кислоте (2 мл) нагревают в герметизированной реакционной ампуле при 125oС в течение 18 ч. Осажденное твердое вещество собирают, промывают ТФК (TFA) и сушат, получая 150 мг (48%) продукта. Перекристаллизация (ТГФ, THF) дает желто-коричневое твердое вещество; т. пл. >300oС, МС (ЭС+) 312 (М+), 1H ЯМР (DМСО-d6) δ 4,00 (с, 2Н), 4,13 (с, 2Н), 7,12 (т, 1Н), 7,37 (т, 2Н), 7,45 (т, 2Н), 7,71 (д, 1Н), 7,95 (д, 1Н), 8,54 (д, 1Н), 10,12 (с, 1Н), 11,79 (с, 1Н). Анал. рассчит. для C20H12N202•0,4 Н2О; С, 75,18; Н, 4,04; N, 8,77. Найдено: С, 75,29, Н, 3,86, N, 8,60.
В. Пример II: 5Н,7Н,13Н-Бензотиено[2,3-а]пирроло[2,3-с]карбазол-6(6Н)он (X=S; R1, R2, R3, R4, R5=H)
Смесь 2-(2-бензофурил)индола 2 (100 мг; 0,4 ммоль) и малеимида (40 мг; 0,4 ммоль) в трифторуксусной кислоте (2 мл) нагревают в герметизированной реакционной ампуле при 125oС в течение 16 ч. Осажденное твердое вещество собирают, промывают холодным метанолом и сушат, получая 80 мг (58%) продукта. Перекристаллизация (ТГФ) дает желто-коричневое твердое вещество; т. пл. >300oС, МС (ЭС+) 328 (М+) 1Н ЯМР (ДМСО-d6) δ 4,10 (с, 2Н), 7,20 (т, 1Н), 7,40-7,60 (м, 4Н), 8,10 (д, 1Н), 8,80 (м, 1Н), 10,86 (с, 1Н), 11,80 (с, 1Н). Анал. рассчит. для C20H12N2SO•0,5•H2О; С, 71,20; Н, 3,88; N, 8,30. Найдено: С, 70,86, Н, 3,61, N, 8,39.
С. Пример III: 5Н,7Н,12Н,13Н-Индоло[2,3-а]пирроло[2,3-с]карбазол-6(6Н) (X=N; R1, R2, R3, R4, R5=Н)
(1) Способ А
К смеси 2-2'-бииндола 1 (250 мг; 110 ммоль) и малеимида (110 мг; 1,2 ммоль), суспендированной в толуоле (50 мл), добавляют трифторуксусную кислоту (0,5 мл). Раствор нагревают при температуре кипения флегмы в течение 18 ч, охлаждают до комнатной температуры и концентрируют до приблизительно 20 мл. Раствор охлаждают на бане со льдом, осажденное твердое вещество собирают, промывают холодным эфиром и сушат, получая 150 мг (55%) продукта. Очистка с помощью колоночной хроматографии (ЕtОАс:гексаны; 2:1) дает коричневое-желтовато-коричневое (brown-tan) твердое вещество, т. пл. >320oС, МС (ЭС+) 311 (М+), 1Н ЯМР (ДМСО-d6) δ 4,00 (с, 2Н), 7,17-7,22 (м, 2Н), 7,37-7,42 (м, 2Н), 7,67 (д, 2Н), 8,03 (д, 1Н), 8,58 (д, 1Н), 10,87 (с, 1Н), 10,92 (с, 1Н), 11,18 (с, 1Н). Анал. рассчит. для C20H12N2O2•0,5•H2O; С, 74,99; Н, 4,41; N, 13,12. Найдено: С, 75,24, Н, 4,02, N, 13,05.
(2) Способ В
Смесь 2-2'-бииндола 1 (100 мг; 0,43 ммоль) и этил цис-β-цианоакрилата (50 мг; 0,4 ммоль) в метиленхлориде (10 мл) добавляют 25 мл SnCl4. Смесь перемешивают при комнатной температуре в течение 30 мин. Суспензию охлаждают на бане со льдом, твердое вещество собирают, промывают холодным эфиром и сушат, получая 36 мг (27%) продукта. Очистка с помощью колоночной хроматографии (ЕtOАс: гексаны; 2:1) дает коричневое-желтовато-коричневое твердое вещество; т. пл. >320oС, МС (ЭС+) 311 (М+), 1H ЯМР (DMCO-d6) δ 4,00 (с, 2Н), 7,17-7,22 (м, 2Н), 7,37-7,42 (м, 2Н), 7,67 (д, 2Н), 8,03 (д, 1Н), 8,58 (д, 1Н), 10,87 (с, 1Н), 10,92 (с, 1Н), 11,18 (с, 1Н). Это соединение показывает спектральные и аналитические характеристики, идентичные характеристикам, полученным способом А.
D. Пример IV: 5Н,7Н,12Н,13Н-Индено[2,3-а]пирроло[2,3-с]карбазол-6(6Н)он (X=СН2; R1, R2, R3, R4, R5=Н)
(1) Способ А
Смесь 2(2-инденил) индола 4 (300 мг; 1,3 ммоль) и малеимида (160 мг; 1,6 ммоль) в трифторуксусной кислоте (2 мл) нагревают в герметизированной реакционной ампуле при 160oС в течение 18 ч. Раствор выпаривают и твердое вещество растворяют в этилацетате, затем промывают водой и сушат (МgSO4), получая коричневый твердый продукт. Неочищенный продукт хроматографируют (силикагель, ЕtOAс:гексаны; 1:1), получая продукт, который обрабатывают ТГФ и фильтруют. Концентрированный остаток растирают с МеОН, получая продукт: т. пл. 275-280oС, МС (ЭС+) 310 (М+), 1Н ЯМР (DMCO-d6) δ 4,00 (с, 2Н), 4,13 (с, 2Н), 7 17 (т, 1Н), 7,25-7,42 (м, 3Н), 7,50 (д, 1Н), 7,71 (д, 1Н), 8,00 (д, 1Н), 8,37 (д, 1Н), 10,75 (с, 1Н), 11,33 (с, 1Н), ИК (KВr) 1650-1700 см-1. Анал. рассчит. для C21H14N2O•0,7 H2O; С, 78,10; Н, 4,81; N, 8,65. Найдено: С, 78,13, Н, 4,41, N, 8,10.
(2) Способ В
Смесь 2(2-инденил) индола 4 (75 мг; 0,32 ммоль) и этил цис-β-цианоакрилата (81 мг; 0,64 ммоль) в трифторуксусной кислоте (1 мл) нагревают в герметизированной реакционной ампуле при 120oС в течение 1 ч, а затем 4 ч при 160oС. Смесь выпаривают при пониженном давлении и остаток растирают с эфиром. Полученное твердое вещество хроматографируют (силикагель; ЕtOАс:гексаны; 1:1), получая 12 мг (12%) желтовато-коричневого твердого продукта; т. пл. 275-280oС, МС (ЭС+) 310 (М+). Это соединение показывает спектральные данные, аналогичные данным, полученным cпособом А.
Е. Пример V: Усиление конденсированными пирроло[2,3-с]карбазол-6-онами, вызванной IFN-γ индукции МНС антиген HLA-DR
Клеточную линию человека, полученную из человеческих моноцитов, ТНР-1 (АТСС TIB 202), которая отвечает на IFN-γ, используют для демонстрации повышения HLA-DR конденсированными пирроло[2,3-С] карбазол-6-онами.
ТНР-1 клетки выращивают в RPMI 1640 среде, содержащей 20 мкМ меркаптоэтанола и 10% фетальной телячьей сыворотки при 37oС в атмосфере, имеющей состав 5% СО2:95% воздуха при 100% влажности. Для определения повышения HLA-DR соединениями данного изобретения клетки либо оставляют необработанными в качестве контроля, обрабатывают только IFN-γ при концентрации 100 единиц/мл, либо обрабатывают соединениями изобретения при конечной концентрации 1 мкМ в течение 30 мин до добавления IFN-γ при концентрации 100 единиц/мл. Во всех экспериментах были использованы идентичные (дублированные) культуры. Обработанные ТНР-1 клетки инкубируют при 37oС в течение 48 часов и затем подготавливают для анализа HLA-DR методом проточной цитометрии. Индуцирование HLA-DR осуществляют путем стандартных процедур, как описано в Interferons and Other Regulatory Cytokines, Edward De Maeyer and Jacqueline De Maeyer Guignard, Chapter 9, John Wiley & Sons, New York, 1988. Клетки препарируют для проточной цитометрии и анализируют на HLA-DR методом проточной цитометрии, как описано в Current Protocols in Immunology. Vol. 1, pages 5.0.1-5.8.8, John Wiley & Sons, 1994. Один миллион клеток от каждой обработки собирают центрифугированием и дважды промывают фосфатно-солевым буферным раствором (PBS). Клетки повторно суспендируют в 100 мкл PBS, содержащего 10 мкг очищенного кроличьего IgG, чтобы блокировать неспецифические сайты на поверхности клеток. После 20 мин выдерживания на льду добавляют 20 мкл анти-HLA-DR моноклонального антитела, меченного флуоресцентной меткой FITC, и клетки оставляют на льду в течение дополнительных 30 мин для того, чтобы дать возможность антителу связаться с HLA-DR. Затем клетки промывают 2 раза PBS и фиксируют в 0,5 мл 0,5% параформальдегида. Фиксированные клетки хранят при 4oС до анализа методом проточной цитометрии.
Повышение HLA-DR представительными конденсированными пирроло[2,3-с] карбазол-6-онами показано на фиг.1. Повышение HLA-DR с помощью только IFN-γ обозначают как 100% на оси Y. Не наблюдается существенной индукции HLA-DR с помощью самих по себе представительных соединений при 1 мкМ (фиг.1). Все из представительных соединений повышают индукцию HLA-DR с помощью IFN-γ сверх индукции только одним IFN-γ, то есть выше 100%. Процентное повышение сверх только одного IFN-γ посредством четырех соединений представлено в таблице 1. Например, при 2 мкМ соединение раздела V(D) (пример IV) усиливает IFN-γ индукцию HLA-DR на 60% по сравнению IFN-γ одного.
F. Пример VI. NT-3 Потенцирование ChAT активности в базальных культурах головного мозга пирроло[2,3-с]карбазол-6-онами
Способность пирроло[2,3-с]карбазол-6-онов потенцировать NT-3 активность в базальных культурах головного мозга определяют, используя холин ацетилтрансферазную (ChAT) активность как меру холинергической нейронной функции или выживаемости. Эти соединения, сами по себе, не оказывают действия на ChAT активность. Однако в присутствии NT-3 представительные соединения дают дозазависимое потенцирование ChAT активности до уровней, больших, чем уровни, которые достигаются с помощью только NT-3. Результаты, представленные в таблице 2, представляют результат единого применения NT-3 и соединения, подлежащего испытанию, на день инициирования культуры, показывая пролонгированное действие на выживаемость или функцию холинергических нейронов базального головного мозга. Применяемые методы описаны в US Patent 5468872, Columns 18 и 19. NT-3 (100 нг/мл) увеличивает ChAT активность 163±5% (среднее ± СО) по сравнению с контрольными необработанными культурами. Испытываемые соединения сами по себе имеют базальный (100%) уровень активности (р<0,05 статистически существенен при сравнении с NT-3 активностью самой по себе согласно Dunnett t статистики).
Специалистам в данной области техники очевидно, что возможны различные изменения и модификации предпочтительных вариантов изобретения и что такие изменения и модификации могут быть сделаны не выходя за рамки сущности данного изобретения. Поэтому имеется в виду, что нижеследующая формула изобретения охватывает все эквивалентные изменения, не выходящие за рамки сущности и объема изобретения. Документы, цитированные на протяжении раскрытия этого патента, включены здесь в качестве уровня техники.
Заявителем получены еще два соединения, входящие в круг соединений по пункту 1: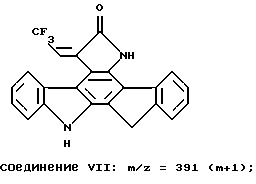
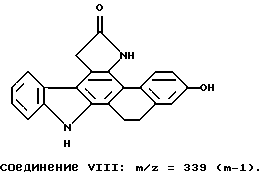
Эти соединения были синтезированы в соответствии с описанными в заявке приемами, методами и способами, а в опытах по усилению вызванной IFN-γ индукции МНС антиген HLA-DR показали активность на уровне соединения примера I и II соответственно, а в опыте NT-3 потенцирования ChAT активности в базальных культурах на уровне соединения I. Что касается свойств, обуславливающих одинаковое назначение заявленных соединений, то заявитель утверждает, что указанной в материалах заявки активностью обладает весь круг заявленных соединений. Это дополнительно подтверждает активность двух вновь полученных соединений, которая, как прогнозировалось заявителем, оказалась соответствующей требуемым параметрам.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНДЕНСИРОВАННЫЕ ИЗОИНДОЛОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ С | 1996 |
|
RU2191175C2 |
| ИНГИБИТОРЫ ПРЕДСТАВЛЕНИЯ АНТИГЕНОВ МОЛЕКУЛАМИ МНС II КЛАССА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2004 |
|
RU2333219C2 |
| ПРОИЗВОДНЫЕ К-252А | 1997 |
|
RU2205184C2 |
| СПОСОБ И КОМПОЗИЦИЯ ДЛЯ СТИМУЛЯЦИИ НЕЙРОГЕНЕЗА И ИНГИБИРОВАНИЯ ДЕГЕНЕРАЦИИ НЕЙРОНОВ | 2006 |
|
RU2440346C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2006 |
|
RU2303597C1 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ПКС ПРИ ТРАНСПЛАНТАЦИИ | 2007 |
|
RU2494738C2 |
| 1,3-ДИОКСО -2,3-ДИГИДРО-1H-ПИРРОЛО[3,4-C]ХИНОЛИНЫ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ (ВАРИАНТЫ), СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБЫ ЛЕЧЕНИЯ (ВАРИАНТЫ) | 2003 |
|
RU2257385C2 |
| ПРОИЗВОДНЫЕ ИЗАТИНА ИЛИ ИЗАТИНОКСИМА, СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИЗАТИНОКСИМА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2114827C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДОБЕНЗИМИДАЗОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТОВ ИЛИ АНТАГОНИСТОВ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2005 |
|
RU2392279C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАН-1,4-ДИАМИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2002 |
|
RU2321579C2 |
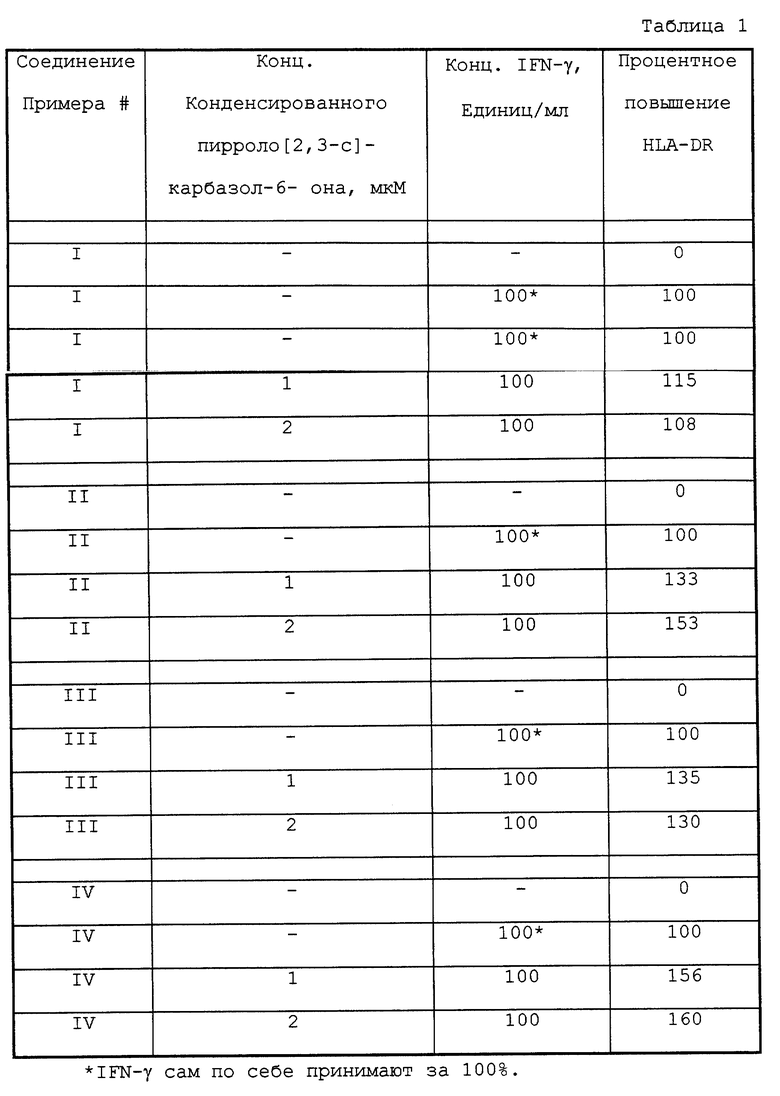
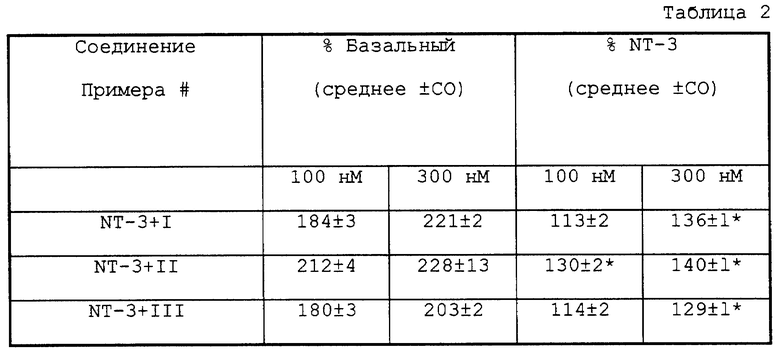
Изобретение относится к новым конденсированным пирроло (2,3-с)карбазол-6-онам, представленным общими формулами (I) и (II).
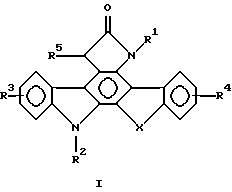
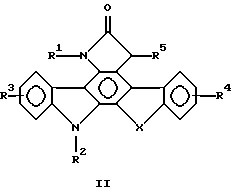
где R1 - Н, С1-С4алкил;
R2 - Н, С1-С8алкил;
R3 и R4 каждый независимо - Н, ОН, С1-С8алкил;
R5 - Н, С1-С8алкил, С1-С8алкенил, необязательно замещенный CF3;
Х - -N-, -О-, -S-, алкилен с 1-3 углеродами. Соединения I и II потенциируют активность человеческого IFN-γ в индуцировании экспрессии МНС на поверхности рецептивных клеток, способны ингибировать рост вируса и/или опухоли. 12 з.п. ф-лы, 7 ил., 2 табл.
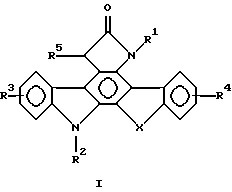
и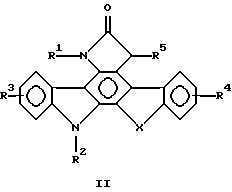
где R1 выбран из группы, состоящей из Н и алкила с 1-4 углеродами;
R2 выбран из группы, состоящей из Н и алкила с 1-8 углеродами;
R3 и R4 каждый независимо выбран из группы, состоящей из Н, ОН и алкила с 1-8 углеродами;
R5 выбран из группы, состоящей из Н, алкила с 1-8 углеродами и алкенила с 1-8 углеродами, необязательно замещенного СF3;
Х выбран из группы, состоящей из -N-, -О-, -S- и алкилена с 1-3 углеродами.
| US 4912107 А, 27.03.1990 | |||
| DE 3803620 A1, 17.08.1989 | |||
| DE 3835842 A1, 26.04.1990 | |||
| DE 3942296 A1, 27.06.1991 | |||
| RU 94015830 A1, 10.01.1996. |
Авторы
Даты
2002-11-20—Публикация
1997-02-20—Подача