ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Область изобретения
Изобретение относится к производным изоксазола, которые могут использоваться, например, в качестве лекарственных средств при лечении аутоиммунных заболеваний, воспалительных заболеваний и тому подобное.
Описание уровня техники
Кислотные нестероидные противовоспалительные лекарственные средства или стероидные лекарственные средства используются в качестве терапевтических лекарственных средств при лечении противовоспалительных заболеваний, но их применение ограничено ввиду наличия побочных эффектов. Кроме того, лечение с использованием таких лекарственных средств, несмотря на их способность улучшать симптомы, не может устранить причину заболевания. По мере развития понимания патофизиологии аутоиммунных заболеваний, таких как ревматоидный артрит, связанный с серьезным воспалением, было высказано предположение, что аутоиммунная система оказывается глубоко затронутой в начале воспаления, по мере его развития и при сохранении хронического состояния. По этим причинам лекарственные средства, способные модифицировать заболевания путем воздействия на иммунную систему, такие как соединения золота и D-пенициллинамин, указываются в качестве лекарственных средств для основного заболевания. Они, однако, не всегда успешны, ввиду присущих им побочных эффектов и недостаточной продолжительности действия.
С другой стороны, сообщалось о производных изоксазола, обладающих различными видами биологической активности. Например, в не прошедшей экспертизу Японской патентной заявке N 63-152368 описаны аралкильные 5-членные гетероциклические производные, включая производные изоксазола, в качестве терапевтических лекарственных средств при аутоиммунных заболеваниях, воспалении, аллергии, астме и тому подобное. В патенте Германии N 2847792 описаны хинолилгуанидиновые производные, включая производные изоксазола, в качестве противовоспалительных, анальгетических и антипиретических лекарственных средств. В J. Med. Chem. 21, 773 (1978) описано, что производные N-циан-N'-изоксазолилгуанидина являются эффективными в качестве гипотензивных лекарственных средств.
Терапевтические лекарственные средства для аутоиммунных заболеваний должны проявлять эффективность в отношении хронического заболевания, которое вызывает разложение ткани. Более того, важно, чтобы они обладали ингибирующим эффектом в отношении заболеваний иммунной системы, ответственной за заболевания, будучи лекарственными средствами для радикального лечения. Кроме того, терапевтические лекарственные средства для заболеваний должны обладать небольшим вредным воздействием, поскольку они часто требуют длительного введения.
Настоящее изобретение относится к соединению, которое может использоваться в качестве терапевтического или профилактического лекарственного средства для аутоиммунных заболеваний, воспалительных заболеваний и тому подобное, обладающему превосходными иммуномодулирующим и антихронически-воспалительными эффектами и проявляющему слабое побочное действие.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения провели серьезные исследования для решения вышеуказанных проблем и в результате обнаружили, что производные изоксазола обладают значительными иммуномодулирующим и антихронически-воспалительными эффектами и небольшими побочными эффектами, что и легло в основу настоящего изобретения.
Таким образом, настоящее изобретение заключается в следующем.
[1] Производное изоксазола, представленное формулой 1: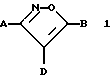
где D представляет атом водорода, атом галогена, гидроксильную группу, меркаптогруппу, нитрогруппу, цианогруппу, карбоксильную группу, замещенную или незамещенную аминогруппу, замещенную или незамещенную гидроксиламиногруппу, замещенную или незамещенную карбамоильную группу, замещенную или незамещенную сульфамоильную группу, сульфогруппу, -R5, -OR5, -CO2R6, -SR7, -(CO)SR7, -(CS)OR7 или -CS2R7, где R5 обозначает замещенную или незамещенную алкильную группу, замещенную или незамещенную алкенильную группу, замещенную или незамещенную алкинильную группу, замещенную или незамещенную циклоалкинильную группу, замещенную или незамещенную циклоалкильную группу, замещенную или незамещенную арильную группу, замещенную или незамещенную гетероциклическую группу, ацильную группу, R6 обозначает замещенную или незамещенную алкильную группу, замещенную или незамещенную алкенильную группу, замещенную или незамещенную алкинильную группу, замещенную или незамещенную арильную группу, замещенную или незамещенную гетероциклическую группу, и R7 обозначает замещенную или незамещенную алкильную группу, замещенную или незамещенную арильную группу;
один из А и В является группой, представленной формулой: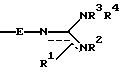
где Е обозначает одинарную связь или алкиленовую группу;
одна из двух пунктирных линий вместе со сплошной линией представляет двойную связь, тогда как другая пунктирная линия вместе со сплошной линией представляет одинарную связь. R1 присоединен к атому азота, который присоединен одинарной связью, представленной пунктирной и сплошной линией; и
R1, R2, R3 и R4 независимо обозначают атом водорода, атом галогена, гидроксильную группу, меркаптогруппу, нитрогруппу, цианогруппу, карбоксильную группу, замещенную или незамещенную аминогруппу, замещенную или незамещенную гидроксиламиногруппу, замещенную или незамещенную карбамоильную группу, замещенную или незамещенную сульфамоильную группу, сульфогруппу, защитную группу для NH группы, -R5, -OR5, -CO2R6, -SR7, -(CO)SR7, -(CS)OR7 или -CS2R7, где R5, R6 и R7 определены выше, любые два из R1, R2, R3 и R4 могут быть взятые вместе с атомом(ами) азота с образованием замещенного или незамещенного гетероциклического кольца; и формула: -NR3R4 может быть группой, представленной следующей формулой: -N=C(NH2)NR43R44, где R43 и R44 определены в (1) или (2)
(1) каждый, независимо, представляет атом водорода; алкильную группу, имеющую от 1 до 4 атомов углерода; -(СН2)n-COCH3, где n равно целому числу от 1 до 3; -(СН2)n-CO2R32, где n определено выше и R32 представляет алкильную группу, имеющую от 1 до 3 атомов углерода; -(СН2)n-CONR33R34, где n определено выше и R33 и R34, независимо, представляют атомы водорода или алкильные группы, имеющие от 1 до 3 атомов углерода; -(СН2)m-OR35, где m равно 2 или 3 и R35 представляет атом водорода, алкильную группу, имеющую от 1 до 3 атомов углерода, или -(СН2)m-OR36, где m определено выше и R36 представляет атом водорода или алкильную группу, имеющую от 1 до 3 атомов углерода; -(СН2)m-NR37R38, где m определено выше и R37 и R38 представляют, независимо, атомы водорода или алкильные группы, имеющие от 1 до 3 атомов углерода, или, взятые вместе с атомом азота, представляют пирролидин, пиперидин, азепан, морфолин или N-метилпиперазин, где указанные пирролидин, пиперидин, азепан, морфолин или N-метилпиперазин могут быть замещены одной или двумя метильными группами; фенильную группу; пиридильную группу; пиримидинильную группу; пиридазинильную группу; пиразинильную группу; тетразолильную группу; бензильную группу; пиридилметильную группу; пиримидинилметильную группу; пиридазинилметильную группу; пиразинилметильную группу; тетразолилметильную группу; гидроксильную группу; алкоксигруппу, имеющую от 1 до 3 атомов углерода; или -NR39R40, где R39 и R40 независимо представляют атом водорода, алкильные группы, имеющие от 1 до 3 атомов углерода; фенильные группы или пиридильные группы;
(2) взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, выбранными из алкильной группы, аминогруппы, гидроксильной группы, алкоксигруппы и оксогруппы; и
другой из А и В является группой, представленной формулой: -J-G, где G представляет замещенную или незамещенную арильную группу или замещенную или незамещенную гетероциклическую группу, где J обозначает -C(R8R9)-, где R8 и R9, независимо представляют атом водорода, замещенную или незамещенную алкоксигруппу, замещенную или незамещенную низшую алкильную группу; R8 и R9 могут быть взяты вместе с атомом углерода с образованием замещенного или незамещенного углеводородного кольца, замещенного или незамещенного 1,3-диоксана, замещенного или незамещенного 1,3-диоксолана,
или его фармацевтически приемлемая соль.
[2] Производное изоксазола или его фармацевтически приемлемая соль по [1], где Е обозначает одинарную связь или низший алкилен.
[3] Производное изоксазола или его фармацевтически приемлемая соль по [1] или [2], где D обозначает атом водорода, нитрогруппу, цианогруппу, карбоксильную группу, замещенную или незамещенную аминогруппу, замещенную или незамещенную гидроксиламиногруппу, замещенную или незамещенную карбамоильную группу, -R5 или -CO2R6, где R5 и R6 определены выше.
[4] Производное изоксазола или его фармацевтически приемлемая соль по [3] , где D обозначает атом водорода, карбоксильную группу, -R5 или -CO2R6, где R5 и R6 определены выше.
[5] Производное изоксазола или его фармацевтически приемлемая соль по [1] -[4], где R1, R2, R3 и R4 независимо обозначают атом водорода, гидроксильную группу, замещенную или незамещенную аминогруппу, замещенную или незамещенную гидроксиламиногруппу, замещенную или незамещенную алкоксигруппу, замещенную или незамещенную алкильную группу, замещенную или незамещенную алкенильную группу, замещенную или незамещенную алкинильную группу, замещенную или незамещенную циклоалкильную группу, замещенную или незамещенную циклоалкенильную группу, замещенную или незамещенную арильную группу, замещенную или незамещенную гетероциклическую группу; и формула: -NR3R4 может быть группой, представленной следующей формулой: -N=C(NH2)NR43R44, где R43 и R44 определены выше; или любые два из R1, R2, R3 и R4 могут быть взятые вместе с атомом(ами) азота с образованием замещенного или незамещенного гетероциклического кольца.
[6] Производное изоксазола или его фармацевтически приемлемая соль по [5] , где R1, R2, R3 и R4 независимо обозначают атом водорода, гидроксильную группу, замещенную или незамещенную аминогруппу, замещенную или незамещенную гидроксиламиногруппу, замещенную или незамещенную алкоксигруппу, замещенную или незамещенную алкильную группу, замещенную или незамещенную алкенильную группу, замещенную или незамещенную алкинильную группу, замещенную или незамещенную циклоалкильную группу; и формула: -NR3R4 может быть группой, представленной следующей формулой: -N=C(NH2)NR43R44, где R43 и R44 определены выше; или любые два из R1, R2, R3 и R4 могут быть взятые вместе с атомом(ами) азота с образованием замещенного или незамещенного гетероциклического кольца.
[7] Производное изоксазола или его фармацевтически приемлемая соль по любому из [1] -[6], где G обозначает замещенную или незамещенную фенильную группу, замещенную или незамещенную нафтильную группу, замещенную или незамещенную фурильную группу, замещенный или незамещенный тиенил, замещенный или незамещенный индолил, замещенный или незамещенный изотиазолил, замещенный или незамещенный бензотиенил, замещенный или незамещенный изобензофуранил, замещенный или незамещенный пирролил, замещенный или незамещенный бензофурил, замещенный или незамещенный имидазолил, замещенный или незамещенный пиразолил, замещенный или незамещенный изоксазолил, замещенный или незамещенный изотиазолил, замещенный или незамещенный тиазолил, замещенный или незамещенный оксазолил, замещенный или незамещенный бензимидазолил, замещенный или незамещенный бензотиазолил, замещенный или незамещенный бензоксазолил, замещенный или незамещенный пиридил, замещенный или незамещенный пиразинил, замещенный или незамещенный пиримидинил, замещенный или незамещенный пиридазинил, замещенный или незамещенный триазинил, замещенный или незамещенный хинолил, замещенный или незамещенный изохинолил, замещенный или незамещенный хиназолинил, замещенный или незамещенный хиноксалинил, замещенный или незамещенный 2,3-дигидробензо[1,4]диоксинил или замещенный или незамещенный карбазолил.
[8] Производное изоксазола или его фармацевтически приемлемая соль по [1], которые представлены формулой: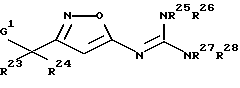
где G1 представляет фенил, бифенил-4-ил, 3-бензоилфенил, 4-бензоилфенил, 1Н-индол-2-ил, 1H-индол-3-ил, 1-метил-1Н-индол-2-ил, 1-метил-1Н-индол-3-ил, 2,3-дигидробензо[1,4] диоксин-6-ил, 1-бензофуран-5-ил, 1-бензофуран-6-ил, хинолил, изохинолил, фенилпиридил, фенилпиримидинил, фенилпиридазинил или фенилпиразинил, где указанные фенил, бифенил-4-ил, 3-бензоилфенил, 4-бензоилфенил, 1Н-индол-2-ил, 1H-индол-3-ил, 1-метил-1Н-индол-2-ил, 1-метил-1Н-индол-3-ил, 2,3-дигидробензо[1,4]-диоксин-6-ил, 1-бензофуран-5-ил, 1-бензофуран-6-ил, хинолил, изохинолил, фенилпиридил, фенилпиримидинил, фенилпиридазинил или фенилпиразинил могут быть замещены одной или двумя группами, произвольно выбранными из группы, включающей атом фтора, атом хлора, атом брома, ацетил, циано, -CO2R29, где R29 представляет арильную группу, имеющую от 1 до 3 атомов углерода, и -CONR30R31, где R30 и R31 независимо представляют атомы водорода или алкильные группы, имеющие от 1 до 3 атомов углерода;
R23 и R24 независимо представляют атомы водорода, алкильные группы, имеющие от 1 до 4 атомов углерода, метокси или этокси, или, взятые вместе, образуют метиленовую группу; и формула: =C(NR25R26)NR27R28 определена в следующих (1), (2) или (3):
(1) R25 и R26 определены в следующих (а) или (b) и R27 и R28 определены в следующих (с) или (d):
(a) каждый представляет, независимо, атом водорода; алкильную группу, имеющую от 1 до 4 атомов углерода;
- (СН2)n-СОСН3, где n определено выше; - (СН2)n-CO2R32, где n и R32 определены выше;
-(СН2)n-CONR33R34, где n, R33 и R34 определены выше;
-(СН2)m-OR35, где m, и R35 определены выше;
-(СН2)m-NR37R38, где m, R37 и R38 определены выше;
фенильную группу; пиридильную группу; пиримидинильную группу; пиридазинильную группу; пиразинильную группу; тетразолильную группу; бензильную группу; пиридилметильную группу; пиримидинилметильную группу; пиридазинилметильную группу; пиразинилметильную группу; тетразолилметильную группу; гидроксильную группу; алкоксигруппу, имеющую от 1 до 3 атомов углерода; или -NR39R40, где R39 и R40 определены выше;
(b) взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из алкильной группы, аминогруппы, гидроксильной группы, алкоксигруппы и оксогруппы;
(c) каждый представляет, независимо, атом водорода; алкильную группу, имеющую от 1 до 4 атомов углерода; -(СН2)n-COCH3, где n определено выше; -(СН2)n-CO2R32, где n и R32 определены выше; -(СН2)n-CONR33R34, где n, R33 и R34 определены выше; -(СН2)m-OR35, где m и R35 определены выше; -(СН2)m-NR37R38, где m, R37 и R38 определены выше; фенильную группу; пиридильную группу; пиримидинильную группу; пиридазинильную группу; пиразинильную группу; тетразолильную группу; бензильную группу; пиридилметильную группу; пиримидинилметильную группу; пиридазинилметильную группу; пиразинилметильную группу; тетразолилметильную группу; гидроксильную группу; алкоксигруппу, имеющую от 1 до 3 атомов углерода; или -NR39R40, где R39 и R40 определены выше;
(d) взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу;
(2) взятые вместе, R26 и R27 образуют с двумя атомами азота и одним атомом углерода 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу; и R25 и R26 независимо представляют атомы водорода, алкильные группы, имеющие от 1 до 3 атомов углерода, ацетил или -(СН2)m-OR36, где m и R36 определены выше;
(3) формула: =С(NR25R26)NR27R28 является группой, представленной следующей формулой:
=C(NR41R42)N=C(NH2)NR43R44, где
R41 и R42 определены в следующих (а') или (b'); и R43 и R44 определены в следующих (с') или (d'):
(а') каждый представляет, независимо, атом водорода; алкильную группу, имеющую от 1 до 4 атомов углерода; -(СН2)n-СОСН3, где n определено выше; -(СН2)n-CO2R32, где n и R32 определены выше; -(СН2)n-CONR33R34, где n, R33 и R34 определены выше; -(СН2)m-OR35, где m и R35 определены выше; -(СН2)m-NR37R38, где m, R37 и R38 определены выше; фенильную группу; пиридильную группу; пиримидинильную группу; пиридазинильную группу; пиразинильную группу; тетразолильную группу; бензильную группу; пиридилметильную группу; пиримидинилметильную группу; пиридазинилметильную группу; пиразинилметильную группу; тетразолилметильную группу; гидроксильную группу; алкоксигруппу, имеющую от 1 до 3 атомов углерода; или -NR39R40, где R39 и R40 определены выше;
(b') взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу;
(с') каждый представляет, независимо, атом водорода, алкильную группу, имеющую от 1 до 4 атомов углерода, -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)n-CONR33R34, где n, R33 и R34 определены выше, -(СН2)m-OR35, где m и R35 определены выше, -(СН2)m-NR37R38, где m, R37 и R38 определены выше, фенильную группу, пиридильную группу, пиримидинильную группу, пиридазинильную группу, пиразинильную группу, тетразолильную группу, бензильную группу, пиридилметильную группу, пиримидинилметильную группу, пиридазинилметильную группу, пиразинилметильную группу, тетразолилметильную группу, гидроксильную группу, алкоксигруппу, имеющую от 1 до 3 атомов углерода, или -NR39R40, где R39 и R40 определены выше;
(d') взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу;
или представлены формулой: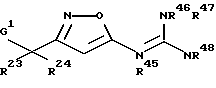
где G1, R23 и R24 указаны выше; формула -N(R45)C(NR46R47)=NR48 определена в следующих (1') или (2'):
(1') R45 представляет алкильную группу, имеющую от 1 до 3 атомов углерода, или ацетильную группу; R48 представляет атом водорода, алкильную группу, имеющую от 1 до 3 атомов углерода, или ацетильную группу; и R46 и R47 определены в следующих (а'') или (b'');
(а'') каждый представляет, независимо, атом водорода, алкильную группу, имеющую от 1 до 4 атомов углерода, -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)n-CONR33R34, где n, R33 и R34 определены выше, -(СН2)m-OR35, где m и R35 определены выше, -(СН2)m-NR37R38, где m, R37 и R38 определены выше, фенильную группу, пиридильную группу, пиримидинильную группу, пиридазинильную группу, пиразинильную группу, тетразолильную группу, бензильную группу, пиридилметильную группу, пиримидинилметильную группу, пиридазинилметильную группу, пиразинилметильную группу, тетразолилметильную группу, гидроксильную группу, алкоксигруппу, имеющую от 1 до 3 атомов углерода, или -NR39R40, где R39 и R40 определены выше;
(b'') взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу;
(2') взятые вместе, R45 и R46 образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, аминогруппу, гидроксильную группу, алкоксигруппу и оксогруппу; и R47 и R48 независимо представляют алкильные группы, имеющие от 1 до 3 атомов углерода, ацетильные группы или -(СН2)m-OR36, где m и R36 определены выше.
[9] Производное изоксазола или его фармацевтически приемлемая соль по [1], которые представлены формулой: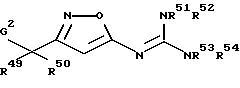
где G2 представляет фенил, 2-фторбифенил-4-ил, 2'-фторбифенил-4-ил, 3-бензоилфенил, R49 представляет метил; R50 представляет водород, метил, метокси или этокси; и формула: =C(NR51R52)NR53R54 определена в следующих (1''), (2'') или (3''):
(1'') R51 и R52 определены в следующих (а'''), (b''') или (с''') и R53 и R54 определены в следующих (d'''), (е''') или (f'''):
(а''') каждый независимо представляет атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода;
(b''') один из них представляет атом водорода и другой представляет -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, -(СН2)n-CONR33R34, где n и R32 определены выше, где n, R33 и R34 определены выше, -(СН2)m-OR35, где m и R35 определены выше, или -(СН2)m-NR37R38, где m, R37 и R38 определены выше;
(с''') взятые вместе, они образуют с атомом азота пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин или пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, и указанные пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин и пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, могут быть замещены одной или двумя метильными группами;
(d''') каждый, независимо, представляет атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода;
(е''') один из них представляет атом водорода и другой представляет -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)n-CONR33R34, где n, R33 и R34 определены выше, - (CH2)m-OR35, где m определено выше и R35 определено выше, или -(СН2)m-NR37R38, где m, R37 и R38 определены выше;
(f''') взятые вместе, они образуют с атомом азота пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин или пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, где указанные пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин и пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, могут быть замещены одной или двумя метильными группами;
(2'') формула: =С(NR51R52)NR53R54 является группой, представленной следующей формулой: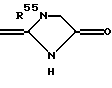
где R55 представляет алкильную группу, имеющую от 1 до 3 атомов углерода, ацетил или -(СН2)m-OR56, где m определено выше и R56 представляет атом водорода или алкильную группу, имеющую от 1 до 3 атомов углерода;
(3) формула: =C(NR51R52)NR53R54 является группой, представленной следующей формулой:
=С(NR57R58)N=C(NH2)NR59R60
где R57 и R58 определены в следующих (а''''), (b'''') или (с''''); и R59 и R60 определены в следующих (d''''), (е'''') или (f''''):
(а'''') каждый независимо представляет атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода;
(b'''') один из них представляет атом водорода и другой представляет -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)n-CONR33R34, где n, R33 и R34 определены выше, -(СН2)m-OR35, где m и R35 определены выше, или -(СН2)m-NR37R38, где m, R37 и R38 определены выше;
(с'''') взятые вместе, они образуют с атомом азота пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин или пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, где указанные пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин и пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, могут быть замещены одной или двумя метильными группами;
(d'''') каждый, независимо, представляет атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода;
(е'''') один из них представляет атом водорода и другой представляет -(СН2)n-СОСН3, где n определено выше, -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)n-CONR33R34, где n, R33 и R34 определены выше, -(СН2)m-ОR35, где m и R35 определены выше, или -(СН2)m-NR37R38, где m, R37 и R38 определены выше;
(f'''') взятые вместе, они образуют с атомом азота пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин или пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, где указанные пирролидин, азепан, морфолин, тиазолин, пиперидин-2-он, пиперидин-4-он, тиаморфолин, пиперазин, который может быть замещен в 4 положении алкильной группой, имеющей от 1 до 3 атомов углерода, пиперидин, который может быть замещен в 4 положении алкоксигруппой, имеющей от 1 до 3 атомов углерода, 4-гидроксипиперидин и пиперидин, замещенный в 4 положении аминогруппой, которая может быть замещена одной или двумя алкильными группами, имеющими от 1 до 3 атомов углерода, могут быть замещены одной или двумя метильными группами.
[10] Производное изоксазола или его фармацевтически приемлемая соль по [1], которое представлено формулой: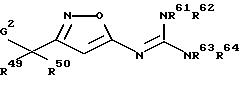
где G2, R49 и R50 указаны выше; формула =С(NR61R62)NR63R64 определена в следующих (1'''), (2''') или (3'''):
(1''') R63 и R64 оба представляют атомы водорода; и R61 и R62 определены в следующих (аv), (bv) или (сv):
(аv) каждый независимо представляет атом водорода или алкильную группу, имеющую от 1 до 4 атомов углерода;
(bv) один из них представляет атом водорода и другой представляет -(СН2)n-CO2R32, где n и R32 определены выше, -(СН2)m-OR65, где m равно 2 или 3 и R65 представляет атом водорода или алкильную группу, имеющую от 1 до 3 атомов углерода, 2-гидроксиэтил или 3-гидроксипропил; или -(СН2)m-NR66R67, где m определено выше и R66 и R67 независимо представляет атомы водорода или алкильные группы, имеющие от 1 до 3 атомов углерода, или, взятые вместе, они образуют с атомом азота пирролидин, пиперидин, морфолин или N-метилпиперазин, где указанные пирролидин, пиперидин, морфолин и N-метилпиперазин могут быть замещены одной или двумя метильными группами;
(сv) взятые вместе, они образуют с атомом азота пирролидин, пиперидин, морфолин и N-метилпиперазин, где указанные пирролидин, пиперидин, морфолин или N-метилпиперазин могут быть замещены одной или двумя метильными группами;
(2''') формула: = C(NR61R62)NR63R64 является группой, представленной следующей формулой: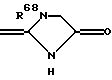
где R68 представляет алкильную группу, имеющую от 1 до 3 атомов углерода; 2-гидроксиэтил или 3-гидроксипропил.
(3''') взятые вместе, R61 и R62 образуют морфолин с атомом азота; и, взятые вместе, R63 и R64 образуют аминоморфолин-4-илметилен.
[11] Производное изоксазола или его фармацевтически приемлемая соль по [1], которое выбрано из группы, включающей следующие соединения:
({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил)амин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илметил)гуанидин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-(4-метилпиперазин-1-ил)метил)амин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино}-морфолин-4-илметил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил]амин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино}морфолин-4-илметил)амин;
[{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино}-(4-метилпиперазин-1-ил)метил]амин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин;
(3-{ 1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] этил} фенил)фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
(3-{ 1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] -1-метилэтил} фенил)фенилметанон;
[3-(1-{ 5-[амино-(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил}-1-метилэтил)фенил]фенилметан;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин.
[12] Фармацевтическая композиция, содержащая в качестве активного ингредиента производное изоксазола или его фармацевтически приемлемую соль по любому из [1]-[11] вместе с фармацевтически приемлемым носителем.
[13] Фармацевтическая композиция по [12] для лечения или профилактики аутоиммунных заболеваний.
[14] Фармацевтическая композиция по [12] для лечения или профилактики воспалительных заболеваний.
[15] Фармацевтическая композиция по [12], представляющая собой противоревматическое средство.
[16] Фармацевтическая композиция по [12], представляющая собой противовоспалительное средство.
[17] Способ лечения или профилактики аутоиммунных заболеваний или воспалительных заболеваний, заключающийся во введении производного изоксазола или его фармацевтически приемлемой соли по любому из [1]-[11] в эффективном количестве в организм человека.
[18] Применение производного изоксазола или его фармацевтически приемлемой соли по любому из [1]-[11] при получении лекарственного средства для лечения или профилактики аутоиммунных заболеваний или воспалительных заболеваний.
На чертеже показан график, показывающий результат испытания соединений, по данному изобретению, используя экспериментальных аллергических энцефаломиелитических мышей, которые являются животными моделями рассеянного склероза.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Арильная группа включает, например, арильные группы с от 6 до 14 атомов углерода. Ее конкретными примерами являются фенил, 1-нафтил, 2-нафтил, фенантрил, антрил и тому подобное. Предпочтительными примерами являются фенил, 1-нафтил и 2-нафтил.
Гетероциклическая группа включает, например, 5-7-членные моноциклические-трициклические насыщенные или ненасыщенные гетероциклические группы, содержащие от 1 до 6 атомов азота, атомов кислорода и/или атомы серы.
Конкретными примерами насыщенных гетероциклических групп являются моноциклические-трициклические 5-членные насыщенные гетероциклические группы, такие как тетрагидрофурил, пирролидинил, пиразолидинил, имидазолинил и т.п.; моноциклические-трициклические 6-членные насыщенные гетероциклические группы, такие как пиперидинил, морфолинил, тиаморфолинил, пиперазинил, гексагидропиримидинил и тому подобное; и моноциклические-трициклические 7-членные насыщенные гетероциклические группы, такие как азепанил и тому подобное.
Конкретными примерами ненасыщенных гетероциклических групп являются моноциклические-трициклические 5-членные ненасыщенные гетероциклические группы, такие как фурил, тиенил, индолил, изотиазолил, бензотиенил, изобензофуранил, пирролил, бензофурил, имидазолил, 4,5-дигидро-1Н-имидазолил, пиразолил, изоксазолил, изотиазолил, тиазолил, оксазолил, бензимидазолил, бензтиазолил, бензоксазолил, карбазолил и тому подобное; моноциклические-трициклические 6-членные ненасыщенные гетероциклические группы, такие как пиридил, пиразинил, пиримидинил, 1,4,5,6-тетрагидропиримидинил, 3,6-дигидро-2Н-[1,3,5]оксадиазинил, пиридазинил, тиазинил, хинолил, изохинолил, хиназолинил, хиноксалинил, хроменил, 2,3-дигидробензо[1,4]диоксинил и тому подобное; и моноциклические-трициклические 7-членные ненасыщенные гетероциклические группы, такие как 4,5,6,7-тетрагидро-1Н-[1,3]диазепинил и тому подобное.
В качестве заместителя каждой замещенной арильной группы и замещенной гетероциклической группы можно привести примеры любых заместителей следующих групп а) - g), и каждая замещенная арильная группа и замещенная гетероциклическая группа может необязательно иметь один или несколько таких заместителей.
а) Атомы галогена, нитрогруппы, цианогруппы, азидные группы, меркаптогруппы, замещенные или незамещенные аминогруппы, замещенные или незамещенные гидроксиламиногруппы, замещенные или незамещенные низшие алкоксиминогруппы, гидроксильные группы, ацильные группы, ацилоксигруппы, карбоксильные группы, замещенные или незамещенные карбамоильные группы, замещенные или незамещенные карбамоилоксигруппы, сульфогруппы и замещенные или незамещенные сульфамоильные группы.
b) -R10, -OR10, -CO2R10, -SО3R10, -SR10, -OCH2R10 и -SCH2R10, где R10 обозначает фенильную группу или моноциклическую гетероциклическую группу, где указанные фенильная группа или моноциклическая гетероциклическая группа могут быть замещены, по меньшей мере, одним членом, необязательно выбранным из группы, содержащей, например, атомы галогена, низшие алкильные группы, низшие галогеналкильные группы, цианогруппы, нитрогруппы, азидные группы, гидроксильные группы, низшие алкоксигруппы, низшие галогеналкоксигруппы, замещенные или незамещенные аминогруппы, замещенные или незамещенные карбамоильные группы, карбоксильные группы, низшие алкилкарбонильные группы, низшие алкоксикарбонильные группы, низшие алкилтиогруппы, низшие алкилсульфинильные группы, низшие алкилсульфонильные группы и тому подобное.
c) Алкильные группы, алкоксигруппы, алкоксикарбонильные группы, алкокси(тиокарбонил)группы, алкилтиогруппы, (алкилтио)-тиокарбонильные группы, (алкилтио)карбонильные группы, алкилкарбонильные группы, алкилтиоильные группы, алкилсульфинильные группы, алкилсульфонильные группы, алкилкарбонилоксигруппы, алкилтиоилоксигруппы и алкилсульфонилоксигруппы, каждая из этик групп может быть замещена, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена; нитро, циано, меркапто, оксо, тиоксогруппы; замещенные или незамещенные аминогруппы; гидроксильные группы; ацильные группы; ацилоксигруппы; карбоксильные группы; замещенные или незамещенные карбамоильные группы; замещенные или незамещенные карбамоилоксигруппы; сульфогруппы; замещенные или незамещенные сульфамоильные группы; -R10; -OR10; -SR10; -OCH2R10; -SCH2R10, где R10 определен выше;
низшие циклоалкильные группы, которые могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, низшие алкильные группы, низшие галогеналкильные группы, замещенные или незамещенные аминогруппы, гидроксильные группы; низшие алкоксигруппы, низшие галогеналкоксигруппы и тому подобное;
низшие алкоксигруппы; низшие алкоксикарбонильные группы; и низшие алкилтиогруппы, где указанные низшие алкоксигруппы; низшие алкоксикарбонильные группы и низшие алкилтиогруппы могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, низшие циклоалкильные группы, моноциклические гетероциклические группы, фенильную группу, цианогруппу, нитрогруппу, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, замещенные или незамещенные аминогруппы; замещенные или незамещенные карбамоильные группы; карбоксильную группу; низшие алкилкарбонильные группы; низшие алкоксикарбонильные группы, низшие алкилтиогруппы, низшие алкилсульфинильные группы, низшие алкилсульфонильные группы и тому подобное.
d) Алкенильные группы, которые могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, замещенные или незамещенные аминогруппы; гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, низшие алкоксикарбонильные группы; низшие алкилтиогруппы, ацильные группы, ацилоксигруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы; -R10; -OR10; -SR10; -OCH2R10 и -SCH2R10, где R10 определен выше, и тому подобное.
e) Алкинильные группы, которые могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, замещенные или незамещенные аминогруппы; гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, низшие алкоксикарбонильные группы; низшие алкилтиогруппы, ацильные группы, ацилоксигруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы; -R10; -OR10; -SR10; -OCH2R10 и -SCH2R10, где R10 определен выше, и тому подобное.
f) Алкенилоксигруппы, алкенилоксикарбонильные группы, алкенилкарбонильные группы, алкенилкарбонилоксигруппы, алкинилоксигруппы и алкинилоксикарбонильные группы, каждая из которых может быть замещена, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, оксогруппы, замещенные или незамещенные аминогруппы, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, ацильные группы, ацилоксигруппы, низшие алкилтиогруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы; низшие алкоксикарбонильные группы, фенильную группу и тому подобное.
g) Низшие циклоалкильные группы, низшие циклоалкилоксигруппы, низшие циклоалкилкарбонильные группы, низшие циклоалкилоксикарбонилоксигруппы, низшие циклоалкилоксикарбонильные группы, низшие циклоалкенильные группы, низшие циклоалкенилокси группы, низшие циклоалкенилкарбонильные группы, низшие циклоалкенилкарбонилоксигруппы и низшие циклоалкенилоксикарбонильные группы, которые могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, низшие алкильные группы, низшие галогеналкильные группы, замещенные или незамещенные аминогруппы, гидроксильные группы; низшие алкоксигруппы, низшие галогеналкоксигруппы, ацильные группы, ацилоксигруппы, низшие алкилтиогруппы, карбоксильные группы, замещенные или незамещенные карбамоильные группы, низшие алкоксикарбонильные группы и тому подобное.
Конкретными примерами заместителя в замещенной арильной группе и замещенной гетероциклической группе являются метил, 2-метил-1-пропил, гексил, 2-метил-2-пропил, 2-пропил, фенил, трифторметил, 2,2,2-трифторэтил, 1,1,2,2,2-пентафторэтил, 6,6,6-трифторгексил, гидроксиметил, гидроксиэтил, метоксиметил, гексилоксиметил, циклопропилметоксиметил, ацетоксиметил, N, N-диметилкарбамоилоксиметил, метансульфонилоксиметил, N,N-диметилсульфамоилоксиметил, 2-(1-пирролидинил)этоксиметил, 2-метоксиэтил, карбоксиметил, метоксикарбонилметил, карбамоилметил, амидинометил, метилтиометил, цианометил, аминометил, аминоэтил, N-ацетиламинометил, этенил, 2-пропенил, этинил, 2-пропинил, 2-метоксикарбонилэтенил, фтор, хлор, бром, нитро, циано, гидроксил, амино, N, N-диметиламино, меркапто, сульфо, карбоксил, амидино, метокси, циклопропилметокси, 2-(1-пирролидинил)этокси, метоксикарбонилметокси, 2-ацетоксиэтокси, 2-гидроксиэтокси, 2-метоксиэтокси, 4,4,5,5,5-пентафторпентокси, 2-метансульфинилэтокси, фенокси, бензилокси, 4-метоксибензилокси, метоксикарбонилокси, 1-пирролидинил, 3-гидрокси-1-пирролидинил, ацетиламино, N-ацетил-N-метиламино, N-метансульфониламино, N-метансульфонил-N-метиламино, метоксикарбонил, 2-метил-2-пропоксикарбонил, 2,2,2-трифторэтоксикарбонил, карбамоил, N,N-диметилкарбамоил, 2-тиазолидинил, 2-оксазолидинил, 5-тетразолил, метансульфинил, сульфамоил, N,N-диметилсульфамоил, ацетил, бензоил, пивалоил, трифторацетил, формил, этилендиоксиметил, имино, метоксиимино и тому подобное.
Из этих заместителей конкретными примерами предпочтительных заместителей являются метил, 2-метил-1-пропил, гексил, 2-метил-2-пропил, 2-пропил, фенил, трифторметил, 2,2,2-трифторэтил, гидроксиметил, гидроксиэтил, метоксиметил, циклопропилметоксиметил, ацетоксиметил, N,N-диметилкарбамоилоксиметил, метансульфонилоксиметил, N, N-диметилсульфамоилоксиметил, 2-(1-пирролидинил)этоксиметил, 2-метоксиэтил, карбоксиметил, метоксикарбонилметил, карбамоилметил, амидинометил, метилтиометил, цианометил, аминометил, аминоэтил, N-ацетиламинометил, фтор, хлор, бром, нитро, циано, гидроксил, амино, N,N-диметиламино, метокси, 2-(1-пирролидинил)этокси, метоксикарбонилметокси, 2-ацетоксиэтокси, 2-гидроксиэтокси, 2-метоксиэтокси, 2-метансульфинилэтокси, 1-пирролидинил, 3-гидрокси-1-пирролидинил, ацетиламино, N-ацетил-N-метиламино, N-метансульфониламино, N-метансульфонил-N-метиламино, метоксикарбонил, 2-метил-2-пропоксикарбонил, 2,2,2-трифторэтоксикарбонил, карбамоил, N,N-диметилкарбамоил, метансульфинил, ацетил, бензоил, пивалоил, трифторацетил и тому подобное.
Число заместителей в каждой арильной группе и гетероциклической группе предпочтительно составляет 1, 2 или 3. Как среди арильных групп, так и гетероциклических групп, незамещенные группы также предпочтительны.
Алкильные группы включают, например, линейные и разветвленные алкильные группы с 1-10 атомами углерода. Конкретными их примерами являются метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метил-1-пропил, 1,1-диметилэтил, пентил, 1,1-диметилпропил, 2,2-диметилпропил, 1-метилбутил, 3-метилбутил, гексил, 2-метилпентил, 3,3-диметилбутил, гептил, 1-этилпентил, 5-метилгексил, октил, 1,5-диметилгексил, 2-этилгексил, нонил, децил и тому подобное. Низшая алкильная группа включает алкильные группы с от 1 до 6 атомами углерода.
В качестве заместителя в замещенной алкильной группе можно привести примеры любых заместителей из следующих групп a)-d), и заместители алкильных групп необязательно могут иметь один или несколько указанных заместителей.
a) Атомы галогена, нитрогруппа, цианогруппа, меркаптогруппа, оксогруппа, тиоксогруппа, замещенные или незамещенные аминогруппы, замещенные или незамещенные гидроксиламиногруппы, замещенные или незамещенные низшие алкоксиаминогруппы, гидроксильная группа, ацильная группа, ацилоксигруппа, карбоксильная группа, замещенные или незамещенные карбамоильные группы, замещенные или незамещенные карбамоилоксигруппы, сульфогруппы и замещенные или незамещенные сульфамоильные группы.
b) Низшие циклоалкильные группы, низшие циклоалкилоксигруппы, низшие циклоалкилкарбонильные группы, низшие циклоалкилоксикарбонилоксигруппы, низшие циклоалкилоксикарбонильные группы, низшие циклоалкенильные группы, низшие циклоаленкилокси группы, низшие циклоалкенилкарбонильные группы, низшие циклоалкенилкарбонилоксигруппы и низшие
циклоалкенилоксикарбонильные группы, каждая из этих групп может быть замещена, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, низшие алкильные группы, низшие галогеналкильные группы, замещенные или незамещенные аминогруппы, гидроксильные группы; низшие алкоксигруппы, низшие галогеналкоксигруппы, ацильные группы, ацилоксигруппы, низшие алкилтиогруппы, карбоксильные группы, замещенные или незамещенные карбамоильные группы, низшие алкоксикарбонильные группы и тому подобное.
с) Алкоксигруппы, алкоксикарбонильные группы, алкокси(тиокарбонил)группы, алкилтиогруппы, (алкилтио)тиокарбонильные группы, (алкилтио)карбонильные группы, алкилкарбонильные группы, алкилтиоильные группы, алкилсульфинильные группы, алкилсульфонильные группы, алкилкарбонилоксигруппы, алкилтиоилоксигруппы и алкилсульфонилоксигруппы, каждая из этих групп может быть замещена, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена; нитрогруппу; цианогруппу; меркаптогруппу; оксогруппу; тиоксогруппу; замещенные или незамещенные аминогруппы; гидроксильную группу; ацильные группы; ацилоксигруппы; карбоксильную группу; замещенные или незамещенные карбамоильные группы; замещенные или незамещенные карбамоилокси группы; сульфогруппу; замещенные или незамещенные сульфамоильные группы; -R10; -OR10; -SR10; -OCH2R10; -SCH2R10, где R10 определен выше;
низшие циклоалкильные группы, которые могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, низшие алкильные группы, низшие галогеналкильные группы, замещенные или незамещенные аминогруппы, гидроксильную группу; низшие алкоксигруппы, низшие галогеналкоксигруппы и тому подобное;
низшие алкоксигруппы; низшие алкоксикарбонильные группы и низшие алкилтиогруппы, где указанные низшие алкоксигруппы, низшая алкоксикарбонильная группа и низшие алкилтиогруппы могут быть замещены, по крайней мере, одним членом, необязательно выбранным из группы, включающей, например, атомы галогена, низшие циклоалкильные группы, моноциклические гетероциклические группы, фенильную группу, цианогруппу, нитрогруппу, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, замещенные или незамещенные аминогруппы, замещенные или незамещенные карбамоильные группы, карбоксильную группу, низшие алкилкарбонильные группы, низшие алкоксикарбонильные группы, низшие алкилтиогруппы, низшие алкилсульфинильные группы и низшие алкилсульфонильные группы и тому подобное.
d) -R10, -OR10, -SR10, -OCH2R10 и -SCH2R10, где R10 указаны выше.
Конкретными примерами замещенной алкильной группы являются трифторметил, 2-нитроэтил, 2-цианпропил, 4-меркаптобутил, 3-оксобутил, 2-пиперидиноэтил, 2-гидроксиэтил, 3-метоксипропил, этоксикарбонилметил, циклопропилметил, циклогексилметил, 6-циклогексилгексил, 3-циклогексилбутил, 2-фенилбутил, бензил, 2-нафтилметил, фенетил, 2-пиридилметил, 3-пиридилметил, 4-пиридилметил, 2-хинолилметил, 3-хинолилметил, 3-тиенилпропил, гидроксиметил, гидроксиэтил, аминометил, аминоэтил, карбоксиметил, эитоксикарбонилметил, карбамоилметил и тому подобное.
Низшая галогеналкильная группа представлена низшей алкильной группой, имеющей от 1 до 5 атомов галогена.
Алкоксигруппа представлена оксигруппой, имеющей присоединенную к ней алкильную группу. Конкретными их примерами являются метокси, этокси, пропокси, 2-пропокси, бутокси, 1,1-диметилэтокси, пентокси, гексокси и тому подобное. В качестве заместителя замещенной алкоксигруппы можно привести примеры таких заместителей, которые приведены выше в качестве примеров заместителя замещенной арильной группы. Конкретными примерами замещенной алкоксигруппы являются циклопропилметокси, трифторметокси, 2-пирролидинэтокси, бензилокси, 2-пиридилметокси и тому подобное.
Галогеналкоксигруппа представлена алкоксигруппой, замещенной от 1 до 5 атомов галогена.
Алкоксикарбонильная группа представлена карбонильной группой, имеющей присоединенную к ней алкоксигруппу. Конкретными их примерами являются метоксикарбонил, этоксикарбонил, пропоксикарбонил, 2-пропоксикарбонил и тому подобное. В качестве заместителя замещенной алкоксикарбонильной группы можно привести примеры таких заместителей, которые приведены выше в качестве примеров заместителя замещенной алкильной группы.
Алкенильная группа включает, например, линейные и разветвленные алкенильные группы с 2-10 атомами углерода, имеющие от 1 до 3 двойных связей. Конкретными их примерами являются этенил, 1-пропенил, 2-пропенил, 1-метилэтенил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-2-пропенил, 1-пентенил, 2-пентенил, 4-пентенил, 3-метил-2-бутенил, 1-гексенил, 2-гексенил, 1-октенил, 2-октенил, 1,3-октадиенил, 2-ноненил, 1,3-нонадиенил, 2-деценил и тому подобное. Предпочтительными примерами алкенильной группы являются, например, этенил, 1-пропенил и 1-бутенил. Низшая алкенильная группа включает алкенильные группы от 2 до 6 атомов углерода.
Заместитель замещенной алкенильной группы включает, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, замещенные или незамещенные аминогруппы, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, низшие алкоксикарбонильные группы, низшие алкилтиогруппы, ацильные группы, ацилоксигруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы, -R10, -OR10, -SR10, -OCH2R10, -SCH2R10, где R10 определен выше, и тому подобное.
Алкенилоксигруппа представлена оксигруппой, имеющей присоединенную к ней алкенильную группу.
Алкинильная группа включает линейные и разветвленные алкинильные группы с 2-10 атомами углерода, имеющие от 1 до 3 тройных связей. Конкретными их примерами являются этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 4-пентинил, 1-октинил, 6-метил-1-гептинил, 2-децинил и тому подобное. Предпочтительными примерами алкинильной группы являются, например, 1-пропинил, 1-бутинил и тому подобное. Низшая алкинильная группа включает алкинильные группы от 2 до 6 атомов углерода.
Заместитель замещенной алкинильной группы включает, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, замещенные или незамещенные аминогруппы, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, ацильные группы, ацилоксигруппы, низшие алкилтиогруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы, низшие алкоксикарбонильные группы, -R10, -OR10, -SR10, -OCH2R10, -SCH2R10, где R10 определен выше, и т.п.
Алкинилоксигруппа представлена оксигруппой, имеющей присоединенную к ней алкинильную группу.
Циклоалкильная группа включает, например, циклоалкильные группы с 3-10 атомами углерода. Конкретными их примерами являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и тому подобное. Низшая циклоалкильная группа включает циклоалкильные группы от 3 до 6 атомов углерода. Циклоалкилоксигруппа представлена оксигруппой, имеющей присоединенную к ней циклоалкильную группу.
Циклоалкенильная группа включает, например, циклоалкенильные группы с 3-10 атомами углерода. Конкретными их примерами являются циклогексенил и тому подобное. Низшая циклоалкенильная группа включает циклоалкенильные группы от 3 до 6 атомов углерода. Циклоалкенилоксигруппа представлена оксигруппой, имеющей присоединенную к ней циклоалкенильную группу.
Заместитель каждой замещенной циклоалкильной группы и замещенной циклоалкенильной группы включает, например, атомы галогена, нитрогруппу, цианогруппу, меркаптогруппу, оксогруппу, тиоксогруппу, низшие алкильные группы, низшие галогеналкильные группы, замещенные или незамещенные аминогруппы, гидроксильную группу, низшие алкоксигруппы, низшие галогеналкоксигруппы, ацильные группы, ацилоксигруппы, низшие алкилтиогруппы, карбоксильную группу, замещенные или незамещенные карбамоильные группы и тому подобное.
Ацильная группа включает, например, ацильные группы формулы: -Z-R11, где Z обозначает -СО-, -CS-, -SO- или -SO2- и R11 представляет замещенную или незамещенную алкильную группу, замещенную или незамещенную арильную группу или замещенную или незамещенную гетероциклическую группу. Конкретными их примерами являются формил, ацетил, пропаноил, 2-пропаноил, пивалоил, валерил, пивалоил, трифторацетил, бензоил, нафтоил, никотиноил, метансульфонил, трифторметансульфонил, п-толуолсульфонил и тому подобное. Предпочтительными примерами ацильной группы являются ацетильная группа и тому подобное. Ацилоксигруппа представлена оксигруппой, имеющей присоединенную к ней ацильную группу.
Заместитель замещенной карбамоильной группы включает, например, алкильные группы, которые могут быть замещены арильной группой или гетероциклической группой, арильные группы, гетероциклические группы и тому подобное. Замещенная карбамоильная группа может иметь множество одинаковых или различных независимо введенных в нее заместителей. Конкретными примерами замещенной карбамоильной группы являются этилкарбамоил, диметилкарбамоил, фенилкарбамоил, 2-пиридилкарбамоил, бензилкарбамоил, (3-пиридилметил)карбамоил и тому подобное.
Заместитель замещенной сульфамоильной группы включает, например, алкильные группы, арильные группы, гетероциклические группы и тому подобное. Замещенная сульфамоильная группа может иметь множество одинаковых или различных независимо введенных в нее заместителей. Конкретными примерами замещенной сульфамоильной группы являются этилсульфамоил, диметилсульфамоил, фенилсульфамоил, 2-пиридилсульфамоил и тому подобное.
Заместитель замещенной аминогруппы включает, например, ацильные группы, алкильные группы и тому подобное. Замещенная аминогруппа может иметь множество одинаковых или различных независимо введенных в нее заместителей. Конкретными примерами замещенной аминогруппы являются ацетамид, пропионамид, бутиламид, 2-бутиламид, метиламино, 2-метил-1-пропионамино, диэтиламино и тому подобное.
Заместитель замещенной гидроксиламиногруппы может быть либо на атоме азота или на атоме кислорода. В качестве заместителя можно привести примеры таких заместителей, которые приведены выше в качестве примеров заместителя замещенной аминогруппы.
Атом галогена включает, например, атом фтора, атом хлора, атом брома, атом иода и тому подобное.
Алкиленовая группа включает, например, линейные и разветвленные алкиленовые группы с 1-10 атомами углерода. Конкретными их примерами являются метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, гептаметилен, октаметилен, нонаметилен, декаметилен, метилметилен, этилметилен, диметилметилен, 1,1-диметилэтилен, 1,2-диметилэтилен, 1-метилтриметилен, 2-метилтриметилен, 1,1-диметилтриметилен, 1,2-диметилтриметилен, 1,3-диметилтриметилен, 2,2-диметилтриметилен, 1-этилтриметилен, 2-этилтриметилен, 1,1-диэтилтриметилен, 1,2-диэтилтриметилен, 1,3-диэтилтриметилен, 2,2-диэтилтриметилен и тому подобное.
Низшая алкиленовая группа включает, например, линейные и разветвленные алкиленовые группы с от 1 до 6 атомами углерода.
В качестве защитной группы для NH группы могут быть использованы различные общеизвестные защитные группы, хотя предпочтительными их примерами являются защитные группы карбаматного типа, такие как метоксикарбонил, этоксикарбонил, трет-бутоксикарбонил, бензилоксикарбонил и тому подобное, защитные группы амидного типа, такие как ацетил, бензоил и тому подобное, бензил, нитро, п-толуолсульфонил, метансульфонил и тому подобное.
В замещенном или незамещенном гетероциклическом кольце, в котором любые два из R1, R2, R3 и R4, взятые вместе, образуют с атомом(ами) азота гетероциклическое кольцо, гетероциклическое кольцо включает, например, 5-7-членные моноциклические насыщенные или ненасыщенные гетероциклические кольца, содержащие от 1 до 6 атомов азота, атомов кислорода и/или атомов серы, и содержит, по меньшей мере, один атом азота. Конкретными примерами являются пирролидин, имидазолидин, 4,5-дигидро-1Н-имидазол, пиперидин, пиперидин-4-он, пиперазин, морфолин, тиаморфолин, 1,4,5,6-тетрагидропиримидин, гексагидропиримидин, 3,6-дигидро-2Н-[1,3,5]оксадиазин и тому подобное. В качестве заместителя замещенного гетероциклического кольца можно привести примеры таких заместителей, которые приведены выше в качестве примеров заместителя замещенной гетероциклической группы.
Замещенное или незамещенное углеводородное кольцо, которое образуют R8 и R9, взятые вместе с атомом углерода, включает, например, замещенные или незамещенные циклоалкановые кольца, содержащие от 3 до 8 атомов углерода, или замещенные или незамещенные циклоалкеновые кольца, содержащие от 3 до 8 атомов углерода. Конкретными примерами циклоалкановых колец или циклоалкеновых колец являются циклопропан, циклобутан, циклопентан, циклогексан, циклогептан, циклопропен, циклобутен, циклопентен, циклогексен, циклогептен и тому подобное. В качестве заместителя замещенного углеводородного кольца можно привести примеры таких заместителей, которые приведены выше в качестве примеров заместителя замещенной циклоалкильной группы.
Когда производное изоксазола формулы 1 имеет полярную функциональную группу, включенную в изоксазольное кольцо, эти соединения обладают улучшенными фармакокинетическими показателями, обладают небольшим побочным эффектом и могут вводиться в течение длительного периода времени.
Настоящее изобретение охватывает все стереоизомеры, оптические изомеры, таутомеры и тому подобное производного изоксазола формулы 1. Настоящее изобретение охватывает также сольваты (например, гидраты и тому подобное) и все кристаллические формы производного изоксазола формулы 1 или его фармацевтически приемлемой соли.
Фармацевтически приемлемая соль производного изоксазола формулы 1 включает соли прибавления кислот и соли прибавления оснований. Соли прибавления кислот включают, например, соли с неорганическими кислотами, такие как гидрохлорид, гидробромид, сульфат, гидройодат, нитрат, фосфат и тому подобное; и соли с органическими кислотами, такие как цитрат, оксалат, ацетат, формиат, пропионат, бензоат, трифторацетат, фумарат, малеат, тартрат, аспартат, глютамат, метансульфонат, бензолсульфонат, камфосульфонат и тому подобное. Соли прибавления оснований включают соли с неорганическими основаниями, такие как натриевая соль, калиевая соль, кальциевая соль, магниевая соль, аммониевая соль и тому подобное; и соли с органическими основаниями, такие как триэтиламмониевая соль, триэтаноламмониевая соль, пиридиниевая соль, диизопропиламмониевая соль и тому подобное.
Производное изоксазола формулы 1 может быть получено, например, одним из пяти способов, описанных далее. Хотя для следующих реакционных формул указывается, что А и В имеют одно из двух сочетаний значений, указанных выше, тем же способом может быть получено производное, в котором А и В имеют другое сочетание значений.
Способ 1 (схема 1, приведенная в конце описания).
Производное изоксазола (1а) по настоящему изобретению может быть получено путем взаимодействия соединения формулы 2а с производным гуанидина формулы 3 в инертном растворителе при температуре реакции 0-25oС в условиях реакции Мицуноби с использованием триалкилфосфина и сложного эфира азодикарбоновой кислоты (Chem. Lett., 1994, 539; Tetrahedron Lett., 35, 977 (1994)). Триалкилфосфин включает, например, трифенилфосфин, трибутилфосфин и тому подобное. Эфир азодикарбоновой кислоты включает, например, диэтил азодикарбоксилат, диизопропил азодикарбоксилат, 1,1'-(азодикарбонил)дипиперидин, N, N, N', N'-тетраметилазодикарбоксамид и N,N,N',N'-тетраизопропилазодикарбоксамид и тому подобное. Предпочтительными примерами растворителя являются тетрагидрофуран, бензол, толуол и тому подобное.
Когда R1, R2, R3 или R4 обозначает защитную группу для NH группы в соединении формулы 1а, можно, если желательно, удалить защитную группу. Это удаление можно осуществить общеизвестным способом, например, способом, описанном в "Protective Groups in Organic Synthesis", 2nd Edition, T.M. Greene and P.G.M. Wuts, John Willey and Sons, inc.. New York (1991), p. 315-362). В качестве защитной группы для NH группы можно использовать различные общеизвестные защитные группы. Предпочтительными их примерами являются защитные группы карбаматного типа, такие как метоксикарбонил, этоксикарбонил, трет-бутоксикарбонил, бензилоксикарбонил и тому подобное, защитные группы амидного типа, такие как N-ацетил, N-бензоил и тому подобное, бензил, нитро, п-толуолсульфонил, метансульфонил и тому подобное.
1) Способ получения соединения формулы 2а, где Е обозначает алкилен (соединение формулы 2а1) (схема 2, приведенная в конце описания).
Соединение формулы 5а может быть получено путем взаимодействия сложноэфирного производного β-дикетона формулы 4 с гидроксиламином или гидрохлоридом гидроксиламина в инертном растворителе в соответствии с известным способом синтеза изоксазолов (например, A.R. Katritzky et al., "Comprehensive Heterocyclic Chemistry", Vol. 6, Pergamon Press Ltd., New York (1984), p. 61). В этом случае соединение формулы 5b также получается в некоторых случаях, однако, также возможно получить только одно из соединения формулы 5а и соединения формулы 5b путем регулирования условий реакции (например, F. Lepage et al., Eur. J. Med. Chem., 27, 581(1992); и вышеприведенная ссылка, A. R. Katritzky et al., "Comprehensive Heterocyclic Chemistry", Vol. 6, Pergamon Press Ltd., New York (1984), p. 62).
Соединение формулы 2а1 может быть получено путем обработки соединения формулы 5b с восстанавливающим агентом в инертном растворителе. Восстанавливающий агент включает, например, литийалюминийгидрид и тому подобное. Температура реакции предпочтительно около 0oС.
2) Способ получения соединения формулы 2а, где Е обозначает одинарную связь (соединение формулы 2а2) (схема 3, приведенная в конце описания).
Амин формулы 7а может быть получен путем взаимодействия ацилнитрила формулы 6 с гидрохлоридом гидроксиламина в инертном растворителе в соответствии с известным способом (например, не подвергнутая экспертизе японская патентная публикация 63-152368).
Далее, соединение формулы 2а2 может быть получено путем гидролиза амина формулы 7а с кислотой в соответствии с известным способом (например, не подвергнутая экспертизе японская патентная публикация 62-84064).
Соединение формулы 2а2 может быть также получено путем взаимодействия производного кислоты Мельдрума формулы 8 с гидрохлоридом гидроксиламина в соответствии с известным способом (например, не подвергнутая экспертизе японская патентная публикация 52-106466).
3) Способ получения соединения формулы 2b, где Е обозначает одинарную связь (соединение формулы 2b2) (схема 4, приведенная в конце описания).
Амин формулы 7b может быть получен обработкой ацилнитрила формулы 6 газообразным гидрохлоридом в метаноле и взаимодействием обработанного ацилнитрила гидрохлоридом гидроксиламина в соответствии с известным способом (например, не подвергнутая экспертизе японская патентная публикация 54-3062).
Используя амин формулы 7b, соединение формулы 2b2 может быть получено тем же способом, что и для получения соединения формулы 2а2 из амина формулы 7а.
Соединение формулы 2b2 также может быть получено путем взаимодействия сложного β-кетоэфира формулы 9 с гидрохлоридом гидроксиламина в соответствии с известным способом (например, N. Jacobsen et al., Can. J. Chem., 62, 1940 (1984)).
Способ 2 (схема 5, приведенная в конце описания).
Соединение формулы 1а1 может быть получено путем взаимодействия производного псевдотиомочевины формулы 10а с амином формулы 11 при температуре 20-140oС необязательно в присутствии добавки и необязательно в инертном растворителе. Добавки включают, например, ацетат аммония, ацетат натрия, уксусную кислоту, щавелевую кислоту, гидроксид натрия, карбонат натрия, гидрокарбонат натрия, 1,8-диазабицикло[5,4,0]ундецен-7-ен, триэтиламин и их смесь и тому подобное. Предпочтительными примерами растворителя являются вода, метанол, этанол, изопропанол, ацетонитрил, N,N-диметилформамид, тетрагидрофуран, 1,4-диоксан, пиридин, толуол, хлороформ, метиленхлорид и их смесь и тому подобное.
Соединение формулы 1а1 может быть получено путем взаимодействия соединения формулы 10a с амином формулы 11 в присутствии нитрата серебра и основания в инертном растворителе при температуре реакции -10-50oС в соответствии со способом Web et al., используя нитрат серебра в качестве добавки (J. Оrg. Chem. , 56, 3009(1991)). Основание включает, например, триэтиламин, и тому подобное. Предпочтительными примерами растворителя являются ацетонитрил и тому подобное.
Когда R13, R14, R15 или R16 обозначает защитную группу для NH группы в соединении формулы 1а1, защита может быть удалена тем же образом, что указано выше, если желательно.
Исходные соединения в способе получения, описанном выше, являются хорошо известными специалистам соединениями или соединениями, которые можно получить хорошо известными синтетическими методами. Например, соединение формулы 10а может быть получено способом, показанным на схеме 6, приведенной в конце описания.
Соединение формулы 10а может быть получено взаимодействием метилгалогенида с производным тиомочевины формулы 12а, которое хорошо известно или может быть получено хорошо известными синтетическими способами (например, не подвергнутая экспертизе японская патентная публикация 63-152368) в инертном растворителе при температуре реакции 40-80oС. Метилгалогенид включает, например, метилиодид и тому подобное. Основание включает, например, карбонат калия, карбонат натрия, водный раствор гидроксида калия, водный раствор гидроксида натрия и тому подобное. Растворитель включает, например, метанол, этанол, тетрагидрофуран, N,N-диметилформамид и тому подобное.
Способ 3 (схема 7, приведенная в конце описания).
Соединение формулы 1а2 может быть получено путем взаимодействия соединения формулы 13а с производным псевдотиомочевины формулы 14 в присутствии основания в инертном растворителе при температуре реакции 20-100oС. Основания включают, например, 1,8-диазабицикло[5,4,0]ундецен-7-ен, триэтиламин и их смесь и тому подобное. Предпочтительными примерами растворителя являются пиридин, ацетонитрил, N,N-диметилформамид и тому подобное.
Соединение формулы 1а2 может быть получено также путем проведения взаимодействия в присутствии нитрата серебра и основания в инертном растворителе при температуре реакции -10-50oС в соответствии со способом Web et al., используя нитрат серебра (J. Org. Chem., 56, 3009(1991)). Основание включает, например, триэтиламин и тому подобное. Предпочтительными примерами растворителя являются ацетонитрил и тому подобное.
Когда R13, R14, R15 или R16 обозначает защитную группу для NH группы в соединении формулы 1а2, защита может быть удалена тем же образом, что указано выше, если желательно.
Соединение формулы 13а может быть получено, например, подвергая соединение формулы 2а галогенированию, преобразованию в азид и тому подобное (например, способ Y. Pei et al. (Tetrahedron Lett., 34, 7509(1993)). Если необходимо, заместитель может быть введен в аминогруппу (например, R.C. Larock, "Comrehensive Organic Transformations", VCH Publishers, Inc., New York (1989), p. 397).
Способ 4 (схема 8, приведенная в конце описания).
Соединение формулы 1а3 может быть получено путем взаимодействия соединения формулы 13а с производным метиленсульфонамида формулы 15 (например, Chem. Ber., 99, 2900(1966)) в инертном растворителе при температуре -20-80oС и затем с амином формулы 11. Предпочтительными примерами растворителя являются ацетонитрил, диэтиловый эфир, тетрагидрофуран, 1,4-диоксан, бензол, толуол, метиленхлорид, тетрахлорид углерода и тому подобное.
Когда Е обозначает одинарную связь, соединение формулы 15 является предпочтительно соединением, в котором оба L1 и L2 являются атомами хлора.
Когда R13, R15 или R16 обозначает защитную группу для NH группы в соединении формулы 1а3, защита может быть удалена тем же образом, что указано выше, если желательно. Также можно удалить группу, представленную -SO2R19 тем же образом, что указано выше, если желательно.
Способ 5 (схема 9, приведенная в конце описания).
Соединение формулы 1а4 может быть получено путем взаимодействия соединения формулы 13а с производным цианамида формулы 16 (например, коммерчески доступным цианоморфином) в инертном растворителе в присутствии основания при температуре 20-130oС. Примерами основания являются гидрид натрия, карбонат калия, амид натрия, амид лития и тому подобное. Предпочтительными примерами растворителя являются N,N-диметилформамид, тетрагидрофуран, толуол, ацетонитрил, трет-бутанол и тому подобное.
Когда R13, R15 или R16 обозначает защитную группу для NH группы в соединении формулы 1а4, защита может быть удалена тем же образом, что указано выше, если желательно.
Соединение, представленное формулой 20а, которое является исходным соединением по вышеуказанному методу могут быть также получены, как показано на схеме 10, приведенной в конце описания.
Соединение формулы 19 может быть получено активированием карбоксильной группы соединения формулы 17, взаимодействием соединения формулы 18, которое, если необходимо, обрабатывают основанием, в инертном растворителе при температуре реакции -78-30oС и с последующим удалением группы, представленной R20. Предпочтительные примеры инертного растворителя включают тетрагидрофуран, метиленхлорид, толуол и тому подобное.
Способ активирования карбоксильной группы может быть осуществлен путем осуществления взаимодействия в инертном растворителе, если необходимо, в присутствии добавки. В качестве активирующего агента, добавки и реакционных условий могут использоваться такие, которые обычно используются, и они указаны, например, в "Reactivity and Structure Concepts in Organic Chemistry, Vol. 21; The Practice of Peptide Synthesis" (M. Bodanszky and A. Bodanszky, Springer-Verlag, Berlin (1984), pp. 87-150). Предпочтительными активирующими агентами являются, например, 1,1' -карбонилдиимидазол, изобутилхлорформиат, н-бутилхлорформиат и тому подобное. Предпочтительными добавками являются, например, триэтиламин, 4-(диметиламино)пиридин, N-метилморфолин и тому подобное. Предпочтительными растворителями являются, например, N,N-диметилформамид, тетрагидрофуран, метиленхлорид, толуол и тому подобное.
Предпочтительными примерами соединения формулы 18 являются цианоацетат, трет-бутилцианоацетат, метилсульфонилацетонитрил, фенилсульфонилацетонитрил и тому подобное. Предпочтительными примерами основания, которым, если необходимо, обрабатывают соединение формулы 18, является 4-(диметиламино)пиридин, диизопропиламид лития, этоксид магния и тому подобное, и более предпочтительными примерами являются гидрид натрия, амид лития и тому подобное.
В качестве способа удаления группы, представленной R20, может быть использован обычный способ. Когда R20 обозначает -CO2R21, способ можно осуществлять, подвергая соединение обработке кислотой при температуре реакции 0-100oС в инертном растворителе. Предпочтительными примерами кислоты являются гидрохлорная кислота, серная кислота, трифторуксусная кислота и тому подобное. Предпочтительными примерами инертного растворителя являются тетрагидрофуран, метиленхлорид, толуол и тому подобное. Когда R20 обозначает -SO2R21, способ можно осуществлять в соответствии с известным способом (например, К.С. Santhosh et al., J. Chem. Soc., Chem. Commun., 1992, 224; R. Giovannini et al., Synlett, 1995, 973).
Амин формулы 20а может быть получен путем взаимодействия соединения формулы 19 с гидроксиламином в соответствии с известным способом (например, не подвергнутая экспертизе японская патентная публикация 63-152368).
Соединение формулы 20а может быть получено непосредственно из соединения формулы 17 без выделения соединения формулы 19. То есть, позволяя соединению формулы 19, как оно получено, реагировать с гидроксиламином в растворимом в воде растворителе, добавляя туда, если необходимо, воду или буферный раствор при температуре реакции 20-100oС, амин формулы 20а может быть получен непосредственно из соединения формулы 17. Предпочтительными примерами растворимого в воде растворителя является этанол, изопропанол, трет-бутанол, N, N-диметилформамид и т.п. Предпочтительными примерами буферного растворителя является раствор фосфатного буфера, раствор ацетатного буфера и тому подобное.
Согласно известному способу, когда есть симметричный атом углерода в положении J, можно получить амин формулы 20а с сохранением его оптической чистоты.
В качестве способа получения производного изоксазола формулы 1, в котором любые два из R1, R2, R3 и R4, взятые вместе, образуют с атомом(ами) азота гетероциклическое кольцо, имеется, например, способ с использованием исходного продукта, имеющего указанную кольцевую структуру, в соответствии с любым из вышеуказанных способов 1-5, и способ осуществления замыкания кольца заместителя на средней или конечной стадии любого из вышеуказанных способов получения [например, реакция конденсации карбоксильной группы с NH группой (например, J. Gen. Chem. U. S. S.R., 18, 2023(1948), и реакция замыкания кольца с использованием следующих реагентов для реакции]. Реагенты реакции, используемые при реакции замыкания кольца, включают 1,3-дибромпропан (J. Chem. Soc. Chem. Commun., 1992, 507), 1,4-диаминобутан (J. Am. Chem. Soc., 70, 430(1948)), бис-хлорметиламин (Европейский патент 428941), параформальдегид (), бутиламин (J. Оrg. Chem., 25, 147(1960)), глиоксаль (Tetrahedron Lett., 32, 5325(1991)), эфиры акриловой кислоты (Heterocycles, 20, 1769(1983)), бензилиденацетон (J. Heterocycl. Chem., 21, 65(1984)), эпиброгидрин (Can. J. Chem., 53, 894(1975)) и тому подобное.
В качестве способа получения производного изоксазола формулы 1, где J представляет -С(=CR8R9)-, где R8 и R9 указаны выше, имеется, например, способ, который включает обработку производного изоксазола формулы 1, где J представляет -C(R8aR9a)-, где R8a представляет низшую алкильную группу, кислотой, такой как трифторуксусная кислота, в инертном растворителе, таком как метиленхлорид.
В качестве способа получения производного изоксазола формулы 1, где каждый из R8 и R9 представляет замещенную или незамещенную низшую алкильную группу, или R8 и R9 присоединены друг к другу, и взятые вместе с атомом углерода, образуют замещенный или незамещенный 1,3-диоксан или замещенный или незамещенный 1,3-диоксолан, имеется, например, способ, который включает взаимодействие сложного эфира 2-кетоалкановой кислоты со спиртом, триалкилортоформиатом или его производным, этиленгликолем или его производным, или 1,3-пропандиолом или его производным в присутствии кислоты (например, "Protective Groups in Organic Synthesis", 2nd Edition, T.M. Greene and P.G. M. Wuts, John Willey and Sons, inc., New York (1991), p. 185-195); преобразование продукта реакции в соединение формулы 6 известным способом (например, не подвергнутая экспертизе японская патентная публикация 63-152368); и дальнейшее преобразование полученного продукта реакции в целевое соединение по способу 1 или 2, как указано выше.
Производное изоксазола формулы 1, где D представляет алкоксикарбонильную группу, могут быть подвергнуты гидролизу и последующему декарбоксилированию с получением производного изоксазола формулы 1, где D представляет атом водорода.
Производное изоксазола формулы 1, имеющее, по меньшей мере, один центр асимметрии в молекуле, может быть получено путем использования соответствующего исходного соединения, имеющего центр асимметрии, или путем введения центра асимметрии в него на стадиях получения целевого соединения. Например, при получении оптического изомера производного изоксазола изомер может быть получен при использовании оптически активного исходного продукта или осуществляя оптическое разделение на стадиях получения целевого соединения.
При использовании в качестве лекарственного средства производное изоксазола или его фармацевтически приемлемая соль по настоящему изобретению могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутримышечно, местно, ректально, чрезкожно или через нос). Фармацевтические формы для перорального введения включают, например, таблетки, капсулы, пилюли, гранулы, порошки, растворы, сиропы, суспензии и тому подобное. Фармацевтические формы для парентерального введения включают, например, водные или масляные препараты для инъекций, мазей, кремов, лосьонов, аэрозолей, суппозиториев, пластырей и тому подобное. Эти препараты получают обычными методами и могут содержать известные приемлемые носители, эксципиеты, связующие, стабилизаторы и тому подобное. Когда указанное производное изоксазола или его соль используют в виде инъекции, может быть добавлен буфер, солюбилизатор, тонизирующий агент и тому подобное, что является приемлемым.
Хотя доза и частота введений производного изоксазола или его фармацевтически приемлемой соли по настоящему изобретению изменяются в зависимости от симптомов, возраста, массы тела и пути введения, производное изоксазола или его соль могут вводиться взрослому обычно в дозе приблизительно 1-2000 мг, предпочтительно, 10-500 мг, относительно соединения по настоящему изобретению в качестве активного ингредиента в день в виде одной порции или нескольких порций.
Конкретные примеры соединений, входящих в настоящее изобретение, описаны далее. Эти соединения, однако, даны для примеров, и настоящее изобретение ими не ограничивается.
N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N,N-диметилгуанидин;
N'-(2-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}этил)-N,N-диметилгуанидин;
N'-(3-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-пропил)-N,N-диметилгуанидин;
N'-(2-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}этил)-N,N-диметилгуанидин;
N'-(3-{ 5-[l-(2-фтopбифeнил-4-ил)этил] изoкcaзoл-3-ил}-пропил)-N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)этил] -4-метилизоксазол-5-ил}-N,N-диметилгуанидин;
N'-{3-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)этил] -4-метилизоксазол-3-ил}-N,N-диметилгуанидин;
N'-{5-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-3-илметил}-N,N-диметилгуанидин;
5-(N', N'-диметилгуанидино)-3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-4-карбоновая кислота;
5-(N', N'-диметилгуанидинометил)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
3-(N', N'-диметилгуанидино)-5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-4-карбоновая кислота;
3-(N',N'-диметилгуанидинометил)-5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-4-карбоновая кислота;
{ 5-(N', N'-диметилгуанидино)-3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-4-ил}уксусная кислота;
{ 5-(N', N'-диметилгуанидинометил)-3-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}уксусная кислота;
{ 3-(N', N'-диметилгуанидино)-5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-4-ил}уксусная кислота;
{ 3-(N', N'-диметилгуанидинометил)-5-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}уксусная кислота;
N'-{ 3-[1-(2-фторбифенил-4-ил)этил] -4-гидроксиметил-изоксазол-5-ил} -N, N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)этил] -4-гидроксиметилизоксазол-5-илметил} -N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)этил] -4-гидроксиметил-изоксазол-3-ил} -N, N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)этил] -4-гидроксиметилизоксазол-3-илметил} -N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N,N-диметилгуанидин;
N'-{3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-3-ил}-N,N-диметилгуанидин;
N'-{5-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-3-илметил}-N,N-диметилгуанидин;
N'-[3-(2-фторбифенил-4-илметил)изоксазол-5-ил]-N,N-диметилгуанидин;
N'-[3-(2-фторбифенил-4-илметил)изоксазол-5-илметил]-N,N-диметилгуанидин;
N'-[5-(2-фторбифенил-4-илметил)изоксазол-3-ил]-N,N-диметилгуанидин;
N'-[5-(2-фторбифенил-4-илметил)изоксазол-3-илметил]-N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)циклопропил] изоксазол-5-ил} -N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)циклопропил] изоксазол-3-ил} -N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-3-илметил}-N,N-диметилгуанидин;
N'-{3-[1-(2-фторбифенил-4-ил)винил]изоксазол-5-ил}-N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)винил] изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{5-[1-(2-фторбифенил-4-ил)винил]изоксазол-3-ил}-N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)винил] изоксазол-3-илметил}-N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-5-ил}-N,N-диметилгуанидин;
N'-{ 3-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-5-илметил} -N, N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-3-ил}-N,N-диметилгуанидин;
N'-{ 5-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-3-илметил} -N, N-диметилгуанидин;
N'-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N,N-диметилгуанидин;
N'-{3-[1-(3-бензоилфенил)этил]изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{5-[1-(3-бензоилфенил)этил]изоксазол-3-ил}-N,N-диметилгуанидин;
N'-{5-[1-(3-бензоилфенил)этил]изоксазол-3-илметил}-N,N-диметилгуанидин;
N'-{3-[1-(4-изобутилфенил)этил]изоксазол-5-ил}-N,N-диметилгуанидин;
N'-{3-[1-(4-изобутилфенил)этил]изоксазол-5-илметил}-N,N-диметилгуанидин;
N'-{5-[1-(4-изобутилфенил)этил]изоксазол-3-ил}-N,N-диметилгуанидин;
N'-{5-[1-(4-изобутилфенил)этил]изоксазол-3-илметил}-N,N-диметилгуанидин;
N'-{ 3-[1-(6-метоксинафталин-2-ил)этил] изоксазол-5-ил} -N,N-диметилгуанидин;
N'-{3-[1-(6-метоксинафталин-2-ил)этил]изоксазол-5-ил-метил}-N,N-диметилгуанидин;
N'-{ 5-[1-(6-метоксинафталин-2-ил)этил] изоксазол-3-ил} -N,N-диметилгуанидин;
N'-{5-[1-(6-метоксинафталин-2-ил)этил]изоксазол-3-ил-метил}-N,N-диметилгуанидин;
({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил-имино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил-имино}пиперидин-1-илметил)амин;
[(2-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}этил-имино)пиперидин-1-илметил]амин;
[(3-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}пропил-имино)пиперидин-1-илметил]амин;
[(2-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}этил-имино)пиперидин-1-илметил]амин;
[(3-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}пропил-имино)пиперидин-1-илметил]амин;
({ 3-[1-(2-фторбифенил-4-ил)этил] -4-метилизоксазол-5-ил-имино} пиперидин-1-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-5-ил-метилимино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил] -4-метилизоксазол-3-ил-имино} пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-3-ил-метилимино}пиперидин-1-илметил)амин;
5-(аминопиперидин-1-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
5-(аминопиперидин-1-илметиленаминометил)-3-[1-(2-фторби-фенил-4-ил)этил] изоксазол-4-карбоновая кислота;
3-(аминопиперидин-1-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
3-(аминопиперидин-1-илметиленаминометил)-5-[1-(2-фтор-бифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
{ 5-(аминопиперидин-1-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{5-(аминопиперидин-1-илметиленаминометил)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{ 3-(аминопиперидин-1-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{3-(аминопиперидин-1-илметиленаминометил)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{ 5-(аминопиперидин-1-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}метанол;
{5-(аминопиперидин-1-илметиленаминометил)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}метанол;
{ 3-(аминопиперидин-1-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}метанол;
{3-(аминопиперидин-1-илметиленаминометил)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}метанол;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил-имино} пиперидин-1-илметил)амин;
({3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илметилимино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-3-ил-имино} пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-3-ил-метилимино}пиперидин-1-илметил)амин;
({ 3-(2-фторбифенил-4-илметил)изоксазол-5-илимино] -пиперидин-1-илметил} амин;
({ 3-(2-фторбифенил-4-илметил)изоксазол-5-илметил-имино] пиперидин-1-илметил}амин;
({ 5-(2-фторбифенил-4-илметил)изоксазол-3-илимино] -пиперидин-1-илметил} амин;
({ 5-(2-фторбифенил-4-илметил)изоксазол-3-илметилимино] -пиперидин-1-илметил}амин;
({ 3-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-5-ил-имино}пиперидин-1-илметил}амин;
({ (3-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-5-ил-метилимино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-3-ил-имино}пиперидин-1-илметил)амин;
({5-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-3-ил-метилимино}пиперидин-1-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)винил] изоксазол-5-илимино} -пиперидин-1-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)винил] изоксазол-5-илметил-имино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)винил] изоксазол-3-илимино} -пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)винил] изоксазол-3-илметил-имино}пиперидин-1-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-5-илимино}пиперидин-1-илметил)амин;
({3-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-5-илметилимино}пиперидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-3-илимино}пиперидин-1-илметил)амин;
({5-[1-(2-фторбифенил-4-ил)-2-метилпропенил]изоксазол-3-илметилимино}пиперидин-1-илметил)амин;
(3-{ 1-[5-(аминопиперидин-1-илметиленамино)изоксазол-3-ил] этил} фенил)фенилметанон;
(3-{ 1-[5-(аминопиперидин-1-илметиленаминометил)изоксазол-3-ил] этил}фенил)фенилметанон;
(3-{ 1-[3-(аминопиперидин-1-илметиленамино)изоксазол-5-ил] этил} фенил)фенилметанон;
(3-{ 1-[3-(аминопиперидин-1-илметиленаминометил)изоксазол-5-ил] этил}фенил)фенилметанон;
({ 3-[1-(4-изобутилфенил)этил] изоксазол-5-илимино} -пиперидин-1-илметил)амин;
({ 3-[1-(4-изобутилфенил)этил] изоксазол-5-илметилимино}-пиперидин-1-илметил)амин;
({ 5-[1-(4-изобутилфенил)этил] изоксазол-3-илимино} -пиперидин-1-илметил)амин;
({ 5-[1-(4-изобутилфенил)этил] изоксазол-3-илметилимино}-пиперидин-1-илметил)амин;
({3-[1-(6-метоксинафталин-2-ил)этил]изоксазол-5-илимино}-пиперидин-1-илметил)амин;
({ 3-[1-(6-метоксинафталин-2-ил)этил] изоксазол-5-илметил-имино} пиперидин-1-илметил)амин;
({5-[1-(6-метоксинафталин-2-ил)этил]изоксазол-3-илимино}-пиперидин-1-илметил)амин;
({ 5-[1-(6-метоксинафталин-2-ил)этил] изоксазол-3-илметил-имино} пиперидин-1-илметил)амин;
({ 3-[1-фторбифенил-4-ил)этил] изоксазол-5-илметилимино} -морфолин-4-илметил)амин;
({5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-морфолин-4-илметил)амин;
[(2-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}этил-имино)морфолин-4-илметил]амин;
[(3-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}пропил-имино)морфолин-4-илметил]амин;
[(2-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}этил-имино)морфолин-4-илметил]амин;
[(3-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}пропил-имино)морфолин-4-илметил]амин;
({ 3-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-5-ил-имино}морфолин-4-илметил)амин;
({3-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-5-ил-метилимино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-3-ил-имино}морфолин-4-илметил)амин;
({5-[1-(2-фторбифенил-4-ил)этил]-4-метилизоксазол-3-ил-метилимино}морфолин-4-илметил)амин;
5-(аминоморфолин-4-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-карбоновая кислота;
5-(аминоморфолин-4-илметиленаминометил)-3-[1-(2-фтор-бифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
3-(аминоморфолин-4-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-карбоновая кислота;
3-(аминоморфолин-4-илметиленаминометил)-5-[1-(2-фтор-бифенил-4-ил)этил] изоксазол-4-карбоновая кислота;
{ 5-(аминоморфолин-4-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}уксусная кислота;
{ 5-(аминоморфолин-4-илметиленаминометил)-3-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{ 3-(аминоморфолин-4-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}уксусная кислота;
{ 3-(аминоморфолин-4-илметиленаминометил)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}уксусная кислота;
{ 5-(аминоморфолин-4-илметиленамино)-3-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}метанол;
{5-(аминоморфолин-4-илметиленаминометил)-3-[1-(2-фторбифенил-4-ил) этил] изоксазол-4-ил}метанол;
{ 3-(аминоморфолин-4-илметиленамино)-5-[1-(2-фторбифенил-4-ил)этил]изоксазол-4-ил}метанол;
{ 3-(аминоморфолин-4-илметиленаминометил)-5-[1-(2-фторбифенил-4-ил)этил] изоксазол-4-ил}метанол;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илметилимино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-3-илимино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-3-илметилимино}морфолин-4-илметил)амин;
{ [3-(2-фторбифенил-4-илметил)изоксазол-5-илметилимино]-морфолин-4-илметил}амин;
{ [5-(2-фторбифенил-4-илметил)изоксазол-3-илимино] морфолин-4-илметил} амин;
{ [5-(2-фторбифенил-4-илметил)изоксазол-3-илметилимино]-морфолин-4-илметил}амин;
({3-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-5-ил-метилимино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)циклопропил] изоксазол-3-ил-имино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)циклопропил]изоксазол-3-ил-метилимино}морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)винил] изоксазол-5-илимино}-морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)винил]изоксазол-5-илметил-имино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)винил] изоксазол-3-илимино}-морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)винил]изоксазол-3-илметил-имино}морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-5-илимино}морфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-5-илметилимино} морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-3-илимино}морфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)-2-метилпропенил] изоксазол-3-илметилимино} морфолин-4-илметил)амин;
(3-{1-[5-(аминоморфолин-4-илметиленаминометил)изоксазол-3-ил]этил}фенил)фенилметанон;
(3-{ 1-[3-(аминоморфолин-4-илметиленамино)изоксазол-5-ил] этил} фенил)фенилметанон;
(3-{ 1-[3-(аминоморфолин-4-илметиленаминометил)изоксазол-5-ил] этил} фенил)фенилметанон;
({ 3-[1-(4-изобутилфенил)этил]изоксазол-5-илметилимино}-морфолин-4-илметил)амин;
({ 5-[1-(4-изобутилфенил)этил] изоксазол-3-илимино} морфолин-4-илметил)амин;
({ 5-[1-(4-изобутилфенил)этил] изоксазол-3-илметилимино} -морфолин-4-илметил)амин;
({ 3-[1-(6-метоксинафталин-2-ил)этил] изоксазол-5-илметил-имино} морфолин-4-илметил)амин;
({ 5-[1-(6-метоксинафталин-2-ил)этил]изоксазол-3-илимино}-морфолин-4-илметил)амин;
({ 5-[1-(6-метоксинафталин-2-ил)этил] изоксазол-3-илметил-имино} морфолин-4-илметил)амин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-гуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}гуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-N'-метилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N'-метилгуанидин;
N-этил-N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил-метил}гуанидин;
N-этил-N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-гуанидин;
N-этил-N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил-метил}гуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-N'-фенилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N'-фенилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N'-фенилгуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-п-толуилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-N'-п-толуилилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N'-п-толуилгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -N'-п-толуилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изoкcaзoл-5-ил} -N'-(4-метоксифенил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-N'-(4-метоксифенил)илгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -N'-(4-метоксифенил)гуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-N'-(4-метоксифенил)гуанидин;
N-бензил-N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидин;
N-бензил-N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}гуанидин;
N-бензил-N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}гуанидин;
N-бензил-N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}гуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-фенетилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-N'-фенетилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N'-фенетилгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-N'-фенетилгуанидин;
N-(2-аминоэтил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-ил}гуанидин;
N-(2-аминоэтил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илметил} гуанидин;
N-(2-аминоэтил)-N'-{ 5-[1-(2-фторбифенил-4-ил)этил] -изоксазол-3-ил}гуанидин;
N-(2-аминоэтил)-N'-{ 5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илметил} гуанидин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперидин-1-ил)метил]амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}-(4-метилпиперидин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино} -(4-метилпиперидин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-(4-метилпиперидин-1-ил)метил]амин;
((2,6-диметилпиперидин-1-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил] изоксазол-5-илимино}метил)амин;
((2,6-диметилпиперидин-1-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил] изоксазол-5-илметилимино}метил)амин;
((2,6-диметилпиперидин-1-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил] изоксазол-3-илимино}метил)амин;
((2,6-диметилпиперидин-1-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил] изоксазол-3-илметилимино}метил)амин;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил-метилимино}метил)пиперидин-4-ол;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-4-ол;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-4-ол;
[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-(4-метоксипиперидин-1-ил)метил]амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}-(4-метоксипиперидин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино}-(4-метоксипиперидин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-(4-метоксипиперидин-1-ил)метил]амин;
((4-аминопиперидин-1-ил)-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илимино}метил)амин;
((4-аминопиперидин-1-ил)-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илметилимино}метил)амин;
((4-аминопиперидин-1-ил)-{5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илимино}метил)амин;
((4-аминопиперидин-1-ил)-{5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илметилимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}метил)амин;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-имино} метил)пиперидин-4-карбоновая кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-метилимино} метил)пиперидин-4-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-4-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-4-карбоновая кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-имино} метил)пиперидин-4-карбоксамид;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-метилимино} метил)пиперидин-4-карбоксамид;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-4-карбоксамид;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-4-карбоксамид;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-имино} метил)пиперидин-3-карбоновая кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-метилимино} метил)пиперидин-3-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-3-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-3-карбоновая кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-имино} метил)пиперидин-3-карбоксамид;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-метилимино} метил)пиперидин-3-карбоксамид;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-3-карбоксамид;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-3-карбоксамид;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил-метилимино} метил)пиперидин-4-он;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-имино} метил)пиперидин-4-он;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил-метилимино} метил)пиперидин-4-он;
((3,5-диметилморфолин-4-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-илимино}метил)амин;
((3,5-диметилморфолин-4-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-илметилимино}метил)амин;
((3,5-диметилморфолин-4-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-3-илимино}метил)амин;
((3,5-диметилморфолин-4-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-3-илметилимино}метил)амин;
((2,6-диметилморфолин-4-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-илимино}метил)амин;
((2,6-диметилморфолин-4-ил)-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-илметилимино}метил)амин;
((2,6-диметилморфолин-4-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-3-илимино}метил)амин;
((2,6-диметилморфолин-4-ил)-{ 5-[1-(2-фторбифенил-4-ил)-этил]изоксазол-3-илметилимино}метил)амин;
({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}-тиаморфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино}-тиаморфолин-4-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-тиаморфолин-4-илметил)амин;
({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}-пиперазин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино}-пиперазин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-пиперазин-1-илметил)амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметилимино} -(4-метилпиперазин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино} -(4-метилпиперазин-1-ил)метил]амин;
[{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}-(4-метилпиперазин-1-ил)метил]амин;
2-[4-амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперазин-1-ил]этанол;
2-[4-амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметилимино}метил)пиперазин-1-ил]этанол;
2-[4-амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино} метил)пиперазин-1-ил]этанол;
2-[4-амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино}метил)пиперазин-1-ил]этанол;
([4-(2-аминоэтил)пиперазин-1-ил] -{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин;
([4-(2-аминоэтил)пиперазин-1-ил] -{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметилимино}метил)амин;
([4-(2-аминоэтил)пиперазин-1-ил] -{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илимино}метил)амин;
([4-(2-аминоэтил)пиперазин-1-ил] -{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметилимино}метил)амин;
1-[4-амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперазин-1-ил]этанон;
1-[4-амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметилимино}метил)пиперазин-1-ил]этанон;
1-[4-амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино} метил)пиперазин-1-ил]этанон;
1-[4-амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино}метил)пиперазин-1-ил]этанон;
(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -гуанидино)уксусная кислота;
(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -гуанидино)уксусная кислота;
(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -гуанидино)уксусная кислота;
(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N-метилгуанидино)уксусная кислота;
(N'-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-N-метилгуанидино)уксусная кислота;
(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -N-метилгуанидино)уксусная кислота;
(N'-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N-метилгуанидино)уксусная кислота;
этил (N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} гуанидино)ацетат;
этил (N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксаэол-3-ил}гуанидино)ацетат;
этил (N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} гуанидино)ацетат;
2-(N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}гуанидино)ацетамид;
2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} гуанидино)ацетамид;
2-(N'-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}гуанидино)ацетамид;
2-(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} гуанидино)ацетамид;
2-(N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-гуанидино)пропионовая кислота;
2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -гуанидино)пропионовая кислота;
2-(N'-{5-[1-(2-фторбифенил-4-ил)этил]иэоксазол-3-ил}-гуанидино)пропионовая кислота;
2-(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -гуанидино)пропионовая кислота;
2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-гуанидино)янтарная кислота;
2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -гуанидино)янтарная кислота;
2-(N'-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-гуанидино)янтарная кислота;
2-(N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -гуанидино)янтарная кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пирролидин-2-карбоновая кислота;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметилимино} метил)пирролидин-2-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илимино} метил)пирролидин-2-карбоновая кислота;
1-(амино-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино} метил)пирролидин-2-карбоновая кислота;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N',N''-диметилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -N',N''-диметилгуанидин;
N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-N',N''-диметилгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -N',N''-диметилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-метил-N''-фенилгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-N'-метил-N''-фенилгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-N'-метил-N''-фенилгуанидин;
N-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-N'-метил-N''-фенилгуанидин;
N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N,N,N',N''-тетраметилгуанидин;
N''-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-N,N,N',N''-тетраметилгуанидин;
N''-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-N,N,N',N''-тетраметилгуанидин;
N''-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N,N,N',N''-тетраметилгуанидин;
(дипиперидин-1-илметилен)-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-ил}амин;
(дипиперидин-1-илметилен)-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илметил}амин;
(дипиперидин-1-илметилен)-{ 5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-ил}амин;
(дипиперидин-1-илметилен)-{5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илметил}амин;
(диморфолин-4-илметилен)-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-ил} амин;
(диморфолин-4-илметилен)-{ 3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илметил}амин;
(диморфолин-4-илметилен)-{5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-ил} амин;
(диморфолин-4-илметилен)-{ 5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илметил}амин;
(дипиперазин-4-илметилен)-{ 3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-ил}амин;
(дипиперазин-4-илметилен)-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илметил}амин;
(дипиперазин-4-илметилен)-{ 5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-ил}амин;
(дипиперазин-4-илметилен)-{5-[1-(2-фторбифенил-4-ил)этил]-изоксазол-3-илметил}амин;
(4,5-дигидро-1Н-имидазол-2-ил)-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}амин;
(4,5-дигидро-1Н-имидазол-2-ил)-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}амин;
(4,5-дигидро-1Н-имидазол-2-ил)-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}амин;
(4,5-дигидро-1Н-имидазол-2-ил)-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-4,5-дигидро-1Н-имидазол-2-иламин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-4,5-дигидро-1Н-имидазол-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-4,5-дигидро-1Н-имидазол-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-4,5-дигидро-1Н-имидазол-2-иламин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -(1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-(1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -(1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-(1,4,5,6-тетрагидропиримидин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -1,4,5,6-тетрагидропиримидин-2-иламин;
(3,6-дигидро-2Н-[1,3,5] оксадиазин-4-ил)-{3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}амин;
(3,6-дигидро-2Н-[1,3,5] оксадиазин-4-ил)-{3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}амин;
(3,6-дигидро-2Н-[1,3,5] оксадиазин-4-ил)-{5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}амин;
(3,6-дигидро-2Н-[1,3,5] оксадиазин-4-ил)-{5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}амин;
3-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-3,6-дигидро-2Н-[1,3,5] оксадиазин-4-иламин;
3-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-3,6-дигидро-2Н-[1,3,5]оксадиазин-4-иламин;
3-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-3,6-дигидро-2Н-[1,3,5] оксадиазин-4-иламин;
3-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-3,6-дигидро-2Н-[1,3,5]оксадиазин-4-иламин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -(1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-(1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -(1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-(1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-(5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-(5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-(5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-(5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -5-метил-1,4,5,6-тетрагидро[1,3,5]триазин-2-ил)амин;
2-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-иламино} -1,4,5,6-тетрагидропиримидин-5-ол;
2-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил-амино}-1,4,5,6-тетрагидропиримидин-5-ол;
2-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-иламино} -1,4,5,6-тетрагидропиримидин-5-ол;
2-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил-амино}-1,4,5,6-тетрагидропиримидин-5-ол;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-(5-метокси-1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -(5-метокси-1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил}-(5-метокси-1,4,5,6-тетрагидропиримидин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -(5-метокси-1,4,5,6-тетрагидропиримидин-2-ил)амин;
2-амино-1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -1,4,5,6-тетрагидропиримидин-5-ол;
2-амино-1-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илметил}-1,4,5,6-тетрагидропиримидин-5-ол;
2-амино-1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -1,4,5,6-тетрагидропиримидин-5-ол;
2-амино-1-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-1,4,5,6-тетрагидропиримидин-5-ол;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -5-метокси-1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -5-метокси-1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -5-метокси-1,4,5,6-тетрагидропиримидин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -5-метокси-1,4,5,6-тетрагидропиримидин-2-иламин;
{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-(4,5,6,7-тетрагидро-1H-[1,3]диазепин-2-ил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил}-(4,5,6,7-тетрагидро-1Н-[1,3]диазепин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-ил}-(4,5,6,7-тетрагидро-1Н-[1,3]диазепин-2-ил)амин;
{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-(4,5,6,7-тетрагидро-1Н-[1,3]диазепин-2-ил)амин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -4,5,6,7-тетрагидро-1H-[1,3]диазепин-2-иламин;
1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -4,5,6,7-тетрагидро-1Н-[1,3]диазепин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-ил} -4,5,6,7-тетрагидро-1H-[1,3]диазепин-2-иламин;
1-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -4,5,6,7-тетрагидро-1Н-[1,3]диазепин-2-иламин;
({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил-имино}пирролидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил} этил] изоксазол-3-илимино}-пирролидин-1-илметил)амин;
({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино}-пирролидин-1-илметил)амин;
(азепан-1-ил-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)амин;
({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -тиазолидин-3-илметил)амин;
1-(амино{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)пиперидин-2-он;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -N'-(2-оксопропил)гуанидин;
этил 3-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)пропионат;
2-(N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-гуанидино)-N,N-диметилацетамид;
3-(N'-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-гуанидино)-N,N-диметилпропионамид;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(3-гидроксипропил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-(2-пирролидин-1-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изoкcaзoл-5-ил} -N'-(2-пиперидин-1-илэтил)гуанидин;
N-{ 3-[1-(2-фтopбифeнил-4-ил)этил] изoкcaзoл-5-ил}-N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-(3-морфолин-4-илпропил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -1-(2-метоксиэтил)имидазолин-4-он;
N-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -метиламинометил)-N'-метилгуанидин;
N'-(диметиламино-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)-N,N-диметилгуанидин;
[[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илметил} -(4-метилпиперазин-1-ил)метилимино]-(4-метилпиперазин-1-ил)-метил]амин;
N-[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)гуанидин;
N-[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)гуанидин;
N-{ { 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}-[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)-этил]гуанидин;
[бис(4-метилпиперазин-1-ил)метилен] -{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}амин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N', N''-бис(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N',N''-бис(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N',N''-бис[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-(метиламино)гуанидин;
N-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-(диметиламино)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(пиридин-2-иламино)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-пиридин-2-илгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-пиридин-4-илгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-пиримидин-2-илгуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(1Н-тетразол-5-ил)гуанидин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(1-оксо[1,4]тиазинан-4-ил)метил]амин;
((1,1-диоксо[1,4]тиазинан-4-ил)-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин;
{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-(имино-морфолин-4-илметил)метиламин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N'-метилгуанидин;
N-этил-N'-{3-[1-(2-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-ил}гуанидин;
N, N-диэтил-N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-ил} гуанидин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} пирролидин-1-илметил)амин;
(азепан-1-ил-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино}метил)амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] -1-метилэтил]изоксазол-5-илимино}-(4-метилпиперазин-1-ил)метил]амин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} тиазолидин-3-илметил)амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] -1-метилэтил]изоксазол-5-илимино}-(4-метилпиперидин-1-ил)метил]амин;
((2,6-диметилморфолин-4-ил)-{3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}метил)амин;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} метил)пиперидин-4-он;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} метил)пиперидин-2-он;
1-(амино-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} метил)пиперидин-4-ол;
[{ 3-[1-(2-фторбифенил-4-ил)этил] -1-метилэтил]изоксазол-5-илимино}-(4-метоксипиперидин-1-ил)метил]амин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино)-[1,4]тиазинан-4-ил)метил]амин;
1-[4-(амино-{3-[1-(2-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-илимино} метил)пиперазин-1-ил]этанон;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-оксопропил)гуанидин;
этил (N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-гуанидино)ацетат;
этил 3-(N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-ил}гуанидино)пропионат;
2-(N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -гуанидино)-N,N-диметилацетамид;
3-(N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -гуанидино)-N,N-диметилпропионамид;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-(3-гидроксипропил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N'-(2-метоксиэтил)гуанидин;
N-(2-диметиламиноэтил)-N'-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-пирролидин-1-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-(2-пиперидин-1-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(3-морфолин-4-илпропил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -1-метилимидазолидин-4-он;
2-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -1-(2-гидроксиэтил)имидазолидин-4-он;
2-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-1-(2-метоксиэтил)имидазолидин-4-он;
N-({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино}метиламинометил-N'-метилгуанидин;
N'-(диметиламино-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}метил)-N,N-диметилгуанидин;
[({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино)морфолин-4-илметилимино)морфолин-4-илметил]амин;
[({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино)-(4-метилпиперазин-1-ил)метилимино]-(4-метилпиперазин-1-ил)метил]амин;
N-[{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)гуанидин;
N-[{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)-гуанидин;
N-{ (3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N',N''-диметилгуанидин;
N''-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илметил}-N,N,N', N''-тетраметилгуанидин;
(диморфолин-4-илметилен)-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}амин;
[бис(4-метилпиперазин-1-ил)метилен] -{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}амин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N',N''-бис-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N',N''-бис-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N',N''-бис-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-метилгуанидин;
N'-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}-N,N-диметилгуанидин;
N-этил-N'-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидин;
N,N-диэтил-N'-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидин;
({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино)-пирролидин-1-илметил}амин;
({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -пиперидин-1-илметил)амин;
(азепан-1-ил-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил]амин;
({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино}-тиазолидин-3-илметил)амин;
[(3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперидин-1-ил)метил]амин;
((2,6-диметилморфолин-4-ил)-{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперидин-4-он;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперидин-2-он;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперидин-4-ол;
[{3-[1-(2'-фторбифенил-4-ил)этил]этил]изоксазол-5-илимино}-(4-метоксипиперидин-1-ил)метил]амин;
((3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино)-[1,4]тиазинан-4-ил)метил]амин;
1-[4-(амино-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперазин-1-ил]этанон;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-оксопропил)гуанидин;
этил (N'-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)ацетат;
этил 3-(N'-{ 3-[1-[2'-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)пропионат;
2-(N'-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидино)-N,N-диметилацетамид;
3-(N'-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидино)-N,N-диметилпропионамид;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(3-гидроксипропил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-метоксиэтил)гуанидин;
N-(2-диметиламиноэтил)-N'-{ 3-[1-(2'-фторбифенил-4-ил)-этил] изоксазол-5-ил}гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-(2-пирролидин-1-илэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-(2-пиперидин-1-илэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(3-морфолин-4-илпропил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино}-1-метилимидазолидин-4-он;
2-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино}-1-(2-гидроксиэтил)имидазолидин-4-он;
2-{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}-1-(2-метоксиэтил)имидазолидин-4-он;
N-({3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}-метиламинометил-N'-метилгуанидин;
N'-(диметиламино-{ 3-[1-(2'-фторбифенил-4-ил)этил] -изоксазол-5-илимино} метил)-N,N-диметилгуанидин;
[({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино)-морфолин-4-илметилимино)морфолин-4-илметил]амин;
[({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино)-(4-метилпиперазин-1-ил)метилимино]-(4-метилпиперазин-1-ил)метил]-амин;
N-[{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}-(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)-гуанидин;
N-[{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илимино}-(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)гуанидин;
N-({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил}-N',N''-диметилгуанидин;
N''-{ 3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-илметил}-N,N,N',N''-тетраметилгуанидин;
(диморфолин-4-илметилен)-{ 3-[1-(2'-фторбифенил-4-ил)этил]-изоксазол-5-ил}амин;
[бис(4-метилпиперазин-1-ил)метилен]-{3-[1-(2'-фторбифенил-4-ил)этил]изоксазол-5-ил}амин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил}-N',N''-бис-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N', N''-бис-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N', N''-бис-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-метилгуанидин;
N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N,N-диметилгуанидин;
N-этил-N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-ил}гуанидин;
N, N-диэтил-N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-ил} гуанидин;
({3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино)пирролидин-1-илметил)амин;
({3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино)пиперидин-1-илметил)амин;
(азепан-1-ил-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино}метил)амин;
({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -морфолин-4-илметил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил]амин;
({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} тиазолидин-3-илметил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(4-метилпиперидин-1-ил)метил]амин;
((2,6-диметилморфолин-4-ил)-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}метил)амин;
((4-диметиламинопиперидин-1-ил)-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}метил)амин;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино} метил)пиперидин-4-он;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино} метил)пиперидин-2-он;
1-(амино-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино} метил)пиперидин-4-ол;
[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]этил]изоксазол-5-илимино}-(4-метоксипиперидин-1-ил)метил]амин;
({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино)-[1,4]тиазинан-4-ил)метил]амин;
1-[4-(амино-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-илимино}метил)пиперазин-1-ил]этанон;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-оксопропил)гуанидин;
этил (N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] -изоксазол-5-ил}гуанидино)ацетат;
этил 3-(N'-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-ил}гуанидино)пропионат;
2-(N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} гуанидино)-N,N-диметилацетамид;
3-(N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} гуанидино)-N,N-диметилпропионамид;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-гидроксиэтил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(3-гидроксипропил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-метоксиэтил)гуанидин;
N-(2-диметиламиноэтил)-N'-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-пирролидин-1-илэтил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-пиперидин-1-илэтил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-(3-морфолин-4-илпропил)гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}-N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}-1-метилимидазолидин-4-он;
2-{ 3-[1-[2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -1-(2-гидроксиэтил)имидазолидин-4-он;
2-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -1-(2-метоксиэтил)имидазолидин-4-он;
N-({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}мeтилaминoмeтил-N'-метилгуанидин;
N'-(диметиламино-{ 3-[1-(2'-фторбифенил-4-ил)-1-метил-этил]изоксазол-5-илимино}метил)-N,N-диметилгуанидин;
[({3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино)морфолин-4-илметилимино)морфолин-4-илметил]амин;
[({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино)-(4-метилпиперазин-1-ил)метилимино]-(4-метилпиперазин-1-ил)метил]амин;
N-[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)гуанидин;
N-[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)-гуанидин;
N-({ 3-[1-[2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-илимино}-[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N',N''-диметилгуанидин;
N''-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N, N, N', N''-тетраметилгуанидин;
(диморфолин-4-илметилен)-{3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}амин;
[бис(4-метилпиперазин-1-ил)метилен] -{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил]изоксазол-5-ил}амин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N',N''-бис-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N',N''-бис-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил}-N',N''-бис-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N'-метилгуанидин;
N-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N'-этилгуанидин;
N'-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N,N-диэтилгуанидин;
(3-{ 1-[5-(аминопирролидин-1-илметиленамино)изоксазол-3-ил] этил} фенил)фенилметанон;
(3-{ 1-[5-(аминоазепан-1-ил-метиленамино)изоксазол-3-ил] этил}фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
(3-{ 1-[5-(аминотиазолидин-3-илметиленамино)изоксазол-3-ил] этил} фенил)фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперидин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
[3-(1-{ 5-[амино(2,6-диметилморфолин-4-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
[3-(1-{ 5-[амино(4-диметиламинопиперидин-1-ил)метиленамино]изоксазол-3-ил}этил)фенил]фенилметанон;
1-(амино-{3-[1-(3-бензоилфенил)этил]изоксазол-5-илимино}-метил)пиперидин-4-он;
1-(амино-{3-[1-(3-бензоилфенил)этил]изоксазол-5-илимино}-метил)пиперидин-2-он;
[3-(1-{ 5-[амино(4-гидроксипиперидин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
[3-(1-{ 5-[амино(4-метоксипиперидин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
(3-{ 1-[5-(амино[1,4] тиазинан-4-илметиленамино)изоксазол-3-ил] этил}фенил)фенилметанон;
1-[4-(амино-{3-[1-(3-бензоилфенил)этил]изоксазол-5-илимино}метил)пиперазин-1-ил]этанон;
N-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N''-(2-оксопропил)гуанидин;
этил (N'-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-гуанидино)ацетат;
этил (N'-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-гуанидино)пропионат;
2-(N'-{ 3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-гуанидино)-N,N-диметилацетамид;
3-(N'-{ 3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-гуанидино)-N,N-диметилпропионамид;
N-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N'-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(3-гидроксипропил)гуанидин;
N-{3-[1-(3-бензоилфенил)этил]зоксазол-5-ил}-N'-(2-метоксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-диметиламиноэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-пирролидин-1-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-пиперидин-1-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил}-N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(3-морфолин-4-илпропил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(3-бензоилфенил)этил]изоксазол-5-илимино}-1-метилимидазолидин-4-он;
2-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино} -1-(2-гидроксиэтил)имидазолидин-4-он;
2-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино} -1-(2-метоксиэтил)имидазолидин-4-он;
N-({ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино} -метиламинометил)-N'-метилгуанидин;
N'-({ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино} -диметиламинометил)-N,N-диметилгуанидин;
[3-(1-{5-[(аминоморфолин-4-илметиленамино)морфолин-4-илметиленамино]изоксазол-3-ил}этил)фенил]фенилметанон;
[3-(1-{ 5-[[амино(4-метилпиперазин-1-ил)метиленамино] -(4-метилпиперазин-1-ил)метиленамино]изоксазол-3-ил}этил)фенил]фенилметанон;
N-[{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино} -(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)гуанидин;
N-[{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-илимино}-(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)гуанидин;
N-{ { 3-[1-(3-бензоилфенил)этил]изоксазол-5-илимино}-[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N',N''-диметилгуанидин;
N''-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N,N,N',N''-тетраметилгуанидин;
(3-{1-[5-(диморфолин-4-илметиленамино)изоксазол-3-ил]-этил}фенил)фенилметанон;
[3-(1-{ 5-[бис(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил]фенилметанон;
N-{ 3-[1-(3-бензоилфенил)этил]изоксазол-5-ил}-N',N''-бис-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N',N''-бис-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N',N''-бис-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(3-бензоилфенил)1-метилэтил]изоксазол-5-ил}-N'-метилгуанидин;
N'-{ 3-[1-(3-бензоилфенил)1-метилэтил] изоксазол-5-ил}-N,N-диметилгуанидин;
N-{3-[1-(3-бензоилфенил)1-метилэтил]изоксазол-5-ил}-N'-этилгуанидин;
N'-{3-[1-(3-бензоилфенил)1-метилэтил]изоксазол-5-ил}-N,N-диэтилгуанидин;
(3-{ 1-[5-(аминопирролидин-1-илметиленамино)изоксазол-3-ил]-1-метилэтил} фенил)фенилметанон;
(3-{ 1-[5-(аминопиперидин-1-илметиленамино)изоксазол-3-ил] -1-метилэтил} фенил)фенилметанон;
(3-{1-[5-(аминоазепан-1-илметиленамино)изоксазол-3-ил]-1-метилэтил}фенил)фенилметанон;
(3-{1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил]-1-метилэтил}фенил)фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперазин-1-ил)метиленамино]-изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
(3-{ 1-[5-(аминотиазолидин-3-илметиленамино)изоксазол-3-ил]-1-метилэтил} фенил)фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперидин-1-ил)метиленамино]-изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
[3-(1-{ 5-[амино(2,6-диметилморфолин-4-ил)метиленамино] -изоксазол-3-ил} -1-метилэтил)фенил]фенилметанон;
[3-(1-{ 5-[амино(4-диметиламинопиперидин-1-ил)метилен-амино] изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
1-(амино-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-илимино} метил)пиперидин-4-он;
1-(амино-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-илимино} метил)пиперидин-2-он;
[3-(1-{ 5-[амино(4-гидроксипиперидин-1-ил)метиленамино] -изоксазол-3-ил} -1-метилэтил)фенил]фенилметанон;
[3-(1-{ 5-[амино(4-метоксипиперидин-1-ил)метиленамино]-изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
(3-{ 1-[5-(амино[1,4] тиазинан-4-илметиленамино)изоксазол-3-ил] -1-метилэтил}фенил)фенилметанон;
1-[4-(амино-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-илимино}метил)пиперазин-1-ил]этанон;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-(2-оксопропил)гуанидин;
этил (N'-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} гуанидино)ацетат;
этил (N'-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} гуанидино)пропионат;
2-(N'-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} гуанидино)-N, N-диметилацетамид;
3-(N'-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} гуанидино)-N, N-диметилпропионамид;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-(3-гидроксипропил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-(2-метоксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил}-N'-(2-диметиламиноэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N'-(2-пирролидин-1-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил}-N'-(2-пиперидин-1-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил}-N'-[2-(4-метилпиперазин-1-ил)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N'-(3-морфолин-4-илпропил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил}-N'-[2-(2-метоксиэтокси)этил]гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-[2-(3-гидроксипропокси)этил]гуанидин;
2-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}-1-метилимидазолидин-4-он;
2-{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}-1-(2-гидроксиэтил)имидазолидин-4-он;
2-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-илимино} -1-(2-метоксиэтил)имидазолидин-4-он;
N-({ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}метиламинометил)-N'-метилгуанидин;
N'-({3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}диметиламинометил)-N,N-диметилгуанидин;
[3-(1-{ 5-[(аминоморфолин-4-илметиленамино)морфолин-4-илметиленамино] изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
[3-(1-{ 5-[[амино(4-метилпиперазин-1-ил)метиленамино] -(4-метилпиперазин-1-ил)метиленамино]изоксазол-3-ил}-1-метилэтил)-фенил]фенилметанон;
N-[{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-илимино} -(2-морфолин-4-илэтиламино)метил]-N'-(2-морфолин-4-илэтил)гуанидин;
N-[{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}-(2-гидроксиэтиламино)метил]-N'-(2-гидроксиэтил)-гуанидин;
N-{{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-илимино}-[2-(2-гидроксиэтокси)этиламино]метил}-N'-[2-(2-гидроксиэтокси)этил]гуанидин;
N-{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N',N''-диметилгуанидин;
N''-(3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N,N,N',N''-тетраметилгуанидин;
(3-{ 1-[5-(диморфолин-4-илметиленамино)изоксазол-3-ил]-1-метилэтил}фенил)фенилметанон;
[3-(1-{ 5-[бис(4-метилпиперазин-1-ил)метиленамидино]-изоксазол-3-ил}-1-метилэтил)фенил]фенилметанон;
N-{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N',N''-бис-(2-морфолин-4-илэтил)гуанидин;
N-{3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N',N''-бис-(2-гидроксиэтил)гуанидин;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил]изоксазол-5-ил}-N',N''-бис-[2-(2-гидроксиэтокси)этил]гуанидин;
({ 3-[1-этокси-1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амин;
(3-{ 1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] -1-этоксиэтил} фенил)фенилметанон;
({ 3-[(2-фторбифенил-4-ил)диметоксиметил] изоксазол-5-илимино}морфолин-4-илметил)амин;
([3-(1-бифенил-4-илвинил)изоксазол-5-илимино]морфолин-4-илметил)амин;
({3-[1-(1-метил-1Н-индол-2-ил)винил]изоксазол-5-илимино}-морфолин-4-илметил)амин;
(морфолин-4-ил-({ 3-[1-(6-фенилпиридазин-3-ил)этил]-изоксазол-5-илимино} метил)амин;
(морфолин-4-ил-({ 3-[1-(5-фенилпиримидин-2-ил)этил]-изоксазол-5-илимино} метил)амин;
(морфолин-4-ил-({ 3-[1-(4-фенилпиримидин-2-ил)этил]-изоксазол-5-илимино} метил)амин;
(морфолин-4-ил-[3-(1-хинолин-6-илэтил)изоксазол-5-илимино]метил)амин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-пиридин-3-илметилгуанидин.
Примеры
Настоящее изобретение объясняется далее примерами и ссылочными примерами, но конечно, не ограничивается ими.
В примерах и тому подобное значения используемой аббревиатуры следующие:
Вос: трет-бутоксикарбонил
Tos: п-толуолсульфонил
Me: метил
Et: этил
Рrn: н-пропил
Вut: трет-бутил
Ph: фенил
Ас: ацетил
ТФУ: трифторуксусная кислота
ТМС: триметилсилил
Пример 1
N'-(трет-Бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N,N-диметилгуанидин (схема 11, приведенная в конце описания).
Соединение (2,10 г), полученное по ссылочному примеру 2, растворяют в ацетонитриле (100 мл), затем добавляют триэтиламин (1,77 г) и по каплям при охлаждении льдом 40%-ный водный раствор диметиламина (1,04 г). Затем в течение 30 минут прибавляют по каплям раствор нитрата серебра (1,33 г) в ацетонитриле (20 мл) и полученную смесь перемешивают при комнатной температуре в течение 18 часов. Нерастворимые продукты отфильтровывают и промывают ацетонитрилом, после чего маточный раствор концентрируют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (1,76 г).
Точка плавления 108-111oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,43 (с, 9Н), 1,66 (д, 3Н, J=7,1 Гц), 3,07 (с, 6Н), 4,16 (кв, 1H, J=7,1 Гц), 5,24 (с, 1Н), 6,74 (с, 1H), 7,07-7,17 (м, 2Н), 7,32-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3383, 2975, 1733, 1614, 1482, 1403.
MS (FD) [m/e]: 452 (М+).
Элементный анализ:
Вычислено: С 66,35; Н 6,46; N 12,38.
Найдено: С 66,22; Н 6,45; N 12,46.
Пример 2
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N''-этилгуанидин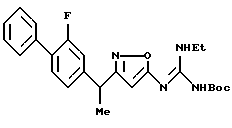
Желаемое соединение получают тем же способом, что и по примеру 1.
Точка плавления 87-92oС.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,21 (т, 3Н, J=7,3 Гц), 1,49 (с, 9Н), 1,67 (д, 3Н, J=7,3 Гц), 3,40 (м, 2Н), 4,14 (кв, 1Н, J=7,3 Гц), 5,32 (с, 1Н), 7,07-7,17 (м, 2Н), 7,31-7,54 (м, 6Н), 7,94 (ушир., 1Н), 8,48 (ушир., 1Н).
ИК (КВr) [см-1]: 3410, 3340, 2980, 1730, 1628, 1603, 1556, 1445, 1240, 1152.
Пример 3
(трет-Бутоксикарбонил)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}пиперидин-1-илметил)амин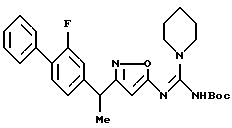
Желаемое соединение получают тем же способом, что и по примеру 1.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,42 (с, 9Н), 1,65 (ушир. с, 6Н), 1,66 (д, 3Н, J=6,3 Гц), 3,40-3,60 (ушир., 4Н), 4,15 (кв, 1H, J=6,3 Гц), 5,24 (с, 1Н), 6,60-6,80 (ушир., 1Н), 7,06-7,17 (м, 2Н), 7,32-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3390, 2940, 1726, 1600, 1483, 1435, 1365, 1152.
Пример 4
(трет-Бутоксикарбонил)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амин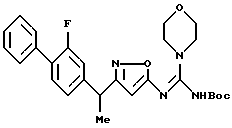
Желаемое соединение получают тем же способом, что и по примеру 1.
Точка плавления 152-153oС.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,44 (с, 9Н), 1,67 (д, 3Н, J=7,2 Гц), 3,57 (м, 4Н), 4,16 (кв, 1H, J=7,2 Гц), 5,28 (с, 1H), 6,86 (с, 1H), 7,06-7,16 (м, 2Н), 7,32-7,53 (м, 6Н).
ИК (КВr) [см-1]: 3374, 2976, 1726, 1609, 1482, 1431, 1115.
MS (FD) [m/e]: 495 (М+1).
Элементный анализ:
Вычислено: С 65,57; Н 6,32; N 11,33.
Найдено: С 65,45; Н 6,39; N 11,36.
Пример 5
трет-Бутил (N'-(трет-бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидино)ацетат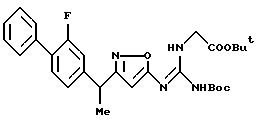
Желаемое соединение получают тем же способом, что и по примеру 1.
Точка плавления 101,5-103,5oС.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,48 (с, 9Н), 1,50 (с, 9Н), 1,66 (д, 3H, J= 7,3 Гц), 4,03 (д, 2Н, J=4,6 Гц), 4,14 (кв, 1Н, J=7,3 Гц), 5,31 (с, 1Н), 7,06-7,16 (м, 2Н), 7,32-7,54 (м, 6Н), 8,50-8,52 (ушир.м, 2Н).
ИК (КВr) [см-1]: 3407, 3351, 2980, 1743, 1643, 1560, 1485, 1452.
MS (FD) [m/e]: 538 (М+).
Элементный анализ:
Вычислено: С 64,67; Н 6,55; N 10,40.
Найдено: С 64,36; Н 6,57; N 10,35.
Пример 6
трет-Бутил (N'-(трет-бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N-метилгуанидино)ацетат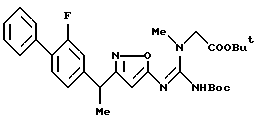
Желаемое соединение получают тем же способом, что и по примеру 1.
Точка плавления 190-198oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,42 (с, 9Н), 1,47 (с, 9Н), 1,65 (д, 3Н, J= 7,2 Гц), 3,12 (с, 3Н), 4,00 (с, 2Н), 4,12 (кв, 1H, J=7,2 Гц), 5,29 (с, 1Н), 6,87 (ушир.с, 1Н), 7,06-7,16 (м, 2Н), 7,32-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3388, 2984, 1744, 1733, 1608, 1483, 1413.
MS (FD) [m/e]: 552 (М+).
Элементный анализ:
Вычислено: С 65,20; Н 6,75; N 10,14.
Найдено: С 64,90; Н 6,74; N 9,93.
Пример 7
Этил (N'-(трет-бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}гуанидино)ацетат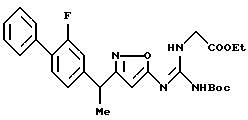
Желаемое соединение получают тем же способом, что и по примеру 1.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,28 (т, 3Н, J=7,1 Гц), 1,50 (с, 9Н), 1,66 (д, 3Н, J= 7,3 Гц), 4,12 (д, 2Н, J=5,0 Гц), 4,16 (кв, 1H, J=7,3 Гц), 4,23 (кв, 2Н, J=7,1 Гц), 5,33 (с, 1H), 7,06-7,16 (м, 2Н), 7,35-7,54 (м, 6Н), 8,54 (ушир.м, 2Н).
ИК (чистый) [см-1]: 3398, 2981, 1732, 1634, 1608, 1557, 1486, 1455.
Пример 8
N'-Бензоил-N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N-метил-N''-пропилгуанидин (схема 12, приведенная в конце описания).
Желаемое соединение получают тем же способом, что и по примеру 1.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 0,90 (т, 3Н, J=7,3 Гц), 1,56 (секст., 2Н, J=7,3 Гц), 1,70 (д, 3Н, J=7,3 Гц), 2,85-2,97 (м, 2Н), 3,51 (с, 3Н), 4,21 (кв, 1Н, J= 7,3 Гц), 5,50 (с, 1Н), 7,02-7,27 (м, 3Н), 7,32-7,52 (м, 8Н), 8,17-8,22 (м, 2Н), 10,30-10, 60 (м, 1Н).
Пример 9
N'-Бензоил-N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N,N''-диметилгуанидин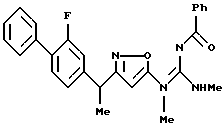
Желаемое соединение получают тем же способом, что и по примеру 1.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,70 (д, 3Н, J=7,3 Гц), 2,74-2,76 (м, 3Н), 3,51 (с, 3Н), 4,21 (кв, 1Н, J=7,3 Гц), 5,49 (с, 1H), 7,04-7,16 (м, 2Н), 7,33-7,55 (м, 9Н), 8,16-8,22 (м, 2Н), 10,20-10,55 (ушир., 1H).
ИК (чистый) [см-1] : 3260, 3070, 2980, 1622, 1495, 1453, 1418, 1396, 1362.
Пример 10
N, N'-Ди(трет-бутоксикарбонил)-N''-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}гуанидин (схема 13, приведенная в конце описания).
Соединение (1,12 г), полученное по ссылочному примеру 10, и 1,3-ди(трет-бутоксикарбонил)-2-метилизомочевина (не подвергнутая экспертизе японская патентная публикация 2-3661) (2,20 г) растворяют в пиридине (5 мл), затем добавляют 1,8-диазабицикло[5,4,0] ундец-7-ен (636 мг) и полученную смесь перемешивают при комнатной температуре в течение 24 часов. Затем к реакционной смеси прибавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель отгоняют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (1,24 г).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,49 (с, 9Н), 1,50 (с, 9Н), 1,69 (д, 3Н, J= 7,1 Гц), 4,26 (кв, 1H, J=7,1 Гц), 4,67 (д, 2Н, J=5,3 Гц), 6,05 (с, 1H), 7,03-7,12 (м, 2Н), 7,33-7,55 (м, 6Н), 8,84 (ушир.с, 1H), 11,47 (ушир.с, 1H).
Пример 11
N, N''-Ди(трет-бутоксикарбонил)-N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N',N'-диметилгуанидин (схема 14, приведенная в конце описания).
Соединение (2,38 г), полученное по ссылочному примеру 7, соединение (2,18 г), полученное по ссылочному примеру 11, и трибутилфосфин (3,49 г) растворяют в тетрагидрофуране, затем добавляют 1,1'-(азодикарбонил)дипиперидин (4,36 г) при 0oС и полученную смесь доводят до комнатной температуры и перемешивают в течение 24 часов. К реакционной смеси прибавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Нерастворимые продукты отфильтровывают, после чего маточный раствор концентрируют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (3,02 г).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,46 (с, 9Н), 1,49 (с, 9Н), 1,68 (д, 3Н, J= 7,1 Гц), 2,98 (ушир. с, 6Н), 4,25 (кв, 1Н, J=7,1 Гц), 4,26 (ушир.с, 1Н), 4,85 (ушир.с, 1Н), 6,09 (с, 1Н), 6,98-7,23 (м, 2Н), 7,28-7,54 (м, 6Н).
ИК (чистый) [см-1]: 2978, 1722, 1680, 1602, 1485, 1417.
MS (FD) [m/e]: 566 (М+).
Пример 12
(трет-Бутоксикарбонил)-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -{ морфолин-1-ил-[(трет-бутоксикарбонил)имино] метил} амин (схема 15, приведенная в конце описания).
Тем же способом, что и по примеру 11, из соединения, полученного по ссылочному примеру 7, и соединения, полученного по ссылочному примеру 13, получают желаемое соединение.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,46 (с, 9Н), 1,48 (с, 9Н), 1,68 (д, 3Н, J= 7,2 Гц), 3,41-3,80 (ушир.м, 8Н), 4,23 (ушир.с, 1Н), 4,24 (кв, 1Н, J=7,2 Гц), 4,87 (ушир.с, 1Н), 6,06 (с, 1Н), 6,98-7,10 (м, 2Н), 7,30-7,63 (м, 6Н).
ИК (чистый) [см-1]: 2978, 1723, 1683, 1595, 1484, 1111.
MS (FD) [m/e]: 608 (М+).
Пример 13
(трет-Бутоксикарбонил)-{ 5-[1-(2-фторбифенил-4-ил)этил] -изоксазол-3-илметил} -{ пиперидин-1-ил[(трет-бутоксикарбонил)-имино] метил}амин (схема 16, приведенная в конце описания).
Из соединения, полученного по ссылочному примеру 7, и соединения, полученного по ссылочному примеру 12, получают желаемое соединение тем же способом, что и по примеру 11, за исключением того, что используют трифенилфосфин и диэтилазодикарбоксилат вместо трибутилфосфина и 1,1'-(азодикарбонил)дипиперидин.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,41-1,54 (м, 6Н), 1,46 (с, 9Н), 1,49 (с, 9Н), 1,68 (д, 3Н, J=7,3 Гц), 3,19 (ушир.с, 1Н), 3,35 (ушир.с, 2Н), 3,77 (ушир.с, 1Н), 4,22 (ушир.с, 1Н), 4,26 (кв, 1Н, J=7,3 Гц), 4,90 (ушир.с, 1Н), 6,12 (с, 1Н), 6,99-7,11 (м, 2Н), 7,33-7,54 (м, 6Н).
Пример 14
N, N'-Ди(трет-бутоксикарбонил)-N''-{ 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N-метилгуанидин (схема 17, приведенная в конце описания).
Соединение (1,50 г), полученное по ссылочному примеру 10, и соединение (2,00 г), полученное по ссылочному примеру 14, растворяют в ацетонитриле (50 мл), и добавляют триэтиламин (1,54 г), после чего при охлаждении льдом прибавляют по каплям нитрат серебра (2,58 г) в ацетонитриле (20 мл) в течение 30 минут и полученную смесь перемешивают при комнатной температуре в течение 2 дней. Нерастворимые продукты отфильтровывают и промывают ацетонитрилом, после чего маточный раствор концентрируют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (2,54 г).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,46 (с, 9Н), 1,48 (с, 9Н), 1,69 (д, 3Н, J= 7,1 Гц), 3,10 (с, 3Н), 4,26 (кв, 1Н, J=7,1 Гц), 4,49 (с, 2Н), 6,04 (с, 1Н), 7,01-7,11 (м, 2Н), 7,32-7,53 (м, 6Н).
Пример 15
1-(трет-Бутоксикарбонил)-2-[(трет-бутоксикарбонил)имино]-3-{5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил} -имидазолидин-4-он (схема 18, приведенная в конце описания).
Тем же способом, что и по примеру 14, из соединения, полученного по ссылочному примеру 10, и соединения, полученного по ссылочному примеру 15, получают желаемое соединение.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,51 (с, 9Н), 1,52 (с, 9Н), 1,67 (д, 3Н, J=7,3 Гц), 4,24 (кв, 1Н, J=7,3 Гц), 4,25 (с, 2Н), 4,81 (с, 2Н), 6,08 (д, 1Н, J=1,0 Гц), 7,02-7,11 (м, 2Н), 7,33-7,55 (м, 6Н).
ИК (КВr) [см-1]: 2980, 1740, 1708, 1659, 1368.
Элементный анализ:
Вычислено: С 64,35; Н 6,10; N 9,68.
Найдено: С 64,02; Н 6,24; N 9,60.
Пример 16
N-({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-иламино}-метиламинометилен)-4-метилбензолсульфонамид (схема 19, приведенная в конце описания).
5-[1-(2-Фторбифенил-4-ил)этил] изоксазол-3-иламин (1,41 г), хорошо известное соединение, при охлаждении льдом прибавляют к раствору N-дихлорметилен-4-метилбензолсульфонамида (Chem. Ber., 992900(1966)) (1,33 г) в ацетонитриле (40 мл). Через 30 минут медленно по каплям прибавляют триэтиламин (0,73 мл) и полученную смесь перемешивают при охлаждении льдом еще 1 час. Прибавляют по каплям метиламин (2 мл 40%-ного этанольного раствора) и перемешивают 1 час с последующей экстракцией. Экстракт очищают колоночной хроматографией на силикагеле с получением желаемого соединения (735 мг).
Точка плавления 125-127oС.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,70 (д, 3Н, J=7,3 Гц), 2,39 (с, 3Н), 2,95 (д, 3Н, J= 4,6 Гц), 4,22 (кв, 1Н, J=7,3 Гц), 5,87 (д, 1Н, J=0,7 Гц), 7,01-7,11 (м, 2Н), 7,25 (д, 2Н, J=8,4 Гц), 7,34-7,55 (м, 6Н), 7,80 (д, 2Н, J=8,4 Гц), 7,97 (м, 1Н), 10,12 (с, 1Н).
Пример 17
N-{3-[1-(2-Фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидин (схема 20, приведенная в конце описания).
Соединение (500 мг), полученное по ссылочному примеру 1, растворяют в N, N-диметилформамиде (2 мл), и добавляют ацетат аммония (5,00 г), после чего полученную смесь перемешивают при 120oС и в течение 1,5 часов пропускают газообразный аммиак. К реакционной смеси прибавляют насыщенный хлорид натрия с последующей экстракцией этилацетатом и продукты экстракции промывают водой и сушат. Растворитель отгоняют при пониженном давлении и нерастворимые продукты очищают колоночной хроматографией на силикагеле с получением желаемого соединения (316 мг).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,54 (д, 3Н, J=7,1 Гц), 4,08 (кв, 1Н, J=7,1 Гц), 5,32 (с, 1Н), 6,02 (ушир.с, 4Н), 7,21-7,25 (м, 2Н), 7,38-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3449, 3345, 3106, 1657, 1614, 1562, 1472, 1414.
Пример 18
Гидрохлорид N-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-метилгуанидина (схема 21, приведенная в конце описания).
Соединение (600 мг), полученное по ссылочному примеру 1, растворяют в N, N-диметилформамиде (5 мл) и затем прибавляют раствор метиламин-вода-уксусная кислота, полученный из 40%-ного водного раствора метиламина (1,31 г) и уксусной кислоты (10 мл), и полученную смесь перемешивают при 120oС в течение 30 минут. К реакционной смеси прибавляют хлороформ (50 мл) и 5М водный раствор гидроксида натрия (300 мл) с последующей экстракцией хлороформом и экстракционный раствор промывают водой и сушат. Растворитель отгоняют при пониженном давлении и нерастворимые продукты очищают колоночной хроматографией на силикагеле и обрабатывают раствором гидрохлорида в изопропаноле с получением желаемого соединения (367 мг).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,2 Гц), 2,85 (с, 3Н), 4,12 (кв, 1H, J=7,2 Гц), 5,19 (с, 1Н), 5,30 (ушир.с, 2Н), 5,59 (ушир.с, 1H), 7,04-7,15 (м, 2Н), 7,33-7,53 (м, 6Н).
ИК (КВr) [см-1]: 3144, 1680, 1637, 1484, 1417.
Пример 19
Гидрохлорид N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N,N-диметилгуанидина (схема 22, приведенная в конце описания).
Соединение (1,68 г), полученное по примеру 1, растворяют в метиленхлориде (20 мл) и затем прибавляют трифторуксусную кислоту (12 мл) и полученную смесь перемешивают при комнатной температуре в течение 2 часов и растворитель отгоняют при пониженном давлении. Остаток растворяют в метиленхлориде и обрабатывают раствором гидрохлорида в диэтиловом эфире с получением желаемого соединения (1,39 г).
Точка плавления 73-81oС (разл.).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,61 (д, 3Н, J=7,0 Гц), 3,08 (с, 6Н), 4,29 (кв, 1H, J=7,0 Гц), 6,04 (с, 1Н), 7,26-7,34 (м, 2Н), 7,37-7,55 (м, 6Н), 8,27 (ушир.с, 2Н).
ИК (КВr) [см-1]: 3132, 1673, 1634, 1484, 1417.
Пример 20
Гидрохлорид N-этил-N'-{ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-ил} гуанидин (схема 23, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 2.
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,31 (т, 3Н, J=7,1 Гц), 1,60 (д, 3Н, J= 7,3 Гц), 3,31 (кв, 2H, J=7,1 Гц), 4,29 (кв, 1H, J=7,3 Гц), 6,17 (с, 1H), 7,24-7,52 (м, 8Н), 8,10-8,70 (ушир., 2H), 8,45-8,65 (ушир., 1H), 11,30-11,65 (ушир., 1H).
ИК (КВr) [см-1]: 3600-2400, 2980, 1675, 1623, 1580, 1482, 1415, 1131.
Пример 21
Гидрохлорид ({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}пиперидин-1-илметил)амин (схема 24, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 3.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,55-1,75 (м, 9Н), 3,52 (ушир., 4Н), 4,15 (кв, 1H, J=7,3 Гц), 5,71 (с, 1Н), 7,02-7,12 (м, 2Н), 7,31-7,50 (м, 6Н), 8,30 (ушир., 2Н), 11,20 (ушир., 1H).
ИК (КВr) [см-1]: 3600-2500, 2945, 1660, 1633, 1538, 1484, 1447, 1418.
Пример 22
Гидрохлорид ({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}морфолин-4-илметил)амина (схема 25, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 4.
Точка плавления 174-176oС (разл.).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,60 (д, 3Н, J=7,1 Гц), 3,56 (м, 4Н), 3,67 (м, 4Н), 4,28 (кв, 1Н, J=7,1 Гц), 6,02 (с, 1Н), 7,26-7,37 (м, 2Н), 7,38-7,54 (м, 6Н), 8,51 (ушир.с, 2Н).
Пример 23
Гидрохлорид (N'-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидино)уксусной кислоты (схема 26, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 5.
Точка плавления 62oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,54 (д, 3Н, J=7,1 Гц), 3,85 (д, 2Н, J= 5,6 Гц), 4,10 (кв, 1Н, J=7,1 Гц), 5,40 (с, 1Н), 6,19 (ушир.с, 2Н), 6,41 (т, 1Н, J=5,6 Гц), 7,21-7,24 (м, 2Н), 7,36-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3142, 2978, 1684, 1624, 1484, 1411.
Пример 24
Гидрохлорид 2-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}-1-метилимидазолидин-4-он (схема 27, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 6.
Точка плавления 158-160oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 3,07 (с, 3Н), 3,97 (с, 2Н), 4,16 (кв, 1Н, J=7,1 Гц), 5,41 (с, 1Н), 7,05-7,15 (м, 2Н), 7,32-7,54 (м, 6Н), 8,91 (ушир.с, 1Н).
ИК (КВr) [см-1]: 3153, 2972, 1761, 1668, 1603, 1578, 1484, 1452, 1418.
Пример 25
Гидрохлорид (N'-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}гуанидино)уксусной кислоты (схема 28, приведенная в конце описания).
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 7.
Точка плавления 144-146oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,26 (т, 3Н, J=7,1 Гц), 1,65 (д, 3Н, J= 7,3 Гц), 4,16-4,28 (м, 3Н), 4,38 (с, 2Н), 5,78 (с, 1H), 7,02-7,10 (м, 2Н), 7,32-7,56 (м, 6Н), 8,00-8,30 (м, 2Н).
ИК (КВr) [см-1]: 3088, 2981, 1736, 1684, 1650, 1589, 1485, 1413.
Пример 26
N-{ 5-[1-(2-Фторбифенил-4-ил)этил] изоксазол-3-илметил} -гуанидин (схема 29, приведенная в конце описания).
Соединение (1,24 г), полученное по примеру 10, растворяют в трифторуксусной кислоте (10 мл) и раствор перемешивают при комнатной температуре в течение 2 часов и затем растворитель отгоняют при пониженном давлении. Остаток растворяют в этилацетате и полученный раствор нейтрализуют 1 н. водным раствором гидроксида натрия, после чего органический слой выпаривают, промывают водой, сушат и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (562 мг).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,50 (д, 3Н, J=6,9 Гц), 4,12 (кв, 1Н, J=6,9 Гц), 4,42 (ушир.с, 2Н), 6,08 (с, 1Н), 6,90-6,97 (м, 2Н), 7,19-7,57 (м, 9Н), 8,21 (ушир.с, 1Н).
Пример 27
Гидрохлорид N'-{ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметил}-N, N-диметилгуанидина (схема 30, приведенная в конце описания).
Соединение (2,69 г), полученное по примеру 11, растворяют в растворе трифторуксусной кислоты (10 мл) и полученный раствор перемешивают при комнатной температуре в течение 2 часов. Растворитель отгоняют при пониженном давлении. Остаток растворяют в метиленхлориде и обрабатывают раствором гидрохлорида в диэтиловом эфире с получением желаемого соединения (897 мг).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,62 (д, 3Н, J=7,0 Гц), 3,00 (с, 6Н), 4,47 (кв, 1Н, J=7,0 Гц), 4,53 (д, 2Н, J=5,9 Гц), 6,40 (с, 1H), 7,22-7,28 (м, 2Н), 7,37-7,54 (м, 6Н), 7,69 (ушир.с, 2Н), 8,06 (т, 1H, J=5,9 Гц).
ИК (КВr) [см-1]: 3422, 3228, 1658, 1630, 1562, 1485, 1418.
Пример 28
Гидрохлорид ({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино} морфолин-4-илметил)амина (схема 31, приведенная в конце описания).
Тем же способом, что и по примеру 27, получают желаемое соединение, за исключением использования соединения, полученного по примеру 12.
Точка плавления 161-163oС.
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,63 (д, 3Н, J=7,3 Гц), 3,46 (м, 4Н), 3,64 (м, 4Н), 4,48 (кв, 1Н, J=7,3 Гц), 4,55 (д, 2Н, J=5,8 Гц), 6,42 (с, 1Н), 7,22-7,29 (м, 2Н), 7,37-7,54 (м, 6Н), 8,00 (ушир.с, 2Н), 8,43 (т, 1Н, J=5,8 Гц).
ИК (КВr) [см-1]: 3393, 3356, 1655, 1612, 1561, 1485, 1418, 1116.
Пример 29
Гидрохлорид ({ 5-[1-(2-фторбифенил-4-ил)этил] изоксазол-3-илметилимино} пиперидин-1-илметил)амина (схема 32, приведенная в конце описания).
Тем же способом, что и по примеру 27, получают желаемое соединение, за исключением использования соединения, полученного по примеру 13.
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,52 (ушир.с, 6Н), 1,62 (д, 3Н, J=7,3 Гц), 3,50 (ушир. с, 4Н), 4,47 (кв, 1Н, J=7,3 Гц), 4,53 (д, 2Н, J=5,6 Гц), 6,37 (с, 1Н), 7,21-7,27 (м, 2Н), 7,39-7,53 (м, 6Н), 7,81 (ушир.с, 2Н), 8,25 (ушир.с, 1Н).
Пример 30
Гидрохлорид N-{5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-илметил}-N'-метилгуанидина (схема 33, приведенная в конце описания).
Тем же способом, что и по примеру 27, получают желаемое соединение, за исключением использования соединения, полученного по примеру 14.
Точка плавления 71-74oС (разл.).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,68 (д, 3Н, J=7,3 Гц), 2,89 (д, 3Н, J= 4,6 Гц), 4,25 (кв, 1Н, J=7,3 Гц), 4,42 (ушир.с, 2Н), 6,17 (с, 1Н), 7,00-7,10 (м, 2Н), 7,36-7,54 (м, 6Н).
ИК (КВr) [см-1]: 3338, 1646, 1602, 1484, 1418.
Пример 31
Гидрохлорид 2-амино-3-{ 5-[1-(2-фторбифенил-4-ил)этил] -изоксазол-3-илметил}-3,5-дигидроимидазол-4-он (схема 34, приведенная в конце описания).
Тем же способом, что и по примеру 27, получают желаемое соединение, за исключением использования соединения, полученного по примеру 15.
Точка плавления 210-232oС (разл.).
1H-ЯМР (270 МГц, d6-ДМСО) δ м.д.: 1,62 (д, 3Н, J=7,1 Гц), 4,31 (с, 2Н), 4,47 (кв, 1Н, J= 7,1 Гц), 4,94 (с, 2Н), 6,45 (с, 1Н), 7,21-7,29 (м, 2Н), 7,37-7,55 (м, 6Н), 9,53 (ушир.с, 3Н).
ИК (КВr) [см-1]: 3061, 2983, 1778, 1706, 1689, 1604, 1544, 1485, 1419.
Пример 32
Метил [2-(N'-(трет-бутоксикарбонил)-N''-{3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)этокси] ацетат (схема 35, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования соли трифторуксусной кислоты (2-аминоэтокси)ацетата.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,49 (с, 9Н), 1,67 (д, 3Н, J=7,3 Гц), 3,59-3,64 (м, 2Н), 3,70-3,76 (м, 2Н), 3,79 (с, 3Н), 4,11-4,18 (м, 1Н), 4,14 (с, 2Н), 5,30 (с, 1Н), 7,07-7,17 (м, 2Н), 7,32-7,46 (м, 4Н), 7,51-7,54 (м, 2Н), 8,28 (ушир.с, 1Н), 8,49 (ушир.с, 1Н).
ИК (чистый) [см-1] : 3399, 3349, 2978, 1750, 1732, 1634, 1606, 1556, 1486, 1455, 1416, 1370, 1241, 1151, 770, 670.
Пример 33
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-ил}изоксазол-5-ил)-N''-[2-(2-гидроксиэтоксиэтил)]гуанидин (схема 36, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования 2-(2-аминоэтокси)-этанола.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,49 (с, 9Н), 1,67 (д, 3Н, J=7,1 Гц), 2,40 (ушир.с, 1Н), 3,55-3,70 (м, 6Н), 3,70-3,80 (м, 2Н), 4,15 (кв, 1H, J=7,1 Гц), 5,32 (с, 1Н), 7,07-7,16 (м, 2Н), 7,32-7,54 (м, 6Н), 8,36 (ушир.с, 1H), 8,51 (ушир.с, 1H).
Пример 34
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-ил} изоксазол-5-ил)-N''-(2-гидроксиэтил)гуанидин (схема 37, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования 2-аминоэтанола.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,50 (с, 9Н), 1,67 (д, 3Н, J=7,1 Гц), 3,56-3,60 (м, 3Н), 3,77-3,82 (м, 2Н), 4,14 (кв, 1H, J=7,1 Гц), 5,34 (с, 1H), 7,06-7,16 (м, 2Н), 7,32-7,46 (м, 4Н), 7,51-7,54 (м, 2Н), 8,41 (ушир.с, 1H), 8,59 (ушир.с, 1H).
Пример 35
трет-Бутил [N'-(трет-бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N-(2-гидроксиэтил)гуанидино]ацетат (схема 38, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования трет-бутил 3-(2-гидроксиэтиламино)пропионата.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,33 (с, 9Н), 1,44 (с, 9Н), 1,64 (д, 3Н, J= 7,1 Гц), 3,55-3,65 (м, 2Н), 3,74-3,82 (м, 2Н), 3,86-3,94 (м, 1Н), 4,02-4,17 (м, 3Н), 5,30 (с, 1Н), 7,04-7,15 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,53 (м, 2Н).
ИК (КВr) [см-1]: 3254, 2979, 2936, 1738, 1614, 1484, 1459, 1418, 1369, 1249, 1152, 1060, 769, 699.
Пример 36
4-[(трет-Бутоксикарбамоил)-{ 3-[1-(2-фторбифенил-4-ил)-этил] изоксазол-5-илимино}метил]морфолин-3-ол (схема 39, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования пиперидин-2-ола.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,48 (с, 9Н), 1,66 (д, 3Н, J=7,0 Гц), 3,44-4,00 (м, 6Н), 4,10-4,25 (м, 1Н), 5,32 (с, 1Н), 6,47 (ушир.с, 0,5Н), 6,66 (ушир. с, 0,5Н), 6,91-6,96 (м, 1Н), 7,07-7,16 (м, 2Н), 7,32-7,53 (м, 6Н).
Пример 37
(трет-Бутоксикарбонил)-({ 3-[1-(4-изобутилфенил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амин (схема 40, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 18.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,89 (д, 6Н, J=6,6 Гц), 1,44 (с, 9Н), 1,62 (д, 3Н, J= 7,3 Гц), 1,83 (м, 1Н, J=6,6 Гц), 2,42 (д, 2Н, J=7,3 Гц), 3,54-3,58 (м, 4Н), 3,72-3,77 (м, 4Н), 4,09 (кв, 1H, J=7,2 Гц), 5,23 (с, 1Н), 7,05-7,09 (м, 2Н), 7,17-7,20 (м, 2Н).
Пример 38
(трет-Бутоксикарбонил)-({ 3-[1-(6-метоксинафталин-2-ил)-этил]изоксазол-5-илимино}морфолин-4-илметил)амин (схема 41, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 19.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,35 (с, 9Н), 1,72 (д, 3Н, J=7,2 Гц), 3,54-3,56 (м, 4Н), 3,71-3,75 (м, 4Н), 3,91 (с, 3Н), 4,25 (кв, 1H, J=7,1 Гц), 5,21 (с, 1Н), 7,10-7,14 (м, 2Н), 7,37 (дд, 1H, J=8,2, 1,5 Гц), 7,66-7,70 (м, 3Н).
Пример 39
Метансульфонат N'-{3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-ил}-N,N-диэтилгуанидина (схема 42, приведенная в конце описания).
Соединение (5,0 г), полученное по ссылочному примеру 2, растворяют в ацетонитриле (100 мл) и прибавляют триэтиламин (3,8 мл), после чего по каплям при охлаждении льдом добавляют 40%-ный водный раствор диметиламина (2,84 мл). Затем прибавляют по каплям раствор нитрата серебра (2,05 г) в ацетонитриле (10 мл) и полученную смесь перемешивают при комнатной температуре в течение 18 часов. Нерастворимые продукты отфильтровывают, после промывки хлороформом маточный раствор концентрируют при пониженном давлении. Остаток растворяют в 83%-ном растворе (по объему) водной трифторуксусной кислоты (100 мл) и раствор перемешивают при комнатной температуре в течение 8 часов, после чего растворитель удаляют азеотропной отгонкой, используя толуол. К остатку прибавляют насыщенный водный раствор бикарбоната натрия и полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 4/1). Очищенный продукт растворяют в 1,4-диоксане и обрабатывают метансульфоновой кислотой (0,56 мл) с получением желаемого соединения (3,42 г).
Точка плавления 154-155oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,21 (т, 6Н, J=7,1 Гц), 1,66 (д, 3Н, J= 7,1 Гц), 2,70 (с, 3Н), 3,42 (кв, 4Н, J=7,1 Гц), 4,17 (кв, 1Н, J=7,1 Гц), 5,69 (с, 1Н), 7,02-7,13 (м, 2Н), 7,26-7,54 (м, 6Н), 8,24 (ушир.с, 2Н), 10,83 (ушир.с, 1Н).
Пример 40
Метансульфонат N'-{3-[l-(2-фтopбифeнил-4-ил)этил]-изоксазол-5-ил}-N,N-бис(2-метоксиэтил)гуанидина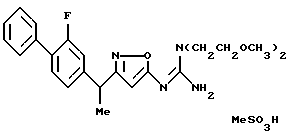
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования бис-(2-метоксиэтил)-амина.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,68 (д, 3Н, J=7,1 Гц), 2,80 (с, 3Н), 3,43 (с, 6Н), 3,65-3,75 (м, 8Н), 4,23 (кв, 1Н, J=7,1 Гц), 6,04 (с, 1Н), 7,07-7,25 (м, 2Н), 7,32-7,54 (м, 6Н), 7,76 (ушир.с, 1Н), 8,00 (ушир.с, 2Н).
Пример 41
Метансульфонат ({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} пирролидин-1-илметил)амина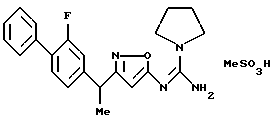
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования пирролидина.
Точка плавления 182-183oС (разл.).
1H-ЯМР (300 МГц, CD3OD) δ м.д.: 1,68 (д, 3Н, J=7,1 Гц), 2,04-2,15 (м, 4Н), 2,67 (с, 3Н), 3,50-3,65 (м, 4Н), 4,28 (кв, 1Н, J=7,1 Гц), 6,03 (с, 1Н), 7,14-7,26 (м, 2Н), 7,35-7,57 (м, 6Н).
Пример 42
Метансульфонат ({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}пиперазин-1-илметил)амина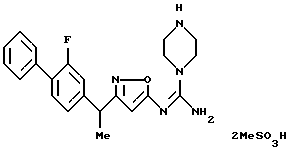
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования пиперазина.
Точка плавления 185oС (разл.).
1H-ЯМР (300 Мгц, CD3OD) δ м.д.: 1,68 (д, 3Н, J=7,1 Гц), 2,69 (с, 6Н), 3,40 (т, 4Н, J= 5,3 Гц), 3,86 (т, 4Н, J=5,3 Гц), 4,28 (кв, 1Н, J=7,1 Гц), 5,99 (с, 1Н), 7,13-7,25 (м, 2Н), 7,35-7,51 (м, 6Н).
Пример 43
Метансульфонат [{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-(4-метилпиперазин-1-ил)метил]амина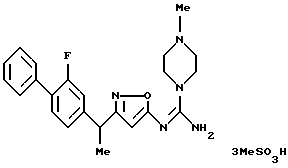
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования 1-метилпиперазина.
Точка плавления 186-187oС (разл.).
1H-ЯМР (300 МГц, СD3ОD) δ м.д.: 1,68 (д, 3Н, J=7,1 Гц), 2,69 (с, 9Н), 2,98 (с, 3Н), 3,31 (ушир.с, 2Н), 3,64 (ушир.с, 4Н), 4,15 (ушир.с, 2Н), 4,28 (кв, 1Н, J=7,1 Гц), 6,00 (с, 1Н), 7,13-7,25 (м, 2Н), 7,32-7,52 (м, 6Н).
Пример 44
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-(2-морфолин-4-илэтил)гуанидин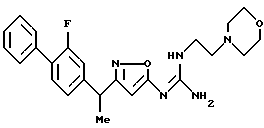
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования 2-морфолин-4-илэтиламина.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,3 Гц), 2,49-2,57 (м, 6Н), 3,30-3,31 (м, 2Н), 3,69 (т, 4Н, J=4,3 Гц), 4,41 (кв, 1H, J=7,3 Гц), 5,18 (с, 1H), 5,70 (с, 1Н), 6,13 (с, 2Н), 7,07-7,17 (м, 2Н), 7,32-7,54 (м, 6Н).
Пример 45
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-метоксиэтил)гуанидин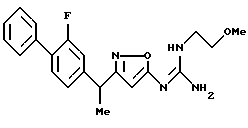
Тем же способом, что и по примеру 39, получают желаемое соединение, за исключением использования 2-метоксиэтиламина.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,3 Гц), 3,38 (с, 3Н), 3,41 (м, 2Н), 3,52 (т, 2Н, J=4,3 Гц), 4,14 (кв, 1H, J=7,3 Гц), 5,19 (с, 1H), 5,50-5,70 (м, 3Н), 7,08-7,16 (м, 2Н), 7,33-7,54 (м, 6Н).
Пример 46
Гидрохлорид ({3-[1-(4-изобутилфенил)этил]изоксазол-5-илимино}морфолин-4-илметил)амина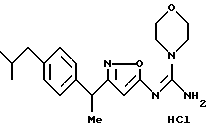
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 37.
Точка плавления 94-99oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,89 (д, 6Н, J=6,6 Гц), 1,60 (д, 3Н, J= 7,1 Гц), 1,78-1,88 (м, 1Н), 2,43 (д, 2Н, J=7,1 Гц), 3,55-3,62 (м, 4Н), 3,72-3,80 (м, 4Н), 4,09 (кв, 1Н, J=7,1 Гц), 5,65 (с, 1Н), 7,08 (д, 2Н, J=8,3 Гц), 7,14 (д, 2Н, J=8,1 Гц), 8,38 (ушир.с, 1Н).
Пример 47
Гидрохлорид ({ 3-[1-(6-Метоксинафталин-2-ил)этил]изоксазол-5-илимино}-морфолин-4-илметил)амина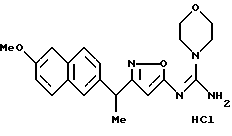
Тем же способом, что и по примеру 19, получают желаемое соединение, за исключением использования соединения, полученного по примеру 38.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,70 (д, 3Н, J=7,1 Гц), 3,44-3,48 (м, 4Н), 3,69-3,73 (м, 4Н), 3,91 (с, 3Н), 4,24 (кв, 1Н, J=7,2 Гц), 5,21 (с, 1Н), 5,31 (ушир.с, 1Н), 7,10-7,13 (м, 2Н), 7,39 (д, 1Н, J=8,6 Гц), 7,66-7,70 (м, 3Н).
Пример 48
Метил [2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)этокси]ацетат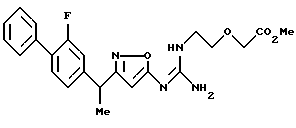
Трифторусусную кислоту (15,0 мл) прибавляют к соединению (5,74 г), полученному по примеру 32, и полученную смесь перемешивают при комнатной температуре в течение одного часа. К реакционной смеси прибавляют насыщенный водный раствор бикарбоната натрия и раствор затем подвергают экстракции этилацетатом, после чего органический слой сушат над сульфатом магния и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (один хлороформ --> хлороформ/метанол = 99/1 --> 39/1) с получением желаемого соединения (4,32 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,1 Гц), 3,44-3,51 (м, 2Н), 3,64-3,67 (м, 2Н), 3,74 (с, 3Н), 4,10 (с, 2Н), 4,10-4,16 (м, 1Н), 5,20 (с, 1Н), 5,60 (ушир.с, 2Н), 6,07 (ушир.с, 1Н), 7,07-7,17 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
ИК (чистый) [см-1] : 3374, 2952, 1749, 1624, 1572, 1483, 1457, 1222, 1132, 969, 915, 769, 729, 699.
Пример 49
N-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-[2-(2-гидроксиэтоксиэтил)]гуанидин
Трифторусусную кислоту (10 мл) прибавляют к соединению (5,09 г), полученному по примеру 33, и полученную смесь перемешивают при комнатной температуре в течение одного часа. Реакционную смесь подвергают азеотропной отгонке с использованием толуола для удаления растворителя и остаток затем растворяют в 1,4-диоксане, после чего раствор обрабатывают 4 н. раствором гидрохлорида в этилацетате и затем концентрируют при пониженном давлении. Концентрированный раствор разбавляют хлороформом, затем нейтрализуют водным раствором гидроксида натрия и затем подвергают экстракции хлороформом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (один хлороформ --> хлороформ/метанол = 30/1) с получением желаемого соединения (3,34 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,0 Гц), 3,42-3,48 (м, 2Н), 3,57-3,66 (м, 4Н), 3,73-3,78 (м, 2Н), 4,13 (кв, 1H, J=7,1 Гц), 5,55 (с, 1Н), 5,69 (ушир.с, 2Н), 7,07-7,16 (м, 2Н), 7,31-7,55 (м, 6Н).
Пример 50
N-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-гидроксиэтил)гуанидин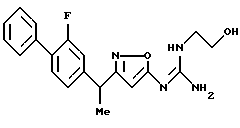
Тем же способом, что и по примеру 49, получают желаемое соединение, за исключением использования соединения, полученного по примеру 34.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,62 (д, 3Н, J=7,1 Гц), 3,28-3,36 (м, 2Н), 3,62-3,66 (м, 2Н), 4,13 (кв, 1Н, J=7,3 Гц), 5,33 (с, 1Н), 7,10-7,21 (м, 2Н), 7,30-7,44 (м, 6Н), 7,49-7,52 (м, 2Н).
ИК (КВr) [см-1]: 3433, 1639, 1572, 1478, 1456, 1417, 1068, 786, 695.
MS (FD) [m/e]: 368 (М+).
Пример 51
({ 3-[1-(2-Фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино}морфолин-4-илметил)амин (схема 43, приведенная в конце описания).
Соединение (4,57 г), полученное по ссылочному примеру 20, растворяют в цианоморфолине (8,64 г) и прибавляют карбонат калия (4,26 г), после чего полученную смесь нагревают с обратным холодильником при 130oС в течение 8 часов. После охлаждения до комнатной температуры прибавляют насыщенный водный раствор хлорида натрия, после чего полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 2/1 --> 1/2) с получением желаемого соединения (1,53 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,71 (с, 6Н), 3,47-3,50 (м, 4Н), 3,71-3,74 (м, 4Н), 5,19 (с, 1Н), 5,39 (с, 2Н), 7,11-7,20 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 52
(Морфолин-4-ил-{3-[1-(2-феноксифенил)этил]изоксазол-5-илимино}метил)амин (схема 44, приведенная в конце описания).
Тем же способом, что и по примеру 51, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 25.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,61 (д, 3Н, J=7,3 Гц), 3,48 (т, 4Н, J= 4,9 Гц), 3,72 (т, 4Н, J=4,9 Гц), 4,08 (кв, 1Н, J=7,3 Гц), 5,21 (с, 1Н), 5,37 (ушир.с, 2Н), 6,80-6,84 (м, 1Н), 6,97-7,12 (м, 5Н), 7,21-7,35 (м, 3Н).
Пример 53
Метансульфонат ({ 3-[1-этокси-1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илимино}морфолин-4-илметил)амин (схема 45, приведенная в конце описания).
Соединение (5,0 г), полученное по ссылочному примеру 21, растворяют в цианоморфолине (7,75 г) и прибавляют карбонат калия (4,24 г), после чего смесь нагревают с обратным холодильником при 130oС в течение 8 часов. После охлаждения до комнатной температуры прибавляют насыщенный водный раствор хлорида натрия, и затем полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом магния и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 2/1 --> 1/2). Очищенный раствор растворяют в 1,4-диоксане и при охлаждении льдом прибавляют метансульфоновую кислоту (0,34 мл) и полученную смесь концентрируют при пониженном давлении. Сырой продукт очищают методом перекристаллизации из изопропанола с получением желаемого соединения (850 мг).
Точка плавления 158-160oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,71 (т, 3Н, J=6,7 Гц), 1,90 (с, 3Н), 2,71 (с, 3Н), 3,32-3,57 (м, 6Н), 3,73-3,75 (м, 4Н), 5,68 (с, 1Н), 7,22-7,54 (м, 8Н), 8,69 (ушир.с, 2Н), 11,16 (ушир.с, 1Н).
Пример 54
(R)-({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин (схема 46, приведенная в конце описания).
1) Гидрид натрия (25 мг, 60%-ный в масле) прибавляют к тетрагидрофурановому раствору (4 мл) соединения (118 мг, 93% е.е. (энантиомерная чистота - пер.)), полученного по ссылочному примеру 26, в атмосфере азота и затем полученную смесь перемешивают при 40oС в течение 10 минут. Вновь охлаждают льдом и затем прибавляют цианморфолин (0,084 мл), после чего доводят опять до комнатной температуры перемешивают в течение 6 часов. Реакционную смесь разбавляют этилацетатом и затем нейтрализуют насыщенным водным раствором хлорида аммония. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 1/1 --> 1/4) с получением желаемого соединения (137 мг, 93% е.е.).
2) ({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амин (3 г)разделяют с использованием препаративной оптически активной колонки (CHIRALCEL OD, зарегистрированная торговая марка DAICEL CHEMICAL INDUSTRIES, LTD., 2 см⊘ • 25 см) с получением желаемого соединения (1,5 г).
Условия разделения:
Элюент: гексан/этанол = =100/15.
длина волны наблюдения: 254 нм.
Скорость потока: 20 мл/мин.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 3,45-3,60 (м, 4Н), 3,70-3,80 (м, 4Н), 4,15 (кв, 1Н, J=7,1 Гц), 5,25 (с, 1Н), 5,37 (ушир.с, 2Н), 7,05-7,17 (м, 2Н), 7,33-7,54 (м, 6Н).
[α]D 22=-20,0o (с: 1,00, СНСl3).
Пример 55
(S)-({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин (схема 47, приведенная в конце описания).
1) Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 27.
2) Выделение осуществляют тем же способом, что и по примеру 54, с получением желаемого соединения.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 3,45-3,55 (м, 4Н), 3,65-3,75 (м, 4Н), 4,15 (кв, 1Н, J=7,1 Гц), 5,25 (с, 1Н), 5,38 (ушир.с, 2Н), 7,05-7,17 (м, 2Н), 7,33-7,54 (м, 6Н).
[α]D 22=+19,8o (с: 1,00, СНСl3).
Пример 56
({ 3-[1-(2-Фтop-2',3',4',5',6'-пентадейтеробифенил-4-ил)этил]изоксазол-5-илимино}морфолин-4-илметил)амин (схема 48, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 29.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 3,47-3,51 (м, 4Н), 3,71-3,75 (м, 4Н), 4,15 (кв, 1Н, J=7,1 Гц), 5,25 (с, 1Н), 5,37 (ушир.с, 2Н), 7,07-7,17 (м, 2Н), 7,37 (т, 1Н, J=8,1 Гц).
ИК (КВr) [см-1]: 3454, 3360, 2971, 1629, 1578, 1548, 1444, 1277, 1124, 1110, 975, 872.
Пример 57
({ 3-[1-(2-Фтор-2'-метоксибифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амин (схема 49, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 30.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,2 Гц), 3,47-3,50 (м, 4Н), 3,71-3,75 (м, 4Н), 3,80 (с, 3Н), 4,15 (кв, 1H, J=7,2 Гц), 5,27 (с, 1H), 5,34 (ушир.с, 2Н), 6,97-7,13 (м, 4Н), 7,23-7,38 (м, 3Н).
Пример 58
({ 3-[1-(2'-Фторбифенил-4-ил)этил] изоксазол-5-илимино}-морфолин-4-илметил)амин (схема 50, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 31.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,1 Гц), 3,48 (т, 4Н, J= 4,8 Гц), 3,72 (т, 4Н, J=4,8 Гц), 4,16 (кв, 1H, J=7,1 Гц), 5,25 (с, 1H), 5,34 (ушир.с, 2Н), 7,10-7,51 (м, 8Н).
Пример 59
({ 3-[1-(2-Фторбифенил-4-ил)циклопропил]изоксазол-5-илимино}морфолин-4-илметил)амин (схема 51, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 22.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,31-1,34 (м, 2Н), 1,46-1,51 (м, 2Н), 3,47 (т, 4Н, J=4,8 Гц), 3,73 (т, 4Н, J=4,8 Гц), 5,17 (с, 1Н), 5,35 (ушир.с, 2Н), 7,14-7,25 (м, 2Н), 7,33-7,55 (м, 6Н).
Пример 60
[(3-Бифенил-4-илметилизоксазол-5-илимино)морфолин-4-илметил] амин (схема 52, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 28.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 3,48 (т, 4Н, J=5,3 Гц), 3,72 (т, 4Н, J= 5,3 Гц), 3,94 (с, 2Н), 5,24 (с, 1Н), 5,34 (с, 2Н), 7,34-7,58 (м, 9Н).
Пример 61
{ [3-(1-Бифенил-4-илэтил)изоксазол-5-илимино] морфолин-4-илметил} амин (схема 53, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 23.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,3 Гц), 3,48 (т, 4Н, J= 4,3 Гц), 3,72 (т, 4Н, J=4,3 Гц), 4,16 (кв, 1Н, J=7,3 Гц), 5,24 (с, 1Н), 5,35 (с, 2Н), 7,30-7,58 (м, 9Н).
Пример 62
{[3-(1-Бифенил-4-ил-1-метилэтил)изоксазол-5-илимино]-морфолин-4-илметил} амин (схема 54, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 24.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,72 (с, 6Н), 3,47 (т, 4Н, J=5,3 Гц), 3,72 (т, 4Н, J=5,3 Гц), 5,18 (с, 1Н), 5,38 (с, 2Н), 7,32-7,58 (м, 9Н).
Пример 63
({ 3-[1-(2-Фтор-4'-метоксибифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амин (схема 55, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 32.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,2 Гц), 3,46-3,50 (м, 4Н), 3,70-3,74 (м, 4Н), 3,85 (с, 3Н), 4,13 (кв, 1Н, J=7,2 Гц), 5,25 (с, 1Н), 5,36 (ушир.с, 2Н), 6,94-7,00 (м, 2Н), 7,05-7,14 (м, 2Н), 7,33 (т, 1Н, J=8,0 Гц), 7,43-7,49 (м, 2Н).
Пример 64
4'-{ 1-[5-(Аминоморфолин-4-илметиленамино)изоксазол-3-ил] этил}-2'-фторбифенил-4-ол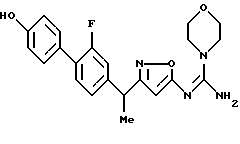
Соединение (5,16 г), полученное по примеру 63, растворяют в тетрагидрофуране (100 мл) в атмосфере азота и затем прибавляют раствор бортрибромида (1,6 мл) в метиленхлориде (40 мл) при -78oС, после чего температуру поднимают до комнатной температуры в течение одного часа и перемешивание затем продолжают при комнатной температуре в течение 3 часов. Реакционную смесь нейтрализуют 15%-ным водным раствором гидроксида натрия и затем подвергают экстракции этилацетатом и метанолом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Реакционную смесь очищают колоночной хроматографией на силикагеле (один хлороформ --> хлороформ/метанол = 50/1 --> 33/1) с получением желаемого соединения (2,67 г).
1H-ЯМР (300 МГц, d6-ДМСО) δ м.д.: 1,52 (д, 3Н, J=7,2 Гц), 3,38-3,44 (м, 4Н), 3,54-3,59 (м, 4Н), 4,06 (кв, 1Н, J=7,2 Гц), 5,39 (с, 1H), 6,43 (ушир.с, 2Н), 6,83 (д, 2Н, J= 8,3 Гц), 7,13-7,20 (м, 2Н), 7,30-7,40 (м, 3Н), 9,61 (ушир.с, 1Н).
ИК (КВr) [см-1] : 3335, 3190, 1660, 1568, 1497, 1448, 1274, 1114, 983, 827.
Пример 65
4'-{ 1-[5-(Аминоморфолин-4-илметиленамино)изоксазол-3-ил] этил}-2'-фторбифенил-2-ол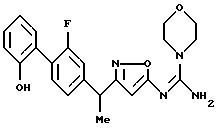
Тем же способом, что и по примеру 64, получают желаемое соединение, за исключением использования соединения, полученного по примеру 57.
1H-ЯМР (300 МГц, d6-ДМСО) δ м.д.: 1,57 (д, 3Н, J=7,1 Гц), 3,21-3,22 (м, 2Н), 3,46-3,51 (м, 4Н), 3,79-3,84 (м, 2Н), 4,21 (кв, 1H, J=7,1 Гц), 6,15 (с, 1Н), 6,84 (т, 1Н, J= 7,5 Гц), 6,91 (д, 1H, J=7,9 Гц), 7,12-7,21 (м, 4Н), 7,26-7,31 (м, 1Н), 9,53 (ушир.с, 1H).
ИК (КВr) [см-1]: 3275, 2964, 1659, 1605, 1493, 1451, 1419, 1358.
Пример 66.
Гидрохлорид N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-гидроксиэтоксиэтил)гуанидина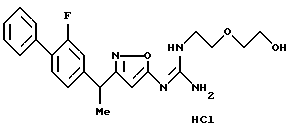
Соединение (3,34 г), полученное по примеру 49, растворяют в 1,4-диоксане и обрабатывают 4 н. соляной кислотой с получением желаемого соединения (521 мг).
Точка плавления 127-128oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,68 (д, 3Н, J=7,3 Гц), 3,48-3,54 (м, 2Н), 3,54-3,62 (м, 2Н), 3,63-3,70 (м, 4Н), 4,27 (кв, 1H, J=7,1 Гц), 5,98 (с, 1Н), 7,12-7,24 (м, 2Н), 7,31-7,52 (м, 6Н).
ИК (КВr) [см-1]: 3223, 3121, 2934, 1684, 1644, 1616, 1582, 1532, 1484, 1418, 1353, 1267, 1137, 1108, 1064, 698.
MS (FD) [m/e]: 413 (М-НСl).
Пример 67
Гидрохлорид N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-[(2-гидроксиэтил)]гуанидина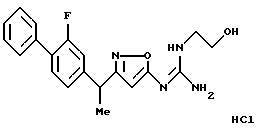
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 50.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,59 (д, 3Н, J=7,1 Гц), 3,47-3,58 (м, 2Н), 3,70-3,83 (м, 2Н), 4,13 (кв, 1Н, J=7,0 Гц), 5,78 (с, 1Н), 7,00-7,07 (м, 2Н), 7,31-7,49 (м, 6Н), 7,98 (ушир.с, 1Н).
Пример 68
Гидрохлорид 4'-{ 1-[5-(аминоморфолин-4-илметиленамино)-изоксазол-3-ил] этил}-2'-фторбифенил-4-ол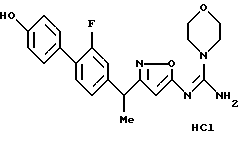
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 64.
Точка плавления 195-210oС (разл.).
1H-ЯМР (300 МГц, d6-ДМСО) δ м.д.: 1,58 (д, 3Н, J=7,2 Гц), 3,40-3,67 (м, 8Н), 4,24 (кв, 1Н, J=7,3 Гц), 5,99 (с, 1Н), 6,84 (д, 2Н, J=8,4 Гц), 7,19-7,45 (м, 5Н), 8,49 (ушир.с, 2Н), 9,67 (ушир.с, 1Н).
ИК (КВr) [см-1]: 3215, 3114, 1647, 1614, 1532, 1495, 1418, 1272, 1116, 820.
Элементный анализ:
Вычислено: С 59,13; Н 5,41; N 12,54.
Найдено: С 59,05; Н 5,26; N 12,47.
Пример 69
Гидрохлорид N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин~4-илэтил)гуанидина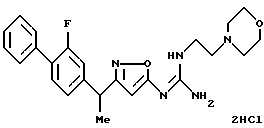
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 44.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,69 (д, 3Н, J=7,3 Гц), 3,43-3,48 (м, 6Н), 3,86 (т, 2Н, J=7,3 Гц), 3,90-4,10 (ушир.с, 6Н), 4,30 (кв, 1Н, J=7,3 Гц), 6,08 (с, 1H), 7,15-7,25 (м, 2Н), 7,36-7,53 (м, 6Н).
Пример 70
Гидрохлорид N-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-(2-метоксиэтил)]гуанидина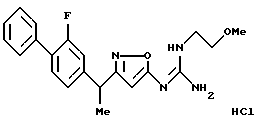
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 45.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,65 (д, 3Н, J=7,3 Гц), 3,39 (с, 3Н), 3,52 (т, 2Н, J= 4,6 Гц), 3,62 (т, 2Н, J=4,6 Гц), 4,28 (кв, 1H, J=7,3 Гц), 5,98 (с, 1Н), 7,15-7,35 (м, 2Н), 7,38-7,52 (м, 6Н).
Пример 71
Гидрохлорид 2-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-1-(2-гидроксиэтил)]имидазолидин-4-она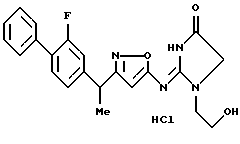
Соединение (3,3 г), полученное по примеру 35, растворяют в тетрагидрофуране (30 мл) и прибавляют концентрированную соляную кислоту, после чего раствор перемешивают при комнатной температуре в течение 30 минут. Реакционную смесь концентрируют при пониженном давлении и очищают методом перекристаллизации из толуола с получением желаемого соединения (1,4 г).
Точка плавления 159-167oС.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,73 (д, 3Н, J=7,3 Гц), 3,71-3,76 (м, 2Н), 3,82-3,86 (м, 2Н), 4,39 (кв, 1H, J=7,1 Гц), 4,53 (с, 2Н), 6,65 (с, 1H), 7,18-7,27 (м, 2Н), 7,35-7,52 (м, 6Н).
ИК (КВr) [см-1]: 3452, 3192, 2939, 1807, 1707, 1616, 1526, 1485, 1450, 1417, 1147, 1051, 697.
(MS) (FD) [m/e]: 444 (М+), 409 (М-НСl).
Пример 72
Метансульфонат ({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил]-изоксазол-5-илимино}морфолин-4-илметил)амина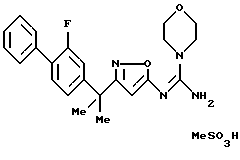
Соединение (1,53 г), полученное по примеру 51, растворяют в 1,4-диоксане и прибавляют при охлаждении льдом метансульфоновую кислоту (0,27 мл), после чего раствор перемешивают в течение 30 минут. Затем очищают методом перекристаллизации из 1,4-диоксана с получением желаемого соединения (1,89 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,71 (с, 6Н), 2,71 (с, 3Н), 3,45-3,52 (м, 4Н), 3,71-3,78 (м, 4Н), 5,51 (с, 1Н), 7,07 (дд, 1Н, J=12,3, 1,8 Гц), 7,13 (дд, 1Н, J= 8,3, 1,8 Гц), 7,34-7,46 (м, 4Н), 7,50-7,54 (м, 2Н), 8,64 (ушир.с, 2Н), 11,10 (ушир.с, 1Н).
Пример 73
Метансульфонат (морфолин-4-ил-{3-[1-(3-феноксифенил)этил]-изоксазол-5-илимино}метил)]амина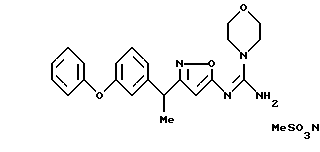
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 52.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,62 (д, 3Н, J=7,2 Гц), 2,72 (с, 3Н), 3,43-3,47 (м, 4Н), 3,72-3,76 (м, 4Н), 4,11 (кв, 1H, J=7,2 Гц), 5,53 (с, 1H), 6,83-7,01 (м, 5Н), 7,09-7,15 (м, 1Н), 7,23-7,37 (м, 3Н), 8,63 (ушир.с, 2Н), 11,10 (ушир.с, 1H).
Пример 74
Метансульфонат ({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амина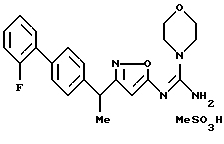
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 58.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,1 Гц), 2,73 (с, 3Н), 3,46-3,50 (м, 4Н), 3,72-3,76 (м, 4Н), 4,18 (кв, 1H, J=7,1 Гц), 5,58 (с, 1H), 7,11-7,61 (м, 8Н), 8,56 (ушир.с, 2Н).
Пример 75
Метансульфонат ({ 3-[1-(2-фторбифенил-4-ил)циклопропил] -изоксазол-5-илимино}морфолин-4-илметил)амина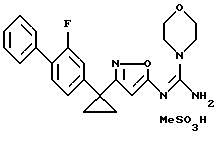
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 59.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,36-1,41 (м, 2Н), 1,47-1,52 (м, 2Н), 2,74 (с, 3Н), 3,46-3,50 (м, 4Н), 3,73-3,78 (м, 4Н), 5,50 (с, 1Н), 7,12-7,23 (м, 2Н), 7,33-7,48 (м, 4Н), 7,51-7,56 (м, 2Н), 8,61 (ушир.с, 2Н), 11,10 (ушир.с, 1Н).
Пример 76
Метансульфонат [(3-бифенил-4-илметилизоксазол-5-илимино)-морфолин-4-илметил]амина
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 60.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 2,69 (с, 3Н), 3,60 (т, 4Н, J=5,3 Гц), 3,77 (т, 4Н, J= 5,3 Гц), 4,02 (с, 2Н), 5,92 (с, 1Н), 7,32-7,45 (м, 5Н), 7,56-7,60 (м, 4Н)
Пример 77
Метансульфонат {[3-(1-бифенил-4-илэтил)изоксазол-5-илимино]морфолин-4-илметил}амина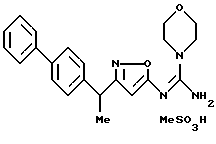
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 61.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,68 (д, 3Н, J=7,3 Гц), 2,69 (с, 3Н), 3,57 (т, 4Н, J= 4,3 Гц), 3,76 (т, 4Н, J=4,3 Гц), 4,23 (кв, 1Н, J=7,3 Гц), 5,91 (с, 1Н), 7,29-7,44 (м, 5Н), 7,57-7,60 (м, 4Н).
Пример 78
Метансульфонат { [3-(1-бифенил-4-ил-1-метилэтил)изоксазол-5-илимино] морфолин-4-илметил}амина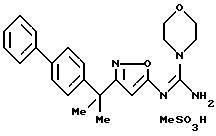
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 62.
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,75 (с, 6Н), 2,68 (с, 3Н), 3,58 (т, 4Н, J= 5,3 Гц), 3,76 (т, 4Н, J=5,3 Гц), 5,83 (с, 1Н), 7,32-7,45 (м, 5Н), 7,56-7,60 (м, 4Н).
Пример 79
Метансульфонат ({ 3-[1-(2-Фтор-4'-метоксибифенил-4-ил)-этил]изоксазол-5-илимино}морфолин-4-илметил)амина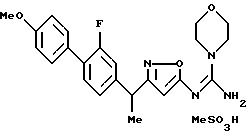
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 63.
Точка плавления 187-189oС (разл.).
1H-ЯМР (300 МГц, d6-ДМСО) δ м.д.: 1,59 (д, 3Н, J=7,0 Гц), 2,29 (с, 3Н), 3,40-3,53 (м, 4Н), 3,63-3,67 (м, 4Н), 3,78 (с, 3Н), 4,26 (кв, 1Н, J=7,2 Гц), 6,00 (с, 1H), 7,02 (д, 2Н, J=8,4 Гц), 7,19-7,30 (м, 2Н), 7,41-7,48 (м, 3Н), 8,40 (ушир.с, 2Н).
ИК (КВr) [см-1]: 3098, 1674, 1634, 1614, 1496, 1456, 1251, 1182, 1116, 1048, 825.
Элементный анализ:
Вычислено: С 55,37; Н 5,62; N 10,76.
Найдено: С 55,32; Н 5,60; N 10,77.
Пример 80
2-[N'-(трет-Бутоксикарбонил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)этокси]уксусная кислота (схема 56, приведенная в конце описания).
Соединение (52 мг), полученное по примеру 32, растворяют в тетрагидрофуране (1 мл) и прибавляют 5%-ный водный раствор гидроксида натрия (1 мл), после чего раствор перемешивают при комнатной температуре в течение 3 часов. К реакционной смеси прибавляют насыщенный водный раствор хлорида аммония и затем полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом магния и затем концентрируют при пониженном давлении. Реакционную смесь очищают колоночной хроматографией на силикагеле (хлороформ/метанол = 9/1) с получением желаемого соединения (25 мг).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,42 (с, 9Н), 1,62 (д, 3Н, J=7,1 Гц), 3,50-3,64 (м, 2Н), 3,65-3,75 (м, 2Н), 4,06 (с, 2Н), 4,06-4,14 (м, 1Н), 5,31 (с, 1Н), 7,05-7,13 (м, 2Н), 7,30-7,42 (м, 4Н), 7,48-7,51 (м, 2Н), 8,18 (ушир.с, 1Н), 8,44 (ушир.с, 1Н).
ИК (чистый) [см-1] : 3397, 3348, 2980, 2934, 1731, 1634, 1606, 1562, I486, 1455, 1418, 1370, 1242, 1150, 912, 770, 733, 699.
Пример 81
Натрий [2-(N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидино)этокси]ацетат (схема 57, приведенная в конце описания).
Соединение (4,32 г), полученное по примеру 48, растворяют в тетрагидрофуране (80 мл) и прибавляют 5%-ный водный раствор гидроксида натрия (80 мл), после чего раствор перемешивают при комнатной температуре в течение одного часа. Реакционную смесь концентрируют при пониженном давлении и затем фильтруют, после чего твердые продукты промывают этилацетатом и водой. Фильтрат концентрируют и затем твердые продукты опять отделяют фильтрацией и затем промывают этилацетатом и водой. Объединенные сырые продукты очищают методом перекристаллизации из воды с получением желаемого соединения (3,08 г).
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,63 (д, 3Н, J=7,1 Гц), 3,38-3,42 (м, 2Н), 3,56-3,60 (м, 2Н), 3,87 (с, 2Н), 4,13 (кв, 1Н, J=7,2 Гц), 5,35 (с, 1Н), 7,11-7,21 (м, 2Н), 7,30-7,43 (м, 4Н), 7,49-7,52 (м, 2Н).
R (чистый) [см-1]: 3429, 1573, 1453, 1430, 1330, 694.
Элементный анализ:
Вычислено: С 57,77; Н 5,07; N 12,25.
Найдено: С 57,86; Н 5,15; N 12,19.
Пример 82
Гидрохлорид (R)-({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амина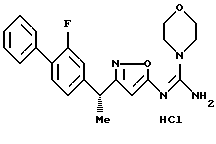
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 54.
Точка плавления 134-136oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,1 Гц), 3,45-3,65 (м, 4Н), 3,70-3,80 (м, 2Н), 4,15 (кв, 1Н, J=7,1 Гц), 5,69 (с, 1Н), 7,03-7,11 (м, 2Н), 7,33-7,52 (м, 6Н), 8,45 (ушир.с, 2Н), 11,31 (ушир.с, 1Н).
[α]D 22=-16,0o (с: 1,00, СНСl3).
Пример 83
Гидрохлорид (S)-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} морфолин-4-илметил)амина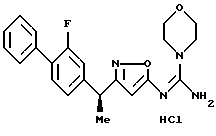
Тем же способом, что и по примеру 66, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
Точка плавления 134-136oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,3 Гц), 3,45-3,60 (м, 4Н), 3,60-3,80 (м, 4Н), 4,15 (кв, 1Н, J=7,3 Гц), 5,69 (с, 1Н), 7,02-7,12 (м, 2Н), 7,32-7,52 (м, 6Н), 8,44 (ушир.с, 2Н).
[α]D 22=+14,4o (с: 1,00, СНСl3).
Пример 84
Фосфат (R)-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина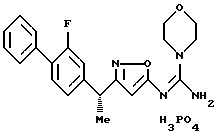
Желаемое соединение получают обработкой соединения, полученного по примеру 54, фосфорной кислотой.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,54 (д, 3Н, J=7,3 Гц), 3,40-3,43 (м, 4Н), 3,55-3,58 (м, 4Н), 4,11 (кв, 1Н, J=7,3 Гц), 5,42 (с, 1Н), 6,46 (ушир.с, 2Н), 7,21-7,26 (м, 2Н), 7,38-7,53 (м, 6Н).
ИК (чистый) [см-1] : 3381, 2973, 2361, 1682, 1618, 1552, 1484, 1456, 1411, 1274, 1113.
[α]D 20=-27,2o (с: 0,60, МеОН).
Пример 85
Фосфат (S)-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина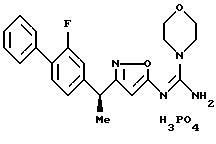
Тем же способом, что и по примеру 84, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: то же, что и по примеру 84.
ИК (чистый) [см-1]: то же, что и по примеру 84.
[α]D 20=+27,7oC (с: 0,52, МеОН).
Пример 86
Метансульфонат (R)-({3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илимино} морфолин-4-илметил)амина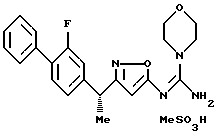
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 54.
Точка плавления 166-167oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 2,72 (с, 3Н), 3,46-3,51 (м, 4Н), 3,71-3,77 (м, 4Н), 4,17 (кв, 1Н, J=7,2 Гц), 5,59 (с, 1Н), 7,02-7,12 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,53 (м, 2Н), 8,62 (ушир.с, 2Н), 11,14 (ушир.с, 1Н).
ИК (чистый) [см-1] : 2974, 1668, 1634, 1548, 1484, 1446, 1270, 1194, 1117, 1043, 776, 699.
[α]D 22=-14,0o (с: 1,00, СНСl3).
Пример 87
Метансульфонат (S)-({3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-илимино} морфолин-4-илметил)амина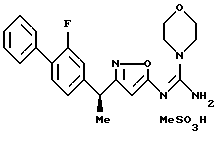
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
Точка плавления 162-165oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,3 Гц), 2,72 (с, 3Н), 3,46-3,51 (м, 4Н), 3,71-3,78 (м, 4Н), 4,17 (кв, 1Н, J=7,1 Гц), 5,59 (с, 1Н), 7,02-7,12 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,53 (м, 2Н), 8,62 (ушир.с, 2Н), 11,13 (ушир.с, 1Н).
ИК (чистый) [см-1] : 2972, 1668, 1634, 1548, 1484, 1446, 1418, 1198, 1116, 1062, 1010, 768, 699.
[α]D 22=+12,0o (с: 0,80, СНСl3).
Пример 88
Бензолсульфонат (R)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амина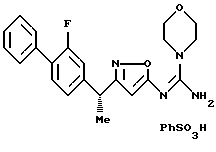
Желаемое соединение получают обработкой соединения, полученного по примеру 54, бензолсульфоновой кислотой.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,59 (д, 3Н, J=7,1 Гц), 3,50 (м, 4Н), 3,66 (м, 4Н), 4,26 (кв, 1Н, J=7,1 Гц), 5,98 (с, 1Н), 7,25-7,59 (м, 13Н).
ИК (чистый) [см-1]: 3135, 1679, 1630, 1552, 1484, 1445, 1418.
[α]D 20=-16,9o (с: 0,53, МеОН).
Пример 89
Бензолсульфонат (S)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амина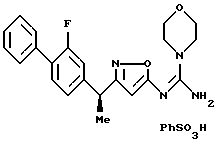
Тем же способом, что и по примеру 88, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: то же, что и по примеру 88.
ИК (чистый) [см-1]: то же, что и по примеру 88.
[α]D 20=+16,8oC (с: 0,51, МеОН).
Пример 90
Сульфат (R)-({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}морфолин-4-илметил)амина
Желаемое соединение получают обработкой соединения, полученного по примеру 54, серной кислотой.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,53 (д, 3Н, J=7,3 Гц), 3,30-3,80 (м, 8Н), 4,07 (кв, 1Н, J=6,8 Гц), 5,72 (с, 1Н), 6,97-7,05 (м, 2Н), 7,28-7,44 (м, 6Н), 7,95 (ушир.с, 2Н).
[α]D 22=-20,2o (с: 1,00, ТГФ).
Пример 91
Сульфат (S)-({ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}морфолин-4-илметил)амина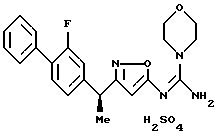
Тем же способом, что и по примеру 90, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,53 (д, 3Н, J=6,8 Гц), 3,30-3,80 (м, 8Н), 4,05-4,10 (м, 1Н), 5,72 (с, 1Н), 6,97-7,05 (м, 2Н), 7,28-7,44 (м, 6Н), 7,95 (ушир.с, 2Н).
[α]D 22=+20,2o (с: 1,00, ТГФ).
Пример 92
D-Камфорсульфат (R)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амина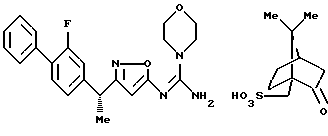
Желаемое соединение получают обработкой соединения, полученного по примеру 54, D-камфорсульфоновой кислотой.
Точка плавления 167-169oС.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,76 (с, 3Н), 0,95 (с, 3Н), 1,23-1,32 (м, 1Н), 1,53-1,62 (м, 1Н), 1,66 (д, 3Н, J=7,3 Гц), 1,79 (д, 1H, J=18,1 Гц), 1,82-1,88 (м, 1Н), 1,96-2,00 (м, 1H), 2,21-2,28 (м, 1Н), 2,35-2,47 (м, 1H), 2,76 (д, 1Н, J=14,6 Гц), 3,26 (д, 1H, J=14,6 Гц), 3,48-3,52 (м, 4Н), 3,73-3,76 (м, 4Н), 4,17 (кв, 1H, J=7,1 Гц), 5,63 (с, 1H), 7,03-7,53 (м, 8Н), 8,35 (ушир.с, 2Н), 11,12 (ушир.с, 2Н).
Пример 93
D-Камфорсульфат (S)-({ 3-[1-(2-Фторбифенил-4-ил)этил] -изоксазол-5-илимино}морфолин-4-илметил)амина
Тем же способом, что и по примеру 92, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,76 (с, 3Н), 0,95 (с, 3Н), 1,24-1,32 (м, 1H), 1,54-1,65 (м, 1H), 1,66 (д, 3Н, J=7,1 Гц), 1,79 (д, 1H, J=18,1 Гц), 1,82-1,91 (м, 1H), 1,96-2,00 (м, 1H), 2,21-2,30 (м, 1H), 2,35-2,47 (м, 1H), 2,75 (д, 1H, J=14,6 Гц), 3,26 (д, 1H, J=14,7 Гц), 3,48-3,52 (м, 4Н), 3,73-3,76 (м, 4Н), 4,17 (кв, 1H, J=7,1 Гц), 5,66 (с, 1H), 7,04-7,14 (м, 2Н), 7,33-7,52 (м, 6Н), 8,53 (ушир.с, 2Н), 11,11 (ушир.с, 1H).
Пример 94
3-Бром-(+)-камфор-10-сульфонат (R)-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина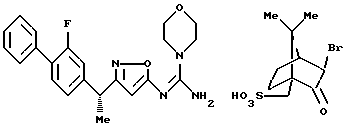
Желаемое соединение получают обработкой соединения, полученного по примеру 54, 3-бром-(+)-камфор-10-сульфоновой кислотой.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,97 (с, 3Н), 1,25 (с, 3Н), 1,47-1,54 (м, 1Н), 1,68 (д, 3Н, J= 7,1 Гц), 1,85-2,00 (м, 1Н), 2,00-2,10 (м, 1Н), 2,23-2,26 (м, 1Н), 2,65-2,69 (м, 1Н), 2,83 (д, 1Н, J=14,8 Гц), 3,23-3,28 (м, 1Н), 3,55-3,59 (м, 4Н), 3,74-3,78 (м, 4Н), 4,27 (кв, 1Н, J=7,1 Гц), 4,76-4,79 (м, 1Н), 5,91 (с, 1Н), 7,13-7,23 (м, 2Н), 7,34-7,51 (м, 6Н).
Пример 95
3-Бром-(+)-камфор-10-сульфонат (S)-({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина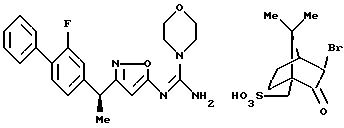
Тем же способом, что и по примеру 94, получают желаемое соединение, за исключением использования соединения, полученного по примеру 55.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,95 (с, 3Н), 1,23 (с, 3Н), 1,49-1,59 (м, 1Н), 1,67 (д, 3Н, J= 7,4 Гц), 1,80-2,15 (м, 2Н), 2,21-2,24 (м, 1Н), 2,62-2,66 (м, 1Н), 2,83 (д, 1Н, J=15,0 Гц), 3,23-3,28 (м, 1Н), 3,53-3,60 (м, 4Н), 3,73-3,77 (м, 4Н), 4,21 (кв, 1Н, J=7,3 Гц), 4,62-4,65 (м, 1Н), 5,79 (с, 1Н), 7,06-7,17 (м, 2Н), 7,30-7,49 (м, 6Н).
Пример 96
3-Бром-(+)-камфор-8-сульфонат (R)-({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина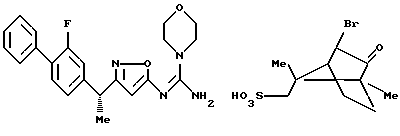
Желаемое соединение получают обработкой соединения, полученного по примеру 54, 3-бром-(+)-камфор-8-сульфоновой кислотой.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,90 (с, 3Н), 1,22 (с, 3Н), 1,37-1,43 (м, 1Н), 1,50-1,63 (м, 1Н), 1,67 (д, 3Н, J=7,1 Гц), 1,90-2,15 (м, 2Н), 2,76 (д, 1Н, J= 14,3 Гц), 2,94 (с, 1Н), 3,15 (д, 1Н, J=14,6 Гц), 3,40-3,52 (м, 4Н), 3,72-3,77 (м, 4Н), 4,17 (кв, 1H, J=7,1 Гц), 4,50 (д, 1Н, J=4,7 Гц), 5,50 (с, 1Н), 7,01-7,12 (м, 2Н), 7,34-7,53 (м, 6Н).
Пример 97
3-Бром-(+)-камфор-8-сульфонат (S)-({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино}морфолин-4-илметил)амина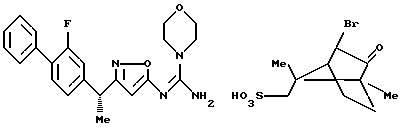
Тем же способом, что и по примеру 96, получают желаемое соединение, за исключением использования соединения, полученного по примеру 54.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,90 (с, 3Н), 1,11 (с, 3Н), 1,37-1,48 (м, 1Н), 1,50-1,63 (м, 1Н), 1,67 (д, 3Н, J=7,1 Гц), 1,95-2,15 (м, 2Н), 2,76 (д, 1Н, J= 14,3 Гц), 2,94 (с, 1Н), 3,15 (д, 1Н, J=14,5 Гц), 3,40-3,52 (м, 4Н), 3,72-3,77 (м, 4Н), 4,18 (кв, 1H, J=7,1 Гц), 4,49 (д, 1Н, J=4,8 Гц), 5,52 (с, 1Н), 7,02-7,12 (м, 2Н), 7,36-7,53 (м, 6Н).
Пример 98
({ 3-[1-(9Н-Карбазол-2-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин (схема 58, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 34.
Точка плавления 113oС (разл.).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,71 (д, 3Н, J=7,1 Гц), 3,42-3,46 (м, 4Н), 3,66-3,71 (м, 4Н), 4,27 (кв, 1H, J=7,1 Гц), 5,26 (с, 1H), 5,35 (ушир.с, 2Н), 7,16-7,23 (м, 2Н), 7,33-7,42 (м, 3Н), 7,96-8,04 (м, 2Н), 8,15 (с, 1H).
Пример 99
{ [3-(2-Фторбифенил-4-илметил] изоксазол-5-илимино] -морфолин-4-илметил} амин (схема 59, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 35.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 3,47-3,51 (м, 4Н), 3,71-3,75 (м, 4Н), 3,92 (с, 2Н), 5,26 (с, 1Н), 5,38 (ушир.с, 2Н), 7,04-7,14 (м, 2Н), 7,33-7,47 (м, 4Н), 7,50-7,55 (м, 2Н).
Пример 100
Метансульфонат {[3-(2-фторбифенил-4-илметил]изоксазол-5-илимино]морфолин-4-илметил}амина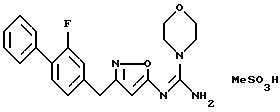
Тем же способом, что и по примеру 72, получают желаемое соединение, за исключением использования соединения, полученного по примеру 99.
Точка плавления 74-74oС (разл.).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 2,73 (с, 3Н), 3,47-3,51 (м, 4Н), 3,69-3,73 (м, 4Н), 3,96 (с, 2Н), 5,63 (с, 1Н), 7,01-7,11 (м, 2Н), 7,34-7,47 (м, 4Н), 7,50-7,54 (м, 2Н), 8,63 (ушир.с, 2Н), 11,2 (ушир.с, 1Н).
Пример 101
({ 3-[1-(2,3-Дигидробензо[1,4] диоксин-6-ил)этил] изоксазол-5-илимино] морфолин-4-илметил}амин (схема 60, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 37.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,58 (д, 3Н, J=7,3 Гц), 3,47 (т, 4Н, J= 4,6 Гц), 3,72 (т, 4Н, J=4,6 Гц), 4,00 (кв, 1Н, J=7,3 Гц), 4,22 (с, 4Н), 5,20 (с, 1Н), 5,35 (ушир.с, 2Н), 6,77-6,80 (м, 3Н).
Пример 102
({ 3-[1-(1-Метил-1Н-индол-3-ил)этил] изоксазол-5-илимино]-морфолин-4-илметил}амин (схема 61, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 38.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,72 (д, 3Н, J=7,3 Гц), 3,43 (т, 4Н, J= 4,6 Гц), 3,68 (т, 4Н, J=4,6 Гц), 3,73 (с, 3Н),
4,40 (кв, 1Н, J=7,3 Гц), 5,24 (с, 1Н), 5,31 (ушир.с, 2Н), 6,92 (с, 1Н), 7,03-7,28 (м, 3Н), 7,61 (д, 1Н, J=7,9 Гц).
Пример 103
({ 3-[1-(1H-Индол-3-ил)этил]изоксазол-5-илимино]морфолин-4 -илметил}амин (схема 62, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 39.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,72 (д, 3Н, J=7,3 Гц), 3,44 (т, 4Н, J= 5,0 Гц), 3,69 (т, 4Н, J=5,0 Гц), 4,41 (кв, 1Н, J=7,3 Гц), 5,23 (с, 1Н), 5,28 (ушир. с, 2Н), 7,04-7,19 (м, 3Н), 7,33 (д, 1Н, J=7,9 Гц), 7,63 (д, 1Н, J=7,9 Гц), 8,03 (ушир.с, 1Н).
Пример 104
({ 3-[1-(1-Метил-1Н-индол-2-ил)этил] изоксазол-5-илимино]-морфолин-4-илметил}амин (схема 63, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 41.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,73 (д, 3Н, J=7,3 Гц), 3,44 (т, 4Н, J= 4,6 Гц), 3,64 (с, 3Н), 3,70 (т, 4Н, J=4,6 Гц), 4,34 (кв, 1H, J=7,3 Гц), 5,12 (с, 1Н), 5,26 (ушир.с, 2Н), 6,45 (с, 1Н), 7,04-7,26 (м, 3Н), 7,56 (д, 1Н, J= 7,3 Гц).
Пример 105
{ [3-(1-Бензофуран-5-илэтил)изоксазол-5-илимино] морфолин-4-илметил}амин (схема 64, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 43.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,3 Гц), 3,46 (т, 4Н, J= 4,6 Гц), 3,71 (т, 4Н, J=4,6 Гц), 4,19 (кв, 1Н, J=7,3 Гц), 5,20 (с, 1Н), 5,34 (ушир. с, 2Н), 6,71 (д, 1Н, J=2,3 Гц), 7,21-7,26 (м, 1Н), 7,42 (д, 1Н, J=8,6 Гц), 7,51 (д, 1Н, J=1,7 Гц), 7,59 (д, 1Н, J=2,3 Гц).
Пример 106
{ [3-(1-Бензофуран-6-илэтил)изоксазол-5-илимино] морфолин-4-илметил}амин (схема 65, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 45.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,68 (д, 3Н, J=7,3 Гц), 3,46 (т, 4Н, J= 4,6 Гц), 3,71 (т, 4Н, J=4,6 Гц), 4,23 (кв, 1Н, J=7,3 Гц), 5,21 (с, 1Н), 5,33 (ушир. с, 2Н), 6,72 (д, 1Н, J=2,3 Гц), 7,19 (дд, 1Н, J=8,3, 1,7 Гц), 7,45-7,52 (м, 2Н), 7,58 (д, 1Н, J=2,3 Гц)
Пример 107
Метансульфонат (3-{1-[5-(аминоморфолин-4-илметиленамино)-изоксазол-3-ил] этил}фенил)фенилметанона (схема 66, приведенная в конце описания).
Тем же способом, что и по примеру 54 и примеру 72, получают желаемое соединение, за исключением использования {3-[1-(5-аминоизоксазол-3-ил)этил] фенил} фенилметанона (не подвергнутая экспертизе японская патентная публикация 63-152368).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,1 Гц), 2,72 (с, 3Н), 3,45-3,51 (м, 4Н), 3,72-3,76 (м, 4Н), 4,22 (кв, 1Н, J=7,1 Гц), 5,57 (с, 1Н), 7,40-7,51 (м, 4Н), 7,57-7,65 (м, 2Н), 7,71 (с, 1Н), 7,77-7,79 (м, 2Н), 8,61 (ушир.с, 2Н), 11,13 (ушир.с, 1Н).
Пример 108
[({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино}-морфолин-4-илметилимино)морфолин-4-илметил]амин (схема 67, приведенная в конце описания).
Смесь соединения (2,20 г) в свободной форме, полученного по примеру 22, 4-морфолинкарбонитрила (2,8 мл) и амида натрия (0,44 мг) перемешивают при комнатной температуре в течение 5 часов. Реакционную смесь выливают в насыщенный водный раствор хлорида аммония и затем подвергают экстракции хлороформом. Органический слой сушат над сульфатом магния и затем концентрируют при пониженном давлении, после чего остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (1,62 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,62 (д, 3Н, J=7,3 Гц), 3,26-3,29 (м, 4Н), 3,54-3,57 (м, 4Н), 3,63-3,66 (м, 8Н), 4,11 (кв, 1Н, J=7,2 Гц), 4,63 (ушир.с, 2Н), 5,01 (с, 1Н), 7,05-7,17 (м, 2Н), 7,33-7,54 (м, 6Н).
Пример 109
Гидрохлорид [({3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}морфолин-4-илметилимино)морфолин-4-илметил]амина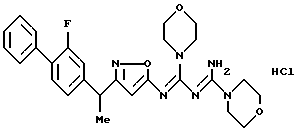
Соединение (1,66 г), полученное по примеру 108, растворяют в 1,4-диоксане (20 мл) и прибавляют раствор 4 н. соляной кислоты в 1,4-диоксане (1,00 мл), после чего реакционную смесь перемешивают при комнатной температуре в течение 2 часов, в процессе чего выпадает осадок. Реакционную смесь нагревают до 100oС для растворения осадка и затем дают медленно остыть при перемешивании. Полученный белый осадок отделяют фильтрацией с получением желаемого соединения (1,19 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,1 Гц), 3,44-3,56 (м, 4Н), 3,60-3,68 (м, 4Н), 3,68-3,83 (м, 8Н), 4,16 (кв, 1H, J=7,0 Гц), 5,52 (с, 1Н), 7,03-7,15 (м, 4Н), 7,35-7,55 (м, 6Н).
Пример 110
({ 3-[1-(2-Фторбифенил-4-ил)винил] изоксазол-5-илимино}-морфолин-4-илметил)амин (схема 68, приведенная в конце описания).
Трифторуксусную кислоту (4 мл) прибавляют к раствору соединения (30,0 мг), полученного по примеру 53, в метиленхлориде (1 мл) и полученную реакционную смесь перемешивают при комнатной температуре в течение 8 часов. После прибавления насыщенного водного раствора хлорида аммония смесь подвергают экстракции этилацетатом и органический слой промывают последовательно насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия, затем сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Реакционную смесь очищают колоночной хроматографией на силикагеле с получением желаемого соединения (20 мг).
Точка плавления 167,5oС (разл.).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 3,51-3,55 (м, 4Н), 3,74-3,78 (м, 4Н), 5,42 (ушир. с, 2Н), 5,54 (с, 1Н), 5,69 (с, 1Н), 5,84 (с, 1Н), 7,26-7,59 (м, 8Н).
Пример 111
{ Морфолин-4-ил-[3-(1-хинолин-3-илэтил)изоксазол-5-илимино] метил} амин (схема 69, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 47.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,76 (д, 3Н, J=7,3 Гц), 3,48 (т, 4Н, J= 4,6 Гц), 3,72 (т, 4Н, J=4,6 Гц), 4,34 (кв, 1Н, J=7,3 Гц), 5,24 (с, 1Н), 5,33 (ушир.с, 2Н), 7,50-7,79 (м, 3Н), 8,02-8,09 (м, 2Н), 8,89 (д, 1Н, J=2,3 Гц).
Пример 112
{ [3-(1-Изохинолин-4-илэтил)изоксазол-5-илимино] морфолин-4-илметил}амин (схема 70, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 48.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,83 (д, 3Н, J=7,3 Гц), 3,45 (т, 4Н, J= 4,6 Гц), 3,68 (т, 4Н, J=4,6 Гц), 4,79 (кв, 1Н, J=7,3 Гц), 5,13 (с, 1Н), 5,40 (ушир. с, 2Н), 7,56-7,72 (м, 2Н), 7,97 (д, 1Н, J=7,6 Гц), 8,14 (д, 1Н, J=8,6 Гц), 8,52 (с, 1Н), 9,15 (с, 1Н).
Пример 113
{ [3-(1-Бифенил-4-илдиметоксиметил)изоксазол-5-илимино] -морфолин-4-илметил}амин (схема 71, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 50.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,28 (с, 6Н), 3,47 (т, 4Н, J=4,6 Гц), 3,71 (т, 4Н, J=4,6 Гц), 5,32 (с, 1Н), 5,36 (ушир.с, 2Н), 7,33-7,45 (м, 3Н), 7,54-7,67 (м, 6Н).
Пример 114
({3-[Диметокси-(1-метил-1Н-индол-2-ил)метил]изоксазол-5-илимино}морфолин-4-илметил)амин (схема 72, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по примеру 52.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,27 (с, 6Н), 3,44 (т, 4Н, J=4,6 Гц), 3,66 (с, 3Н), 3,69 (т, 4Н, J=4,6 Гц), 5,26 (с, 1Н), 5,30 (ушир.с, 2Н), 6,87 (с, 1Н), 7,06-7,28 (м, 3Н), 7,62 (д, 1Н, J=7,6 Гц).
Пример 115
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-ил}-N''-фенилгуанидин (схема 73, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,54 (с, 9Н), 1,68 (д, 3Н, J=7,1 Гц), 4,16 (кв, 1Н, J=7,1 Гц), 5,45 (с, 1H), 7,07-7,17 (м, 3Н), 7,27-7,46 (м, 6Н), 7,51-7,61 (м, 4Н), 8,63 (ушир.с, 1H), 10,10 (ушир.с, 1H).
Пример 116
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N''-пиридин-3-илгуанидин (схема 74, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,55 (с, 9Н), 1,69 (д, 3Н, J=7,1 Гц), 4,18 (кв, 1H, J=7,1 Гц), 5,45 (с, 1Н), 7,07-7,25 (м, 2Н), 7,27-7,46 (м, 4Н), 7,51-7,55 (м, 2Н), 8,14-8,18 (м, 1H), 8,32-8,35 (м, 1H), 8,69-8,71 (м, 2Н), 10,22 (ушир.с, 1H).
Пример 117
(трет-Бутоксикарбонил)-({ 3-[1-(2-фторбифенил-4-ил)этил] -изоксазол-5-илимино}тиаморфолин-4-илметил)амин (схема 75, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,43 (с, 9Н), 1,66 (д, 3Н, J=7,3 Гц), 2,68-2,74 (м, 4Н), 3,84 (ушир.с, 4Н), 4,16 (кв, 1H, J=7,1 Гц), 5,28 (с, 1H), 6,81 (ушир.с, 1H), 7,07-7,16 (м, 2Н), 7,34-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 118
1-([(трет-Бутоксикарбонил)амино]-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)пиперидин-4-он (схема 76, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,46 (с, 9Н), 1,68 (д, 3Н, J=7,3 Гц), 2,60 (т, 4Н, J= 6,2 Гц), 3,84 (т, 4Н, J=6,2 Гц), 4,18 (кв, 1H, J=7,0 Гц), 5,34 (с, 1H), 7,06 (ушир. с, 1Н), 7,07-7,17 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 119
1-([(трет-Бутоксикарбонил)амино]-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)пиперидин-4-ол (схема 77, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,43 (с, 9Н), 1,55-1,68 (м, 3Н), 1,66 (д, 3Н, J=7,3 Гц), 1,85-1,99 (м, 2Н), 3,25-3,40 (м, 2Н), 3,84-3,99 (м, 3Н), 4,12 (кв, 1H, J=7,1 Гц), 5,25 (с, 1H), 6,75 (ушир.с, 1H), 7,07-7,16 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 120
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-N''-гидроксигуанидин (схема 78, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,51 (с, 9Н), 1,66 (д, 3Н, J=7,1 Гц), 4,16 (кв, 1H, J=7,1 Гц), 5,79 (с, 1Н), 6,20 (ушир.с, 1Н), 7,06-7,14 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н), 7,78 (ушир.с, 1H), 9,89 (ушир.с, 1H).
Пример 121
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил)-этил]изоксазол-5-ил}-N''-метоксигуанидин (схема 79, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,51 (с, 9Н), 1,68 (д, 3Н, J=7,1 Гц), 3,78 (с, 3Н), 4,19 (кв, 1H, J=7,1 Гц), 5,87 (с, 1H), 7,08-7,17 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н), 7,70 (ушир.с, 1H), 9,86 (ушир.с, 1H).
Пример 122
N-(трет-Бутоксикарбонил)-N'-(2-диметиламиноэтил)-N''-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} гуанидин (схема 80, приведенная в конце описания).
Тем же способом, что и по примеру 1, получают желаемое соединение.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,49 (с, 9Н), 1,67 (д, 3Н, J=7,1 Гц), 2,26 (с, 6Н), 2,49 (т, 2Н, J=6,2 Гц), 3,42-3,49 (м, 2Н), 4,14 (кв, 1Н, J=7,1 Гц), 5,31 (ушир.с, 1H), 7,07-7,17 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н), 8,18 (ушир.с, 1H), 8,48 (ушир.с, 1H).
Пример 123
N-{3-[1-(2-Фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-фенилгуанидин (схема 81, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 115.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,1 Гц), 4,14 (кв, 1H, J= 7,1 Гц), 5,18 (с, 1H), 5,48 (ушир.с, 2Н), 7,05-7,15 (м, 2Н), 7,23-7,47 (м, 3Н), 7,32-7,47 (м, 6Н), 7,51-7,55 (м, 3Н).
Пример 124
N-{3-[1-(2-Фторбифенил-4-ил)этил]изоксазол-5-ил}-N'-пиридин-3-илгуанидин (схема 82, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 116.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,1 Гц), 4,14 (кв, 1Н, J= 7,1 Гц), 5,33 (с, 1Н), 5,75 (ушир.с, 2Н), 7,04-7,11 (м, 2Н), 7,13-7,26 (м, 1Н), 7,31-7,45 (м, 5Н), 7,49-7,52 (м, 2Н), 7,90 (д, 1Н, J=8,3 Гц), 8,28 (д, 1Н, J=4,2 Гц), 8,46 (ушир.с, 1Н).
Пример 125
({ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино}-тиаморфолин-4-илметил)амино (схема 83, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 117.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,1 Гц), 2,62-2,66 (м, 4Н), 3,80-3,85 (м, 4Н), 4,14 (кв, 1Н, J=7,1 Гц), 5,24 (с, 1Н), 5,35 (ушир.с, 1Н), 7,07-7,20 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 126
1-(Амино-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперидин-4-он (схема 84, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 118.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,1 Гц), 2,55 (т, 4Н, J= 6,2 Гц), 3,83 (т, 4Н, J=6,2 Гц), 4,16 (кв, 1Н, J=7,1 Гц), 5,28 (с, 1Н), 5,47 (ушир.с, 2Н), 7,07-7,18 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 127
1-(Амино-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино} метил)пиперидин-4-ол (схема 85, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 119.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,50-1,64 (м, 3Н), 1,65 (д, 3Н, J=7,1 Гц), 1,81-1,94 (м, 2Н), 3,18-3,28 (м, 2Н), 3,81-3,96 (м, 3Н), 4,14 (кв, 1Н, J=7,1 Гц), 5,22 (с, 1Н), 5,34 (ушир.с, 2Н), 7,07-7,17 (м, 2Н), 7,33-7,45 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 128
N-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-гидроксигуанидин (схема 86, приведенная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 120.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,63 (д, 3Н, J=7,1 Гц), 4,12 (кв, 1Н, J= 7,1 Гц), 5,34 (с, 1Н), 5,59 (ушир.с, 2Н), 7,04-7,12 (м, 2Н), 7,33-7,45 (м, 6Н), 7,49-7,54 (м, 2Н).
Пример 129
N-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-метоксигуанидин (схема 87, представленная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 121.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,1 Гц), 3,73 (с, 3Н), 4,14 (кв, 1Н, J=7,1 Гц), 5,32 (ушир.с, 2Н), 5,41 (с, 1Н), 7,06-7,15 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 130
N-(2-Диметиламиноэтил)-N'-{ 3-[1-(2-фторбифенил-4-ил)этил]-изоксазол-5-ил}гуанидин (схема 88, представленная в конце описания).
Тем же способом, что и по примеру 48, получают желаемое соединение, за исключением использования соединения, полученного по примеру 122.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,1 Гц), 2,29 (с, 6Н), 2,50-2,55 (м, 2Н), 3,26-3,32 (м, 2Н), 4,14 (кв, 1Н, J=7,1 Гц), 5,19 (с, 1Н), 5,98 (ушир.с, 1Н), 6,34 (ушир.с, 1Н), 7,07-7,17 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример 131
[(3-{ 1-Метил-1-[3-(2-фенил[1,3] диоксолан-2-ил)фенил] -изоксазол-5-илимино}морфолин-4-илметил]амин (схема 89, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 53.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,66 (с, 6Н), 3,44-3,48 (м, 4Н), 3,70-3,73 (м, 4Н), 4,05 (с, 4Н), 5,07 (с, 1Н), 5,31 (ушир.с, 2Н), 7,20-7,35 (м, 6Н), 7,47-7,58 (м, 3Н).
Пример 132
(3-{ 1-[5-(Аминоморфолин-4-илметиленамино)изоксазол-3-ил] -1-метилэтил} фенил]фенилметанон (схема 90, приведенная в конце описания).
Соединение (8,8 г), полученное по примеру 131, растворяют в 90%-ном водном растворе уксусной кислоты (2 мл) с последующим перемешиванием в течение 40 часов. Реакционный раствор экстрагируют этилацетатом и экстракционный раствор промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Полученный остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (8,3 мг).
1H-ЯМР (300 МГц, СD3OD) δ м.д.: 1,72 (с, 6Н), 3,46-3,50 (м, 4Н), 3,70-3,74 (м, 4Н), 5,14 (с, 1Н), 5,39 (ушир.с, 2Н), 7,35-7,61 (м, 6Н), 7,76-7,84 (м, 3Н).
Пример 133
(Морфолин-4-ил-{ 3-[1-(6-фенилпиридин-3-ил)этил] изоксазол-5-илимино}метил)амин (схема 91, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение исходя из соединения, полученного по ссылочному примеру 55.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,69 (д, 3Н, J=7,3 Гц), 3,48 (т, 4Н, J= 5,0 Гц), 3,72 (т, 4Н, J=5,0 Гц), 4,18 (кв, 1Н, J=7,3 Гц), 5,23 (с, 1Н), 5,36 (ушир.с, 2Н), 7,39-7,50 (м, 3Н), 7,67 (м, 2Н), 7,95 (дд, 2Н, J=8,3, 1,7 Гц), 8,64 (с, 1Н).
Пример 134
(Морфолин-4-ил-{ 3-[1-(5-фенилпиридин-2-ил)этил] изоксазол-5-илимино}метил)амин (схема 92, приведенная в конце описания).
Тем же способом, что и по примеру 54, получают желаемое соединение исходя из соединения, полученного по ссылочному примеру 57.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,74 (д, 3Н, J=7,3 Гц), 3,48 (т, 4Н, J= 5,3 Гц), 3,72 (т, 4Н, J=5,3 Гц), 4,34 (кв, 1Н, J=7,3 Гц), 5,20-5,45 (м, 3Н), 7,32-7,57 (м, 6Н), 7,80 (дд, 1Н, J=7,9, 2,3 Гц), 8,78 (д, 1Н, J=2,3 Гц).
Ссылочный пример 1
1-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил}-2-метилизотиомочевина (схема 93, приведенная в конце описания).
3-[1-(2-Фторбифенил-4-ил)этил]изоксазол-5-илтиомочевину (не подвергнутая экспертизе японская патентная публикация 63-152368) (3,03 г) растворяют в N, N-диметилформамиде (90 мл) с последующим добавлением метилйодида (1,51 г) и карбоната калия (0,86 г), и полученную смесь перемешивают при 40oС в течение 2 часов. К реакционной смеси добавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (2,67 мг).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,67 (д, 3Н, J=7,2 Гц), 2,44 (с, 3Н), 4,17 (кв, 1Н, J=7,2 Гц), 5,50 (с, 1Н), 5,92 (ушир.с, 2Н), 7,06-7,15 (м, 2Н), 7,32-7,54 (м, 6Н).
Ссылочный пример 2
1-(трет-Бутоксикарбонил)-3-{ 3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}-2-метил)изотиомочевина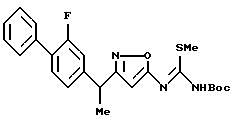
Гидрид натрия (4,22 г, 60%-ный в масле) суспендируют в тетрагидрофуране (80 мл) и при охлаждении льдом прибавляют по каплям раствор в тетрагидрофуране (100 мл) соединения, полученного по ссылочному примеру 1 (25,0 г), после чего медленно по каплям прибавляют раствор трет-бутилазидоформиата ("Organic Syntheses" Coll. Vol. 5, John Wiley and Sons, Inc., New York 1973), p. 157) (15,1 г) в тетрагидрофуране (50 мл) в течение периода в 65 минут и полученную смесь перемешивают при охлаждении льдом в течение 1 часа и затем при комнатной температуре в течение ночи. К реакционной смеси прибавляют воду с последующей экстракцией диэтиловым эфиром и сушат. Растворитель отгоняют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (21,1 г).
Точка плавления 124-126oС (разл.).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,49 (с, 9Н), 1,68 (д, 3Н, J=7,1 Гц), 2,37 (с, 3Н), 4,18 (кв, 1Н, J=7,1 Гц), 5,63 (с, 1Н), 7,06-7,15 (м, 2Н), 7,35-7,53 (м, 6Н), 8,93 (ушир.с, 1Н).
ИК (КВr) [см-1]: 3382, 2980, 1750, 1588.
Ссылочный пример 3
3-Бензоил-1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-1-метилтиомочевина (схема 94, приведенная в конце описания).
Раствор, содержащий {3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-ил}метиламина (4,06 г), пиридина (40 мл) и бензоилизотиоцианата (2,5 г) перемешивают в течение ночи при комнатной температуре. Раствор концентрируют и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (5,28 мг).
Точка плавления 115-116oС.
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,59 (д, 3Н, J=7,3 Гц), 3,79 (с, 3Н), 4,14 (кв, 1H, J=7,3 Гц), 5,83 (с, 1Н), 6,92-6,97 (м, 2Н), 7,16 (т, 1H, J=8,2 Гц), 7,34-7,52 (м, 8Н), 7,68-7,73 (м, 2Н), 8,79 (с, 1H).
ИК (КВr) [см-1]: 3440, 3275, 3125, 2980, 1690, 1612, 1515, 1488, 1424, 1360, 1266, 1230, 1168.
Ссылочный пример 4
3-Бензоил-1-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил}-1,2-диметилизотиомочевина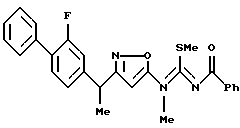
Карбонат калия (4,1 г) и метилйодид (1,25 мл) прибавляют к раствору N, N-диметилформамида (60 мл, 5,22 г) соединения, полученного по ссылочному примеру 3, и полученную смесь перемешивают при комнатной температуре в течение 5 часов. Реакционную смесь разбавляют этилацетатом и затем добавляют воду с последующей экстракцией. Экстракт очищают колоночной хроматографией на силикагеле с получением желаемого соединения (4,87 мг).
Точка плавления 124-126oС (разл.).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,66 (д, 3Н, J=7,3 Гц), 2,28 (с, 3Н), 3,56 (с, 3Н), 4,19 (кв, 1H, J=7,3 Гц), 6,06 (с, 1Н), 7,00-7,10 (м, 2Н), 7,33-7,52 (м, 9Н), 9,03 (д, 2Н, J=7,7 Гц).
Ссылочный пример 5
Этил 5-(2-фторбифенил-4-ил)-2-гидрокси-4-оксогекс-2-еноат (схема 95, приведенная в конце описания).
3-(2-Фторбифенил-4-ил)бутан-2-он (не подвергнутая экспертизе японская патентная публикация 54-144347) (116 мг) растворяют в толуоле (2 мл) с последующим добавлением гидрида натрия (29 мг, 60%-ный в масле) и смесь перемешивают при комнатной температуре в течение 1 часа. Затем прибавляют диэтилоксалат (105 мг) и полученную смесь перемешивают при 40oС в течение 3 часов. К реакционной смеси добавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (163 мг).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,35 (т, 3Н, J=7,2 Гц), 1,54 (д, 3Н, J= 7,1 Гц), 3,86 (кв, 1Н, J=7,1 Гц), 4,32 (кв, 2Н, J=7,2 Гц), 6,37 (с, 1Н), 7,04-7,12 (м, 2Н), 7,31-7,55 (м, 7Н).
ИК (КВr) [см-1]: 2925, 1734, 1636, 1484.
Ссылочный пример 6
Этил 5-[1-(2-фторбифенил-4-ил)этил]изоксазол-3-карбоксилат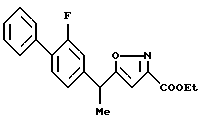
Соединение (163 мг), полученное по ссылочному примеру 5, и гидрохлорид гидроксиламина (40 мг) растворяют в этаноле (2 мл) и полученный раствор перемешивают при 60oС в течение 9 часов. К реакционной смеси добавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (143 мг).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,41 (т, 3Н, J=7,1 Гц), 1,73 (д, 3Н, J= 7,3 Гц), 4,34 (кв, 1Н, J=7,3 Гц), 4,43 (кв, 2Н, J=7,1 Гц), 6,45 (с, 1Н), 7,02-7,12 (м, 2Н), 7,33-7,55 (м, 6Н).
ИК (КВr) [см-1]: 2983, 1733, 1625, 1584, 1484, 1418.
Ссылочный пример 7
{5-[1-(2-Фторбифенил-4-ил)этил]изоксазол-3-ил}метанол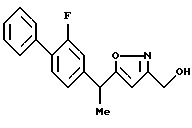
Соединение (2,45 мг), полученное по ссылочному примеру 6, растворяют в тетрагидрофуране (20 мл) и прибавляют литийалюминийгидрид (300 мг) при 0oС и полученный раствор перемешивают в течение 1,5 часов. К реакционной смеси добавляют воду с последующей экстракцией метиленхлоридом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток перекристаллизовывают из метиленхлорида с получением желаемого соединения (2,09 г).
Точка плавления 127-127,5oС.
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,70 (д, 3Н, J=7,3 Гц), 4,28 (кв, 1Н, J= 7,3 Гц), 4,74 (с, 2Н), 6,09 (с, 1Н), 7,03-7,13 (м, 2Н), 7,33-7,55 (м, 6Н).
ИК (КВr) [см-1]: 3308, 1603, 1485, 1418.
Элементный анализ:
Вычислено: С 72,71; Н 5,42; N 4,71.
Найдено: С 72,61; Н 5,45; N 4,88.
Ссылочный пример 8
3-Бромметил-5-[1-(2-фторбифенил-4-ил)этил]изоксазол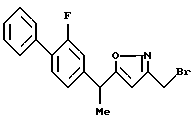
Соединение (2,03 мг), полученное по ссылочному примеру 1, растворяют в метиленхлориде (80 мл) и прибавляют тетрабромид углерода (3,40 г) и трифенилфосфин (2,69 г) и полученный раствор перемешивают в течение 1 часа. К реакционной смеси добавляют насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией метиленхлоридом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (6,83 г).
Точка плавления 102-103oС.
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,71 (д, 3Н, J=7,3 Гц), 4,27 (кв, 1Н, J= 7,3 Гц), 4,39 (с, 2Н), 6,12 (д, 1Н, J=0,7 Гц), 7,03-7,13 (м, 2Н), 7,33-7,55 (м, 6Н).
ИК (КВr) [см-1]: 1600, 1484, 1417.
Элементный анализ:
Вычислено: С 60,02; Н 4,20; N 3,89.
Найдено: С 59,86; Н 4,17; N 4,04.
Ссылочный пример 9
3-Азидометил-5-[1-(2-фторбифенил-4-ил)этил]изоксазол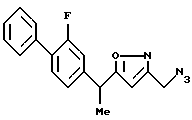
Соединение (2,08 мг), полученное по ссылочному примеру 8, и азид натрия (749 мг) растворяют в N, N-диметилформамиде (20 мл) и полученный раствор перемешивают при 50oС в течение 3 часов. К реакционной смеси добавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (1,85 г).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,71 (д, 3Н, J=7,3 Гц), 4,28 (кв, 1Н, J= 7,3 Гц), 4,39 (с, 2Н), 6,07 (с, 1Н), 7,02-7,12 (м, 2Н), 7,33-7,55 (м, 6Н).
ИК (чистый) [см-1]: 2978, 2933, 2104, 1596, 1485.
Элементный анализ:
Вычислено: С 67,07; Н 4,69; N 17,38.
Найдено: С 66,93; Н 4,78; N 17,56.
Ссылочный пример 10
{5-[1-(2-Фторбифенил-4-ил)этил]изоксазол-3-илметил}амин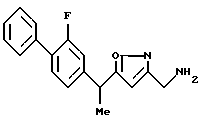
Соединение (1,82 мг), полученное по ссылочному примеру 9, растворяют в тетрагидрофуране (15 мл) с последующим добавлением боргидрида лития (641 мг) и полученный раствор перемешивают при кипячении с обратным холодильником. В течение 1 часа прибавляют по каплям метанол (3 мл) и перемешивают 3 часа, после чего реакционный раствор охлаждают до комнатной температуры. Прибавляют раствор 1 н. НСl (6 мл) и разделяют. Водный слой промывают гексаном, устанавливают рН 11 с помощью 15%-ной водного раствора гидроксида натрия и затем экстрагируют метиленхлоридом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (1,13 г).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,70 (д, 3Н, J=7,2 Гц), 3,91 (с, 2Н), 4,26 (кв, 1H, J=7,2 Гц), 6,01 (с, 1Н), 7,03-7,13 (м, 2Н), 7,33-7,55 (м, 6Н).
Ссылочный пример 11
N', N''-Ди(трет-бутоксикарбонил)-N, N-диметилгуанидин (схема 96, приведенная в конце описания).
1,3-Ди(трет-бутоксикарбонил)-2-метилизотиомочевину (не подвергнутая экспертизе японская патентная публикация 2-3661) (3,00 г) растворяют в 50%-ном водном растворе диметиламина (40 мл) и полученный раствор перемешивают при комнатной температуре в течение 18 часов. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (2,58 г).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,50 (с, 18Н), 3,07 (с, 6Н).
Ссылочный пример 12
(трет-Бутоксикарбонил)-[(трет-бутоксикарбонил)иминопиперидин-1-метил]амин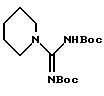
Тем же способом, что и по ссылочному примеру 11, получают желаемое соединение.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,49 (с, 18Н), 1,64 (ушир.с, 6Н), 3,52 (ушир.с, 4Н), 10,13 (ушир.с, 1Н).
Элементный анализ:
Вычислено: С 58,69; Н 8,93; N 12,83.
Найдено: С 58,46; Н 8,86; N 12,79.
Ссылочный пример 13
(трет-Бутоксикарбонил)-[(трет-бутоксикарбонил)иминоморфолин-4-илметил] амин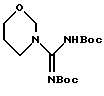
Тем же способом, что и по ссылочному примеру 11, получают желаемое соединение.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,48 (с, 9Н), 1,50 (с, 9Н), 3,59 (ушир. с, 4Н), 3,72-3,76 (м, 4Н), 10,21 (ушир.с, 1Н).
Ссылочный пример 14
1,3-Ди(трет-бутоксикарбонил)-1,2-диметилизотиомочевина (схема 97, приведенная в конце описания).
1,3-Ди(трет-бутоксикарбонил)-2-метилизотиомочевина (не подвергнутая экспертизе японская патентная публикация 2-3661) (2,00 г) растворяют в N,N-диметилформамиде (20 мл) с последующим добавлением 60%-ного гидрида натрия (331 мг) и полученную смесь перемешивают при 50oС в течение 2 часов. Затем смесь охлаждают до 0oС, прибавляют метилйодид (1,96 г) и полученную смесь перемешивают при комнатной температуре в течение 2 часов. К реакционной смеси добавляют воду с последующей экстракцией этилацетатом и экстракционный раствор промывают водой и сушат. Растворитель удаляют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (2,07 г).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,48 (с, 9Н), 1,51 (с, 9Н), 2,39 (с, 3Н), 3,12 (с, 3Н).
ИК (чистый) [см-1]: 2979, 1720, 1624.
Элементный анализ:
Вычислено: С 51,29; Н 7,95; N 9,20.
Найдено: С 51,06; Н 8,08; N 9,31.
Ссылочный пример 15
Этил [1,3-ди(трет-бутоксикарбонил)-2-метилизотиоуреидо]-ацетат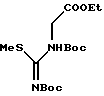
Тем же способом, что и по ссылочному примеру 14, получают желаемое соединение.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,29 (т, 3Н, J=7,1 Гц), 1,48 (с, 9Н), 1,51 (с, 9Н), 2,45 (с, 3Н), 4,22 (кв, 2Н, J=7,1 Гц), 4,30 (с, 2Н).
ИК (чистый) [см-1]: 2981, 1725, 1615, 1369, 1315.
Элементный анализ:
Вычислено: С 51,05; Н 7,50; N 7,44.
Найдено: С 50,76; Н 7,56; N 7,50.
Ссылочный пример 16
1-{ 3-[1-(4-Изобутилфенил)этил] изоксазол-5-ил} -2-метилизотиомочевина (схема 98, приведенная в конце описания).
В атмосфере азота 2-(4-изобутилфенил)пропионовую кислоту (15,0 г) растворяют в этаноле (200 мл) и прибавляют конц. серную кислоту (1 мл), после чего раствор перемешивают при нагревании с обратным холодильником в течение 15 часов. Реакционную смесь охлаждают до комнатной температуры, концентрируют при пониженном давлении, разбавляют этилацетатом и затем нейтрализуют насыщенным водным раствором бикарбоната натрия. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением этил 2-(4-изобутилфенил)пропионата.
К гидриду натрия (4,34 г, 60%-ный в масле) прибавляют тетрагидрофуран (100 мл) и затем при нагревании с обратным холодильником в течение более одного часа по каплям прибавляют раствор, полученный растворением вышеуказанного сложного эфира (около 17,0 г) и ацетонитрила (7,56 г) в тетрагидрофуране (150 мл). После перемешивания при нагревании с обратным холодильником в течение 6 часов полученную смесь охлаждают до комнатной температуры и прибавляют небольшое количество воды, после чего смесь разбавляют этилацетатом и прибавляют насыщенный водный
раствор бикарбоната натрия. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из гексана с получением 4-(4-изобутилфенил)-3-оксопентанитрила (10,2 г).
Этот цианокетон (10,2 г) растворяют в этаноле (150 мл) и затем прибавляют пиридин (30 мл) и гидрохлорид гидроксиламина (6,17 г), после чего полученную смесь перемешивают при комнатной температуре в течение 24 часов. Реакционную смесь концентрируют при пониженном давлении, разбавляют этилацетатом и затем нейтрализуют насыщенным водным раствором бикарбоната натрия, после чего нейтрализованный раствор подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением 3-[1-(4-изобутилфенил)этил]изоксазол-5-иламина (11,35 г).
Изоксазол (11,35 г) растворяют в этилендихлориде (200 мл) и затем прибавляют бензоилизотиоцианат (11,9 мл), после чего полученную смесь перемешивают при 60oС в течение 5 часов. Реакционную смесь концентрируют при пониженном давлении и прибавляют небольшое количество воды, после чего полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток выделяют колоночной хроматографией на силикагеле (гексан/этилацетат = 2/1) и затем очищают методом перекристаллизации из толуола с получением 1-бензоил-3-{3-[1-(4-изобутилфенил)этил]изоксазол-5-ил}тиомочевина (4,65 г).
Эту тиомочевину (4,65 г) растворяют в тетрагидрофуране (50 мл) и затем прибавляют метанол (50 мл) и карбонат калия (3,15 г), после чего смесь перемешивают при 50oС в течение 5 часов. К реакционной смеси прибавляют небольшое количество воды и полученную смесь подвергают экстракции этилацетатом. Органический слой промывают насыщенным водным раствором хлорида натрия, затем сушат над сульфатом натрия и после этого концентрируют при пониженном давлении с получением 3-[1-(4-изобутилфенил)-этил]изоксазол-5-илтиомочевины (15,52 г).
Желаемое соединение получают тем же способом, что и по ссылочному примеру 1, за исключением использования тиомочевины.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,89 (д, 6Н, J=6,6 Гц), 1,63 (д, 3Н, J= 7,3 Гц), 1,83 (м, 1Н), 2,43 (д, 2Н, J=6,1 Гц), 2,44 (с, 3Н), 4,11 (кв, 1H, J=7,2 Гц), 5,45 (с, 1Н), 5,91 (ушир.с, 2Н), 7,06-7,09 (м, 2Н), 7,17-7,20 (м, 2Н).
Ссылочный пример 17
1-{ 3-[1-(6-Метоксинафталин-2-ил)этил] изоксазол-5-ил} -2-метилизотиомочевина (схема 99, приведенная в конце описания).
Тем же способом, что и по ссылочному примеру 16, получают желаемое соединение, за исключением использования 2-(6-метоксинафталин-2-ил)пропионовой кислоты.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,72 (д, 3Н, J=7,2 Гц), 2,42 (с, 3Н), 3,91 (с, 3Н), 4,27 (кв, 1H, J=7,2 Гц), 5,46 (с, 1H), 5,90 (ушир.с, 2Н), 7,10-7,15 (м, 2Н), 7,37 (дд, 1H, J=8,4, 1,8 Гц), 7,65-7,71 (м, 3Н).
Ссылочный пример 18
1-(трет-Бутилкарбонил)-3-{ 3-[1-(4-изобутилфенил)этил] изоксазол-5-ил}-2-метилизотиомочевина (схема 100, приведенная в конце описания).
Тем же способом, что и по ссылочному примеру 2, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 16.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 0,89 (д, 6Н, J=6,6 Гц), 1,50 (с, 9Н), 1,65 (д, 3Н, J=7,3 Гц), 1,84 (м, 1Н, J=6,6 Гц), 2,36 (с, 3Н), 2,44 (д, 2Н, J= 7,1 Гц), 4,12 (кв, 1Н, J=7,3 Гц), 5,58 (с, 1Н), 7,08-7,11 (м, 2Н), 7,17-7,20 (м, 2Н), 8,95 (ушир.с, 1Н).
Ссылочный пример 19
1-(трет-Бутоксикарбонил)-3-{3-[1-(6-метоксинафтален-2-ил)этил]изоксазол-5-ил}-2-метил)изотиомочевина (схема 101, приведенная в конце описания).
Тем же способом, что и по ссылочному примеру 2, получают желаемое соединение, за исключением использования соединения, полученного по ссылочному примеру 17.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,50 (с, 9Н), 1,74 (д, 3Н, J=7,2 Гц), 2,34 (с, 3Н), 3,91 (с, 3Н), 4,29 (кв, 1Н, J=7,3 Гц), 5,59 (с, 1Н), 7,10-7,16 (м, 2Н), 7,36 (дд, 1Н, J=8,4, 1,6 Гц), 7,65 (с, 1H), 7,68-7,71 (м, 2Н), 8,95 (ушир.с, 1Н).
Ссылочный пример 20
{ 3-[1-(2-Фторбифенил-4-ил)-1-метилэтил] изоксазол-5-иламин (схема 102, приведенная в конце описания).
В атмосфере азота 2-(2-фторбифенил-4-ил)пропионовую кислоту (15,0 г) растворяют в N,N-диметилформамиде (150 мл) и затем прибавляют гидрид натрия (6,14 г, 60%-ный в масле), и полученную смесь перемешивают в течение одного часа. Затем прибавляют йодметан (9,5 мл) и смесь перемешивают в течение 12 часов. К реакционной смеси прибавляют небольшое количество воды и полученную смесь затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из гексана с получением метил 2-(2-фторбифенил-4-ил)-2-метилпропионата (14,2 г).
К гидриду натрия (2,70 г, 60%-ный в масле) прибавляют тетрагидрофуран (100 мл) и затем при нагревании с обратным холодильником в течение более одного часа по каплям прибавляют раствор, полученный растворением вышеуказанного сложного эфира (12,2 г) и ацетонитрила (4,66 мл) в тетрагидрофуране (100 мл). Полученную смесь перемешивают при нагревании с обратным холодильником в течение 8 часов и затем охлаждают до комнатной температуры и прибавляют небольшое количество воды, после чего смесь разбавляют этилацетатом и прибавляют насыщенный водный раствор бикарбоната натрия. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола с получением 4-(2-фторбифенил-4-ил)-4-метил-3-оксопентанитрила (6,27 г).
Этот цианокетон (9,98 г) растворяют в этаноле (200 мл) и затем прибавляют пиридин (40 мл) и гидрохлорид гидроксиламина (2,47 г), после чего полученную смесь перемешивают при 50oС в течение 5 часов. Реакционную смесь концентрируют при пониженном давлении, разбавляют этилацетатом, нейтрализуют насыщенным водным раствором бикарбоната натрия, после чего подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола с получением желаемого соединения (7,00 г).
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,69 (с, 6Н), 4,37 (ушир.с, 2Н), 4,86 (с, 1Н), 7,10-7,34 (м, 2Н), 7,32-7,46 (м, 4Н), 7,50-7,55 (м, 2Н).
Ссылочный пример 21
3-[1-Этокси-1-(2-фторбифенил-4-ил)этил] изоксазол-5-иламин (схема 103, приведенная в конце описания).
В атмосфере азота этил 2-(2-фторбифенил-4-ил)пропионат (не подвергнутая экспертизе японская патентная публикация 52-105144) (15,0 г) растворяют в N, N-диметилформамиде (300 мл) с последующим добавлением гидрида натрия (4,16 г, 60%-ный в масле), после чего полученную смесь перемешивают в течение одного часа. Затем прибавляют йодэтан (10,4 мл) и смесь перемешивают в течение 12 часов. К реакционной смеси прибавляют небольшое количество воды и этанола и затем растворитель удаляют азеотропной отгонкой с использованием толуола. К остатку прибавляют этилацетат и полученную смесь нейтрализуют насыщенным водным раствором бикарбоната натрия и затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением этил 2-этокси-2-(2-фторбифенил-4-ил)пропионата.
К смеси гидрида натрия (4,16 г, 60%-ный в масле) и тетрагидрофурана (100 мл) при нагревании с обратным холодильником в течение более одного часа по каплям прибавляют раствор, полученный растворением вышеуказанного сложного эфира (5,43 мл) в тетрагидрофуране (200 мл). После перемешивания при нагревании с обратным холодильником в течение 4 часов смесь охлаждают до комнатной температуры и прибавляют небольшое количество воды, после чего смесь разбавляют этилацетатом и затем прибавляют насыщенный водный раствор бикарбоната натрия. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением 4-этокси-4-(2-фторбифенил-4-ил)-3-оксопента-нитрила, производного цианокетона.
Этот цианокетон растворяют в этаноле (300 мл) и затем прибавляют пиридин (60 мл) и гидрохлорид гидроксиламина (5,42 г), после чего полученную смесь перемешивают при 50oС в течение 5 часов. Реакционную смесь концентрируют при пониженном давлении, разбавляют этилацетатом, нейтрализуют насыщенным водным раствором бикарбоната натрия и затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 3/1) с получением желаемого соединения (11,3 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,26 (т, 3Н, J=7,0 Гц), 1,86 (с, 3Н), 3,35-3,60 (м, 2Н), 4,39 (ушир. с, 2Н), 5,03 (с, 1Н), 7,25-7,46 (м, 6Н), 7,51-7,55 (м, 2Н).
Ссылочный пример 22
3-[1-(2-Фторбифенил-4-ил)циклопропил] изоксазол-5-иламин (схема 104, приведенная в конце описания).
В атмосфере азота метил (2-фторбифенил-4-ил)ацетат (5 г) растворяют в тетрагидрофуране (50 мл) и затем при охлаждении льдом прибавляют гидрид натрия (8,29 г, 60%-ный в масле), после чего полученную смесь перемешивают в течение 30 минут. Затем прибавляют последовательно N,N-диметилформамид (100 мл) и 1,2-дибромэтан (17,6 мл), после чего полученную смесь перемешивают в течение 1,5 часов. К реакционной смеси прибавляют раствор 4 н. соляной кислоты в 1,4-диоксане (60 мл) и раствор затем нейтрализуют насыщенным водным раствором хлорида аммония и затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 20/1) с получением 1-(2-фторбифенил-4-ил)циклопропанкарбоксилата (4,28 г).
Желаемое соединение получают из этого сложного эфира тем же способом, как и во второй половине ссылочного примера 20.
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,30 (кв, 2Н, J=3,7 Гц), 1,48 (кв, 2Н, J=3,7 Гц), 4,34 (ушир.с, 2Н), 4,88 (с, 1Н), 7,13-7,23 (м, 2Н), 7,35-7,47 (м, 4Н), 7,52-7,55 (м, 2Н).
Ссылочный пример 23
2-(1-Бифенил-4-илэтил)изоксазол-5-иламин (схема 105, приведенная в конце описания).
После монометилирования с помощью этил 4-бифенилацетоацетата желаемое соединение может быть получено тем же способом, как и во второй половине ссылочного примера 20.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,3 Гц), 4,12 (кв, 1Н, J= 7,3 Гц), 4,40 (с, 2Н), 4,92 (с, 1Н), 7,30-7,45 (м, 5Н), 7,52-7,59 (м, 4Н).
Ссылочный пример 24
2-(1-Бифенил-4-ил-1-метилэтил)изоксазол-5-иламин (схема 106, приведенная в конце описания).
После деметилирования с помощью этил 4-бифенилацетоацетата желаемое соединение может быть получено тем же способом, как и во второй половине ссылочного примера 20.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,70 (с, 6Н), 4,32 (с, 2Н), 4,84 (с, 1Н), 7,33-7,59 (м, 9Н).
Ссылочный пример 25
3-[1-(3-Феноксифенил)этил] изоксазол-5-иламин (схема 107, приведенная в конце описания).
Используя кальций 2-(3-феноксифенил)пропионат, желаемое соединение может быть получено тем же способом, как и во второй половине ссылочного примера 20.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,59 (д, 3Н, J=7,1 Гц), 4,12 (кв, 1Н, J= 7,1 Гц), 4,41 (ушир.с, 2Н), 4,87 (с, 1Н), 6,81-6,86 (м, 1Н), 6,96-7,11 (м, 5Н), 7,21-7,36 (м, 3Н).
Ссылочный пример 26
(R)-3-[1-(2-Фторбифенил-4-ил)этил]изоксазол-5-иламин (схема 108, приведенная в конце описания).
В атмосфере азота трет-бутилцианоацетат (0,57 мл) прибавляют по каплям к смеси тетрагидрофурана (5 мл) и гидрида натрия (160 мг, 60%-ный в масле) при охлаждении льдом. Полученную смесь перемешивают при охлаждении льдом, затем перемешивают при комнатной температуре в течение 20 минут и опять перемешивают при 0oС. Отдельно прибавляют по каплям изобутилхлорформиат (0,26 мл) к тетрагидрофурановому раствору (20 мл) (R)-2-(2-фторбифенил-4-ил)пропионовой кислоты (449 мг, 93% е.е.) и N-метилморфолина (0,22 мл) при -15oС при перемешивании. Через 5 минут этот раствор прибавляют по каплям к предыдущей смеси. Через 20 мин все выливают в насыщенный водный раствор бикарбоната натрия и полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. К вязкому осадку, полученному таким образом, прибавляют гидрохлорид гидроксиламина (278 мг) и этанол (10 мл) и полученную смесь перемешивают в течение 4 часов при кипячении с обратным холодильником. После охлаждения до комнатной температуры этанол удаляют отгонкой и к осадку прибавляют насыщенный водный раствор бикарбоната натрия и полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 3/2) с получением желаемого соединения (226 мг, 93% е.е.).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,63 (д, 3Н, J=7,1 Гц), 4,09 (кв, 1Н, J= 7,1 Гц), 4,46 (ушир.с, 2Н), 4,91 (с, 1Н), 7,05-7,18 (м, 2Н), 7,31-7,47 (м, 4Н), 7,50-7,76 (м, 2Н).
Ссылочный пример 27
(S)-3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-иламин (схема 109, приведенная в конце описания).
Тем же способом, что и по ссылочному примеру 29, получают желаемое соединение, за исключением использования (S)-2-(2-фторбифенил-4-ил)пропионовой кислоты.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,61 (д, 3Н, J=7,1 Гц), 4,08 (кв, 1Н, J= 7,1 Гц), 4,55 (ушир.с, 2Н), 4,89 (с, 1Н), 7,05-7,17 (м, 2Н), 7,31-7,44 (м, 4Н), 7,50-7,76 (м, 2Н).
Ссылочный пример 28
3-Бифенил-4-илметилизоксазол-5-иламин (схема 110, приведенная в конце описания).
Используя 4-бифенилацетоуксусную кислоту, желаемое соединение может быть получено тем же способом, как и во второй половине ссылочного примера 20.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 3,89 (с, 2Н), 4,36 (с, 2Н), 4,94 (с, 1Н), 7,31-7,59 (м, 9Н).
Ссылочный пример 29
3-[1-(2-Фтор-2', 3', 4',5',6'-пентадейтеробифенил-4-ил)-этил]изоксазол-5-иламин (схема 111, приведенная в конце описания).
В атмосфере азота к нитриту натрия (4,8 г) прибавляют дейтерид бензола (56 мл) и воду (6 мл) и полученную смесь перемешивают при 60oС. К этому раствору прибавляют по каплям при перемешивании в течение более 3 часов раствор, полученный растворением диметил 2-(4-амино-3-фторфенил)-2-метилмалоната (не подвергнутая экспертизе японская патентная публикация 2-223542) (10,0 г) и ледяной уксусной кислоты (4,24 г) в дейтериде бензола (19 мл). После перемешивания в течение 2 часов полученный раствор промывают насыщенным водным раствором сульфата натрия и концентрируют при пониженном давлении. Остаток растворяют в 85%-ном водном растворе серной кислоты (17,7 мл) и полученный раствор подвергают экстракции толуолом-гексаном. Его промывают 1 н. водным раствором карбоната натрия и затем насыщенным водным раствором хлорида натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 13/1) с получением диэтил 2-(2-фтор-2', 3',4',5',6'-пентадейтеробифенил-4-ил)-2-метилмалоната (5,99 г).
Эту карбоновую кислоту (3,84 г) растворяют в этаноле (20 мл) и затем прибавляют толуол (10 мл) и конц. серную кислоту (50 мг), после чего полученную смесь перемешивают при 60-80oС в течение 4 часов. Реакционную смесь разбавляют этилацетатом, нейтрализуют карбонатом натрия и затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением этил 2-(2-фтор-2',3',4', 5',6'-пентадейтеробифенил-4-ил)пропионата (4,26 г).
Этот эфир (5,98 г) растворяют в этаноле (39 мл) и затем добавляют 50% водный раствор гидроксида натрия (3,42 мл) при -15oС, после чего полученную смесь перемешивают при комнатной температуре в течение 6 часов. К реакционной смеси добавляют маленькое количество воды и 3 н. соляной кислотой рН раствора устанавливают 8, после чего смесь экстрагируют хлороформом. рН водного слоя устанавливают 1 и затем экстрагируют этилацетатом, после чего органический слой сушат над сульфатом магния и затем концентрируют при пониженном давлении. Добавляют ледяную уксусную кислоту (4,24 г) к остатку и полученную смесь нагревают с обратным холодильником в течение 17 часов. Охлаждают на льду и затем добавляют воду (12 мл), после чего полученную смесь фильтруют и остаток промывают 50% уксусной кислотой с получением 2-(2-фтор-2',3',4',5',6'-пентадейтерийбифенил-4-ил)пропионовой кислоты (3,84 г).
К гидриду натрия (1,11 г, 60%-ный в масле) прибавляют тетрагидрофуран (30 мл) и затем при нагревании с обратным холодильником в течение более 40 минут по каплям прибавляют раствор, полученный растворением вышеуказанного сложного эфира (4,26 г) и ацетонитрила (1,14 мл) в тетрагидрофуране (10 мл). После нагревания с обратным холодильником в течение 2 часов раствор охлаждают до комнатной температуры и затем прибавляют изопропанол (15 мл), после чего полученную смесь нейтрализуют 3 н. соляной кислотой при охлаждении льдом и затем подвергают экстракции этилацетатом хлороформом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток растворяют в этаноле (20 мл) и затем прибавляют пиридин (7 мл) и гидрохлорид гидроксиламина (2,13 г), после чего полученную смесь перемешивают при комнатной температуре в течение 24 часов. Реакционную смесь концентрируют при пониженном давлении и затем прибавляют небольшое количество воды, после чего полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением остатка. Остаток очищают методом перекристаллизации из этанола с хлороформом с получением желаемого соединения (3,24 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,64 (д, 3Н, J=7,1 Гц), 4,11 (кв, 1Н, J= 7,1 Гц), 4,39 (ушир.с, 2Н), 4,94 (с, 1Н), 7,06-7,19 (м, 2Н), 7,38 (т, 1Н, J= 7,9 Гц).
Ссылочный пример 30
3-[1-(2-Фтор-2'-метоксибифенил-4-ил)этил] изоксазол-5-иламин (схема 112, приведенная в конце описания).
Тем же способом, что и по ссылочному примеру 29, получают желаемое соединение, за исключением использования метоксибензола.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,64 (д, 3Н, J=7,1 Гц), 3,81 (с, 3Н), 4,11 (кв, 1Н, J=7,1 Гц), 4,37 (ушир.с, 2Н), 4,95 (с, 1Н), 6,96-7,13 (м, 5Н), 7,23-7,48 (м, 2Н).
Ссылочный пример 31
3-[1-(2'-Фторбифенил-4-ил)этил] изоксазол-5-иламин (схема 113, приведенная в конце описания).
В атмосфере азота к хлориду алюминия (20,1 г) прибавляют метиленхлорид (100 мл) и при комнатной температуре прибавляют раствор, полученный растворением 2-фторбифенил (20,0 г) и ацетилхлорида (10,7 мл) в метиленхлориде (100 мл). После перемешивания в течение 4 часов к реакционной смеси прибавляют воду и смесь подвергает экстракции хлороформом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола с получением 1-(2'-фторбифенил-4-ил)этанона (17,53 г).
Этот кетон (17,53 г) растворяют в морфолине (130 мл) и затем прибавляют серу (5,25 г), после чего полученную смесь перемешивают при нагревании с обратным холодильником в течение 10 часов. Смесь охлаждают до комнатной температуры и затем прибавляют 1 н. соляную кислоту (500 мл), после чего реакционную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола с получением 2-(2'-Фторбифенил-4-ил)-1-морфолин-4-илэтантиона (21,69 г).
Это соединение растворяют в этаноле (200 мл) и затем прибавляют 15%-ный водный раствор гидроксида натрия (50 мл), после чего полученную смесь перемешивают при нагревании с обратным холодильником в течение 4 часов. После охлаждения до комнатной температуры растворитель концентрируют при пониженном давлении и прибавляют разбавленную соляную кислоту, после чего полученную смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола с получением (2'-фторбифенил-4-ил)уксусной кислоты (13,46 г).
Диизопропиламин (16,4 мл) растворяют в тетрагидрофуране (100 мл) и затем прибавляют гексановый раствор (30,3 мл, 1,66 М) н-бутиллития при охлаждении льдом, после чего полученную смесь перемешивают в течение 15 минут. Затем при охлаждении льдом прибавляют раствор, полученный растворением вышеуказанной карбоновой кислоты (13,44 г) в тетрагидрофуране (100 мл), и затем прибавляют гексаметилфосфортриамид (40 мл), после чего полученную смесь перемешивают в течение одного часа. Затем к полученной смеси прибавляют йодметан (3,63 мл) и полученную смесь перемешивают в течение 3 часов. К реакционной смеси прибавляют 10%-ную соляную кислоту и затем раствор подвергают экстракции этилацетатом. Органический слой промывают насыщенным водным раствором хлорида натрия, затем сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением 2-(2'-фторбифенил-4-ил)-пропионовой кислоты (16,64 г).
Эту карбоновую кислоту растворяют в этаноле (100 мл) и к раствору прибавляют конц. серную кислоту (2 мл), после чего раствор перемешивают при нагревании с обратным холодильником в течение 4 часов. Реакционную смесь разбавляют этилацетатом, нейтрализуют карбонатом натрия и затем подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 4/1) с получением этил 2-(2'-фторбифенил-4-ил)пропионата (9,26 г).
К гидриду натрия (2,12 г, 60%-ный в масле) прибавляют тетрагидрофуран (100 мл) и затем при нагревании с обратным холодильником в течение более одного часа по каплям прибавляют раствор, полученный растворением вышеуказанного сложного эфира (9,62 г) и ацетонитрила (3,67 мл) в тетрагидрофуране (100 мл). После нагревания с обратным холодильником в течение 5 часов полученную смесь охлаждают до комнатной температуры и затем прибавляют небольшое количество воды, после чего полученную смесь разбавляют этилацетатом и добавляют водный бикарбонат натрия. После экстракции этилацетатом органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 3/1) с получением 4-(2'-фторбифенил-4-ил)-3-оксопентанитрила (7,33 г).
Этот цианокетон растворяют в этаноле (120 мл) и затем прибавляют пиридин (20 мл) и гидрохлорид гидроксиламина (2,86 г), после чего полученную смесь перемешивают при 60oС в течение 8 часов. Реакционную смесь концентрируют при пониженном давлении, затем разбавляют этилацетатом и потом нейтрализуют водным раствором бикарбоната натрия, после чего смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 4/1) с получением желаемого соединения (6,31 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,65 (д, 3Н, J=7,1 Гц), 4,12 (кв, 1Н, J= 7,1 Гц), 4,36 (ушир.с, 2Н), 4,92 (с, 1Н), 7,10-7,53 (м, 8Н).
Ссылочный пример 32
3-[1-(2-Фтор-4'-метоксибифенил-4-ил)этил] изоксазол-5-иламин (схема 114, приведенная в конце описания).
2-(2-Фторбифенил-4-ил)пропионовую кислоту (104,2 г) растворяют в метаноле (410 мл) и затем прибавляют конц. серную кислоту (60,2 г), после чего полученную смесь перемешивают при 40oС в течение 2,5 часов. Смесь охлаждают до комнатной температуры, разбавляют толуолом, затем нейтрализуют насыщенным водным раствором бикарбоната натрия и потом подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением метил 2-(2-фторбифенил-4-ил)пропионата (110,2 г).
В атмосфере азота к хлориду алюминия (125,1 г) прибавляют этилендихлорид (700 мл) и затем прибавляют 2-фторбифенил (20,0 г). Раствор, полученный растворением ацетилхлорида (73,7 г) в этилендихлориде (300 мл), прибавляют по каплям при охлаждении льдом в течение более 2 часов. После перемешивания при 20-30oС в течение 2 часов температуру повышают до 40-60oС и перемешивание проводят в течение 3 часов. После охлаждения до комнатной температуры прибавляют небольшое количество воды к реакционной смеси и затем прибавляют соляную кислоту, после чего полученную смесь подвергают экстракции этилендихлоридом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают колоночной хроматографией на силикагеле (гексан/этилацетат = 10/1 --> 7/1) с получением метил 2-(4'-ацетил-2-фторбифенил-4-ил)пропионата (107,6 г).
Этот сложный эфир растворяют в метиленхлориде (670 мл) и затем прибавляют при комнатной температуре м-хлорнадбензойную кислоту (110,3 мг), после чего полученную смесь перемешивают при нагревании с обратным холодильником в течение 20 часов. После охлаждения до комнатной температуры м-хлорнадбензойную кислоту удаляют фильтрацией и остаток промывают 20% водным раствором тиосульфата натрия и затем насыщенным водным раствором бикарбоната натрия. Маточный раствор экстрагируют хлороформом и затем органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают методом перекристаллизации из этанола из гексанаэтилацетата (130/1) с получением метил 2-(4'-ацетокси-2-фторбифенил-4-ил)пропионата (97,0 г).
Это соединение растворяют в метаноле (1000 мл) и затем прибавляют 20%-ный водный раствор гидроксида натрия (200 мл), после чего полученную смесь перемешивают при 35oС в течение 3 часов. После охлаждения до комнатной температуры растворитель концентрируют при пониженном давлении и прибавляют воду (1500 мл) и затем прибавляют 4 н. соляную кислоту для установления рН 1. Остаток промывают водой и затем сушат в вакууме при 60oС с получением 2-(2-фтор-4'-гидроксибифенил-4-ил)пропионовой кислоты (68,6 г).
Эту карбоновую кислоту (67,6 г) растворяют в ацетоне (1300 мл) и затем прибавляют карбонат калия (100,9 г) и диметилсульфат (92,1 г), после чего полученную смесь перемешивают при нагревании с обратным холодильником в течение 5 часов. Реакционную смесь фильтруют и полученный фильтрат концентрируют при пониженном давлении.
К этому осадку прибавляют метанол (1000 мл) и затем 20% водный раствор гидроксида натрия (150 мл), после чего полученную смесь перемешивают при 35oС в течение 2 часов. После охлаждения до комнатной температуры растворитель концентрируют при пониженном давлении и затем прибавляют воду (1000 мл), после чего прибавляют 4 н. соляную кислоту для установления рН 1 и проводят экстракцию хлороформом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении.
Остаток растворяют в этаноле (300 мл) и затем прибавляют конц. серную кислоту (34,4 г), после чего полученную смесь перемешивают при нагревании с обратным холодильником в течение 2 часов. Реакционную смесь охлаждают до комнатной температуры, разбавляют толуолом, нейтрализуют насыщенным водным раствором бикарбоната натрия и потом подвергают экстракции толуолом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением этил 2-(2-фтор-4'-метоксибифенил-4-ил)пропионата (82,9 г).
После прибавления к гидриду натрия (19,7 г, 60%-ный в масле) тетрагидрофурана (300 мл) по каплям при нагревании с обратным холодильником в течение более 45 минут прибавляют раствор, полученный растворением вышеуказанного эфира (82,9 г) и ацетонитрила (20,3 г) в тетрагидрофуране. После перемешивания при нагревании с обратным холодильником в течение 1,5 часов полученную смесь охлаждают до комнатной температуры и прибавляют изопропанол (50 мл), после чего смесь нейтрализуют 3 н. соляной кислотой и затем подвергают экстракции хлороформом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением 4-(2-фтор-4'-метоксибифенил-4-ил)-3-оксопентанитрила (89,1 г).
После того, как этот цианокетон растворяют в этаноле (200 мл), прибавляют пиридин (60 мл) и гидрохлорид гидроксиламин (38,1 г) и полученную смесь перемешивают при 70oС в течение 4 часов. Реакционную смесь концентрируют при пониженном давлении, разбавляют этилацетатом, после чего нейтрализуют водным раствором бикарбоната натрия и затем смесь подвергают экстракции этилацетатом. Органический слой сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением желаемого соединения (79,36 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,63 (д, 3Н, J=7,3 Гц), 3,85 (с, 3Н), 4,09 (кв, 1H, J=7,3 Гц), 4,38 (ушир.с, 2Н), 4,93 (с, 1H), 6,94-7,00 (м, 2Н), 7,04-7,13 (м, 2Н), 7,31-7,38 (м, 2Н), 7,44-7,49 (м, 2Н).
Ссылочный пример 33
Метил 2-(9Н-карбазол-2-ил)пропионат (схема 115, приведенная в конце описания).
Желаемое соединение получают тем же способом, что и по известному способу [P. S. Manchand et al., Heterocycles, 39, 833 (1994)] за исключением использования карбазола.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,59 (д, 3Н, J=7,1 Гц), 3,67 (с, 3Н), 3,89 (кв, 1H, J=7,1 Гц), 7,15-7,25 (м, 2Н), 7,36-7,43 (м, 3Н), 7,98-8,10 (м, 3Н).
Ссылочный пример 34
{3-[1-(9Н-карбазол-2-ил)этил]изоксазол-5-ил}амин (схема 116, приведенная в конце описания).
Желаемое соединение получают тем же способом, что и по второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 33.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 1,71 (д, 3Н, J=7,1 Гц), 4,24 (кв, 1Н, J= 7,1 Гц), 4,90 (с, 1Н), 7,15-7,25 (м, 2Н), 7,34-7,44 (м, 3Н), 7,98-8,05 (м, 3Н).
Ссылочный пример 35
3-(2-Фторбифенил-4-илметил)изоксазол-5-иламин (схема 117, приведенная в конце описания).
Желаемое соединение получают тем же способом, что и по ссылочному примеру 26, за исключением использования (2-фторбифенил-4-ил)уксусной кислоты.
1H-ЯМР (300 МГц, СDСl3) δ м.д.: 3,88 (с, 2Н), 4,97 (с, 1Н), 7,04-7,14 (м, 2Н), 7,33-7,47 (м, 4Н), 7,51-7,55 (м, 3Н).
Ссылочный пример 36
Этил 2-(2,3-дигидробензо[1,4]диоксин-6-ил)пропионат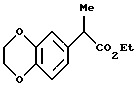
В атмосфере азота на ледяной бане 60%-ный гидрид натрия (1,13 г) прибавляют к раствору в N,N-диметилформамиде (65 мл) 3,4-этилендиоксифенилацетата [М. Sasamoto, Chem. Pharm. Bull., 8, 324 (1969)] (6,00 г). Затем по каплям прибавляют метилйодид (1,76 мл) и полученную смесь перемешивают при охлаждении льдом в течение 4 часов. К реакционной смеси прибавляют 1 н. соляную кислоту и полученную смесь подвергают экстракции диэтиловым эфиром, после чего экстракционный раствор промывают водой и сушат. Растворитель удаляют отгонкой при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (5,57 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,22 (т, 3Н, J=7,3 Гц), 1,44 (д, 3Н, J= 7,3 Гц), 3,59 (кв, 1Н, J=7,3 Гц), 4,05-4,17 (м, 2Н), 4,24 (с, 4Н), 6,74 (м, 3Н).
Ссылочный пример 37
3-[1-(2,3-Дигидробензо[1,4]диоксин-4-ил)этил]изоксазол-5-иламин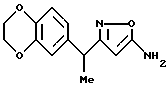
Желаемое соединение получают тем же способом, что и во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 36.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,56 (д, 3Н, J=7,3 Гц), 3,97 (кв, 1Н, J= 7,3 Гц), 4,23 (с, 4Н), 4,33 (ушир.с, 2Н), 4,88 (с, 1Н), 6,73-6,82 (м, 3Н).
Ссылочный пример 38
3-[1-(1-Метил-1H-индол-3-ил)этил]изоксазол-5-иламин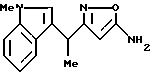
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования этил 2-(1-метил-1Н-индол-3-ил)-пропионата [L. K. Mehta et al., J. Chem. Soc., Perkin Trans. 2, 1488 (1997)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,69 (д, 3Н, J=7,3 Гц), 3,74 (с, 3Н), 4,26 (ушир. с, 2Н), 4,36 (кв, 1Н, J=7,3 Гц), 4,88 (с, 1Н), 6,91 (с, 1Н), 7,04-7,29 (м, 3Н), 7,62 (д, 1Н, J=7,9 Гц).
Ссылочный пример 39
3-[1-(1H-Индол-3-ил)этил]изоксазол-5-иламин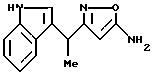
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования этил 2-(1H-индол-3-ил)пропионата [М. Julia et al., Bull. Soc. Chim. Fr. 2291 (1966)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,70 (д, 3Н, J=7,3 Гц), 4,25 (ушир.с, 2Н), 4,37 (кв, 1Н, J=7,3 Гц), 4,87 (с, 1Н), 7,05-7,21 (м, 3Н), 7,34 (д, 1Н, J=8,2 Гц), 7,62 (д, 1Н, J=7,9 Гц), 8,04 (ушир.с, 1Н).
Ссылочный пример 40
Метил 2-(1-метил-1Н-индол-2-ил)пропионат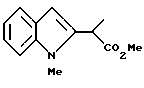
Смесь 1-метил-2-(2'-карбоксиметоксивинил)индола [F.E. Ziegler et al., J. Am. Chem. Soc., 95, 7146 (1973)] (335 мг), 10%-ного палладия/активного угля (50 мг) и тетрагидрофурана (4 мл) подвергают гидрированию при комнатной температуре в течение 30 минут. Реакционную смесь фильтруют для удаления катализатора и затем концентрируют при пониженном давлении, после чего остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (168 мг).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,65 (д, 3Н, J=7,3 Гц), 3,69 (с, 3Н), 3,72 (с, 3Н), 3,97 (кв, 1Н, J=7,3 Гц), 6,43 (с, 1Н), 7,05-7,31 (м, 3Н), 7,57 (д, 1Н, J=7,9 Гц).
Ссылочный пример 41
3-[1-(1-Метил-1Н-индол-2-ил)этил]изоксазол-5-иламин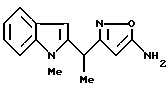
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 40.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,72 (д, 3Н, J=7,3 Гц), 3,64 (с, 3Н), 4,30-4,33 (м, 3Н), 4,81 (с, 1Н), 6,44 (с, 1Н), 7,05-7,28 (м, 3Н), 7,57 (д, 1Н, J=7,9 Гц).
Ссылочный пример 42
Этил 2-бензофуран-5-илпропионат (схема 118, приведенная в конце описания).
К раствору 5-бензофуранкарбонитрила (не подвергнутая экспертизе японская патентная публикация 9-124631) (1,30 г) в тетрагидрофуране (5 мл) прибавляют 0,87 М раствор метилмагнийбромида в тетрагидрофуране (21 мл) и полученную смесь нагревают с обратным холодильником в течение 4 часов в атмосфере азота. Реакционную смесь подкисляют конц. серной кислотой и добавляют воду, после чего полученную смесь подвергают экстракции диэтиловым эфиром. Экстракционный раствор промывают водой, сушат и затем отгоняют при пониженном давлении для удаления растворителя. Остаток очищают колоночной хроматографией на силикагеле с получением 1-бензофуран-5-илэтанона (1,21 г).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 2,67 (с, 3Н), 6,86 (д, 1Н, J=2,3 Гц), 7,55 (д, 1Н, J= 8,9 Гц), 7,70 (д, 1Н, J=2,3 Гц), 7,97 (дд, 1Н, J=8,9, 1,7 Гц), 8,26 (д, 1Н, J=1,7 Гц).
Смесь 1-бензофуран-5-илэтанона (850 мг), триметилсилилцианида (0,85 мл), йодида цинка (34 мг) и хлороформа (21 мл) нагревают с обратным холодильником в течение 3,5 часов в атмосфере азота. Растворитель удаляют отгонкой при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого циано производного (1,21 г).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 0,18 (с, 9Н), 1,91 (с, 3Н), 6,80 (м, 1Н), 7,45-7,54 (м, 2Н), 7,67 (д, 1Н, J=2,0 Гц), 7,81 (с, 1Н).
К раствору этого цианосоединения (1,21 г) в уксусной кислоте (10 мл) прибавляют дигидрат хлорида олова (II) и полученную смесь перемешивают при комнатной температуре в течение 10 минут, после чего прибавляют конц. соляную кислоту (20 мл) и смесь перемешивают при комнатной температуре в течение ночи. Реакционную смесь затем нагревают и перемешивают при 100oС в течение 2,5 часов и добавляют воду, после чего полученную смесь подвергают экстракции диэтиловым эфиром. Экстракционный раствор промывают водой и сушат. Растворитель отгоняют при пониженном давлении и к осадку прибавляют этанол (4 мл) и конц. серную кислоту (0,05 мл), после чего полученную смесь нагревают и перемешивают при 80oС в течение 2,5 часов. Растворитель удаляют отгонкой при пониженном давлении и к осадку добавляют воду, после чего полученную смесь подвергают экстракции диэтиловым эфиром. Экстракционный раствор промывают водой и сушат. Растворитель удаляют отгонкой при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (601 мг).
1H-ЯМР (270 МГц, СD3Сl) δ м.д.: 1,20 (т, 3Н, J=7,3 Гц), 1,54 (д, 3Н, J= 7,3 Гц), 3,80 (кв, 1Н, J=7,3 Гц), 4,05-4,19 (м, 2Н), 6,74 (д, 1Н, J=2,3 Гц), 7,24 (д, 1Н, J=8,6 Гц), 7,45 (д, 1Н, J=8,6 Гц), 7,54 (с, 1Н), 7,61 (д, 1Н, J=2,3 Гц).
Ссылочный пример 43
3-(1-Бензофуран-5-илэтил)изоксазол-5-иламин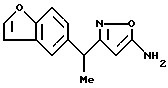
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 42.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,3 Гц), 4,17 (кв, 1H, J= 7,3 Гц), 4,32 (ушир.с, 2Н), 4,86 (с, 1Н), 6,72 (д, 1H, J=2,3 Гц), 7,22 (дд, 1H, J=8,6, 1,7 Гц), 7,43 (д, 1H, J=8,6 Гц), 7,51 (д, 1H, J=1,7 Гц), 7,60 (д, 1H, J=2,3 Гц).
Ссылочный пример 44
Этил 2-бензофуран-6-илпропионат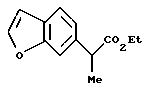
Желаемое соединение получают тем же способом, что и по ссылочному примеру 42.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,21 (т, 3Н, J=7,3 Гц), 1,55 (д, 3Н, J= 7,3 Гц), 3,82 (кв, 1H, J=7,3 Гц), 4,06-4,18 (м, 2Н), 6,74 (д, 1H, J=2,3 Гц), 7,20 (д, 1H, J=7,9 Гц), 7,47 (с, 1H), 7,53 (д, 1H, J=7,9 Гц), 7,6 (д, 1H, J= 2,3 Гц).
Ссылочный пример 45
3-(1-Бензофуран-6-илэтил)изоксазол-5-иламин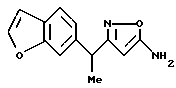
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 44.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,66 (д, 3Н, J=7,3 Гц), 4,19 (кв, 1H, J= 7,3 Гц), 4,32 (ушир.с, 2Н), 4,87 (с, 1Н), 6,73 (д, 1H, J=2,3 Гц), 7,18 (д, 1H, J=8,3 Гц), 7,44 (с, 1H), 7,52 (д, 1H, J=8,3 Гц), 7,59 (д, 1H, J=2,3 Гц).
Ссылочный пример 46
(S)-3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-иламин (схема 119, приведенная в конце описания).
В качестве способа, отличающегося от способа получения соединения по ссылочному примеру 27, осуществляют следующий способ: в атмосфере азота смесь тетрагидрофурана (73 мл) и амида лития (1,61 г) нагревают при 68oС и прибавляют по каплям трет-бутилцианоацетат (11,1 г). Затем раствор концентрируют до количества в 30 г при продувании смеси азотом и затем охлаждают до комнатной температуры. Прибавляют тетрагидрофуран до достижения количества содержимого в 50 г и затем полученную смесь охлаждают до -10oС. В отдельном реакционном сосуде в атмосфере азота прибавляют по каплям (S)-2-(2-фторбифенил-4-ил)пропионовую кислоту (10,1 г, 99% е.е.) и прибавляют по каплям к тетрагидрофурановому раствору (27 мл) изобутилхлорформиата (5,57 г), тетрагидрофурановый раствор (27 мл) N-метилморфолина (5,2 мл), при -10oС. Через 10 минут этот раствор добавляют к предшествующей смеси, после чего полученную смесь перемешивают при комнатной температуре в течение ночи.
Кристаллический осадок отделяют фильтрацией и сушат при пониженном давлении с получением желаемой литиевой соли.
1H-ЯМР (300 МГц, d6-DMSO) δ м.д.: 1,31 (д, 3Н, J=6,8 Гц), 1,37 (с, 9Н), 4,21 (кв, 1H, J=6,8 Гц), 7,15-7,22 (м, 2Н), 7,35-7,52 (м, 6Н).
Nа2НРO4 (826 мл) растворяют в воде (11,6 мл) и у полученного раствора устанавливают рН 8,0 с помощью 1 н. фосфорной кислоты, после чего прибавляют гидрохлорид гидроксиламина (78,1 г). К полученной смеси прибавляют по каплям раствор литиевой соли (1,40 г), полученной выше, в изопропаноле (11,7 мл) при 80oС и полученную смесь перемешивают в течение одного часа, после чего температуру возвращают до комнатной температуры и к смеси прибавляют воду (27 мл) для кристаллизации желаемого соединения. Кристаллы отделяют фильтрацией и сушат при пониженном давлении с получением желаемого амина (875 мг, 98% е.е.).
Ссылочный пример 47
3-(1-Хинолин-3-илэтил)изоксазол-5-иламин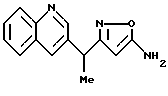
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования метилового эфира 2-хинолин-3-илпропионовой кислоты [Т. Sakamoto et al., Heterocycles, 36, 2509 (1997)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,71 (д, 3Н, J=7,3 Гц), 4,27 (кв, 1Н, J= 7,3 Гц), 4,61 (ушир.с, 2Н), 4,87 (с, 1Н), 7,49-7,79 (м, 3Н), 8,01-8,09 (м, 2Н), 8,84 (д, 1Н, J=2,0 Гц).
Ссылочный пример 48
3-(1-Изохинолин-4-илэтил)изоксазол-5-иламин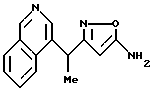
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования метилового эфира 2-изохинолин-4-илпропионовой кислоты [Т. Sakamoto et al., Heterocycles, 36, 2509 (1997)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,81 (д, 3Н, J=7,3 Гц), 4,52 (ушир.с, 2Н), 4,71-4,78 (м, 2Н), 7,57-7,74 (м, 2Н), 7,98 (д, 1Н, J=7,6 Гц), 8,14 (д, 1Н, J=8,2 Гц), 8,50 (с, 1Н), 9,16 (с, 1Н).
Ссылочный пример 49
Метиловый эфир бифенил-4-илдиметоксиуксусной кислоты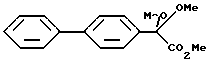
Смесь метилового эфира бифенил-4-илоксоуксусной кислоты (А.Т. Jeffries et al. , J.Org.Chem.,46, 2885(1981)) (10 г), триэтилороформиат (43 мл), метанол (60 мл) и конц. серную кислоту (3 мл) нагревают с обратным холодильником в течение 8,5 часов в атмосфере азота. Полученную смесь выливают в насыщенный водный раствор бикарбоната натрия и полученную смесь подвергают экстракции диэтиловым эфиром. Органический слой промывают насыщенным водным раствором хлорида натрия, затем сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением желаемого соединения (10,5 г).
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,31 (с, 6Н), 3,75 (с, 3Н), 7,35-7,47 (м, 3Н), 7,58-7,69 (м, 6Н).
Ссылочный пример 50
3-(Бифенил-4-илдиметоксиметил)изоксазол-5-иламин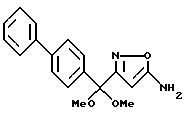
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 49.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,27 (с, 6Н), 4,38 (ушир.с, 2Н), 5,02 (с, 1Н), 7,31-7,46 (м, 3Н), 7,56-7,67 (м, 6Н).
Ссылочный пример 51
Метиловый эфир диметокси-(1-метил-1Н-индол-2-ил)уксусной кислоты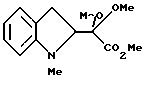
Желаемое соединение получают тем же способом, что и по примеру 49, за исключением использования метилового эфира (1-метил-1Н-индол-2-ил)оксоуксусной кислоты [F.E. Ziegler, et al., J. Am. Chem. Soc., 95, 7146 (1973)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,32 (с, 6Н), 3,77 (с, 3Н), 3,78 (с, 3Н), 6,85 (с, 1Н), 7,10-7,35 (м, 3Н), 7,63 (д, 1Н, J=7,9 Гц).
Ссылочный пример 52
3-[Диметокси-(1-метил-1Н-индол-2-ил)метил]изоксазол-5-иламин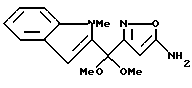
Желаемое соединение получают тем же способом, что представлен во второй половине ссылочного примера 20, за исключением использования соединения, полученного по ссылочному примеру 51.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 3,27 (с, 6Н), 3,68 (с, 3Н), 4,38 (ушир. с, 2Н), 4,92 (с, 1Н), 6,86 (с, 1Н), 7,08-7,31 (м, 3Н), 7,63 (д, 1Н, J=7,9 Гц).
Ссылочный пример 53
3-{ 1-Метил-1-[3-(2-фенил[1,3] диоксолан-2-ил)фенил]этил}-изоксазол-5-иламин (схема 120, приведенная в конце описания).
Кетопрофен (10 г) растворяют в N,N-диметилформамиде (50 мл) в атмосфере азота. К раствору прибавляют гидрид натрия (3,95 г, 60%-ный в масле) с последующим перемешиванием. Спустя тридцать минут после перемешивания прибавляют метилйодид (6,1 мл) и затем перемешивают в течение 10 часов. К реакционному раствору прибавляют ледяную воду и насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Экстракционный раствор промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом натрия и затем концентрируют при пониженном давлении с получением осадка (12,78 г).
Часть осадка растворяют в бензоле (100 мл) и к полученному раствору прибавляют этиленгликоль (10 мл) и п-толуолсульфоновую кислоту (10 г) с последующим дегидратированием при нагревании с обратным холодильником в течение 200 часов. К полученному раствору прибавляют насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Экстракционный раствор промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом натрия и концентрируют при пониженном давлении с получением остатка (9,30 г).
Часть осадка (1,00 г) растворяют в метаноле (10 мл) и к полученному раствору прибавляют 10%-ный водный раствор гидроксида калия (10 мл) с последующим перемешиванием в течение 10 часов. Реакционный раствор концентрируют отгонкой метанола. К полученному продукту прибавляют 2 н. соляную кислоту с последующей экстракцией этилацетатом. Экстракционный раствор промывают насыщенным водным раствором хлорида натрия, сушат над сульфатом натрия и концентрируют при пониженном давлении с получением остатка (0,56 г).
С другой стороны к гидриду натрия (220 мг, 60%-ный в масле) прибавляют по каплям тетрагидрофуран (10 мл) и затем трет-бутилцианоацетат (0,76 мл) при охлаждении льдом в атмосфере азота. Затем полученную смесь перемешивают при охлаждении льдом с получением натриевой соли трет-бутилцианоацетата.
С другой стороны, раствор остатка (0,56 г), полученного выше, и N-метилморфолина (0,24 мл) в тетрагидрофуране (5 мл) прибавляют по каплям к раствору изопропилхлорформиата (0,26 мл) в тетрагидрофуране (5 мл) при перемешивании при -15oС. Тридцать минут спустя после перемешивания к полученному раствору прибавляют по каплям натриевую соль трет-бутилцианоацетата, полученного выше. Через один час к полученной смеси прибавляют насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетатом. Экстракционный раствор сушат над сульфатом натрия и концентрируют при пониженном давлении с получением вязкого остатка.
К остатку прибавляют гидрохлорид гидроксиламина (500 мг), этанол (16 мл) и пиридин (4 мл) с последующим перемешиванием при 50oС в течение 4 часов. После охлаждения реакционного раствора до комнатной температуры этанол отгоняют с получением остатка. К остатку прибавляют насыщенный водный раствор гидрокарбоната натрия с последующей экстракцией этилацетата. Экстракт сушат над сульфатом натрия и концентрируют при пониженном давлении с получением остатка.
Остаток очищают колоночной хроматографией на силикагеле с получением желаемого соединения (37,9 г).
1H-ЯМР (300 МГц, СD3Сl) δ м.д.: 1,66 (с, 6Н), 4,05 (с, 4Н), 4,26 (ушир. с, 2Н), 4,73 (с, 1Н), 7,21-7,60 (м, 9Н).
Ссылочный пример 54
Метиловый эфир 2-(6-фенилпиридин-3-ил)пропионовой кислоты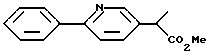
Желаемое соединение получают из 5-бром-2-фенилпиридина [J.W. Tilley, et al. , J. Am. Chem. Soc., 53, 386 (1988)] известным способом, описанным [Т. Sakamoto et al., Heterocycles, 36, 2509 (1997)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,57 (д, 3Н, J=7,3 Гц), 3,67 (с, 3Н), 3,80 (кв, 1H, J=7,3 Гц), 7,41-7,50 (м, 3Н), 7,71-7,72 (м, 2Н), 7,97 (д, 2Н, J=6,6 Гц), 8,61 (с, 1H).
Ссылочный пример 55
3-[1-(6-Фенилпиридин-3-ил)этил]изоксазол-5-иламин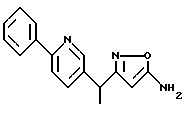
Желаемое соединение получают исходя из соединения, полученного по ссылочному примеру 54 тем же способом, что описан во второй половине ссылочного примера 20.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,67 (д, 3Н, J=7,3 Гц), 4,14 (кв, 1Н, J= 7,3 Гц), 4,43 (ушир.с, 2Н), 4,91 (с, 1Н), 7,40-7,49 (м, 3Н), 7,70 (м, 2Н), 7,96 (дд, 2Н, J=8,3, 1,7 Гц), 8,63 (с, 1Н).
Ссылочный пример 56
Метиловый эфир 2-(5-фенилпиридин-2-ил)пропионовой кислоты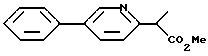
Желаемое соединение получают из 2-бром-5-фенилпиридина [M.G. Knize, et al. , Heterocycles, 24, 1815 (1986)] известным способом, описанным [Т. Sakamoto et al., Heterocycles, 36, 2509 (1993)].
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,61 (д, 3Н, J=7,3 Гц), 3,72 (с, 3Н), 4,01 (кв, 1Н, J=7,3 Гц), 7,34-7,59 (м, 6Н), 7,85 (дд, 1Н, J=8,2, 2,3 Гц), 8,78 (д, 1Н, J=2,3 Гц).
Ссылочный пример 57
3-[1-(5-Фенилпиридин-2-ил)этил]изоксазол-5-иламин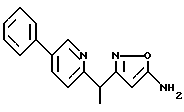
Желаемое соединение получают исходя из соединения, полученного по ссылочному примеру 54 тем же способом, что описан во второй половине ссылочного примера 20.
1H-ЯМР (270 МГц, СDСl3) δ м.д.: 1,71 (д, 3Н, J=7,3 Гц), 4,30 (кв, 1Н, J= 7,3 Гц), 4,39 (ушир.с, 2Н), 5,08 (с, 1Н), 7,32-7,57 (м, 6Н), 7,81 (дд, 2Н, J=8,3, 2,3 Гц), 8,79 (д, 1Н, J=2,3 Гц).
Пример А1
Оксим (3-{ 1-[5-(аминоморфолин-4-илметиленамино)-изоксазол-3-ил]метилэтил}фенил)фенилметанона (схема 121, приведенная в конце описания).
Желаемое соединение было получено исходя из соединения, полученного в ссылочном примере В1 по способу примера 54.
1H-ЯМР (300 МГц) (СDСl3): 1,66 (с, 4,8Н), 1,69 (с, 1,2Н), 3,45-3,49 (м, 4Н), 3,69-3,74 (м, 4Н), 5,12 (с, 0,8Н), 5,15 (с, 0,2Н), 5,38 (ушир. с, 2Н), 7,09-7,46 (м, 9Н), 7,64 (ушир.с, 1Н).
Пример А2
Метансульфонат (3-{1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] метилэтил}фенил)фенилметанона (схема 122, приведенная в конце описания).
К раствору соединения, полученного по примеру А1 (1,06 г), в тетрагидрофуране (5 мл) добавляли 3 н. соляную кислоту (15 мл) и перемешивали в течение 60 часов. После подщелачивания полученного раствора путем добавления насыщенного водного раствора гидрокарбоната натрия реакционный раствор экстрагировали этилацетатом, сушили над сульфатом натрия и концентрировали при пониженном давлении. Полученный остаток растворяли в 1,4-диоксане (20 мл) с последующим добавлением метансульфокислоты (0,17 мл). Затем раствор перемешивали в течение 30 минут. Полученный реакционный раствор концентрировали и полученный остаток перекристаллизовывали в толуоле с получением желаемого соединения (0,79 г).
1H-ЯМР (300 МГц) (СDСl3): 1,75 (с, 6Н), 2,68 (с, 3Н), 3,55-3,59 (м, 4Н), 3,74-3,78 (м, 4Н), 5,86 (с, 1Н), 7,49-7,76 (м, 9Н).
Пример A3
(трет-Бутоксикарбонил)-[{ 3-[1-(2-фторбифенил-4-ил)-этил] изоксазол-5-илимино} -(1-оксо-[1,4] тиазинан-4-ил)метил] амин (схема 123, приведенная в конце описания).
Соединение, полученное в примере 117 (2,55 г), растворяли в хлороформе (20 мл) с последующим добавлением гидрокарбоната натрия (0,84 г). К раствору при охлаждении добавляли метахлорпербензойную кислоту (1,30 г) и перемешивали в течение 30 минут при охлаждении льдом. К полученному раствору добавляли насыщенный водный раствор гидрокарбоната натрия (20 мл), и избыток перекиси поглощали сульфитом натрия. Полученную смесь экстрагировали хлороформом, и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и сушили. Растворитель отгоняли при пониженном давлении, и полученный остаток очищали путем колоночной хроматографии на силикагеле с получением желаемого соединения (2,62 г).
1H-ЯМР (300 МГц) (СDСl3): 1,44 (с, 9Н), 1,67 (д, 3Н, J=7,3 Гц), 2,81-2,99 (м, 4Н), 3,95-4,22 (м, 5Н), 5,33 (с, 1Н), 7,06-7,17 (м, 3Н), 7,31-7,48 (м, 4Н), 7,49-7,54 (м, 2Н).
Пример 4А
(трет-Бутоксикарбонил)-((1,1-диоксо-[1,4] тиазинан-4-ил)-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино}-метил)амин (схема 124, приведенная в конце описания).
Соединение, полученное по примеру 117 (2,55 г), растворяли в хлороформе (20 мл) и добавляли гидрокарбонат натрия (0,84 г). К раствору при комнатной температуре добавляли метахлорпербензойную кислоту (1,30 г) и перемешивали в течение 1,5 часа при комнатной температуре. К полученному раствору добавляли насыщенный водный раствор гидрокарбоната натрия (20 мл), и избыток перекиси поглощали сульфитом натрия. Полученную смесь экстрагировали хлороформом, и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и сушили. Растворитель отгоняли при пониженном давлении, и полученный остаток очищали путем колоночной хроматографии на силикагеле с получением желаемого продукта (1,29 г).
1H-ЯМР (300 МГц) (СDСl3): 1,44 (с, 9Н), 1,67 (д, 3Н, J=7,1 Гц), 3,15-3,21 (м, 4Н), 4,00-4,07 (м, 4Н), 4,18 (кв, 1Н, J=7,1 Гц), 5,38 (с, 1Н), 7,04-7,17 (м, 2Н), 7,22 (ушир. 1Н), 7,32-7,47 (м, 4Н), 7,48-7,54 (м, 2Н).
Пример А5
N-(трет-Бутоксикарбонил)-N'-{ 3-[1-(2-фторбифенил-4-ил) этил] изоксазол-5-ил} -N''-пиридин-3-илметилгуанидин (схема 125, приведенная в конце описания).
Желаемое соединение получали способом, указанным в примере 1.
1H-ЯМР (300 МГц) (СDСl3): 1,48 (с, 9Н), 1,67 (д, 3Н, J=7,3 Гц), 4,14 (кв, 1H, J=7,3 Гц), 4,57 (д, 2Н, J=5,7 Гц), 5,35 (с, 1H), 7,07-7,17 (м, 2Н), 7,24-7,29 (м, 1Н), 7,32-7,45 (м, 4Н), 7,50-7,54 (м, 2Н), 7,64-7,71 (м, 1H), 8,41 (ушир. 1H), 8,50-8,54 (м, 1H), 8,57-8,61 (м, 2Н).
Пример А6
[{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-илимино} -(1-оксо[1,4]тиазинан-4-ил)метил]амин (схема 126, приведенная в конце описания).
Желаемое соединение получали исходя из соединения, полученного по примеру A3 способом, указанным в примере 48.
1H-ЯМР (300 МГц) (СDСl3): 1,68 (д, 3Н, J=7,1 Гц), 2,80 (т, 4Н, J=5,0 Гц), 4,02-4,10 (м, 4Н), 4,15 (кв, 1Н, J=7,1 Гц), 5,28 (с, 1H), 5,45 (ушир, 2Н), 7,07-7,17 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример А7
(1,1-Диоксо-[1,4] тиазинан-4-ил-{3-[1-(2-фторбифенил-4-ил)этил]изоксазол-5-илимино}метил)амин (схема 127, приведенная в конце описания).
Желаемое соединение получали исходя из соединения, полученного по примеру А4 способом, указанным в примере 48.
1H-ЯМР (300 МГц) (СDСl3): 1,67 (д, 3Н, J=7,1 Гц), 3,10 (т, 4Н, J=5,2 Гц), 4,00 (т, 4Н, J=5,2 Гц), 4,16 (кв, 1H, J=7,1 Гц), 5,33 (с, 1H), 5,48 (ушир, 2Н), 7,06-7,17 (м, 2Н), 7,33-7,46 (м, 4Н), 7,50-7,54 (м, 2Н).
Пример А8
N-{ 3-[1-(2-Фторбифенил-4-ил)этил] изоксазол-5-ил}-N'-пиридин-3-илметилгуанидин (схема 128, приведенная в конце описания).
Желаемое соединение получали исходя из соединения, полученного по примеру А5 способом, указанным в примере 48.
1H-ЯМР (300 МГц) (СDСl3): 1,68 (д, 3Н, J=7,1 Гц), 4,11 (кв, 1H, J=7,1 Гц), 4,46 (д, 2Н, J=4,4 Гц), 5,25 (с, 1H), 5,48 (ушир, 2Н), 5,71 (ушир., 1H), 7,04-7,14 (м, 2Н), 7,21-7,25 (м, 1Н), 7,32-7,46 (м, 4Н), 7,49-7,53 (м, 2Н), 7,65 (д, 1Н, J=7,9 Гц), 8,44-8,49 (м, 2Н).
Ссылочный Пример В1
Оксим { 3-[1-(5-аминоизоксазол-3-ил)-1-метилэтил] -фенил} фенилметана (схема 129, приведенная в конце описания).
В атмосфере азота кетопрофен (10 г) растворяли в N,N-диметилформамиде (50 мл). К раствору добавляли гидрид натрия (4,72 г, 60% в масле) и перемешивали. Через 30 минут добавляли метилйодид (6,1 мл) и перемешивали в течение 10 часов. К полученному реакционному раствору добавляли ледяную воду и насыщенный водный раствор гидрокарбоната натрия и экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия и концентрировали при пониженном давлении с получением остатка (10,28 г). Полученный остаток растворяли в метаноле (70 мл) и к раствору добавляли 10% водный раствор гидроксида калия (70 мл). Полученный раствор перемешивали в течение 24 часов. Полученный реакционный раствор концентрировали и подкисляли добавлением 4 н. соляной кислоты. Раствор экстрагировали этилацетатом, и органический слой промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия и концентрировали при пониженном давлении с получением остатка (9,31 г).
В атмосфере азота к гидриду натрия (4,2 г, 60% в масле) добавляли тетрагидрофуран (100 мл) при охлаждении льдом, и при перемешивании по каплям добавляли трет-бутилцианоацетат (14,8 мл). Затем полученную смесь перемешивали при охлаждении льдом в течение 30 минут с получением цианацетата натрия.
С другой стороны, в другом реакционном сосуде, в атмосфере азота к раствору изобутилхлорформиата (5,40 мл) в тетрагидрофуране (100 мл) по каплям добавляли раствор остатка, полученного, как указано выше (9,31 г), и N-метилморфолина (4,57 мл) в тетрагидрофуране (100 мл) при 15oС при перемешивании. Через 30 минут полученный раствор по каплям добавляли к полученному выше цианацетату натрия. Спустя час, полученный реакционный раствор выливали в насыщенный водный раствор хлорида натрия и экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия и концентрировали при пониженном давлении с получением вязкого жидкого остатка. Полученный остаток промывали гексаном с получением осадка (19,73 г). Полученный осадок растворяли в 1,4-диоксане (150 мл) и к раствору добавляли раствор метансульфокислоты (20 мл) в воде (10 мл) с последующим кипячением с обратным холодильником при нагревании. Через четыре часа реакционный раствор концентрировали и к остатку добавляли насыщенный водный раствор хлорида натрия с последующей экстракцией этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия и концентрировали при пониженном давлении с получением осадка (10,5 г). К осадку добавляли гидрохлорид гидроксиламина (8,2 г), этанол (150 мл) и пиридин (30 мл). Смесь перемешивали при 50oС в течение 8 часов и затем перемешивали при комнатной температуре в течение 60 часов. Из реакционного раствора отгоняли этанол и к полученному остатку добавляли насыщенный водный раствор гидрокарбоната натрия, экстрагировали этилацетатом, сушили над сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали путем колоночной хроматографии на силикагеле с получением желаемого соединения (7,63 г), которое представляло собой смесь двух пространственных изомеров в соотношении 4:1.
1H-ЯМР (300 МГц) (СDСl3): 1,57 (с, 4,8Н), 1,61 (с, 1,2Н), 4,71 (с, 0,2Н), 4,76 (с, 0,8Н), 7,18-7,46 (м, 10Н).
Пример А9
Фенил-(3-{ 1-[5-(тетрагидро-2(1Н)-пиримидинилиденамино)-3-изоксазолил] этинил}фенил)метанон (схема 130, приведенная в конце описания).
3-{1-[3-(2-Фенил-1,3-диоксолан-2-ил)фенил]-5-изоксазолил}-(дитиоимидокарбонат) (2,1 г), полученный по ссылочному примеру В2, описанному выше, растворяли в этаноле (10 мл) при комнатной температуре с последующим добавлением 1,3-пропандиамина (0,47 мл). Полученную смесь кипятили с обратным холодильником в течение 4 часов. После охлаждения до комнатной температуры реакционную смесь выливали в воду, затем экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия и концентрировали при пониженном давлении.
К остатку добавляли трифторацетат (20 мл) и воду (4 мл) с последующим перемешиванием при комнатной температуре в течение 2 часов. Реакционный раствор сразу же концентрировали при пониженном давлении. К остатку добавляли хлороформ (50 мл) и насыщенный водный раствор бикарбоната натрия (50 мл) и затем экстрагировали хлороформом. Органический слой промывали насыщенным водным раствором хлорида натрия, сушили над сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали путем колоночной хроматографии на силикагеле (СНСl3/МеОН=20/1) с получением желаемого соединения (1,3 г).
1H-ЯМР (300 МГц) (СDСl3): 1,64 (д, 3Н, J=7,1 Гц), 1,94 (тт, 2Н, J=5,9, 5,9 Гц), 3,37 (т, 4Н, J=5,9 Гц), 4,15 (кв, 1Н, J=7,1 Гц), 5,00 (с, 1Н), 5,99 (ушир. с, 2Н), 7,37-7,64 (м, 6Н), 7,75-7,80 (м, 3Н).
Пример А10
[3-(1-{ 5-[(1,3-Диметил-2-имидазолидинилиден)амино] -3-изоксазолил} этил)фенил](фенил)метанон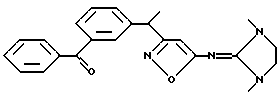
Желаемое соединение получали исходя из соединения, полученного в ссылочном примере В2 по способу примера А9.
1H-ЯМР (300 МГц) (СDСl3): 1,65 (д, 3Н, J=7,3 Гц), 2,74 (с, 6Н), 3,40 (с, 4Н), 4,17 (кв, 1Н, J=7,0 Гц), 5,04 (с, 1Н), 7,34-7,63 (м, 6Н), 7,75-7,80 (м, 3Н).
Пример A11
(3-{1-[5-(2-Имидазолидинилиденамино)-3-изоксазолил]-этил}фенил)(фенил)метанон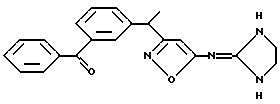
Желаемое соединение получали исходя из соединения, полученного в ссылочном примере В2 по способу примера А9.
1H-ЯМР (300 МГц) (СDСl3): 1,65 (д, 3Н, J=7,1 Гц), 3,64 (с, 4Н), 4,14 (кв, 1Н, J= 7,1 Гц), 5,11 (с, 1Н), 5,75 (ушир. с, 2Н), 7,37-7,62 (м, 6Н), 7,75-7,81 (м, 3Н).
Пример А12
{ 3-[1-(5-{[1-(2-Гидроксиэтил)тетрагидро-2(1Н)пиримидинилиден]амино}-3-изоксазолил)этил]фенил}(фенил)метанон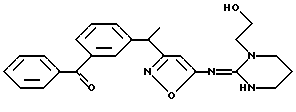
Желаемое соединение получали исходя из соединения, полученного в ссылочном примере В2 по способу примера А9.
1H-ЯМР (300 МГц) (СDСl3): 1,64 (д, 2Н, J=7,3 Гц), 2,01 (тт, 2Н, J=5,9, 5,9 Гц), 3,34-3,42 (м, 4Н), 3,62-3,65 (м, 2Н), 3,77-3,80 (м, 2Н), 4,15 (кв, 1H, J=7,1 Гц), 5,11 (с, 1Н), 5,43 (ушир. с, 1H), 6,55 (ушир. с, 1H), 7,24-7,64 (м, 6Н), 7,75-7,80 (м, 3Н).
Пример А13
{ 3-[1-(5-{ [1-(2-Гидроксиэтил)-2-имидазолидинилиден]-амино}-3-изоксазолил)этил]фенил}(фенил)метанон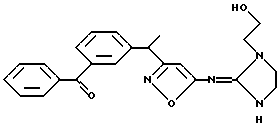
Желаемое соединение получали исходя из соединения, полученного в ссылочном примере В2 по способу примера А9.
1H-ЯМР (300 МГц) (СDСl3): 1,64 (д, 3Н, J=7,1 Гц), 3,43-3,47 (м, 2Н), 3,61 (с, 4Н), 3,78-3,81 (м, 2Н), 4,17 (кв, 1H, J=7,1 Гц), 4,57 (ушир. с, 1H), 5,19 (с, 1H), 6,05 (ушир. с, 1H), 7,31-7,65 (м, 6Н), 7,75-7,80 (м, 3Н).
Ссылочный Пример В2
Диметил 3-{ 1-[3-(2-фенил-1,3-диоксолан-2-ил)фенил] -5-изоксазолил} -(дитиоимидокарбонат) (схема 131, приведенная в конце описания).
3-{ 1-[3-(2-Фенил-1,3-диоксолан-2-ил)фенил] этил} -5-изоксазоламин (не прошедшая экспертизу японская патентная публикация 63-152368) (10 г) растворяли ДМФА (160 мл) с последующим добавлением 4 н. водного раствора гидроксида натрия (8 мл) при охлаждении льдом. Полученную смесь перемешивали в течение 30 минут с последующим добавлением дисульфида углерода (3,6 мл). Затем полученную смесь перемешивали в течение 30 минут с последующим добавлением к ней 4 н. водного раствора гидроксида натрия (8 мл) при охлаждении льдом. Полученную смесь перемешивали в течение 2,5 часов с последующим добавлением метилйодида (3,7 мл). Полученную смесь нагревали до комнатной температуры и затем перемешивали в течение 1 часа. Реакционный раствор выливали в воду и экстрагировали этилацетатом. Органический слой промывали насыщенным водным раствором хлорида натрия и сушили над сульфатом натрия, и затем концентрировали при пониженном давлении. Остаток очищали путем колоночной хроматографии (гексан/АсОЕt=2/1) с получением желаемого соединения (8,8 г).
1H-ЯМР (300 МГц) (СDСl3): 1,64 (д, 3Н, J=7,1 Гц), 2,57 (ушир. с, 6Н), 4,05 (с, 4Н), 4,18 (кв, 1H, J=7,1 Гц), 5,63 (с, 1H), 7,18-7,35 (м, 6Н), 7,48-7,51 (м, 3Н).
Пример испытания 1
Ингибирование артрита, вызванного адьювантом
В качестве исследуемых объектов используют самцов SD крыс. Убитых термообработкой Mecobacterium butiricum, суспендированные в жидком парафине, в концентрации 0,5% вводят подкожно в заднюю правую лапу каждой крысы. Через 17 дней животные, у которых также ясно появляется начало второго воспаления на задней левой лапе, отбираются и каждое изобретение по настоящему изобретению, суспендированное в растворе 0,5% метилцеллюлозы, перорально вводят этим животным в течение 5 последующих дней. Объем каждой задней лапы после завершения введения сравнивают с тем, который был при начале введения, и оценивают ингибирующий опухоль эффект по разнице между ними. Результаты показаны в табл. 1 - 3.
Пример испытания 2
Ингибирование аллергической реакции III типа
В качестве исследуемых объектов используют самцов BALB/c мышей. Суспензию, полученную суспендированием овечьих красных кровяных телец в физиологическом растворе в концентрации 20%, вводят внутривенно в хвост каждой мыши и через 14 дней эту процедуру повторяют для иммунизации животных. Через еще 5 дней 100%-ную суспензию овечьих красных кровяных телец вводят подкожно в заднюю правую лапу каждой мыши для того, чтобы вызвать аллергию III типа, и спустя 3 часа после введения измеряют толщину правой и левой задних лапок. Эффективность лекарственного средства оценивают по разнице между толщиной правой и левой задней лапок в виде объема отека. Каждое соединение по настоящему изобретению суспендируют в 0,5% растворе метилцеллюлозы и вводят перорально за 24 часа до и спустя 1 час после индуцирования воспаления. В табл. 4 показана степень ингибирования отека, вычисленная путем сравнения объема отека у группы, которой вводят соединение, с контрольной группой.
Пример испытания 3
Действие на экспериментальный аллергический энцефаломиелит
Лечебное действие соединений оценивают, используя экспериментальный аллергический энцефаломиелит на мышах, который является одной из животных моделей рассеянного склероза. Экспериментальный аллергический энцефаломиелит вызывают методом, описанным Bell et al. (J. Immunology, 150: 4085-4092, 1993). А именно, 200 мкг миелинового базового белка (выделенного из мозга кролика, сигма), смешанный с добавкой Френда (Freund's complete adjuvant), вводят подкожно в бедро самки мыши (PL • SJL) F1 в возрасте 8 недель (Jackson Laboratories, Bar Harbor, ME). В день сенсибилизации и 2 дня спустя внутрибрюшинно вводят 200 нг токсина коклюша (List Biological Laboratories, Campbell, CA). Степень серьезности симптома указывают в баллах в соответствии со следующими критериями:
1: паралич хвоста,
2: легкая слабость задних конечностей,
3: паралич задних конечностей и/или слабость передних и задних конечностей,
4: полный паралич задних конечностей и/или от средней до сильной слабость передних и задних конечностей,
5: квадрилегия или агония,
6: смерть.
Соединение по данному изобретению суспендируют в 0,5% растворе метилцеллюлозы и вводят перорально в соотношении 0,1 мл/10 г массы тела. Контрольной группе перорально вводят только 0,5% раствор метилцеллюлозы. Введение начинают от сенсибилизации и осуществляют один раз в день последовательно в течение 42 дней.
Полученные результаты показаны на чертеже. У мышей контрольной группы вызывается сильный экспериментальный аллергический энцефаломиелит и все животные (10 мышей) погибают в период проведения исследования. С другой стороны, у мышей, обработанных соединением по примеру 22 (50 мг/кг), также вызывается экспериментальный аллергический энцефаломиелит, хотя симптомы слабые и умирают 3 мыши из 10 мышей.
Как описано выше, производные изоксазола и тому подобное по настоящему изобретению являются замечательно эффективными в исследуемых системах, включая животные модели хронического воспаления (например, вызванный адьювантом артрит у крыс), животную модель иммунного заболевания (например, ингибирование аллергической реакции III типа), экспериментальный аллергический энцелофаломиелит (например, рассеянный склероз и тому подобное). Следовательно, производные изоксазола и тому подобное по настоящему изобретению являются очевидно эффективными против хронического воспаления и, кроме того, действуют на иммунные заболевания, ответственные за хронические воспаления. Таким образом, производные изоксазола и тому подобное эффективны также против аутоиммунных заболеваний, таких как ревматоидный артрит и противовоспалительные заболевания.
Препаративный пример 1
Получение таблеток
Таблетки могут быть получены путем смешивания всех ингредиентов и, если необходимо, после гранулирования смеси, таблетированием и тому подобное. - Количество (мг/таблетка)
Соединение по примеру 85 - 20
Лактоза - 70
Кукурузный крахмал - 17
Гидроксипропилцеллюлоза с низкой степенью замещения - 8
Гидроксипропилцеллюлоза - 4
Стеарат магния - 1
Всего - 120 мг
Препаративный пример 2
Получение таблеток
Таблетки могут быть получены путем смешивания всех ингредиентов и, если необходимо, после гранулирования смеси, таблетированием и тому подобное. - Количество (мг/таблетка)
Соединение по примеру 43 - 20
D-Маннитол - 60
Двухосновный фосфат кальция - 25
Кальций кармеллоза - 8
Гидроксипропилметилцеллюлоза - 4
Тальк - 3
Всего - 120 мг
Препаративный пример 3
Получение капсулы
Препарат в виде капсулы может быть получен путем смешивания всех ингредиентов и, если необходимо, после гранулирования смеси, заполнением капсул этой смесью. - Количество (мг/капсула)
Соединение по примеру 69 - 20
Лактоза - 150
Кукурузный крахмал - 40
Гидроксипропилцеллюлоза с низкой степенью замещения - 8
Стеарат магния - 2
Всего - 220 мг
Препаративный пример 4
Получение капсулы
Препарат в виде капсулы может быть получен путем смешивания всех ингредиентов и, если необходимо, после гранулирования смеси, заполнением капсул этой смесью. - Количество (мг/капсула)
Соединение по примеру 72 - 20
D-Маннитол - 123,5
Кальций кармеллоза - 5
Стеарат магния - 1,5
Всего - 150 мг
Препаративный пример 5
Получение порошка
Порошок может быть получен путем смешивания всех ингредиентов и, если необходимо, гранулированием смеси. - Количество (мг/1 г)
Соединение по примеру 74 - 40
Лактоза - 750
Кукурузный крахмал - 200
Стеарат магния - 10
Всего - 1000 мг
Препаративный пример 6
Получение порошка
Порошок может быть получен путем смешивания всех ингредиентов и, если необходимо, гранулированием смеси. - Количество (мг/1 г)
Соединение по примеру 107 - 40
D-Маннитол - 700
Кукурузный крахмал - 200
Стеарат магния - 10
Всего - 1000 мг
Производные изоксазола и их фармацевтически приемлемые соли по настоящему изобретению могут использоваться в качестве терапевтических или профилактических лекарственных средств для аутоиммунных заболеваний [например, ревматоидный артрит, системная красная волчанка, системная склеродермия, синдром Сьегрена (Sjцgren), болезнь Хашимото (Hashimoto), миастения гравис, базедова болезнь, болезнь Аддисона (Addison), ювенильный диабет (диабет I типа), аутоиммунная гемодискразия (например, гипопластическая анемия, гемолитическая анемия и идиопатическая тромбоцитопения и тому подобное), язвенный колит, хронический гепатит в стадии обострения, гломерулонефрит, кишечно-легочный фиброз, рассеянный склероз и тому подобное] и воспалительных заболеваний (например, остеоартрит, подагра, атопический дерматит и псориаз и тому подобное).
Исследование токсичности заявленных соединений на примере соединения по примеру 22
1) Острая и подострая токсичности
Острую токсичность исследовали на крысах-самцах SD при пероральном введении соединения (500, 1000 и 2000 мг/кг) и наблюдали в течение 14 дней. В этих исследованиях случаев смерти животных не наблюдалось.
В 14-дневном исследовании подострой токсичности соединение вводили в дозе 100, 300 и 1000 мг/кг крысам-самцах SD. Не отмечалось ни смертности, ни клинических знаков. На аутопсии не наблюдалось никаких аномалий. При дозах 300 мг/кг и выше наблюдалась гипертрофия гепатоцитов центральной доли. При дозах 1000 мг/кг наблюдались пониженный прирост массы тела, повышенная относительная масса печени и гипертрофия клеток фолликулярного эпителия щитовидной железы.
2) Мутагенность
Мутагенность соединения оценивали с помощью теста Ames, с метаболической активацией или без таковой. Исследованное вещество давало отрицательные результаты при всех использовавшихся дозах (до 5000 мкг на планшет). Т
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ПОЛИЕНОВОГО СПИРТА (ВАРИАНТЫ), СУЛЬФОНОВОЕ СОЕДИНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2196133C2 |
| РОДСТВЕННОЕ ВИТАМИНУ A СОЕДИНЕНИЕ И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2188193C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА АМИДНОГО ТИПА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ | 2001 |
|
RU2232761C2 |
| ПРОИЗВОДНЫЕ N-ГЕТЕРОАРИЛНИКОТИНАМИДА, ИНСЕКТИЦИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2294329C2 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ (ВАРИАНТЫ) | 2001 |
|
RU2264395C2 |
| ПРОИЗВОДНЫЕ 4-МЕРКАПТОПИРРОЛИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАРНЕЗИЛТРАНСФЕРАЗЫ | 1996 |
|
RU2191773C2 |
| ИНГИБИТОРЫ ИНТЕРЛЕЙКИН-1 БЕТА-ПРЕВРАЩАЮЩЕГО ФЕРМЕНТА | 1995 |
|
RU2242480C2 |
| 8-АЗАБИЦИКЛО[3.2.1]ОКТАН-8-КАРБОКСАМИДНОЕ ПРОИЗВОДНОЕ | 2010 |
|
RU2574597C2 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1990 |
|
RU2029472C1 |
| АНТИБАКТЕРИАЛЬНЫЕ АГЕНТЫ | 1999 |
|
RU2246941C2 |
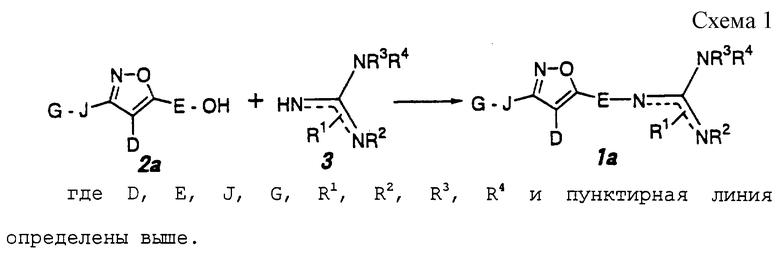

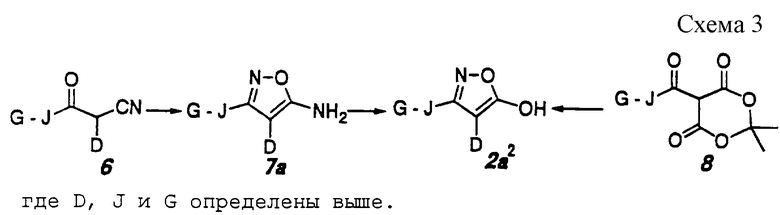
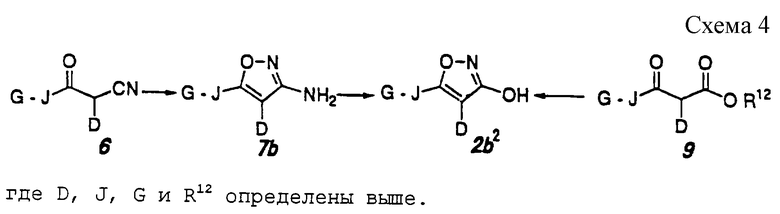
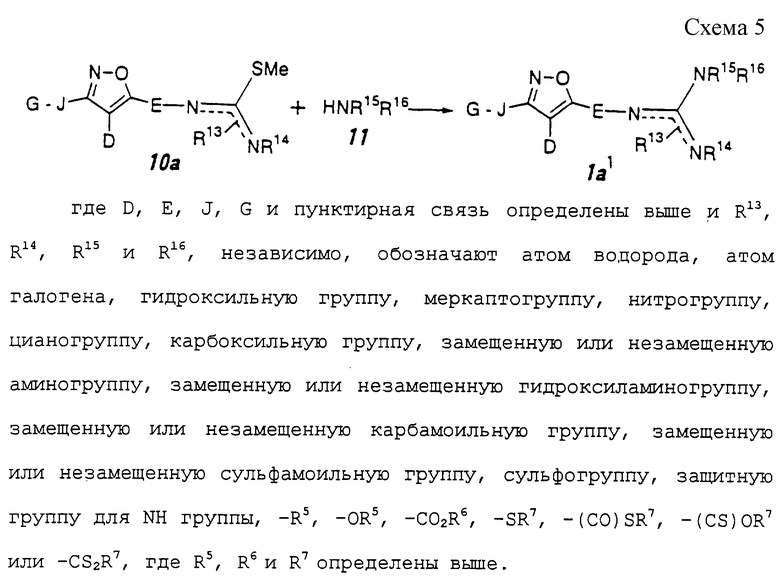
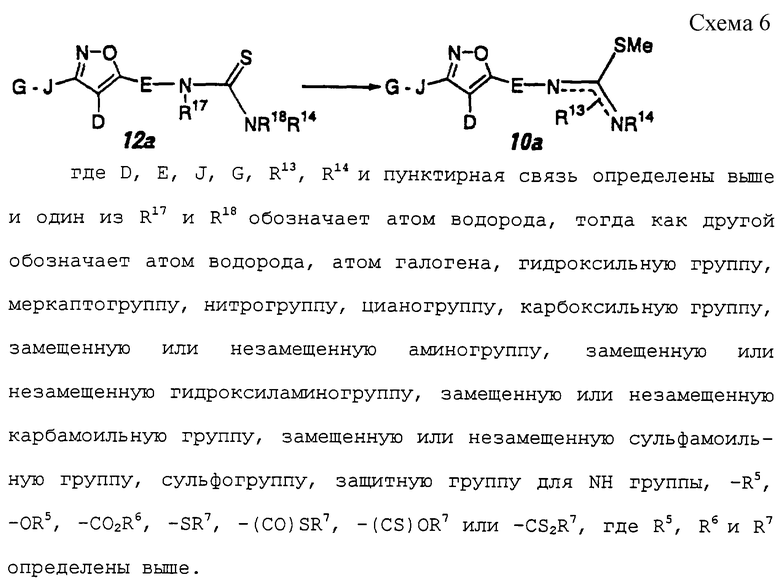
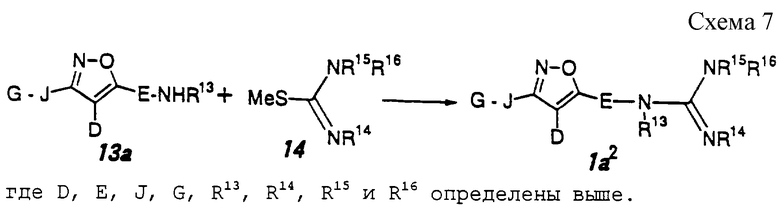
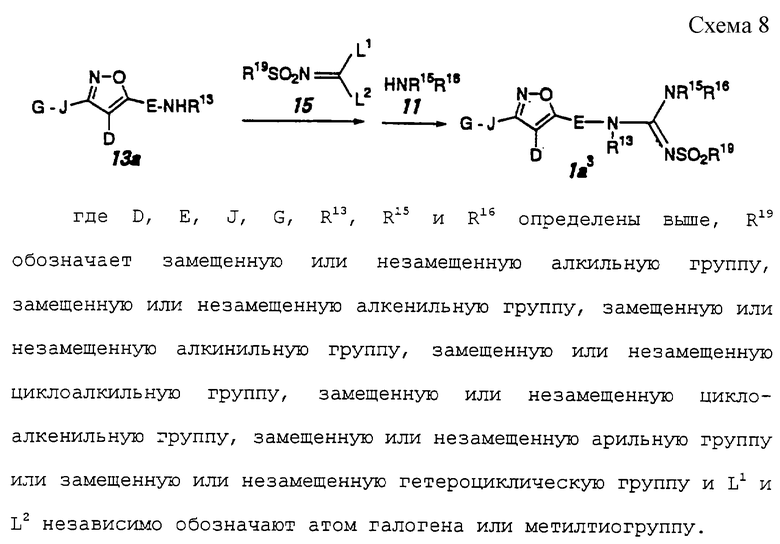
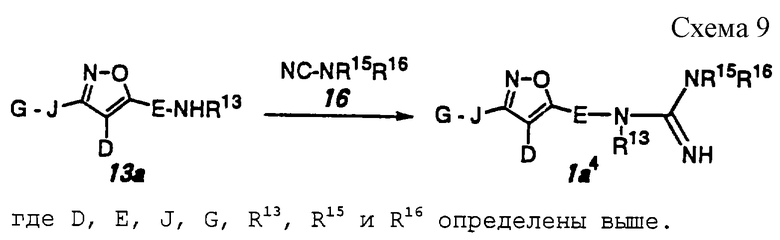
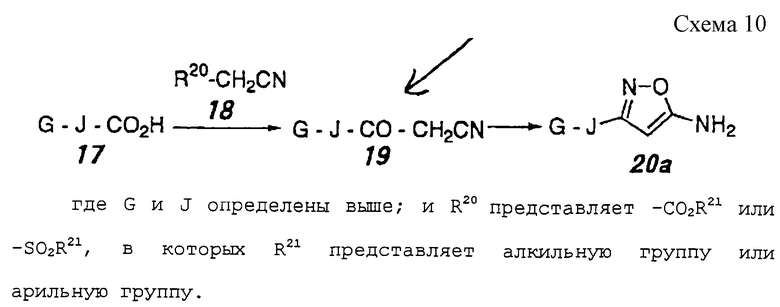
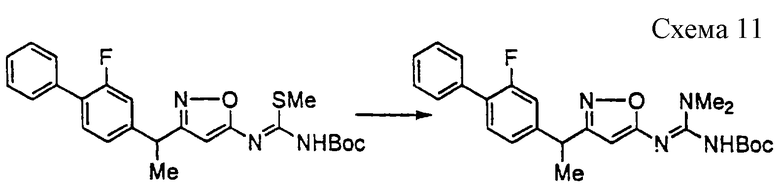
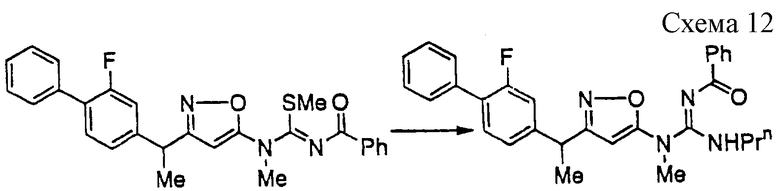
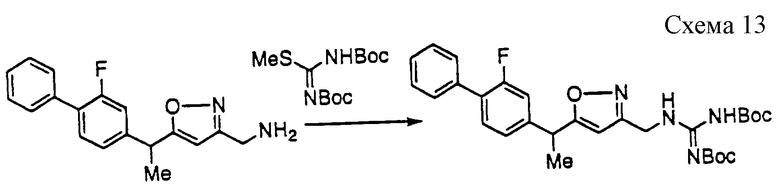
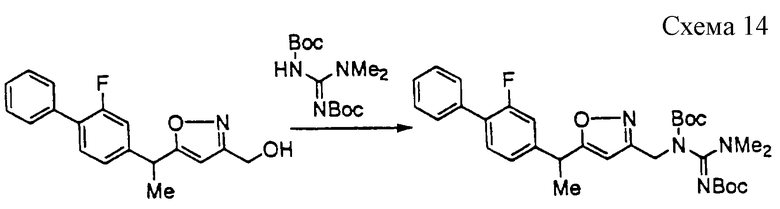
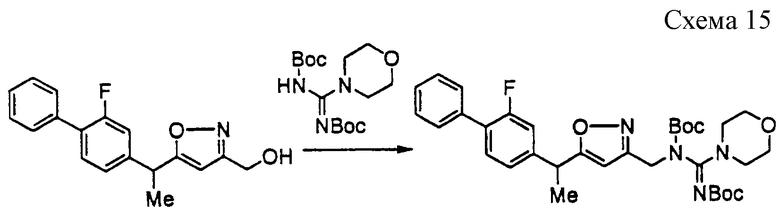
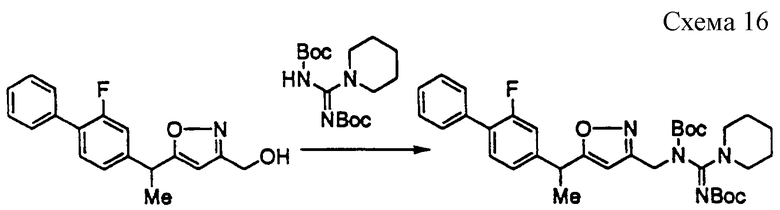
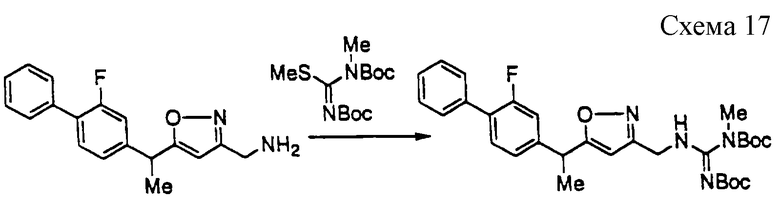
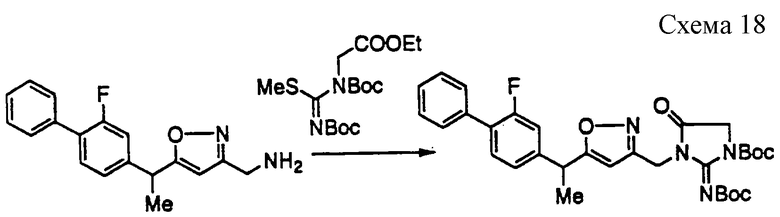
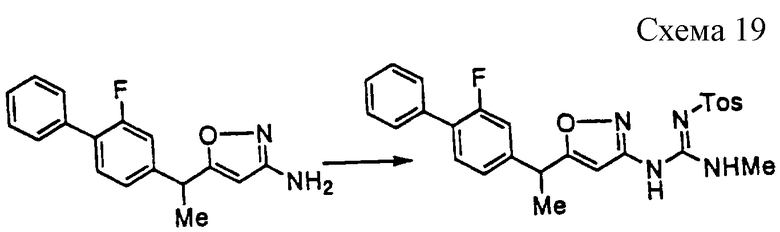
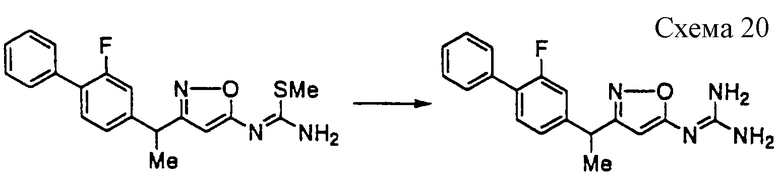
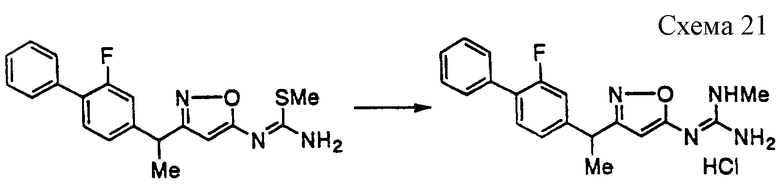
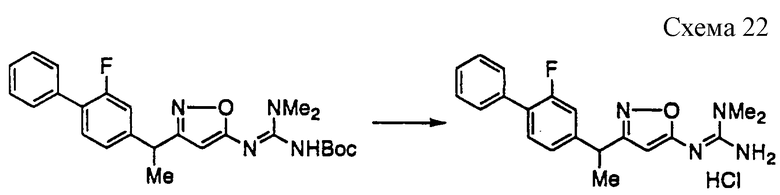
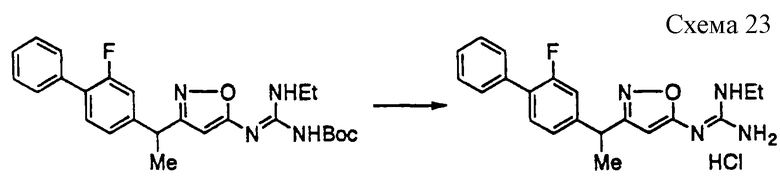

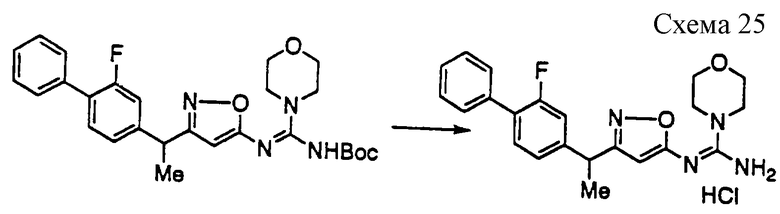
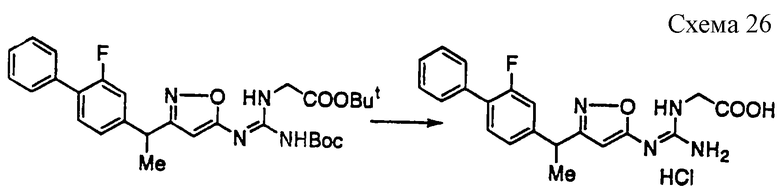
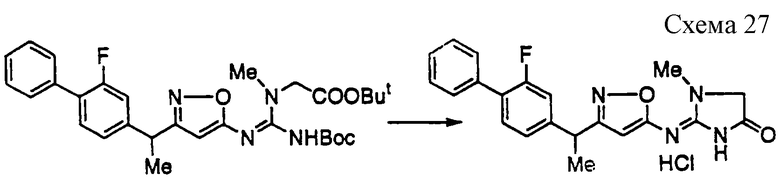
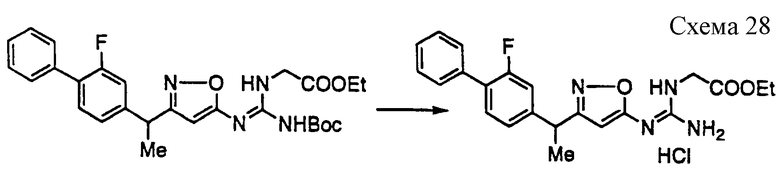
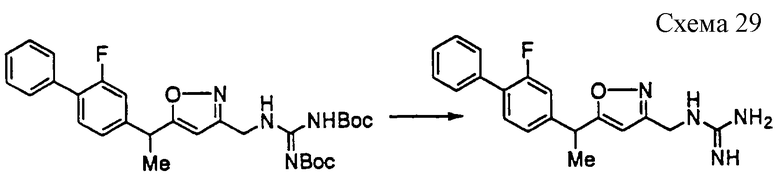
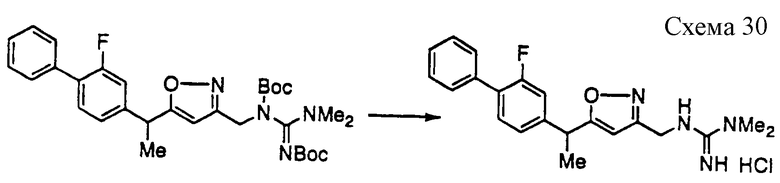
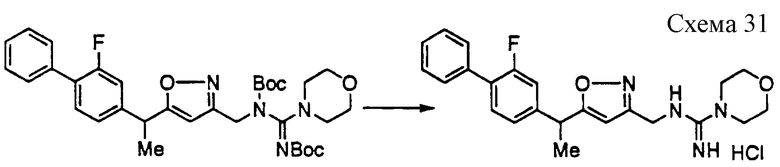

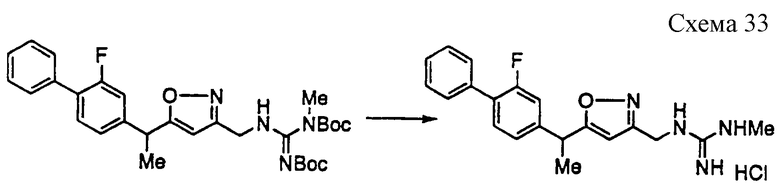
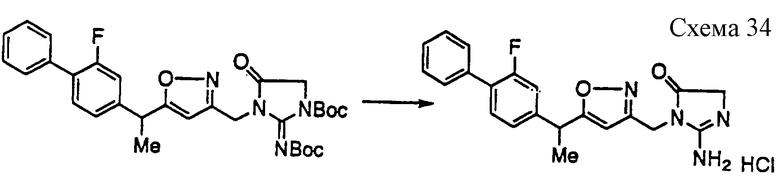
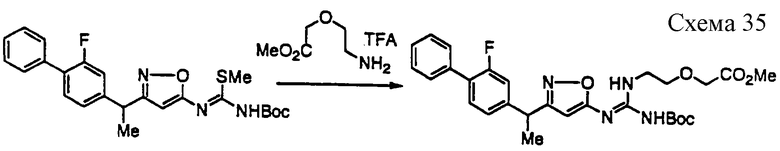
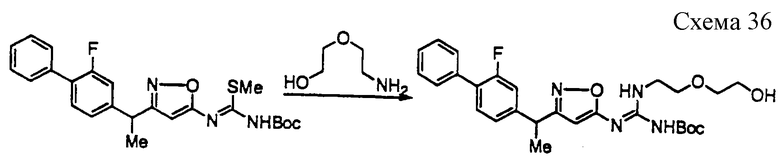
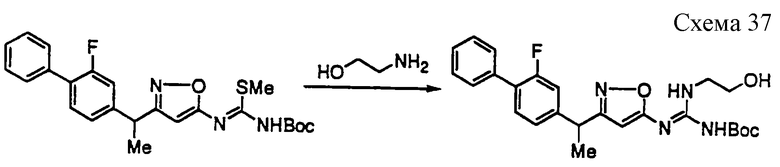
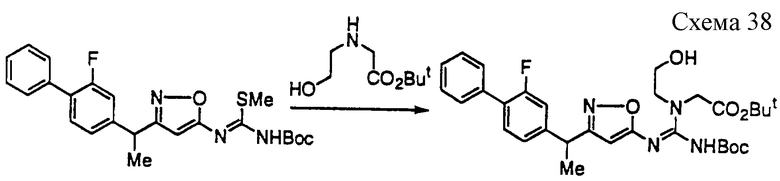
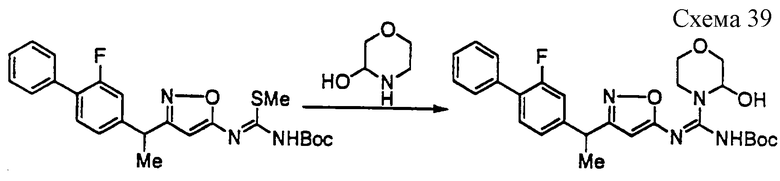
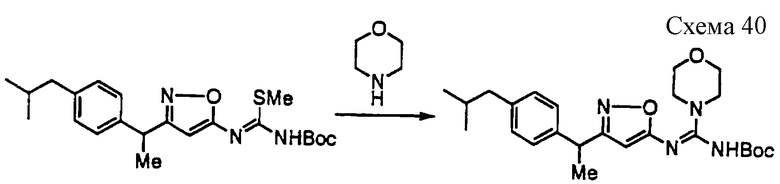
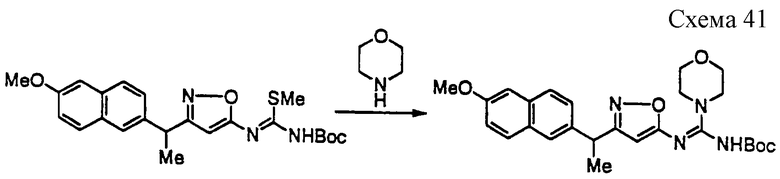
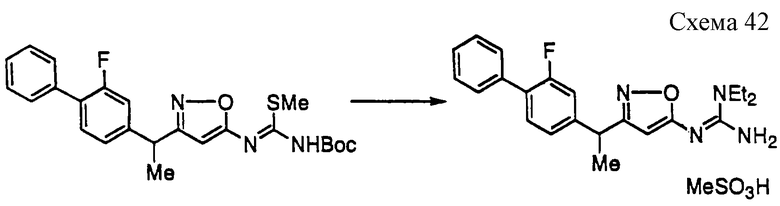
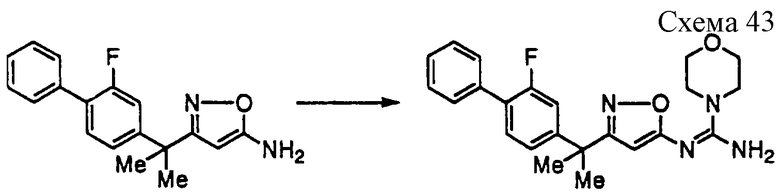
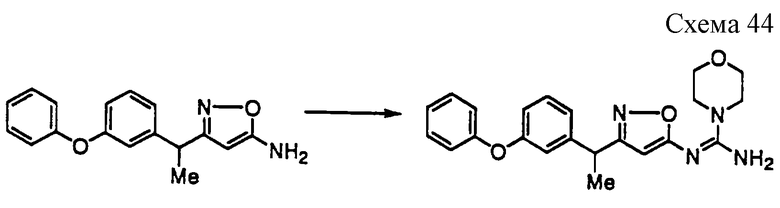
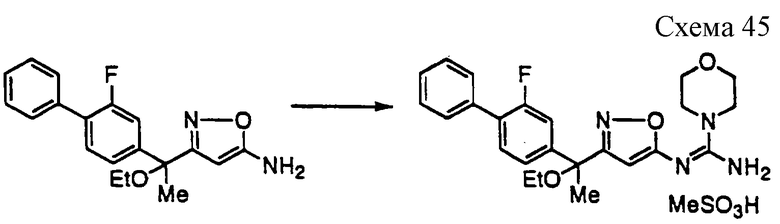
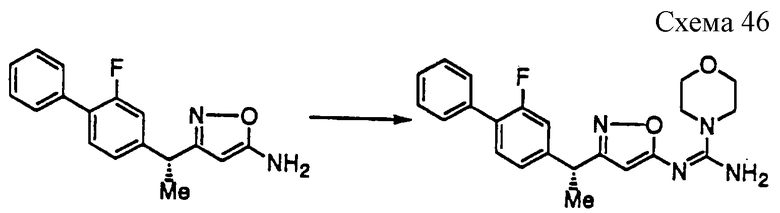
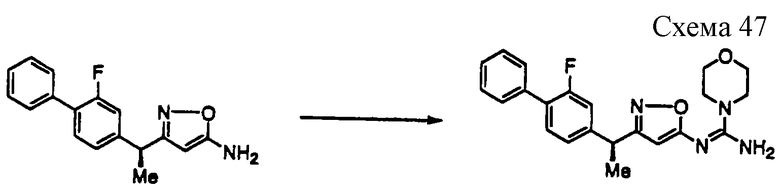

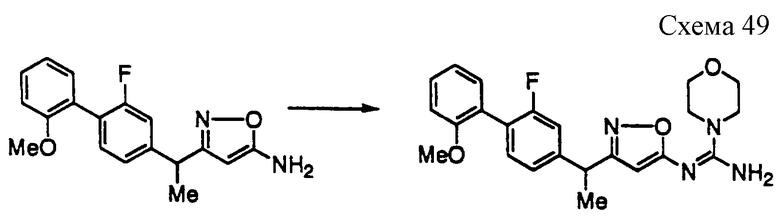
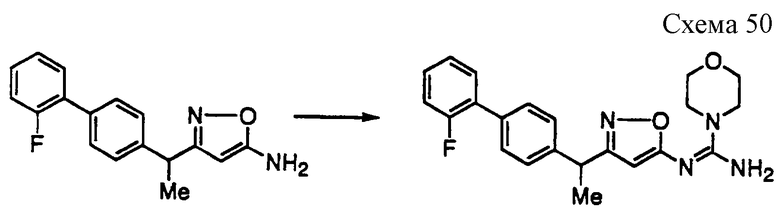
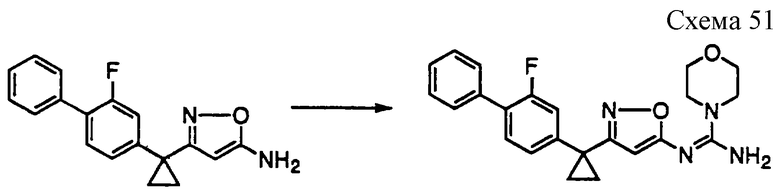
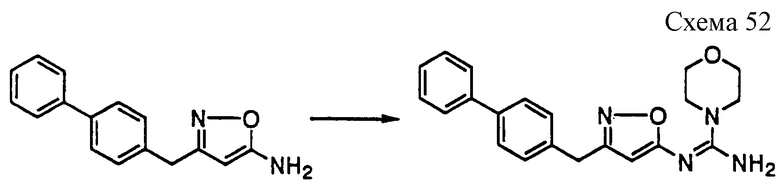
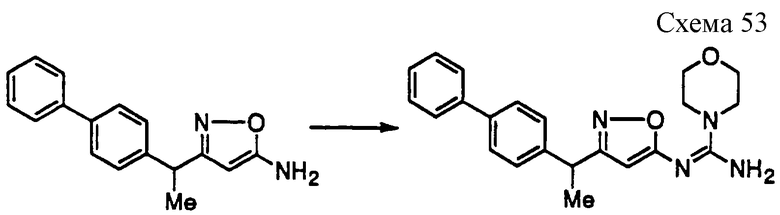
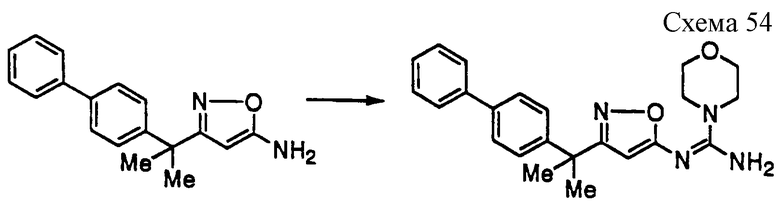
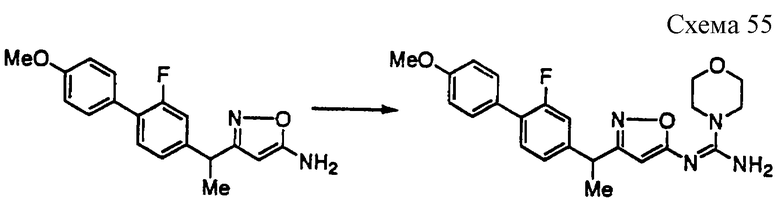
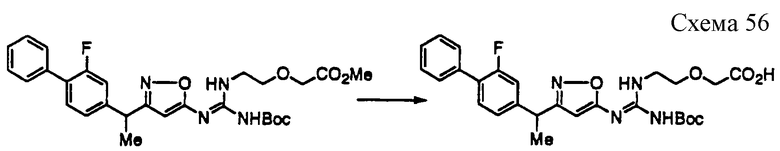

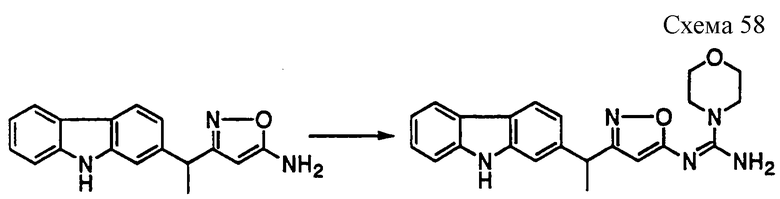
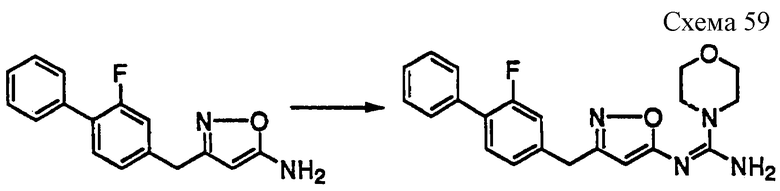
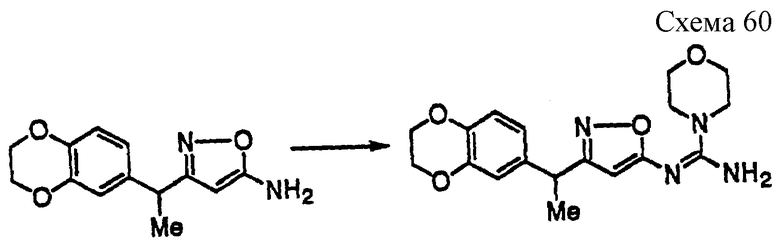
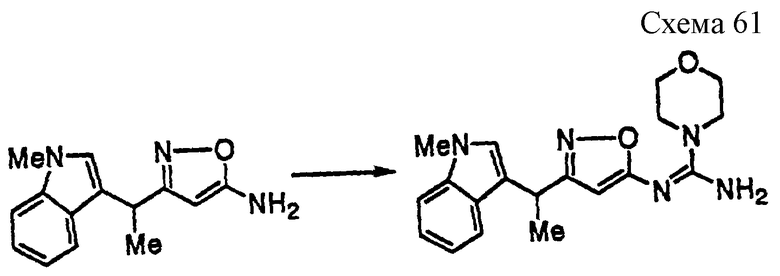
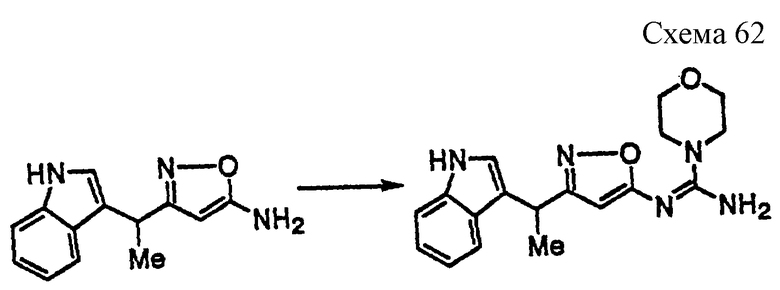
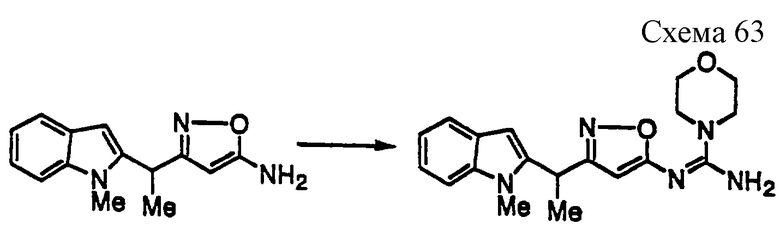
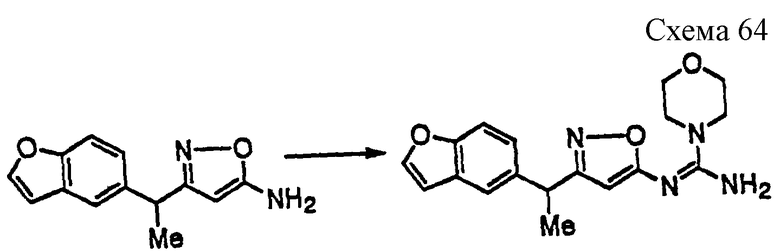
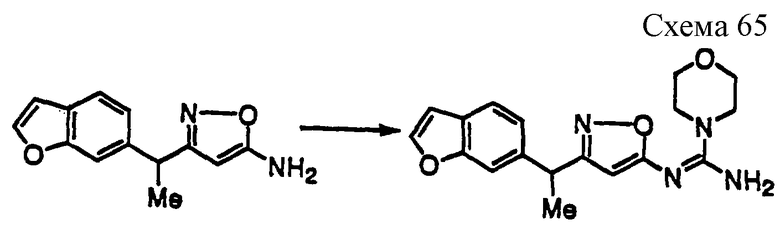
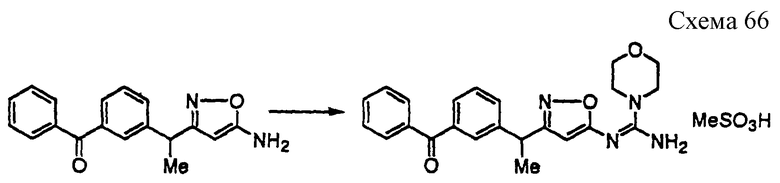
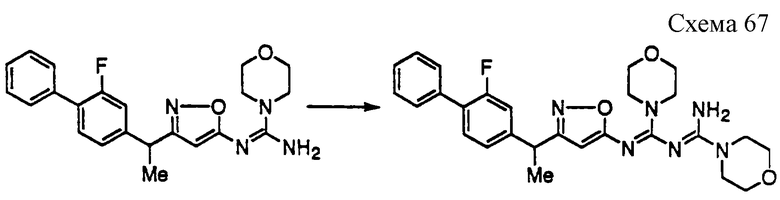
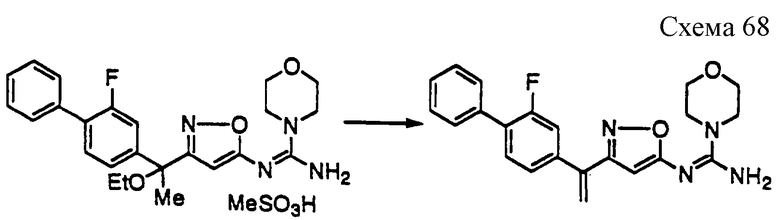
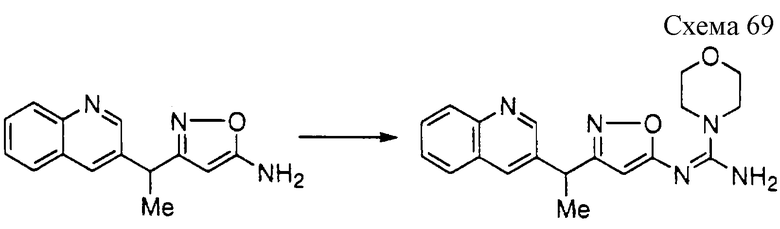
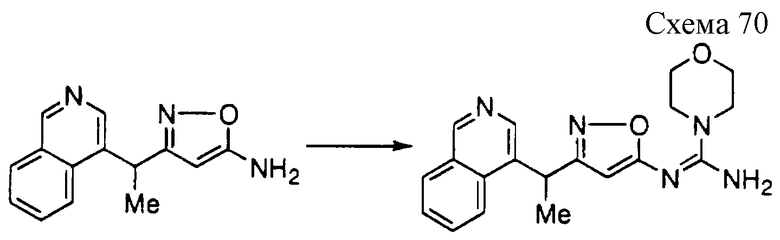
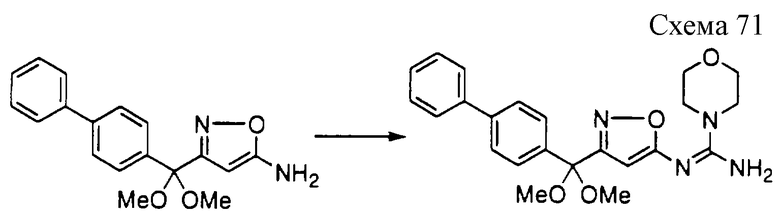
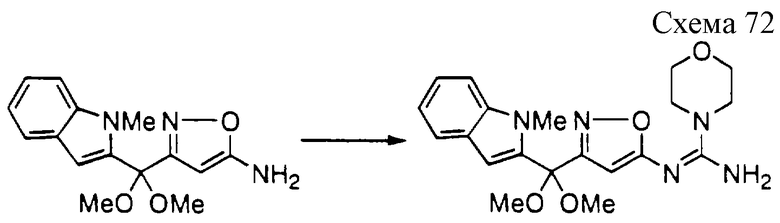
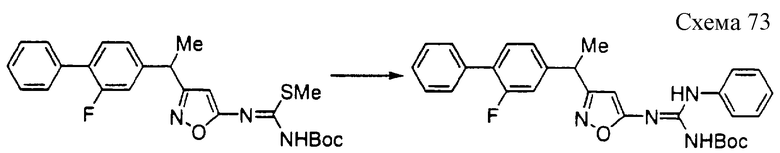
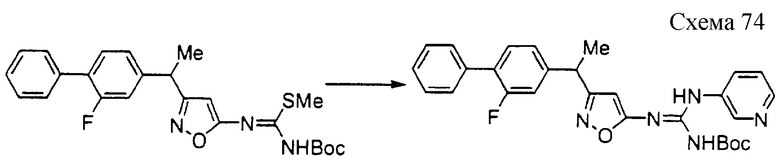
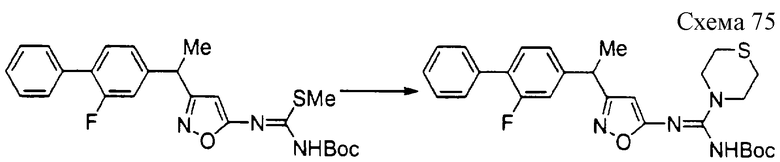
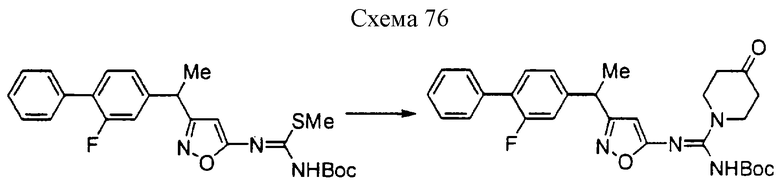
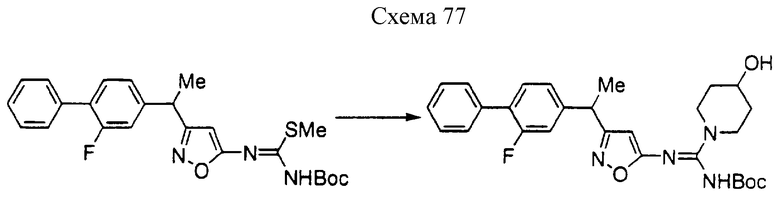
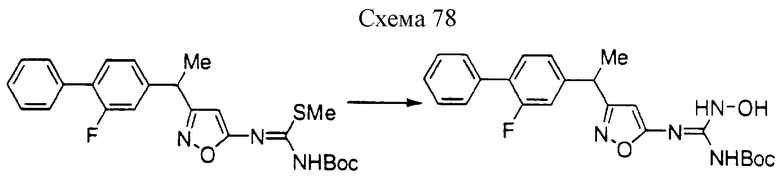
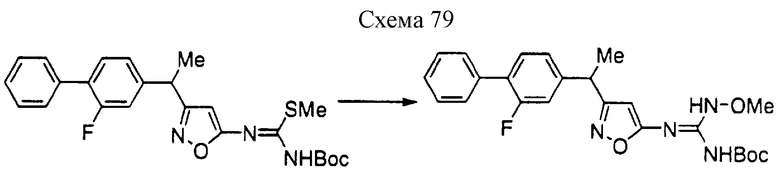
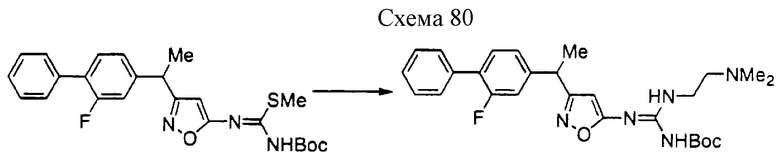
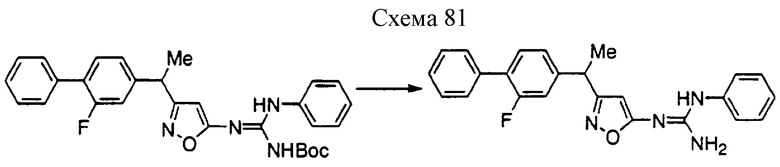

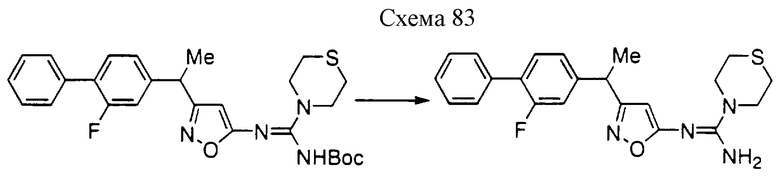
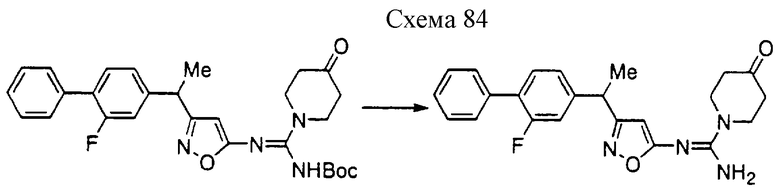
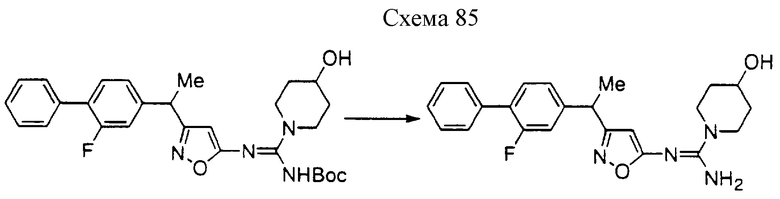
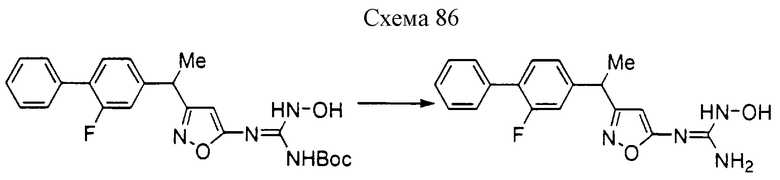
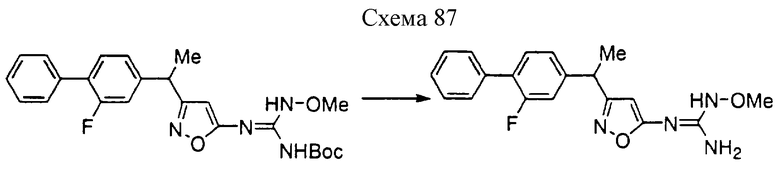
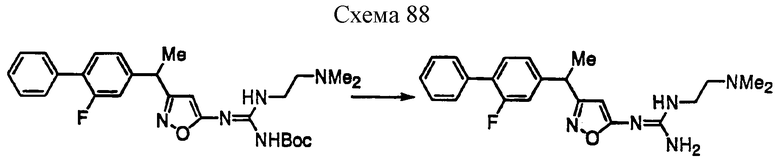

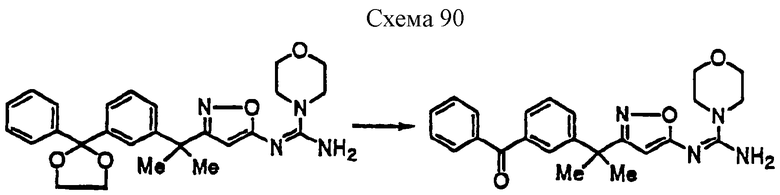
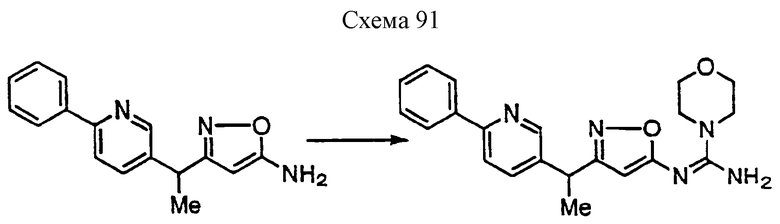
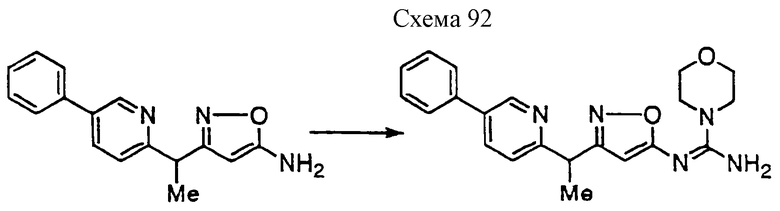
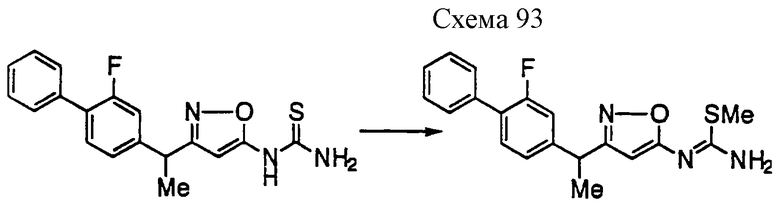
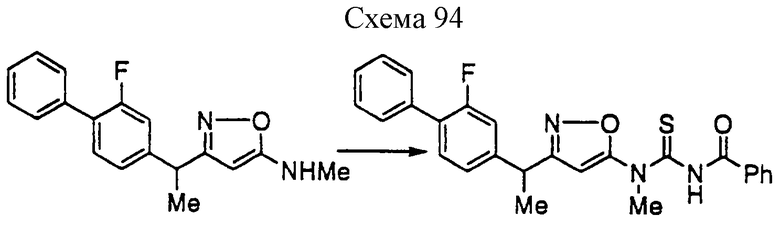
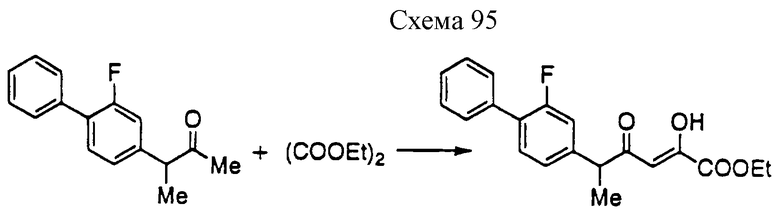
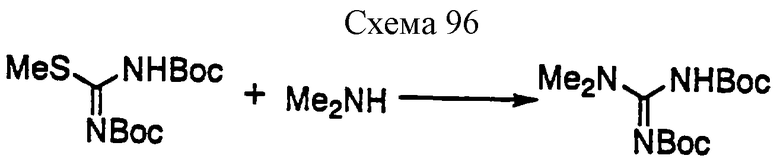
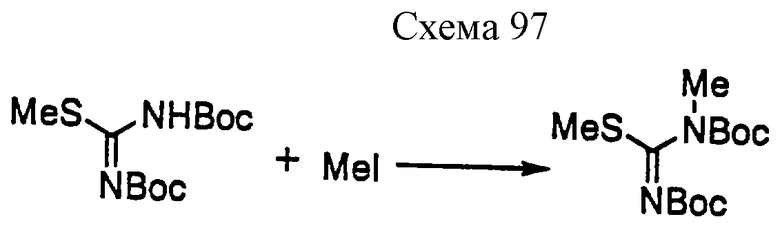

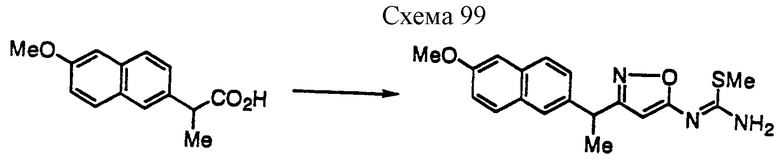
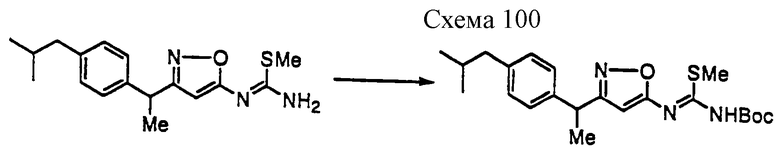
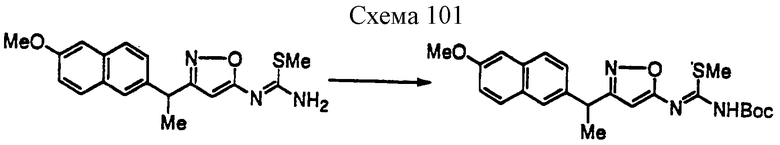
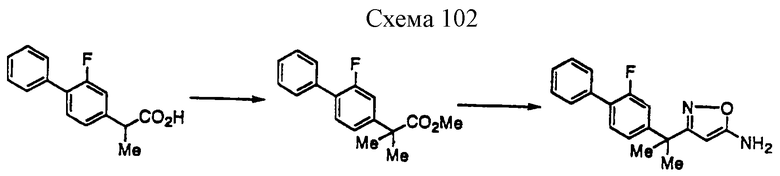
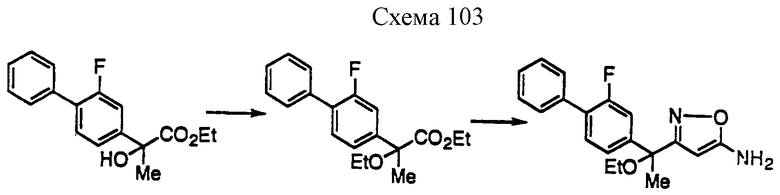
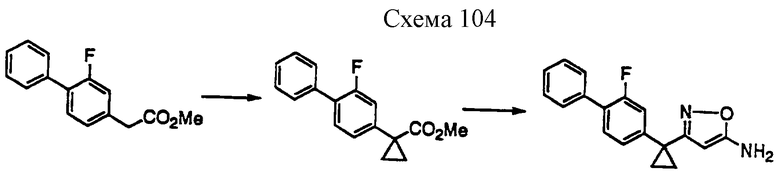
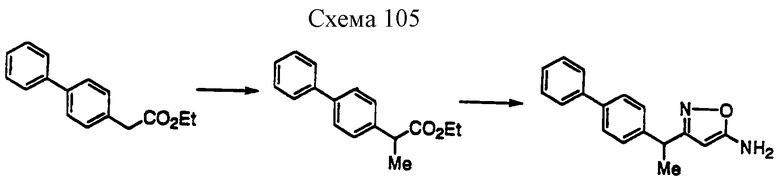
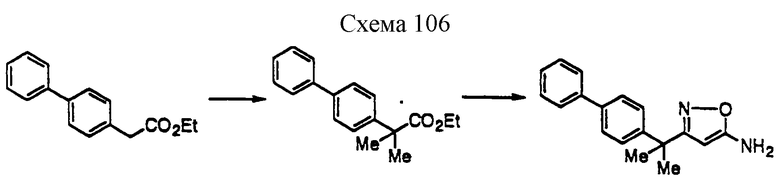
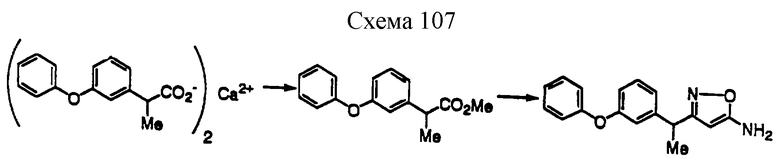
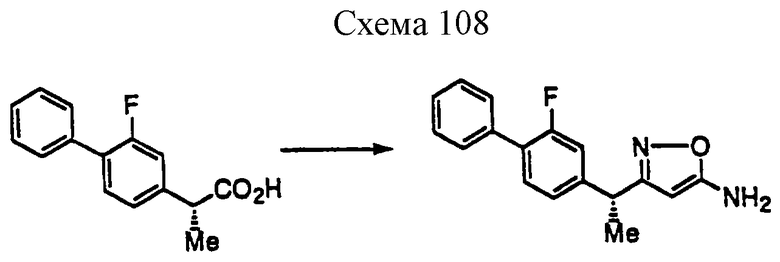
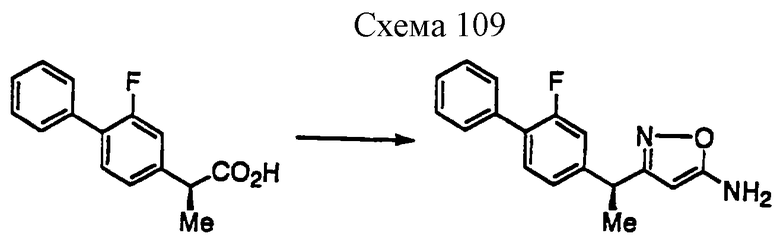
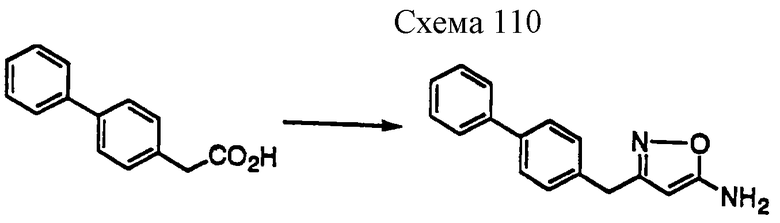
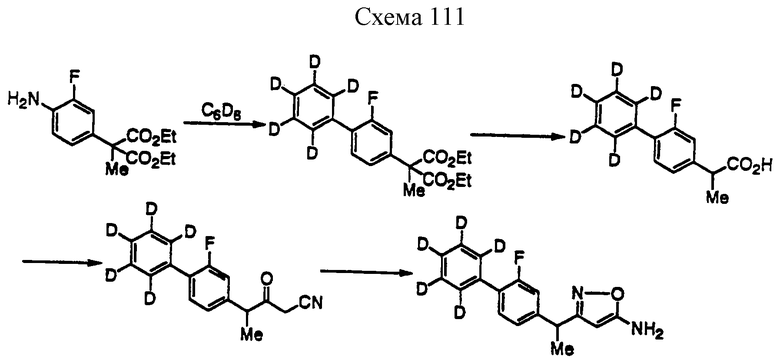
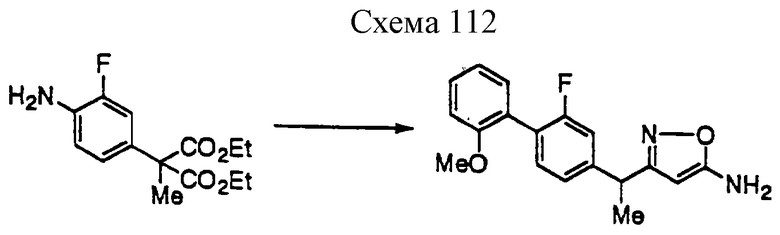
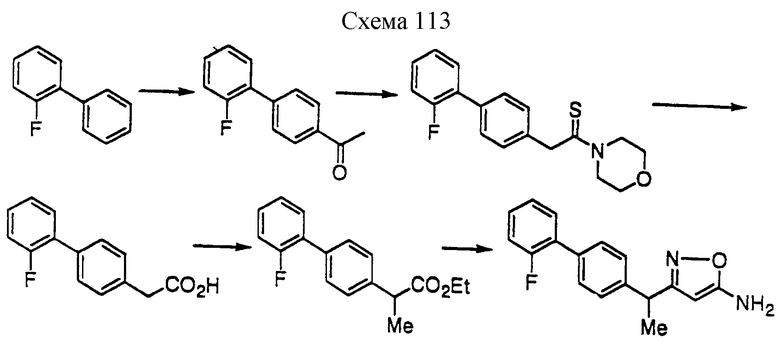
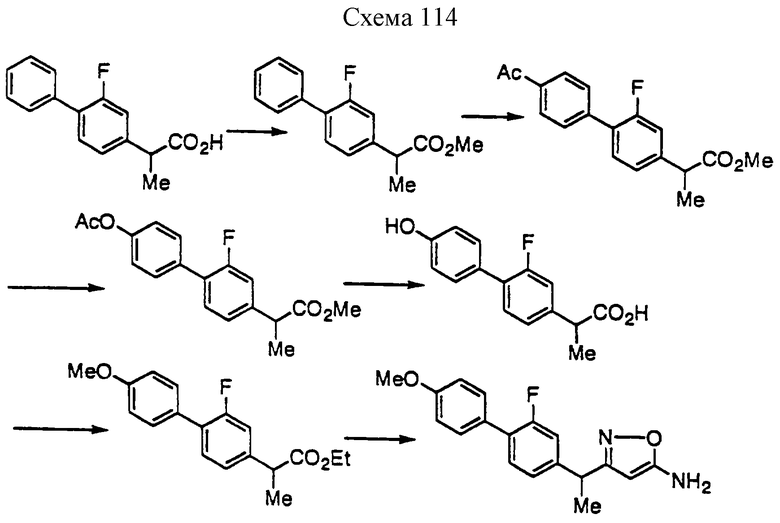
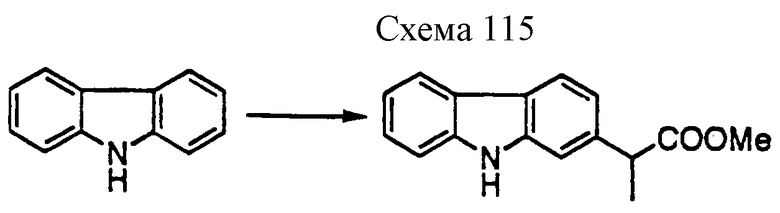
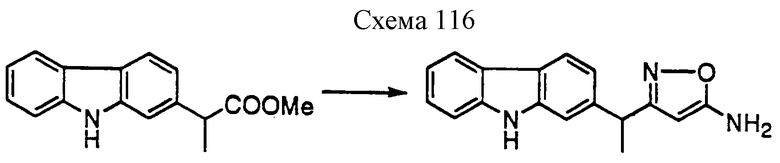
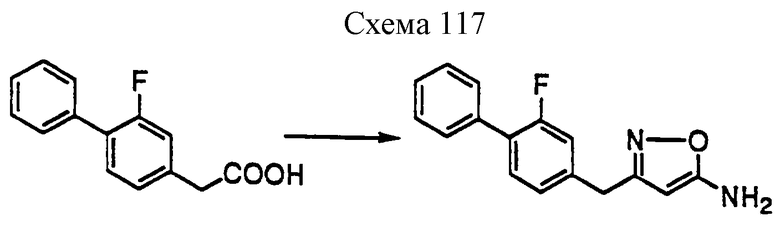
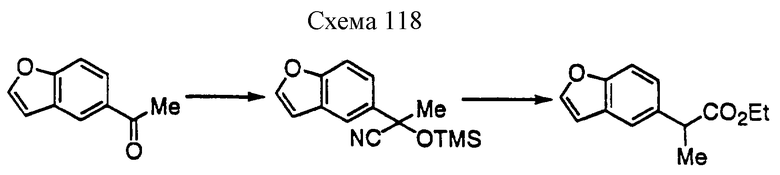
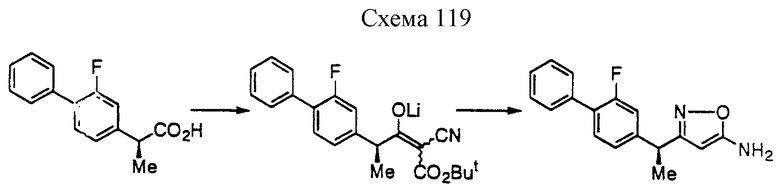
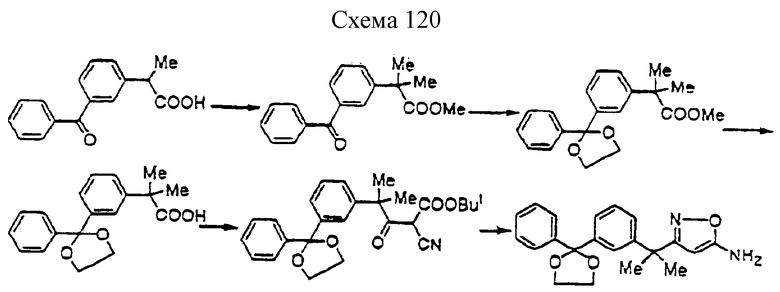
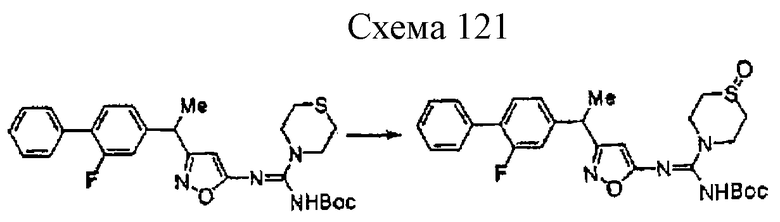
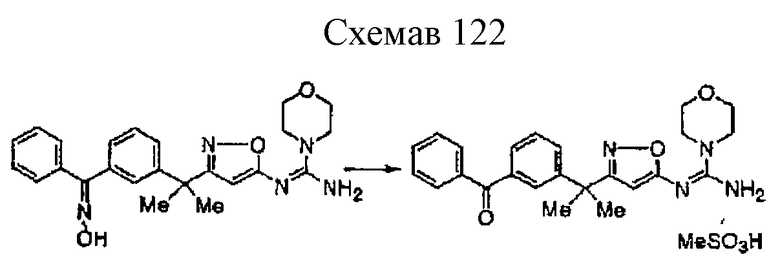
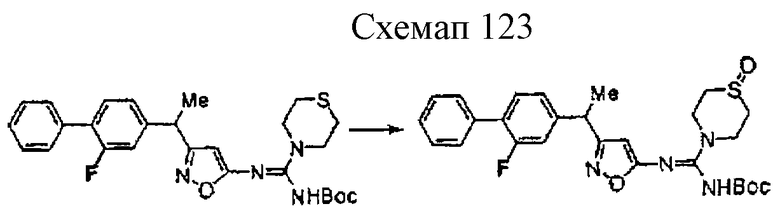
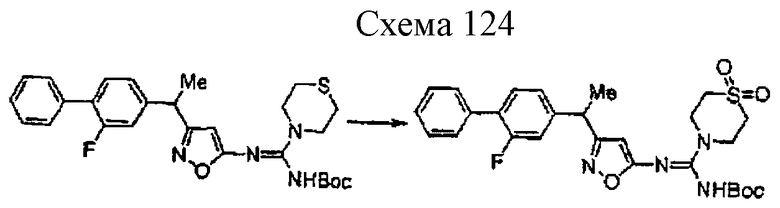
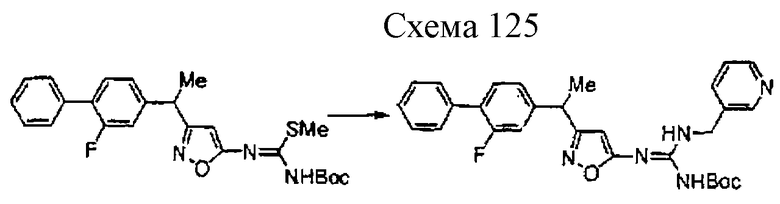
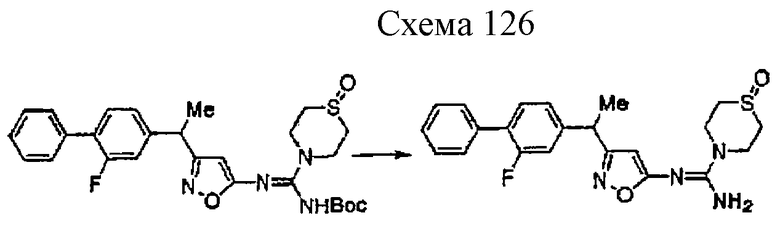

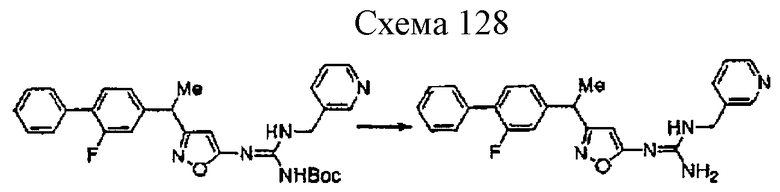
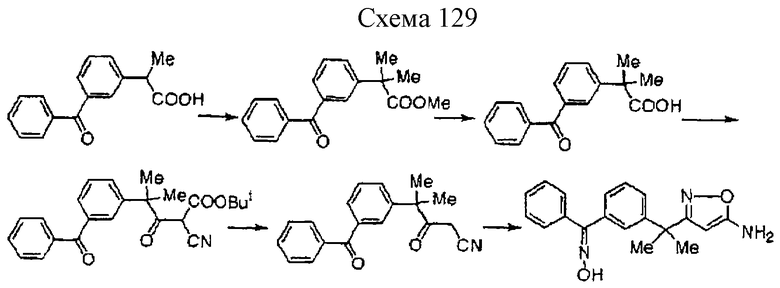
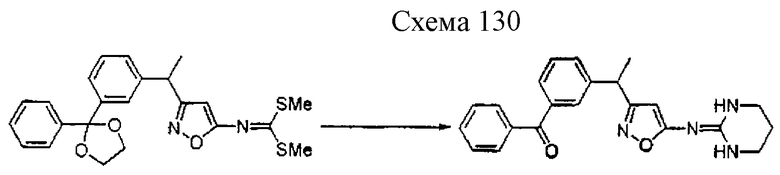

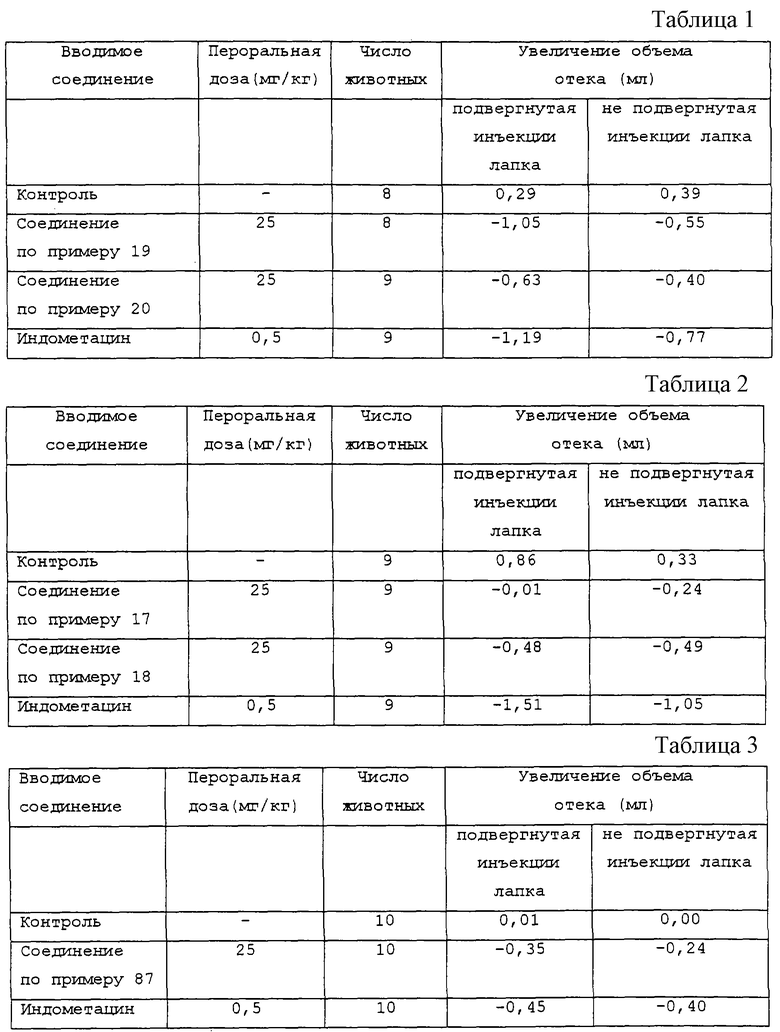
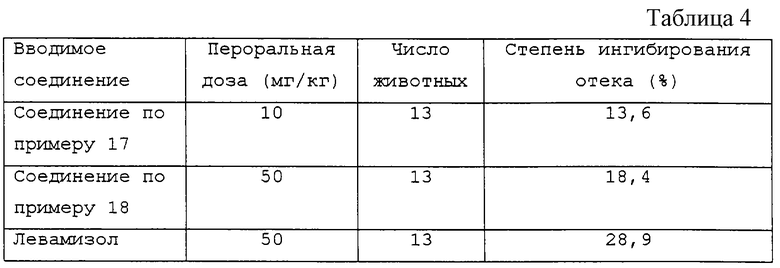
Изобретение относится к новым производным изоксазола формулы 1, где D представляет водород; один из А и В является группой (1) -E-N= C(NR25R26)NR27R28; E обозначает прямую связь или алкиленовую группу; R25 и R26 каждый представляет собой, независимо, водород; С1-4-алкил; -(CH2)n-CO2R32, n равно целому числу 1-3 и R32 представляет водород, C1-4-алкил; -(CH2)m-CO2R35, m равно 2 или 3 и R35 представляет водород, C1-4-алкил; -(СН2)m-ОН, m определено выше, или -(CH2)n-C(O)R36, n определен выше и R3 представляет водород, С1-4-алкил; и т. д. ; или взятые вместе образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, которая может быть замещена одним или двумя заместителями, выбранными из алкильной группы, гидроксильной группы и оксогруппы; R27 и R28 каждый представляет, независимо, водород; -(CO)OR32, R32 представляет C1-4-алкил; или R26 и R27 образуют с двумя атомами азота и одним атомом углерода 5-7-членную насыщенную азотсодержащую гетероциклическую группу, которая может быть замещена одним или двумя заместителями, выбранными из алкильной группы, -(СН2)m-ОН; и R25 и R26 независимо представляют водород, C1-3-алкил или -(СН2)m-ОН; и т.д.; (2) -Е-N(R45)C(NR46R47)=NR48; R45 представляет водород, C1-4-алкил, -(CO)OR32; R48 представляет водород, бензильную группу, и т.д.; R46 и R47 каждый представляет водород, C1-4-алкил, -(CO)OR32; или взятые вместе образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу; и т.д.; один из А и В представляет собой группу формулы -J-G, где G представляет фенил, бифенил, бензоилфенил, и т.д.; J представляет -C(R8R9)- или -C(=CR8R9)-, R8 и R9 независимо представляет водород, низшую алкоксигруппу, низшую алкильную группу, и т.д.; или их фармацевтически приемлемые соли. Фармацевтическая композиция для лечения аутоиммунных заболеваний или воспалительных заболеваний, содержащая в качестве активного ингредиента производное изоксазола формулы 1 или его фармацевтически приемлемую соль вместе с фармацевтически приемлемым носителем. Способ лечения аутоиммунных заболеваний или воспалительных заболеваний, заключающийся во введении производного изоксазола формулы 1 или его фармацевтически приемлемой соли в эффективном количестве в организм человека. Технический результат - новые производные изоксазола. 3 с. и 9 з.п. ф-лы, 1 ил., 4 табл.
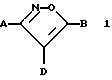
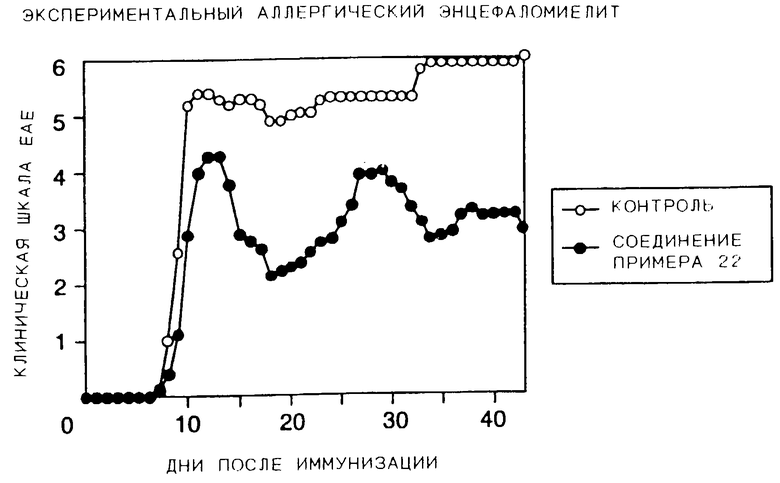
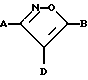
где D представляет собой атом водорода;
один из А и В является группой, представленной формулой
-E-N= C(NR25R26)NR27R28,
где Е обозначает прямую связь или алкиленовую группу;
R25, R26, R27 и R28 определены в указанных далее (1), (2) или (3):
(1) R25 и R26 определены в указанных далее (а) или (b), и R27 и R28 определены в указанном далее (с): (а) каждый представляет собой, независимо, атом водорода; алкильную группу, содержащую от 1 до 4 атомов углерода; -(CH2)n-CO2R32, где n равно целому числу от 1 до 3 и R32 представляет собой атом водорода, алкильную группу, содержащую от 1 до 4 атомов углерода; - (CH2)m-OR35, где m равно 2 или 3 и R35 представляет собой атом водорода, алкильную группу, содержащую от 1 до 4 атомов углерода, -(СН2)m-OH, где m определено выше, или -(СН2)n-(CO)OR36, где n определено выше и R36 представляет собой атом водорода или алкильную группу, содержащую от 1 до 4 атомов углерода; -(СН2)m-NR37R38, где m определено выше и R37 и R38 независимо представляют собой атом водорода или алкильную группу, содержащую от 1 до 4 атомов углерода, или, взятые вместе с атомом азота, представляют собой морфолин; фенильную группу; пиридильную группу; гидроксильную группу; алкоксигруппу, содержащую от 1 до 4 атомов углерода; пиридилметильную группу; (b) взятые вместе, они образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, гидроксильную группу и оксогруппу; (c) каждый представляет собой, независимо, атом водорода; -(СО)OR32, где R32 представляет собой алкильную группу, содержащую от 1 до 4 атомов углерода;
(2) взятые вместе, R26 и R27 образуют с двумя атомами азота и одним атомом углерода 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная азотсодержащая гетероциклическая группа может быть замещена одним или двумя заместителями, произвольно выбранными из группы, включающей алкильную группу, -(СН2)m-ОН, где m определено выше, и оксогруппы; и R25, и R26 независимо представляют собой атомы водорода, алкильные группы, содержащие от 1 до 3 атомов углерода или -(СН2)m-OH, где m определено выше;
(3) формула = С(NR25R26)NR27R28 является группой, представленной следующей формулой:
= С(NR41R42)N= C(NH2)NR43R44,
где R41 и R42, и R43 и R44, взятые вместе, образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу;
или группой, представленной формулой
-E-N(R45)C(NR46R47)= NR48,
где Е обозначает прямую связь или алкиленовую группу;
R45, R46, R47 и R48 определены в указанных далее (1') или (2'):
(1') R45 представляет собой атом водорода или алкильную группу, содержащую от 1 до 4 атомов углерода или -(СО)OR32, где R32 определено выше; R48 представляет собой атом водорода, бензильную группу, п-толуолсульфонильную группу или -(СО)OR32, где R32 определено выше; и R46 и R47 определены в следующих (а'') или (b''); (а'') каждый представляет собой, независимо, атом водорода, алкильную группу, содержащую от 1 до 4 атомов углерода или -(СО)OR32, где R32 представляет собой алкильную группу, содержащую от 1 до 4 атомов углерода; (b'') взятые вместе, образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу;
(2') взятые вместе, R45 и R46 или R45 и R48 образуют с атомом азота 5-7-членную насыщенную азотсодержащую гетероциклическую группу, где указанная 5-7-членная насыщенная азотсодержащая гетероциклическая группа может быть замещена оксогруппой; и R46, R47 и R48 независимо представляют собой, независимо, атом водорода или -(CO)R32, где R32 определено выше;
один из А и В представляет собой группу, представленную формулой:
-J-G,
где G представляет собой фенил, бифенил, бензоилфенил, бензофуранил, 1H-индолил, фенилпиридил, хинолил, изохинолил, нафталенил, феноксифенил, 9Н-карбазолил, 2-фенил-[1,3] диоксолан-2-ил-фенил или фенил(гидроксиимино)-метилфенил, указанный G может быть замещен одной или двумя группами, выбранными из группы, включающей низшую алкильную группу, низшую алкоксигруппу, гидроксигруппу, атом фтора, атом хлора или атом брома;
J представляет собой -C(R8R9)- или -С(= CR8R9)-, где R8 и R9 независимо представляют собой атом водорода, низшую алкоксигруппу, или низшую алкильную группу; R8 и R9, взятые вместе, могут образовывать с атомом углерода циклопропан или 1,3-диоксолан,
или его фармацевтически приемлемая соль.
-J-G
и В представляет собой группу, представленную формулой
-E-N= C(NR25R26)NR27R28
или группу, представленную формулой
-E-N(R45)С(NR46R47)= NR48,
где J, G, Е, R25, R26, R27, R28, R45, R46, R47 и R48 определены в п. 1.
({ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин;
[{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил] амин;
N-{ 3-[1-(2-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
({ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} морфолин-4-илметил)амин;
[{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил] амин;
N-{ 3-[1-(2-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
({ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -морфолин-4-илметил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)этил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил] амин;
N-{ 3-[1-[2'-фторбифенил-4-ил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
({ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} морфолин-4-илметил)амин;
[{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-илимино} -(4-метилпиперазин-1-ил)метил] амин;
N-{ 3-[1-(2'-фторбифенил-4-ил)-1-метилэтил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
(3-{ 1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] этил} фенил)фенилметанон;
[3-(1-{ 5-[амино(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил} этил)фенил] фенилметанон;
N-{ 3-[1-(3-бензоилфенил)этил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин;
(3-{ 1-[5-(аминоморфолин-4-илметиленамино)изоксазол-3-ил] -1-метилэтил} фенил)фенилметанон;
[3-(1-{ 5-[амино-(4-метилпиперазин-1-ил)метиленамино] -изоксазол-3-ил} -1-метилэтил)фенил] фенилметан;
N-{ 3-[1-(3-бензоилфенил)-1-метилэтил] изоксазол-5-ил} -N'-(2-морфолин-4-илэтил)гуанидин.
Приоритет по пунктам и признакам:
21.04.1997 по п. 1, за исключением соединений, где А и В соответствуют случаю (3), R8 и R9, взятые вместе, могут образовывать с атомом углерода 1,3-диоксалан;
24.12.1997 по пп. 2-12.
| Фильтрующий элемент | 1977 |
|
SU639574A1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ | 0 |
|
SU292937A1 |
| МИКШЕР ПРОГРАММ ЦВЕТНОГО ТЕЛЕВИДЕНИЯ | 1971 |
|
SU434620A1 |
| РАСХОДОМЕР ПЫЛИ | 0 |
|
SU313091A1 |
| US 4399075 А, 16.08.1983 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ КАРБОКСАМИДОТИАЗОЛОВ | 0 |
|
SU253685A1 |
Авторы
Даты
2003-01-20—Публикация
1998-04-20—Подача