Изобретение относится к области ветеринарной медицины, в частности иммунологии с/х животных и птиц.
В настоящее время иммунитет является актуальной проблемой в ветеринарии. Для диагностики иммунного статуса определяют микробицидные свойства системы крови, в частности определения кислой фосфатазы в нейтрофильных гранулоцитах. Фосфатазы относятся к гидролазам (3), кислая фосфатаза (3.1.3.2.), которая способна разрывать связи Р---О. Кислая фосфатаза катализирует реакцию гидролиза моноэфира ортофосфата, расщепляя на спирт и фосфорную кислоту
Моноэфир ортофосфат + Н2О = Спирт + Н3РО4
Активность кислой фосфатазы присуща молодым клеткам. По повышению или понижению активности кислой фосфатазы в той или иной степени можно судить о патологическом процессе в организме животных. Так, снижение активности фермента в лимфоцитах наблюдается при хроническом лимфолейкозе, а повышение - при инфекционном мононуклеозе. Определение активности кислой фосфатазы в мазках крови относится к тестам II уровня диагностики иммунного статуса организма животных и птиц. В настоящее время иммунитет является наиболее актуальной проблемой ветеринарии. Снижение иммунитета влечет за собой нарушение гомеостаза организма и вытекающие из него последствия: снижение сохранности молодняка, снижение репродуктивной способности и т.д.
Известно определение кислой фосфатазы в тканях [cм. Gomori (1952 г.) Ф. Г. Дж. Хейхоу, Д. Кваглино. Гематологическая цитохимия. Лабораторные методы. Пер. с англ. Е.В. Самочатовой, под ред. проф. Н.С. Кисляк. Москва, "Медицина", 1983, стр.144-145] на гистологических срезах.
Также известен способ определения кислой фосфатазы в мазках крови и костного мозга человека [(cм. Burstone M.S. (1959) New histochemical techniques for the demonstration of tissue oxidase (Cytochrome oxidase). - Histochem. Cytochem. , 1959, 7, p.112], включающий подготовку и фиксацию биологического субстрата, обработку его буферно-инкубационной смесью, инкубацию биологического субстрата с последующим высушиванием и микроскопированием.
Недостатками данного метода является затруднительное получение буферной смеси с определенным рН, которое имеет важное значение, а также методики окраски ядер нейтрофилов.
Техническим решением задачи является повышение эффективности иммунологических исследований.
Способ определения активности кислой фосфатазы в мазках крови, включающий подготовку и фиксацию биологического субстрата, обработку его буферно-инкубационной смесью, инкубацию биологического субстрата с последующим высушиванием и микрокопированием, качестве биологического субстрата используют мазки крови, для приготовления буферной смеси используют 0,2 М раствор янтарной кислоты, добавляют 12-13 мг ЭДТА (этилендиаминтетрауксусная кислота) и 0,2 М NaOH, доводят рН до 4,9-5,1, а затем в инкубационную смесь добавляют 0,6612 мл буферной смеси для обеспечения рН 5,0. При этом инкубацию проводят в темноте 2 часа при t=37oС, промывают дистиллированной водой, высушивают, дополнительно окрашивают мазки крови краской 0,5% водным раствором метиленовым синим в течении 0,5-1 минуты, затем промывают дистиллированной водой, сушат и по количеству окрашенных гранул красно-коричневого цвета в цитоплазме нейтрофилов определяют процент активности фермента кислой фосфатазы.
Фиксацию мазков осуществляют в парах 40% формалина 1-3 минуты, а для приготовления инкубационной смеси используют α-нафтилфосфатом натрия, в количестве 2,0 мг растворяют в 1,3 мл дистиллированной воды с добавлением 0,6512 мл буферной смеси небольшими порциями, помешивая, затем берут 5-6 мг красителя нейтрального прочного синего В и растворяют его в 2,5 мл буферной смеси, смешивая их постепенно (рН 5,0), полученные растворы смешивают, фильтруют в темноте через стеклянный фильтр.
Новизна заявляемого предложения обусловлена тем, что способ является точным и быстрым по сравнению с известными методиками, т.к. фермент поступает из тканей, где они выполняют определенные внутриклеточные функции в форменные элементы крови и локализуется в их цитоплазме в виде гранул (лизосом) по сравнению с известным методом определения кислой фосфатазы в сыворотке крови, как с научной, так и с экономической стороны, осуществляют подбор сочетания солей, обладающих буферными свойствами, с получением определенного рН системы и не способны ингибировать активность определяемого фермента, кроме того осуществляют дополнительно окраску ядер клеток в мазках крови 0,5%-водным раствором метиленовой сини, позволяющая легко определить нейтрофилов по форме ядер.
Данный способ может быть экспресс-методом для проведения цитохимического анализа активности кислой фосфатазы в нейтрофильных гранулоцитах в мазках крови.
Применение методики основано на взаимодействии кислой фосфатазы с α-нафтилфосфатом натрия. Фосфатаза катализирует гидролиз α-нафтилфосфата натрия с образованием α-нафтола и фосфорнокислого двузамещенного натрия. Для активации кислой фосфатазы в систему вводили буферную смесь, предложенную нами, состоящую из янтарной кислоты (С4Н6О4 с молекулярной массой М=118,09) - является естественным субстратом клеточных ферментов, участвующая в основном при внутриклеточном дыхании в синтезе АТР, а фосфатазы катализируют процессы с участием АТР. В буферную смесь входил 0,2 М раствор NaOH, а также трилон Б (ЭДТА), который ингибирует щелочную фосфатазу. Затем α-нафтол взаимодействует с красителем - нейтральным прочным синим В с образованием комплексного соединения азокрасителя. Образовавшийся комплекс (азокраситель) окрашивает кислую фосфатазу, содержащуюся внутри в виде гранул в цитоплазме нейтрофильных гранулоцитов.
Кислая фосфатаза:
Первичная реакция (реакция ферментативного расщепления) - гидролиза α-нафтилфосфата с участием фермента кислой фосфатазы (3.1.3.2) из класса 3 - гидролаз: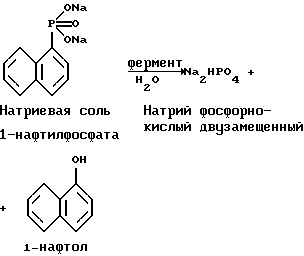
2) Вторичная реакция (реакция сочетания) т.е. взаимодействия 1-нафтола с нейтральным прочным синим В.
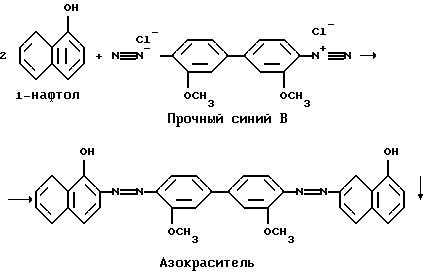
Предложенный способ показывает непосредственное содержание изучаемого фермента в нейтрофильных гранулоцитах и возможность оценки цитохимической реакции, что невозможно определить в сыворотке крови. В мазке определяются состояние микробицидных систем крови, принимающих участие в формировании неспецифической резистентности организма. Определяется активность кислой фосфазы в клетках крови по четырем ступеням.
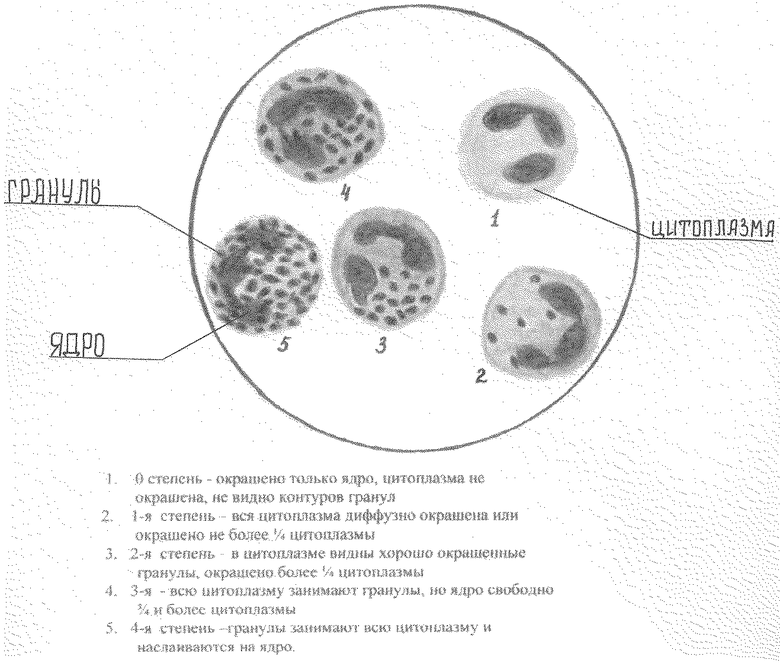
Сущность изобретения поясняется чертежом, где представлена микроскопия по степеням активности ферментов, локализованных в нейтрофилах.
Пример конкретного осуществления способа определения активности кислой фосфатазы в мазках крови
Кровь для исследования брали у животных из яремной вены. У птицы кровь брали из крыловой вены. Из крови делали мазок. Для этого каплю крови наносили на край сухого обезжиренного стекла, которое удерживали между большим и средним пальцами левой руки. Впереди капли под углом 45o подводили шлифованный край покровного стекла так, чтобы образовавшейся угол между стеклами был равномерно заполнен кровью. Движением правой руки от себя каплю распределяем тонким слоем по предметному стеклу. Хорошим мазком будет такой, в котором кровь располагается на поверхности стекла без просветов, в виде равномерной полоски, не выходящей за ее края. Мазки сушат на воздухе и фиксируют в парах 40% формалина в течение 3-4 минут. Для этого на дно эксикатора наливают около 150 мл формалина, оставляют под закрытой крышкой на 30 минут для возгонки паров формалина. Затем осторожно снимают крышку и на решетку эксикатора помещают мазки и закрывают крышкой. Таким образом, мазки фиксируются.
Приготовление буферных растворов
Вначале проводили калибровку иономера рН - 150. В состав буферной смеси входили 0,2 М раствор янтарной кислоты (с молекулярной массой 118,09), из которого готовили раствор - А, для этого брали 2,362 г янтарной кислоты и растворяли в дистиллированной воде в объеме на 100 мл; затем готовили раствор - Б, состоящий из 0,2 М NaOH (молекулярной массой 36,465);
Затем 25 мл раствора А - (янтарной кислоты), добавляли 12 мг ЭДТА и раствором Б - 0,2М NaOH 32 мл доводили рН до 5,0. Очень важно подобрать буферную смесь для получения рН 5,0, а также способности состава буферной смеси активировать фермент - кислую фосфатазу. Если взять количество ЭДТА меньше или больше 12 мг, то невозможно будет довести pH до 5,0 при предложенном количестве других компонентов смеси.
Приготовление инкубационной смеси
Правильное приготовление инкубационной смеси имеет немаловажное значение для дальнейшей окраски мазков. Готовить инкубационную смесь желательно в затемненной комнате. Для ее приготовления готовят раствор 1 и 2.
Приготовление раствора 1
α-нафтилфосфата натрия берут 2,0-2,1 мг, оптимальным количеством α-нафтилфосфата является 2,0 мг. Для растворения добавляли 1,3 мл дистиллированной воды, 0,6612 мл буферной смеси небольшими порциями, помешивая.
Приготовление раствора 2
Берут 5 мг красителя нейтрального прочного синего и растворяют его в 2,5 мл буферной смеси смешивая их постепенно (рН 5,0).
Полученные растворы смешивают, фильтруют в темноте желательно через стеклянный фильтр.
Инкубация мазков
Инкубация мазков проводится исключительно в темноте в течение 2 часов. После фиксации мазки сушат на воздухе в темном месте. На фиксированные формалином мазки наносится равномерным слоем инкубационная смесь. Периодически необходимо добавлять смесь, т.к. происходит испарение жидкости, которая включает в себя легко улетучивающееся вещество (α-нафтол) и при температуре 37-38oС. Необходимо строго соблюдать температурный режим, т.к. активен фермент при заданной температуре. После инкубации мазки промывают под проточной водой, затем в дистиллированной водой и высушивают на воздухе в темном месте.
Для дифференцировки нейтрофильных гранулоцитов от других клеток крови в дальнейшем окрашиваем ядра (желательно на следующий день для лучшей реакции инкубационной смеси) клеток краской 0,5% водным раствором метиленовой сини в течение от 30 секунд до 1 минуты. После окраски краску сливают, промывают дистиллированной водой и высушивают на воздухе в темноте.
Микроскопия мазков
Микроскопию проводят с использованием иммерсионной системы при увеличении (90•15).
Результаты полученных данных при микроскопии мазков.
Активность кислой фосфатазы определяют по количеству гранул красно-коричневого цвета в цитоплазме нейтрофилов, ядра которых докрашены в голубой цвет.
Визуально проводят оценку цитохимической реакции
0 - степень - окрашено только ядро, цитоплазма не окрашена, не видно контуров гранул
1-я степень - вся цитоплазма диффузно окрашена или окрашено не более 1/4 цитоплазмы
2-я степень - в цитоплазме видны хорошо окрашенные гранулы, окрашено более 1/4 цитоплазмы
3-я - всю цитоплазму занимают гранулы, но ядро свободно 3/4 и более цитоплазмы
4-я степень - гранулы занимают всю цитоплазму и наслаиваются на ядро.
Средний цитохимический индекс выводят по следующей формуле, предварительно подсчитывая 100 нейтрофилов: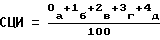
где а, б, в, г, д - количество клеток соответственно 0, 1, 2, 3, 4-й степени.
Данный способ позволяет экспресс-методом определить микробицидные свойства системы крови, в частности определения кислой фосфатазы в нейтрофильных гранулоцитах. Определение активности кислой фосфатазы в мазках крови относится к тестам II уровня диагностики иммунного статуса организма животных и птиц. Концентрация содержания фермента кислой фосфатазы указывает на состояние иммунного статуса и общее клиническое состояние организма.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В МАЗКАХ КРОВИ КРУПНОГО РОГАТОГО СКОТА И ПТИЦ | 2000 |
|
RU2212843C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ КИСЛОЙ ФОСФАТАЗЫ ГОМОГЕНАТА ИЗ ОРГАНОВ И ТКАНЕЙ ПЧЕЛ | 2003 |
|
RU2256918C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ КИСЛОЙ ФОСФАТАЗЫ В МАЗКАХ ГЕМОЛИМФЫ У ПЧЕЛ | 2003 |
|
RU2256919C2 |
| СПОСОБ ЦИТОХИМИЧЕСКОГО ОПРЕДЕЛЕНИЯ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ В МАЗКАХ КРОВИ ЖИВОТНЫХ | 2000 |
|
RU2196509C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В ГОМОГЕНАТЕ ИЗ ОРГАНОВ И ТКАНЕЙ У ПЧЕЛ | 2003 |
|
RU2256703C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В МАЗКАХ ГЕМОЛИМФЫ У ПЧЕЛ | 2003 |
|
RU2253679C2 |
| СПОСОБ ВЫЯВЛЕНИЯ ЩЕЛОЧНОЙ ФОСФАТАЗЫ В ИММУНОКОМПЕТЕНТНЫХ ОРГАНАХ ЖИВОТНОГО | 2000 |
|
RU2198404C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДИФФЕРЕНЦИРОВКИ T-, B-, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ ЖИВОТНЫХ И ПТИЦ | 2000 |
|
RU2192638C2 |
| Способ определения активности миелопероксидазы нейтрофилов в мазках крови животных | 2015 |
|
RU2612149C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РАКА ШЕЙКИ МАТКИ | 2012 |
|
RU2488823C1 |
Изобретение относится к ветеринарной медицине. Способ заключается в том, что в качестве субстрата используют мазки крови, для приготовления буферной смеси используют 0,2 М раствор янтарной кислоты, добавляют 12 мг ЭДТА и 0,2 М NaOH и доводят рН до 5,0, затем в инкубационную смесь добавляют 0,6612 мл буферной смеси для обеспечения рН 5,0, инкубацию проводят в темноте 2 ч, промывают дистиллированной водой, высушивают и дополнительно окрашивают мазки крови краской 0,5%-ным водным раствором метиленовым синим в течение 0,5-1 мин и по количеству окрашенных гранул красно-коричневого цвета в цитоплазме нейтрофилов, ядра которых докрашены в голубой цвет, определяют процент активности фермента кислой фосфатазы, по степеням определяют средний цитохимический индекс. Способ обеспечивает повышение эффективности иммунологических исследований и экономической эффективности. 1 ил.
| ХЕЙХОУ Ф.Г., ДЖ., КВАГЛИНО Д | |||
| Гематологическая цитохимия, Лабораторные методы | |||
| - М.: Медицина, 1983, с.144-145 | |||
| BURSTONE M.S | |||
| New histochemical technigues for the demonstration of tissue oxidase | |||
| Cytochome oxidase | |||
| J.Histochem | |||
| Cytochem | |||
| Автоматический сцепной прибор американского типа | 1925 |
|
SU1959A1 |
| КОЗИНЦЕВ Г.И | |||
| и др | |||
| Исследование системы крови в клинической практике | |||
| - М.: Триада-Х, 1977, с.314-317 | |||
| ПИРС Э | |||
| Гистохимия | |||
| М.: Иностранная литература, 1956, с.409 | |||
| СИМОНЯН Г.А | |||
| и др | |||
| Ветеринарная гематология | |||
| - М.: Колос, 1995, с.97, 98. | |||
Авторы
Даты
2003-01-20—Публикация
2000-04-17—Подача