Изобретение относится к обнаружению продуцирования антител, в частности к обнаружению активного синтеза антител в образцах крови в ответ на инфекцию или вакцинацию и т.д. посредством модифицированного твердофазного иммуноферментного анализа (ELISA).
Анализ ELISA давно используют для обнаружения и измерения антитела (или антигена). Чаще всего ELISA используют как серологический анализ, но его также используют для изучения иммунохимических свойств антигенов или антител и, кроме того, его часто применяют, например, в оценке и характеризации иммунных ответов, для исследования продуцирования антител клеточными культурами, в гибридомной технологии и т.д.
Благодаря своей чувствительности, простоте и легкости и скорости осуществления этот метод широко используется для диагностики, и в настоящее время он обычно применяется в клинических лабораториях для обнаружения антител к инфекционным агентам в сыворотке или плазме крови после инфицирования или вакцинации. Так, например, многие тесты на инфицирование человека вирусом иммунодефицита (ВИЧ) основаны на обнаружении антител к вирусу в сыворотке или плазме крови пациентов с использованием анализа ELISA.
Хотя простой серологический ELISA-тест позволяет обнаружить присутствие нужного антитела в образце, однако он не позволяет выявить различие между синтезом антител, в ответ на антиген, и антителами, уже продуцированными в результате инфекции или пассивного переноса и т.д. В некоторых случаях может оказаться достаточным просто получение информации относительно присутствия антитела, тогда как в других случаях бывает необходимо определить: синтезируются ли нужные антитела лимфоцитами именно во время тестирования, например во время курса вакцинации или при диагностике заражения у младенцев, или эти антитела являются просто пассивно перенесенными материнскими антителами. Эта цель не может быть достигнута классическим методом ELISA.
Поэтому были разработаны другие методы, которые дают возможность выявления текущего синтеза антител. В этом отношении особенно можно отметить твердофазный иммунноферментный спот-анализ (ELISPOT) (также известного как спот-ELISA или ELISA-анализ методом бляшек), как было описано, например, в публикации Сзеркинский и др. в "ELISA и другие твердофазные иммуноанализы" (Czerkinsky et al., ELISA and other Solid Phase Immunoassays, Ed. D.M.Kenneny and S. J. Challacombe, 1988, Chapter 10, 217-239). Эта техника, основанная на способе ELISA, дает возможность количественного определения лимфоцитов, секретирующих антитело против одного или более антигенов-мишеней. По существу ELISPOT является вариантом метода ELISA, в котором клетки, секретирующие антитело (ASC), могут быть обнаружены путем культивирования лимфоцитов в специально модифицированных ELISA-лунках, сенсибилизированных антигеном-мишенью и путем замены стандартных реагентов для ELISA анализа фермент-субстратными комплексами, продуцирующим окрашенные преципитаты (пятна), примыкающие к секретирующей клетке. Эти пятна могут затем быть сосчитаны, что позволяет определить число антителопродуцирующих клеток. Ингибиторы синтеза белка могут быть включены в культуральную среду для подтверждения того, что детектируемые пятна присутствуют благодаря новому синтезу антител во время периода инкубации in vitro.
Хотя способ ELISPOT доказал высокую эффективность в изучении динамики гуморальных иммунных ответов и используется для определения спонтанных ASC, которые кратковременно появляются в периферическом кровотоке иммунизированных индивидуумов, однако некоторые особенности этого способа накладывают ограничения на его использование при установлении клинического диагноза. Во-первых, так как для каждого образца необходимо сосчитать индивидуальные пятна, что может потребовать определенных затрат времени и труда, то этот способ не совсем подходит для анализа большого числа образцов, как это происходит в клинической диагностической лаборатории. Во-вторых, в данном случае оценивается только ряд клеток, выделяющих антитело в каждом образце, что требует относительно больших объемов образцов, т.е. несколько миллилитров. Кроме того, ELISPOT-планшеты являются дорогостоящими, и анализ нелегко поддается автоматизации.
Поэтому очевидно, что несмотря на достижения в разработке способов обнаружения антител, необходимость в анализе, который был бы недорогостоящим и эффективным по своей простоте и быстроте осуществления, который позволял бы точно определять количество спонтанно продуцируемых антител и идентифицировать вновь синтезируемые антитела, и, в особенности, который мог бы быть осуществлен на пробах крови, взятых для диагностических целей, до сих пор остается актуальной. На разработку такого способа и направлено настоящее изобретение.
Следовательно, в одном из своих аспектов настоящее изобретение относится к способу обнаружения активного продуцирования антител в ответ на антиген-мишень в образце крови, причем указанный способ включает:
контактирование в присутствии и в отсутствие ингибитора синтеза белка, аликвоты указанного образца или, необязательно, лимфоцитов, непосредственно выделенных из указанного образца, с твердой фазой в условиях, благоприятствующих продуцированию и секреции антител лимфоцитами;
определение в растворе, связывания антитела с указанным антигеном(ами) на твердой фазе; и
сравнение указанного связанного антитела в присутствии или в отсутствие ингибитора синтеза белка, в целях определения уровня активной секреции антитела в ответ на указанный антиген(ы).
Используемый в настоящем описании термин "активное продуцирование антител" относится к спонтанно выделяемым антителам, продуцируемым лимфоцитами в образце, которые являются антителами, активно продуцируемыми в процессе анализа вследствие активно проходящего иммунного ответа. Во всех случаях эти антитела направлены против антигенов, которые присутствуют in vivo, а не in vitro, или до, или во время осуществления анализа методом настоящего изобретения.
Используемый в настоящем описании термин "активная секреция антител в ответ на указанный антиген" подразумевает, что активно продуцируемые антитела связываются с антигеном, используемым в анализе, хотя используемый антиген может не являться иммуногеном, в первую очередь стимулирующим иммунный ответ. Так, например, антиген, используемый в анализе, и иммуноген, простимулировавший или стимулирующий продуцирование антител in vivo, могут связываться с детектируемыми антителами благодаря идентичным или очень схожим антигенным детерминантам, но в других отношениях, антиген и иммуноген могут быть неидентичными. Антиген, используемый в способе изобретения, может быть веществом, содержащим все или некоторые части релевантного иммуногена, например полученного от инфицированных особей, или очищенные части того же самого или подобного вещества, либо этот антиген может быть просто получен синтетически, например путем химического синтеза или рекомбинантной экспрессии, и иметь добавленные или делетированные части по сравнению с природным антигеном. Таким образом могут быть использованы гибридные белки или молекулы, экспрессирующие лишь подходящие эпитопы.
В общих чертах указанный способ настоящего изобретения включает инкубирование лимфоцитов из образца крови в контакте с подходящей твердой поверхностью для иммобилизации детектируемых антител в условиях, стимулирующих продуцирование и секрецию антител лимфоцитам, а затем удаление клеток и определение антитела, связанного с антигеном на твердой фазе. Вновь синтезированные антитела могут быть идентифицированы и подсчитаны путем сравнения уровня определяемых связанных антител в присутствии или в отсутствие ингибитора синтеза белка.
Неожиданно было обнаружено, что способ изобретения позволяет использовать небольшие объемы образцов крови (например, микролитровые (мкл) объемы меньше чем 1 мл) непосредственно для определения спонтанного продуцирования антител нестимулированными лимфоцитами без предшествующей стадии предварительного культивирования лимфоцитов до инкубации с твердой фазой. Другими словами, в способе анализа по данному изобретению лимфоциты из образца используют непосредственно без какой-либо предшествующей обработки или стимуляции, например стимуляции in vitro антигеном. Таким образом, могут быть определены антитела, секретируемые лимфоцитами во время испытания. Так, например, используя даже небольшие объемы образцов, спонтанно происходящий синтез антитела в ответ на тест-антиген может быть успешно дифференцирован от "фоновой" активации лимфоцитов. Лимфоциты также анализируются в ситуации, когда они спонтанно секретируют антитела без стимуляции клеток для обнаружения какой-либо памяти. В противоположность этому другие опубликованные способы используют in vitro антигенную стимуляцию для увеличения чувствительности теста. В настоящем изобретении, с другой стороны, используется спонтанная секреция антитела, что позволяет обнаружить антитела в крови и свидетельствует заражение конкретным тест-антигеном; при этом лимфоциты плазмы будут секретировать антитело против тест-антигена в первые несколько недель после инфицирования или вакцинации и т.д. Обнаружение таких антител способом настоящего изобретения дает возможность диагностировать или обнаруживать инфекцию или контролировать ответ антител на вакцинацию и т.д. Этот способ особенно эффективен для младенцев и новорожденных, когда важно дифференцировать вновь синтезируемое антитело от пассивно перешедших материнских антител. Тот же образец крови может быть проанализирован на антитела против нескольких определенных инфекционных агентов либо в отдельных анализах, либо в одном и том же анализе, с использованием множества соответствующих антигенов. Таким образом, это позволяет использовать определенные контактирующие антигены, соответствующие клиническому синдрому, имеющемуся у пациента. В диагностике инфекций также важно иметь возможность отличать вновь синтезированные антитела от антител, уже присутствовавших в результате более раннего заражения. Иммунологическая память на повторную антигенную стимуляцию in vitro несовместима с анализом, нацеленным на идентификацию текущей острой инфекции, и, следовательно, предшествующие способы, основанные на антигенной стимуляции, не имеют преимущества данного способа. Также включение стадии антигенной стимуляции будет неблагоприятно влиять на преимущественный временной фактор анализа настоящего изобретения, который является очень быстрым для осуществления по сравнению с известными способами.
Антигены, на которые нацелены антитела, обнаруживаемые способом изобретения, могут быть как бактериальными, так и вирусными антигенами. Клинически важными антигенами являются, но не ограничиваются ими, например, антиген вируса простого герпеса (HSV), цитомегаловируса, вируса иммунодефицита человека (HIV) и любого из вирусов гепатита. Обнаружение таких антигенов могло бы быть использовано для быстрого установления инфицированы ли пациенты, например, в целях отбора крови или для установления и/или контроля заражения. Этот способ особенно эффективен благодаря своей простоте и может быть использован в случаях, когда сложное оборудование недоступно, например в полевых условиях.
Используемые в настоящем описании термины "обнаружение" и "определение количества" означают как количественную, так и качественную оценку уровня продуцирования антител для получения абсолютного значения количества антител, продуцируемых в образце, и индекса, соотношения, процента или аналогичных параметров уровня продуцирования антител, а также полуколичественную и качественную оценку.
Главное преимущество настоящего изобретения заключается в том, что для осуществления анализа требуются лишь небольшие объемы образцов, например 50-500 мкл, предпочтительно 100-300 мкл и обычно 100-200 мкл крови, или продукта крови в объеме, сравнимом с источником цельной крови, в противоположность классическим диагностическим тестам, для которых обычно требуются объемы сыворотки в несколько мл. Это особенно важно в случае отбора крови у новорожденных, так как способ изобретения требует только микролитровые объемы.
Образец крови, обычно образец периферической крови, может быть непосредственно использован в анализе, хотя может оказаться предпочтительным сначала выделить лимфоциты из образца. Это может быть сделано с использованием стандартных методик, хорошо известных специалистам. Так, например, могут быть использованы различные препараты цельной крови, например, гепаринизированная кровь, ЭДТА-кровь (EDTA) и т.д., которые обычно изготавливаются в клинических лабораториях. Хотя это не имеет большого значения, эритроциты, присутствующие в образце, могут быть подвергнуты лизису, например с использованием обычных способов кратковременного выдерживания образца в дистиллированной воде или в хлористом аммонии, или с использованием других хорошо известных методов гемолиза. При этом следует принять во внимание, что все обогащенные или очищенные препараты должны содержать лимфоциты, присутствующие в цельной крови, из которой был получен препарат, для того чтобы можно было определить спонтанное продуцирование антител. Если необходимо, лимфоциты могут быть выделены, например, с использованием стандартных сред выделения лимфоцитов, например лимфопреп (Limphoprep, Nyegaard Co., Осло, Норвегия), или с использованием иммуномагнитного разделения (IMS), или аналогичной системы для твердофазного разделения, или другие стандартные способы. В случае использования IMS или аналогичных методов разделения твердая фаза, например магнитные шарики, покрытые антителом, специфическим для определенных популяций лейкоцитов, могут быть использованы для селективного выделения полезных лимфоцитов. В случае использования выделенных лимфоцитов перед их использованием клетки могут быть промыты до использования стандартными методами промывки. Замечено, однако, что экстенсивная промывка клеток не требуется. Действительно, без экстенсивной промывки может быть улучшена жизнеспособность клеток, и способ будет более быстрым.
Затем образец крови, обработанный, если требуется, как указано выше, или выделенные лимфоциты подвергают контакту с твердой фазой, несущей подходящего связывающего партнера для иммобилизации обнаруживаемого антитела или антител. Обычно таким связывающим партнером является тест-антиген или антигены, узнаваемые определяемым антителом или антителами. В одном из вариантов своего осуществления настоящее изобретение относится к способу обнаружения активного продуцирования антител в образце крови, причем указанный метод включает:
контактирование в присутствии и в отсутствие ингибитора синтеза белка аликвоты указанного образца или, необязательно, лимфоцитов, непосредственно выделенных из указанного образца, с твердой фазой, несущей один или более антигенов, опознаваемых антителом или антителами для определения;
определение в растворе связывания антитела с указанным антигеном(ами); и
сравнение указанного связывания антитела в присутствии или в отсутствие ингибитора синтеза белка для определения уровня активной секреции антител в ответ на указанный антиген(ы).
Могут также быть использованы альтернативные связывающие партнеры, например белок А, белок G или антитела, которые опознают и связывают определяемое антитело. В последнем случае высоко специфичное связывание не требуется, так как в данном варианте осуществления анализа специфичность имеет место в последующем связывании антигенов, которые специфически связываются с определяемыми антителами. Таким образом, во всех вариантах осуществления способа создается специфический комплекс антиген-антитело. Присутствие таких комплексов, иммобилизованных на твердой подложке, устанавливается на стадии детекции при осуществлении способа настоящего изобретения. Твердая фаза может быть любой из хорошо известных подложек или матриц, которые широко используются в настоящее время или предлагаются для иммобилизации, разделения и т. д. Они могут иметь форму частиц, пластин, гелей, фильтров, мембран или полосок, пробирок или планшетов для микротитрования и т.д. и могут быть изготовлены из полимерного материала. Однако для легкости и простоты проведения анализа могут быть использованы стандартные планшеты и лунки, предпочтительно стандартные ELISA-планшеты.
Твердая фаза может также быть модифицирована для обнаружения антител, специфичных для ряда различных антигенов. Так, например, диски или полоски и т.д. из материала, подходящего для твердой фазы, например нитроцеллюлозы или тому подобного, могут быть сенсибилизированы различными антигенами и добавляться одновременно в лунки для микротитрования или другой подходящий сосуд, не содержащий какого-либо контактирующего антигена. Способы определения связывания антител могут затем быть использованы для отличия разных антигенов друг от друга. Наборы дисков, каждый из которых сенсибилизирован соответствующими антигенами, соответствующими определенному клиническому состоянию или синдрому, могут быть использованы для того, чтобы идентифицировать, какой из предполагаемых агентов вызывает заболевание. Затем эти диски должны быть индивидуально подвергнуты обработке в отдельных лунках. Особенность этой методики заключается в том, что она позволяет экономить материал, поскольку эти тесты могут быть выполнены для одновременного тестирования множества различных антигенов (либо от того же самого инфекционного агента или от различных агентов, относящихся к данному клиническому синдрому или состоянию в каждом случае) с использованием того же самого небольшого объема крови. Альтернативный способ заключается в использовании множества образцов крови в отдельных лунках, каждая из которых покрыта различными связывающими партнерами, например антигенами или антителами; и в разработке соответствующего теста.
Методика для связывания связывающего партнера, например антигена, с твердой фазой, также очень хорошо известна и широко описана в литературе. Многие стандартные методы сенсибилизации антигеном описаны, например в "ELISA and other Solid Phase Immunoassays, Theoretical and Practical Aspects"; Ed. D.M.Kenneny S.J.Challacombe, John Wiley&Sons. Если необходимо, чашки могут быть промыты и блокированы также с использованием стандартной методики. Так, например, стандартные планшеты для микротитрования, например ELISA-планшеты, могут просто быть покрыты связывающим партнером путем инкубации планшетов в течение ночи при 4oС в подходящем буфере, например в забуференном фосфатом физиологическом растворе (PBS), содержащем связывающего партнера, например белка, в концентрации от 0.01 до 150 мкг/мл, с последующим блокированием с использованием подходящей блокирующей среды (обычно среды для культивирования культуры) и инкубацией, например, при 37oС от 1 до 5 часов. После удаления блокирующего раствора чашки готовы к использованию.
Удобно, однако, чтобы материалы, требуемые для выполнения способа по данному изобретению, были бы доступны в виде набора, в котором твердая подложка уже покрыта связывающим партнером и соответствующим образом блокирована.
Как отмечено выше, стадия контактирования обычно включает инкубацию образца или отделенных лимфоцитов в присутствии твердой фазы в условиях, стимулирующих синтез и выделение антител. Для этого могут быть использованы стандартные условия инкубации по методу ELISPOT, как описано, например Czerkinsky et al., 1988 (см.выше). Обычно образец или клетки инкубируют при 37oС с 5% СО2 в воздухе, когда среда, в которой инкубируют клетки, воспринимает СО2 как часть буферной системы. Могут быть также использованы СО2-независимые среды, в которых действуют альтернативные буферные системы, такие как среда, содержащая хорошо известный HEPES-компонент. В этих случаях клетки просто инкубируют при 37oС, что в дальнейшем упрощает анализ и его требования к лабораторному оборудованию. Время инкубирования может варьироваться, но обычно оно составляет, по меньшей мере, 1-2 часа. Было установлено, что время инкубирования от 2 до 6 часов, например от 2 до 4 часов, приводит к хорошим результатам, хотя в некоторых случаях могут оказаться предпочтительными более продолжительные периоды инкубации, например до 12 или 24 часов, или в течение ночи. Подходящие среды для инкубации хорошо известны специалистам, такими средами являются любые стандартные среды для культивирования клеток, например модифицированная по способу Дульбекко среда Игла (DMEM), RPMI или хорошо известная клеточная культуральная среда с использованием HEPES, в качестве СО2-независимой буферной системы, содержащей подходящие сыворотки, например фетальную телячью сыворотку (FCS) или другие компоненты, например глутамин, если это необходимо. Необязательными дополнительными компонентами в среде могут служить антибиотики, например гентамицин, пенициллин, стрептомицин и т.д., другие аминокислоты, факторы роста и т.д.
Может оказаться предпочтительным разбавить суспензию образца/клеток перед стадией контактирования и для этого может быть использован подходящий интервал разведений клеток/образца. Разведение обычно осуществляют с использованием культуральной среды в качестве разбавителя.
Для того чтобы выявить текущий синтез антитела, инкубацию осуществляют в присутствии или в отсутствие ингибитора синтеза белка. Например, перед инкубацией к части образца/клетки аликвоты добавляют ингибитор, чтобы блокировать белок, и с этого момента антитело, синтез и части ингибируют без ингибитора. В этих целях может быть использован любой из обычно известных ингибиторов синтеза белка, например циклогексимин. Могут быть использованы концентрации 10-5000 мкг/мл, например 50-500 мкг/мл циклогексимина.
Предпочтительно также включать ингибитор АТФазы, такой как азид натрия или другие подобные ингибиторы, вместе с ингибитором синтеза белка для того, чтобы быстро и полностью прекратить клеточный метаболизм.
После инкубации образец/клетки удаляют с твердой фазы. Обычно это может быть осуществлено путем простой промывки с использованием подходящей среды, например буфера, такого как PBS (забуференный фосфатом физиологический раствор). Однако, как было установлено, экстенсивная промывка не требуется.
Твердая фаза затем подвергается стадии детекции на связывание антитела. Стадия детекции, то есть регистрация сигнала, происходит в растворе. Может быть использован любой из известных способов определения связывания антитела при условии, что в данном растворе генерируется четкий сигнал; например, способ, основанный на флуоресценции, хемолюминисценции, калориметрии или ферментативной реакции с продуцированием определяемого сигнала. Однако, обычно, для обнаружения антител используют иммунный анализ, а предпочтительнее твердофазный иммуноферментный анализ (ELISA).
Иммуноанализ, а в частности ELISA-методика, хорошо известны специалистам и описаны в литературе (см., например, ELISA and other Solid Phase Immunoassays, Theoretical and Practical Aspects; Ed. D.M.Kenneny S.J.Challacombe, John Wiley&Sons).
После удаления образца/клеток может быть добавлен конъюгат фермент-антитело, например, в методе определения ELISA, который связывается с антителом, связанным с антигеном на твердой фазе. Аналогично, если определяемое антитело связано с твердой фазой не специфически, а посредством связывающего партнера, например антитела против антител к различным образцам, то может быть добавлен конъюгат фермент-антитело, который будет специфически связываться с иммобилизованным определяемым антителом. Затем для получения детектируемого сигнала добавляют ферментный субстрат для того, чтобы получить определяемый сигнал. В настоящем изобретении удобно использовать растворимый субстрат, продуцирующий к детектируемому сигналу в растворе. Такое использование является преимуществом, так как облегчает и упрощает обработку большого числа образцов и позволяет оценить продуцирование антител, хотя, как отмечалось выше, определение абсолютного количества не является необходимым, и при желании можно ограничиться качественными или полуколичественными результатами. Для удобства, может быть выбран такой сигнал, который дает спектрофотометрически детектируемый сигнал, который может быть считан просто путем регистрации оптической плотности, например, с использованием стандартного аппарата для прочтения ELISA-планшетов (ридер). Действительно, могут быть использованы стандартные ELISA-реагенты, что имеет преимущество для проведения анализа по данному изобретению, совместимого с существующими способами и методами, обычно используемыми в клинических лабораториях. Однако могут быть использованы и другие сигнал-генерирующие системы, дающие сигналы, которые могут быть обнаружены посредством флуоресценции, хемолюминисценции и т.д.
Для усиления сигнала и увеличения чувствительности могут также быть использованы мммуноферментные методы амплификации, например, методы с использованием авидин-биотина, такие как экстравидиновая система, поставляемая Sigma. Биотинилированные "вторые" антитела используют в качестве ELISA-реагентов в комбинации с комплексом "пероксидаза-авидин". Так как одна молекула авидина может связываться с несколькими молекулами биотина, то использование авидин-биотин-пероксидазных комплексов увеличивает поверхностную концентрацию молекул пероксидазы, повышая чувствительность способа.
Материалы и средства, требуемые для осуществления стадии инкубации клеток (контактирования) и стадии определения связывания антитела, могут также поставляться в форме набора вместе с твердой фазой, покрытой связывающим партнером. Информация, полученная в результате проведения анализа по данному изобретению, может быть дополнена использованием других методов анализа. Дополнительные и полезные данные относительно антител, уже присутствовавших в сыворотке/плазме, могут быть получены классическим методом ELISA. Кроме того, после выделения лимфоцитов из образца крови, если эту стадию осуществляют, оставшаяся плазма может быть использована для определения ранее существовавших антител с применением той же самой твердой фазы, сенсибилизированной связывающим партнером, которую используют в анализе по данному изобретению.
Для гарантии надежности способа анализа по данному изобретению могут быть использованы соответствующие средства контроля. Во-первых, сравнение между блокированными лунками и неблокированными лунками будет гарантировать, что в анализе по изобретению регистрируется продуцирование антител тест-клетками, а не просто антитела, ранее присутствовавшие в периферической крови. В случае использования очищенных лимфоцитных препаратов в качестве образца такое сравнение будет гарантировать, что следовые количества захваченных антител из периферической крови в лимфоцитном образце не будут оказывать неблагоприятного влияния на результаты теста. Во-вторых, чтобы удостовериться, что регистрируемая разница между сигналами от блокированных и неблокированных лунок происходит не благодаря спорадически и неспецифически активированным ("фоновым") лимфоцитам, используется антиген негативного контроля. Этот антиген может быть получен от инфекционного агента, который имеет наименьшую вероятность ответственности за острое заболевание пациента, например, токсоид столбняка. Число таких "фоновых" активированных лимфоцитов будет в любом случае при всех обстоятельствах много ниже, чем требуется для положительного результата теста, проводимого способом настоящего изобретения. Это обстоятельство учитывалось при разработке настоящего изобретения.
Как отмечено выше, благодаря своей легкости, скорости и простоте осуществления анализ настоящего изобретений пригоден для диагностического или клинического применения либо для использования в ветеринарной практике, например в рыбоводстве. Кроме возможности использования небольших объемов образцов, дополнительным преимуществом настоящего метода является то, что в нем требуется только один образец, а не пары сыворотки, отобранные с интервалом от двух до трех недель, так как это требуется в большинстве традиционных серологических тестов. При этом не требуется применения сложного оборудования, и анализ легко автоматизируется. Кроме того, если требуется, вполне возможно протестировать различные изотипы иммуноглобулина.
Вышеизложенный способ анализа по данному изобретению обеспечивает возможность определить присутствие или степень присутствующей инфекции посредством анализа на спонтанную секрецию специфических антител к определенному антигену. Такой способ может быть эффективно использован для оценки уже известного заболевания, для которого доступны антигены, родственные соответствующему иммуногену, что таким образом обеспечивает наличие специфического маркера инфекции. Однако в некоторых клинических ситуациях конкретное заболевание или инфекция могут не быть идентифицированными и/или подходящий антиген может быть недоступен для использования в анализе. В таких случаях анализ может быть модифицирован для определения присутствия или уровня неспецифических индикаторов инфекции. Так, например, лимфоцитсодержащие образцы, например цельная кровь или очищенные или обогащенные лимфоцитные препараты из нее, могут быть исследованы в отношении продуцирования инфекционных маркеров, например цитокинов или интерферонов, например интерферона-γ.
Таким образом, в еще одном своем аспекте настоящее изобретение относится к способу определения присутствия неспецифических индикаторов инфекции в образце крови, при этом указанный метод включает:
(a) контактирование в присутствии и в отсутствие ингибитора синтеза белка аликвоты указанного образца или необязательно лимфоцитов, непосредственно выделенных из указанного образца, с твердой фазой в условиях, которые допускают продуцирование и выделение индикаторов инфекции лимфоцитами;
(b) определение в растворе связывания индикаторов инфекции с партнером связывания на твердой фазе; и
(c) сравнение указанного связывания индикатора инфекции в присутствии или в отсутствие ингибитора синтеза белка, в целях определения количества индикаторов инфекции в указанном образце.
Для выполнения этого способа на твердой фазе могут быть сенсибилизованы походящие молекулы захвата, например антитела к определяемым индикаторам инфекции. Для определения присутствия указанных индикаторов инфекции, иммобилизованных на твердой фазе, могут быть использованы методы, описанные выше, например использование меченых антител или лигандов. В этом способе специфические маркеры могут быть идентифицированы путем соответствующего отбора иммобилизирующей молекулы или детектируемой молекулы. Так, например, все белки в образце могут быть иммобилизованы на твердой подложке, и определение может быть осуществлено с использованием меченного специфического антитела или лиганда. Альтернативно, специфический связывающий партнер может быть использован для иммобилизации подходящих индикаторов инфекции, которые затем могут быть соответствующим образом
помечены или положительно, или отрицательно, например, в первом случае путем связывания с доменом, присутствующем на индикаторе инфекции, но не единственным для этой молекулы, или во втором случае путем мечения свободного связывающего партнера на твердой фазе. Наборы для осуществления этого способа также являются частью настоящего изобретения.
Ниже приводится более подробное описание изобретения со ссылкой на соответствующие неограничивающие примеры, в которых способ анализа по настоящему изобретению упоминается как Plasmacute-анализ.
Пример 1
Общая методика
Клетки: гепаринизированная кровь, взятая через различные промежутки времени после вакцинации у добровольцев, получивших инактивированную вакцину гриппа. Кровь смешивают с равным объемом PBS. Лимфоциты отделяют с помощью Lymphoprep (Nyegard и Со, Осло). Клетки промывают дважды в забуференном фосфатом физиологическом растворе (PBS), ресуспендируют (разведения) в модифицированной по способу Дульбекко среде Игла (DMEM) с добавлением 20% фетальной телячьей сыворотки FCS, 2 мМ L-глутамина, 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина (Pen+Strep) = MEDIUM (СРЕДА).
Останавливающий (стоп) раствор: 1 мкг/ мл циклогексимида, растворенного в PBS, содержащем 10% азида натрия.
ELISA и антигены гриппа: очищенные поверхностные антигены от трех вирусных штаммов в вакцине гриппа были использованы в клинических опытах, обозначенные для краткости H3N2, H1N1 и В.
Чашки ELISA: Грейнеровские EIA чашки 655001 F-формы или костаровские EIA чашки 3590. Покрывают в количестве 100 мкл/лунку раствором 10 мкг/мл белка в PBS, выдерживают ночь при 4oС. Блокируют средой в течение 1 часа при комнатной температуре. Промывают один раз PBS.
ТЕСТ: 100 мкл разведения клеточных суспензий в среде добавляли к резервуарам в трех экземплярах в двух параллельных комплектах для каждого из трех антигенов гриппа. Один комплект из трех лунок блокируют на первоначальной стадии добавлением 50 мкл стоп-раствора. Инкубируют различное время при 37oС в инкубаторе с 5% СО2 в воздухе. ELISA-чашки промывают один раз PBS, затем дважды PBS с 0.05% Tween 20. Добавляют 50 мкл/лунку соответствующим образом разведенного конъюгата кроличьего антитела против иммуноглобулина (Ig) человека с пероксидазой (Sigma) и оставляют при комнатной температуре на 1 час. Чашку впоследствии проявляют, используя субстрат о-фенилен диамин (OPD) и регистрируют оптическую плотность при 492 нм.
Образцы крови через 11 дней после вакцинации приведены в табл.А.
Время инкубации клеток: 4 часа, 0 часов = блокированные лунки.
Данные означают среднюю величину для трех лунок и выражены в виде оптической плотности х1000, диапазон погрешности ±10%.
Вывод: 6.6 х 104=66000 клеток дают значительное увеличение сигнала через 4 часа инкубации. Оптическая плотность H3N2 возросла на 98%, H1N1 на 153% и В на 50%.
Это представительный пример. Дополнительные тесты показали, что инкубация клеток в течение ночи дает еще более четкое различие между блокированными и неблокированными лунками с оптической плотностью выше 1000. Система также работает для более короткого времени инкубации, например 2-3 часа. 10-кратное число клеток, например 6.6 х 103 клеток на лунку, может также, но не всегда, давать более четкое различие.
Пример 2
Общая методика
Клетки: гепаринизированная кровь, взятая через 7 дней после вакцинации у добровольцев, получивших инактивированную вакцину гриппа. Кровь смешивают с равным объемом PBS. Лимфоциты отделяют с помощью Lymphoprep (Nyegard &Co, Осло). Клетки промывают дважды в PBS, ресуспендируют в модифицированной по способу Дульбекко среде Игла с добавлением 20% FCS, 2 мМ L-глутамина, 100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина (Pen+Strep) = MEDIUM (СРЕДА).
Останавливающий (стоп) раствор: 1 мкг/мл циклогексимина, приготовленного в PBS, содержащем 10% азида натрия.
Тест-антигены: очищенные поверхностные антигены от трех вирусных штаммов в вакцине гриппа были использованы в клинических опытах, обозначенные здесь для краткости H3N2, H1N1 и В.
Контрольный антиген: токсоид столбняка (не адсорбирован алюминием, Lederle).
ELISA-планшеты: Грейнеровские EIA планшеты 655001 F-формы или костаровские EIA чашки 3590 покрывают в количестве 100 мкл/лунку раствором 10 мкг/мл белка в PBS, выдерживают в течение ночи при 4oС. Блокируют средой в течение 1 часа при комнатной температуре. Промывают один раз PBS.
ТЕСТ: 100 мкл разведения клеточных суспензий в среде добавляли к лункам в трех экземплярах в двух параллельных комплектах для каждого из трех антигенов гриппа и контрольного антигена токсоида столбняка. Один комплект лунок блокируют на первоначальной стадии добавлением 50 мкл стоп-раствора. Инкубируют различное время при 37oС в инкубаторе с 5% СО2 в воздухе. После инкубации ELISA-планшеты промывают один раз PBS, затем дважды PBS с 0.05% Tween 20. После этого добавляют 50 мкл/лунку соответствующим образом разведенного конъюгата кроличьего антитела против иммуноглобулина (Ig) человека с пероксидазой (Sigma) и оставляют при комнатной температуре на 1 час. Планшет впоследствии проявляют, используя субстрат о-фенилендиамин (OPD; Sigma) и регистрируют оптическую плотность при 492 нм. [Для увеличения чувствительности тест может быть модифицирован дополнительной стадией до добавления субстрата, проводимой в течение 1 часа с использованием экстравидин/пероксидазы. Для этого необходимо использование биотинилированного конъюгата вместо пероксидазного конъюгата (Sigma)].
Результаты представительного примера (без экстравидина) приведены в табл.Б.
7 дней после вакцинации (2 человека, #1 и #2)
Время инкубации клеток: 3 часа, 0 часов = блокированные лунки
Данные отвечают среднему их трех значений и выражены в виде оптической плотности х1000, диапазон погрешности ±16%.
Обследованные люди были подростками (16 лет). Хорошо известно, что молодежь реагирует особенно хорошо на A/H1N1 вакцину гриппа. Как видно из вышеуказанной таблицы, оба субъекта #1 и #2 обнаруживали хорошую реакцию. Однако обычно люди, подвергаемые вакцинации, реагируют по-разному на различные компоненты вакцины, так что можно было ожидать такое различие в увеличении оптической плотности. Показано, что субъект #1 слабо реагирует на В-вирус, в то время как субъект #2 значительно отреагировал только на H1N1 вирус. Как ожидалось, ни один из них не прореагировал на токсоид столбняка. Однако, если клетки были стимулированы in vitro токсоидом в течение периода в несколько дней, их более ранняя иммунологическая память (от вакцинации в детстве) могла привести к продуцированию антитела против токсоида столбняка. В реальном случае заражения, диагностируемого в лаборатории, способом настоящего изобретения только один тест-агент/антиген будет давать положительный сигнал.
Пример 3
Общая методика
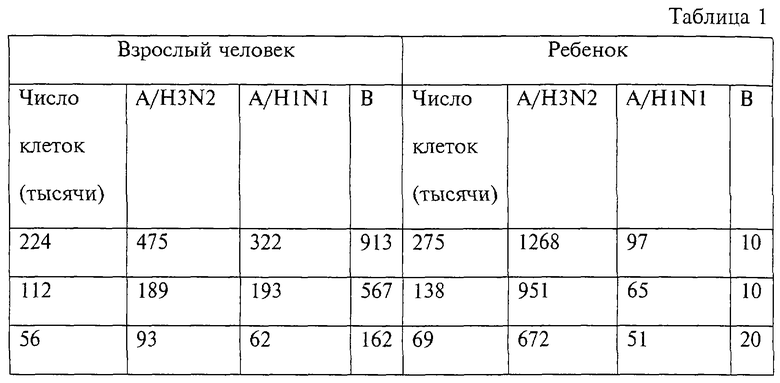
Клетки: гепаринизированная кровь, взятая через 6 дней после вакцинации у взрослого (мужчина 24 лет) и ребенка (мальчик 3 лет), получивших инактивированную субъединицу вакцины гриппа. Лимфоциты отделяли, как описано в примерах 1 и 2. Клетки подвергали контакту с твердой фазой, несущей антиген H3N2, H1N1 и В, как описано в примерах 1 и 2, в течение 3 часов при 37oС, и тест осуществляли, как описано (в этом эксперименте стоп-раствор или контрольный антиген не использовались).
В табл.1 представлены результаты для двух людей, где показания для каждого антигена означают среднюю величину для трех дубликатов лунок и выражены в виде оптической плотности х1000.
Результаты показывают, что маленький ребенок, имевший только один более ранний случай гриппа, A/H3N2-инфекция, дает очень сильный иммунный ответ на A/H3N2-компонент в трехкомпонентной вакцине. Как ожидалось для этого ребенка, не было ответа на A/H1N1 и В-компоненты. Такие маленькие дети обычно требуют 2 дозы вакцины с интервалом в несколько недель, чтобы дать удовлетворительный иммунный ответ. Около 70 000 лимфоцитов, соответствующих примерно 70 мкл объему полной крови, было достаточно, чтобы получить определенный положительный результат. Для взрослого человека, имевшего множество случаев заболевания гриппом, реакция была незначительной, но тем не менее достаточной на все три компоненты вакцины, хотя и в различной степени. Для В-компонента потребовалось примерно 100 000 лимфоцитов для получения положительного ответа, в то время как два А-компонента потребовали минимально 100 000 клеток, предпочтительно 200 000 клеток.
Пример 4. Обнаружение вируса простого герпеса типа 2 классическим методом и методом Plasmacute-анализа
Общая методика
Культивирование ткани и серологические анализы
Материал от гениталий пяти человек, имеющих симптомы предполагаемого заражения генитальным вирусом герпеса, был подвергнут стандартной процедуре выращивания тканей в попытке обнаружить реплицирующийся вирус в образцах (выполнено в вирусной лаборатории больницы университета Хаукеланд, Берген). В той же лаборатории были проведены обычные серологические анализы образцов плазмы с использованием коммерческих наборов для ELISA-анализа (Behringer Enzygnost от Behringer, Germany), содержащее антигены HSV для детекции иммуноглобулина IgG и иммуноглобулина IgM.
Выделение лимфоцитов
Лимфоциты выделяют с использованием Lymphoprep (Nycomed) путем центрифугирования в градиенте плотности гепаринизированной крови от пяти человек с симптомами предполагаемого генитального инфицирования вирусом герпеса, взятой одновременно с больничными образцами. Клетки промывают трижды в PBS и ресуспендируют в культуральной среде DMEM, содержащей 20% FCS, 1 мМ L-глутамина, 50 МЕ/мл пенициллина и 50 мкг/мл стрептомицина (DMEM/FCS). Жизнеспособные клетки подсчитывают исключением по трипановому синему (0.2%).
Plasmacute-анализ ELISA с использованием антител IgM и IgG против HSV от Берингер Энзигност (Beringer Enzygnost).
Анти-HSV IgM и IgG Берингер Энзигност поставляют в виде полосок, содержащих 8 лунок, сенсибилизированных антигеном, полученным от перманентных клеток почки обезьян, зараженных герпесом, и 8 лунок, сенсибилизированных контрольным антигеном от неинфицированных клеток. Полоски блокируют 200 мкл/лунку DMEM/FCS при 37oС в 5% СО2 в течение 1 часа. Затем добавляют 100 мкл/лунку подходящего разведения лимфоцитов и инкубируют в течение 3 часов при 37oС в 5% СО2. Все последующие процедуры проводят в соответствии с инструкциями поставщика наборов. Планшеты проявляют, используя конъюгаты, реагенты и буферы, поставляемые тем же поставщиком. Субстрат, тетраметилбензидин гидрохлорид (ТМВ), требуемый для регистрации оптической плотности (ОП) при 450 нМ, используя стандартный планшет-ридер Titertek Multiscan MCC/340 (Flow Laboratories).
Plasmacute-анализ с использованием иммуноглобулина IgG против HSV-2 Bioelisa.
Твердофазный иммуноферментный анализ (ELISA) (BIOKIT, Испания) с использованием IgG против HSV-2 Bioelisa поставляется в виде полосок, содержащих 8 лунок, которые сенсибилизированы инактивированным HSV-2 антигеном. Полоски блокируют 200 мкл/лунку DMEM/FCS при 37oС в 5%-ном СО2 в течение 1 часа. Затем добавляют 100 мкл на лунку подходящего разведения лимфоцитов и инкубируют в течение 3 часов при 37oС в 5% СО2. Все последующие процедуры осуществляют в соответствии с инструкциями поставщика наборов. Планшеты проявляют, используя конъюгаты, реагенты и буферы, поставляемые тем же поставщиком. Субстрат, гидрохлорид тетраметилбензидина (ТМВ), требуемый для прочтения ОП при 450 нМ, используя доступный планшет-ридер Titertek Multiscan MCC/340 (Flow Laboratories).
Plasmacute-анализ с использованием анти-HSV IgM Bioelisa (анализ методом иммунозахвата)
Анти-HSV IgM-анализ Bioelisa (методом иммунозахвата) (BIOKIT, Испания) поставляется в виде полосок, содержащих 8 лунок, сенсибилизированных кроличьими антителами против иммуноглобулинов IgM человека. Полоски блокируют 200 мкл/лунку DMEM/FCS при 37oС в 5%-ном СО2 в течение 1 часа. Затем добавляют 100 мл на лунку лимфоцитов подходящего разведения и инкубируют в течение 3 часов при 37oС в 5%-ном СО2. Все процедуры были выполнены согласно инструкциям производителя. Конкретно, связанное антитело обнаруживают с помощью 100 мл/лунку HSV антигена, меченного пероксидазой хрена (очищенного и инактивированного HSV, который был получен в процессе размножения in vitro в человеческих фибропластах) и для минимизации неспецифических реакций немеченного контрольного антигена, состоящего из неинфицированных клеточных компонентов (поставляемых в наборе) 10 мкл HSV антигена и 10 мкл контрольного антигена на полоску. Планшеты считывали в Titertek Multiskan MCC/340 при 450 нМ (Flow Laboratories).
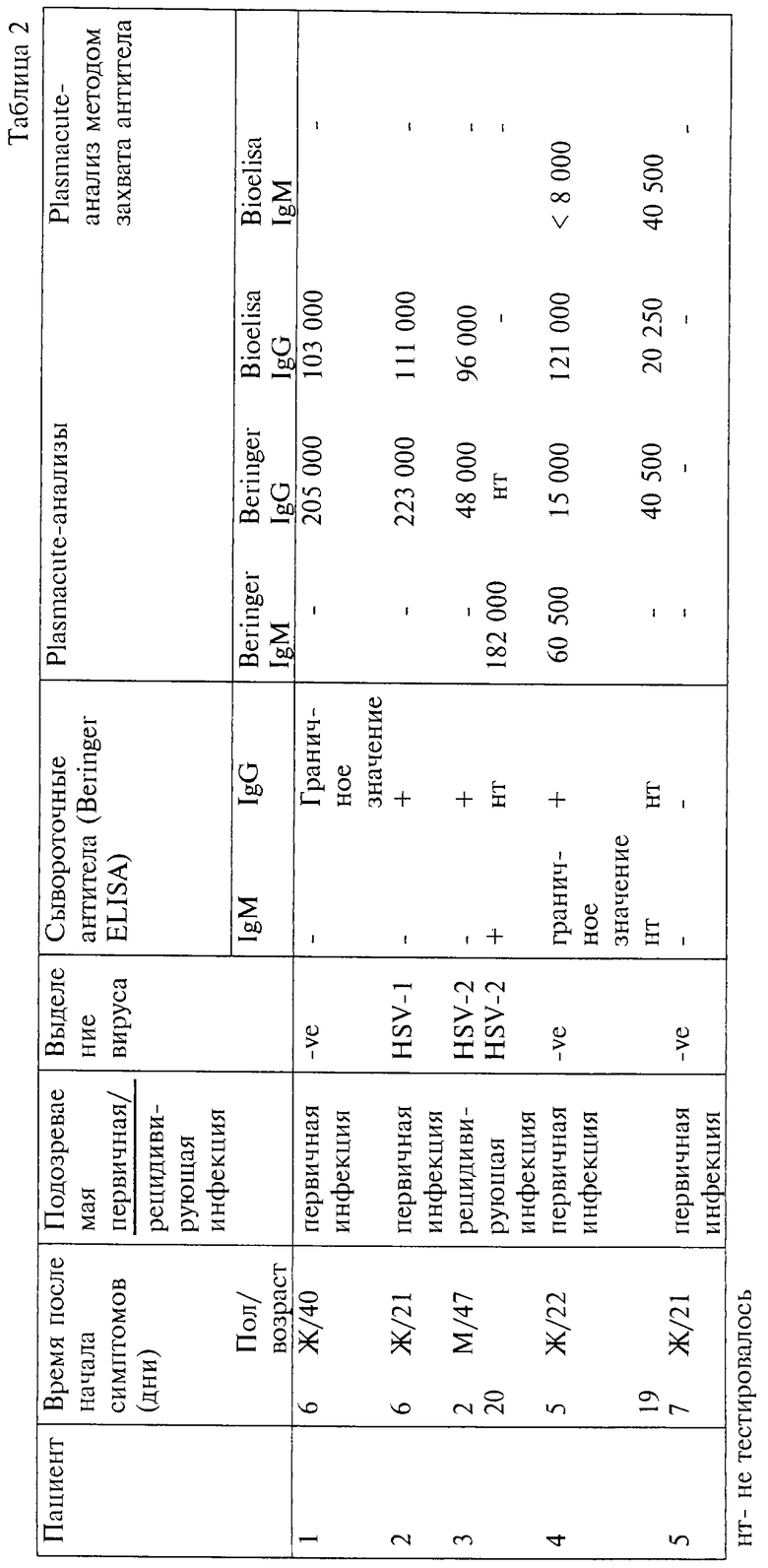
Результаты эксперимента показаны в табл.2.
В табл.2 систематизированы данные для пациентов 1-5. Диагностическая лаборатория в больнице университета Хаукеланд попыталась выделить вирус из клинических образцов и также выполнила обычные ELISA-тесты на сыворотки IgG и IgM, используя ELISA-наборы Beringer Enzygnost. Тип выделенного вируса установлен, -ve означает отрицательное выделение. Предельные величины ELISA для сыворотки определены производителем набора; + = ОП>0.2, граничное значение ОП=0.1-0.2, определенная производителями как ненадежный результат анализа; и -- = ОП<0.1.
Для Plasmacute-анализа мы использовали ОП>0.2 как положительный результат и табулировали число лимфоцитов, необходимое для получения такого ответа.
Только IgG-тест Bioelisa идентифицирует антитела к HSV2, в то время как другие указывают на заражение герпесом (HSV 1 и/или 2).
Результаты
Пациент 1 имел клинические симптомы первичного инфицирования HSV-2. Больничные тесты не смогли выделить вирус из клинического образца и IgM не был обнаружен стандартными тестами ELISA. В подтверждение этих результатов не было обнаружено клеток, продуцирующих антитело IgM в плазматическом анализе. Анализы IgG-Behringer и IgG-Bioelisa обнаруживали клетки, продуцирующие антитело IgG против HSV. Для получения предельного поглощения в анализе Behringer потребовалось 205 000 лимфоцитов, а в анализе IgG Bioelisa для получения предельного поглощения потребовалось 103 000 лимфоцитов.
Пациент 2 подвергался первичному инфицированию, что было подтверждено выделением вируса HSV тип-1. Сывороточный IgM не был определен больничной лабораторией, но было обнаружено антитело IgG. В Plasmacute-анализе не были выявлены клетки, продуцирующие IgM, однако как анализ Behringer, так и анализ Bioelisa обнаруживали IgG-продуцирующие клетки, для чего потребовалось 223 000 и 111 000 клеток, соответственно.
Пациент 3 имел рецидивирующую HSV-2 инфекцию, подтвержденную выделением вируса HSV-2 из клинических образцов. IgG присутствовал в образце сыворотки, взятой через 2 дня после появления клинических симптомов, однако при этом не был обнаружен сывороточный IgM. В Plasmacute-анализе IgM не был определен через два дня после появления клинических симптомов, однако анализы как Behringer, так и Bioelisa обнаружили IgG-продуцирующие клетки (потребовалось 48 000 - 96 000 клеток). Антитела IgM в сыворотке были определены в больнице в образце сыворотке, взятой через 20 дней после появления клинических симптомов. 182 000 клеток потребовалось для получения предельного поглощения в Plasmacute-анализе IgM-Behringer, однако клетки не были обнаружены плазматическим анализом IgM-Bioelisa.
Пациент 4 имел первичную HSV-инфекцию. Вирус не был обнаружен в клиническом образце, посланном в больничную лабораторию. Были обнаружены пограничные уровни сывороточных антител IgM и положительные уровни сывороточных антител IgG. Антитела IgM и IgG были обнаружены в Plasmacute-анализе с использованием наборов Behringer и Bioelisa в образцах крови, взятой на 5-й и 19-й (IgM-Behringer не определяли) день после появления клинических симптомов. В Plasmacute-анализе меньше чем 8 000 клеток потребовалось для IgM-анализа Bioelisa и 60 500 клеток потребовалось для IgM-анализа Behringer, каждый из которых потребовал менее 100 мкл гепаринизированной крови.
У пациента 5 подозревали первичное инфицирование вирусом герпеса (HSV). Однако вирус не был выделен в лаборатории и сывороточные антитела не были обнаружены. В Plasmacute-анализе не были определены клетки, продуцирующие или IgG, или IgM антитело против HSV.
Обсуждение
Plasmacute-анализ показал, что он работает как в случае первичной, так и при рецидивирующей инфекции вируса герпеса. Во всех случаях плазматический анализ выполнялся по крайней мере равно хорошо, как традиционные ELISA-методики, использованные здесь. В частности, для пациента 1, хотя и не было выделено вируса из клинического образца и отмечалась только положительная граница (т. е. неубедительная) в стандартном анализе больницы, Plasmacute-анализ (Bioelisa IgG и Behringer IgG) показал, что примерно 100 000 клеток и 200 000 клеток, соответственно, дали недвусмысленный положительный результат. Возможно, что этот пациент имел двойную инфекцию (HSV1 и HSV2), из которой в месте выделения вируса был выделен только HSV1. Однако нельзя исключить, что положительный HSV2 результат (Bioelisa IgG) был вызван серологической перекрестной реакцией. Для двух образцов, взятых в различные периоды времени от пациента 4, для которого вирус не был выделен, Plasmacute-анализ показал сдвиг числа герпесспецифических IgM и IgG продуцирующих лимфоцитов от ранней фазы к более поздней фазе заражения, что согласуется с хорошо известной динамикой после первичного инфицирования, и ясно подтверждает активный иммунный ответ. IgM-тест Bioelisa был особенно чувствительным, при этом для получения положительного сигнала в первом из двух образцов потребовалось менее чем 8 000 лимфоцитов.
В этом примере мы показали, что плазматический метод работает в клинических случаях вирусных инфекций у людей.
Эксперимент 5. Множественные диски - Покрытие нитроцеллюлозных дисков иммобилизованными антителами, направленными против антител IgG, IgA и IgM
Этот эксперимент был осуществлен для того, чтобы установить, может ли быть использована система из множества дисков в плазматическом анализе для определения антител различной специфичности.
Общая методика
Гепаринизированные образцы цельной крови были отобраны у двух здоровых взрослых людей. Так как у этих людей отсутствовала какая-либо инфекция в острой фазе, мы поставили цель проанализировать спонтанное выделение антител IgG, IgM и IgA независимо от их (неизвестной) антигенной специфичности.
Субъект 1 был приглашен участвовать в эксперименте для того, чтобы установить, может ли быть использована система, имеющая диски с 3 различными антигенами, в одной лунке в Plasmacute-анализе. Одна лунка ( 1).
Субъект 2 был приглашен участвовать в эксперименте для того, чтобы установить, будет ли ослабляться сигнал в присутствии ряда дисков, покрытых тем же антигеном. Три отдельные лунки в Plasmacute-анализе (лунки 2, 3 и 4).
Выделение лимфоцитов
Лимфоциты были выделены с использованием Lymphoprep (Nycomed) путем центрифугирования в градиенте плотности гепаринизированной крови. Клетки промывали трижды в PBS и ресуспендировали в культуральной среде DMEM, содержащей 20% FCS, 1 мМ L-глутамина, 50 МЕ/мл пенициллина и 50 мкг/мл стрептомицина (DMEM/FCS). Жизнеспособные клетки подсчитывались исключением по трипану голубому (0.2%).
Plasmacute-анализ с использованием дисков в качестве твердой фазы
Смешанные эфиры целлюлозных дисков с размером пор 8 мкМ (Millipore SCWP 013 00) покрывали 10 мкг/мл козьих антител, направленных против определенных классов иммуноглобулинов человека (Sigma, aнти-IgG I-3382; анти-IgA I-0884; анти-IgM I-0759), разведенных в PBS азиде (0.001%), в течение ночи при комнатной температуре. Диски блокировали DMEM/FCS при 37oС в 5% СО2 в течение 1 часа. Были добавлены лимфоциты через 12-мм чистый передающий резервуар с размером пор 0.4 мкM (Costar 3460), и чашки помещали вниз и инкубировали в течение 3 часов при 37oС в 5% СО2. Отдельные диски переносили в отдельные лунки 24-луночного планшета (Costar) и три раза промывали PBS и три раза PBS Tween (0.05%). Связанное антитело детектировали с использованием 200 мкл/лунку козьих антител, направленных против определенных классов иммуноглобулинов человека (Sigma IgG A-6029, IgA A-4165, IgM A-4290), и конъюгированных с пероксидазой хрена, которые разводили в DMEM/FCS и инкубировали в течение 2 часов при комнатной температуре. Диски промывали для удаления несвязанных антител, как описано ранее, и проявляли, используя 200 мкл/лунку о-фенилендиамина дигидрохлорида (OPD) (Sigma P-7288) в 0.05 М фосфат-нитратном буфере (рН 5.0). Через 30 минут после добавления субстрата проявление прекращали с использованием 100 мкл/лунку 1М H2SO4. 100 мкл на лунку было перенесено в 96-луночный ELISA-планшет (Greiner EIA чашки 655001 F-формы) и считывали ОП в планшет-ридере Titertek Multiskan MCC/340 при 492 нМ (Flow Laboratories).
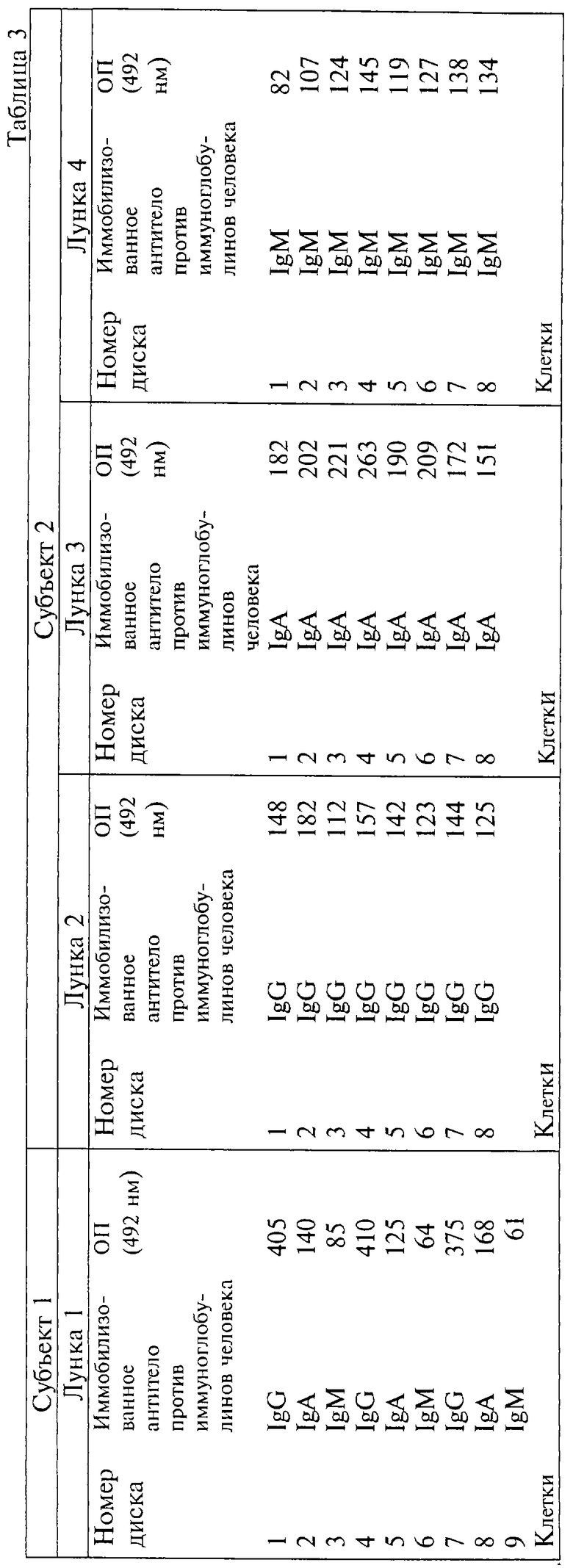
Результаты эксперимента показаны в табл.3, в которой показание для каждого захваченного антитела означает средние значения для лунок в 3-х дубликатах и выражены в виде оптической плотности х1000.
Лунка 1 содержала 2 миллиона лимфоцитов, лунки 2-4 содержали 1 миллион лимфоцитов. Ссылка "клетки" приводится для индикации, какой номер диска был расположен наиболее близко к клеточному слою.
Результаты
Тест с участием индивидуума 1 показал, что даже 9 дисков легко могут быть использованы в лунке, содержащей лимфоциты. Реакция для трех IgG-дисков, трех IgA-дисков и трех IgA-дисков для всех практических целей была идентична для каждой серии, что свидетельствует о том, что действительное положение диска относительно антитело-секретирующих лимфоцитов не имеет решающего значения. Тест с лимфоцитами от индивидуума 2 показал, что по меньшей мере 8 идентично покрытых дисков могут быть помещены в одну лимфоцитосодержащую лунку, чтобы дать фактически одинаковые показания. Таким образом, настоящее изобретение позволяет проводить множество анализов для одного и того же лимфоцитного препарата в одной лунке.


Изобретение относится к иммунологии и может быть использовано для определения иммунного статуса организма. Способ определения наличия иммунного ответа основывается на оценке активного продуцирования антител в образце крови. Способ включает контактирование в присутствии и в отсутствие ингибитора синтеза белка аликвоты указанного образца с твердой фазой в условиях, которые способствуют продуцированию антител и их выделению лимфоцитами, определение в растворе связывания антитела с указанным(и) антигеном(ами) на твердой фазе и сравнение указанного связывания антитела в присутствии или в отсутствие ингибитора синтеза белка в целях определения количества активного продуцирования антител в ответ на указанный антиген(ы). Способ также модифицирован для оценки активного продуцирования неспецифических индикаторов инфекции в ответ на инфекционный антиген-мишень. Изобретение позволяет упростить определение за счет использования микролитровых объемов крови, что важно при работе с новорожденными. 2 с. и 15 з.п. ф-лы, 5 табл.
| Устройство для контроля блоков памяти | 1974 |
|
SU526952A1 |
| US A 5188942, 23.02.1993. | |||
Авторы
Даты
2003-01-27—Публикация
1996-02-21—Подача