Изобретение относится к сильнодействующим факторам активации макрофагов, полученным путем олигосахаридного расщепления клонированного белка, связывающего витамин D (Gc-белка), и клонированного домена III Gc-белка, и к применению указанных факторов активации макрофагов в случае различных раковых заболеваний, ВИЧ-инфекции и остеопороза, и в качестве адъюванта в случае иммунизации и вакцинации, а также к разработке способов диагностики и прогнозирования с использованием специфического фермента α-N-ацетилгалактозаминидазы, обнаруженного в кровотоке раковых и ВИЧ-инфицированных больных.
Таблица терминов
Gc-белок - белок, связывающий витамин D3
MAF - фактор активации макрофагов
GcMAF - полученный из Gc-белка фактор активации макрофагов
GcMAFc - полученный из клонированного Gc-белка фактор активации макрофагов домен III Gc - область домена III Gc-белка
CdMAF - полученный из клонированного домена III фактор активации макрофагов
NagAg - α-N-ацетилгалактозаминидаза в качестве антигена
Краткое изложение сущности изобретения
Белок, связывающий витамин D (Gc-белок) и его малый домен (пептид длиной приблизительно 18% длины Gc, известный также как домен III), клонируют с помощью вектора на основе бакуловируса. Клонированный Gc-белок и клонированный доменный (Cd) пептид обрабатывают иммобилизованной β-галактозидазой и сиалидазой и получают факторы активации макрофагов GcMAF и CdMAF соответственно. Эти клонированные факторы активации макрофагов и GcMAF можно применять при лечении рака, ВИЧ-инфекции и остеопороза, и также можно применять в качестве адъюванта при иммунизации и вакцинации. Разработаны способы и набор для ELISA с использованием иммуносэндвича для обнаружения присутствия в сыворотке или плазме α-N-ацетилгалактозаминидазы у раковых и ВИЧ-инфицированных пациентов и использованы в качестве диагностических и прогностических показателей.
Описание чертежей
Другие цели и многие сопутствующие особенности настоящего изобретения можно будет легко оценить и понять, обратившись к приведенному далее подробному описанию в сочетании с прилагаемыми чертежами, описанными ниже.
Фиг.1А является схематической иллюстрацией образования фактора активации макрофагов (MAF).
Фиг.1Б является схематической иллюстрацией дегликозилирования Gc-белка в кровотоке ракового или ВИЧ-инфицированного пациента.
На фиг.2 показана аминокислотная последовательность клонированного GcMAF, которая является последовательностью No 1 (SEQ ID No: 1), представляющей собой полный клонированный белок Gc.
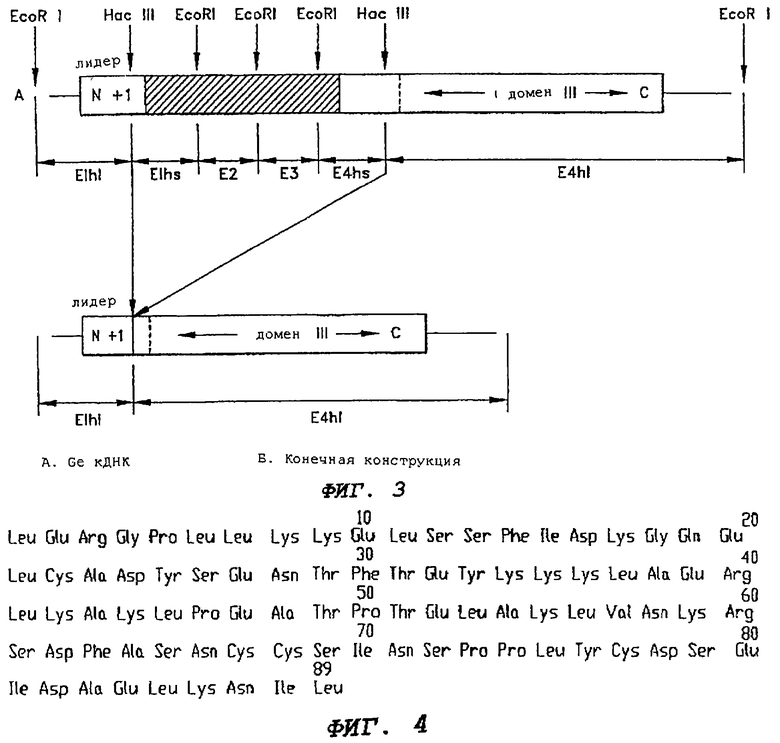
На фиг.3 показано конструирование ДНК-фрагмента, кодирующего лидерную последовательность, EcoRI фрагмент E1, и области домена III Gc-белка; А - полная кДНК для Gc-белка;
Б - конструкция, которую вставляют в негибридный вектор;
заштрихованный участок показывает сжатую область в 1000 пар оснований (п.о.).
На фиг.4 показана последовательность 89 аминокислот, послед. No 2 (SEQ ID No: 2), клонированного домена III (CdMAF1), при использовании негибридного вектора.
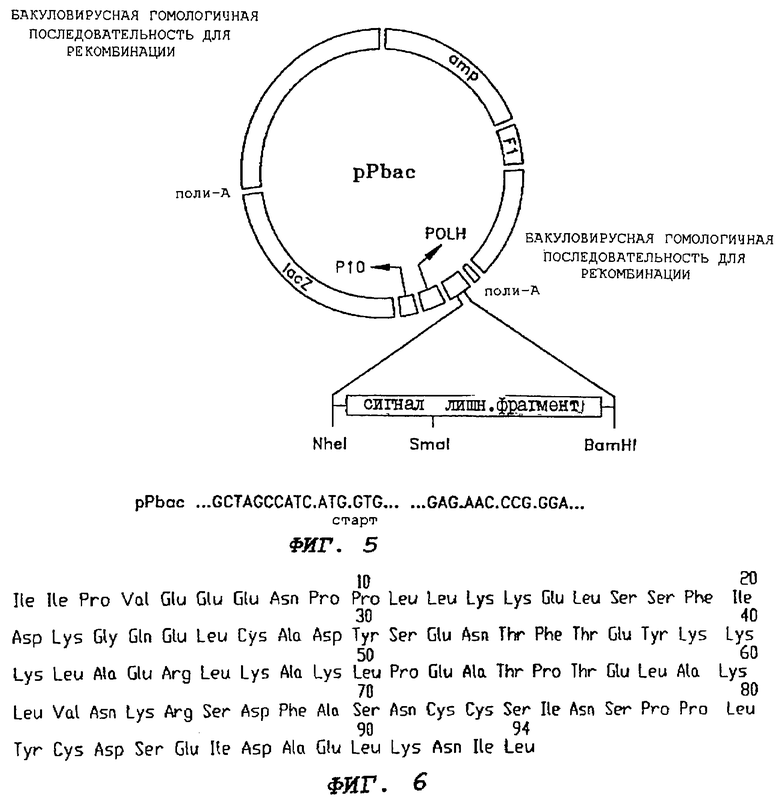
На фиг.5 показан бакуловирусный гибридный вектор для клонирования домена III Qc-белка.
На фиг.6 показана последовательность 94 аминокислот, послед. No 3 (SEQ ID No: 3), клонированного домена III (CdMAF2), при использовании гибридного вектора.
На фиг.7 приводится корреляция между активностью α-N-ацетилгалактозаминидазы плазмы и опухолевым грузом (подсчет всех клеток) в брюшной полости из асцитной опухоли Эрлиха.
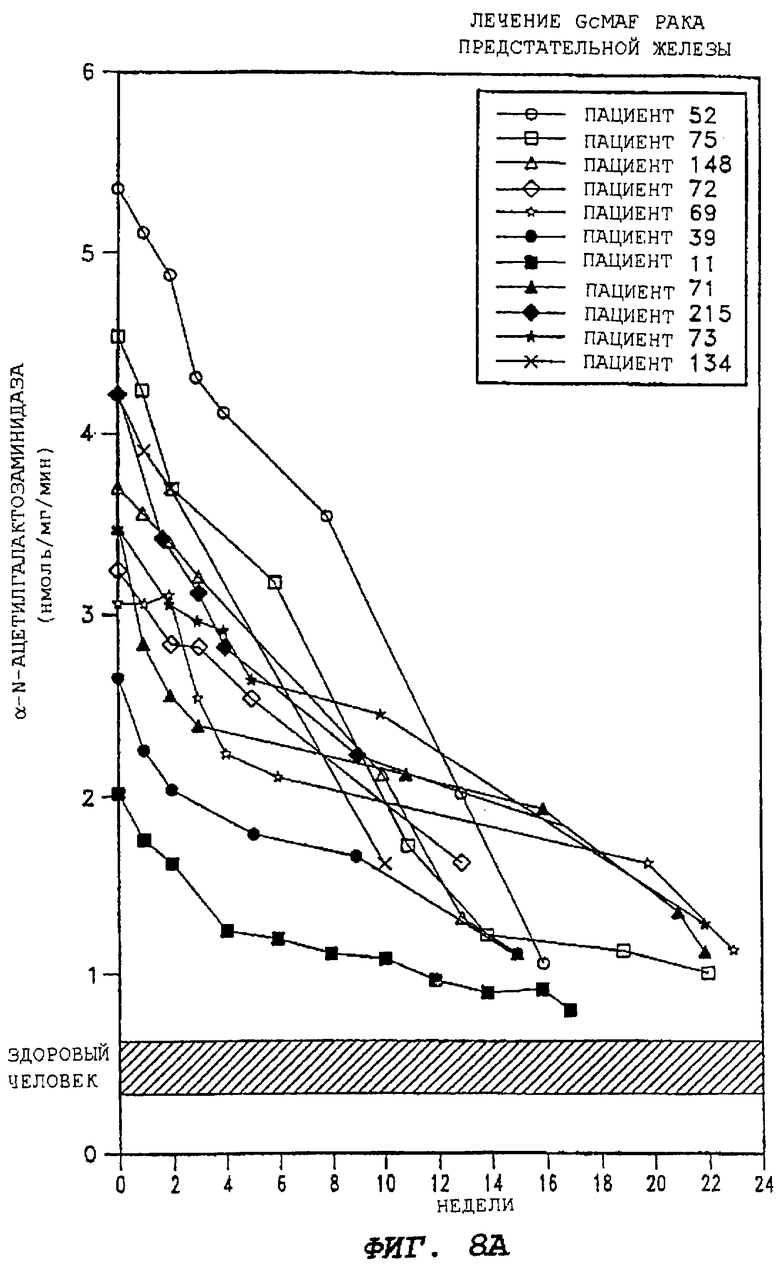
На фиг.8А показывается терапевтическое действие GcMAF согласно настоящему изобретению на взрослых людей, страдающих от рака предстательной железы.
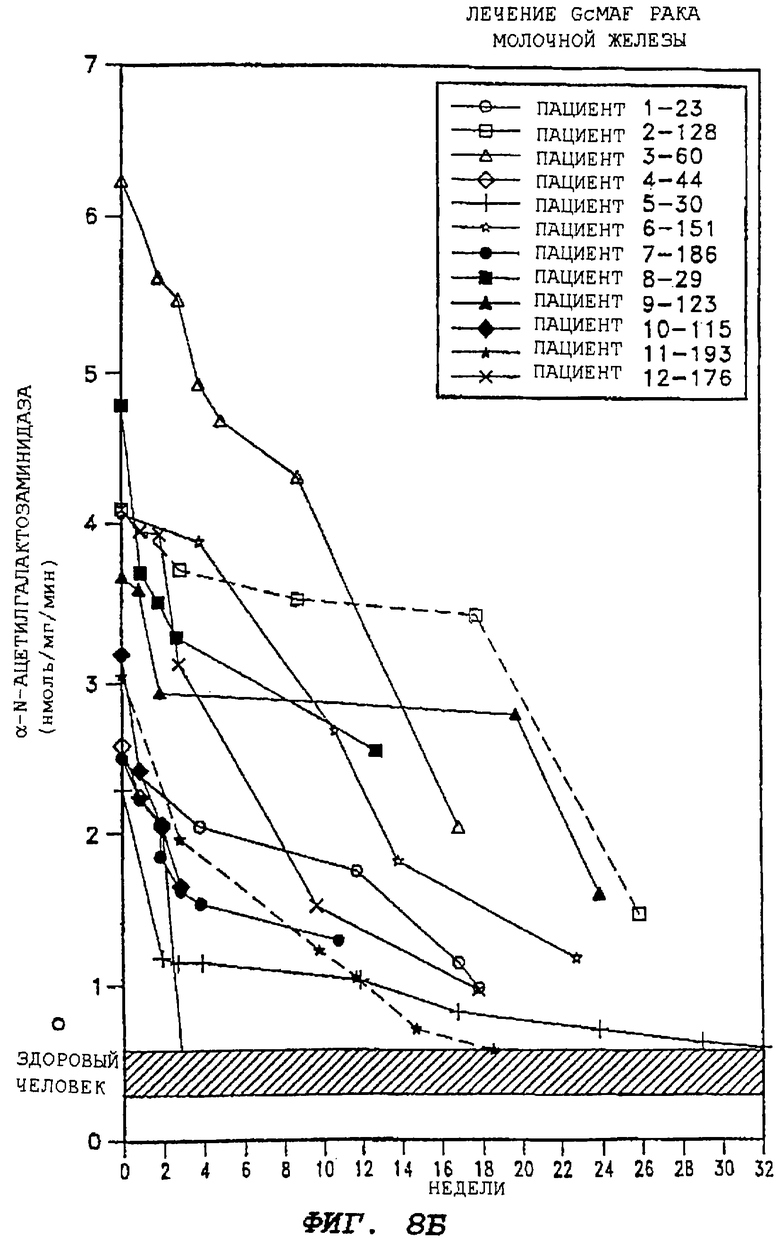
На фиг.8Б показывается терапевтическое действие GcMAF согласно настоящему изобретению на взрослых людей, страдающих от рака молочной железы.
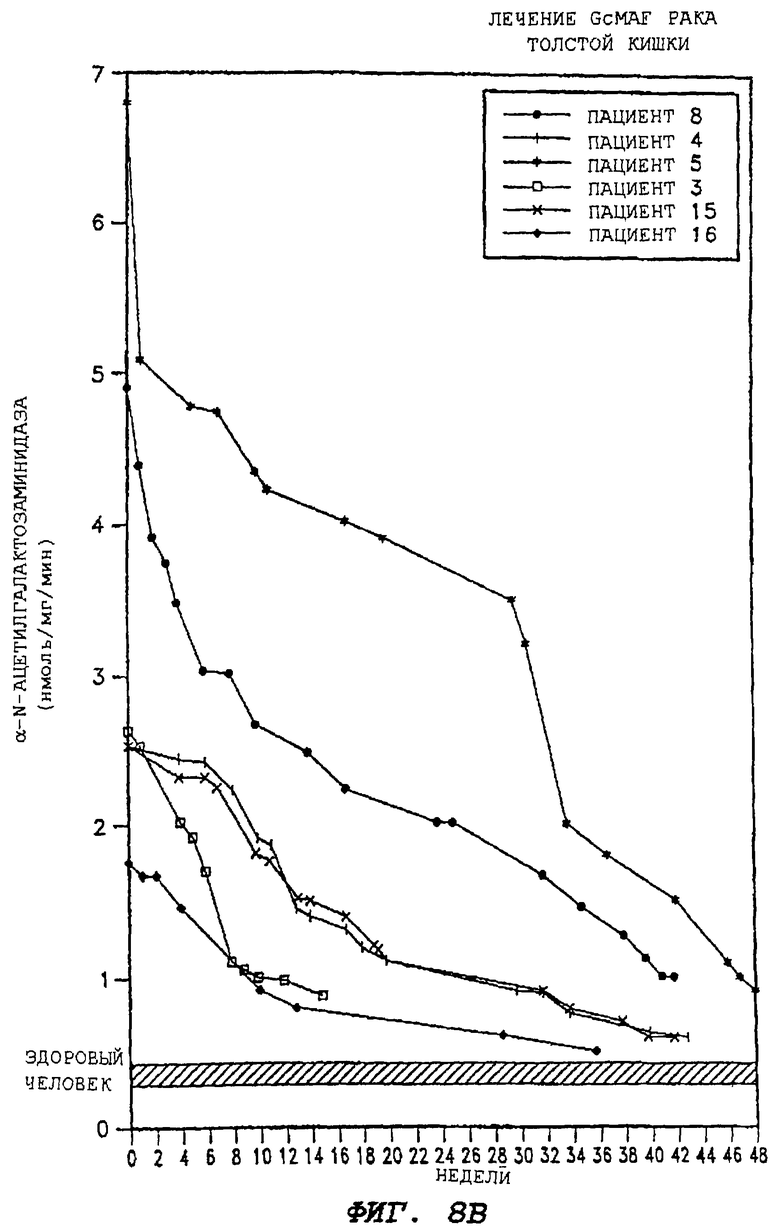
На фиг.8В показывается терапевтическое действие GcMAF по настоящему изобретению на взрослых людей, страдающих от рака толстой кишки.
Предпосылки создания изобретения
А. Воспалительная реакция приводит к активации макрофагов
Воспаление приводит к активации макрофагов. При воспалительных нарушениях выделяются лизофосфолипиды. Введение мышам небольших доз (5-20 мкг/мышь) лизофосфатидилхолина (лизо-Рс) и других лизофосфолипидов вызывает весьма повышенную фагоцитируюшую и супероксидгенерирующую способность макрофагов (Ngwenya and Yamamoto, Proc. Soc. Exp. Biol. Med., 193:118, 1990; Yamamoto et al., Inf. Imm., 61:5388, 1993; Yamamoto et al.. Inflammation, 18:311, 1994).
Такая активация макрофагов требует участия В- и Т-лимфоцитов и сывороточного белка, связывающего витамин D (DBP; человеческий DBP известен как Gc-белок). Активация in vitro мышиных перитонеальных макрофагов лизо-Рс требует постадийной модификации Gc-белка β-галактозидазой обработанных лизо-Рс В-клеток и сиалидазой Т-клеток для генерации фактора активации макрофагов (MAF) - белка с N-ацетилгалактозамином в качестве сохраняющейся группы сахара (фиг.1А) (Yamamoto et al., Proc. Natl. Acad. Sci. USA, 88:8539, 1991; Yamamoto et al., J. Immunol., 151:2794, 1993; Naraparaju and Yamamoto, Immunol. Lett., 43:143, 1994). Таким образом, Gc-белок является предшественником MAF.
Инкубация Gc-белка с иммобилизованной β-галактозидазой и сиалидазой генерирует заметно возросшие титры MAF (GcMAF) (Yamamoto et al., Proc. Natl. Acad. Sci. USA, 88:8539, 1991; Yamamoto et al., J. Immunol., 151:2794, 1993; Naraparaju and Yamamoto, Immunol. Lett., 43:143, 1994; патент США No 5177002; патент США No 5326749). Введение ничтожного количества (10 пг/мышь; 100 нг на человека) GcMAE приводит к сильному повышению фагоцитирующей и супероксидгенерирующей способностей макрофагов.
Когда моноциты/макрофаги (называемые здесь макрофагами) периферической крови 326 пациентов - носителей различных типов рака обрабатывают in vitro 100 пг GcMAF на мл, макрофаги всех раковых пациентов активируются в отношении фагоцитирующей и супероксидгенерирующей способностей макрофагов. Это наблюдение показывает, что макрофаги раковых пациентов способны активироваться. Однако активность предшественника MAF Gc-белка плазмы теряется или снижается приблизительно у 70% больных раком. Обнаружено, что потеря или снижение активности Gc-белка как предшественника происходит вследствие дегликозилирования плазменного Gc-белка и α-N-ацетилгалактозаминидазой, обнаруженной в кровотоке больных раком. Дегликозилированный Gc-белок не может превратиться в MAF (фиг.1Б). Таким образом, потеря активности Gc-белка как предшественника МАЕ предотвращает генерацию MAF. Следовательно, активация макрофагов у некоторых раковых больных развиваться не может. Так как активация макрофагов является первой стадией в развитии иммунного каскада, такие раковые больные становятся больными с подавленным иммунитетом. Этим можно объяснить по меньшей мере частично, почему раковые больные умирают от инфекции, которую не могут преодолеть.
Подобным образом, когда макрофаги периферической крови 196 ВИЧ-инфицированных или больных СПИДом обрабатывают in vitro 100 пг GcMAF на мл, макрофаги у всех больных активируются в отношении фагоцитирующей и супероксидгенерирующей способностей. Однако активность Gc-белка плазмы как предшественника MAF снижается приблизительно у 35% ВИЧ-инфицированных пациентов. Как и у больных раком, у этих больных плазменный Gc-белок дегликозилируется α-N-ацетилгалактозаминидазой, обнаруженной в кровотоке ВИЧ-инфицированных больных. Этот механизм объясняет, почему ВИЧ-инфицированные больные (больные СПИДом) находятся в тяжелом иммунодепрессивном состоянии.
Как раковые, так и ВИЧ-инфицированные больные, у которых резко понижена активность Gc-белка как предшественника, имеют большое количество α-N-ацетилгалактозаминидазы, в то время как больные с умеренной активностью предшественника имеют средний уровень активности плазменной α-N-ацетилгалактозаминидазы. Пациенты с высокой активностью предшественника, включая бессимптомных ВИЧ-инфицированных пациентов, имеют низкий, но существенный уровень активности плазменной α-N-ацетилгалактозаминидазы. Так как в кровотоке присутствует большое количество Gc-белка (260 мкг/мл), низкое содержание фермента не влияет на активность предшественника. Однако активность α-N-ацетилгалактозаминидазы обнаруживается в плазме всех раковых и ВИЧ-инфицированных больных, и она обратно пропорциональна активности их плазменного Gc-белка как предшественника. Таким образом, увеличение у пациента сывороточной или плазменной активности α-N-ацетилгалактозаминидазы ответственно за снижение активности предшественника Gc-белка плазмы. Эти наблюдения привели автора к предположению, что сывороточная или плазменная α-N-ацетилгалактозаминидаза играет некую роль в подавлении иммунитета у раковых и ВИЧ-инфицированных больных (больных СПИДом). Таким образом, активность сывороточной или плазменной α-N-ацетилгалактозаминидазы у больных может служить в качестве диагностического и прогностического показателя.
Б. Дефект в каскаде активации макрофагов служит доказательством остеопороза
Оказывается, что процесс активации макрофагов, который вызывается воспалением, является главным каскадом активации макрофагов, в котором участвуют другие фагоциты, такие как остеокласты и моноциты. Отсутствие индуцибельной β-галактозидазы В-лимфоцитов в каскаде активации макрофагов является причиной дисфункции остеокластов, что ведет к проявлению остеопороза (Yamamoto et al., J. Immunol., 152:5100, 1994), недостаточности или задержке формирования костного мозга у новорожденных.
Аутосомальный рецессивный остеопороз характеризуется избыточным накоплением костной массы в скелете в результате дисфункции остеокластов, приводящей к снижению костной резорбции (Marks, Clin. Orthop., 189:239, 1984). У животных моделей остеопороза в зависимости от степени дисфункции остеокластов развитие полости костного мозга и прорезывание зубов либо задерживается, либо, чаще, отсутствует (Marks, Am. J. Med. Genet., 34:43, 1989). При младенческом остеопорозе человека при непреодолеваемой инфекции обычно в пределах первой декады жизни наступает смерть (Reeves, Pediatrics, 64:202, 1979), что указывает на иммунодепрессию. Накопленные факты позволяют предположить, что недостаточность или дисфункция остеокластов при остеопетрозе млекопитающих, включая человека, часто сопровождаются недостаточностью или дисфункцией макрофагов. Исследования автора настоящего изобретения по активации как остеокластов, так и макрофагов при изменениях при врожденном системном остеопетрозе показали, что остеокласты и макрофаги можно активировать с помощью обычного сигнализирующего фактора - фактора активации макрофагов, и что недостаток β-галактозидазы В-клеток сводит на нет процесс генерации фактора активации макрофагов (Yamamoto et al., J. Immunol., 152:5100, 1994). Так как GcMAF и его клонированные производные обходят функции лимфоцитов и Gc-белка и действуют непосредственно на макрофаги и остеокласты, введение этих факторов носителям остеопетроза должно исправлять костные нарушения. Действительно, автор настоящего изобретения недавно обнаружил, что четыре введения GcMAF или клонированного фактора активации макрофагов (GcMAFc) (100 пг в неделю) ор-мутантным мышам, в первые четыре недели, начиная с рождения, приводят к активации как макрофагов, так и остеокластов, и к последующей резорбции избытка скелетной основы и возрастанию размера полости костного мозга.
В. Терапевтическое применение GcMAF и его клонированных производных при раке
Несмотря на дефекты в каскаде активации макрофагов у раковых, ВИЧ-инфицированных больных и больных остеопетрозом, GcMAF обходит функции лимфоцитов и Gc-белка и действует непосредственно на макрофаги (или остеокласты) в отношении активации. Макрофаги, когда они активированы, обладают потенциалом для ликвидации раковых клеток и ВИЧ-инфицированных клеток. Когда раковых больных лечат 100 нг GcMAF на пациента в неделю в течение нескольких месяцев, GcMAF показывает заметное лечебное действие при многих, без различия, видах рака человека.
Вместо того, чтобы получать GcMAF из человеческой крови как источника, его можно получать из клонированного Gc-белка или его малого домена, ответственного за активацию макрофагов. Клонированный Gc-белок требует эукариотного вектора/хозяина, способного гликозилироватъ клонированные продукты. Gc-белок с молекулярной массой приблизительно 52000 (и с 458 аминокислотными остатками) является многофункциональным белком и несет три разных домена (Cooke and Haddad, Endocrine Rev., 10:294, 1989).
Домен I взаимодействует с витамином D, в то время как домен III взаимодействует с актином (Hadded et al., Biochem., 31:7174, 1992). Химически и протеолитически фрагментированный Gc-белок дает возможность показать, что наименьший домен - домен III содержит 80 аминокислотных остатков, включая сайт гликозилирования, необходимый пептид для активации макрофагов. Соответственно автор клонирует как Gc-белок, так и весь пептид домена III, используя вектор на основе бакуловируса и насекомое-хозяина, и обрабатывает их иммобилизованной λ-галактозидазой и сиалидазой, и получает мощные факторы активации макрофагов, названные GcMAFc и CdMAF соответственно. Как и в случае GcMAF, оказывается, что указанные клонированные GcMAFc и CdMAF обладают заметным лечебным действием при различных раковых заболеваниях.
Г. Сильная адъювантная активность GcMAF при иммунизации антигенами или вакцинами
Макрофаги являются антигенпредставляющими клетками. Макрофаги, активированные GcMAF, быстро фагоцитируют антиген-мишени или клетки и представляют процессированные антигены антитело-продуцирующим клеткам. Автор наблюдал быстрое развитие большого количества секретирующих антитела клеток сразу же (1-4 суток) после инокуляции небольшого количества GcMAF (100 пг на мышь) и овечьих эритроцитов (SRBC). Это открытие показывает, что GcMAF и его клонированные производные GcMAFc и CdMAF должны служить в качестве сильных адъювантов при иммунизации и вакцинации.
Описание способов генного клонирования факторов активации макрофагов
А. Клонирование кДНК Gc-белка в вирус насекомого
Из библиотеки кДНК печени человека в бактериофаге β-gtll (Clontech, Palo Alto, CA) выделяют кДНК полной длины, кодирующую человеческий Gc-белок, используя набор для иммунного скрининга pico BlueТМ, доступный от Stratagene, La Jolla, CA. Бакуловирусная экспрессирующая система в клетках насекомого имеет ряд преимуществ полиэдронного белка: (а) он экспрессируется на очень высоком уровне в инфицированных клетках, где он составляет более половины общего клеточного белка в позднем инфекционном цикле; (б) он несущественен для инфекции или репликации вируса, что означает, что рекомбинантный вирус не требует хелперной функции; (в) вирусы, не имеющие гена полиэдрона, имеют морфологию бляшек, отличную от вирусов, содержащих клонированный ген; и (г) в отличие от бактериальных клеток клетка насекомого эффективно гликозилирует клонированные генные продукты.
Одним из достоинств указанной экспрессирующей системы является визуальный скрининг, позволяющий различать и подсчитывать рекомбинантные вирусы. Полиэдронный белок продуцируется в очень большом количестве в ядрах инфицированных клеток в позднем вирусном инфекционном цикле. Аккумулированный полиэдронный белок образует тела окклюзии, которые также содержат включенные вирусные частицы. Эти тела окклюзии размером до 15 мкм являются сильно преломляющими, что придает им яркий блеск, который легко визуализуется в оптическом микроскопе. Клетки, инфицированные рекомбинантными вирусами, не имеют тел окклюзии. Чтобы отличить рекомбинантный вирус от вируса дикого типа, трансфекционный супернатант (лизат, содержащий рекомбинантный вирус) наносят на монослой клеток насекомого. Затем бляшки скринируют в оптическом микроскопе на присутствие (указывающее на вирус дикого типа) или отсутствие (указывающее на рекомбинантный вирус) тел окклюзии.
Кроме того, бакуловирусная экспрессирующая система использует хелпернезависимый вирус, который можно до высокого титра размножить в клетках насекомого, адаптированных для роста в суспензионных культурах, что делает возможным получение большого количества рекомбинантного белка с относительной легкостью. Большая часть сверхсинтезированного белка остается растворимой в клетках насекомого, в отличие от нерастворимых белков, полученных, как правило, из бактерий. Кроме того, вирусный геном большой (130 кб) и, таким образом, может разместить большие сегменты чужеродной ДНК.
1) Выбор бакуловирусного вектора
Все доступные бакуловирусные векторы основаны на pUC и обеспечивают устойчивость к ампициллину. Каждый такой вектор содержит промотор полиэдронного гена, вариабельные длины последовательности, кодирующей полиэдрон, и сайт (сайты) инсерции для клонирования чужеродного представляющего интерес гена, фланкированные вирусными последовательностями, которые располагаются 5' к промотору и 3' к чужеродной генной вставке. Эти фланкирующие последовательности облегчают гомологичную рекомбинацию между вектором и бакуловирусной ДНК дикого типа (Ausubel et al., Current Protocols in Mol. Biol., 1990). В основном, при выборе соответствующего бакуловирусного экспрессирующего вектора учитывают, экспрессирует ли он рекомбинант в виде слитого или неслитого белка. Так как гликозилирование Gc-пептида требует лидерной сигнальной последовательности для переноса пептида в эндоплазматический ретикулум, кДНК, содержащая инициирующий кодон (-16 Met) лидерной последовательности до +1 аминокислоты (leu) нативного Gc-белка, должна быть введена в негибридный вектор с полилинкером, несущим сайт EcoRI pLV1393 (Invitrogen, San Diego, CA).
Во время частичного расщепления кДНК Gc-белка в λ-gtll ферментом EcoRI кДНК Gc полной длины с концами EcoRI выделяют с помощью электрофореза, смешивают с EcoRI разрезанной pVL.1393 и лигируют Т4-лигазой. Эта конструкция при правильной ориентации должна экспрессировать полный Gc-пептид, все 458 аминокислоты (фиг.2). Чтобы получить правильную конструкцию, компетентные клетки Е. coli HB101 трансформируют pVL-вектором и отбирают трансформанты на агаровых пластинках со средой Луриа, содержащих ампициллин (СЛ/ампициллиновые пластинки). Получают ДНК для процедуры секвенирования, чтобы определить, какая колония содержит вставку или ген с должной ориентацией считывания, отыскивая сначала участок 3'-поли-А. Клоны с 3'-поли-А (из поли-А-"хвоста" мРНК) затем секвенируют от 5'-конца для подтверждения правильной ориентации ДНК полной длины для Gc-пептида.
2) Котрансфекция клеток насекомого клонированной плазмидной ДНК и вирусной ДНК дикого типа
Монослой клеток Spodoptera frugiperda (Sf9) (2,5·106 клеток на каждом матрасе в 25 см2) контрансфецируют клонированной плазмидной (векторной) ДНК (2 мкг) и ДНК бакуловируса дикого типа (AcMNPV) (10 мкг) в 950 мкл буфера для трансфекции (Ausubel et al., в Curr. Protocols in Mol. Biol., 1990). Когда клетки культивируют в течение 4 или 5 суток, трансфекционный супернатант содержит рекомбинантные вирусы.
3) Идентификация рекомбинантного бакуловируса
Котрансфекционные лизаты разводят 104, 105 или 106 и высевают на клетки Sf9 для культивирования в течение 4-6 суток. После хорошего образования бляшек идентифицируют бляшки, содержащие отрицательные на окклюзию клетки, с частотой 1,3%. Выделяют несколько предполагаемых рекомбинантных вирусных бляшек и дважды реплакируют для очистки. Выделяют чистые клоны рекомбинантных вирусных бляшек.
Б. Анализ представляющего интерес белка из рекомбинантного бакуловируса
1) Получение лизата рекомбинантного вируса
Монослой клеток насекомого Sf9 (2,5·106 клеток на матрасе 25 см2) инфицируют клоном рекомбинантного вируса и культивируют в 5 мл бессывороточной среды GIBCO (от GIBCO Biochemicals, Роквилл, Мэриленд) или среды с добавлением 0,1% яичного альбумина, чтобы избежать загрязнения сывороточным бычьим белком, связывающим витамин D. Культуральные матрасы инкубируют при 27°C и ежедневно проверяют на признаки инфекции. Через 4-5 суток клетки собирают, осторожно сдвигая их с матраса, и клетки, и культуральную среду переносят в центрифужные пробирки и центрифугируют в течение 10 мин при 1000·g при 4°C. Чтобы максимизировать инфекцию для продукции рекомбинантного белка в 100-мл вращающейся колбе для суспензионной культуры выращивают клетки Sf9 в 50 мл полной среды до 2·106 клеток/мл. Клетки собирают, центрифугируют при 1000·g в течение 10 мин и ресуспендируют в 10-20 мл бессывороточной среды, содержащей рекомбинантный вирус при множественности заражения (MOI) 10. После 1-часовой инкубации при комнатной температуре инфицированные клетки переносят в 200-мл роллерную колбу, содержащую 10 мл бессывороточной среды, и инкубируют в течение 40 ч. Более 40% секретированного белка являются белком, представляющим интерес. Выделяют белок в супернатанте.
2) Качественная оценка представляющего интерес белка
Для оценки качества экспрессированного белка используют окрашивание кумасси голубым полиакриламидного геля с ДСН, при нагрузке 20-40 мкг общего белка клеток на полосу. Поскольку образцы содержат клеточные белки, рекомбинантный белок легко обнаружить путем сравнения с белками неинфицированных клеток.
3) Ферментативное превращение клонированного Gc-белка в фактор активации макрофагов (GcMAFc)
Клонированный Gc-белок (2 мкг) с молекулярной массой 52000 и 458 аминокислотными остатками (фиг.2) выделяют с помощью колонки, аффинной к витамину D (Link et al., Anal. Biochem., 157:262, 1986), и обрабатывают иммобилизованной β-галактозидазой и сиалидазой. Полученный в результате клонированный фактор активации макрофагов (GcMAFc) добавляют к мышиным и человеческим макрофагам и анализируют на фагоцитирующую и супероксидгенерирующую способность. Инкубация макрофагов с 10 пг GcMAFc/мл в течение 3 часов приводит к 5-кратно возросшей фагоцитирующей активности и к 15-кратному возрастанию способности макрофагов генерировать супероксиды.
В. Субклонирование домена, необходимого для активации макрофагов
I. Процедура клонирования I: негибридный вектор
1) Клонирование домена, ответственного за активацию макрофагов (CdMAF)
Полную кДНК-последовательность для Gc-белка в λ-gtll, включающую 76 п.о. в обратном направлении 5' фланкирующей области и 204 п.о. 3' фланкирующего участка, фрагментируют с помощью EcoRI и получают четыре рестрикционных фрагмента, обозначаемых Е1, 120 п.о.; Е2, 314 п.о.; Е3, 482 п.о. и Е4, 748 п.о. соответственно. Каждый фрагмент клонируют в сайт EcoRI плазмиды pSP65 от Promega (Мэдисон, W1) по методу Cooke и David (J. Clin. Invest., 76:2420, 1985). Хотя автор обнаружил, что область меньше половины домена III ответственна за активацию макрофагов, малые сегменты - менее 40 аминокислотных остатков не могут быть экспрессированы в клетках насекомого. Кроме того, короткие пептиды быстро разрушаются протеазами в человеческой плазме и, таким образом, не являются клинически полезными. Соответственно полный домен III (приблизительно 80 аминокислотных остатков) следует клонировать в вирусе насекомого, где автор прогнозирует эффективное продуцирование и гликозилирование пептида в инфицированных клетках.
2) Субклонирование кДНК-фрагмента в полиэдронный ген бакуловируса
Так как гликозилирование пептида требует лидерной сигнальной последовательности для переноса пептида в эндоплазматический ретикулум, следует вставить в вектор ДНК-сегмент E1, содержащий инициирующий кодон (-16 Met) лидерной последовательности до аминокислоты +1 (Leu) нативного Gc-белка. Поскольку этот сегмент несет инициирующий кодон для Gc-белка, используют негибридный вектор pVL1393 (Invitrogen, San Diego, CA). Сегмент, содержащий инициирующий кодон - лидерную последовательность кДНК клона Е1, и сегмент кДНК, кодирующий 85 С-концевых аминокислот (полный домен III) плюс 3' некодирующий участок кДНК Е4 клона, лигируют вместе и клонируют в сайт EcoRI вектора pVL вируса насекомого. Чтобы успешно создать такую конструкцию, как Е1-, так и Е4-ДНК, фрагментируют HaeIII и получают в каждом случае два фрагмента: E1hl (87 п.о.), E1hs (33 п.о.) и E4hs (298 п.о.), E4hl (450 п.о.) соответственно. Оба более крупных фрагмента E1hl и E4hl выделяют с помощью электрофореза, смешивают с EcoRI-разрезанным pVL и лигируют Т4-лигазой, как показано на фиг.3. Эта конструкция при правильной ориентации должна экспрессировать полный домен III со всеми 89 аминокислотами, включая 4 аминокислоты E1hl, называемый здесь также CdMAF1, как показано на фиг.4. Чтобы получить правильную конструкцию, компетентные клетки Е. coil HB101 трансформируют вектором pVL и отбирают трансформанты на СЛ/ампициллиновых пластинках. Получают ДНК для процедур секвенирования, чтобы определить, какая колония содержит конструкцию с правильной ориентацией считывания, отыскивая сначала участок 3'-поли-dA. Эти клоны с 3'-поли-dA (из поли-А хвоста мРНК) затем секвенируют от 5'-конца, чтобы подтвердить правильную ориентацию фрагмента E1hl. Автор нашел, что указанный вектор содержит полную конструкцию (домен III) в правильной ориентации.
3) Выделение рекомбинантного бакуловируса, очистка клонированного доменного пептида (Cd) и ферментативная генерация клонированного фактора активации макрофагов (CdMAF)
Монослои клеток Spodoptera frugiperda (Sf9) (2,5·106 клеток на каждом матрасе в 25 см2) контрансфецируют клонированной плазмидной ДНК (2 мкг) и ДНК бакуловируса дикого типа (AcMNPV) (10 мкг) в 950 мкл буфера для трансфекции. Рекомбинантные бакуловирусные бляшки выделяют и используют для продуцирования пептида домена III Gc в клетках насекомого. Клонированный домен с молекулярной массой (Мм) 10000 и 89 аминокислотами, показанный на фиг.4, очищают с помощью актин-аффинной колонки (Haddad et al., Biochemistry, 31:7174, 1992). Обрабатывают 2 мкг пептида клонированного домена (Cd1) иммобилизованной β-галактозидазой и сиалидазой и получают клонированный фактор активации макрофагов, обозначаемый CdMAF1.
II. Процедура клонирования II: гибридный вектор
1) Клонирование домена, ответственного за активацию макрофагов (CdMAF)
Бакуловирусный гибридный вектор - вектор pPbac (Stratagene, La Jolla, CA) содержит сигнальные последовательности секреции человеческой плацентарной щелочной фосфатазы, которые направляют образующийся клонированный пептид в секреторный путь клеток, ведущий к секреции в культуральную среду. Сигнальная последовательность отщепляется сигнальной пептидазой, когда образующийся клонированный пептид направляется в русло секреторного пути клеток насекомого-хозяина, ведущего к секреции пептида клонированного домена (Cd). На фиг.5 показано, что вектор несет "лишний" (stuffer) фрагмент для генного замещения и lacZ-ген для идентификации генной инсерции.
Лишний фрагмент вектора pPbac вырезают посредством переваривания векторной ДНК рестрикционными ферментами SmaI и BamHI и удаляют с помощью электроэлюции. Фрагмент кДНК Е4 Gc-белка переваривают HaeIII и BamHI, получая фрагмент, практически такой же, как E4hl (см. фиг.3). Этот фрагмент смешивают с указанным выше вектором pPbac и лигируют Т4-лигазой. Такая стратегия не только фиксирует ориентацию лигирования, но также соединяет фрагмент в рамке считывания. Реакционной смесью трансформируют клетки Е. coli DH5aF. Клонированную ДНК-вставку выделяют из ряда колоний после переваривания HaeIII и BamHl. Вставку подтверждают путем секвенирования. Последовательность подтверждает правильную ориентацию.
2) Выделение рекомбинантного бакуловируса путем трансфекции клеток Sf9 насекомого бакуловирусом дикого типа и клонированной ДНК-вставкой
Для трансфекции клеток насекомого (Spodoptera frugiperda, Sf9) используют линейную ДНК бакуловируса дикого типа (AcMNPV) и инсектин-липосомы (Invitrogen, San Diego, СА). Опосредованная липосомами трансфекция клеток насекомого является наиболее эффективным пригодным способом трансфекции. С целью трансфекции к монослою клеток Sf9 (2·106) в 60-мм чашке осторожно добавляют следующую смесь:
3 мкг клонированной плазмидной ДНК,
10 мкл линейной ДНК бакуловируса дикого типа (AcMNPV) (0,1 мкг/мл),
2 мл среды,
29 мкл инсектин-липосом.
Чашки инкубируют при комнатной температуре в течение 4 часов при легком покачивании. После трансфекции добавляют 1 мл среды и инкубируют при 27°C в увлажненной окружающей среде в течение 48 часов. Полученный в результате трансфекционный лизат анализируют на бляшкообразование. Очистку рекомбинантного вируса, выделение клонированного доменного пептида (Cd2) и ферментативную генерацию клонированного фактора активации макрофагов, обозначенного CdMAF2, описывают так, как при процедуре клонирования I. Этот CdMAF состоит из 94 аминокислотных остатков, как показано на фиг.6, включая 9 аминокислот из гибридного вектора, и обозначается здесь как CdMAF2. Хотя CdMAF2содержит на пять аминокислот больше, чем CdMAF1 - пептид, полученный из негибридного вектора, они обнаруживают одинаковую биологическую активность.
Описание методов анализа активности α-N-ацетилгалактозаминидазы в кровотоке раковых и ВИЧ-инфицированных больных
1. Протокол анализа на обнаружение α-N-ацетилгалактозаминидазы в кровотоке раковых и ВИЧ-инфицированных больных СПИДом (схематическая иллюстрация)
Процедура обнаружения дегликозилирующего фермента сывороточного Gc-белка α-N-ацетилгалактозаминидазы в кровотоке раковых и ВИЧ-инфицированных больных или больных СПИДом
Стадия I. Этап осаждения плазмы или сыворотки 30% и 70% раствором сульфата аммония
Плазма/сыворотка (1 мл) + раствор сульфата аммония 30%, а затем 70% насыщения
70%-ный преципитат --> растворение в 50 мМ цитратфосфатном буфере (рН 6,0) --> диализ против того же буфера при 4°C в течение ночи.
Стадия II. Ферментный анализ α-N-ацетилгалактозаминидазы
Реакционная смесь: 100 мкл диализованного образца +1,0 мл 50 мМ цитратфосфатного буфера (рН 6,0), содержащего 5 мкмолей п-нитрофенил-N-ацетил-α-D-галактозаминида в качестве субстрата.
Время инкубации 60 мин, по окончании добавляют 200 мкл 0,5 М раствора Na2CO3.
Измерение активности: по поглощению выделившегося п-нитрофенола при 420 нм, выражается в нмоль/мг/мин.
2. Процедура ферментного анализа на α-N-ацетилгалактозаминидазу
Плазму/сыворотку (1 мл) здорового человека и больных осаждают раствором сульфата аммония 70% насыщения. Аммоний-сульфатный преципитат растворяют в 50 мМ цитратфосфатном буфере (рН 6,0) и диализуют против того же буфера при 4°С. Объем диализата доводят до 1 мл. Осаждение сульфатом аммония отделяет фермент от ингибиторов. Ферментную активность определяют при 37°C в 500 мкл реакционной смеси, содержащей 50 мМ цитратфосфатного буфера (рН 6,0) и 5 мкмолей п-нитрофенил-N-ацетил-α-D-галактозаминида в качестве субстрата. Реакцию инициируют путем добавления 250 мкл диализованных образцов и останавливают через 60 мин, добавляя 250 мкл 0,5 М раствора Na2CO3. Реакционную смесь центрифугируют и количество выделившегося п-нитрофенола определяют по поглощению супернатанта при 420 нм и выражают в виде нмоль/мг/мин.
3. Твердофазный иммуноферментный анализ (ELISA) для обнаружения α-N-ацетилгалактозаминидазы как антигена
При иммуноферментной процедуре обнаружения сывороточной или плазменной α-N-ацетилгалактозаминидазы (Nag) как антигена (NagAg) готовят набор антитело-сэндвич ELISA.
1) Получение антитела. Получают поликлональные антитела (козьи и кроличьи) и моноклональные антитела против α-N-ацетилгалактозаминидазы (NagAg). Иммуноглобулиновую фракцию очищают от антисыворотки или моноклональной асцитной жидкости, используя фракционирование раствором сульфата аммония (насыщение 50%) и ионообменные (DE52) колонки или колонки с белком А.
2) Конъюгация щелочной фосфатазы с антителами. Диализуют раствор 5 мг/мл антитела в 0,1 М фосфатном буфере при рН 6,8 (ЗФР) в течение ночи при 4°С. Добавляют 100 мкл диализованного раствора антитела (3 мг/мл) к 90 мкл 10 мг/мл раствора щелочной фосфатазы (чистой для иммуноанализа; Boehringer Mannheim, Индианаполис, Индиана) в 1,5-мл микроцентрифужной пробирке. Добавляют 5 мкл 25% глутаральдегида и осторожно перемешивают. Оставляют стоять при комнатной температуре. Отбирают 25-мкл образцы через 0, 5, 10, 15, 30, 60 и 120 мин и помещают их в отдельные 1,5-мл микроцентрифужные пробирки. Добавляют 125 мкл ЗФР к каждому образцу, затем добавляют 1,1 мл раствора трис/овальбумина. Диализуют образцы против ЗФР в течение ночи при 4°С. Испытывают каждый образец на активность щелочной фосфатазы, используя прямой ELISA, и определяют, какое время конъюгации дает наиболее активную конъюгацию фермента. Наилучшая активность фермента наблюдается при времени конъюгации 30 мин. Это оптимальное время конъюгации используют для получения большего количества конъюгатов щелочной фосфатазы и антител.
3) Получение микротитрационных планшетов, покрытых антителом. Используя многоканальные пипетки и насадки, распределяют 50 мкл раствора 2-10 мкг/мл иммуноглобулина в ЗФР-N (ЗФР, содержащий 0,05% азида натрия) в каждую лунку микротитрационного планшета (микролунку). Упаковывают планшеты в пластиковую упаковку, запаивают и инкубируют в течение 2 час при 37°C или в течение ночи при комнатной температуре. Ополаскивают сенсибилизированный планшет, заливая его дистиллированной водой более трех раз. Заполняют каждую лунку блокирующим буфером (ЗФР, содержащий 0,05% твина 20, 1 мм ЭДТК, 0,25% БСА и 0,05% NaN3), подавая его в виде струи из бутыли, и инкубируют 30 мин при комнатной температуре. Промывают планшет три раза дистиллированной водой и оставшуюся жидкость удаляют, осторожно прижимая лицевой стороной к бумажной салфетке.
4) Получение антигена (NagAg)
(а) Стандартный антиген для стандартной кривой. Готовят серию разведений стандартного антигена посредством последовательных разведений 1:3 исходного антигена в блокирующем буфере. Диапазон разведения от 0,1 до 1000 нг/мл.
(б) Испытание антигена. Разводят сыворотку/плазму раковых или ВИЧ-инфицированных больных в 10-100 раз, чтобы они содержали 20-1000 нг апопротеина на мл сыворотки/плазмы пациента.
5) Анализ
Стадия I. Добавляют 50-мкл аликвоты растворов испытываемых антигенов и разведения стандартного антигена в покрытые антителами лунки и инкубируют в течение 2 час при комнатной температуре. Ополаскивают планшет дистиллированной водой три раза. Наполняют каждую лунку блокирующим буфером и инкубируют 10 мин при комнатной температуре. Промывают лунки три раза водой и удаляют оставшуюся жидкость.
Стадия II. Добавляют 50 мкл специфического конъюгата антитела и щелочной фосфатазы (как правило, 25-400 нг/мл) и инкубируют 2 часа при комнатной температуре. Промывают планшет так же, как на стадии I.
Стадия III. Добавляют 75 мкл раствора субстрата п-нитрофенилфосфата (NPP) в каждую лунку и инкубируют 1 час при комнатной температуре. Ферментная активность вызывает изменение цвета раствора. Интенсивность окрашивания соотносится с присутствием или отсутствием NagAg. Снимают показания на спектрофотометре для прочтения микротитрационных планшетов с фильтром 405 нм.
б) Результаты анализа. Получают стандартную кривую, построенную на данных, полученных при серийном разведении стандартного антигена. Концентрацию антигена откладывают по оси X, которая является логарифмической шкалой, а поглощение - по оси Y, которая представляет линейную шкалу. Интерполируют концентрацию антигена (NagAg) в испытываемом растворе. Вычисляют активность α-N-ацетилгалактозаминидазы. Так как антитела к раковым и ВИЧ-ферментам специфичны по отношению к соответствующим ферментам (NagAg), этот ELISA с использованием иммуносэндвича различает отдельный фермент, а также антиген (α-галактозидазу) при контроле. Активность сывороточной/плазменной α-N-ацетилгалактозаминидазы также определяют путем интерполяции концентрации NagAg в другой стандартной кривой, полученной для зависимости активности α-N-ацетилгалактозаминидазы от концентрации NagAg. Анализ на ферментную активность методом ELISA является не только точным, но также экономичным.
Наблюдения в поддержку изобретения
А. Действие клонированных факторов активации макрофагов GcMAFc и CdMAF на культивированные фагоциты (макрофаги и остеокласты)
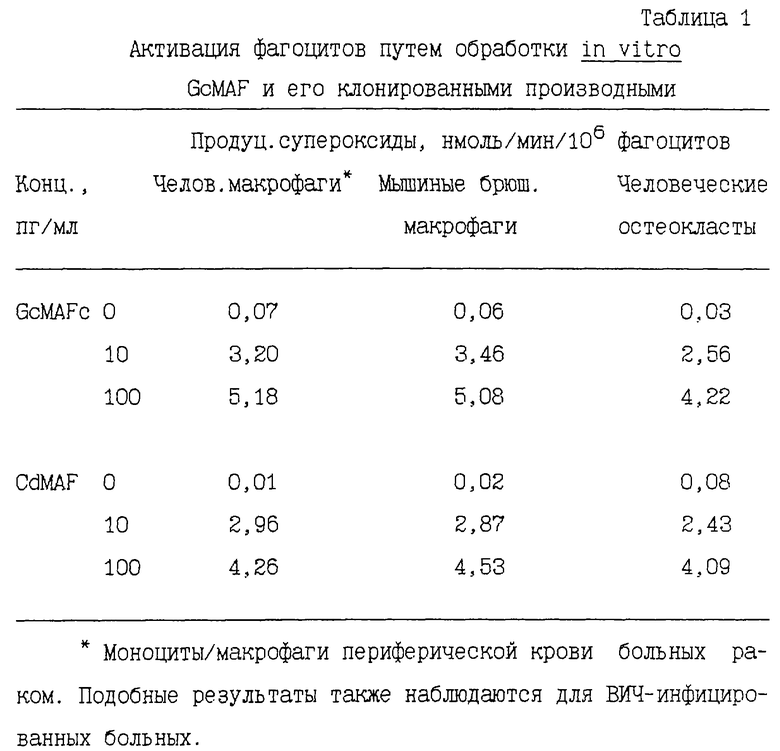
Трехчасовая обработка человеческих макрофагов и остеокластов пикограммовыми количествами (пг) клонированных факторов активации макрофагов GcMAFc и CdMAF приводит к значительно усиленной способности этих фагоцитов генерировать супероксиды, как показано в табл. 1. Уровень активации фагоцитов подобен уровню активации макрофагов с помощью GcMAF (Yamamoto et al., AIDS Res. Human Ret., 11:1373, 1995).
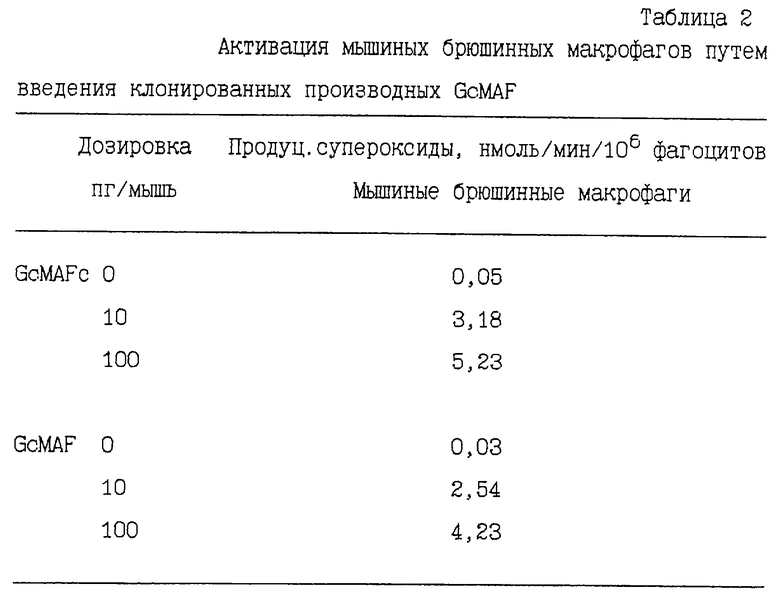
Б. Активация мышиных брюшинных макрофагов путем введения клонированных факторов активации макрофагов GcMAFc и CdMAF
Спустя сутки после введения мышам BALB/c пикограммового количества (10 и 100 пг/мышь) GcMAFc или CdMAF выделяют брюшинные макрофаги и анализируют на супероксидгенерирующую способность. Как показано в табл. 2, макрофаги активируются эффективно. Эти результаты схожи с результатами активации макрофагов GcMAF (Naraparaju and Yamamoto, Immunol. Lett., 43:143, 1994).
В. Терапевтическое действие GcMAF, GcMAFc или CdMAF на мышей - носителей опухолей и мышей с остеопетрозом
1) Терапевтическое действие GcMAF. GcMAFc или CdMAF на мышей - носителей асцитной опухоли Эрлиха
Когда мышам BALB/c вводят GcMAF, GcMAFc или CdMAF (100 пг/мышь), и они получают 105 клеток асцитной опухоли Эрлиха на мышь, они живут в течение по меньшей мере 5 недель. Все контрольные мыши получают только клетки асцитной опухоли и погибают приблизительно за 2 недели. Когда мышам вводят дополнительное количество GcMAF, GcMAFc или CdMAF (100 пг/мышь) на 4 сутки после трансплантации, опухолевые клетки исчезают полностью (табл.3).
2) Терапевтическое действие GcMAF и клонированных производных GcMAF (GcMAFc и CdMAF) на мышей с остеопетрозом
Введение GcMAFc или CdMAF новорожденному приплоду мыши с остеопетрозом ор/ор осуществляют посредством еженедельной инъекции по 100 пг в течение четырех недель, начиная со следующего дня после рождения. На 28 день мышей умерщвляют. Из обработанных и контрольных мышей извлекают большебедренные кости, разделяют надвое в продольном направлении и рассматривают под препаровальной лупой, чтобы определить размер полости костного мозга. Размер полости выражают в процентах от расстояния между эпифазарными пластинками большебедренной кости. В группе необработанных мышей костный мозг формируется на 30% общей длины большебедренной кости. В группе обработанных мышей определяют образование костного мозга, увеличенное на 20% по сравнению с группой необработанных мышей. Это повышенное образование полости костного мозга является показателем активации остеокластов и возросшей костной резорбции благодаря остеокластам.
Г. Источник иммунодепрессии у раковых и ВИЧ-инфицированных больных
Представляется, что источником плазменной α-N-ацетилгалактозаминидазы у раковых больных являются раковые клетки. Высокая активность α-N-ацетилгалактозаминидазы обнаруживается в гомогенатах опухолевых тканей различных органов, включая ткани одиннадцати различных опухолей, в том числе 4 опухоли легких, 3 - молочной железы, 3 - толстой кишки и 1 - цервикальной опухоли, хотя активность α-N-ацетилгалактозаминидазы меняется от 15,9 до 50,8 нмоль/мг/мин. Хирургическое удаление злокачественных патологических изменений при раке человека приводит к едва различимому снижению активности плазменной α-N-ацетилгалактозаминидазы и сопутствующему возрастанию активности предшественника, особенно, если злокачественные клетки локализуются.
В преклинической мышиной модели опухоли мышам BALB/c в брюшинную полость трансплантируют 5·105 клеток асцитной опухоли Эрлиха на мышь и проводят анализ на активность сывороточной α-N-ацетилгалактозаминидазы. Когда уровень фермента в сыворотке измеряют по мере роста трансплантированной асцитной опухоли Эрлиха в брюшинной полости мышей, активность фермента прямо пропорциональна опухолевому грузу (общее число опухолевых клеток в брюшинной полости), как показано на фиг.7. Это также подтверждается на мышах, которым трансплантированы КВ-клетки (клеточная линия носоглоточной эпидермальной карциомы человека). Активность сывороточной α-N-ацетилгалактозаминидазы возрастает с ростом размера (измеренной по массе) твердой опухоли. Таким образом, автор использует активность плазменной α-N-ацетилгалактозаминидазы в качестве прогностического показателя для контроля лечения.
Лучевая терапия при раке человека снижает активность плазменной α-N-ацетилгалактозаминидазы с одновременным возрастанием активности предшественника. Это означает, что лучевая терапия снижает число раковых клеток, способных секретировать α-N-ацетилгалактозаминидазу. Эти результаты также подтверждают, что активность плазменной α-N-ацетилгалактозаминидазы обратно пропорциональна активности предшественника MAF Gc-белка. Даже после хирургического удаления опухолевых нарушений у раковых больных у большинства послеоперационных больных в кровотоке имеется значительное количество активной α-N-ацетилгалактозаминидазы. Рудименты повреждений ракового характера у этих послеоперационных больных нельзя обнаружить никакими другими процедурами, например рентгенографией, сцинтиграфией и т.п. Автор применяет указанный наиболее чувствительный ферментный анализ в качестве прогностического показателя во время лечения GcMAF.
Оказалось, что ВИЧ-инфицированные клетки секретируют α-N-ацетилгалактозаминидазу в кровоток. Когда мононуклеарные клетки периферической крови (РВМС) ВИЧ-инфицированных больных культивируют и обрабатывают митомицином в качестве провирусиндуцирующего агента (Sato et al., Arch. Virol., 54:333, 1977), α-N-ацетилгалактозаминидаза секретируется в культуральную среду. Эти результаты привели автора к предположению, что α-N-ацетилгалактозаминидаза является кодируемым вирусом продуктом. Действительно, оказывается, что белок ВИЧ-оболочки gp120 несет активность α-N-ацетилгалактозаминидазы.
Д. Терапевтическое действие GcMAF, GcMAFc и CdMAF на больных раком человека и инфицированных вирусом больных
1. Больные раком: терапевтическое действие GcMAF на больных раком предстательной железы, раком молочной железы и раком толстой кишки и на взрослых лейкозных больных
Введение GcMAF (100 и 500 нг/человека) здоровым добровольцам приводит к значительно усиленной активации макрофагов, что определяется по 7-кратно усиленной фагоцитирующей способности и возросшей в 15 раз супероксидгенерирующей способности макрофагов. Введение GcMAF не показывает каких-либо побочных эффектов у реципиентов. Введение различных доз (от 100 пг до 10 нг на мышь) нескольким мышам не дает ни болезненных эффектов, ни гистологических изменений в различных органах, включая печень, легкие, почки, селезенку, головной мозг и т.д. Когда больных различными видами рака лечат GcMAF (100 нг в неделю), наблюдают заметное лечебное действие при различных видах рака. Терапевтическую эффективность GcMAF для пациентов с различными видами рака оценивают по специфической, связанной с опухолью, активности сывороточной α-N-ацетилгалактозаминидазы, поскольку содержание фермента в сыворотке пропорционально общему количеству раковых клеток (опухолевому грузу). Лечебное действие GcMAF в случае рака предстательной железы, молочной железы и толстой кишки иллюстрируется фиг.8А-8В. После 25-недельного введения 100 нг GcMAF у большинства (>90%) больных раком предстательной железы и раком молочной железы обнаруживается ничтожно низкое содержание сывороточного фермента. Подобный результат также наблюдается после 35 введений GcMAF больным раком толстой кишки. Подобное лечебное действие GcMAF наблюдают при раке легких, печени, желудка, головного мозга, мочевого пузыря, почек, матки, яичников, гортани, пищевода, ротовой полости и кожи. Таким образом, оказывается, что GcMAF эффективен при различных видах рака, без исключения. Однако GcMAF не показывает явного побочного действия на больных после более чем 6-месячного лечения. Это также подтверждается показателем числа клеток крови, функции печени и почек, и т.п.
Когда двум больным раком предстательной железы вводят, каждому, GcMAFc (100 нг в неделю) и CdMAF (100 нг в неделю), лечебное действие подобно действию, которое наблюдают в случае GcMAF.
2. Больные, инфицированные вирусом
Обработка макрофагов периферической крови ВИЧ-инфицированных больных (больных СПИДом) GcMAF (100 пг/мл) приводит к сильно возрастающей активации макрофагов (Yamamoto et al., AIDS Res. Human Ret., 11:1373, 1995). ВИЧ-инфицированные больные несут антитела против ВИЧ. ВИЧ-инфицированные клетки экспрессируют вирусные антигены на поверхности клеток. Таким образом, макрофаги, когда они активированы, имеют потенциал для ликвидации инфицированных клеток через опосредованный Fc-рецептором киллинг/фагоцитоз клеток.
Подобным образом обработка GcMAF (100 нг/мл) макрофагов периферической крови больных, хронически инфицированных вирусом Эпштейна-Барра (EBV) и вирусом опоясывающего герпеса, приводит к весьма повышенной активации макрофагов. Подобно ВИЧ, EBV заражает лимфоциты (В-клетки). Так как эти содержащие оболочки вирусы кодируют α-N-ацетилгалактозаминидазу, а зараженные клетки секретируют ее в кровоток, активность этого фермента в сыворотке пациента можно использовать в качестве прогностического показателя при лечении. Приблизительно после 25 введений GcMAF (100 нг в неделю) больным, хронически инфицированным EBV и вирусом опоясывающего герпеса, активность фермента снижается до уровня у здоровых людей. Когда зараженным EBV больным вводят GcMAFc (100 нг в неделю) и CdMAF (100 нг в неделю), наблюдают лечебное действие, подобное действию GcMAF.
Е. Адъювантная активность GcMAF, GcMAFc и CdMAF в случае иммунизации и вакцинации: быстрое возрастание у мышей числа клеток, секретирующих антитела (PFC), после введения GcMAF и овечьих эритроцитов
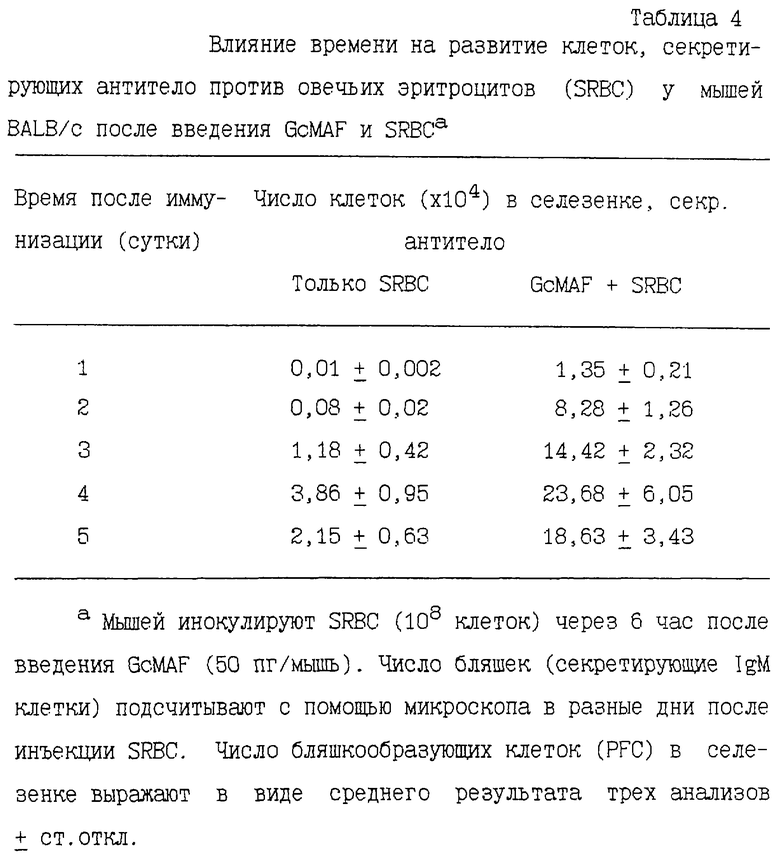
Мышей BALB/c инокулируют SRBC через 6 часов после интраперитонеального введения 50 пг GcMAF на мышь. В различные периоды после иммунизации (1-5 суток) определяют число клеток, секретирующих IgM-антитела в селезенке, применяя анализ методом бляшек по Ерне (Jerne et al., Cell-bound antibodies, Wistar Institute Press, 1963). Через день после введения GcMAF и SRBC в селезенке образуется 1,35·104 PFC. Через два дня после введения GcMAF и SRBC число клеток, секретирующих антитела, возрастает в селезенке до 8,2·104 PFC. На 4-е сутки число клеток, секретирующих антитела, достигает максимального уровня 23,6·104 PFC в селезенке), как показано в табл. 4. В противоположность этому мыши, которые получают инъекцию только SRBC, через 4 дня после инъекции SRBC продуцируют в селезенке 3,8·104 PFC.
Чтобы выяснить эффект дозы, мышей инъецируют SRBC через 6 часов после введения различных доз GcMAF от 1 до 50 пг/мышь. На 4-е сутки после введения GcMAF и SRBC методом бляшек по Ерне определяют число клеток в селезенке, секретирующих антитела. На 4-е сутки после введения отмечается возрастание числа бляшкообразующих клеток, соразмерное возрастанию концентрации GcMAF сверх 1 пг на мышь. При дозе GcMAF 5, 10 и 50 пг/мышь автор обнаруживает 12,6·104, 20,2·104 и 24,3·104 PFC в селезенке соответственно. Следовательно, GcMAF является сильным адъювантом при иммунизации.
Без дополнительных уточнений, вышесказанное будет достаточно полно иллюстрировать настоящее изобретение, чтобы другие специалисты, применяя сегодняшние или специальные знания, адаптировали его для применения в различных условиях работы.
Источники информации, перечисленные далее, полностью включены в настоящее изобретение в качестве ссылок, которые упоминаются выше в описании.
Источники информации
Патенты США
Патенты США No 5177001, 5177002 и 5326749 (Yamamoto).
Другие публикации
1. Jerne, N. K., Nordin, A. A. and Herny, C., The agar plaque technique for recognizing antibody producing cells. In Amos and Koprowski (eds). Cell-bound Antibody. Wistar Institute Press, Philadelphia, PA (1963).
2. Sato, M., Tanaka, H., Yamada, T. and Yamamoto, N., Persistent infection of BHK/WI-2 cells with rubella virus and characterization of rubella variants. Arch. Virology 54:333-343 (1977).
3. Reeves, J. D., August, C S., Humbert, J. R., Weston, W. L., Host defense in infantile osteoporosis. Pediatrics. 64:202 (1979).
4. Marks, S. C., Jr., Congenital osteopetrotic mutations as probes of the origin, structure and function of osteoclasts. Clin. Orthop. 189:239 (1984).
5. Link, R. P., Periman, K. L., Pierce, E. A., Schnoes, H. K., DeLuca, H. F. Purification of human serum vitamin D-binding protein by 25-hydroxyvitamin D3-Sepharose chromatography. Anal. Biochem. 157:262-269 (1986).
6. Cooke, N. E. and Haddad, J. G., Vitamin D binding protein (Gc-globulin). Endocrine Rev. 10:294-307 (1989).
7. Marks, S. C., Jr., Osteoclast biology: Lessons from mammalian mutations. Am. J. Med. Genet. 34:43-54 (1989).
8. Ngwenya, B.Z. and Yamamoto, N., Contribution of lysophosphatidylcholine treated nonadherent cells to mechanism of macrophage stimulation. Proc. Soc. Exp. Biol. Med. 193:118-124 (1990).
9. Ausubel, F. A., Brent, R., Kingston, R. E., Moore, D. D., Seidman, J. G., Smith, J. A. and Struhl, K. (eds.), Expression of proteins in insect cells using baculoviral vectors. Current Protocols in Molecular Biology. Sections 16.8.1-16.11.7. Greene Publishing and Wiley-Interscience, New York (1990).
10. Yamamoto, N. and Homma, S., Vitamin D3 binding protein (group-specific component, Gc) is a precursor for the macrophage activating signal from lysophosphatidylcholine-treated lymphocytes. Proc. Natl Acad, Sci. USA. 88:8539-8543 (1991).
11. Cooke, N. E. and David, E. V., Serum vitamin D-binding protein is a third member of the albumin and alpha-fetoprotein gene family. J. Clin. Invest. 76:2420-2424 (1985).
12. Haddad, J. G., Hu, Y. Z., Kowalski, M. A., Laramore, C., Ray, K., Robzyk, P. and Cooke, N. E., Identification of the sterol- and actin-binding domains of plasma vitamin D binding protein (Gc-globulin). Biochemistry 31:7174-7181 (1992).
13. Yamamoto, N. and Kumashiro, R., Conversion of vitamin D3, binding protein (Group-specific component) to a macrophage activating factor by stepwise action of β-galactosidase of B cells and sialidase of T cells. J. Immunol. 151:27-94-2902 (1993).
14. Yamamoto, N., Kumashiro, R., Yamamoto, M.. Willett, N. P. and Lindsay, D.D.. Regulation of inflammation-primed activation of macrophages by two serum factors, vitamin D3-binding protein and albumin. Inf. Imm. 61:5388-539I (1993).
15. Yamamoto, N., Lindsay, D. D., Naraparaju, V. R., Irelalnd, R. A. and Popoff, S.M., A defect in the inflammation-primed macrophage activation cascade in osteopetrotic (op) rats. J. Immunol. 152:100-5107 (1994).
16. Yamamoto, N., Willett, N.P. and Lindsay, D.D., Participation of serum proteins in the inflammation-primed activation of macrophagcs. Inflammation. 18:311-322 (1994).
17. Naraparaju, V. R. and Yamamoto, N., Roles of β-galactosidase of B lymphocytes and sialidase of T lymphocytes in inflammation-primed activation of macrophages. Immunol. Lett. 43:143-148 (1994).
18. Yamamoto, N, Naraparaju, V.R. and Srinivasula, S.M., Structural modification of serum vitamin D3-binding protein and immunosuppression in HTV-infected patients. AIDS Res. Human Ret. 11:1373-1378 (1995).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения и определения специфической активности фактора активации макрофагов GcMAF | 2023 |
|
RU2823530C1 |
| СПОСОБ ТОРМОЖЕНИЯ РОСТА ПОДКОЖНОГО ТРАНСПЛАНТАТА ЭКСПЕРИМЕНТАЛЬНОЙ ГЛИОБЛАСТОМЫ ЧЕЛОВЕКА U-87, ПЕРЕВИТОГО ИММУНОДЕФИЦИТНЫМ МЫШАМ NU/J | 2019 |
|
RU2717218C1 |
| МОДИФИЦИРОВАННЫЙ БИОТИН-СВЯЗЫВАЮЩИЙ БЕЛОК, СЛИТЫЕ БЕЛКИ НА ЕГО ОСНОВЕ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2632651C2 |
| УСИЛЕНИЕ ИММУННЫХ ОТВЕТОВ, ОПОСРЕДОВАННЫХ БЕЛКАМИ, СЛИТЫМИ ИЗ АНТИТЕЛА И ЦИТОКИНА, ПОСРЕДСТВОМ СОВМЕСТНОГО ВВЕДЕНИЯ ИНГИБИТОРА АНГИОГЕНЕЗА | 1999 |
|
RU2229305C2 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ И СПОСОБ РАЗРАБОТКИ ВАКЦИНЫ, ОСНОВАННОЙ НА СЛИТОМ БЕЛКЕ | 2004 |
|
RU2407749C2 |
| ПОЛУЧЕНИЕ БИОЛОГИЧЕСКИ АКТИВНЫХ БЕЛКОВ | 2007 |
|
RU2441911C2 |
| МОДИФИЦИРОВАННЫЕ МОНОЦИТЫ/МАКРОФАГИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ, И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2766690C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ МОДУЛЯЦИИ ГЕПСИНОМ СТИМУЛИРУЮЩЕГО МАКРОФАГИ БЕЛКА | 2010 |
|
RU2539772C2 |
| СЛИТЫЙ БЕЛОК SIRPα-4-1BBL И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2018 |
|
RU2769769C2 |
| УСЛОВНО РЕПЛИЦИРУЮЩИЙСЯ РЕТРОВИРУСНЫЙ ВЕКТОР (ВАРИАНТЫ), СПОСОБ ЕГО ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЯ (ВАРИАНТЫ), ВЫДЕЛЕННАЯ И ОЧИЩЕННАЯ МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ | 1996 |
|
RU2270250C2 |

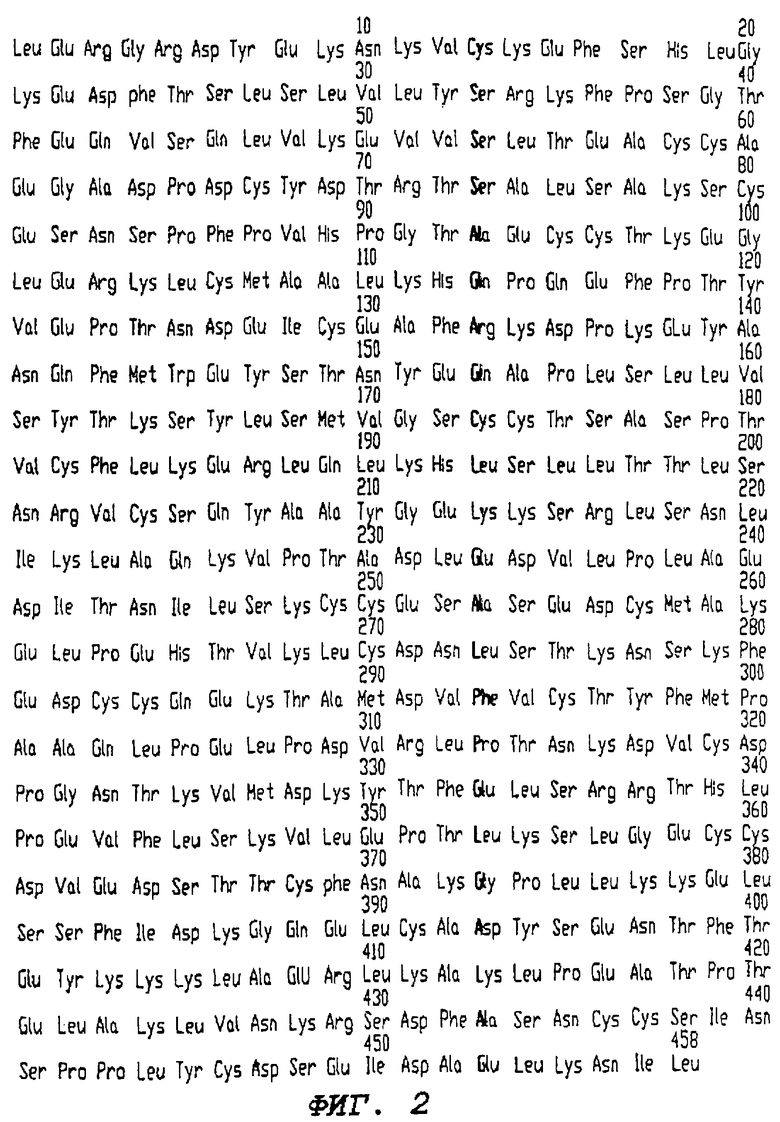

Изобретение относится к сильнодействующим факторам активации макрофагов. Связывающий витамин D3 белок (Gc-белок) и его малый домен (приблизительно 1/5 Gc-пептида, известный также как домен III) клонируют с помощью бакуловирусного вектора. Клонированный Gc-белок и клонированный пептид домен III (Cd) обрабатывают иммобилизованной β-галактозидазой и сиалидазой и получают факторы активации макрофагов GcMAFc и CdMAF соответственно. Эти клонированные факторы активации макрофагов и GcMAF можно использовать в качестве адъювантов при иммунизации и вакцинации. Изобретение позволяет лечить такие заболевания, как остеопетроз. 10 н.п. ф-лы, 8 ил., 4 табл.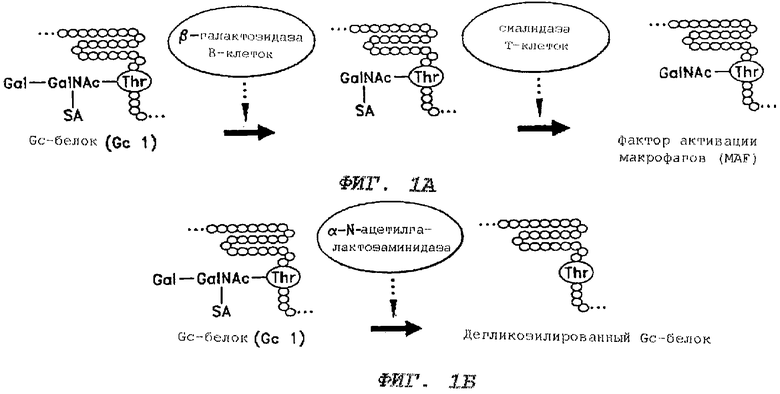
| WO 9307288 А4, 15.04.1993 | |||
| WO 9204459 А4, 19.03.1992 | |||
| GENOMICS, vol | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| BIOCHIMICA ET BIOPHYSICA ACTA, vol.1216, 1993, р.385-394 | |||
| PROCEEDINGS OF THE NATIONAL ACADAMY OF SCIENCE, vol.82, DEC.1985, p.7994-7998 | |||
| МАНИАТИС Г | |||
| и др | |||
| Методы генетической инженерии | |||
| - М.: Мир, 1984, с.205-224. | |||
Авторы
Даты
2003-02-10—Публикация
1996-06-05—Подача