Изобретение относится к микрочастицам, имеющим улучшенную устойчивость при хранении, и к способу получения таких микрочастиц. Более конкретно, настоящее изобретение относится к фармацевтическим композициям, включающим микрочастицы контролируемого высвобождения, имеющие улучшенную устойчивость при хранении, причем указанные микрочастицы включают активные вещества, инкапсулированные внутри полимерной матрицы, и к способу получения таких частиц.
Соединения могут быть инкапсулированы в форме микрочастиц (например, частиц, имеющих средний размер в диапазоне от нанометра до миллиметра, в частности в диапазоне от 1 до 500 мкм, особенно от 25 до 180 мкм) с помощью различных известных способов. Особенно выгодно инкапсулировать биологически активное или фармацевтически активное вещество внутрь биосовместимого, биодеградируемого, образующего стенку материала (например, полимера) для обеспечения продолжительного или отсроченного высвобождения лекарственных препаратов или других активных средств. При этих способах подлежащий инкапсулированию материал (лекарственный препарат или другое активное вещество) в целом растворяется, диспергируется или эмульсифицируется с использованием известных способов смешивания в растворителе, содержащем образующий стенку материал. Затем растворитель удаляется из микрочастиц и после этого получается продукт в виде микрочастиц.
Очень часто растворители, используемые в известных способах микроинкапсуляции, представляют собой галогенизированные углеводороды, в частности хлороформ или метиленхлорид, которые действуют в качестве растворителей как для активного вещества, так и для инкапсулированного полимера. Однако присутствие мелких, но выявляемых остатков галогенизированных углеводородов в конечном продукте нежелательно ввиду их общей токсичности и возможной канцерогенной активности.
В патенте WO-95/13799 был раскрыт способ получения биодеградируемых, биосовместимых микрочастиц, включающих биодеградируемый, биосовместимый связывающий полимер и биологически активное вещество, в котором для растворения и вещества, и полимера используют смесь, по меньшей мере, двух по существу нетоксичных растворителей, свободных от галогенизированных углеводородов. Эту смесь растворителей диспергируют в водном растворе для образования эмульсии, которую затем добавляют в водную экстракционную среду, которая предпочтительно содержит, по меньшей мере, один из растворителей смеси, с помощью которой контролируется скорость экстракции каждого растворителя, после чего образуются биодеградируемые, биосовместимые микрочастицы, содержащие биологически активное вещество.
В патенте WO-95/13814 также описан рисперидон, инкапсулированный в микрочастицы, полученные с использованием системы растворителя, содержащей бензиловый спирт и этилацетат.
Однако было установлено, что во время хранения эти продукты в виде микрочастиц распадаются. Поэтому существует необходимость в веществах, с помощью которых может быть уменьшена скорость распада, увеличивая таким образом устойчивость продукта при хранении и повышая возможность его промышленного производства.
Неожиданно в настоящий момент было установлено, что скорость распада продукта можно уменьшить с помощью снижения уровня остаточного обрабатывающего растворителя. Считается, что один из процессов распада происходил, по меньшей мере, частично, в результате гидролиза полимерной матрицы, и что на скорость гидролиза непосредственное влияние оказывает уровень остаточного обрабатывающего растворителя (например, бензилового спирта) в продукте. С помощью снижения уровня остаточного растворителя в микрочастицах уменьшается скорость распада, увеличивая таким образом устойчивость при хранении.
Таким образом, в соответствии с одним аспектом, изобретение предоставляет способ получения биодеградируемых, биосовместимых микрочастиц, причем указанный способ включает: контактирование микрочастиц, включающих биодеградируемую, биосовместимую полимерную матрицу, содержащую активное (например, фармацевтическое или диагностическое) средство, и органического растворителя с водной системой растворителя, посредством чего содержание указанного органического растворителя в указанных микрочастицах снижено до 2% или менее массы указанных микрочастиц, причем указанная система растворителя такова, чтобы удовлетворить, по меньшей мере, одному из условий: (а) что оно, по меньшей мере, часть времени, в течение которого она контактирует с указанными частицами, имеет повышенную температуру (например, от 25 до 40oС) и (b) что она содержит воду и смешиваемый с водой растворитель для указанного органического растворителя; и извлечение указанных микрочастиц из указанной водной системы растворителя.
В способе изобретения исходное содержание органического растворителя в частицах составляет обычно выше 3,5%, чаще всего выше 4,0%, от общей массы частиц. Выгодно, чтобы способ снижал это содержание до уровня менее чем 2%, предпочтительно до менее чем 1,5% и наиболее предпочтительно до менее чем 1%. Рассматриваемый органический растворитель предпочтительно содержит гидрофобную группу, содержащую, по меньшей мере, 5 углеродов, например арильную группу, такую как нафтил, или, в частности, фенильную группу.
Органический растворитель в частицах, как правило, присутствует в результате процесса образования частиц, в котором частицы были получены из раствора, образующего матрицу полимерного материала, в органическом растворителе или в композиции или смеси растворителей, содержащей органический растворитель. Органический растворитель предпочтительно представляет собой негалогенизированный растворитель и, особенно предпочтительно, по меньшей мере, частично, представляет собой смешиваемый с водой растворитель, такой как спирт (например, бензиловый спирт), линейный или циклический простой эфир, кетон или сложный эфир (например, этилацетат). Когда органический растворитель представляет собой один растворитель в такой комбинации композиции или смеси растворителей, любой другой растворитель в композиции или смеси будет предпочтительно негалогенизированным растворителем и, особенно предпочтительно, будет, по меньшей мере, частично представлять собой смешиваемый с водой растворитель, такой как спирт (например, С1-C4 алканол, такой как этанол), линейный или циклический сложный эфир, кетон или простой эфир.
Если используется смешиваемый с водой растворитель в водной системе растворителя (т. е. промывающей жидкости), то он аналогичным образом будет предпочтительно представлять собой негалогенизированный растворитель и, особенно предпочтительно, будет, по меньшей мере, частично представлять собой смешиваемый с водой растворитель, такой как спирт (например, С1-C4 алканол, такой как этанол), линейный или циклический сложный эфир, кетон или простой эфир.
Контактирование с водной системой растворителя может осуществляться в одну или более стадий, например одиночным контактом или серией промываний, необязательно с различным образом составленными системами растворителя. Предпочтительно общее время контакта составляет период от десяти минут до нескольких часов, например от 1 до 48 ч.
Конечно, полимерный материал, образующий матрицу, должен иметь достаточно ограниченную растворимость в используемой водной системе растворителя, так что частицы полностью не растворяются в системе растворителя в течение периода контакта.
Особенно предпочтительно частицы, используемые в способе изобретения, готовят путем получения двухфазной жидкой системы, в которой первая дисперсная жидкая фаза присутствует во второй непрерывной жидкой фазе. Первая жидкая фаза включает образующий матрицу полимер, растворенный в первой системе растворителя, в которой растворено или диспергировано активное вещество. Первая система растворителей включает органический растворитель, необязательно и предпочтительно совместно с одним или более совместных растворителей, причем различные растворители предпочтительно представляют собой спирты, простые эфиры, сложные эфиры или кетоны и предпочтительно не включают какие-либо галогенизированные растворители. Предпочтительно один из растворителей в первой системе растворителя имеет гидрофильную группу, например арильную группу, такую как фенильная группа, особенно предпочтительно она представляет собой бензиловый спирт. Предпочтительно второй растворитель с более высокой растворимостью в воде, например этилацетат, присутствует в первой системе растворителя. Вторая жидкая фаза предпочтительно включает один или более растворителей, таких как вода, и предпочтительно является таковой, что полимер менее растворим в ней, чем в первой системе растворителя, но такой, что растворители первой системы растворителей являются, по меньшей мере, частично растворимыми в ней, позволяя таким образом частицам образовываться путем диффузии растворителя из первой жидкой фазы во вторую жидкую фазу. Вторая жидкая фаза может преимущественно содержать гидроколлоид или сурфактант.
Способ настоящего изобретения может проводиться с использованием предварительно образованных частиц или более предпочтительно может дополнительно включать получение частиц при использовании жидкой фазы, содержащей в качестве растворителя или совместного растворителя органический растворитель, указанный выше, а также полимер, образующий матрицу, и активное вещество. Затем образование частиц может осуществляться, например, с помощью высушивания распылением или более предпочтительно с помощью образования эмульсии с использованием второй жидкой фазы, например водной фазы, при этом первая фаза является дисперсной, а вторая фаза является непрерывной, т.е. как описано выше.
В другом аспекте изобретение также предоставляет материал в виде частиц, включающий микрочастицы биодеградируемой, биосовместимой полимерной матрицы, содержащей активное вещество и органический растворитель, причем указанный органический растворитель присутствует в указанных микрочастицах в количестве 2% или менее от общей массы указанных микрочастиц.
В альтернативном аспекте изобретение предоставляет материал в виде частиц, включающий микрочастицы биодеградируемой, биосовместимой полимерной матрицы, содержащей активное вещество, причем указанные микрочастицы получены с помощью способа в соответствии с изобретением.
Еще в одном аспекте изобретение предоставляет фармацевтическую композицию, включающую микрочастицы в соответствии с изобретением совместно с, по меньшей мере, одним фармацевтически приемлемым носителем или наполнителем.
С точки зрения еще одного аспекта, изобретение предоставляет применение частиц, полученных с помощью способа изобретения, для производства лекарственного препарата для использования в способе диагностики или лечения.
С точки зрения еще одного аспекта, изобретение предоставляет способ лечения организма человека или животного (например, млекопитающего), включающий введение в него композиции в соответствии с изобретением.
Настоящее изобретение предоставляет усовершенствованный способ получения фармацевтической композиции в форме микрочастиц, предназначенной для контролируемого высвобождения эффективного количества препарата в течение продолжительного периода времени, посредством чего композиция проявляет повышенную устойчивость при хранении. Возможную продолжительность хранения можно увеличить приблизительно до двух или более лет для микрочастиц, изготовленных в соответствии со способом настоящего изобретения. Изобретение также относится к новой композиции как таковой, которая включает, по меньшей мере, одно активное вещество, по меньшей мере, одно биосовместимое, биодеградируемое инкапсулирующее связывающее вещество и менее чем приблизительно 2 мас. % остаточного растворителя, причем остаточный растворитель получают из растворителя, применяемого при получении микрочастиц.
В одном предпочтительном варианте реализации способ настоящего изобретения включает:
А) получение первой фазы, включающей:
(1) биодеградируемое, биосовместимое полимерное инкапсулирующее связывающее вещество и
(2) имеющее ограниченную растворимость в воде активное вещество, растворенное или диспергированное в первом растворителе;
B) получение водной второй фазы;
C) комбинирование указанной первой фазы и указанной второй фазы под воздействием смешивающего средства для образования эмульсии, в которой указанная первая фаза является дисперсной, а указанная вторая фаза является непрерывной;
D) отделение указанной дисперсной первой фазы от указанной непрерывной второй фазы и
Е) промывание указанной дисперсной первой фазы
(1) водой при температуре в диапазоне от приблизительно 25oС до приблизительно 40oС или
(2) водным раствором, включающим воду и второй растворитель для остаточного первого растворителя в указанной первой фазе,
снижая таким образом уровень остаточного первого растворителя до менее чем приблизительно 2 мас.% указанных микрочастиц.
В предпочтительном аспекте описанного выше способа между этапами С) и D) дополнительно выполняется этап прекращения реакции.
Водная вторая фаза может представлять собой водный раствор гидрофильного коллоида или сурфактанта. Водная вторая фаза может представлять собой воду.
В другом предпочтительном варианте реализации способ настоящего изобретения включает получение первой дисперсной фазы (также именуемой здесь как "масляная фаза" или "органическая фаза"), содержащей от приблизительно 5 до приблизительно 50 мас.% твердых веществ, из которых от приблизительно 5 до приблизительно 95 мас.% представляют собой раствор биодеградируемого, биосовместимого полимерного инкапсулирующего связывающего вещества, и включающего от приблизительно 5 до приблизительно 95 мас.% активного вещества на основе полимерного связывающего вещества, в смеси растворителя, причем смесь включает первый и второй взаимно смешиваемые совместные растворители, причем каждый имеет растворимость в воде от приблизительно 0,1 до приблизительно 25 мас.% при 20oС; образование эмульсии, содержащей 1 часть по массе первой фазы в количестве от 1 до 10 частей по массе среды обработки эмульсии, для образования микрокапелек композиции дисперсной первой фазы в среде обработки непрерывной или "водной" второй фазы; добавление комбинированных первой и второй фаз в водную экстракционную охлаждающую жидкость для прекращения реакции на уровне от приблизительно 0,1 до приблизительно 20 л водной охлаждающей жидкости для прекращения реакции на 1 г полимера и активного вещества, причем охлаждающая жидкость для прекращения реакции содержит более растворимый в воде совместный растворитель смеси на уровне от приблизительно 20% до приблизительно 70% уровня насыщения более растворимого в воде совместного растворителя в охлаждающей жидкости для прекращения реакции при используемой температуре; извлечение микрочастиц из охлаждающей жидкости для прекращения реакции; промывание дисперсной первой фазы водой при повышенной температуре (т.е. выше комнатной температуры) или водным раствором, включающим воду и растворитель для остаточного растворителя в первой фазе, снижая таким образом уровень остаточного растворителя в микрочастицах. Уровень остаточного растворителя в микрочастицах предпочтительно снижается до приблизительно 2 мас.% микрочастиц.
В другом предпочтительном варианте реализации способ настоящего изобретения включает:
(А) получение первой фазы, включающей:
1) биодеградируемое, биосовместимое полимерное инкапсулирующее связывающее вещество, выбранное из поли(гликолевой кислоты), поли-D,L-молочной кислоты, поли-L-молочной кислоты и их сополимеров, и
2) активное вещество, выбранное из рисперидона, 9-гидроксирисперидона и их фармацевтически приемлемых солей, растворенных или диспергированных в смеси, включающей этилацетат и бензиловый спирт, причем указанная смесь свободна от галогенизированных углеводородов;
B) получение второй фазы, включающей поливиниловый спирт, растворенный в воде;
C) комбинирование указанной первой фазы и указанной второй фазы в статическом миксере для образования эмульсии, в которой указанная первая фаза является дисперсной, а указанная вторая фаза является непрерывной;
D) погружение указанных первой и второй фаз в охлаждающую жидкость для прекращения реакции;
Е) выделение указанной дисперсной первой фазы в форме микрочастиц и
F) промывание указанной дисперсной первой фазы водным раствором, включающим воду и этанол, что снижает уровень бензилового спирта до менее чем 2 мас.% указанных микрочастиц.
В другом предпочтительном варианте реализации способ изобретения включает:
A) получение первой фазы, причем указанная первая фаза включает активное вещество (например, биологически активное вещество), биодеградируемый, биосовместимый полимер и первый растворитель;
B) получение второй фазы, в которой указанная первая фаза является по существу не смешиваемой;
C) пропускание потока указанной первой фазы через статический миксер при первой скорости потока;
D) пропускание потока указанной первой фазы через статический миксер при второй скорости потока так, что указанная первая фаза и указанная вторая фаза текут одновременно через указанный статический миксер, образуя таким образом микрочастицы, содержащие указанное активное вещество;
Е) выделение указанных микрочастиц и
F) промывание указанных микрочастиц водой при повышенной температуре или водным раствором, включающим воду и второй растворитель для остаточного первого растворителя в указанных микрочастицах, что снижает уровень остаточного первого растворителя до менее чем приблизительно 2 мас.% указанных микрочастиц.
В других вариантах реализации изобретения первая фаза может быть получена путем растворения биологически активного вещества в растворе полимера, растворенного в растворителе, свободном от галогенизированных углеводородов, и получения дисперсии, включающей активное вещество в растворе полимера, или получения эмульсии, включающей активное вещество в растворе полимера.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, включающей биодеградируемые и биосовместимые микрочастицы в фармацевтически приемлемом носителе. Микрочастицы включают полимерное инкапсулирующее связывающее соединение, имеющее в себе диспергированное или растворенное активное вещество и менее чем приблизительно 2 мас.% остаточного растворителя, в котором остаточный растворитель является остатком растворителя, применявшегося при получении микрочастиц.
В другом аспекте настоящее изобретение относится к фармацевтической композиции, включающей биодеградируемые и биосовместимые микрочастицы, размер которых находится в диапазоне от приблизительно 25 до 180 мкм, в фармацевтически приемлемом носителе. Микрочастицы включают сополимер поли(гликолевой кислоты) и поли(D,L-молочной кислоты), в котором молярное отношение лактида к гликолиду находится в диапазоне от приблизительно 85:15 до приблизительно 50: 50, и имеющий от приблизительно 35 до приблизительно 40% диспергированного или растворенного в нем активного вещества, включающего рисперидон или 9-гидроксирисперидон, и от приблизительно 0,5 до приблизительно 1,5 мас.% бензилового спирта.
Преимущество способа настоящего изобретения состоит в том, что он может применяться для производства, наряду с другими, биодеградируемой, биосовместимой системы, которая может инъецироваться пациенту. Способ обеспечивает возможность смешивания микрочастиц, содержащих различные лекарственные препараты, для получения микрочастиц, свободных от остатков галогенизированных углеводородов, и для программирования высвобождения для обеспечения по необходимости более высокой или более низкой скорости высвобождения препарата (т. е. можно получить образец многофазного высвобождения). Кроме того, при применении способа достигается улучшенная устойчивость при хранении в результате сниженного содержания остаточного растворителя в конечном продукте.
Преимущество продуктов, полученных с помощью способа настоящего изобретения, состоит в том, что можно получить продолжительность действия в диапазоне от 7 до более чем 200 дней, например от 14 до 100 дней, в зависимости от типа отобранных микрочастиц. В предпочтительных вариантах реализации микрочастицы могут иметь структуру, обеспечивающую возможность лечения пациентов в течение периодов действия от 14 до 60 дней, от 20 до 60 дней, от 30 до 60 дней и от 60 до 100 дней. Особенно выгодной считается продолжительность периода действия, составляющая 90 дней. Продолжительность действия можно контролировать с помощью изменений композиции полимера, соотношения полимер : препарат, размера микрочастиц и концентрации остаточного растворителя, остающегося в микрочастице после обработки.
Другим важным преимуществом микрочастиц, полученных с помощью способа настоящего изобретения, является то, что практически все активное вещество доставляется пациенту, потому что полимер, применяемый в способе настоящего изобретения, является биодеградируемым, позволяя таким образом всему захваченному активному веществу высвобождаться в организм пациента.
Еще одним важным преимуществом микрочастиц, полученных с помощью способа настоящего изобретения, является то, что содержание остаточного растворителя (растворителей) в конечном продукте в виде микрочастиц может быть снижено приблизительно на порядок величины, посредством чего можно увеличить полезную устойчивость продукта при хранении от приблизительно шести месяцев для продукта, изготовленного без этапа промывания (т.е. контактирования) настоящего изобретения, до приблизительно двух или более лет для частиц, изготовленных с этапом промывания.
Еще одним преимуществом способа настоящего изобретения является то, что он может оказаться благоприятным в контролировании характеристик высвобождения активного вещества in vivo или уменьшении содержания нежелательного или, возможно, вредного растворителя.
Для обеспечения ясности последующего описания предоставляются следующие определения. Под "микрочастицами" или "микросферами" подразумеваются твердые частицы, которые содержат активное вещество, диспергированное или растворенное внутри биодеградируемого, биосовместимого полимера, который служит в качестве матрицы частицы. Под "ограниченной растворимостью в воде" подразумевается наличие растворимости в воде в диапазоне от приблизительно 0,1 до приблизительно 25 мас.% при 20oС. Под "галогенизированными углеводородами" подразумеваются галогенизированные органические растворители, например С1-С4 галогенизированные алканы, например метиленхлорид, хлороформ, метилхлорид, тетрахлорид углерода, этилендихлорид, этиленхлорид, 2,2,2-трихлорэтан и им подобные. Под "биодеградируемым" подразумевается материал, который будет распадаться под влиянием процессов в организме на продукты, легко выводимые организмом и не накапливающиеся в организме, оказывая вредное воздействие. Продукты биологического распада должны также быть биосовместимы с организмом. Под "биосовместимым" подразумевается, что упоминаемый материал не токсичен для организма человека, является фармацевтически приемлемым, не является канцерогенным и не вызывает значительного воспаления в тканях организма. Под "мас.%" или "% по массе" подразумеваются части по массе на общую массу микрочастицы. Например, 10 мас.% вещества означало бы 10 частей вещества по массе и 90 частей полимера по массе. Если нет других уточнений, упоминаемые здесь процентные доли представлены по массе, если не ясно из контекста, что это не так.
В способе настоящего изобретения растворитель, предпочтительно свободный от галогенизированных углеводородов, может применяться для производства биодеградируемых, биосовместимых микрочастиц, включающих, по меньшей мере, одно биологически активное вещество. Особенно предпочтительным растворителем является смесь растворителей, включающая, по меньшей мере, два растворителя. Первый растворяющий компонент смеси растворителей предпочтительно представляет собой слабый растворитель для активного вещества, но хороший растворитель для биодеградируемого, биосовместимого полимера. Второй растворяющий компонент смеси растворителей предпочтительно представляет собой хороший растворитель для активного вещества. Активное вещество растворено или диспергировано в растворителе. В содержащую вещество среду добавляют материал полимерной матрицы, что обеспечивает получение продукта, имеющего желательную загрузку активного вещества. Необязательно все ингредиенты продукта в виде микрочастиц могут смешиваться вместе в среде смеси растворителей.
Предпочтительная система растворителя представляет собой смесь, по меньшей мере, двух растворителей. Растворители в смеси растворителей являются предпочтительно
(1) взаимно смешиваемыми друг с другом,
(2) способными при смешивании растворять или диспергировать активное вещество,
(3) способными при смешивании растворять материал полимерной матрицы,
(4) химически инертными по отношению к активному веществу,
(5) биосовместимыми,
(6) по существу не смешиваемыми с любой применяемой жидкостью для остановки реакции, например имеющими растворимость от приблизительно 0,1 до 25%, и
(7) растворители, кроме галогенизированных углеводородов.
Идеальная смесь растворителей для инкапсулирования активного вещества должна иметь высокую растворимость для полимерного инкапсулирующего вещества в целом, по меньшей мере, приблизительно 5 мас.% и предпочтительно, по меньшей мере, приблизительно 20 мас.% при 20oС. Верхний предел растворимости не имеет принципиального значения, но если он выше приблизительно 50 мас.% раствора инкапсулирующего полимера, раствор может стать слишком вязким для эффективного и удобного обращения с ним. Это, конечно, зависит от природы инкапсулирующего полимера и его молекулярной массы.
Система растворителя, хотя и по существу не смешиваемая с непрерывной фазой обрабатывающей среды и любой охлаждающей жидкостью для прекращения реакции, которые обычно представляют собой воду или основаны на воде, предпочтительно имеет ограниченную растворимость в ней. Если бы система растворителя была бесконечно растворима в обрабатывающей среде, то микрочастицы были бы неспособны образовываться во время эмульсионной фазы; однако, если бы растворимость системы растворителя в экстрактивной среде для остановки реакции была бы слишком низкой, потребовались бы большие количества среды для остановки реакции. В целом, для использования в обрабатывающей среде и любой среде для остановки реакции приемлема растворимость растворителя от приблизительно 0,1 до приблизительно 25%. Для контроля скорости потери первого растворителя из микрочастиц в среду для остановки реакции в случаях применения среды для остановки реакции выгодно, чтобы она содержала от приблизительно 70 до приблизительно 20 мас.% точки насыщения первого растворителя, т. е. растворителя более высокой растворимости в среде для остановки реакции.
Дополнительные соображения при выборе компонента смеси растворителя настоящего изобретения включают точку кипения (т.е. легкость, с которой растворители могут по желанию испаряться для образования конечного продукта) и удельный вес (тенденция дисперсной или масляной фазы плавать во время эмульсификации и остановки реакции). Наконец, система растворителя должна иметь низкую токсичность.
В целом, композиция смеси растворителя из двух компонентов будет содержать от приблизительно 25 до приблизительно 75 мас.% первого растворителя и соответственно от приблизительно 75 до приблизительно 25 мас.% второго растворителя.
Эксперименты с использованием одного бензилового спирта в качестве растворителя привели в результате к контролю размера микрочастиц по данным определения путем обследования содержимого резервуара для остановки реакции с помощью оптической микроскопии. Однако после высушивания в результате было обнаружено в целом низкое качество. Часто извлечение было затруднено вследствие прилипания. Также имелась тенденция к подъему остатков растворителя. Использование системы растворителя из этилацетата и бензилового спирта для дисперсной или масляной фазы улучшало качество микрочастиц и характеристики высвобождения.
Смесь растворителя настоящего изобретения предпочтительно представляет собой смесь, по меньшей мере, двух из следующих веществ: сложный эфир, спирт и кетон. Предпочтительные сложные эфиры имеют структуру R1COOR2, где R1 и R2 независимо отобраны из группы, состоящей из алкиловых частей, имеющих от 1 до 4 атомов углерода, т.е. метила, этила, пропила, бутила и их изомеров. Наиболее предпочтительным сложным эфиром для использования в качестве компонента используемой в практике настоящего изобретения смеси растворителей является этилацетат.
Предпочтительные спирты имеют структуру R3СН2ОН, где R3 выбран из группы, состоящей из водорода, алкила, имеющего от 1 до 3 атомов углерода, и арила, имеющего от 6 до 10 атомов углерода. Более предпочтительно, чтобы R3 представлял собой арил. Наиболее предпочтительным спиртом для использования в качестве одного компонента смеси растворителей, применяемой в практике настоящего изобретения, является бензиловый спирт.
Предпочтительные кетоны имеют структуру R4COR5, где R4 выбран из группы, состоящей из алкиловых частей, имеющих от 1 до 4 атомов углерода, т.е. метила, этила, пропила, бутила и их изомеров, a R5 выбран из группы, состоящей из алкиловых частей, имеющих от 2 до 4 атомов углерода, т.е. этила, пропила, бутила и их изомеров. Наиболее предпочтительным кетоном для использования в качестве одного компонента смеси растворителей, применяемой в практике настоящего изобретения, является метилэтилкетон.
Материал полимерной матрицы микрочастиц, полученных с помощью способа настоящего изобретения, является биосовместимым и биодеградируемым. Материал матрицы должен быть биодеградируемым в том смысле, что он должен распадаться под влиянием процессов в организме на продукты, легко выводимые организмом, и не должен накапливаться в организме. Продукты биодеградации также должны быть биосовместимыми с организмом, как и любой остаточный растворитель, который может остаться в микрочастицах.
Предпочтительные примеры материалов полимерной матрицы включают поли(гликолевую кислоту), поли(D,L-молочную кислоту), поли(L-молочную кислоту), сополимеры указанных веществ и им подобные. В способе настоящего изобретения могут использоваться различные имеющиеся в продаже поли(лактидные-со-гликолидные) материалы (PLGA). Например, поли(D,L-молочная-со-гликоливая кислота) имеется в продаже у Medisorb Technologies International L.P., например 50: 50 поли(D, L-молочная-со-гликоливая кислота), известная как MEDISORB® 50:50 DL. Этот продукт имеет состав (в мол. %): 50% лактида и 50% гликолида. Другими подходящими имеющимися в продаже продуктами являются MEDISORB® 65: 35 DL, 75:25 DL, 85:15 DL и пoли(D,L-мoлoчнaя кислота) (D,L-ПMK). Поли(лактид-со-гликолиды) также имеются в продаже у Boehringer Ingelheim, например PLGA 50:50 (Resomer® RG 502), PLGA 75:25 (Resomer® RG 752) и d,l-PLA (Resomer® RG 206), и у Birmingham Polymers. Эти сополимеры имеются в широком диапазоне молекулярной массы и соотношений молочной кислоты и гликолевой кислоты.
Самым предпочтительным полимером для использования в практике этого изобретения является сополимер поли(D,L-лактид-со-гликолид). Предпочтительно, чтобы молярное соотношение лактида и гликолида в таком сополимере было в диапазоне от приблизительно 85:15 до приблизительно 35:65, более конкретно от приблизительно 75:25 до приблизительно 50:50, например 85:15, 75:25, 65: 35 или 50:50.
Следует понимать, что проблема, на которую нацелен способ настоящего изобретения, заключается в нежелательно низкой устойчивости при хранении, вызванной действием активного вещества на полимер матрицы, в котором растворитель или, по меньшей мере, один из растворителей смеси растворителей, используемых в производстве микрочастиц, остается в достаточной концентрации в конечном продукте для усиления разлагающего взаимодействия между активным веществом и полимером. Эта проблема, например, наблюдается при использовании активного вещества, имеющего основную часть, такую как рисперидон, и матричный полимер, который имеет группу или связь, восприимчивую к катализируемому основанием гидролизу. Однако специалисты в этой области легко поймут, что концепция настоящего изобретения шире, чем описанная проблема устойчивости при хранении, и скорее направлена на более общее решение проблемы промывания продуктов, имеющих остатки определенного вязкого растворителя, отмывающей жидкостью, включающей воду и водорастворимый растворитель для вязкого растворителя (растворителей) в продукте.
Определенное значение имеет молекулярная масса материала полимерной матрицы. Молекулярная масса должна быть достаточно высокой для обеспечения образования удовлетворительного полимерного покрытия, т.е. полимер должен быть хорошим образователем пленки. Обычно удовлетворительная молекулярная масса находится в диапазоне от 5,000 до 500,000 дальтон, предпочтительно от 50,000 до 400,000, более предпочтительно, от 100,000 до 300,000, особенно от 100,000 до 200,000 и, в частности, приблизительно 150,000 дальтон. Однако поскольку свойства пленки также частично зависят от конкретного используемого материала полимерной матрицы частиц, то очень трудно определить диапазон молекулярной массы, соответствующий всем полимерам. Молекулярная масса полимера также важна с точки зрения ее влияния на скорость биодеградации полимера.
Для диффузионного механизма высвобождения препарата полимер должен оставаться интактным до тех пор, пока весь препарат не высвободится из микрочастиц, и затем распадаться. Препарат может также высвобождаться из микрочастиц по мере биологического распада полимерного наполнителя. С помощью соответствующего отбора полимерных материалов может быть изготовлена композиция в виде микрочастиц, в которой полученные в результате микрочастицы проявляют как свойства диффузионного высвобождения, так и биодеградационного высвобождения. Это может использоваться при достижении типов многофазного высвобождения.
Специалистам в данной области будет понятно, что удаление остаточного растворителя с помощью этапа промывания настоящего изобретения может оказывать воздействие на скорость высвобождения препарата, причем это влияние может быть или вредным, или благоприятным, в зависимости от обстоятельств. Например, когда остаточный растворитель действует в качестве пластификатора для матричного полимера, может наблюдаться снижение температуры стеклования, возможно, ускоряющее таким образом скорость высвобождения активного вещества. Если в данной ситуации желательна более высокая скорость высвобождения, этот результат будет благоприятным. Однако, если скорость становится достаточно высокой для того, чтобы отрицательно воздействовать на желаемое действие активного вещества на пациента, обязанностью лица, составляющего композицию, будет использование средств для уменьшения возросшей скорости высвобождения. При необходимости такие модификации способа находятся в пределах возможностей рядовых специалистов в соответствующих областях и могут осуществляться без излишнего экспериментирования.
Композиция, полученная с помощью способа настоящего изобретения, содержит активное вещество, диспергированное в полимерном матричном материале в виде микрочастиц. Количество такого вещества, включенного в микрочастицы, обычно находится в диапазоне от приблизительно 1 до приблизительно 90 мас.%, предпочтительно от 30 до 50 мас.%, более предпочтительно от 35 до 40 мас.%. Под мас. % подразумевается масса вещества в процентах от общей массы микрочастиц. Например, 10 мас.% вещества может означать 10 частей вещества и 90 частей полимера по массе.
При реализации способа настоящего изобретения, когда это включает образование микрочастиц, инкапсулирующий полимер должен по существу быть на 100% растворен в растворителе или смеси растворителей во время эмульсификации раствора. Активное вещество может быть диспергировано или растворено в растворителе или смеси растворителей во время, когда его добавляют в среду обработки непрерывной фазы. Содержание обычно твердого материала (активное вещество плюс инкапсулирующий полимер) в смеси растворителей во время его первой эмульсификации должно быть, по меньшей мере, 5 мас.%, а предпочтительно, по меньшей мере, 20 мас.%. Сведение к минимуму содержания растворителя в дисперсной или масляной фазе обеспечивает микрочастицы лучшего качества и требует меньшего количества экстракционной среды.
Предпочтительными активными веществами, которые могут инкапсулироваться с помощью способа настоящего изобретения, являются те, которые включают, по меньшей мере, одну основную часть, например третичную аминогруппу. Особенно предпочтительными активными веществами, которые могут инкапсулироваться с помощью способа настоящего изобретения, являются 1,2-бензазолы, более конкретно 3-пиперидинилзамещенные 1,2-бензизосксазолы и 1,2-бензизотиазолы. Наиболее предпочтительными активными веществами этого вида для лечения с помощью способа настоящего изобретения являются 3-[2-[4-(фтор-1,2-бензисоксазол-3-ил)-1-пиперидинил] этил] -6,7,8,9-тетрагидро-2-метил-4Н-пиридо[1,2-а] пиримидин-4-он (рисперидон) и 3-[2-[4-(фтор-1,2-бензисоксазол-3-ил)-1-пиперидинил] этил] -6,7,8,9-тетрагидро-9-гидрокси-2-метил-4Н-пиридо[1,2-a] пиримидин-4-он (9-гидроксирисперидон) и их фармацевтически приемлемые соли. Наиболее предпочтителен рисперидон (используемое здесь название которого предназначено для включения его фармацевтически приемлемых солей).
Другие биологически активные вещества, которые могут применяться с использованием способа настоящего изобретения, включают желудочно-кишечные терапевтические средства, такие как гидроокись алюминия, карбонат кальция, карбонат магния, карбонат натрия и им подобные; нестероидные противозачаточные средства; парасимпатомиметические средства; психотерапевтические средства, такие как галоперидол, бромперидол, флюфеназин, сулпирид, карпипрамин, клокапрамин, мосапрамин, оланзепин и сертиндол; большие транквилизаторы, такие как хлорпромазин НСl, клозапин, мезоридазин, метиапин, резерпин, тиоридазин и им подобные; малые транквилизаторы, такие как хлордиазэпоксид, диазепам, мепробамат, темазепам и им подобные; ринологические противоотечные средства; седативно-снотворные средства, такие как кодеин, фенобарбитал, фенобарбитал натрий, секобарбитал натрий и им подобные; стероиды, такие как тестостерон и тестостерон пропионат; сульфониламиды; симпатомиметические средства; вакцины; витамины и питательные вещества, такие как незаменимые аминокислоты; незаменимые жиры и им подобные; противомалярийные средства, такие как 4-аминохинолины, 8-аминохинолины, пириметамин и им подобные; средства против мигрени, такие как мазиндол, фентермин, сумматриптан и им подобные; средства против паркинсонизма, такие как L-допа; спазмолитические средства, такие как атропин, метскополамин бромид и им подобные; спазмолитические и антихолинергические средства, такие как желчная терапия, средства, способствующие пищеварению, ферменты и им подобные; средства против кашля, такие как декстрометорфан, носкапин и им подобные; бронхолитические средства; сердечно-сосудистые средства, такие как гипотензивные соединения, алкалоиды раувольфии, коронарные сосудорасширяющие средства, нитроглицерин, органические нитраты, пентаэритритотетранитрат и им подобные; электролитные заместители, такие как хлорид калия; алкалоиды спорыньи, такие как эрготамин с кофеином и без него, гидрогенизированные алкалоиды спорыньи, дигидроэргокристин метансульфат, дигидроэргокристин метансульфонат, дигидроэргокроиптин метансульфат и их комбинации; алкалоиды, такие как атропин сульфат, красавка, гиосцин гидробромид и им подобные; анальгетические средства; наркотические средства, такие как кодеин, дигидрокодиенон, меперидин, морфин и им подобные; ненаркотические средства, такие как салицилаты, аспирин, ацетоминофен, d-пропоксифен и им подобные; антибиотики, такие как цефалоспорины, хлорамфеникол, гентамицин, канамицин А, канамицин В, пенициллины, ампициллин, стрептомицин А, антимицин А, хлоропамтениол, метромидазол, окситетрациклин, пенициллин G, тетрациклины и им подобные; противораковые средства; противосудорожные средства, такие как мефенитоин, фенобарбитал, триметадион; противорвотные средства, такие как тиэтилперазин; антигистаминные средства, такие как хлорфиназин, дименгидринат, дифенгидрамин перфеназин, трипеленнамин и им подобные; противовоспалительные средства, такие как гормональные средства, гидрокортизон, преднизолон, негормональные средства, аллопуринол, аспирин, индометацин, фенилбутазон и им подобные; простагландины; цитотоксические препараты, такие как тиотепа, хлорамбуцил, циклофосфамид, мелфалан, азотистый иприт, метотрексат и им подобные; антигены таких микроорганизмов, как Neisseria gonorrhea, Mycobacterium tuberculosis, вирус Herpes (Humonis, типы 1 и 2), Candida albicans, Candida tropicalis, Trichomonas vaginalis, Haemophilus vaginalis, Streptococcus ecoli группы В, Micoplasma hominis, Hemophylus ducreyi, Granuloma inguinale, Lymphopathia venereum, Treponema pallidum, Brucella abortus, Brucella melitensis, Brucella suis, Brucella canis, Campylobacter fetus, Campylobacter fetus intestinalis, Leptospira роmоnа, Listeria monocytogenes, Brucella ovis, вирус 1 лошадиного герпеса, вирус лошадиного артериита, вирус IBR-IBP, вирус BVD-MB, Chlamydia psittaci, Trichomonas foetus, Toxoplasma gondii, Escherichia coli, Actinobacillus equuli, Salmonella abortus ovis, Salmonella abortus equi, Pseudomonas aeruginosa, Corynebacterium equi, Corynobacterium pyrogenes, Actinobacillus seminis, Mycoplasma bovigenitalium, Aspergillus fumigatus, Absidia ramosa, Trypanosoma equiperdum, Babesia caballi, Clostridium tetani и им подобных; антитела, противодействующие указанным выше микроорганизмам, и ферменты, такие как рибонуклеаза, нейрамидиназа, трипсин, гликоген фосфорилаза, молочная дегидрогеназа спермы, гиалуронидаза спермы, аденозинтрифосфатаза, щелочная фосфатаза, щелочная фосфатаза эстераза, аминопептидаза, трипсин, химотрипсин, амилаза, мурамидаза, акросомальная протеиназа, диэстераза, дегидрогеназа глутаминовой кислоты, дегидрогеназа янтарной кислоты, бета-гликофосфатаза, липаза, АТФаза, альфа-пептат-гамма-глутамилотранспептидаза, стерол-3-бета-ол-дегидрогеназа и ДФН-ди-апрораза.
Другие подходящие активные вещества включают эстрогены, такие как диэтилстильбестрол, 17-бета-эстрадиол, эстрон, этинилэстрадиол, местранол и им подобные; прогестины, такие как норэтиндрон, норгестрил, этинодиол диацетат, линеэстренол, медроксипрогестерон ацетат, диместистерон, мегестрол ацетат, хлормадинон ацетат, норгестимат, норэтистерон, этистерон, меленгестрол, норэтинодрел и им подобные, и спермицидные соединения, такие как нонилфеноксиполиоксиэтилен гликоль, бензетоний хлорид, хлоринданол и им подобные.
Еще одни микромолекулярные биологически активные вещества, которые могут быть выбраны для включения, включают факторы свертываемости крови, гемопоэтические факторы, цитокины, интерлейкины, колониестимулирующие факторы, факторы роста и их аналоги и фрагменты, но не ограничиваются ими.
Микрочастицы могут смешиваться по размеру или по типу с тем, чтобы обеспечить доставку активного вещества пациенту многофазным образом и/или образом, доставляющим пациенту различные активные вещества в различное время или смесь активных веществ в одно и то же время. Например, вторичные антибиотики, вакцины или любое желаемое активное вещество или в форме микрочастиц, или в обычной неинкапсулированной форме может смешиваться с первичным активным веществом и доставляться пациенту.
Смесь ингредиентов в системе растворителя дисперсной или масляной фазы эмульсифицирована в обрабатывающей среде непрерывной фазы, причем среда непрерывной фазы такова, что дисперсия микрочастиц, содержащих указанные ингредиенты, образуется в среде непрерывной фазы.
Хотя это и не является абсолютно необходимым, предпочтительно насыщать обрабатывающую среду непрерывной фазы, по меньшей мере, одним из растворителей, образующих систему растворителя непрерывной или масляной фазы. Это представляет устойчивую эмульсию, предотвращающую транспорт растворителя из микрочастиц перед остановкой реакции. Аналогичным образом, как и в патенте США 4389330, может применяться вакуум. Когда компонентами системы растворителя являются этилацетат и бензиловый спирт, водная или непрерывная фаза эмульсии предпочтительно содержит от 1 до 8 мас.% этилацетата и от 1 до 4 мас.% бензилового спирта.
Обычно для предотвращения агломерации микрочастиц растворителя и для контроля размера микрокапелек растворителя в эмульсии в обрабатывающую среду добавляют сурфактант или гидрофильный коллоид. Примеры соединений, которые могут
использоваться в качестве сурфактантов или гидрофильных коллоидов, включают, но не ограничиваются ими: поли(виниловый спирт), карбоксиметилцеллюлозу, желатин, поли(винилпирролидон), Tween® 80, Tween® 20 и им подобные. Концентрация сурфактанта или гидрофильного коллоида в обрабатывающей среде должна быть достаточной для стабилизации эмульсии и влияния на конечный размер микрочастиц. В целом, концентрация сурфактанта или гидрофильного коллоида в обрабатывающей среде будет от приблизительно 0,1 до приблизительно 10 мас. % на основании обрабатывающей среды, в зависимости от используемых сурфактанта или гидрофильного коллоида, системы растворителя дисперсной или масляной фазы и обрабатывающей среды. Предпочтительной комбинацией диспергирующей среды является от 0,1 до 10 мас.%, более предпочтительно, от 0,5 до 2 мас.%, раствор поли(винилового спирта) в воде.
Эмульсия может образовываться с помощью механического перемешивания смешанных фаз или с помощью добавления мелких капель дисперсной фазы, которая содержит активное вещество и образующий стенки материал, в обрабатывающую среду непрерывной фазы. Температура во время образования эмульсии не имеет особого принципиального значения, но может повлиять на размер и качество микрочастиц и растворимость активного вещества в непрерывной фазе. Конечно, желательно иметь в непрерывной фазе насколько возможно меньше активного вещества. Более того, в зависимости от применяемой смеси растворителей и обрабатывающей среды непрерывной фазы, температура не должна быть слишком низкой, иначе растворитель и обрабатывающая среда могут быть твердыми или стать слишком вязкими для практических целей. С другой стороны, она не должна быть настолько высокой, чтобы обрабатывающая среда испарялась, или такой, что не будет поддерживаться жидкая обрабатывающая среда. Более того, температура эмульсии не может быть настолько высокой, чтобы неблагоприятно воздействовать на устойчивость активного вещества в виде частиц, включенного в микрочастицы. Соответственно процесс диспергирования может проводиться при любой температуре, которая сохраняет устойчивые условия работы, предпочтительно от приблизительно 20oС до приблизительно 60oС, в зависимости от отобранного активного вещества и наполнителя.
Как указано выше, с целью создания микрочастиц, содержащих активное вещество, комбинируются органическая или масляная (дисперсная) фаза и водная фаза. Органическая и водная фазы являются в значительной степени или по существу не смешиваемыми, причем водная фаза составляет непрерывную фазу эмульсии. Органическая фаза включает активное вещество, а также образующий стенки полимер, т.е. материал полимерной матрицы. Органическую фазу получают путем растворения или диспергирования активного вещества (веществ) в системе органического растворителя. Органическая фаза и водная фаза предпочтительно комбинируются под воздействием средства для смешивания, предпочтительно статического миксера. Предпочтительно комбинированные органическая и водная фазы прокачиваются через статический миксер для образования эмульсии, включающей микрочастицы, содержащие активное вещество, инкапсулированное в материал полимерной матрицы, и затем в большой объем охлаждающей жидкости для прекращения реакции с целью получения микрочастиц, содержащих активное вещество, инкапсулированное в материал полимерной матрицы. Предпочтительно микрочастицы затем перемешиваются в контейнере, содержащем раствор для остановки реакции с целью удаления большей части органического растворителя из микрочастиц, что приводит к образованию отвердевших микрочастиц. Особенно предпочтительный способ смешивания статическим миксером раскрыт Ramstack et al. в патенте WO 95/13799.
Одним из преимуществ использования статического миксера является то, что может производиться точное и надежное масштабирование от размеров лабораторных до промышленных партий при достижении в то же время узкого и хорошо определенного распределения размеров микрочастиц, содержащих биологически или фармацевтически активные вещества. Еще одно преимущество этого способа состоит в том, что одно и то же оборудование может использоваться для образования микрочастиц, содержащих активные вещества точно определенного распределения по размерам для различных размеров партий. В дополнение к улучшению технологии способа статические миксеры требуют небольшого объема технического обслуживания и ремонта и занимают меньше места, чем динамические миксеры, у них меньше энергетическая потребность и они требуют сравнительно низких инвестиционных затрат.
После перемещения микрочастиц из статического миксера и вхождения в резервуар для остановки реакции обрабатывающая среда непрерывной фазы разбавляется и большая часть растворителя в микрочастицах удаляется путем экстракции. На этом этапе экстрактивной остановки реакции микрочастицы могут суспендироваться в той же обрабатывающей среде непрерывной фазы, использовавшейся во время эмульсификации, с гидрофильным коллоидом или сурфактантом или без них, или в другой жидкости. Экстракционная среда удаляет значительную часть растворителя из микрочастиц, но не растворяет их. Во время экстракции экстракционная среда, содержащая разведенный растворитель, может необязательно удаляться и замещаться свежей экстракционной средой.
После завершения этапа остановки реакции микрочастицы могут выделяться, как описано выше, а затем, по желанию, могут высушиваться под воздействием воздуха или с помощью других обычных методик высушивания, таких как вакуумная сушка, сушка над осушителем или им подобных. Этот способ очень эффективен при инкапсуляции активного вещества, поскольку могут быть получены основные загрузки, достигающие приблизительно 80 мас.%, предпочтительно до приблизительно 50 мас.%.
Когда для образования капелек органической или масляной фазы в эмульсии используется смесь растворителей, один из растворителей в смеси растворителей будет экстрагироваться на этапе остановки реакции более быстро, чем другой растворитель, например, первый растворитель, этилацетат, в случае предпочтительной смеси этилацетат/бензиловый спирт. Таким образом, задерживаются большие остатки второго растворителя (в данном случае бензилового спирта). Благодаря высокой точке кипения бензилового спирта его не легко удалить с помощью воздействия на микрочастицы воздуха или других обычных выпаривающих средств. Для повышения эффективности этой процедуры в среду экстрактивной остановки реакции перед добавлением эмульсии может добавляться какой-либо из более быстро экстрагируемых растворителей. Концентрация более быстро экстрагируемого растворителя в среде экстрактивной остановки реакции составляет от приблизительно 20 до приблизительно 70% точки насыщения растворителя в среде при температуре, которую предполагается использовать для экстракции. Таким образом, когда в охлаждающую жидкость для прекращения реакции добавляется эмульсия, экстракция более быстро экстрагируемого растворителя замедляется, а большая часть второго, медленнее экстрагируемого растворителя, удаляется.
Точное максимальное количество этого более быстро экстрагируемого растворителя, добавляемого в охлаждающую жидкость для прекращения реакции, имеет важное значение для окончательного качества микрочастиц. Слишком большое количество растворителя (т. е. близкое к точке насыщения) приводит к образованию пористых микрочастиц с видимым на поверхности активным веществом, вызывая то, что может быть нежелательно высокой скоростью высвобождения. Слишком маленькое количество растворителя в среде для остановки реакции приводит к высокому остаточному уровню более медленно экстрагируемого растворителя и низкому качеству микрочастиц. Температура среды для остановки реакции также важна, поскольку она воздействует на растворимость и скорость экстракции растворителя.
Можно подобрать и температуру, и максимальное количество растворителя для благоприятного влияния на желательные характеристики конечного продукта, т.е. высокопористые микрочастицы с быстрым высвобождением или микрочастицы с медленным высвобождением, имеющие низкую пористость.
Охлаждающая жидкость для прекращения реакции может быть простой водой, водным раствором или другой подходящей жидкостью, объем, количество и тип которой зависят от растворителей, используемых в эмульсионной фазе. Предпочтительно охлаждающая жидкость для прекращения реакции представляет собой воду. В целом, объем охлаждающей жидкости для прекращения реакции приблизительно в 10 раз выше насыщенного объема (т.е. в 10 раз больше объема для остановки реакции, необходимого для полного поглощения объема растворителя в эмульсии). Однако в зависимости от системы растворителя объем охлаждающей жидкости для прекращения реакции может варьироваться, превышая в от приблизительно 2 до приблизительно 20 раз насыщенный объем. Целесообразно, кроме того, описать потребность в объеме охлаждающей жидкости для прекращения реакции относительно размера партии (продукта в виде микрочастиц). Это соотношение представляет собой показание эффективности этапа экстракции и, в некоторых случаях, диктует размер партии для данного комплекта оборудования. Чем большее соотношение, тем больший объем требуется на массу продукта. С другой стороны, при меньшем соотношении из того же количества объема охлаждающей жидкости для прекращения реакции может быть получено больше продукта. Это соотношение может варьироваться от приблизительно 0,1 до приблизительно 10 л объема охлаждающей жидкости для прекращения реакции на 1 г полученных микрочастиц. Предпочтительны способы с соотношением менее чем приблизительно 1 л на 1 г.
При использовании предпочтительной комбинации растворителей бензилового спирта и этилацетата, как представляется, содержание этилацетата в охлаждающей жидкости для прекращения реакции воздействует на остаточный уровень растворителя в микрочастицах продукта. При низком содержании этилацетата в охлаждающей жидкости для прекращения реакции остатки бензилового спирта высоки, в то время как этилацетат может быть почти не выявляемым. При высоком содержании этилацетата в охлаждающей жидкости для прекращения реакции микрочастицами может удерживаться больше этилацетата, чем бензилового спирта. При объеме охлаждающей жидкости для прекращения реакции, составляющем приблизительно 1 л на 1 г активного вещества и подвергающегося охлаждению полимерного инкапсулирующего материала, оптимальное содержание этилацетата в охлаждающей жидкости для прекращения реакции составляет приблизительно 2-4 мас.% при 0-10oС.
После этапа прекращения реакции микрочастицы выделяются из водного охлаждающего раствора для прекращения реакции с помощью любого удобного средства отделения - жидкость можно слить из микрочастиц или суспензию микрочастиц можно профильтровать с использованием, например, ситчатой колонны. По желанию можно использовать различные другие комбинации методик отделения. Предпочтительна фильтрация.
Затем отфильтрованные микрочастицы подвергаются этапу промывания настоящего изобретения для дальнейшего снижения в них уровня остаточного растворителя (растворителей), предпочтительно до уровня в диапазоне от приблизительно 0,2 до 2,0%. На практике было установлено, что в случае использования предпочтительного двойного растворителя из этилацетата/бензилового спирта без этапа промывания настоящего изобретения уровни остаточного бензилового спирта в целом еще находятся в диапазоне от 4 до 8%. Как представляется, этот уровень остаточного растворителя в микрочастицах достаточен для ускорения процесса распада, что снижает таким образом устойчивость при хранении. Распад микрочастиц может, например, происходить путем нежелательного гидролиза гидролизуемых связей матричного полимера основным активным веществом. Таким образом, этап (этапы) промывания настоящего изобретения применяются для снижения содержания остаточного бензилового спирта или другого растворителя в микрочастицах для задержки процесса распада.
Как указано выше, раствор для промывания включает или одну воду или предпочтительно воду и смешиваемый с ней растворитель, который также является хорошим растворителем для остаточного растворителя в микрочастицах. В случаях, когда как и в предпочтительном способе настоящего изобретения, остаточным растворителем является бензиловый спирт, для использования в промывающем растворе предпочтительны С1-С4 алифатические спирты. Этими спиртами являются метанол, этанол, пропанол, бутанол и их изомеры. Наиболее предпочтительным спиртом является этанол.
Концентрация спирта в промывном растворе может варьироваться в зависимости от конкретных обстоятельств. В целом, спирт будет составлять менее 50 мас. % с нижним пределом, составляющим приблизительно 5%. Таким образом, предпочтительный диапазон для концентрации спирта обычно будет составлять от приблизительно 5 до приблизительно 50 мас.%. Более предпочтительно концентрация будет находиться в диапазоне от приблизительно 15 до приблизительно 30%.
Температура промывного раствора также важна для эффективности этапа промывания. В целом, повышение температуры уменьшит время, необходимое для промывания с целью снижения содержания остающегося растворителя до желаемого уровня.
С другой стороны, слишком высокая температура может оказывать повреждающее воздействие в том, что можно приблизиться или превзойти температуру размягчения полимера матрицы микрочастиц, вызывая тем самым образование комков или слипание. Напротив, слишком низкая температура может вызвать чрезмерное затвердевание материала матрицы, замедляя таким образом скорость, с которой могут экстрагироваться остатки, посредством чего способ может стать неприемлемо дорогим. Было установлено, что удобным и эффективным является диапазон температуры от приблизительно 5oС до приблизительно 40oС. Предпочтительно, используемая температура будет охватывать комнатную температуру, т. е. от приблизительно 10oС до приблизительно 30oС. Когда в качестве промывающего растворителя используется только вода, она будет применяться при повышенной температуре, т. е. выше комнатной температуры, предпочтительно в диапазоне от приблизительно 25oС до приблизительно 40oС, наиболее предпочтительно приблизительно при 37oС.
Обычно будет желательно применять более одного этапа промывания, как правило, два или три. После каждого такого этапа микрочастицы будут отделяться из промывного раствора с помощью хорошо известных средств отделения, например фильтрации, декантации, центрифугирования и им подобных. Предпочтительна фильтрация.
После каждого этапа отделения микрочастицы могут по желанию полностью или частично высушиваться с использованием обычных средств сушки при температуре, по существу аналогичной температуре раствора предшествующего промывания. Было установлено, что особенно применимым и удобным является применение сухого сжатого воздуха при температуре в диапазоне от приблизительно 10oС до приблизительно 30oС, что и является предпочтительным.
Продукт в виде микрочастиц обычно составлен из частиц сферической формы, хотя иногда микрочастицы могут иметь неравномерную форму. Микрочастицы могут варьироваться по размеру в диапазоне диаметра от субмикрона до миллиметра. Предпочтительно получают микрочастицы размером от 1 до 500 мкм, более предпочтительно от 25 до 180 мкм, в результате чего введение микрочастиц пациенту может осуществляться иглой стандартного калибра.
Предпочтительно загруженные препаратом микрочастицы отпускаются пациентам в виде однократного введения, высвобождая препарат в организме пациента постоянным или пульсирующим образом и устраняя необходимость в повторных инъекциях.
Микрочастицы, содержащие активное вещество, получаются и хранятся в качестве сухого материала. Перед введением пациенту сухие микрочастицы могут суспендироваться в приемлемом фармацевтическом жидком носителе, таком как 2,5 мас.% раствор карбоксиметилцеллюлозы, после чего суспензия инъецируется в тело.
Микрочастицы могут смешиваться по размеру или по типу с тем, чтобы обеспечить доставку активного вещества пациенту многофазным образом и/или образом, обеспечивающим доставку различных активных веществ пациенту в различное время или смеси активных веществ в одно и то же время. Например, вторичные антибиотики, вакцины или любое желаемое активное вещество или в форме микрочастиц, или в обычной, неинкапсулированной форме, может смешиваться с первичным активным веществом и вводиться пациенту.
Для тех материалов, у которых нет групп, оказывающих повреждающее воздействие на целостность полимера матрицы, дополнительный этап (этапы) промывания настоящего изобретения могут оказаться благоприятными в таких аспектах, как контроль характеристик высвобождения активного вещества in vivo или уменьшение содержания нежелательного или, возможно, вредного растворителя.
Теперь изобретение будет далее проиллюстрировано следующими неограничивающими примерами со ссылкой на сопровождающие чертежи, в которых:
фиг.1 представляет собой график, показывающий снижение уровней бензилового спирта в конечном продукте как функцию концентрации этанола (5%, 15%, 20%, 25%) в растворе для промывания, содержащем этанол : воду;
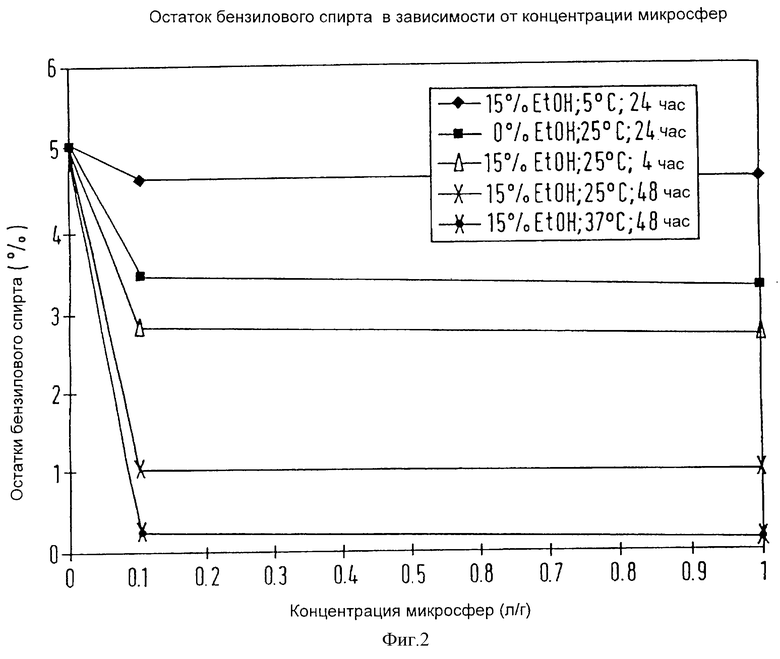
фиг. 2 представляет собой график, показывающий воздействие концентрации микрочастиц на уровень остаточного бензилового спирта (БС) в конечном продукте;
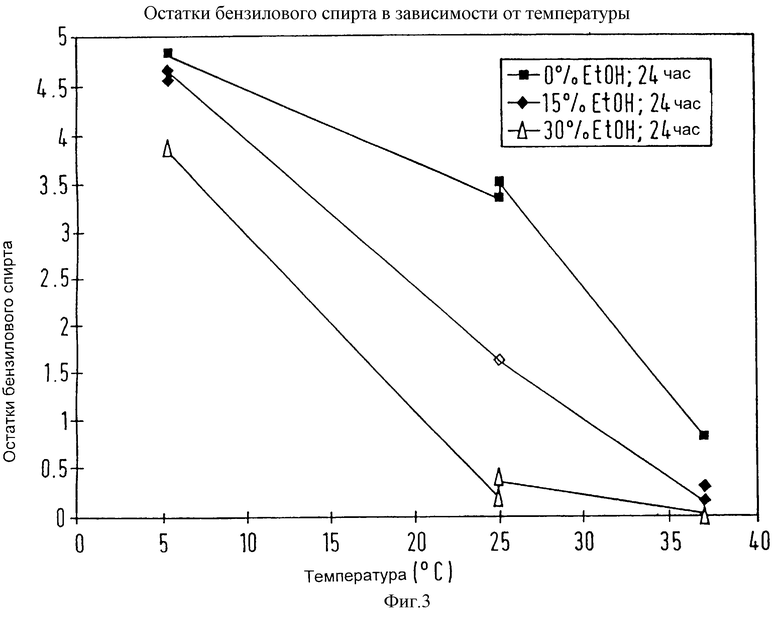
фиг. 3 представляет собой график, показывающий воздействие температуры этапа промывания на уровень остаточного бензилового спирта (БС) в конечном продукте, и
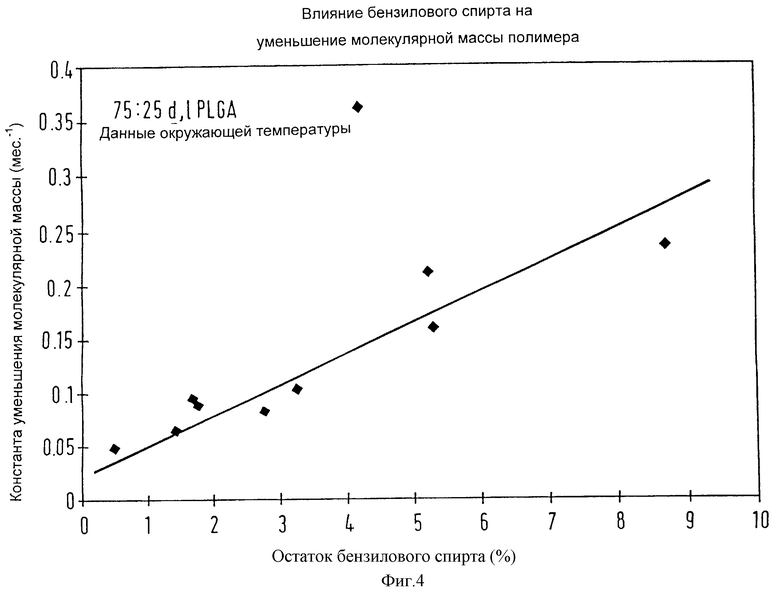
фиг.4 представляет собой график, показывающий влияние уровня остаточного растворителя (бензилового спирта) на снижение молекулярной массы полимерной матрицы.
Пример 1.
При обычной партии 125 г 75 г лактидно-гликолевого сополимера (75:25) Medisorb® и 50 г рисперидона растворяют в 275 г бензилового спирта и 900,25 г этилацетата в качестве органической фазы. Водная фаза включает 90,9 г поливинилового спирта, 8910 г воды, 646,4 г этилацетата и 298,3 г бензилового спирта. Органическую и водную фазы прокачивают через статический миксер для образования эмульсии. Полученную в результате эмульсию пропускают в охлаждающую жидкость для прекращения реакции, содержащую 17 кг воды, 4487,8 г этилацетата, 371,0 г карбоната натрия и 294,0 г бикарбоната натрия. Через 20 ч приблизительно при 10oС полученные в результате микросферы затем фильтруют и промывают первым промывающим раствором, содержащим 11,25 кг этанола и 33,75 кг воды, в течение 2 ч при 10oС. Затем микросферы фильтруют и промывают раствором, содержащим 11,25 кг этанола и 33,75 кг воды, в течение 6 ч при 25oС. Затем при 25oС в течение 1 ч на профильтрованный продукт подают третий раствор для промывания, содержащий 756 г лимонной кислоты, 482 г фосфата натрия и 45,0 кг воды. Затем продукт прополаскивают водой, фильтруют и высушивают. Три партии, произведенные в соответствии с этой процедурой, обеспечивают содержание рисперидона 37,4, 37,0 и 36,6 мас.%. Уровни бензилового спирта были 1,36, 1,26 и 1,38 мас.%. Уровни этилацетата были 0,09, 0,08 и 0,09 мас.%.
Пример 2.
Влияние способа промывания на характеристики микрочастиц.
Образец загруженных рисперидоном микросфер подвергают серии экспериментов с промыванием для определения воздействия на характеристики конечного продукта и выявления благоприятных условий промывания. Образец включал рисперидон, инкапсулированный в лактидно-гликолевом сополимере (75: 25) Medisorb®. Перед экспериментами с промыванием содержание препарата было 36,8 мас.%, а уровень бензилового спирта был приблизительно 5,2 мас.%. Микросферы переносят в среду для промывания, образцы удаляют через отобранные периоды времени и высушивают под вакуумом.
На фиг.1 показано снижение уровней бензилового спирта в конечном продукте как функция концентрации этанола (5%, 15%, 20% и 25%) в растворе для промывания, содержащем этанол/воду. Более высокие уровни этанола давали более низкое содержание остаточного бензилового спирта в конечном продукте.
Фиг.2 показывает, что в диапазоне от 0,1 до 1,0 л раствора на 1 г микросфер концентрация микросфер на этапе промывания не влияет на уровень остаточного бензилового спирта (БС) в конечном продукте.
На фиг. 3 показано воздействие температуры этапа промывания на уровень остаточного бензилового спирта в конечном продукте.
В таблице показано увеличение температуры стеклования (Tg) конечных микросфер по мере увеличения времени промывания и по мере увеличения концентрации этанола и снижения соответствующей концентрации бензилового спирта.
Загруженные рисперидоном микросферы с различными уровнями бензилового спирта были подвергнуты исследованиям устойчивости при комнатной температуре. На фиг. 4 показано, что на процесс распада, по данным измерения скорости гидролиза биодеградируемого, биосовместимого полимера, сильно влияет уровень остаточного растворителя в конечном продукте. Был построен график зависимости константы снижения молекулярной массы от остаточного уровня бензилового спирта для десяти различных образцов микросфер.
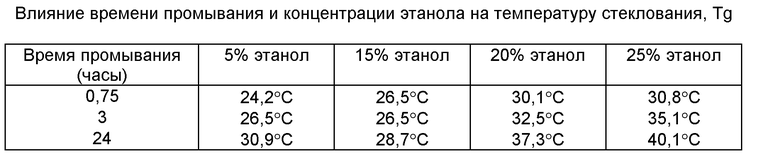
Изобретение используется в медицине. Микрочастицы включают биодеградируемую, биосовместимую полимерную матрицу с инкапсулированным активным веществом и остаточный органический растворитель. Активное вещество имеет ограниченную растворимость в воде. Органический растворитель является свободным от галогенированных углеводородов и выбран из спирта, линейного или циклического простого эфира, кетона и сложного эфира. Микрочастицы контактируют с водной системой, посредством чего содержание указанного органического растворителя в микрочастицах снижается до 2% или менее от массы микрочастиц. Водная система содержит воду и при контакте с микрочастицами имеет повышенную температуру от 25 до 40oС. Водная система может содержать воду и смешиваемый с водой растворитель - алифатический спирт С1-С4. Снижение уровня остаточного органического растворителя обеспечивает снижение скорости распада инкапсулированного в микрочастицах биологически активного вещества и повышение устойчивости продукта при хранении, а также снижение общей токсичности продукта и возможной канцерогенной активности. 5 с. и 14 з.п.ф-лы, 4 ил. , 1 табл.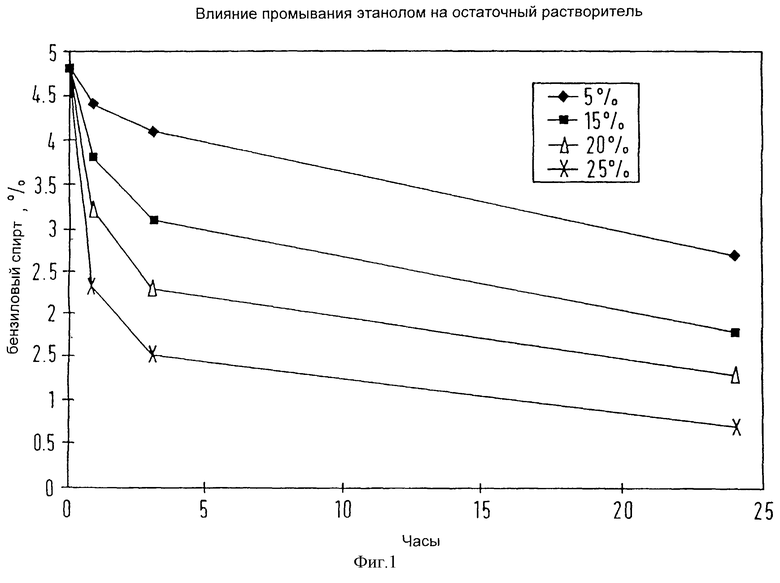
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| US 5478564 А, 26.12.1995 | |||
| US 4389330 А, 21.06.1983 | |||
| Металлический термостойкий упругофрикционный демпфер | 1977 |
|
SU669128A2 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| ПРОМЫШЛЕННЫЙ СПОСОБ ФОРМИРОВАНИЯ МИКРОЧАСТИЦ (ВАРИАНТЫ) И МИКРОЧАСТИЦЫ, ПОЛУЧЕННЫЕ ЭТИМ СПОСОБОМ (ВАРИАНТЫ) | 1996 |
|
RU2159148C2 |
Авторы
Даты
2003-03-27—Публикация
1997-05-06—Подача