Предлагаемое изобретение относится к медицине и может быть использовано для создания лекарственных средств (препаратов) и лечения ВИЧ-инфекции.
Уровень техники
Подходы к химиотерапии ВИЧ-инфекции, как известно, включают в себя ингибирование различных стадий репродукции ВИЧ (Фундаментальные и прикладные вопросы проблемы СПИД, М, 1988 г.).
Наиболее успешно развивающиеся из них стратегические направления химиотерапии связаны с подавлением функционирования обратной транскриптазы вируса аномальными нуклеозидами, т.е. модифицированными предшественниками нуклеиновых кислот. В связи с этим не случайно, что в настоящее время оба утвержденных для медицинской практики лекарственных препарата - азидотимидин (тимазид) и дидезоксиинозин относятся к классу предшественников нуклеиновых кислот. В то же время данное направление имеет ряд ограничений, среди которых на первом месте - корреляция антивирусного действия препаратов данного класса с их токсичностью, что существенно ограничивает лечение химиотерапевтическим воздействием. Относительно безопасными являются композиции на основе сериновых ингибиторов протеазы, подавляющие в зараженных клетках, в частности моноцитах, репликацию вируса (Патент РФ 2126266, 1999 г.) Однако их эффективность в клиническом плане не подтверждена.
В последние годы широкое распространение получили исследования по разработке препаратов на основе естественных дезоксирибонуклеиновой кислоты (ДНК) и рибонуклеиновой кислоты (РНК). Многие из них, как показывают предварительные испытания, обладают антивирусной и иммунотропной активностью (Патенты РФ 2136286, 1996 г., и 2137477, 1995 г.) Ряд препаратов, содержащих металлокомплексы ДНК, обнаружили активность и против вируса иммунодефицита человека (Патенты РФ 2108797, 1998, 2158592, 2000 г.). В то же время активность вышеуказанных препаратов исследована только в опытах "in vitro" и в настоящее время еще нет обнадеживающих сведений о том, какую активность будут проявлять те или иные препараты на основе ДНК в условиях жизнедеятельности организма.
Ряд исследований по изучению препаратов, содержащих модифицированную РНК, выявили также их противовирусную направленность, в том числе у некоторых препаратов против вирусов иммунодефицита человека (ЕР 0213921, 1987 г.). Так, эта активность установлена для гибрида ДНК-РНК, полученного способом, описанным в патенте РФ 2108796 от 1998 г.
В то же время есть данные, свидетельствующие о том, что токсичность препаратов на основе нуклеиновых кислот в значительной степени определяется содержанием в них РНК (В.И. Масычева В.И. и др. Журнал Антибиотики, 1986, 5, стр. 374-378). Это, возможно, и объясняет тот факт, что до последнего времени не существовало препарата на основе ДНК или РНК, за исключением первых ДНК-вакцин, допущенных к клиническим испытаниям в терапии СПИДа (Медицинские новости, 1998, 5, стр. 30-31).
Приходится констатировать также, что нет определенной точки зрения на то, как конкретно связаны те или иные физико-химические свойства препаратов на основе нуклеиновых кислот с их биологической, в частности, противовирусной, особенно селективной вирусной активностью, при введении препарата "in vivo" и это затрудняет целенаправленный синтез препаратов.
Таким образом, в настоящее время препаратов и способов для эффективного лечения ВИЧ-инфекции чрезвычайно мало. Применяемые в настоящее время для лечения ВИЧ-инфекции препараты и способы лечения имеют основной недостаток - низкую эффективность лечения ВИЧ-инфекции.
В качестве прототипа заявленному способу может быть принят способ лечения ВИЧ-инфекции, заключающийся по крайней мере во введении в организм человека лекарственного средства, обладающего вирусоподавляющим действием, например тимазида (Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А - Механотерапия, 608 с.).
Основным недостатком прототипа является низкая эффективность лечения ВИЧ-инфекции и высокая токсичность.
Сущность изобретения
Известно, разрешено к применению лекарственное средство (лекарственный препарат) натрия нуклеоспермат (см. Временную фармакопейную статью ВФС 42-2566-95, введенную в действие с 27 октября 1995 года). Лекарственное средство (лекарственный препарат) имеет сложную биологически активную основу, представляющую собой смесь натриевых солей полихлоргидратов дериватов дезоксирибонуклеиновой и рибонуклеиновой кислот из молоки осетровых рыб с отношением азота к фосфору от 1.3 до 1.8 с молекулярной массой 66000-400000 Дальтон, причем более 90% действующего начала препарата составляет ДНК, а среди остальных - в фармакологически значимых количествах (до 6%) присутствует РНК. Натрия нуклеоспермат применяется в качестве гемостимулятора для лечения лейкопений, возникающих после стандартных химиотерапии или для предупреждения глубокой лейкопении при применении высоких доз цитостатиков. Отмечается при этом низкая токсичность препарата и отсутствие побочных последствий.
Кроме того, известен, разрешен к применению и хорошо зарекомендовал себя в клинической практике препарат - раствор натрия нуклеоспермата (см. Временную фармакопейную статью ВФС 42-2565-95, введенную в действие с 27 октября 1995 года), состоящий из натрия нуклеоспермата (1.5 г), натрия хлорида (0.1 г) и воды для инъекций (до 100 мл). Раствор натрия нуклеоспермата предназначен для коррекции последствий химиолучевой терапии, обладает свойством стимулировать лейкопоэз. Для этих целей его вводят по 75-150 мг в 5-10 мл 1,5% раствора подкожно (Патент РФ 2110995, 1998 г.).
Как выяснилось в дальнейшем, натрия нуклеоспермат обладает свойством репаративной регенерации тканей, что позволило на его основе создать средство для регенерации различных тканей организма человека (Патент РФ 2115424, 1999 г.) у больных с длительно незаживающими ранами или язвами.
Известен плазмозамещающий раствор для внутривенного введения, обладающий иммуномодулирующими и гемокоррегирующими свойствами (Патент РФ 2166944, 2001 г.). В описываемом плазмозамещающем растворе в качестве активного ингредиента, вызывающего стимуляцию гемопоэза, применено низкомолекулярное ДНК, которое характеризуется физико-химическими параметрами, поглощающими физико-химические параметры нуклеоспермата натрия. Т.е. вышеописанный плазмозамещающий раствор является, в частности, одной из лекарственных форм натрия нуклеоспермата, применяемых для стимуляции гемопоэза человека.
Известна лекарственная форма в виде липосомного фармацевтического препарата (Заявка на выдачу патента 95102712/14 от 23/02/95 г., положительное решение 139 НК/97 от 21/10/97 г.). В указанном препарате в качестве активной составляющей липосомы используется низкомолекулярная ДНК, которая характеризуется физико-химическими параметрами, поглощающими физико-химические параметры нуклеоспермата натрия. Т. е. вышеописанный липосомный фармацевтический препарат является, в частности, одной из лекарственных форм натрия нуклеоспермата, применяемых для стимуляции гемопоэза человека.
Известны энтеральные лекарственные формы, в частности назальная, представляющая из себя 0.25% р-р вышеупомянутой в данном описании натриевой соли ДНК, а также мягкие мазевые и свечевые лекарственные формы, включающие натриевую соль ДНК с вышеперечисленными физико-химическими характеристиками в качестве активного ингредиента (US Patent #5547684 August, 20, 1996).
В связи с выявлением новых свойств натрия нуклеоспермата его изучение было продолжено, при этом обнаружено, что натрия нуклеоспермат в чистом виде обладает свойством лечить (подавлять) ВИЧ-инфекцию как в опытах "in vitro", так и в ВИЧ-инфицированном организме (Статья "Надежды компас земной", еженедельник Московские новости 10, 6-12 марта 2001 года), при этом имеется корреляция активности препарата с его молекулярной массой.
Задачами изобретения являются:
А. Повышение эффективности лечения ВИЧ-инфекции за счет применения в качестве лекарственного средства (препарата) для лечения ВИЧ-инфекции известного лекарственного средства натрия нуклеоспермата.
Б. Сокращение расходов и времени на создание нового лекарственного препарата для лечения ВИЧ-инфекции и расширение номенклатуры лечебных препаратов для лечения ВИЧ-инфекции для дальнейшего их совместного применения.
Сущность изобретения заключается в:
1. Применении натрия нуклеоспермата в качестве средства (препарата) для лечения ВИЧ-инфекции или в качестве активного начала (составной части) лекарственного средства для лечения ВИЧ-инфекции.
Это обеспечит:
А. Повышение эффективности лечения ВИЧ-инфекции за счет применения в качестве лекарственного средства (препарата) для лечения ВИЧ-инфекции известного лекарственного средства натрия нуклеоспермата.
Б. Сокращение расходов и времени на создание нового лекарственного препарата для лечения ВИЧ-инфекции и расширение номенклатуры лечебных препаратов для лечения ВИЧ-инфекции для дальнейшего их совместного применения.
2. В разработке способа лечения ВИЧ-инфекции, включающего введение в организм человека лекарственного средства (препарата) и использовании при этом в качестве лекарственного средства или в качестве активного начала (составной части) лекарственного средства по крайней мере натрия нуклеоспермата.
Это обеспечит:
А. Повышение эффективности лечения ВИЧ-инфекции за счет применения в качестве лекарственного средства (препарата) для лечения ВИЧ-инфекции известного лекарственного средства натрия нуклеоспермата и использования новой методики его применения.
Б. Сокращение расходов и времени на создание нового лекарственного препарата для лечения ВИЧ-инфекции и расширение номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции для дальнейшего их совместного применения.
Как известно, натрия нуклеоспермат при традиционном парентеральном введении может вызывать тканевую и температурную реакцию. Эти реакции, с учетом клинических особенностей СПИДа, особенно нежелательны у таких пациентов. Изучение фармакокинетики препарата позволило предложить ректальный путь его введения. При этом возможно также использовать его традиционный 1,5% раствор, но разовую дозу препарата следует увеличить, например, до 20-50 мл. Такая лекарственная форма и способ ее введения обеспечивает удобство, простоту и безболезненность применения при той же точности дозирования. Препарат доставляется к местам необходимого воздействия эндолимфатическим путем транспорта его в большой круг кровообращения.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в качестве средства (препарата) для лечения ВИЧ-инфекции или в качестве активного начала (составной части) лекарственного средства для лечения ВИЧ-инфекции.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат с молекулярной массой от 66000 Дальтон до 320000 Дальтон.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат с молекулярной массой от 70000 Дальтон до 270000 Дальтон.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, натрия нуклеоспермат включает смесь натриевых солей дезоксирибонуклеиновой и рибонуклеиновой кислот, в которой отношение процентного весового содержания азота к процентному весовому содержанию фосфора в пересчете на сухое вещество составляет от 1.3 до 1.8.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат, включающий смесь натриевых солей полихлоргидратов дериватов дезоксирибонуклеиновой и рибонуклеиновой кислот, с гиперхромным эффектом от 33 до 47%, характеристической вязкостью от 1,55•102 до 3,25•102 мл/г, содержанием хлорид-иона в пересчете на сухое вещество от 7 до 13,5%, содержанием сульфатной золы от 0.001 до 30% по весу (по массе), содержанием тяжелых металлов в сульфатной золе от 0.000001 до 0,001%, содержанием белка от 0.001 до 1,5% в пересчете на сухое вещество, содержанием нуклеиновых кислот в пересчете на натрия дезоксирибонуклеат в пределах от 90 до 105% в пересчете на сухое вещество, содержанием дериватов рибонуклеиновых кислот в пересчете на натрия рибонуклеинат до 5% в пересчете на сухое вещество, содержанием этилового спирта от 0.00001 до 0,3% в пересчете на сухое вещество.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат совместно по крайней мере с одним противовирусным лекарственным средством, в частности тимазидом.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат совместно по крайней мере с одним лекарственным средством, подавляющим по крайней мере одну СПИД-ассоциируемую или оппортунистическую инфекцию, например герпетическую, в частности, с ридостином или зовираксом.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в сочетании или смеси по крайней мере с одним плазмозамещающим раствором, в частности полиглюкином, или макродексом, или декстраном, или интрадексом, или плазмодексом, или онковертином, или реополиглюкином, или реомакродексом, или ломодексом, или декстраном-40, или гемодексом.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в виде мягкой лекарственной формы или в качестве составляющей части (активного ингредиента) мягкой лекарственной формы, в частности мази, пасты, лиминента, суппозитория, например ректальных свечей.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в виде жидкой лекарственной формы или в качестве составляющей части (активного ингредиента) жидкой лекарственной формы, в частности раствора, суспензии, например стабилизированной суспензии наночастиц.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в виде раствора, в частности водного, включающего от 0,6 до 2 г натрия нуклеоспермата на 100 мл растворителя.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, применяют натрия нуклеоспермат в качестве активного ингредиента, связанного с молекулярным переносчиком через биологическую мембрану и элементом лекарственной формы замедленного высвобождения, в виде, например, липосом свободных или полимеризованных, в частности липосом с инкапсулированным натрия нуклеосперматом, окруженным фосфолипидным слоем (слоями) и с внешней оболочкой из полиэтиленгликоля и/или в качестве элемента конвенциональной липосомы, получаемой, в частности, из глицерил-фосфолипидов с замещением глицерола, например, рибозой, и являющейся основой карбоксилатного скелета; и/или в качестве элемента, связанного с пептидной или пептидоподобной (пептидное производное или моноклональное антитело, повторяющее пептид по свойствам) системой доставки по принципу рецепторно-опосредованного трансцитоза.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения ВИЧ-инфекции включает введение в организм человека лекарственного средства, в качестве которого или в качестве активного начала (составной части) которого используют по крайней мере натрия нуклеоспермат.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения ВИЧ-инфекции включает введение лекарственного средства в организм человека энтеральным путем, в частности ректально и/или назально; и/или парентеральным путем, в частности подкожно и/или внутримышечно и/или внутривенно и/или трансдермально.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что лекарственный препарат вводят в организм человека по крайней мере в виде мягкой лекарственной формы или в качестве составляющей части (активного ингредиента) мягкой лекарственной формы, в частности мази, пасты, лиминента, суппозитория, например ректальных свечей; и/или вводят в виде жидкой лекарственной формы или в качестве составляющей части жидкой лекарственной формы, в частности раствора, суспензии, например стабилизированной суспензии наночастиц.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что лекарственное средство вводят в организм человека в разовой дозе, включающей 10-50 мл 0,6-2% раствора натрия нуклеоспермата в воде (например, полуторапроцентный раствор натрия нуклеоспермата) или другом растворителе, фармацевтически приемлемом для организма человека.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что препарат, содержащий натрия нуклеоспермат вводят в организм человека ректально 2-3 раза в неделю по две разовые дозы в день, например утром и вечером, или с перерывом между введением в 5 - 12 часов.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что в организм человека дополнительно вводят по крайней мере одно лекарственное средство, например тимазид.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что натрия нуклеоспермат вводят в организм человека в форме активного ингредиента, связанного с молекулярным переносчиком через биологическую мембрану и элементом лекарственной формы замедленного высвобождения, в виде, например, липосом свободных или полимеризованных, в частности липосом с инкапсулированным натрия нуклеосперматом, окруженным фосфолипидным слоем (слоями) и с внешней оболочкой из полиэтиленгликоля и/или в качестве элемента конвенциональной липосомы, получаемой, в частности, из глицерил-фосфолипидов с замещением глицерола, например, рибозой, и являющейся основой карбоксилатного скелета; и/или в качестве элемента, связанного с пептидной или пептидоподобной (пептидное производное или моноклональное антитело, повторяющее пептид по свойствам) системой доставки по принципу рецепторно-опосредованного трансцитоза.
С целью повышения эффективности лечения ВИЧ-инфекции, расширения номенклатуры лечебных препаратов и методик лечения ВИЧ-инфекции, способ лечения заключается в том, что в организм человека вводят нуклеоспермат натрия в смеси с одним или более химическими веществами, не входящими в состав натрия нуклеоспермата, в количестве, не превышающем высшую разовую терапевтическую дозу для этих веществ, например натрий фосфорнокислый однозамещенный 2-водный в количестве 1,5-3,5% по весу от количества натрия нуклеоспермата и/или натрий фосфорнокислый двузамещенный 12-водный в количестве 2-4% по весу от количества натрия нуклеоспермата.
Под термином ВОДА понимается жидкость, основной частью которой является оксид водорода - Н2О. Вода - обязательный компонент практически всех технологических процессов как промышленного, так и сельскохозяйственного производства. Вода особой чистоты применяется в производстве продуктов питания, а также в медицине, новейших отраслях промышленности
Под термином ЛЕЧЕНИЕ понимается совокупность мероприятий, направленных на устранение страданий больного и восстановление его здоровья (См. стр. 542, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А - Механотерапия, 608 с.). Различают этиотропное, патогенетическое и симптоматическое лечение. Этиотропное лечение применяют в тех случаях, когда установлена причина, вызвавшая заболевание, и можно воздействовать на нее. Примером его является использование антибиотиков при пневмонии, специфической сыворотки при дифтерии или хинина при малярии, удаление инородного тела при ранении и др. (См. стр. 542, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А -Механотерапия, 608 с.). Этиотропная терапия, направленная на устранение причины заболевания, осуществляется в основном с помощью химиотерапевтических лекарственных средств, подавляющих жизнедеятельность возбудителей инфекционных заболеваний (См. стр. 534, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999. -Т. 1, А - Механотерапия, 608 с.). Патогенетическое лечение - лечебные методы, воздействующие на патогенез заболевания в целом или на отдельные его звенья. Патогенетическое лечение может быть направлено на восстановление нарушенных в результате заболевания функций органов и систем (См. стр. 542, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А-Механотерапия, 608 с.).
Под термином ЛЕКАРСТВЕННЫЕ СРЕДСТВА понимаются химические вещества природного или синтетического происхождения, или сочетания веществ, употребляемые для лечения, предупреждения и диагностики заболеваний человека и животных (См. стр.534. Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999. -Т. 1, А - Механотерапия, 608 с.).
Под термином ЛЕКАРСТВЕННЫЕ ФОРМЫ понимаются удобные для применения и хранения состояния лекарственных средств или лекарственного растительного сырья, обеспечивающие оптимальное лечебное действие (См. стр. 535, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А - Механотерапия, 608 с).
Под термином ИНФЕКЦИЯ (позднелат. Infectio заражение) понимается внедрение в организм и размножение в нем микробов с последующим развитием различных форм их взаимодействия - от носительства возбудителей до клинически выраженной болезни. Процесс, развивающийся в организме в результате внедрения в него патогенного возбудителя, принято называть инфекционным процессом (См. стр. 422, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999. -Т. 1, А - Механотерапия, 608 с.).
Под термином ВИЧ-инфекция понимается инфекционная болезнь, развивающаяся в результате многолетнего персистирования в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (ВИЧ) и характеризующаяся медленно прогрессирующим дефектом имунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (СПИД), или от подострого энцефалита (См. стр. 137, Краткая медицинская энциклопедия: В 2т./ Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А - Механотерапия, 608 с.).
Под термином ДОЗА (греч. Dosis порция) понимается доза, назначаемая на один прием, называется разовой, а принимаемая в течение суток - суточной. В ряде случаев устанавливаются дозы на весь курс лечения - курсовые дозы. Минимальная доза, в которой лекарственное средство оказывает лечебное действие, обозначается как минимальная терапевтическая доза, а наибольшая допустимая доза - как высшая терапевтическая доза. Различают высшие разовые и высшие суточные дозы. В практике чаще всего используют средние терапевтические дозы (См. стр. 338, Краткая медицинская энциклопедия: В 2 т. / Под ред. Академика РАМН В.И. Покровского. - М.: НПО "Медицинская энциклопедия", 1999.-Т. 1, А - Механотерапия, 608 с.).
Таким образом, поставленная цель изобретения достигается.
Патентоспособность изобретений была оценена в соответствии с требованиями "Правил составления, подачи и рассмотрения заявки на выдачу патента на изобретение". Автор при разработке изобретений не обнаружил сведений о применении и способах применения натрия нуклеоспермата для лечения ВИЧ-инфекции.
Сведения, подтверждающие возможность осуществления изобретения.
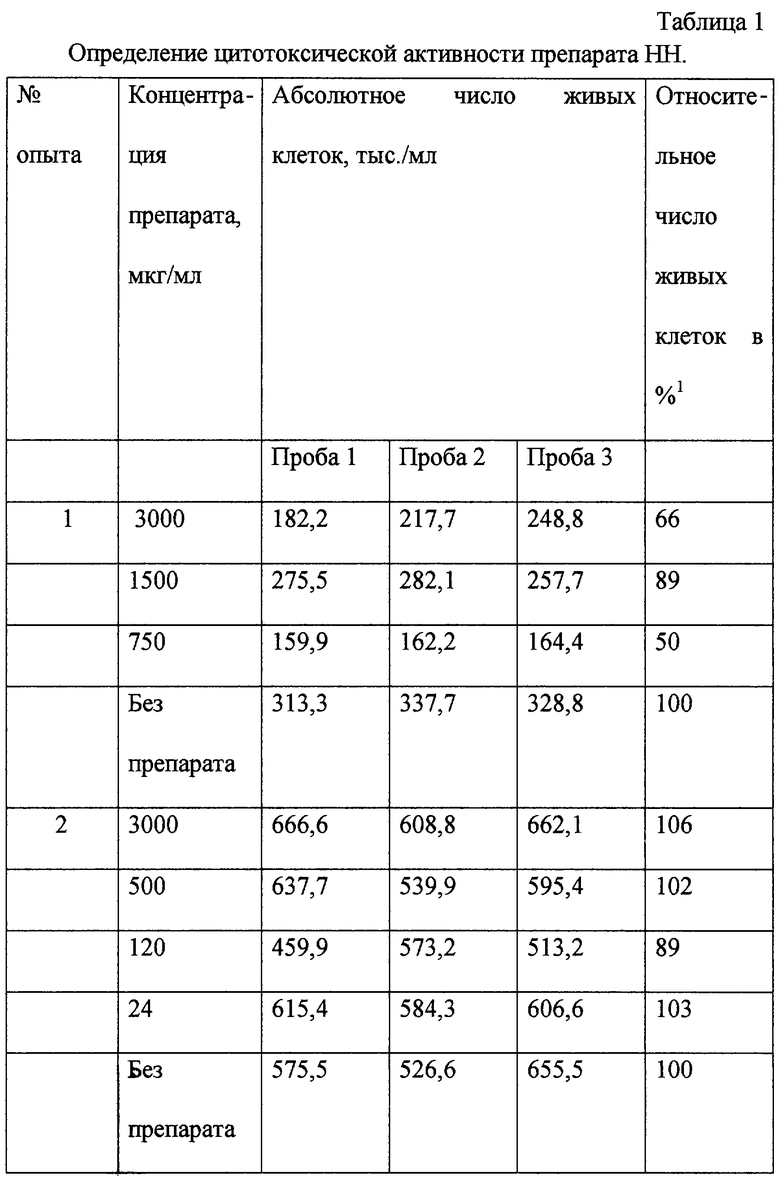
Испытание "раствора натрия нуклеоспермата" (далее раствора НН) в качестве препарата для лечения ВИЧ-инфекции проводились в два этапа. На первом этапе исследовалась цитотоксическая активность препарата, на втором этапе - специфическая противовирусная активность. В работе использовалась перевиваемая линия человеческих Т-клеток МТ-4, характеризующаяся высокой чувствительностью к ВИЧ-1 и лабораторный штамм ВИЧ-1 IIIВ. На всех этапах работы проводилось сравнение действия препарата и азидотимидина.
Исследование цитотоксической активности препарата НН в отношении ВИЧ-инфекции
При исследовании цитотоксической активности препарата использовали 24-луночные культуральные плашки. Первый ряд плашек использовали для приготовления пяти- или двукратных разведении препарата. Разведения препаратов проводили в культуральной среде (КС) с 5% сывороткой эмбрионов коровы (СЭК) без антибиотика. Для каждого разведения использовали новую пипетку. В остальные лунки вносили по 0,8 мл клеточной взвеси с концентрацией 150-300 000 клеток/мл. Клетки предварительно отмывали 100-кратным объемом среды без гарамицина, разводили КС без антибиотика, подсчитывали концентрацию в камере Горяева и разливали по 0,8 мл взвеси в лунки 24-луночных плашек. Затем к клеткам добавляли по 0,2 мл препарата. Для каждого разведения использовали по три лунки. В три лунки вносили культуральную среду. Плашки помещали в термостат.
Через 3-4 дня проводили подсчет живых клеток в камере Горяева в присутствии трипанового синего. Испытания для каждого образца проводили трижды. Для каждого разведения препарата в каждом опыте определяли среднее значение процента жизнеспособности клеток. За 100 процентов принимали количество клеток в пробе без препарата. По точкам, полученным в трех независимых опытах, строили кривую зависимости жизнеспособности клеток от концентрации препарата в полулогарифмической шкале и по этой кривой определяли 50% токсическую дозу препарата. Количество клеток в пробах в день постановки опыта принималось за фоновое значение. Результаты 3 независимых опытов представлены в табл. 1. На основании полученных результатов была определена 50% цитотоксическая доза (ТД50) для данного препарата,
соответствующая такой его концентрации, которая на 50% снижает ростовые свойства клеток.
На основании полученных результатов можно сделать следующие выводы:
1. Препарат НН характеризуется низкой цитотоксической активностью на линии клеток МТ-4.
2. НН оказывается более чем в 1000 раз менее цитотоксичным, чем азидотимидин.
Исследования спецефической противовирусной активности препарата НН в отношении ВИЧ-инфекции
На втором этапе исследований изучалась противовирусная активность НН. В работе использовали перевиваемую Т-клеточную линию МТ-4, полученную от Prof. Robin Weiss, Chester Beatty Laboratories, The Institute of Cancer Research, London, United Kingdom). Ранее было показано, что данная линия клеток является высокочувствительной к ВИЧ-1 и может быть быть использована для тестирования противовирусных препаратов (Pauwels R., De Clercq E. et. al. Sensitive and rapid assay on MT-4 cells for detection of antiviral compaunds against the AIDS virus. J. Virol Meth. 1987; 16:171-185).
Для заражения клеток использовали стандартный лабораторный штамм ВИЧ-1 - IIIB (Gallo R.C. et al. Isolation of human T-cell leukemia virus in aquired immune deficiency syndrome (ADDS). Science 1983; 220:865-867) из музея вирусных культур НИИ вирусологии имени Д.И.Ивановского РАМН.
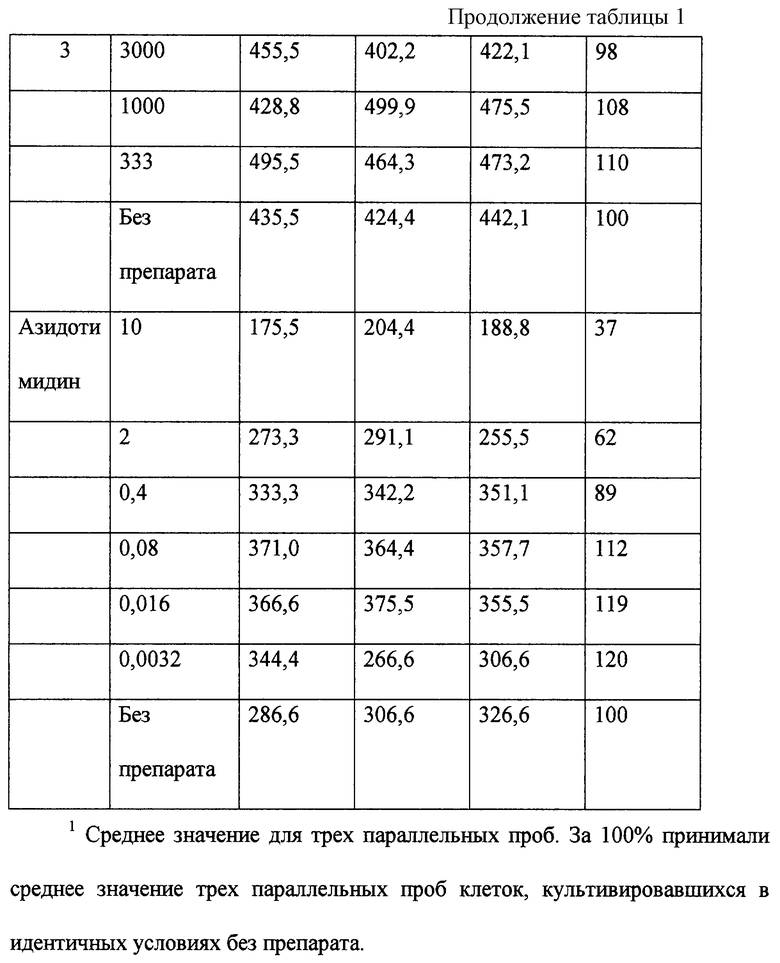
Исследование вирулицидного действия препарата НН
Исходная концентрация препарата составила 15 мг/мл.
К 0,2 мл образца препарата добавляли 0,1 мл вируссодержащей культуральной жидкости с титром 107 ИД50/мл (это соответствует 10 мг препарата и 3•l06ИД50 в 1 мл раствора), пробы инкубировали 15 мин при комнатной температуре, затем добавляли 0,7 мл культуральной среды и 0,1 мл раствора добавляли к 0,9 мл суспензии клеток МТ-4 с концентрацией 250000 клеток/мл. Таким образом, множественность инфекции составила 0,5 ИД50 на клетку.
Клетки культивировали в 24-луночных культуральных плашках при 37oС в присутствии 3% углекислого газа в течение 72 часов.
Для оценки результатов использовали метод, предложенный Pauwels R., De Clercq E. et. al. (Sensitive and rapid assay on MT-4 cells for detection of antiviral compaunds against the AIDS virus. J. Virol Meth 1987; 16:171-185). Суть метода заключается в том, что заражение клеток МТ-4 ВИЧ-1 приводит к их гибели. Если испытуемое соединение обладает противовирусным действием, то оно предотвращает их гибель. Поэтому антивирусное действие оценивают по увеличению количества живых клеток в культурах, зараженных вирусом, обработанным испытываемым соединением. В этом случае подсчитывают количество живых клеток в пробах (каждая проба включает по три параллельных образца) в камере Горяева в присутствии трипанового синего и затем определяют процент живых клеток, принимая за 100% количество клеток в пробе, не содержащей вируса.
Результаты данного испытания представлены в табл. 2.
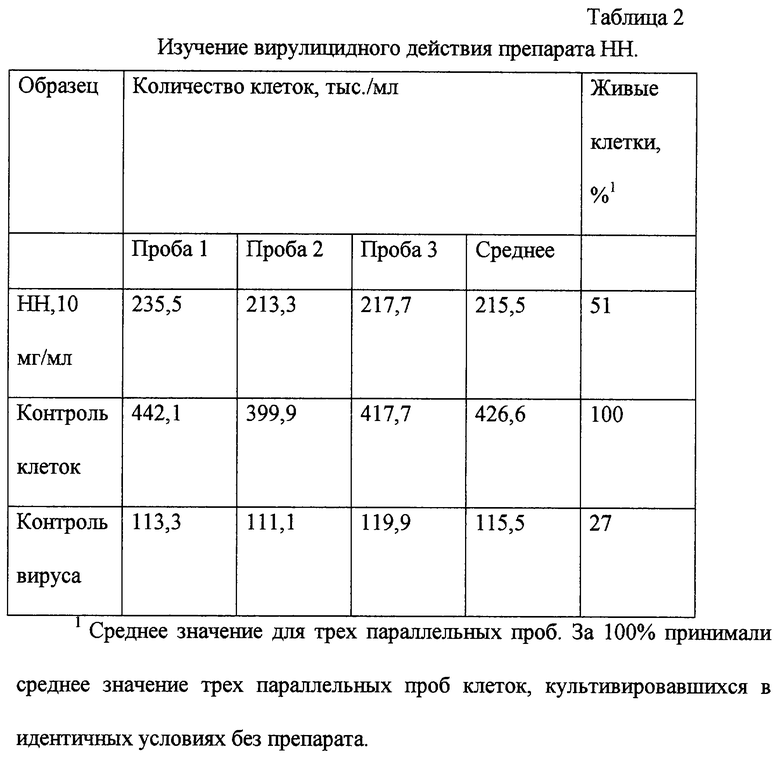
Изучение антирепликативного действия препарата НН
Клетки (500000 клеток/мл) по 1 мл вносили в лунки 24-луночных культуральных плашек, добавляли по 0,1 мл вируссодержащей культуральной жидкости. При этом инфекционные дозы составляли 0,01 ИД50/кл или 0,02 ИД50/клетку. Затем пробы инкубировали в термостате в стандартных условиях 2 часа и затем вносили по 0,3 мл препарата до конечной концентрации 3 мг/мл. Плашки помещали в термостат и учет результатов проводили через 96 часов по методике, указанной ранее. Результаты опыта представлены в табл. 3.
Из табл. 3 видно, при данных условиях эксперимента препарат НН проявляет противовирусную активность, сравнимую с активностью азидотимидина в концентрации 0,1 мкг/мл.
Таким образом, предварительный этап испытаний образцов препарата НН позволил сделать следующие выводы:
1. Препарат НН обладает противовирусной активностью, в частности, в концентрации 3 мг/мл.
2. Наибольший противовирусный эффект наблюдается при добавлении препарата только после того как пройдут, по крайней мере, ранние этапы инфекционного процесса - адсорбция и проникновение вирусных частиц в клетки.
На основании результатов, полученных на предварительном этапе испытаний, было проведено изучение противовирусной активности НН с использованием коммерческих тест-систем для определения содержания белка р24 ВИЧ-1 и РНК ВИЧ-1.
- VIRONOSTIKA HIV-1 ANTIGEN, microelisa system - ELISA (Organon Teknika, USA);
- AMPLICOR HIV-1 MONITOR Test Kit, version 1,5, ART:11 1048 9, US:87674, 24 теста, фирма Roche, USA.
Клетки МТ-4 ( 80-100 мл) через 24 или 48 часов после пересева осаждали при 500 об/мин в течение 7 мин, осадок промывали трижды ростовой культуральной средой без антибиотиков. Осадок клеток суспендировали в 5-7,5 мл среды в зависимости от исходной концентрации клеток, но так, чтобы их концентрация соответствовала 107 кл./мл, затем к ним добавляли 1/10 часть стандартной вируссодержащей культуральной жидкости в разведении 1:10. Таким образом, множественность инфекции составляла 0,01 ИД50/кл., и далее использовали один из следующих вариантов постановки опыта:
1. Клетки с вирусом помещали в термостат и инкубировали, помешивая каждые 15-20 мин. Через 90 мин клетки промывали три раза 100-кратным объемом свежей среды, чтобы избавиться от свободного, не проникшего в клетки вируса, затем разливали клетки в отдельные культуральные одноразовые пробирки, вносили препараты соответственно схеме испытаний и культивировали далее в термостате в стандартных условиях.
2. Клетки с вирусом разливали по 1 мл в культуральные пробирки объемом 15 мл, вносили препараты соответственно схеме опыта и помещали их в термостат для инкубации в стандартных условиях. Через 18 часов клетки каждой пробы отмывали три раза 100-кратным объемом культуральной среды, суспендировали их затем в свежей среде при соответствующей концентрации препарата по схеме опыта и помещали в термостат. Через 96 часов после заражения в обоих случаях клетки осаждали при 1000 об/мин 10 мин, отбирали надосадочную жидкость и использовали ее затем для оценки накопления в ней белка р24 ВИЧ-1. Часть проб использовали для дополнительного анализа накопления в них РНК ВИЧ-1. Каждая исследуемая точка включала по три параллельные пробы.
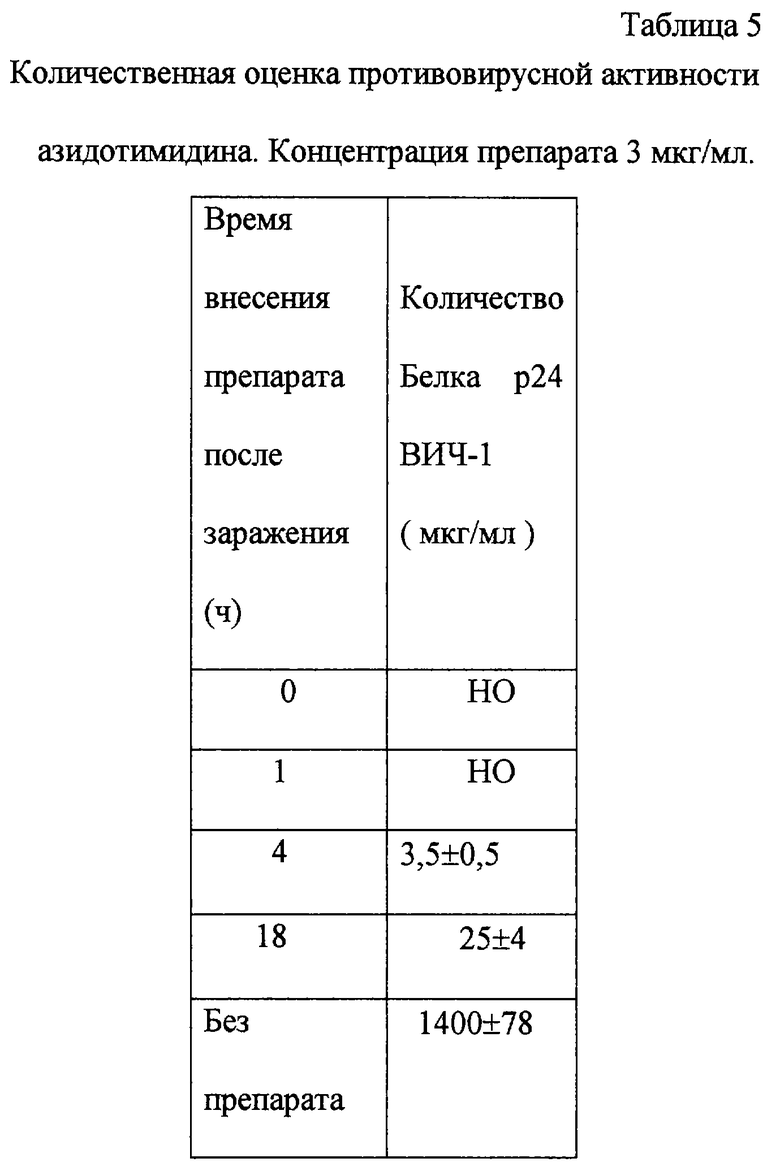
В первом опыте образец 1 препарата НН в конечной концентрации 3 мг/мл вносили через 0, 1, 4 и 18 часов после заражения клеток. При определении полуколичественной концентрации накопления белка р24 в пробах готовили их серийные десятикратные разведения. Для анализа использовали 0,1 мл каждого из полученных разведений. Полученные результаты представлены в табл. 4. Для сравнения в табл. 5 представлены результаты эксперимента с азидотимидином.
На основании полученных результатов можно сделать заключение о том, что наилучший противовирусный эффект наблюдается при добавлении препарата после того, как осуществятся такие этапы инфекционного процесса, как адсорбция вируса на поверхности клетки и слияние клеточной и вирусных мембран. Сходный противовирусный эффект обнаруживается и при добавлении вируса в более поздние этапы первого цикла инфекционного процесса и на этапе второго цикла инфекционного процесса (внесение препарата через 18 часов после заражения).
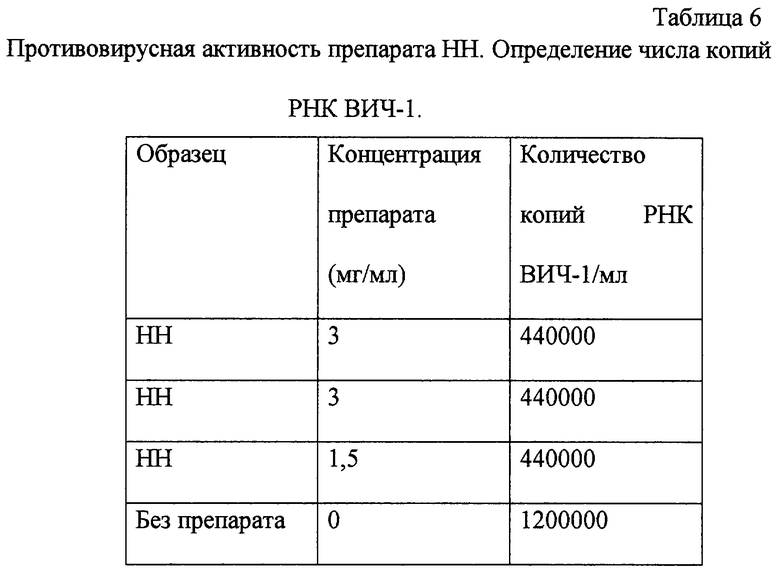
Культуральная жидкость проб из представленных выше опытов, в которых по показаниям р24 белка ВИЧ-1 наблюдалась наилучшая противовирусная активность, были изучены на наличие в них количества копий РНК с помощью тест системы AMPLICOR HIV-1 MONITOR. Результаты анализа представлены в табл. 6.
Из данных табл. 6 следует, что препарат, исследованный с помощью тест-системы AMPLICOR HIV-1 MONITOR, демонстрирует определенную противовирусную активность. Полученные данные согласуются с результатами определения р24 ВИЧ-1 и числа жизнеспособных клеток, представленными выше.
Таким образом, проведенные нами исследования "in vitro" в отношении ВИЧ показали наличие определенной противовирусной активности препарата, предложенного для тестирования. Суммируя данные определения числа жизнеспособных клеток, белка р24 ВИЧ-1 в культуральной жидкости, а также числа копий вирусспецифической РНК в культуральной среде, можно сделать вывод о том, что препарат НН оказывается способным подавлять репродукцию вируса ВИЧ-1 штамма IIIВ в чувствительных клетках МТ-4. При этом 50% -ная эффективная доза препарата находилась в пределах 0,9-2,1 мг/мл. Препарат обладает низкой цитотоксичностью. Расчетное значение ТД50 составило 15,85 мг/мл. Однако индекс селективности НН оказывается на два порядка меньше, чем индекс селективности азидотимидина. Необходимо также отметить, что наибольший противовирусный эффект достигался при внесении препарата только через некоторое время после заражения чувствительных клеток. В связи с этим можно предположить, что его противовирусное действие может происходить путем связывания с определенными сигнальными рецепторами на клеточной поверхности, вовлеченными в негативную регуляцию размножения вируса. Важно также подчеркнуть относительную нестабильность данного препарата при инкубации в культуральной жидкости, однако этот недостаток не представляется нам существенным, так низкая цитотоксичность препарата, по-видимому, позволит поддерживать достаточно высокие его концентрации в организме.
Результаты экспериментов при ректальном способе введения НН
Изучена фармакокинетика меченного тритием натрия нуклеоспермата (3H-HH) в крови мышей после однократного ректального введения препарата.
Учитывая специфику природы и химической структуры изучаемого препарата НН, разработка метода идентификации его в биологических субстратах проводилась в единственно возможном направлении: получение меченого НН путем введения в его структуру радиоизотопной метки.
Получение 3H-HH проводили с помощью метода термической активации трития. Для мечения использовали мишени двух типов. Сначала мишень готовили, нанося суспензию порошка НН в этаноле на стенки цилиндрического реакционого сосуда диаметром 7 см с вольфрамовой спиралью, расположенной вдоль реакционного сосуда. После замораживания жидким азотом этанол удаляли под вакуумом. Полученную мишень подвергали обработке атомарным тритием и растворяли в воде. Раствор НН замораживали и повторяли обработку атомарным тритием.
Для получения атомарного трития атомизатор - вольфрамовую проволоку - нагревали до 1900 К. Давление молекулярного трития в системе составляло 0,5 Па, что обеспечивало свободный пробег атомов трития от атомизатора до мишени. Каждые 10 с проводили обновление газовой фазы, вакуумируя реактор и напуская новую порцию трития. Во время реакции стенки сосуда с мишенью охлаждали жидким азотом.
Мечению подвергали три порции НН по 30 г каждая с различной молекулярной массой.
Начальная радиоактивность раствора составила 50 мКи. Раствор подвергали диализу в течение 2 суток в холодильнике. Затем провели очистку препарата: 3H-HH осадили, добавив ацетат аммония до 2М концентрации и 2 объема этанола. Выдержали 2 час при -20oС, затем после центрифугирования полученный осадок высушили и растворили в 3 мл воды. Провели 3 экстракции равными объемами смеси фенол-хлороформ (1:1) и одну экстракцию смесью хлороформ-изоамиловый спирт (24: 1) или многократной экстракцией смесью фенол-хлороформ. К водной фазе добавили ацетат аммония до 2М концентрации и 2 объема этанола, выдержали 2 мин и осадили 3H-HH центрифугированием. Осадок промыли 70% этанолом, высушили, взвесили и растворили в воде. Препарат 3H-HH анализировали с помощью аналитического агарозного гельэлектрофореза с бромистым этидием в сравнении с исходной НН и маркером λPStI. Меченная тритием НН была аналогична исходному препарату по набору фрагментов ДНК длиной от -300 до -500 п.о. с небольшой примесью -1200 п.о. до -3000 п.о.
В результате очистки общая радиоактивность препаративной смеси снизилась с ~ 50 до 7 мКи и вес очищенной НН для каждого из образцов составлял 2 г. Радиоактивность препарата на определенных стадиях очистки определяли на жидкостном сцинтилляционном счетчике "Mark" (Holland).
Эксперименты проводили на мышах-самцах линии ВДF1, весом 25 г. Для подтверждения зависимости скорости всасывания (биодоступности) препарата НН от его средней молекулярной массы наиболее демонстративными оказались эксперименты с использованием трех образцов препарата со средней ММ 70 КД, 150КД и 270 КД.
При ректальном введении каждый из 3 образцов препарата НН вводили однократно группам мышей по три животных в группе в дозе 150 мг (1,83x109 dpm)/Kг или 3,7 (4,57•107 dpm) на мышь в виде 3% водного раствора объемом 0,125 мл.
При ректальном способе введения препарата на анальное отверстие животных накладывали зажим, который снимали через 1 час. Содержание 3H-HH в слепой и толстой кишке определяли сразу после снятия зажима у каждой особи отдельно в группе из 3 животных. Пробы крови отбирали индивидуально у каждой мыши из интраорбитального синуса в объеме 50 мкл в группе из 3 животных через 0, 25; 0,5; 1, 3, 5 и 24 час после введения препарата.
Общую радиоактивность в биологических образцах (крови, сыворотке, форменных элементах, тканях, моче и фекалиях) определяли радиоизотопным методом после сжигания в азотной кислоте в соотношении 1:5 на кипящей водяной бане в течение 10-20 мин. Добавляли 0,1 мл полученного раствора во флаконы, содержащие 15 мл сцинтилляционной жидкости ЖС-8, и проводили радиометрические измерения на β-счетчике LKB (Швеция) "Wallac".
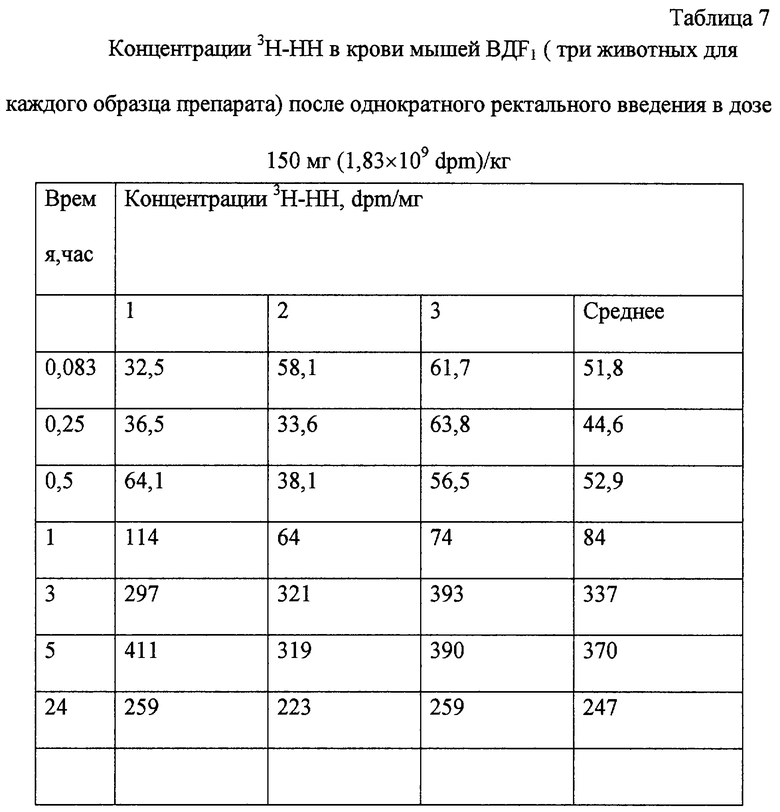
В табл. 7 представлена для примера фармакокинетика 3H-HH в крови 2-й группы мышей BДF1 после однократного ректального введения препарата в дозе 150 мг (1,83•109dрm)/кг.
Были получены индивидуальные, для 3 животных, фармакокинетически кривые, описывающие изменение концентрации 3H-соединений в крови для каждого из образцов препарата НН. Образцы крови у мышей отбирали из интраорбитального синуса в объеме 50 мкл. Как следует из экспериментальных данных, три индивидуальные кривые для одного образца препарата как качественно, так и количественно сходны по своим параметрам. В то же время, как видно из табл. 8, скорость процесса всасывания падает с увеличением молекулярной массы образца препарата НН.
В интервале времени 0-5 час происходит достаточно быстрое повышение концентрации 3H-HH в крови, когда скорость процесса всасывания превышает скорость элиминации. Затем, к 24 час, наблюдается фаза снижения уровня 3H-соединений, связанная с превалированием распределения препарата в органах и тканях и выведения 3H-соединений из организма животных. Таким образом, концентрация препарата в крови животных в максимальных точках и через сутки после введения близки по своим значениям.
В связи с тем, что у мышей отсутствует сфинктер, введение животным препарата ректально сопровождалось наложением на анальное отверстие зажима. Через 1 час после введения зажимы были сняты, и в слепой и толстой кишке (вместе с содержимым) было определено количество препарата, не всосавшегося к тому времени.
Из полученных данных выяснилось, что в слепой кишке определяется незначительное количество 3H-НН, а в толстой кишке - в среднем до 80% от введенной дозы.
Данные по выведению 3H-соединений с мочой и калом животных после однократного ректального введения 3H-НН показывают, что за 24 час с мочой и калом экскректируется около 64% от введенной дозы, с мочой 2,5%, с калом 61,5%.
Таким образом, анализируя в комплексе все полученные данные, можно сделать вывод о том, что препарат 3H-НН обладает способностью всасываться в толстой кишке животных. Не смотря на то, что зажим с ануса у мышей был снят через 1 час, часть препарата абсорбируется в прямой кишке животных и не выводится с калом одномоментно. Процесс всасывания продолжается длительное время: в течение 5 час скорость поступления 3H-НН в кровь мышей превышает скорость элиминации, отражающей процессы распределения 3H-НН в органах и тканях и выведения препарата и метаболитов из организма. Затем отмечается переход фармакокинетической кривой из фазы всасывания в фазу выведения.
Проведенные исследования позволили прийти к выводу, что препарат 3H-НН, введенный ректально, обладает биодоступностью для организма. В организм мышей при ректальном введении поступало от 40% от введенной дозы (для образца с ММ 70 КД) до 9,2% (для образца с ММ 270 КД). Из полученных экспериментальных данных следует, что для ректального введения предпочтительно использовать препарат НН с молекулярной массой в пределах до 270 КД, дальнейшее увеличение молекулярной массы препарата приводит к резкому падению его биодоступности, что в свою очередь делает его применение малоэффективным.
Клинические исследования вирусоподавляющей активности НН на группе ВИЧ-инфицированных добровольцев
Клинические исследования проводились в соответствии с разрешением Департамента государственного контроля качества, эффективности, безопасности лекарственных средств и медицинской техники Министерства здравоохранения РФ.
Согласно протоколу в исследовании участвовали 20 ВИЧ-инфицированных пациентов, составляющих 2 группы:
Группа П - 10 пациентов (основная группа):
- средний возраст пациентов составил 29,9 лет, в группе находились 2 женщины и 8 мужчин;
- срок инфицирования (давность установлентя диагноза) от 2-х до 14-ти лет, у 4-х - более 9-ти лет, у 6-х - более 2-х лет;
- путь инфицирования: 5 - внутривенный, 3 - гетеросексуальный путь, 1 - внутрибольничный, 1 - гомосексуальный путь.
Группа К - 10 пациентов (группа сравнения):
- средний возраст пациентов составил 22,8 лет, в группе состояли 4 женщины и 6 мужчин;
- срок инфицирования от 1-го до 10-ти лет, у 2-х более 3-х лет, у 7-х более 2-х лет, у 1-го более 10-ти лет;
путь инфицирования: 8 - внутривенный путь (наркоманы), 1 - гетеросексуальный путь, 1 - внутрибольничный.
Данное испытание проводилось на ВИЧ-инфицированных пациентах на стадиях A3, B1, B2, В3 при установленном диагнозе ВИЧ-инфекции методом ELISA и подтвержденном WESTERN BLOT.
К началу данного испытания:
В группе П наблюдались: генерализованная лимфоаденопатия у 8-ми пациентов, кандидоз ротоглотки у 4-х, дисбактериоз у 2-х, протеинурия у 2-х, увеличение щелочной фосфатазы у 8-ми, увеличение АЛТ/АСТ у 2-х, моноцитоз у 3-х, эозинофилия у 2-х, эритропения у 1-го, тромбоцитопения у 1-го пациента.
В группе К наблюдались: генерализованная лимфоаденопатия у 7-ми пациентов, кандидоз ротоглотки у 5-ти, протеинурия у 3-х, увеличение щелочной фосфатазы у 8-ми, увеличение АЛТ/АСТ у 2-х, эозинофилия у 2-х, эритропения у 1-го пациента.
Согласно утвержденному протоколу для лечения ВИЧ инфицированных пациентов была применена следующая схема терапии:
В группе П (основная группа) в течение 25 недель:
НН в 1,5% растворе 2-3 раза в неделю в дневной дозе до 50 мл ректально (2 раза по 25 мл в течение дня) + тимазид (по 200 мг 3 раза в день, перорально, ежедневно. Первые два месяца использовали НН с молекулярной массой 70-100 КД, следующие 2 месяца использовали НН с ММ 120-170 КД, последние два месяца использовали НН с ММ 220-320 КД. Молекулярная масса всех используемых в процессе лечения образцов препарата НН находилась в пределах, установленных фармакопейной статьей.
В группе К (группа сравнения) в течение 25 недель:
Тимазид по 200 мг 3 раза в день, перорально, ежедневно.
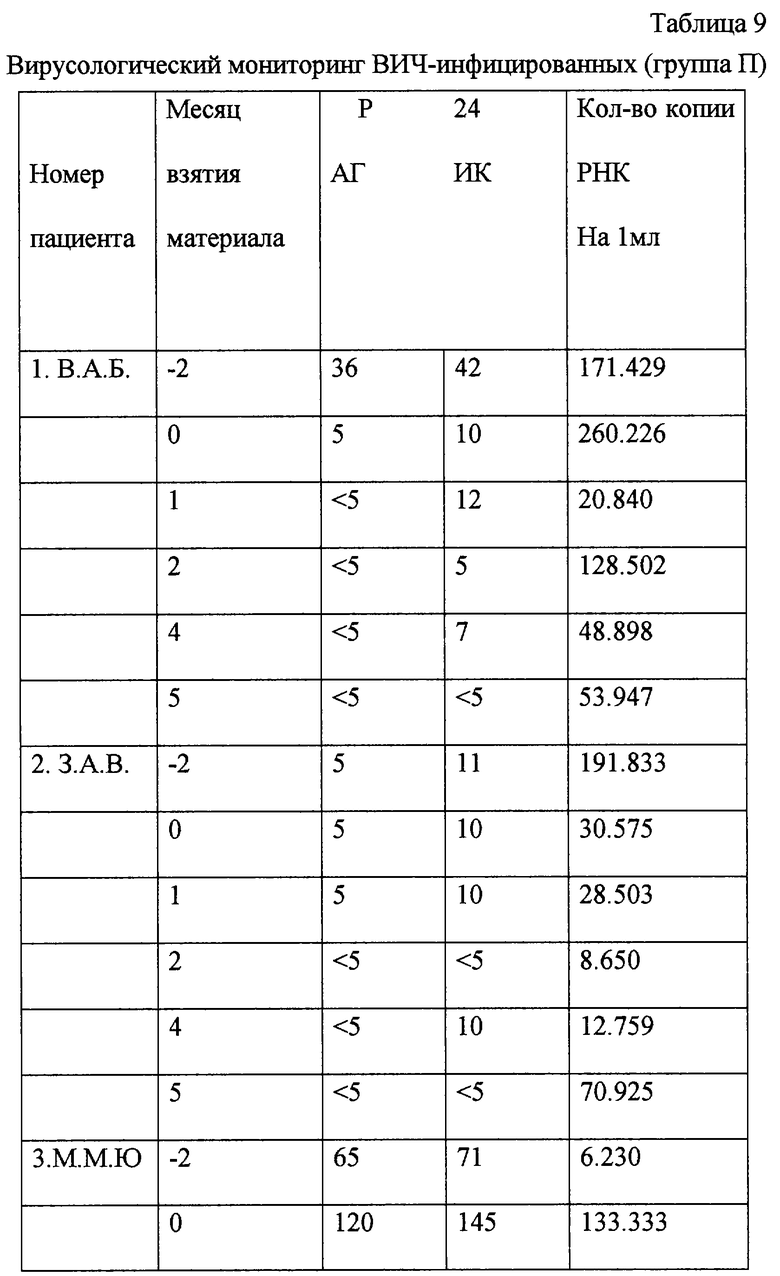
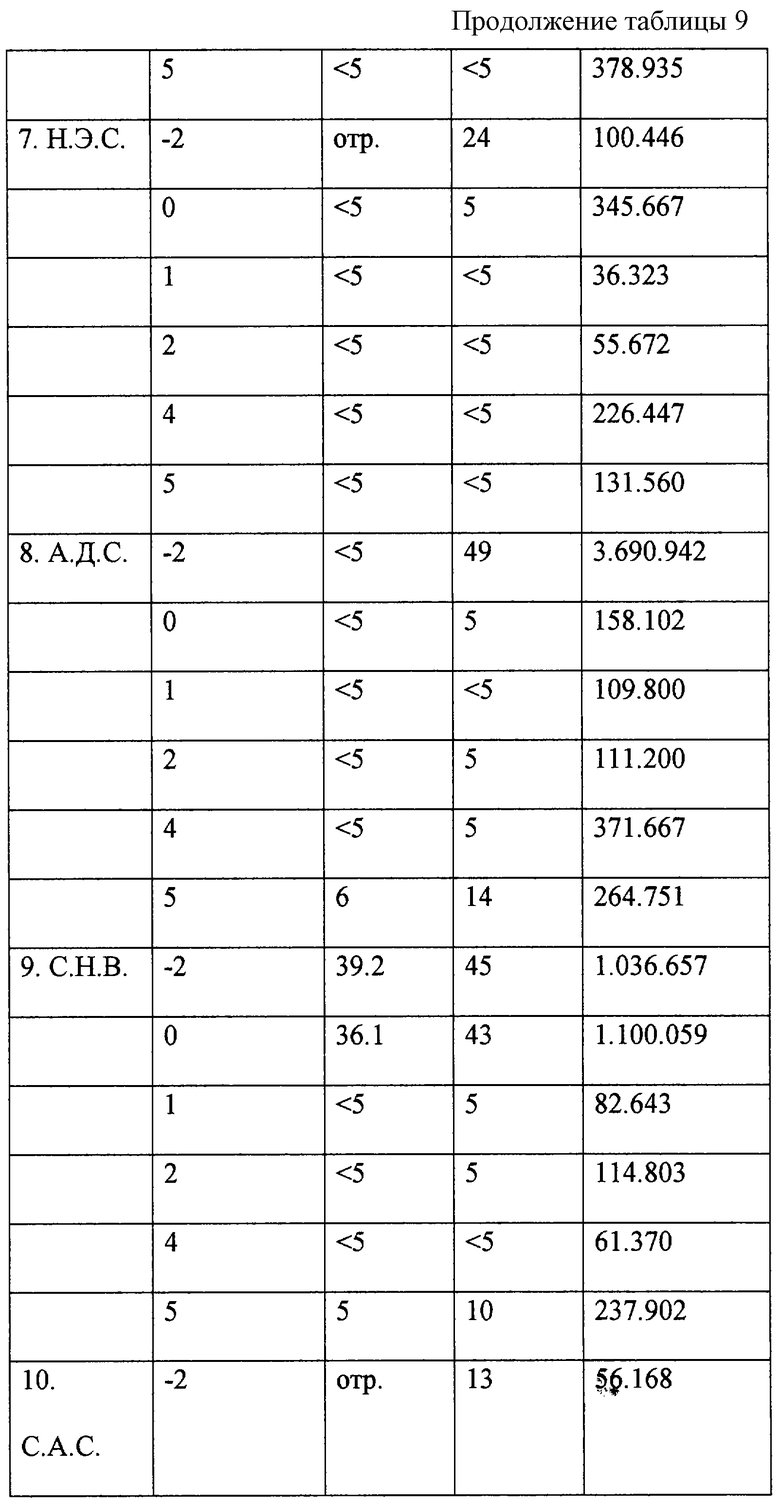
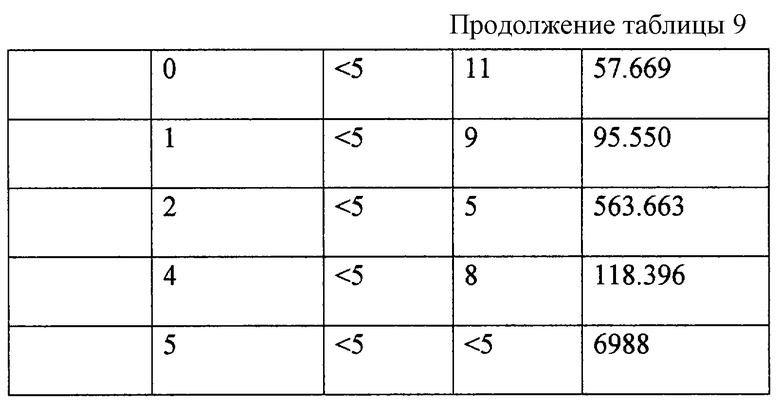
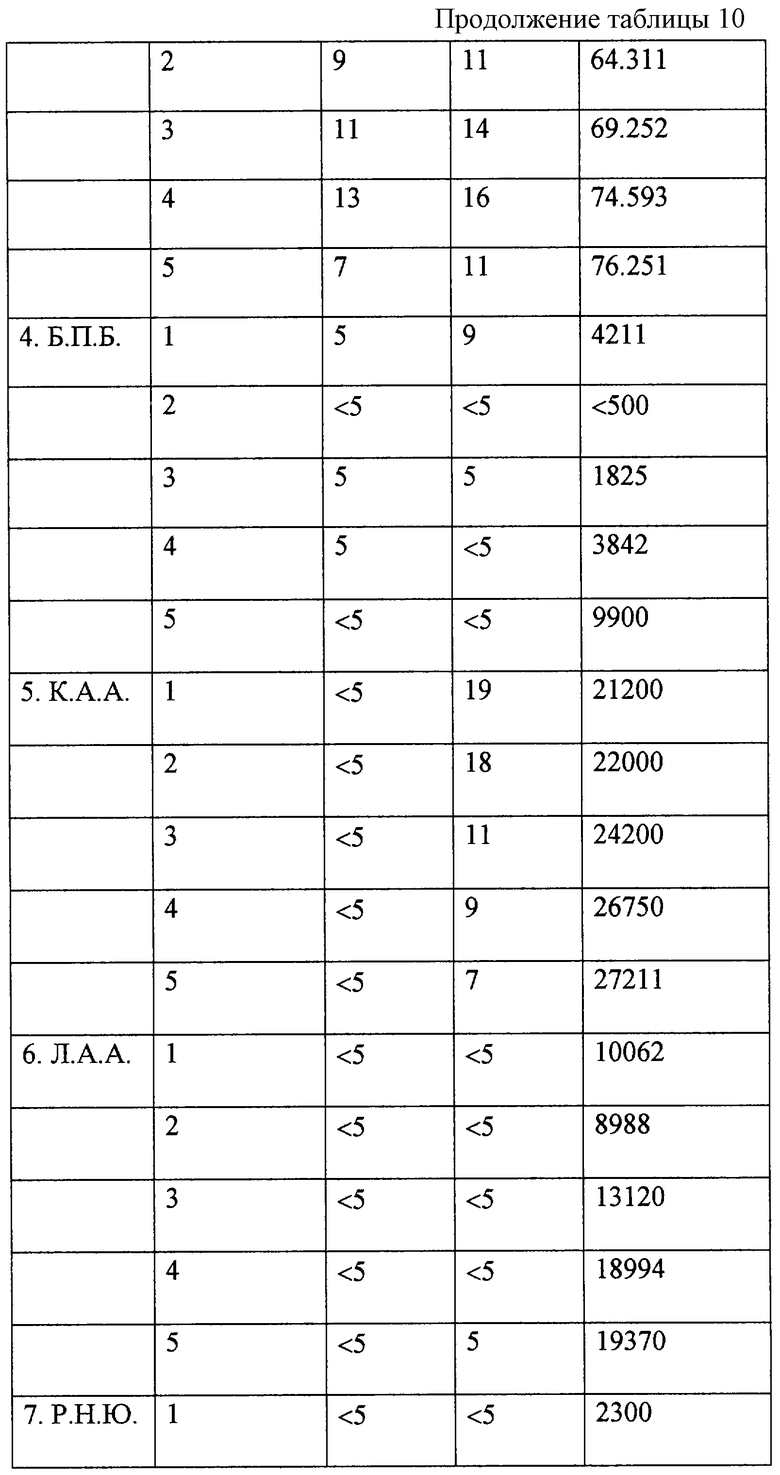
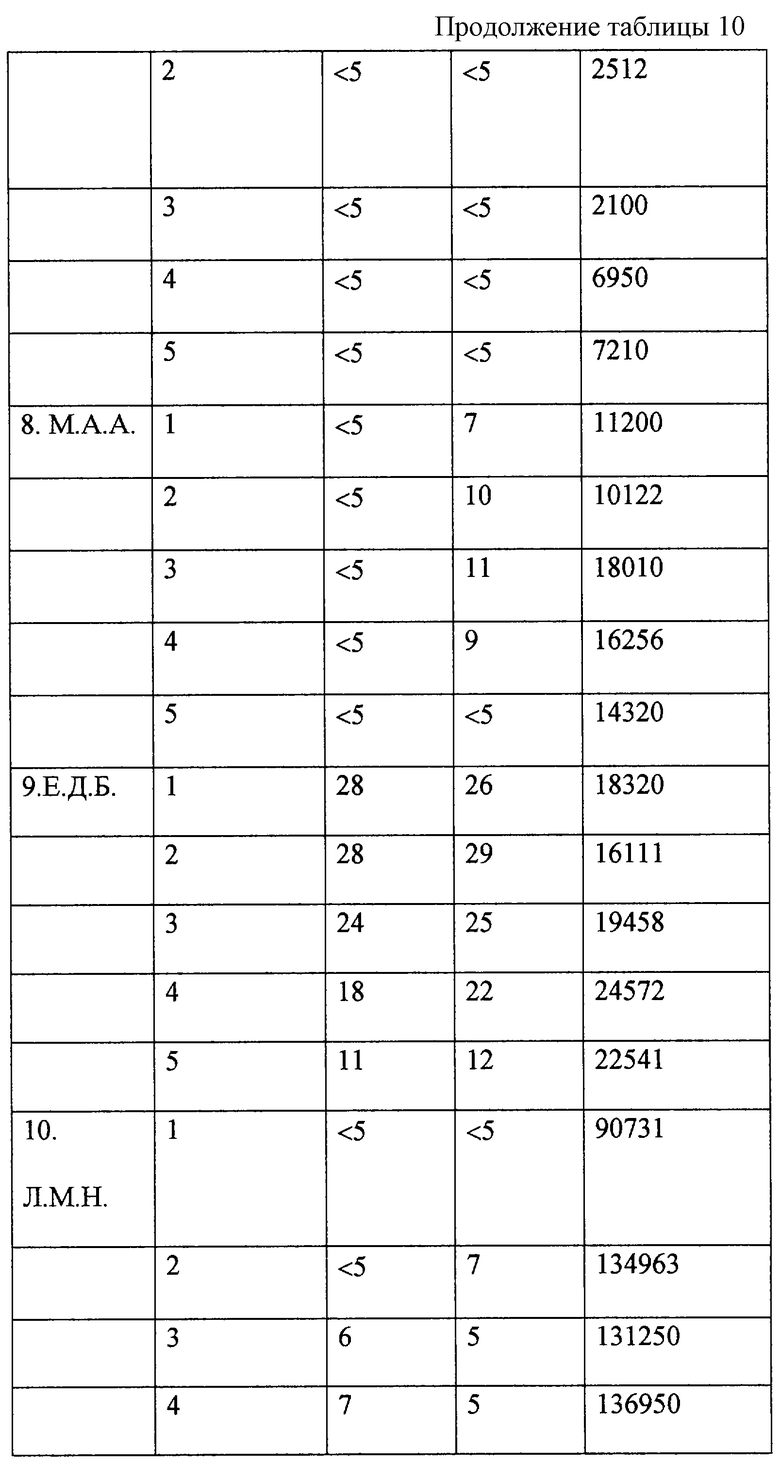
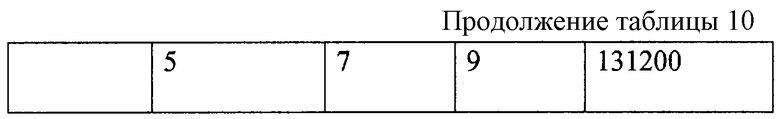
Результаты исследования группы П приведены в табл. 9, группы К - в табл. 10.
Результаты 1-го месяца терапии показали, что у 9 пациентов основной группы из 10 отмечено значительное снижение вирусной нагрузки (максимальное снижение у пациента 8 в 17,3 раза), у одного пациента 9 отмечено незначительное увеличение количества вирусных копий РНК на мл (0,6 раз). При тщательном сборе анамнеза пациента 9 (с участием его близких родственников) выяснилось, что в данный момент пациент эпизодически продолжал прием внутривенных наркотических средств.
Результаты 1-го месяца терапии тимазидом показали, что у 9 пациентов контрольной группы из 10 отмечено несущественное снижение вирусной нагрузки, у одного пациента 4 отмечено снижение количества вирусных копий РНК на мл в 8 раз.
Результаты 3-месячного курса показали, что у 9 пациентов основной группы из 10 отмечено дальнейшее существенное снижение количества вирусных копий РНК на мл до 9,7 раз ( 7). У одного пациента ( 9) отмечалось дальнейшее повышение вирусной нагрузки в 9,7 раз.
Результаты 3-месячного курса показали, что у 9 пациентов контрольной группы из 10 отмечено незначительное увеличение количества вирусных копий РНК на мл до 2,2 раз ( 4). У одного пациента ( 7) уровень вирусной нагрузки не изменился.
По результатам 6-месячного курса лечения основной группы у 4 пациентов отмечалось увеличение количества РНК копий на мл от 3,1 ( 5) до 7,2 ( 8) раз. У 6 пациентов из 10 отмечалось дальнейшее снижение вирусной нагрузки от 2 до 17,8 раз ( 10) Пациент 10 был включен в программу исследования с заведомо самым низким числом РНК копий на мл - 8.932. Уровень вирусной нагрузки пациента 10 снижен до порогового < 500 копий на мл.
По результатам 6-месячного курса лечения контрольной группы уровень вирусной нагрузки незначительно увеличился у 9 пациентов. У пациента 1 отмечено незначительное снижение количества РНК копий на мл в 3,1 раза.
По результатам помесячного мониторинга видно, что эффективность препарата в отношении снижения вирусной нагрузки в первые два месяца значительно превышает его эффективность в последние два месяца и это понижение коррелируется с увеличением ММ применяемого для лечения препарата в течение всего курса лечения.
Таким образом, применение препарата НН в комбинации с тимазидом по сравнению с контрольной группой, принимающей только тимазид, приводит к положительному эффекту, заключающемуся в подавлении вируса ВИЧ у пациента и значительном снижении вирусной нагрузки после одно месячного курса у 80% пациентов, после трехмесячного курса у 90% пациентов. Применение препарата НН в комбинации с тимазидом после 6-месячного курса менее эффективно и приводит к положительному эффекту в 60% случаев. Из представленных данных можно сделать вывод о достаточно высокой эффективности препарата натрия нуклеоспермат в области молекулярной массы (ММ) от 66000 Д (66000 Дальтон) до 320000 Д и нецелесообразности применения этого препарата для подавления ВИЧ-инфекции в области его ММ более 320000 Д.
Все вышеизложенное по нашему мнению определяет перспективность использования натрия нуклеоспермата в комплексной терапии ВИЧ-инфекции. С учетом того, что НН является промышленно выпускаемым лекарственным средством, уже прошедшим все необходимые этапы контроля и испытаний, его использование в новом качестве имеет не только важное медицинское значение, но и обеспечивает большой экономический эффект.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИВИРУСНАЯ КОМПОЗИЦИЯ, СПОСОБ ПОЛУЧЕНИЯ ЕЕ АКТИВНОЙ КОМПОНЕНТЫ И СПОСОБ ЛЕЧЕНИЯ ВИЧ-ИНФИЦИРОВАННЫХ БОЛЬНЫХ ЭТОЙ КОМПОЗИЦИЕЙ | 2001 |
|
RU2192870C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ СИСТЕМНЫМ ДЕЙСТВИЕМ, ЕГО ПРИМЕНЕНИЕ, ФАРМКОМПОЗИЦИИ, СПОСОБЫ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ | 2007 |
|
RU2366697C2 |
| ПЛАЗМОЗАМЕЩАЮЩИЙ РАСТВОР С ГЕМОКОРРЕГИРУЮЩИМИ И ИММУНОМОДУЛИРУЮЩИМИ СВОЙСТВАМИ | 1998 |
|
RU2166944C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ТЕРАПИИ ЧЕЛОВЕКА, ОБЛАДАЮЩАЯ ИММУНОТРОПНЫМ ДЕЙСТВИЕМ | 2001 |
|
RU2188659C1 |
| СПОСОБ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ КОРОНАВИРУСНОЙ И ДРУГИХ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2022 |
|
RU2794315C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО (ВАРИАНТЫ) И СПОСОБ ЛЕЧЕНИЯ НА ЕГО ОСНОВЕ | 2005 |
|
RU2331420C2 |
| КОМБИНАЦИЯ ПРОТИВОВИРУСНЫХ СРЕДСТВ, НАБОР И СПОСОБ ЛЕЧЕНИЯ НА ЕЕ ОСНОВЕ | 2018 |
|
RU2726210C2 |
| Ингибитор входа вируса гепатита и фармацевтическая композиция для лечения гепатита | 2017 |
|
RU2662161C1 |
| СУППОЗИТОРИИ ИНДУКТОРА ИНТЕРФЕРОНА | 2005 |
|
RU2328272C2 |
| КОМПЛЕКСНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2521392C2 |




Изобретение относится к медицине и касается применения натрия нуклеоспермата в качестве лекарственного средства для лечения ВИЧ-инфекции. Изобретение позволяет повысить эффективность лечения ВИЧ-инфекции. 2 с. и 16 з. п.ф-лы, 10 табл.
| RU 94036344 A1, 20.07.1996 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДА ДНК-РНК, ОБЛАДАЮЩЕГО ИММУНОТРОПНОЙ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2108796C1 |
| RU 94041110 A1, 20.09.1996 | |||
| МЕЛЬНИКОВ Д.Ю., ВАЙНБЕРГ Ю.П., КАППИНА Э.Н | |||
| Преодоление резистентности и повышения избирательности действия при химиотерапии/ IV съезд онкологов России (г | |||
| Ростов-на-Дону, ноябрь, 1995) www | |||
| derinad | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| aspю | |||
Даты
2003-06-20—Публикация
2001-04-10—Подача