Изобретение относится к медицине и ветеринарии и касается профилактики и лечения желчекаменной болезни.
В основе этиологии желчекаменной болезни (ЖКБ) лежат: застой желчи (закупорка желчных протоков), воспалительные процессы, нарушение химизма желчи (уменьшение содержания в желчи желчных кислот - гликохолевой и таурохолевой, поставляемых в кишечный тракт печенью через желчный проток, которые, будучи эффективными детергентами, эмульгируют жиры и облегчают действие на них липаз).
На фоне желчекаменной болезни развиваются острый холецистит, холецистопанкреотит, желчекаменная кишечная непроходимость.
Лечение желчекаменной болезни - одна из наиболее актуальных проблем в медицине, поскольку имеет не только медицинское, но и социальное значение. Больные ЖКБ нередко теряют трудоспособность, они вынуждены часто обращаться за медицинской помощью, находясь на амбулаторном, стационарном и санаторно-курортном лечении.
Значительное увеличение заболеваемости ЖКБ отмечается после 40-х годов нашего столетия во всех странах Европы и Северной Америки. Распространенность желчекаменной болезни наиболее высока в возрастной группе 50-60 лет и составляет 14% для мужчин и 20,2% для женщин (Glambek J., Kvna Le G., Amesye В. , Soreide // Scand. J. Gastroenterology, 1987, vol. 22, p. 1089-1094; Gracie W. A, Ransohff D.F. // Gallstone, 1985, p. 27-48). За последние годы заболеваемость ЖКБ во всем мире резко увеличилась (Горчакова Л.А. и соавт. // Клинич. мед., 1989, 11, с. 65-67; Логинов А.С., Ильченко А.А., Шибаева Л. О. // Российский гастроэнтерологический журнал, 1997, 4, с. 29-33).
В последние годы отмечается тенденция к увеличению частоты ЖКБ и в детском возрасте, преимущественно у школьников. Большая частота ЖКБ у девочек связана с гормональными особенностями их развития, в том числе повышенной эстрогенизацией (Запрудников А. М., Харитонова Л.А.// В кн.: Перспективные проблемы в гастроэнтерологии. Т. 1. - Москва. 1994. С. 192-193).
В то же время остаются спорными многие медицинские аспекты проблемы профилактики, диагностики и лечения ЖКБ на ранних стадиях заболевания, поскольку диагностику заболевания осуществляют на стадии образования желчных камней или по изменениям стенки желчного пузыря.
Существующие в настоящее время способы лечения и профилактики заключаются в следующем.
I. Профилактика (Радбиль О.С. Проблемы гастроэнтерологии, 1991, 3, 4(5), с. 10-14):
1) диета с ограничением калорийности, включение в рацион продуктов, богатых пищевой клетчаткой, с добавлением растительных жиров (Мансуров Х.Х. Профилактика желчекаменной болезни. - Клиническая медицина, 1985, 1, с. 10-16);
2) регулярная физическая нагрузка;
3) медикаментозная стимуляция синтеза и секреции желчных кислот, а также подавление синтеза или секреции холестерина (этим требованиям более других препаратов соответствуют хенодезоксихолевая (ХДХК) и урсодезоксихолевая (УДХК) кислоты) (Мансуров Х.Х., Мансурова Ф.Х. Опыт длительного применения хенодезоксихолевой кислоты у больных желчекаменной болезнью // Тер. архив, 1984, 1, с. 43-47);
4) лечение и профилактика сопутствующих заболеваний, ассоциированных с ЖКБ, таких как:
- заболевания желудка
- двенадцатиперстной кишки
- поджелудочной железы
- сахарного диабета
- мочекаменной болезни
- патологии желчевыделительной системы и другие патологии, способствующие застою желчи (Миншуткин О.Н.и др. // Рос. жур. гастроэнтерол., гепатол. , колопрокт. , 1996, т. 6, 4, с. 260; Миншуткин О.Н., Масловский Л.В., Шапошникова О.Ф. // 3-ий Рос. Национ. Конгресс "Человек и лекарство". Тезисы - М., 1996, с. 166).
II. Из лечебных мероприятий чаще всего применяется хирургическое лечение - холецистэктомия (лапроскопия и лапротомия) (Малая инвазивная медицина. / Под ред. Бронштейна А.С. чл.-кор. МАИ и проф. Ривкина В.Л. - М: Лаком, 1998, с. 16-26; Малая медицинская энциклопедия. - т. 2, - М.: Советская энциклопедия, 1991, с. 179-182).
Используемые в настоящее время в клинической практике растворители желчных конкрементов позволяют добиться положительного эффекта лишь у 50-60% больных. Это обстоятельство обусловлено недостаточной мощностью применяемых растворителей, отсутствием универсальных препаратов, способных лизировать камни различного состава. Каждый из применяемых растворителей действует лишь на отдельные структуры, входящие в состав желчного конкремента. Также отрицательным моментом применения литолитических препаратов является длительность их применения (не менее 1,5-2 лет).
Таким образом, фармакотерапия ЖКБ в настоящее время не является решенным вопросом. Очевидно, что большую перспективу имеет профилактическая направленность, которая требует меньших фармакологических затрат, снижает возможность побочных явлений лекарственной терапии и способна дать больший социальный и экономический эффект.
Одним из путей нехирургического лечения желчекаменной болезни являются способы лечения ЖКБ путем назначения больным препаратов, обладающих желчегонным и антибактериальным действием.
К таким способам лечения ЖКБ относятся, например, способ лечения ЖКБ путем перорального введения фармакологического средства на основе композиции, содержащей N-гидроксиметилникотинамид ("Никодин"), крахмал, тальк, стеариновую кислоту (RU 2155041, 27.08.2000), или на основе растительного сырья - на основе травы астрогала (RU 2155056, 27.08.2000), на основе растительного сырья корневища и корня девясила, софоры, кровохлебки, бузины, плодов боярышника (RU 2159123, 20.11.2000), на основе травы зубчатки обыкновенной (RU 2160598, 20.12.2000). Данные средства обладают повышенной желчегонной и противовоспалительной активностью.
Другим путем лечения ЖКБ являются способы выведения желчных камней из организма пациента:
а) прямое контактное растворение желчных камней с использованием растворяющих средств, подводимых через дренажи и катетеры (Alien M.J., Barody T.J, Thistle J. L. In vitro dissolution of cholesterol gallstones. A study of factors influencing rate and comparison of solvents // Gastroenterology, 1985, v. 89, 5, p. 1097-1103.);
б) экстракорпоральная литотрипсия (Королев П.А., Пиковский Д.Л. Экстракорпоральная хирургия желчевыводящих путей. - М.: Медицина, 1990, с. 240; Иванников И.О., Ульянов В.И., Бегачев В.Б. Эффективность литотрипсии в сочетании с холелитической терапией у больных желчекаменной болезнью // Материалы I Рос. гастроэнтерологической недели. 27 ноября - 2 декабря, 1995, С-Пб. , с. 36-37);
в) интракорпоральное разрушение камней с использованием физических методов (лазера, УЗ и др. силовыми методами) (Дзяк Г.В., Зорин А.Н., Монтян С.А. , Перерва А.Н. Новый способ профилактики желчекаменной болезни // Материалы I Рос. гастроэнтерологической недели. 27 ноября - 2 декабря, 1995, С-Пб., с. 78; Воробьев Л.П., Салова Л.В., Мешков В.М., Чубаров В.Г. Возможности лечения дискенизий желчевыводящих путей с помощью лазерного излучения // Клинич. медицина, 1990, 5, с. 110-115);
г) механическая инструментальная фрагментация желчных камней (Lygidakis N.J.// Heterogastroenterology, 1989, v. 36, 3, р. 212-222.)
Известен, например, способ лечения ЖКБ путем выведения желчных камней из организма пациента путем использования в качестве секвесторов (веществ, понижающих уровень реабсорбции желчных кислот) алкилированного поперечносшитого полимера (RU 2160742, 20.12.2000).
Однако приведенные нехирургические методы лечения ЖКБ дают до 50%: рецидивов (Яковлева Л.М., Иванов Л.Н. // В кн.: Новое в гастроэнтерологии. - Москва. т. 2, 1996, с. 158-159).
Наиболее близким по технической сущности к данному изобретению является известный способ профилактики и лечения желчекаменной болезни путем перорального введения фармакологического средства - препаратов хенодезоксихолевой кислоты (ХДХК) и урсодезоксихолевой кислоты (УДХК) (Мансуров Х.Х., Мансурова Ф.Х, Опыт длительного применения хенодезоксихолевой кислоты у больных желчекаменной болезнью // - Тер. архив, 1984, 1, с. 43-47).
Данные препараты стимулируют синтез и секрецию желчных кислот, а также подавляют синтез и секрецию холестерина, способствуют растворению камней.
Технической задачей данного изобретения является создание способа, предотвращающего образование камней в желчном пузыре и их дальнейшего роста.
Поставленная техническая задача достигается способом лечения и профилактики желчекаменной болезни путем перорального введения пациенту (приема пациентом) фармакологического средства. В качестве фармакологического средства используют водный раствор кислого белка - гликопротеина, выделенного изоэлектрическим фокусированном из желчи млекопитающих, обладающего биологической активностью в концентрациях 10-14-10-22 моль/л, вводимого (принимаемого) порциями по 50-100 мл 3-4 раза в день за 5-40 мин до еды в течение 10-30 дней.
Используемый в способе по изобретению кислый белок - гликопротеин из желчи млекопитающих выделяют, используя, в частности, следующие этапы:
а) высаливание белков желчи;
б) собственно выделение (разделение и очистка) кислого гликопротеина (белка) методом изоэлектрической фокусировки;
в) идентифицирование и определение биологической активности, биологического эффекта кислого гликопротеина (Ямскова В.П., Резникова М.М. Адгезин - фактор из сыворотки крови животных и человека // Журнал общей биологии, 1984, т. 45, 3, с. 373-382).
Методом изоэлектрической фокусировки выделяют различные фракции белков, при этом кислые гликопротеины мигрируют к аноду. Сам метод изоэлектрической фокусировки является одним из традиционных методов разделения и очистки белков. Метод широко используется в физико-химической и аналитической химии.
Изоэлектрическое форсирование основано на создании под действием внешнего электрического поля стабильного градиента рН, причем значение рН возрастает от анода к катоду. В такой системе каждый белок перемещается в том или ином направлении в соответствии со знаком своего заряда до тех пор, пока не достигнет участка, в котором значение рН совпадает с его изоэлектрической точкой (рI). На этом участке дальнейшее его перемещение под действием электрического поля прекращается, так как заряд белка становится равным 0.
Выделенные кислые гликопротеины, используемые в данном способе по изобретению, проявляют биологическую активность в сверхмалых дозах, соответствующих концентрациям 10-14-10-22 моль/л, и имеют биологический эффект от 135 до 170% и, возможно, выше (чертеж).
На чертеже приведена зависимость вязкоупругих свойств плазматической мембраны гепатоцитов мышей от концентрации кислого гликопротеина, выделенного из желчи крупного рогатого скота, в условиях кратковременного множественного органного культивирования in vitrо ([С] - концентрация исследуемого гликопротеина, моль/л, К - контрольный опыт).
Биологический эффект, вызываемый указанными кислыми гликопротеинами, определяют по определенной формуле, приведенной ниже. Выделенные кислые гликопротеины из желчи млекопитающих растворимы в насыщенном (100%) растворе сернокислого аммония, сохраняют свою активность при многократном замораживании-размораживании, а также после нагревания при 100oС в течение 10 минут. Кажущаяся молекулярная масса гликопротеинов по данному изобретению составляет от 8 до 100 кДа; степень гликозилирования от 0,1 до 75%; изоэлектрическая точка (рI) выделенных кислых гликопротеинов ниже 3,0.
Ниже приведены примеры выделения используемого в способе гликопротеина из желчи млекопитающих и иллюстрирующие способ по изобретению.
Пример 1. Выделение кислого белка из желчи крупного рогатого скота.
1.1. Высаливание белков желчи.
В желчь консервированную медицинскую (регистрационный номер 70/529/5; ОАО "Самсон", г. Санкт-Петербург) при интенсивном перемешивании постепенно добавляют сухой сернокислый аммоний до образования насыщенного раствора соли (4oС, рН 8,0-8,5). Образовавшийся осадок примесных белков осаждают центрифугированием при 35000 g в течение 30 мин, супернатант собирают и длительно диализуют против дистиллированной воды, используя целлюлозную пленку отечественного производства (ГОСТ 7730-89). Во время диализа дистиллированную воду многократно заменяют на свежую. После полного удаления ионов аммония супернатант концентрируют до объема 100 мл, используя упаривание на роторном испарителе в вакууме при температуре 35-40oС, и повторяют процедуру высаливания в тех же условиях. Аналогично полученный второй супернатант также диализуют против дистиллированной воды до полного удаления ионов аммония и далее разделяют методом изоэлектрофокусирования (ИЭФ).
1.2. Изоэлектрофокусирование супернатанта тканевого экстракта.
Изоэлектрофокусирование проводят в градиенте сахарозы, используя колонку LKB-440 (LKB, Швеция) и амфолиты (Serva, Швеция) диапазона рН 3,5-10,0, при температуре 4oС в течение 100 часов и при напряжении 500-1500 В. Супернатант в виде раствора вводят в тяжелый градиентный раствор в количестве не более 100 мг общего белка. Детекцию фракций осуществляют спектрофотометрически при 280 нм. Диализ фракций после ИЭФ проводят в мешках из целлюлозной пленки против дистиллированной воды. Собирают фракцию кислых гликопротеинов, мигрирующих к положительно заряженному электроду.
Идентифицированные гликопротеины проявляют биологическую активность в сверхмалых дозах, соответствующих концентрациям 10-14-10-22 моль/л (а также, возможно, и ниже) водного раствора гликопротеина.
1.3. Исследование биологической активности.
Исследование биологической активности проводят на мышах линии CBAxC57BL (самцы весом 18-20 г) при помощи адгезиометрического метода, в основе которого лежит экспериментальная оценка параметра, характеризующего вязкоупругие свойства ткани при стандартном деформационном воздействии, оказываемом на фрагмент ткани (Ямскова В.П., Туманова Н.Б. // Изв. акад. наук, сер. биол., 1994, 5, с. 732-737).
Исследование биологической активности проводят посредством множественного органного культивирования фрагментов ткани печени весом 1,0-2,0 мг в 1 мл питательной среды Игла, содержащей 0,1 мл сыворотки крупного рогатого скота, в которую вносят определенный объем исследуемого белкового препарата - кислого гликопротеина желчи, и инкубируют в течение 2 ч при 37oС.
Изменение вязкоупругих свойств ткани оценивают с помощью адгезиометрического метода, сущность которого заключается в следующем: каждый фрагмент ткани после культивирования осушают и подвергают диспергированию в 0,1 мл питательной среды, содержащей 1% раствор трипанового синего, в специальном дезинтеграторе ткани с зазором 50 мкм в условиях стандартного деформационного воздействия. Полученную суспензию клеток и клеточных ядер исследуют микроскопически в камере Горяева.
Для исследования биологической активности в интервале концентраций от 10-6 моль/л до 10-22 моль/л препарат последовательно разводят в питательной среде Игла. В контрольный опыт исследуемый препарат не добавляют. В каждом отдельном эксперименте на каждую экспериментальную точку просчитывают по 5 фрагментов ткани. Биологический эффект рассчитывают по формуле, принимая контроль за 100% (Ямсков И.А., Ямскова В.П., Даниленко А.Н., Клеменкова З.С., Антипов Б. Г. и др. Экспериментальные доказательства роли физико-химических факторов в механизме биологического действия сверхмалых доз // Рос. хим. ж. (Ж. Рос. хим. об-ва им. Д.И. Менделеева), 1999, т. 43, 5, с. 34-39):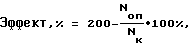
где Non - количество клеточных ядер, выделившихся при деформационном стандартном воздействии из 1-2 мг ткани - органной культуры печени в опыте;
Nk - количество клеточных ядер, выделившихся при деформационном стандартном воздействии из органной культуры печени в контроле.
Результаты экспериментальных данных приведены на чертеже.
Как следует из приведенного чертежа, кислый гликопротеин, выделенный из желчи крупного рогатого скота, проявляет биологическую активность с величиной эффекта от 135 до 173% в диапазоне концентраций от 10-14 до 10-22 моль/л водного раствора.
Пример 2. Влияние кислого гликопротеина желчи на размер частиц в желчи человека in vitro.
Исследование указанным способом проводят на желчи не менее 8 больных ЖКБ.
Больная М. , 53 лет (история болезни 700). Находилась на лечении в ГКБ 71 с 17.01. по 28.01.00). Поступила в хирургическое отделение с жалобами на постоянные ноющие боли в правом подреберье, тошноту после приема жирной пищи, горечь во рту, желтую окраску склер и кожных покровов. Желчекаменной болезнью страдает в течение 4 лет.
При объективном исследовании склеры и кожные покровы желтушные, язык влажный, у корня обложен густым желтым налетом, имеются отпечатки зубов. При пальпации живот болезненный, в правом подреберье положительные симптомы Кера-Гаусмана, Ортнера. Сердечно-сосудистая, дыхательная системы без особенностей.
Оперирована по поводу острого калькулезного холецистита, механической желтухи. Произведена холецистэктомия, дренирование холедоха по Холстеду. В послеоперационном периоде исследовалась протоковая желчь, полученная по дренажу, и пузырная желчь, полученная интраоперационно.
К 10 мл желчи добавляли 1 мл водного раствора кислого гликопротеина желчи (КГЖ) в концентрации 10-14 М. Полученную суспензию встряхивают и помещают в кювету. Проводят измерение размера частиц желчи с помощью микродиффузного метода (Лычников Д.С., Гильмитова И.В. // Международный сельскохозяйственный журнал, 1993, 3, с. 52-54; Лычников Д.С. и др. // Методические указания к проведению практических занятий по дисциплине "физико-химические методы исследования". М.: РЭА им. Г.В. Плеханова. 2000, с. 63).
При действии КГЖ средний диаметр частиц уменьшался с 56,9 до 28,9 нм, тогда как в контрольном измерении (желчь с дистиллированной водой) радиус частиц практически не менялся, средний радиус частиц колебался с 63,3 до 45,5 нм. Для контрольных и опытных изучении проведено не менее 8 измерений для каждого образца желчи с интервалом между измерениями 20-40 минут. Во всех случаях с КГЖ было отмечено уменьшение радиуса частиц.
Пример 3. Влияние водного раствора КГЖ в концентрации 10-14 M npu пероральном приеме на размер частиц желчи человека.
Исследование проводилось на добровольцах (всего 8 человек).
Доброволец Л., мужчина, 60 лет.
Жалоб не предъявляет. При ультразвуковом исследовании (УЗИ) гепатобилиарной зоны обнаружено умеренное уплотнение стенки желчного пузыря, желчь гомогенная. Признаки жировой дистрофии печени.
Принимал водный раствор КГЖ в концентрации 10-14 моль/л в течение 21 дня по 100 мл 3 раза в день за 30 минут до еды. Желчь получают путем дуоденального зондирования (Методическое пособие для самостоятельной работы студентов по методам обследования больных с заболеваниями желудочно-кишечного тракта, печени, желчевыводящих путей. Под ред. Л.П. Воробьева. - М.: ММСИ, 1989. с. 59-63).
Исследовалась порция "В" - до начала приема препарата, через 1, 3, 6, 10, 16, 21 день (интервалы между заборами желчи взяты эмпирически). Желчь исследовалась микродиффузионным методом.
Средний размер частиц уменьшался с 52 нм (контрольная порция - без препарата) до 17,0 нм на 16 день приема КГЖ и продолжал оставаться примерно на том же уровне в 5-й пробе (на 21 день). Во время приема препарата рацион пищи не изменялся.
Доброволец К., женщина, 23 года.
Жалоб не предъявляет. При УЗИ гепатобилиарной зоны патологии не выявлено. Желчь гомогенная.
Принимала водный раствор КГЖ, приготовленный аналогичным образом (см. предыдущий пример) по 100 мл 3 раза в день за 30 минут до еды (пищевой рацион не менялся). Также исследовалась желчь порции "В", полученная при дуоденальном зондировании:
1) до начала приема препарата;
2) через 1 день после приема препарата;
3) через 4 дня;
4) через 8 дней;
5) через 14 дней;
6) через 20 дней.
Исследование желчи проводилось микродиффузным методом. Средний радиус частиц до начала эксперимента соответствовал 38,4 нм. Отмечено уменьшение размера частиц на 8-й день после приема препарата и продолжал уменьшаться до 20-го дня, причем разница в уменьшении радиуса частиц желчи на 14-й и 20-й день была незначительной.
Таким образом, радиус частиц уменьшился с 38,4 нм в контрольной пробе до 14,5 нм на 20 день после приема препарата.
Вышеприведенные примеры показывают, что способ по изобретению позволяет улучшить состояние больных желчекаменной болезнью и может быть использован для лечения и профилактики желчекаменной болезни.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОФТАЛЬМОЛОГИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ И ПОВРЕЖДЕНИЙ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА | 2003 |
|
RU2232586C1 |
| НОВЫЙ КЛАСС ФИЗИОЛОГИЧЕСКИ АКТИВНЫХ ГЛИКОПРОТЕИНОВ | 2000 |
|
RU2223781C2 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ЖЕЛЧЕКАМЕННОЙ БОЛЕЗНЬЮ ПЕРВОЙ СТАДИИ | 2012 |
|
RU2519198C2 |
| СПОСОБ ЛЕЧЕНИЯ АТЕРОСКЛЕРОЗА | 2006 |
|
RU2311209C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАСЛА ИЗ СЕМЯН ТЫКВЫ, ИСПОЛЬЗУЕМОГО В ЛЕЧЕБНЫХ, ПИЩЕВЫХ И КОСМЕТИЧЕСКИХ ЦЕЛЯХ И БИОЛОГИЧЕСКИ АКТИВНОЕ СРЕДСТВО | 2010 |
|
RU2445111C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕХАНИЧЕСКОЙ ЖЕЛТУХИ | 2006 |
|
RU2349322C2 |
| СПОСОБ РАННЕЙ РЕАБИЛИТАЦИИ БОЛЬНЫХ ПОСЛЕ ОПЕРАЦИЙ ПО ПОВОДУ ДОБРОКАЧЕСТВЕННЫХ ЗАБОЛЕВАНИЙ ПИЩЕВАРИТЕЛЬНОЙ СИСТЕМЫ | 2017 |
|
RU2639581C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ОБУСЛОВЛЕННЫХ И СОПРОВОЖДАЮЩИХСЯ НАРУШЕНИЕМ МЕТАБОЛИЗМА ЖЕЛЧНЫХ КИСЛОТ И ХОЛЕСТЕРИНА | 2005 |
|
RU2294207C2 |
| НАБОР "ПРЕДСТАР", ЕГО ПРИМЕНЕНИЕ И СПОСОБ ПРЕДУПРЕЖДЕНИЯ ПРЕЖДЕВРЕМЕННОГО СТАРЕНИЯ ОРГАНИЗМА | 2007 |
|
RU2351350C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ "ПЕЛВИТ" И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1995 |
|
RU2094051C1 |
Изобретение относится к медицине и касается лечения и профилактики желчекаменной болезни. Способ заключается в том, что больным желчекаменной болезнью вводят перорально 50-100 мл водного раствора кислого гликопротеина, выделенного изоэлектрическим фокусированием из желчи млекопитающих, в концентрации 10-14-10-22 моль/л. Введение осуществляют 3-4 раза в день за 5-40 мин до еды в течение 10-30 дней. Способ обеспечивает уменьшение кристаллизации желчи и образования "зародышей" желчных камней. 1 ил.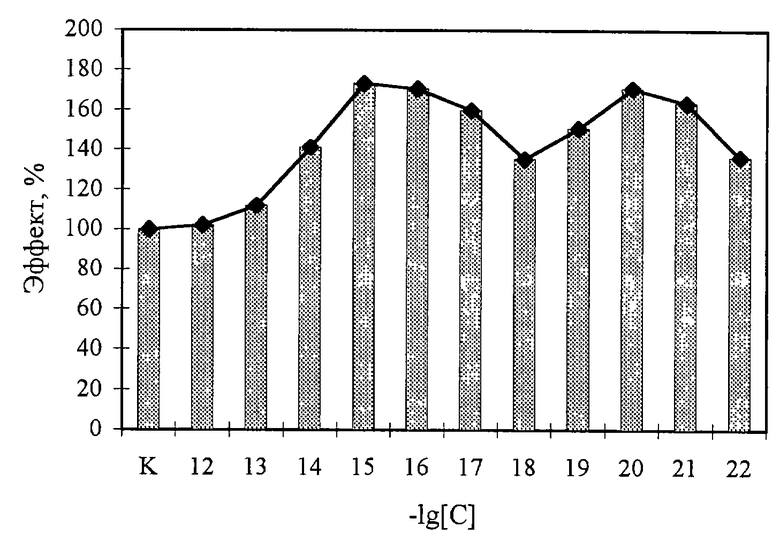
Способ профилактики и лечения желчекаменной болезни путем перорального приема фармакологического средства, отличающийся тем, что в качестве фармакологического средства используют водный раствор кислого белка - гликопротеина, выделенного изоэлектрическим фокусированием из желчи млекопитающих, обладающего биологической активностью, в концентрациях 10-14-10-22 моль/л, который принимают порциями по 50-100 мл 3-4 раза в день за 5-40 мин до еды в течение 10-30 дней.
| МАНСУРОВ Х.Х | |||
| и др | |||
| Тер.архив | |||
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| ФАРМАКОЛОГИЧЕСКИ АКТИВНАЯ СУБСТАНЦИЯ ЗАЩИТНОГО СОЕДИНЕНИЯ ОРГАНИЗМА 3СО, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 1990 |
|
RU2104704C1 |
| RU 97103056 А, 20.04.1999 | |||
| ALLEN M.J | |||
| et al | |||
| In Gastroenterology | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
Авторы
Даты
2003-06-27—Публикация
2001-04-04—Подача