Изобретение относится к оригинальным клеткам, которые экспрессируют протеины гетерологичного связывания и способам скрининга соединений с пептидосвязывающей активностью, а также способам использования новых клеток.
Предпосылки изобретения
Специфическое связывание пары пептидов друг к другу вызывает множество функциональных ответов в живой клетке. Например, специфическое связывание лиганда к поверхности рецептора служит в качестве переключателя ответов клетки по отношению к многим внешним сигналам. У млекопитающих клетки реагируют на большое разнообразие циркулирующих пептидных гормонов часто посредством одних трансмембранных доменов-рецепторов. Конечно, признается, что цитокиновый рецептор превосходно иллюстрирует разнообразные аспекты клеточной функции и физиологические реакции. Последние исследования функции цитокинового рецептора выявили различающиеся лиганд-рецептор протеиновые стехиометрии, включающие как 2-протеин (лиганд/рецептор) (Cunningman et al., 1991; Staten et al., 1993), так и 3-протеин (лиганд/рецептор/рецептор или лиганд/рецептор/трансдуктор) взаимодействия (Young, 1992; Taga and Kishimoto, 1992; Mui and Miyajima, 1994). Сложность таких протеиновых ассоциаций исследовали используя in vitro, часто трудоемкие методы (Fuh et al., 1992; 1993; Davis et al., 1993), поскольку генетически податливые системы экспрессии были недоступны. Данное изобретение имеет отношение к оригинальным модифицированным системам хозяина, которые могут использоваться для исследований таких протеинов, тем не менее, будучи новой, она значительно менее трудоемка.
Описанные недавно системы относятся к 2-гибридной системе, как обсуждалось Fields and Song, 1989, а также Chein el al., 1991, 2-гибридная система включает дифференциальное взаимодействие между связыванием отделимой ДНК и доменами активации транскрипционного активатора дрожжей Gal4. Гетерологичные протеины экспрессируются как гибридные протеины, присоединившиеся к любой половине Gai4 (для обсуждения 2 гибридной системы см. фиг.1; Fields and Song, 1989; Chein et al., 1991). Продуктивное взаимодействие с этими гетерологичными протеинами приводит эти две половины Ga14-протеина в непосредственную близость, активизируя экспрессию переписываемого гена-репортера. До настоящего времени такая 2-гибридная система выявилась полезной для определения того, обладает ли данная тестовая последовательность первого пептида связывающей активностью к другой известной последовательности другого пеитида при условии, что сродство тестового пептида к данному пептиду неизвестно. Исследования, использующие такую систему, были направлены на анализ внутриклеточных белков, таких как факторы транскрипции и киназно нацеленные взаимодействия белков (Yang et al. , 1992; Durfee et al., 1993; Lee et al., 1994).
Оригинально модифицированные в этом изобретении клетки и новые методы, оперирующие с этими клетками, обеспечивают значительное продвижение в изучении и выявлении пептидной мимикрии, включая лигандную и рецепторную имитацию. При этом никто не разработал эффективную и специфическую скрининговую систему для исследования в этой области. Используя в клетке пептидную пару с известным сродством, данное изобретение дает возможность проводить исследование пар связанных пептидов, таких как лиганд и рецептор, при условии, что пептиды связываются посредством внеклеточных взаимодействий. Это изобретение предоставляет возрастающие преимущества для открытия соединений, которые могут взаимодействовать как лиганды для специфических рецепторов или трансдукторов. Потенциальные лиганды включают (но не сводятся к ним) гормоны млекопитающих с рецепторами, являющимися родственными им внеклеточными лигандосвязывающими пептидами. Более того, данное изобретение описывает использование клеточных систем, которые экспрессируют многочисленные гетерологичные протеины, в том числе два гетерологично связанных протеина на основе специфического и обратимого связывания лиганда и рецептора. Специфическое взаимодействие вышеописанного связывания легко обнаруживается фиксацией изменений клеточного фенотипа, например роста на селективной среде.
Резюме изобретения
Один аспект настоящего изобретения относится к оригинально модифицированным клеткам хозяина для экспрессии протеинов гетерологичного связывания. Оригинально модифицированные клетки хозяина включают:
а) генную последовательность, кодирующую протеин гетерологичного связывания, именуемый протеином связывания, включающим первый пептид пары пептидного связывания или сегмент упомянутого первого пептида, который присоединен либо к ДНК связывающему домену, либо к соответствующему домену транскрипциональной активации транскрипционального активационного протеина;
b) генную последовательность, кодирующую протеин гетерологичного связывания, именуемый протеином связывания, состоящим из второго пептида пары пептидного связывания в (а), или сегмента упомянутого второго пептида, присоединенного либо к ДНК связывающему домену, либо к соответствующему домену трнскрипциональной активации, какой бы ни применялся в (а);
с) ген-репортер, оперативно ассоциированный с трнскрипциональным активационным протеином или его частью;
d) выборочно удаление или изменение хромосомной ДНК дрожжевой клетки хозяина для трнскрипционального активационного протеина, если он присутствует в клетке хозяина.
Эти оригинальные модифицированные клетки хозяина в настоящем изобретении могут использоваться для определения взаимодействия тестового образца с подобранным пептидом пары пептидного связывания, например клетка может использоваться для определения взаимодействия тестового образца с подобранным лигандом или рецептором.
Второй аспект настоящего изобретения относится к оригинально модифицированным клеткам и методам скрининга, которые показывают взаимодействие тестового образца с подобранным пептидом или рецептором через узнаваемое изменение в фенотипе. Клетка показывает изменение в фенотипе только в присутствии тестового соединения, имеющего связывающее сродство к паре пептидного связывания, например сродство лиганда и его рецептора.
Третий аспект настоящего изобретения относится к новым клеткам и методам скрининга, которые позволяют определить, к какому пептиду пары пептидного связывания присоединяется тестовый образец.
Четвертый аспект настоящего изобретения относится к новым клеткам, которые экспрессируют три и более гетерологичных компонента для изучения более высокого порядка в мультипротеиновых ассоциациях между тремя и более пептидами (например, таловыми при исследовании лигандозависимой димеризации).
Определяемые понятия:
Термин пара пептидного связывания относится к любой паре пептидов, имеющих известное сродство связывания, для которой последовательность ДНК известна или может быть установлена. Пептиды этой пары пептидного связывания должны демонстрировать предпочтительное связывание друг к другу более, чем для любых других компонентов модифицированной клетки.
Термин пептид, как он используется в вышеупомянутом резюме и здесь, означает любой пептид, полипептид или белок, пока не оговаривается иначе. Как отмечается выше, пептиды в паре пептидного связывания могут быть лигандом и соответствующим ему рецептором или лигандом и любым пептидом, имеющим известное сродство связывания для этого лиганда.
Гетерологичные, как используется в вышеупомянутом резюме и здесь, означают пептиды, которые (1) не экспрессируются встречающейся в природе клеткой хозяина или (2) экспрессируются модифицированной клеткой хозяина с помощью метода экспрессии, отличного от такового, с помощью которого клетка хозяина нормально экспрессировала бы этот пептид.
Если не оговаривается иначе, понятие рецептор, используемое здесь, охватывает термины рецептор, растворимый рецептор, трансдуктор или связывающий белок. Применительно ко всему изобретению использование понятия рецептор означает рецептор или растворимый рецептор, более предпочтительным при этом является рецептор.
Рецептор, как используется здесь, означает плазматические мембранные белки, которые связывают специфические молекулы, такие как факторы роста, гормоны или нейропередатчики (нейромедиаторы), а затем передают сигнал клеточному содержимому, что заставляет клетку отвечать специфическим образом. Сюда относятся простые трансмембранные протеины.
Растворимый рецептор, как используется здесь, означает не трансмембранную форму рецептора, которая способна связать лиганд. Это рецепторы, высвобождаемые из клетки либо путем протеолиза, либо альтернативно сцепленной мРНК.
Связывающий протеин обозначает белки, которые демонстрируют сродство связывания для специфического лиганда. Связывающие протеины могут синтезироваться на обособленных и отдельных генах. Для данного лиганда связывающие протеины, синтезируемые на специфических генах, отличаются от лиганд связывающего домена рецептора или его растворимого рецептора.
Трансдуктор означает молекулу, которая позволяет превращать один вид сигнала в другой, и молекулу, хорошо известную как "датчик" для одного или нескольких пептидов пары пептидного связывания, например для группы лиганд/рецептор.
Краткое описание чертежей
Фигура 1 представляет схематическую диаграмму клетки, которая экспрессирует из отдельных плазмид два протеина гетерологичного связывания (один, являясь лигандом, связан с доменом активации транскрипционального активационного протеина, а другой, будучи рецептором, связан с ДНК связывающим доменом транскрипционального активационного протеина). Фигура показывает экспрессию этих двух связанных протеинов и связывание лиганда с рецептором, которое сводит вместе связывающий и активационный домены, переорганизовывая транскрипциональный активационный протеин. Стоит транскрипциональному активационному протеину переорганизоваться и присоединиться с помощью ДНК связывающего домена к локусу Upstream Activation Sequences, противоточных активационных последовательностей (UAS), инициализируется транскрипция гена-репортера (HIS3).
Фигура 2 содержит фотографии пластин, показывающих результаты экспериментов по росту, выполненных по примеру 1 для штаммов CY722, CY723, CY724 и CY781 на селективной и неселективной средах, фотографии А и В соответственно.
Фигура 3 представляет схематическую диаграмму димерной модели, в которой лиганд присоединяется к системе двухкомпонентного рецептора. Схематическая диаграмма изображает клетку, которая экспрессирует протеины от трех отдельных плазмид. Два протеина гетерологичного связывания (один связанный протеин, будучи первым рецептором, присоединен к домену активации транскрипционального активационного протеина, а другой, будучи вторым рецептором, присоединен к ДНК связывающему домену транскрипционального активационного протеина) подвергаются экспрессии и свободный лиганд (например, лиганд, который не присоединен к какому-либо из двух доменов транскрипционального активационного протеина) экспрессируется от третьей плазмиды. Фигура показывает экспрессию этих двух связанных протеинов и связывание свободного лиганда и двух связывающих рецепторов, которые соединяют связывающий домен и активационный домен, переформировывая транскрипциональный активационный протеин. Как только транскрипциональный активационный протеин переформировался и зафиксировался ДНК связывающим доменом с сайтом противоточных активационных последовательностей (UAS), инициализируется транскрипция гена-репортера (HIS3).
Фигура 4 представляет фотографию пластинки роста, полученной для штаммов CY846 и CY847 из примера 3, показывая лигандзависимую стимуляцию димеризации рецептора.
Подробное описание изобретения
Модифицируемой клеткой в этом изобретении служит клетка хозяина. Пригодная клетка хозяина в настоящем изобретении просто требует, чтобы она была определена генетически с целью организации соответствующей экспрессии протеинов гетерологичного связывания, репортера(ов) и любых других желаемых генетических манипуляций. Клетка хозяина может быть любой эукариотической клеткой позвоночного или беспозвоночного. Клетка хозяина может быть клеткой млекопитающего в той же степени, как и земноводного, например клетка яйца Xenopus (шпорцевая лягушка). Предпочтительно, чтобы клетка хозяина была клеткой гриба, например Aspergilla или Neuropora. Более предпочтительное воплощение клетка дрожжей. С другой стороны, предпочтение можно отдать дрожжевым клеткам Sаsccharomyces cerevisiae, Schizosaccharomyces pombe или Pichia pastoris.
Модифицируемая клетка хозяина задействует, по крайней мере, два гена для экспрессии отдельно двух протеинов гетерологичного связывания. Один из этих слитых протеинов включает в себя первый пептид пары пептидного связывания или сегмент названного первого пептида, который присоединен либо к ДНК связывающему домену или к соответствующему транскрипциональному активационному домену транскрипционального активационного протеина. Второй связанный протеин - второй пептид пары пептидного связывания или сегмент того, что перечислялось. Второй пептид присоединен либо к ДНК связывающему домену, либо к соответствующему транскрипциональному активационному домену, какой бы ни использовался в качестве первого протеина гетерологичного связывания. Активность связывания между пептидами в паре пептидного связывания наблюдается при использовании гена-репортера, который оперативно связывается с транскрипциональным активационным протеином, используемом в случае этих двух слитых протеинов.
Транскрипциональный активационный протеин может широко варьировать пока ДНК связывающие домены и активационные домены известны или могут быть установлены доступными научными методами. Транскрипциональный активационный протеин может быть любым протеином, имеющим два компонента, ДНК связывающий компонент и активационный компонент, при условии, что транскрипциональный активационный протеин содержит кислоты и альфа-виток для активации транскрипции. Предпочтительно транскрипциональный активационный протеин выбирается из Gal4, Gen4, Hapl, Adrl, Swi5, Stel2, Mcml, Yapl, Acel, Ppr1, Arg81, Lac9, Qua IF, VP16, LexA, ядерных рецепторов не млекопитающих (например, экдизон), или ядерных рецепторов млекопитающих (например, эстроген, андрогены, глюкокортикоиды, минералокортикоиды, ретиновая кислота и прогестерон; см. также Picard et al., 1990). Предпочтительно транскрипциональный активационный протеин является протеином дрожжей, а более предпочтительно, чтобы транскрипциональный дрожжевой протеин выбирался из Gal4, Gcn4 или Adrl. Заметим, что может использоваться тот ДНК связывающий протеин, который функционирует с доменом активации. ДНК связывающий протеин может заменяться для ДНК связывающего домена транскрипционального активационного протеина, если узнавающие последовательности, оперативно связанные с геном-репортером, соответственно организованы. Иллюстративным для недрожжевых ДНК связывающих протеинов являются стероидные рецепторы млекопитающих и бактериальный LexA (см. Wilson et al., 1990).
Ген-репортер в общем случае выбирается для того, чтобы связывание доменов с транскрипциональным активационным протеином могли регистрироваться хорошо известными н прямыми методами. Предпочтительно, чтобы ген-репортер был подобран по своему назначению (цене), легкость измерения его активности и низкий фон (например, активность может определяться при относительно низких уровнях экспрессии гена-репортера из-за высокого отношения сигнал:шум и/или из-за относительно низкой или отсутствующей индуцированной активности). Репортер может быть любым репортером, для которого активность может обнаруживаться любым доступным способом. Иллюстрацией репортеров, которые могут использоваться в настоящем изобретении, являются гены-репортеры, подобранные из группы:
а) lасZ, ген люциферазы, ген зеленого флюоресцентного протеина, CAT;
б) гены, комплементирующие ауксотрофии, такие как HIS, URA, LEU, ARG, MET, ADE, LYS, TRP;
в) ген, дающий сопротивляемость антибиотикам, такой как neo, KAN;
г) гены, дающие чувствительность к химикатам, такие как CYH2, CAN1 (устойчивость к канавину). Во многих случаях это может быть приемлемым для гена-репортера для предотвращения роста (CYH2), предпочтительно, чтобы активность гена-репортера индицировалась колориметрическими или флюоресцентными методами и/или измерением роста дрожжевой клетки.
Как отмечено ранее, пептид, используемый в модифицированной клетке, является пептидом пары пептидного связывания, для которого ДНК последовательность известна так же, как и для второго пептида в паре. Пептиды могут также быть пептидами в комплексе пептидного связывания, содержащего два или более пептида, которые взаимно связываются с образованием комплекса. Пептиды в паре пептидного связывания могут быть специфическим лигандом и соответствующим рецептором или любыми другими пептидами, которые предпочтительно связываются один с другим, как субьединицы в ферменте.
Одним из значительных преимуществ этого изобретения является открытие того, что модифицированная клетка, задействующая связывание ДНК и активационные домены транскрипционального протеина, может быть использована для наблюдения за связыванием пептидов в паре пептидного связывания, которые связываются посредством внеклеточного взаимодействия. Конечно, если желаемые пептиды связываются посредством внутриклеточного взаимодействия, они также могут быть задействованы в любой из новых модифицированных клеток и любом из методов данного изобретения. Пептид может быть из клетки млекопитающего или клетки не млекопитающего. Одно из наиболее важных воплощений настоящего изобретения относится к применению новых модифицированных клеток и соответствующих способов скрининга этого изобретения для изучения многочисленных взаимодействий пептидов млекопитающих. Пептиды млекопитающих включают взаимодействия у млекопитающих по типу лиганд/рецептор, такие как взаимодействия гормон/рецептор. Иллюстрацией пептидных гормонов, которые могут быть использованы в настоящем изобретении, являются пептиды, подобранные из (но не ограничиваясь приведенными) одной из следующих групп: (а) группа, состоящая из цитокинов, интерлейкинов, гематопоетик-ростовых факторов, инсулина, инсулиноподобных ростовых факторов, гормона роста, пролактина, интерферонов и факторов роста; (b) лиганды для G-протеин спаренных рецепторов; (с) лиганды для рецепторов беспозвоночных; (d) лиганды для гуанилциклазных рецепторов; (е) лиганды для тирозин-фосфатазных рецепторов.
Альтернативным вариантом пептида является фактор роста (ФР) из эпидермы, ФР нервов, фактор ингибирования лейкемии, фибробластный ФР, ФР пластиночного происхождения, ФР сосудистого эндотелия, фактор опухолевого некроза, онкостатин М, мерцательный нейротропный фактор, эритропоетин, фактор закаливания (steel), плацентарный лактоген н трансформирующий β-ФР.
В различных предпочтительных вариантах пептидный гормон является лигандом для G-протеин спаренного рецептора, такого как фактор, высвобождающий гормон роста, секретин, вазоактивный ингибиторный пептид, глюкагон, тиротропин, интерлейкин 8, лютеинизируюший гормон (LH) и фоликулярный стимулрующий гормон (FSH).
В дополнительных альтернативных вариантах используемый пептид является пептидом беспозвоночных, таким как выбираемый из тех, что входят в группу из растительного системина и пептидов дифференцировки насекомых. Однако в предпочтительных вариантах пептид выбирается из группы, состоящей из пептидов млекопитающих, и более предпочтительно из пептидных гормонов млекопитающих.
Также отмечается, что специфические типы рецепторов могут также быть пептидом пары пептидного связывания или комплекса пептидного связывания. Иллюстрацией различных рецепторов служат выбираемые из следующих групп: (а) молекула клеточной адгезии; (b) иммуномодуляторный антиген распознавания или молекула представления или другие родственные пептиды. Иллюстрациями молекул клеточной адгезии являются ICAM, VCAM, ЕСАМ, фибронектин, интегрин, селектин и фибриноген. Иллюстрацией иммуномодуляторного антигена распознавания или молекулы представления являются комплекс рецептора Т клетки, комплекс рецептора В-клетки, Fc-рецепторы, мажорный комплекс гистосовместимости I, мажорный комплекс гистосовместимости II, CD4, CD8, CD27, CD30, MAC комплекс.
Также отмечается, что специфическими типами трансдукторов могут также быть использованы пептид пары пептидного связывания или комплекс пептпдного связывания. Применяемые протеины-трансдукторы могут быть любым из протеинов-трансдукторов, которые связывают, по крайней мере, один из пептидов пары пептидного связывания или комплекса пептидного связывания. Протеины-трансдукторы включают gp130, kn97, AIC2A, AIC2B.
Предпочтительно протеины гетерологичного связывания экспрессируются путем трансформации дрожжевой клетки автономно реплицирующейся плазмидой, способной экспрессировать протеин связывания, хотя они могут экспрессироваться путем хромосомной модификации.
Как отмечалось, методы скрининга в этом изобретении выполнены для того, чтобы обнаружить способность тестового образца воздействовать на связывание пептидов в паре пептидного связывания, например взаимодействие лиганда с рецептором. По существу, способ включает определение активности гена-репортера при добавлении тестового образца к модифицированной клетке хозяина в настоящем изобретении в условиях, пригодных для обнаружения активности в присутствии образца или в условиях, для которых модифицированная клетка хозяина выявляет такую активность только в присутствии образца, обладающего связывающим взаимодействием с пептидом пары связывания. Предпочтительно активность гена-репортера определяется при измерении изменения в избранном фенотипе, которое прямо скоррелировано с активностью репортера.
Новые модифицируемые клетки в этом изобретении легко задействуются в различных методах скрининга для определения активности связывания тестового образца. Тестовый образец может быть пептидом, желательно длиной в две аминокислоты или непептидным химическим соединением. Ненептидный тестовый образец включает соединения, комплексы или соли, равно как и продукты природного происхождения, такие как растительные экстракты или материалы, полученные из ферментационного "бульона". Модифицированные клетки хозяина выращиваются в условиях, пригодных для роста, чтобы изучить взаимодействие тестового образца на связывание с парой пептидного связывания. Модифицированные клетки хозяина помещаются в питательную среду, которая предпочтительно содержит агар, с тестовым образцом, помещенным на поверхность питательной среды. Ростовая среда предпочтительно является обычной жидкой средой с ростовыми реагентами и водой, такой как дрожжевая синтетическая среда (YSM, пригодная от BIO101 (см. также Rose et al., Methods in Yeast Genetics, 1990).
Одно из воплощений настоящего изобретения направлено на новые модифицированные клетки хозяина и способ скрининга, который показывает взаимодействие тестового соединения с подобранной парой пептидного связывания посредством выявляемого изменения в фенотипе. Эта модифицированная клетка хозяина показывает изменение в фенотипе только в присутствии тестового соединения, обладающего активностью связывания по отношению к одному из пептидов в паре пептидного связывания. Эта клетка хозяина упоминается здесь как система "спасения". Нормально, ответ клетки показывается, когда два домена транскрипционального протеина активации взаимодействуют. Однако в системе спасения положительной индикации изменения в фенотипе не происходит, когда взаимодействуют два домена транскрипционального активационного протеина. Положительная индикация изменений в фенотипе происходит только, когда тестовый образец прерывает взаимодействие этих двух доменов транскрипционального активационного протеина. В системе спасения модифицированная клетка хозяина способна экспрессировать, по крайней мере, два протеина гетерологичного связывания. Далее, клетка хозяина включает ген-репортер, оперативно связанный с транскрипциональным активационным протеином, при условии, что, как указывалось, ген-репортер препятствует проявлению специфического фенотипа на селективной среде, благодаря экспрессии транскрипционального активационного протеина или его части. Мутация хромосомной ДНК клетки хозяина приводят к полному изменению в детектируемом фенотипе на питательной среде при отсутствии экспрессии гена-репортера. Если необходимо, происходит удаление или мутация в хромосомной ДНК клетки хозяина для транскрипционального активационного протеина, чтобы транскрипциональная активация происходила только при результативном взаимодействии подобранной пары связывания, только когда тестовый образец прерывает взаимодействие двух доменов транскрипционального активационного протеина, он позволяет модифицированной клетке расти, или выживать, или проявить подобранный фенотип. Предпочтительно фенотип соответствует росту клетки.
Когда способ определения, как обсуждалось выше, используется для определения того, взаимодействует ли тестовый образец, или только разрушает пептидное связывание, наблюдаемое в отсутствии тестового образца, для определения специфического сродства связывания тестового образца применяется вторичный скрин(инг), например к какому пептиду из пары пептидного связывания присоединяется тестовый образец. В этом изобретении вторичные скрининги используют новые клетки при условии, что они приспособлены проявлять фенотип или изменение фенотипа только в присутствии тестового образца, который связывает один из пептидов пары пептидного связывания. Один из предпочтительных методов для определения специфической характеристики связывания тестового образца включает применение клеток, которые содержат эффективное (и относительно большое) число копий того или иного протеина связывания, содержащего один из пептидов. Эффективное число копий - это любое число копий, достаточное для определения специфического связывания тестового образца. Предпочтительно генное число копий составляет, по крайней мере, 5, а желательный диапазон примерно от 5 до 50, с большим наиболее подходящим значением. Другого протеина связывания может оставаться относительно мало (от 1 до 2 копий на клетку) с той или иной интеграцией в клеточную хромосому или с использованием хромосомных центромерных последовательностей в плазмиде экспрессии. Если используется большое число копий первого пептида в клетке в этом изобретении, клетка будет более чувствительной в присутствии тестового образца, который присоединяет второй пептид пары пептидного связывания, поскольку лимитирующее количество второго пептида определяет уровень активности гена-репортера (т. е. наблюдаемое изменение в фенотипе). Наоборот, если используется большое число копий гена, кодирующего второй пептид пары пептидного связывания, клетка будет более чувствительной к присутствию тестового образца, который связывает первый пептид, поскольку лимитующее количество второго пептида определяет уровень активности ген-репортера (т.е. наблюдаемое изменение в фенотипе). Прямое сравнение эффектов тестового соединения на фенотипы двух штаммов (рецептор>>>лиганд против лиганд>>>рецептор) демонстрирует специфическое протеиновое взаимодействие соединения. Как обсуждалось ранее, гены, экспрессирующие пептиды, как и ген-репортер, преимущественно экспрессируются путем трансформации дрожжевой клетки автономно реплицирующейся плаамидой.
Дополнительные модифицированные клетки хозяина в этом изобретении направлены на клетки, которые могут быть использованы для изучения пептидпых лигандов, которые задействуют двойные рецепторы или рецептор и трансдуктор для активации или передачи сигнала от связывания компонентов в составном пептиде, т.е. трех и более связывающихся пептидных компонентов.
Димеризация рецептора является первым критическим шагом в преобразовании сигнала для определенных классов рецепторов. Димерные структуры рецептора могут состоять из идентичных рецепторных единиц (примеры: инсулиновый рецептор, IGF-I рецептор, PDGF рецептор, киназный инертный доменный рецептор (KDR), или колониестимулирующий фактор (CSF)-I рецептор) или неидентичных рецепторных единиц (примеры: IL-6R + gp130; инсулин-IGF-I гибридный рецептор; LIF + gp130; CNTF + gp130; различные рецепторы интерферона).
Компоненты модифицированной клетки хозяина для мониторинга активности связывания пептида, имеющего систему "дуального" рецептора, следующие: генная последовательность (а) является генной последовательностью, кодирующей протеин гетерологичного связывания; упомянутый связанный протеин, состоящий из одного пептида мультиплетного комплекса пептидного связывания или сегмента упомянутого пептида, который присоединен либо к ДНК связывающему домену, либо к его соответствующему домену транскрипциональной активации транскрипционального активационного протеина; и генная последовательность (б) является генной последовательностью, кодирующей протеин гетерологичного связывания; упомянутый связанный протеин, состоящий из второго пептида упомянутого мультиплетного комплекса пептидного связывания или сегмента упомянутого рецептора, который присоединен либо к ДНК связывающему домену, либо к его соответствующему домену транскрипциональной активации, какой бы из них ни использовался в (а). Модифицированная клетка хозяина для изучения мультиплетного комплекса пептидного связывания, такого как дуальная рецепторная система, также включает соответствующий ген-репортер и хромосомные мутации для специфического анализа лиганд-рецепторного взаимодействия, как обсуждается ниже. Можно экспрессировать третий пептид (например, лиганд) для установления контроля при сравнительном или конкурентном тестировании.
Как отмечалось выше, для изучения мультиплетных комплексов пептидного связывания, т.е. протеинов высшего порядка, которые содержат три и более пептида, в настоящем изобретении для экспрессии трех и более пептидов можно фактически использовать модифицированную клетку хозяина. В случае трипептидного комплекса связывания любые два из этих пептидов могут быть присоединены к этим двум компонентам транскрипционального активационного протеина. Например, для изучения взаимодействия лиганда, который взаимодействует через димеризацию рецептора, можно экспрессировать рецепторы как слитые протеины с лигандом, который экспрессируется как несвязанный протеин. Эта система клетки хозяина может также применяться в изучении многопротеиновых ферментных комплексов. Для любого многопептидного комплекса связывания можно идентифицировать новые пептиды, которые взаимодействуют с комплексом путем экспрессии новых протеинов из случайных комплементарных ДНК последовательностей (например, хромосомная сДНК библиотека), присоединенных к одному из доменов транскрипционального активационного протеина. В такой системе один из известных пептидов пептидного комплекса связывания присоединен к другому домену транскрипционального активационного протеина, пока другие единицы пептидного комплекса связывания экспрессируются как неприсоединенные пептиды. В дальнейшем отмечается, что количество пептидов, экспрессируемых модифицированной клеткой хозяина, должно быть ограничено только доступными средствами обнаружения и емкостью клетки хозяина.
Новые способы определения могут быть использованы для идентификации соединений, взаимодействующих с любой парой пептидного связывания, например любой рецептор и/или лиганд. Также эти модифицированные клеточные системы с геном-репортером для создания средства определения могут быть использованы в любом протеин-протеиновом взаимодействии для обнаружения новых соединений, которые разрушают это взаимодействие. Специфические примеры: а) протеинкиназы, вовлеченные в образование раковых опухолей, могут быть быстро вставлены в систему, чтобы быстро отыскать новые соединения, блокирующие киназно-нацеленное взаимодействие и таким образом могут служить уникальным противораковым терапевтическим средством; б) протеины оболочки вирусов, такие как гликопротеины вируса иммунодефицита человека и соответствующие рецепторные протеины клеточной поверхности, такие как CD4, могут быть быстро вставлены в систему, чтобы быстро отыскать новые соединения, которые нарушают такое взаимодействие и соответственно могут служить как антивирусные агенты; в) две субьединицы рибонуклеотид редуктазного энзима Plasmodium могут быть вставлены в систему для поиска соединений, которые препятствуют такой специфической ассоциации белков и таким образом могут служить как новые антималярийные агенты.
Следующие примеры обеспечивают дальнейшую иллюстрацию различных аспектов настоящего изобретения. Их не следует истолковывать как ограничивающие изобретение.
Пример 1: Специфическое и обратимое лиганд-рецепторное взаимодействие
Гены, кодирующие протеины связывания, генерируются клонированном сДНК-последовательностей гормона роста (GН) и его рецептора в плазмиды, содержащие кодирующую область для доменов Gal4. Слияния ДНК-связывающего домена (Gal4) конструируются в pAS2, который описан у Wade Harper и др. Слияния домена генной активации (Gal4) конструируются в рАСТ-II, который идентичен рАСТ (описанному у Durfee et al., 1993) за исключением модификации полилинкерной области. В Bgl II сайт была добавлена следующая последовательность: Bgl II - эпитоп гемагглютинина NdeI-NcoI-SmaI-BamHI-EcoRI-Xhol-Bgl II, адаптированную из полилинкерной последовательности pAS2 (Wade Harper et al., 1993). сДНК, кодирующая зрелый пептид порцина GH, сгенерирована, используя стандартную методику полимеразной цепной реакции (PCR) (см. Feeny, 1993).
Олигонуклеотиды, приготовленные в АВI олигосинтезаторе согласно опубликованной сДНК последовательности предназначены для свиного GH (см. Su и El-Gewely, 1988). 30 оснований 5'-олигонуклеотида содержали NcoI сайт (5'-C-A-T-G-C-C-A-T-G-G-A-G-G-C-C-T-T-C-C-C-A-G-C-C-A-T-G-C-C-C-3') и 27 оснований 3' олигонуклеотида содержали BamHI сайт (5'-C-G-G-G-A-T-C-C-G-C-A-A-C-T-A-G-A-A-G-G-C-A-C-A-G-C-Т-3'). GH сДНК получена, используя лямбда gt11 библиотеку гипофиза свиньи в качестве темплатного источника. Был получен 540 bр фрагмент, привязанный к pCR II вектору (Invitrogen Corp.), рекомбинанты подтверждены рестрикцией с помощью переваривающего фермента, и ДНК получена как описано у Maniatus et al., 1982. сДНК последовательность подтверждена с помощью ди-деокситерминатор-реакции с использованием реагентов и протоколов Perkin Elmer Cetus Corp. и ABI 373A автоматизированного секвенатора. ОН сДНК направлено клонированы в рАСТ-II через NcoI и BamHI сайты. сДНК, кодирующая внутриклеточный домен GHR, сгенерирована с использованием стандартных PCR методов. 33 основания 5'-олигонуклеотида, содержащего NcoI сайт (5'-C-A-T-G-C-C-A-T-G-G-A-G-A-T-G-T-Т-Т-С-С-Т-G-G-А-А-G-Т-G-G-G-G-C-T-3') и 39 оснований 3'-олигонуклеотида, содержащего кодон прерывания, за которым следовал NcoI сайт (5'-С-A-T-G-C-C-A-Т-G-G-С-C-T-A-C-C-G-G-A-A-A-T-C-T-T-C-T-T-C-A-C-A-T-G-C-T-G-C-C-3'), были использованы для генерации 742 bp фрагмента, кодирующего аминокислоты 1-247 GHR крысы (Baumbach et al., 1989). Этот GHR сДНК клонировали в pCRII вектор, как описано выше, а затем субклонировали в NcoI сайт pAS2 вектора. ДНК окончательных рекомбинантных векторов трансформировали в штамм(ы) дрожжей с помощью литий-ацетатного метода (Rose et al., 1990).
Дрожжевой хозяин (Y190), содержащий UASGAL-HIS ген-репортер, приготовлен по процедуре, описанной Wade Harper et al., 1993. Генотип штамма Y190-МАТа leu2-3, l 12 urа3-52 trpl-901 his3d200 ade2-101 gal4 gal80 URA3::GAL-lacZ LYS2: : GAL-HIS3 cyh. Штамм Y190 трансформирован по обеим конструкциям связывания или по одной плюс противолежащий вектор, не содержащий гетерологичных последовательностей. Для всех штаммов найдено проявление одинакового роста на неселективной среде (фигура 2А). Затем эти штаммы тестировались на рост на селективной среде (т.е. на ростовой среде с недостатком аминокислоты, которая синтезируется при активации гена-репортера). Только штамм, содержащий оба гибридных протеина (CY722), способен к росту, в то время как штамм, содержащий только либо лиганд, либо рецептор связывания, не проявляет роста (CY724 и CY723 соответственно; фигура 2В). Два независимых образца каждого штамма образуют полосы на синтетической среде, содержащей 2% глюкозы, дрожжевую азотную основу, сульфат аммония, 0,1 мМ аденина и 60 мМ 3-аминитриазола (пластина В) или на той же среде, дополненной гистидином (пластина А). Пластина А выдерживается при 30oС трое суток; пластина В пять суток. Эти результаты демонстрируют, что GH и GHR могут быть связующим звеном для Саl4-зависимой активации гена-репортера при взаимодействии с предполагаемым связыванием лиганда и рецептора.
Пример 1А. Конкурирующий экспрессируемый свободный лиганд (GH) к присутствии GH и GHR протеинов связывания
Чтобы доказать неоспоримое связывание GH к своему рецептору в чуждой среде ядра дрожжей, систему модифицировали добавлением третьей плазмиды, выступающей посредником экспрессии "свободного" лиганда, чтобы показать, что GH пептид конкурирует с GH-Gal4 протеином связывания, обращая 2-гибридное взаимодействие, показанное в примере 1. Родительский штамм Y190 (Wade Harper et al., 1993) выращивается на среде, содержащей 2-фтор оротат, чтобы выбрать производные, которые спонтанно теряют URA3 ген (см. Rose et al., 1990). Получающийся в результате штамм, обозначенный как CY770, используется для всех экспериментов, выясняющих эффект протеина, одновременно экспрессирующегося из третьего компонента, а именно третьей плазмиды. сДНК, лидирующая GH, генерируется с помощью методов PCR, используя 38 основной 5'-олигонуклеотид, содержащий EcoRI сайт (5'-C-C-G-A-A-T-T-C-A-A-A-А-Т-G-G-C-С-Т-Т-С-С-С-A-G-С-С-A-T-G-C-C-C-T-T-G-T-C-C-3') и 26-основной 3'-олигонуклеотид, содержащий HindIII сайт (5'-C-C-A-A-G-C-T-T-C-A-A-C-T-A-G-A-A-G-G-C-A-C-A-G-C-Т-3') для последующего субклонирования в вектор pCUP. pCUP является индуцибельным вектором экспрессии дрожжей, производным pRS316 (Hill et al., 1986). Короче говоря, этот вектор конструируется вставкой 3'-конца дрожжевого PGK гена (из pPGK; Kang et al., 1990) в pRS316 клонирующий регион как BamHI-SalI фрагмент, чтобы служить транскрипциональным прерывателем. Что касается этой плазмиды, то CUP1 промотор-регион (Butt et al., 1984) амплифицируется с помощью PCR как SacI-EcoRI фрагмент и вставляется в соответствующие сайты плазмиды для создания pCUP. Плазмида GН экспрессии (GH-pCUP) затем трансформируется с GH и GHR конструкциями слияния в штамм CY770 для генерации CY781. Показано, что конкурентная экспрессия свободных GH и GHR протеинов связывания (CY781) блокирует GH-GHR-зависимый клеточный рост на селективной среде (фигура 2В). Этот эксперимент является типичным испытанием конкуренции in vivo и демонстрирует обратимость лиганд-рецепторного взаимодействия.
Пример 1В. Связывание пептидного гормона пролактина (PRL) и его рецептора
Для расширения и проверки правильности данной технологии была разработана подобная система с использованием пептидного гормона пролактина (PRL) и его рецептора. Пролактин структурно напоминает GH, а пролактиновый рецептор (PRLR) - также член надсемейства цитокиновых рецепторов. В отличие от человеческого GH, субприматный GH не связывает легко PRLR (Young and Bazer, 1989), ни PRL не связывает легко GHR (Leung et al., 1987). Зрелый свиной PRL сгенерирован как продукт присоединения к домену активации GAL4. Олигонуклеотиды конструировались для свиного PRL (получен из генного банка X14068) и использовались для получения зрелого свиного протеинового гормона PRL из свиной гипофизной лямбда gt11 библиотеки с использованием стандартных PCR методов. 31-основной 5'-олигонуклеотид включает Е сoRI сайт (5' -C-G-G-А-А-Т- Т-С-T-G-C-C-C-A-T-C-T-G-C-C-C-C-A-G-C-G-G-G-C-C-T-3') и соответствует последовательностям, кодирующим аминокислоты 1-7. 30-основной 3'-олигонуклеотид содержит EcoRI сайт (5'-G-А-А-Т-Т-С-А-С-G-T-G-G-G-C-Т-Т-A-G-C-A-G-T-T-G-C-T-G-T-T-G-3') и соответствует региону сДНК 3', относящемуся к эндогенному кодону прерывания. Получен 600 bр фрагмент, присоединенный к pCR II вектору, что подтверждено переработкой рестрикционным энзимом и анализом последовательностей. PRL сДНК клонирована в рАСТ-11 через EcoRI сайт.
Внеклеточный домен свиного PRL рецептора (PRLR) сгенерирован как присоединенный к GAL4 ДНК домену связывания. Олигонуклеотиды оформлялись, исходя из последовательности мышиного PRLR (Davis and Linzer, 1989). 31-основной 5'-олигонуклеотид содержит Smal сайт (5'-Т-С-С-С-C-C-G-G-G-G-A-T-G-T-C-A-T-C-T-G-C-A-C-T-T-G-C-Т-Т-А-С-3'), в то время как 31-основной 3'-олигонуклеотид содержит кодон прерывания, за которым идет SalI сайт (5'-T-C-C-G-T-C-G-A-C-G-G-T-C-T-T-T-C-A-A-G-G-T-G-A-A-G-T-C-A-T-T-3'). Эти олигонуклеотиды примыкают к внеклеточному домену PRLR, кодирующему аминокислоты 1-229. В качестве темплатного источника использовалась свиная гипофазная лямбда gt11 библиотека. Используя стандартные PCR методы, сгенерирован 687 bр фрагмент, присоединенный к pCRII, и подтверждена нуклеотидная последовательность. PRLR сДНК клонирована в pAS2 вектор через Smal и SalI сайты рестрикции.
Штамм Y190 был трансформирован с помощью PRL или PRLR плазмид экспресии связывания либо один (CY727 или CY728 соответственно), либо вместе (CY726). Клетки, экспрессирующие как PRL, так и PRLR слияния, способны расти на селективной среде, в то время как штаммы, содержащие только один лиганд или рецептор связывания, не способны. Эти результаты отражают полученные для GH-GHR системы в примерах, приведенных выше, и доказывают общую способность 2-гибридной системы для изучения лигандного связывания с членами этого надсемейства рецепторов.
Пример 1С. Дополнительное подтверждение лиганд-рецепторной специфичности для системы новых дрожжевых клеток хозяина
Для оценки лиганд-рецепторной специфичности разработаны дополнительные штаммы. URA минус штаммы, экспрессирующие GH и GHR протеины связывания, трансформированы с помощью pCUP или PRL-pCUP; в то время как штаммы, экспрессирующие PRL и PRLR протеины связывания, трансформированы pCUP илиPRL-pCUP. Короче, PRL-pCUP создается в манере, подобной той, которая описана для GH-pCUP. PRL сДНК сгенерирована с помощью PCR, используя 33-основной 5'-олигонуклеотид с EcoII сайтом (5'-G-A-A-T-T-C-A-A-A-A-T-G-C-T-G-C-C-C-A-T-C-T-G-C-C-C-C-A-G-C-G-G-G-3') и 3'-олигонуклеотид, приведенный в примере 1В. Результирующий фрагмент введен в pCUP через EcoRI сайт. Как продемонстрировано в примерах выше, штамм, экспрессирующий GH и GHR связывания, без какого-либо конкурентного компонента растет на селективной среде, и этот рост прекращается при коэкспрессии свободного GН. Пролактиновый эксперимент приводит к подобным результатам, которые подтверждают специфичность лиганд-рецепторного связывания в дрожжевой клетке. Штамм, несущий PRL и PRLR связывания (CY787), может расти на селективной среде, и этот рост останавливается экспрессией свободного PRL (CY786; таблица).
Чтобы испытать селективность GHR, штамм, содержащий GH и GHR связывания, трансформировался с помощью PRL-pCUP. Этот штамм растет на селективной среде (CY785, таблица). Эти данные показывают, что связывание GH со своим рецептором в этой системе может эффективно конкурировать с избытком GH (CY751). Результаты приведенных экспериментов, экспрессирующих три гетерологичных протеина, иллюстрируют специфичность лиганд-рецепторного(ых) взаимодействия(ий) в системе, составляющей данное изобретение.
Пример 2. Скрининг соединений, нарушающих лиганд-рецепторное взаимодействие
Слабокопирующие плазмиды, экспрессирующие GHR- или GH-Gal4 протеины связывания (рOZ153 и pOZ152 соответственно), создаются для сокращения экспрессии этих протеинов. Вдобавок, новый ген-репортер создается для предотвращения пролиферации клеток на селективной среде пока не прервана экспрессия. Для создания плазмиды GHR экспрессии связывания SacI-BamHI фрагмент рестрикции, содержащий дрожжевой конститутивный промотор и GAL4 последовательности, изолируется из pASI (Durfee et al., 1988). Внеклеточный домен GHR затем присоединяется к GAL4 лигатурно как NcoI фрагмент, как описано в примере 1, создавая pOZ153. Для создания GH конструкции экспрессии связывания полный GH-Gal4 регион с последовательностями промотора и прерывателя изолируется из плазмиды, описанной в примере 1, как PvuI-SalI фрагмент. Этот сегмент ДНК клонируется в pUNl00 (Elledge and Davis, 1988), образуя рOZ152. Ген-репортер создается выделением дрожжевого CYH2 кодирующего региона и оперативным присоединением его к GAL промотору в дрожжевой плазмиде экспрессии. Короче, GAL1 промоторный регион вставляется в Yep352 (Hill et al., 1986) как 685 bр EcoRI-BamHI фрагмент. CYH2 последовательности амплифицируются с помощью PCR при помощи олигонуклеотидных праймеров (5'-G-G-A-T-C-C-A-A-T-C-A-A-G-A-A-T-G-C-C-T-T-C-C-A-G-A-T-3' и 5'-G-C-A-T-G-C-G-T-C-A-T-A-G-A-A-A-T-A-A-Т-А-С-A-G-3') и pAS2 в качестве темплата. Продукт PCR перерабатывается BamHI плюс SphI и клонируется в соответствующие сайты в YEp352-GAL вектор. Эти плазмиды трансформируются в дрожжевой штамм CY770, который несет мутацию в хромосомном CYH2 гене, приводя к резистентности штамма к ингибитору синтеза белка циклогексимиду. Присутствие всех трех плазмид необходимо, чтобы образовалась чувствительность к циклогексимиду (суh.).
Штамм (CY857), содержащий плазмиды связывания лиганда и рецептора плюс плазмиду репортера, образует основу для простого первичного скрининга соединений, которые прерывают связывание GH со своим рецептором. Штатм CY857 помещается в стандартную дрожжевую питательную среду, содержащую 10.0 μг/мл циклогексимида. В результате лиганд-рецепторного взаимодействия, управляющего экспрессией CYH2 гена-репортера, штамм является суh. и таким образом неспособным к росту. В эту тестовую среду вносятся химические соединения. Соединения, которые ослабляют GH-GHR связывание, идентифицируются по росту клеток, окружающих соединение (место внесения), потому что в отсутствие CYH2 экспрессии клетки становятся устойчивыми к циклогексимиду, присутствующему в среде.
Вторичный скрининг для определения мишеней образца.
Повреждение лиганд-рецепторного связывания в этом тесте происходит в результате реакции соединения либо с рецептором, либо с лигандом как компонентом связывания. Специфическая мишень нового соединения определяется простым вторичным тестом, использующим штаммы, избыточно экспрессирующие один из протеинов связывания. Штамм CY858 экспрессирует GHR-GAL4 связывание в большом избытке благодаря тому, что в пределах клетки поддерживается высокое число копий (pOZ149), в то время как GH-связывание (pOZ152) поддерживается на уровне таком же, как у базового штамма (CY857). Наоборот, штамм CY859 экспрессирует GH-GAL4 связывание в большом избытке благодаря тому, что в пределах клетки поддерживается высокое число копий (pKY14), в то время как GHR-связывание (рOZ153) поддерживается на уровне таком же, как у базового штамма (CY857). Соединения, восстанавливающие рост в первичном скрининге с использованием CY857 (GH и GHR связывания экспрессируются на слабокопирующих плазмидах), затем тестируются тем же самым способом, используя CY858 (GHR>>GH) или CY859 (GH>>GHR) как тестовые штаммы. Например, когда лиганд-рецепторное связывание ингибируется соединением, реагирующим с GHR, вторичный скрининг продемонстрирует детектируемое изменение в измеряемом фенотипе. Вторичное тестирование восстанавливающего соединения на штамме CY858, который сверхэкспрессирует GHR-связывание, проявляет меньший рост в присутствии соединения, чем наблюдаемый у CY859. Это детектируемое изменение в измеряемом фенотипе происходит потому, что сверхобилие GHR титрует соединение, таким образом увеличивая CYH2 экспрессию и ингибируя клеточный рост. CY859 продуцирует детектируемое изменение, подобное CY857, потому что лимитирует GHR протеин связывания. Соединение, взаимодействующее с лигандом связывания, в этом вторичном тесте демонстрирует обратное изменение в измеряемом фенотипе.
Пример 3. Демонстрация лигандзависимой димеризации рецептора.
Мультиплетные протеиновые взаимодействия (например, лиганд-рецептор-рецептор) исследуются с помощью расширенной системы, которая репрессирует третий протеин, используя следующую схему.
Одна единица димера рецептора генерируется как протеин связывания либо с помощью Gal4 ДНК связывания, либо домена активации. Другая единица димеpa рецептора генерируется как протеин связывания с помощью соответствующего Gal ДНК связывания или домена активации, какой бы ни использовался для первого связывания. Ген, кодирующий лиганд, экспрессируется из третьей плазмиды и продуцируется как свободный (без связывания) лиганд. Взаимодействие протеинов связывания происходит только в присутствии лиганда (см. фигуру 3).
Взаимодействие фактора роста клеток сосудистого эндотелия (VEGF) с доменом лигандного связывания его родственного рецептора (KDR, рецептор, содержащий домен киназной вставки) описано как пример этой системы. KDR является тирозин-киназным рецептором и предполагается, что образование димера (1 лиганд-2 рецептора) важно для гормониндуцируемой рецепторной функции. сДНК, кодирующая лигандный домен KDR (Тerman et al., 1991), изолирована как NcoI-BamHI фрагмент и клонирована как в рАСТ-2, так и в pAS2 векторы. сДНК, кодирующая зрелый протеин для VEGF, сгенерирована с использованием стандартных PCR методик. Олигонуклеотиды получены по опубликованной последовательности (см. Tischer et al., 1991). 34-основной 5' олигонуклеотид, содержащий EcoRI сайт (5'-C-G-G-A-A-T-T-C-G-A-A-G-T-A-T-G-G-C-A-C-C-C-A-T-G-G-C-A-G-A-A-G-G-A-3') и 28-основной 3'-олигонуклеотид, содержащий EcoRI сайт (5'-C-G-G-A-A-T-Т-С-G-G-A-T-C-T-T-C-A-T-T-C-A-T-T-C-A-T-C-A-3'), использованы для генерации 450 bp фрагмента, кодирующего зрелый протеин, и клонированы в EcoRI сайт pCUP. ДНК окончательных рекомбинантных векторов трансформирована в дрожжи литий ацетатным методом для генерации подходящих штаммов.
Дрожжевой штамм хозяина (CY770) трансформирован с помощью KDR-рАСТ-2, KDR-pAS2 и VEGF-pCUP для генерации штамма CY846; или трансформирован с помощью как рецепторного связывания, так и pCUP, дав штамм CY847. Дополнительно как KDR-pACT-2, так и KDR-pAS2 трансформированы совместно (CY845) или отдельно (CY843 или CY844), или только VEGF-pCUP (CY841) как контрольные штаммы. Штаммы тестировались на рост на селективной среде. Штамм (CY846), который экспрессирует VEGF лиганд плюс два рецепторных протеина связывания, проявляет существенный рост на селективных средах по сравнению со штаммом CY847, который не экспрессирут VEGF лиганд (см. фигуру 4). Эти результаты показывают, что эффективные клетки в данном изобретении могут использоваться для изучения лигандзависимой димеризации рецептора.
Пример 4. Скрининг соединений, которые действуют как лиганды в димерной рецепторной системе.
Димеризация (олигомеризация) рецепторных единиц является часто важным первым шагом в активации рецепторов, таких как рецепторы ростовых факторов, цитокины и описанные ранее. Оригинальная клеточная система, описанная в примере 3, может быть применена для обнаружения новых соединений, которые промотируют (или блокируют) димеризацию рецептора. Такие новые взаимодействующие соединения могут служить эффективными терапевтическими средствами для патологий, связанных с этими рецепторами.
Плазмиды, экспрессирующие димерную(ые) рецепторную(ые) единицу(ы) как связанные протеины, генерируются как обсуждалось в примере 3. Штамм (CY845), содержащий KDR-pACT-II и KDR-pAS2 связывания, служит примером простого первичного скрининга рецепторов, проявляющих димерную структуру. Штамм CY845 внедрен на синтетическую агаровую среду с недостатком гистидина (Rose et al. , 1990). Тестовые соединения наносились на верх этой тестовой среды. Химические соединения, которые индуцируют взаимодействие этих двух связываний рецептора (в отсутствие лиганда), приводят к перестройке эндогенного транскрипционального активатора, который присоединен к гену-репортеру, такому как HIS3. Реорганизация идентифицируется по росту клеток, окружающих соединение.
Цитируемые публикации:
Baumbach WR, Horner D. and JS Logan (1989). The growth hоrmone binding protein in rat serum is an alternatively spliced form of the rat growth hormone receptor. Genes & Devel. 3: 1199-1205 [Ростовой гормональный протеин связывания в сыворотке крысы является альтернативно сращенной формой ростового гормонального рецептора крысы].
Butt TR, Sternberg EJ, German JA, Clark P, Hamer D, Rosenbеrg M and ST Crooke (1984). Copper metallothiоnein of yeast, structure of the gene and regulation of expressison. Proc. Natn. Acad. Sci. USA 81: 3332-3336 [Медный металлотионеин дрожжей, структура гена и регуляция экспресии].
Chein C-T., Bartel PL, Sternglanz R and S Fields (1991). The two hybrid system: A method to identify and clone genes for protein that interact with a protein of interest. Proc. Natn. Acad. Sci. USA. 88: 9578-9582 [Двухгибридная система: Способ идентификации и клонирования генов для белков, которые взаимодействуют с интересуемым белком].
Cunningham ВС, Ultsh M, De Vos AM, Mulkerrin МG, Clauser KR and JA Wells (1991). Dimerization of the extracellular domain of the human growth hormone receptor by a single, hormone molecule. Science. 254: 821-825 [Димеризация внеклеточного домена гормонального ростового рецептора человека посредством единственной молекулы гормона].
Davis J and DIH Linzer (1989). Expression of multiple forms ci the prolactine receptor in the mouse liver. Mol. Endocrinol. 3: 674-680 [Экспрессия мультиплетных форм пролактинового рецептора в печени мыши].
Davis S, Aldrich TH. Stahl N, Pan L, Taga T, Kishimoto T. Ip NY and G Yancopoulos (1993). LIFR and gp l30 as heterodimerizing signal transducers of the tripartate CNTF receptor. Science. 260: 1805-1808 [LIFR и gp 130 в качестве трансдукторов гетеродимеризирующих сигналов трипартатного CNTF рецептора].
Durfee Т, Becherer К, Chen P-L, Yeh S-H, Yang Y, Kilburn AE, Lee W-H and SJ Elledge (1993). The retinoblastoma protein associated with the protein phosphatase type 1 catalytic subunit. Genes and Devel. 7: 555-569 [Ретинобластомадьный протеин, связанный с каталитической единицей протеи н-фосфатазы типа 1].
Elledge. SJ and RW Davis (1988). A family of versatile centromeric vectors disigned for use in the secreting shuffle mutagenesis assay in the Sacchaiumyces cerevisiae. Gene. 70: 303-312 [Семейство многосторонних ценромерных векторов, предназначенных для использования в секреторно-случайном мутагенном тесте на Saccharomyces cerevisiae].
Fields S and О Song (1989). A novel genetic system to detect рrotein-protein interaction. Nature. 340: 245-246 [Оригинальная генетическая система для детектирования протеин-протеин взаимодействий].
Finny М (1992). The polymerase chain reaction. In: Current Protocols in Molecular Biology. Chapter 15. Eds (FM Ausubel, R Brent, RE Kingston, DD Moore, JG Seidman, J Smith and К Struhl). John Willey & Sons, NY [Полимеразная цепная реакция].
Fuh G, Cunningham ВС, Fukunaga R, Nagata S, Goeddel DV and JA Wells (1992). Rational design of potent antagonists to the human growth hormone receptor. Science. 256: 1677-1680 [Рациональный замысел мощных антагонистов человеческого рецептора гормона роста].
Fuh G, Colosi P, Wood WI and JA Wells (1993). Mechanisms based design of prolactine receptor antagonists. J. Biol. Chem. 8: 5376-5381 [Механизмы - базовая концепция антагонистов пролактинового рецептора].
Hill JE, Myers AM, Koerner TJ and A Tzagoloff (1986). Yeast /E.Coli shuttle vectors with multiple unique restriction sites. Yeast. 2: 163-167 [Дрожжевые /E. Coli челночные векторы с мультиплетными уникальными сайтами рестрикции].
Kang Y-S, Kane J, Kurjan J, Stadel JM and DJ Tipper (1990). Effects of expression of mammalian G and hybrid mammalian-yeast G proteins on the yeast pheromone response signal transduction pathway. Mol. Cell. Biol. 10: 2582-2590 [Эффекты экспресии G-млекопитающих и гибридных G-млекопитающе-дрожжевых протеинов на пути преобразования сигнала феромона дрожжей].
Kondo M, Takeshita Т, Ishii N, Nakamura M, Watenabe S, Arai К-i and К Sugamura (1993). Sharing of the interleukin-2 (IL-2) receptor chain between receptors for. Science. 262: 1874-1877 [Разделение цепи рецептора интерлейкин-2 (IL-2) между рецепторами IL-2 и IL-4].
Leung DW, Spencer SA, Cacianes G, Hammonds G, Collins C, Henzel WJ, Barnard R, Waters MJ and WI Wood (1987). Growth hormone receptor and serum binding protein: purification, cloning and expression. Nature. 330: 537-543 [Рецептор гормона роста и сывороточный связывающий протеин: очистка, клонирование и экспрессия].
Li JJ and I Herskowitz (1993). Isolation of ORG6, a component of the yeast origin recognition complex by a one-hybrid system. Science. 262: 1870-1874 [Выделение ORG6, компонента комплекса распознавания дрожжевого происхождения с помощью одногибридной системы].
Maniatus Т, Fritsch EF and J Sambrook (1982). Molecular Cloning. Cold Spring Harbor Laboratory Press [Молекулярное клонирование].
Mui A and A Miyajima (1994). Citokine receptors and signal transduction. In: Progress in Growth Factor Research, pp. 15-35. Pergamon Press. NY (Цитокиноьые рецепторы и преобразование сигналов].
Noguchi M, Nakamura Y, Russell SM, Zeigler SF, Tsang M, Сao Х and WJ Leonard (1993). Interleiikin-2 receptor chain: A functional component of the interleukin-7 receptor. Science. 262: 1877-1880 [Цепь интерлейкин-2 рецептора: функциональный компонент интерлейкин-7 рецептора].
Picard D, Schena M and KR Yamamoto (1990). An inducible expression vector for both fission and budding yeast. Gene. 86: 257-261 [Вектор индуцируемой экспресии как для делящихся, так и почкующихся дрожжей].
Rose MD, Winston F and P Hieter (1990). Methods in yeast genetics. Cold Spring Harbor Laboratory Press [Методы генетики дрожжей].
Staten NR, Byatt JC and GG Krivi (1993). Ligand specific dimerization of the extracellular domain of the bovine growth hormone receptor. J. Biol. Chem. 268: 18467-18473 [Лигандно-специфическая димеризация внеклеточного домена рецептора бычьего гормона роста].
Su T-Z and MR El-Geweley (1988). A multisite - directed mutagenesis using T7 DNA polymerase: application for the reconstructing a mammalian gene. Gene. 69: 81-89 [Многосайтовый направленный мутагенез с использованием Т7 ДНК полимеразы: применение для реконструкции гена млекопитающих].
Taga Т and Т Kishimoto (1993). Cytokine receptors and signal transduction. FASEB J. 7: 3387-3396 [Цитокиновые рецепторы и преобразование сигналов].
Taga T, Hibi M, Matsuda Т, Hirano T and T Kishimoto (1993). IL-6-induced homodimerization of gp l30 and associated activation of a tyrosuie kinase. Science. 260: 1808-1810 [lL-6-индуцированная гомодимеризация gpl30 и связанная с ней активация тирозин-киназы].
Terman BI, Dougher-Vermanzen M, Carrion ME, Dimitruv D, Armellina DC, Gospodarowitz D and P Bohlen (1992). Identification of the KDR tyrosine kinase as a receptor for vascular endothelial cell growth factor. Biochem. Biophys. Res. Comm. 187: 1579-1586 [Идентификация KDR тирозин-киназы как рецептора клеточного фактора роста эндотелия сосудов].
Terman BI, Carrion ME, Kovach E, Rasmussen BA, Eddy RL and В Shaws (1991). Identification of a new endothelial cell growth factor receptor tyrosine kinase. Oncogene. 6: 1677-1683 [Идентификация новой клеточной эндотелиадьной рост-фактор-рецепторнои тирозин-киназы].
Tischer E, Mitchell R, Hartman T, Silva T, Gospodarowitz D, Fiddes JC and JA Abraham (1991). The human gene for vascular endothelial growth factor. Multiple protein forms are encoded through alternative exon splicing. J. Biol. Chem. 266: 11947-11954 [Человеческий ген сосудистого эндотелиального фактора роста. Мультиплетные протеиновые формы кодируются посредством альтернативного сращивания экзона].
Yaug X, Hubbard JA and M Carlson (1992). A protein kinase substrate identified by the two-hybrid system. Science. 257: 31-33 [Протеин-киназный субстрат, идентифицированный с помощью двухгибридной системы].
Young KH and FW Bazer (1989). Porcine endometrial prolactine receptors detected by homologous radioreceptor assay. Mol. and Cell. Endocrinol. 64: 145 154 [Свиные внутриматочные пролактиновые рецепторы, детектируемые при помощи гомологичного радиорецепторного теста].
Young PR (1992). Protein hormones and their receptors. Curr. Opin. Biotech. 3: 408-421 [Белковые гормоны и их рецепторы].
Wade Harper J, Adami GR, Wei N, Keyomarsk К and SJ Elledge (1993). The p21 Cdk-interacting protein Cip1 is a potent inhibitor of Gl Cyclin-dependent kinase. Cell. 75: 805-816 [p21 Cdk-взаимодействующий протеин Cip1 является мощным ингибитором Gl циклинзависимой киназы].
Wilson ТЕ, Fahrner TJ, Johnston M and J Milbrandt (1991). Identification of the DNA binding site for NGFI-B by genetic selection in yeast. Science. 252: 1296-1300 [Идентификация ДНК-связывающего сайта для NGFI-B с помощью генетической селекции дрожжей].
Пример А.
Гормон роста (GH) вызывает димеризацию родственного с ним рецептора (GHR).
Предпосылки.
Взаимодействие гормона роста (GH) со связывающей лиганд областью соответствующего ему рецептора (GHR) описано в примерах 1 и 1А данной заявки. GH может взаимодействовать с соответствующим ему рецептором в стехиометрическом соотношении 1:1, а также 1:2. Взаимодействие GH с первой молекулой GHR является связыванием с высоким сродством, а далее реакция молекулы GH со второй молекулой GHR является взаимодействием с более низким сродством. Области, участвующие в лиганд-рецепторном взаимодействии в GH-модели димеризации, используют различные участки GH-лиганда, но идентичные участки двух молекул рецептора (Cunningham et al., 1991, Cunningham and Wells, 1993). Модифицированные клетки по изобретению можно использовать для того, чтобы найти подходящие методы исследования, касающиеся взаимодействия белков, вовлеченных в GH/GHR-димеризацию, как показано ниже.
Экспериментальная часть.
Олигонуклеотиды получают на синтезаторе олигонуклеотидов ABI в соответствии с последовательностью, опубликованной для GHR-крысы (Baumbach et al., 1989). кДНК, кодирующую внеклеточную область, GHR, получают стандартными методами PCR (ПНР). Смысловой олигонуклеотид из 31 основания, содержащий сайт Bgl II (5'-G-A-A-G-A-T-C-T-G-G-A-T-G-T-T-T-C-C-T-G-G-A-A-G-T-G-G-G-G-C-T-3') и антисмысловой олигонуклеотид из 37 оснований, содержащий стоп-коды и сайт Bgl II (5'-G-A-A-G-A-T-C-T-C-C-T-A-C-C-G-G-A-A-A-T-C-T-T-C-T-T-C-A-C-A-T-G-C-T-G-C-C-3'), используют для получения фрагмента из 742 пар оснований, кодирующего аминокислоты 1-257 GHR крысы. Эту кДНК, кодирующую внеклеточную область GH, клонируют в вектор pCR II, как описано в данной заявке (см. пример 1), а затем субклонируют сайту Bgl II плазмиды рАСТ II, как описано в данной заявке. Эта плазмида экспрессирует GHR в виде слияния с дрожжевым Gal4 ДНК-связывающим белком. ДНК конечных векторов GHR-pAS2 (описано в примере 1), GH-pCUP (описано в примере 1А) и GHR-pACT II трансформируют в дрожжи литийацетатным методом, получая соответствующие штаммы.
Штамм дрожжевых клеток-хозяев (CY770) трансформируют с помощью GHR-pACT II, GHR-pAS2 и GH-pCUP, получая штамм CY886; или трансформируют с помощью GHR-pACT II, GHR-pAS2 и pCUP, получая штамм CY887. Дополнительные штаммы получают трансформацией с помощью GHR-pACT-II, GHR-pAS2 и GH-pCUP для штамма CY901; или трансформацией рАСТ II, GHR-pAS2 и GH-pCUP для штамма CY899, и они служат в качестве контрольных штаммов. Штаммы испытывают на стимуляцию транскрипции репортерного гена UASGAL-HIS3, как указано, выращивая на среде для количественного определения (синтетическая среда, не содержащая гистидина, лейцина, триптофана и урацила), дополненной 60 мМ аминотриозола. Штаммы CY901 и CY899, экспрессирующие единственное слияние с рецептором и неслитый GH-лиганд, не растут на элективной среде. У штаммов (CY886), экспрессирующих свободный GH-лиганд плюс два белка, слитых с GH-рецептором, наблюдается значительный рост на элективной среде по сравнению со штаммом CY887, который не экспрессирует GH-лиганд (см. фигура А декларации). Это открытие показывает полезность изобретения для демонстрации как мономерных, так и димерных белковых комплексов в соответствии со структурными данными для GH и GHR (Cunningham et al., 1991). Модифицируемые клетки, заявляемые в формуле изобретения, включающие GH или GHR (пример 2) или GH/GHR/GHR, можно адаптировать для осуществления в качестве механизма основы для скрнинга с целью обнаружения новых молекул, действующих на эти различные мономерные или димерные комплексы.
Прилагаемая фигура А описывается следующим образом. Штаммы, экспрессирующие указанные белки, засевают штрихом на среду для количественного определения (синтетическая среда, не содержащая лейцина, триптофана, урацила и гистидина), дополненной 60 мМ 3-аминотриозола, инкубируют 5 дней. Индекс на верху AD указывает, что внеклеточный домен GHR экспрессирует в виде слитого белка с доменом активации Gal4; верхний индекс BD указывает, что внеклеточный домен GHR экспрессирует в виде слитого белка с ДНК-связывающим доменом белка Gal4. GH без верхнего индекса показывает экспрессию в виде неслитого белка при использовании pCUP. Черточки (тире) указывают, что штамм несет немодифицированный вектор (рАСТ-II, pAS2 или pCUP). Два независимых изолята каждого штамма содержатся в каждом квадранте.
Пример В.
Взаимодействие инсулиноподобного фактора роста I (IGF-I) с лигандсвязывающей областью соответствующего ему рецептора.
Предпосылки (основание).
Лигандсвязывающая область рецептора IGF-I содержится в альфа-субъединице рецептора IGF-I. Рецептор, рецептор тирозинкиназы, имеет тетрамерную структуру, состоящую из двух альфа и двух бета субъединичных белковых цепей. Альфа-субъединица образуется ферментативным расщеплением одиночного мембранного белка, содержащего альфа и бета аминокислотные последовательности, после введения в клеточную мембрану. Альфа-цепь локализована вне клетки (экстрацеллюлярно) и взаимодействует с внеклеточной частью бета-цепи с помощью внеклеточных цистеиновых мостиков.
Экспериментальная часть.
Олигонуклеотид синтезируют на синтезаторе олигонуклеотидов ABI и "проектируют" в соответствии с опубликованной последовательностью кДНК для IGF-I крысы (Roberts et al., 1987). Смысловой олигонуклеотид из 36 оснований содержит сайт EcoRI (5'-C-G-A-A-T-T-C-C-C-A-T-G-G-T-C-A-T-G-T-C-G-T-C-T-T-C-A-C-A-T-C-T-C-T-T-C-3') и антисмысловой олигонуклеотид из 28 оснований содержит сайт EcoRI (5'-G-G-A-A-T-T-C-T-G-C-T-C-A-A-G-C-A-G-C-A-A-A-G-G-A-T-C-T-3'). кДНК IGF-I получают стандартными PCR-методами. Источником ДНК-темплата служит библиотека на основе лямбда gtl 1 печени крыс (Clontech Corp.). Получают фрагмент из 526 пар оснований, кодирующий гормон и лигируют в вектор pCRII, и рекомбинанты подтверждают расщеплением с помощью рестриктаз. кДНК подтверждают, анализируя нуклеотидную последовательность. Для конструкции IGF-I-рАСТ-II смысловой олигонуклеотид из 36 оснований, содержащий сайт EcoRI (5'-C-G-A-A-T-T-C-G-A-A-A-A-A-T-G-T-C-G-T-C-T-T-C-A-C-A-T-C-T-C-T-T-C-3'), и антимысловой олигонуклеотид (см выше) используют для получения фрагмента из 523 пар оснований, кодирующего гормон, и лигируют в вектор pCRII. Строение кДНК подтверждают анализом нуклеотидной последовательности. кДНК IGF-I клонируют по сайту EcoRI плазмиды рАСТ-II. Для получения IGF-I-pAS2 фрагмент NcoI-XhoI IGF-1-pACT-II непосредственно клонируют по сайтам NcoI-SalI плазмиды pAS. Вектор pAS идентичен pAS2, но ген CYH2 отсутствует.
Альфа-субъединицу рецептора IGF-I (IGF-IRa) получают в виде слитого белка с ДНК-связывающим доменом Gal4. Олигонуклеотид "планируют" на основе последовательности IGF-IR человека (Ulrich et al., 1986). Смысловой олигонуклеотид из 34 оснований содержит сайт EcoRI (5'-C-G-G-A-A-T-T-C-G-A-A-G-T-A-T-G-G-A-A-A-T-C-T-G-C-G-G-G-C-C-A-G-G-A-3'), того как антисмысловой олигонуклеотид из 32 оснований содержит терминирующий кодон с последующим сайтом EcoRI (5'-C-G-G-A-A-T-T-C-T-C-A-T-C-T-C-C-G-C-T-T-C-C-T-T-T-C-A-G-G-T-C-T-3'). Эти олигонуклеотиды фланкируют альфа-субъединицу рецептора IGF, кодирующего аминокислоты 1-710. РНК тимуса свиньи используется в реакции обратной транскрипции, примированной случайными шестичленниками, и служит в качестве матричной ДНК для RT-PCR методов получения фрагмента из 2253 пар оснований. PCR-фрагмент лигируют в вектор pCRII и субклонируют с помощью сайтов рестрикции EcoRI в сайт EcoRI плазмиды рАСТ-II. Строение рекомбинантной плазмиды IGF-IRa-pACT-II подтверждают анализом нуклеотидной последовательности.
Штамм дрожжевых клеток-хозяев (CG1945; Clontech), содержащих маркерный ген UASGAL-HIS3, трансформируют при использовании конечных ДНК. Генотип штамма CG1945 представляет собой MATa, ura3-52, his3-200, lys2-801, trp 1-901, ade2-201, leu2-3,112, gal4-542, gal80-538, LYS::UASGAL-HIS3, cyh2, URA3:: (Gal4 17 mers)3-CYCl-lacZ. Репортерный (маркерный) ген HIS3 в этом штамме регулируется более строго благодаря последовательности ТАТА-бокса HIS3, что приводит в результате к пониженной фоновой экспрессии при использовании этого репортерного гена. Это является благоприятным для опытных испытаний, которые можно проводить, используя низкие или нулевые концентрации 3-аминотриазола. Штамм CG1945 трансформируют с применением IGF-1-pAS и IGF-IRa-pACT-II, получая штамм CG11; или трансформируют с помощью pAS и IGF-IRa-pACT-II, получая штамм CG14; или трансформируют с помощью IGF-1-pAS и рАСТ-II, получая штамм CG15. Клетки, экспрессирующие слитый белок лиганда или слитый белок рецептора с немодифицированным вектором, плохо растут на элективной среде без гистидина, лейцина или триптофана. Клетки, экспрессирующие слитый белок как лиганда, так и рецептора, растут на элективной среде (фигура В).
В этой системе слитый белок IGF-I содержит как часть слитого белка сигнальную последовательность из 22 аминокислот. Это может придать повышенную гибкость домену активации Gal4 слитого белка IGF-I. Создан другой слитый белок IGF-I, в котором отсутствует сегмент кДНК (IGF-IDss). Олигонуклеотид синтезируют в соответствии с опубликованными последовательностями (Roberts et al. , 1987). Смысловая последовательность из 32 оснований содержит сайт Ncol (5'-G-G-G-C-C-A-T-G-G-A-G-G-G-A-C-C-A-G-A-G-A-C-C-C-T-T-T-G-C-G-G-G-3'), а антисмысловая олигонуклеотидная последовательность из 30 оснований содержит сайт BamHI (5'-G-C-G-G-G-A-T-C-C-G-G-C-T-C-A-A-G-C-A-G-C-A-A-A-G-G-A-T-C-T-3'). Фрагмент из 473 пар оснований получают стандартными PCR-методами, используя в качестве матрицы кДНК IGF-I. Этот фрагмент клонируют в pCRII, субклонируют в NcoI-BamHI плазмиды pAS и подтверждают анализом нуклеотидной последовательности. Штаммы для анализа получают, трансформируя дрожжи (CY770 и CY1945) при использовании плазмид IGF-IDss-рАS и IGF-IR-pACT-II. Дополнительные штаммы, экспрессирующие одно слияние (один слитый белок) и немодифицированный вектор, служат в качестве контрольных. Эти штаммы испытывают на среде количественного определения (синтетическая среда, не содержащая гистидина, лейцина и триптофана) в присутствии или в отсутствие 3-аминотриазола.
На прилагаемой фигуре В изображено следующее: штаммы, экспрессирующие указанные белки, наносят штрихом на среду для анализа (синтетическая среда без гистидина, лейцина и триптофана) и инкубируют 5 дней при 30oС. Верхний индекс AD показывает экспрессию в виде слитого белка доменом активации Gal4. Верхний индекс BD показывает экспрессию в виде слитого белка с ДНК-связывающим доменом Gal4. Верхняя плашка (плашка А) содержит четыре изолята каждого контрольного штамма. В случае дрожжей, экспрессирующих pAS и IGF-I-pACT (CG14), три изолята демонстрируют фенотип непрерывного роста относительно прототрофии гистидина и один ревертантный изолят (b). В случае экспрессии контрольного штамма IGF-1-pAS и рАСТ (CG15) все четыре изолята демонстрируют аналогичный фенотип роста в отношении прототрофии гистидина. На нижних плошках (В) два изолята каждого штамма наносят штрихом на среду для анализа в отсутствие (слева) или в присутствии 1 мМ 3-аминотриазола. Изоляты для штамма CG11, экспрессирующих IGF-I-слияние и IGF-I-IR-слияние, показывают интенсивный рост.
Список вышеприведенных ссылок.
Ullrich A., Gray A., Tam A. W., Yang-Feng Т., Tsubokawa M., Collins С., Henzel W., Le Воn Т., Kathuria S., Chen, Jacobs S., Francke U., Ramachandran J. , and Y. Fujita-Yamaguchi, 1986. Первичная структура рецептора инсулиноподобного фактора роста I: сравнение с рецептором инсулина помогает найти структурные детерминанты, которые определяют специфичность. EMBO J. 5: 2503-2512.
Roberts С. Т., Lasky S.R., Lowe W.L., Seaman W.T. and D. LeRoith. 1987. Молекулярное клонирование комплементарных дезоксирибонуклеиновых кислот инсулиноподобного фактора роста I крыс: дифференциальный процессинг матричной рибонуклеиновой кислоты и регуляция с помощью гормона роста во внепеченочных тканях. Mol. Endocrinol. 1,243-248.
Пример С.
VEGF-гомодимеризация молекул лиганда.
Предпосылки.
Гормон VEGF состоит из двух идентичных молекул, которые димеризуются с помощью дисульфидных связей, образуя активный лиганд (Gospodarowicz et al., 1989). Функциональный VEGF зависит от образования внутримолекулярных и межмолекулярных цистеиновых связей, по-видимому, образующих мотив "узел" (MacDonald and Hendrickson, 1993). Так как функциональный VEGF должен образовывать гомодимер, эта структура предполагает, что идентичные сайты лиганда взаимодействуют с идентичными сайтами двух молекул рецептора, что дает стехиометрию 2: 2 (Portgens et al., 1994). Взаимодействие двух молекул VEGF составляет взаимодействие белок-белок циркулирующих внеклеточных белков. Данный пример демонстрирует возможность изучения функционального взаимодействия между субъединицами лигандов, например, для VEGF и возможность использовать модифицированные клетки и способы по изобретению заявителей для нового дизайна скрининга, нацеленного на идентификацию соединений, блокирующих или усиливающих образование функциональных (полисубъединичных) лигандов.
Экспериментальная часть.
Следующие конструкции необходимы для создания системы VEGF/VEGF: кДНК, кодирующую VEGF, вырезают из рекомбинантного вектора в виде фрагмента EcoRI, VEGF-pCUP (описан в примере 3 данной заявки) и лигируют по сайту EcoRI плазмиды рАСТ-II, получая VEGF-pACT-II. Тем же способом кДНК для VEGF вырезают (эксцизия) в виде фрагмента NcoI-XhoI из VEGF-pACT-II и лигируют по сайту NcoI-SalI плазмиды pAS, получая VEGF-pAS. Строение конечных векторов (VEGF-pACT-II и VEGF-pAS) подтверждают анализом нуклеотидной последовательности и трансформируют в дрожжи литийацетатным методом, получая соответствующие штаммы.
Клетки-хозяева дрожжей штамма CY770 трансформируют при использовании VEGF-pACT-II и VEGF-pAS, получая штамм CY874. Клетки-хозяева штамма дрожжей трансформируют при использовании VEGF-pACT-II и нерелевантного слитого дрожжевого белка, Snf4-pAS, получая контрольный штамм SY31; или трансформируют с помощью VEGF-pAS и Snfl-pACT, получая контрольный штамм SY32. Штаммы испытывают на среде для количественного определения (синтетическая среда, не содержащая гистидина, лейцина и триптофана), дополненной 60 мМ 3-аминотриазола. Штамм CY874, экспрессирующий оба слитых белка VEGF, растет энергично на избирательной (элективной) среде. Однако штаммы, экспрессирующие только один VEGF-слитый белок с/и нерелевантным дрожжевым слитым белком (CY31 или CY32), не растут на элективной среде для количественного определения (фигура С). Это открытие демонстрирует полезность изобретения заявителей при установлении взаимодействия между субъединицами лиганда, обычно обнаруживаемыми в кровотоке млекопитающих.
Список вышеприведенных ссылок (Литература).
MacDonald N.Q. и W.A.Hendrickson, 1993. Структурное суперсемейство факторов роста, содержащих мотив цистеинового узла. Cell 73: 421-424.
Gospodarowicz D., Abrahoam Y.A., Shilling J. 1989. Выделение и характеристика митогена сосудистых эндотелиальных клеток, продуцируемого клетками folliculo sellate гипофиза. PNAS 86:7311-7315.
Potgens A. J.С., Lusbsen N.H., vanAltena M.C., Vermeulen R., Bakker A., Schoenmakers J.G.G., Ruiter D.J., de Waals R.W.W., 1994. Ковалентная димеризация фактора роста сосудистого эндотелия существенна для его биологической активности, доказательство мутаций cys в ser, J. Biol. Chem. 269:32879-32885.
Прилагаемая фигура С обобщает следующее: штаммы, экспрессирующие указанные белки, наносятся штрихом на среду для количественного определения (синтетическая среда, не содержащая гистидина, лейцина и триптофана) и инкубируют при 30oС в течение 3 дней. Верхний индекс AD указывает на экспрессию в виде слияния с доменом активации Gal4; верхний индекс BD указывает на экспрессию в виде слитого белка с ДНК-связывающим доменом. Единственный репрезентативный изолят нанесен штрихом в каждом квадранте.
Пример Д.
Клетки-хозяева, модифицированные согласно авторской заявке, для высокопроизводительного скрининга целевых полибелковых комплексов.
Обоснование (предпосылки).
Штамм дрожжей CY770 способен сохранять три различные аутосомные плазмиды, используя селективные маркерные гены LEU2, TRP 1 и URA3. Такие штаммы экспрессируют слитый белок с доменом активации транскрипции Gal4 при использовании плазмиды с маркером LEU2 (меченой LEU2) и слитый белок с ДНК-связывающим доменом Gal4 при использовании плазмиды, меченой TRP1. Маркер URA3 используют с целью выбора плазмид, образованных из pCUP, для экспрессии неслитых белков в качестве конкурентов при связывании (пример 1) или в виде свободного лиганда в рецепторных димеризационных системах (пример 3). При высокопроизводительном скрининге маркерный ген UASGal-CYH продолжает плазмиду, меченную URA3 (пример 2). В этих примерах мы не экспрессировали как неслитый белок, так и репортерный ген CYH, так как оба требуют отбора с помощью URA3. Мы полагаем, что желательно применить наши "инструменты" и методологию скрининга на взаимодействие "полибелков" (многобелковое), таких как два рецепторных слияния плюс пептид лиганда, одновременно экспрессируемые, так что интактный полибелковый ("мультипротеиновый") комплекс можно оценить по индукции репортерного (маркерного) гена. Таким образом можно идентифицировать соединения, которые уменьшают активность любого компонента комплекса. С этой целью CY770 дополнительно модифицируют, чтобы сделать возможным выбор четвертой плазмиды. Модифицированные клетки-хозяева на основе штамма, подобного CY770, можно использовать для быстрого высокопроизводительного скрининга на новые соединения, блокирующие образование многобелковых комплексов лиганд/рецептор/рецептор, конкретно опосредуемой VEGF димеризации KDR (пример 3).
Экспериментальная часть.
CY770 имеет генотип МАТа leu2-3, 112 ura3-52 trp 1-901 his3_200 ade2-101 gal4 gal80 LYS2::UASGAL-HIS3 cyh', как описано в примере 1. Этот штамм трансформируют в аргининовые ауксотрофы с помощью следующих методов. Ген дрожжей ARG4 амплифицируют полимеразной цепной реакцией (PCR) при использовании геномной ДНК дрожжей, используя праймеры с последовательностями (5'-G-G-G-С-С-С-A-G-А-С-Т-G-T-Т-Т-С-С-Т-Т-G-Т-А-Т-С-С-А-С-3') и (5'-C-T-C-G-A-G-T-C-A-C-T-T-A-T-A-T-T-C-A-A-C-C-A-T-C-A-C-3'). Эти праймеры добавляют к концам сайтов рестрикции АраI и XhoI. Амплифицированную ДНК ARG4 клонируют в вектор pCR (Invitrogen. Corp. , San Diego, CA). Ген дрожжей URA3 амплифицируют с помощью PCR, используя олигонуклеотиды, имеющие последовательности (5'-G-А-С-G-Т-С-G-А-А-С-G-A-A-G-G-A-A-G-G-A-G-С-А-С-A-G-A-С-3') и (5'-G-C-T-A-G-C-G-A-T-T-C-C-C-G-G-G-T-A-A-T-A-A-C-T-G-A-T-A-3'). Эти праймеры вводят сайты рестрикции AatII и NheI, фланкирующие ген URA3. Амплифицированный ген URA3 клонируют в pCR. Оба клона ARG4 и URA3 расщепляют при помощи AatII и Nhel. При этом удаляется 825 пар оснований ARG4, которые затем замещают фрагментом ДНК URA3. Эту конструкцию arg4::URA3 расщепляют с помощью НраI плюс XhoI, чтобы нацелить ее в геном CY770 гомологичной рекомбинацией. Образующийся в результате штамм представляет собой Arg- вследствие замещения ARG4 на arg4:: URA3. Этот штамм выращивают на среде, содержащей 5-фторортовую кислоту, с целью отбора Ura--производных (М.D.Rose, F.Winston and Hieter, Methods in yeast genetics. Cold Spring Harbor Laboratory Press, 1990). Конечный штамм, названный CY585, способен сохранять четыре плазмиды, использующие маркеры LEU2, TRP1, URA3 и ARG4. АРС4-производные UASGaL-CYH репортерной плазмиды р02146 (пример 2) конструируют, выделяя ARG4 на фрагменте рестрикции ApaI-HindIII из описанной выше плазмиды. Эту ДНК ARG4 используют для замещения большей части маркерного гена URA3 в pOZ146. АRG4-производное плазмиды pOZ146 названо pOZ186.
CY585 трансформируют, используя репортерную плазмиду pOZ186. Образующийся штамм трансформируют с помощью трех плазмид, используемых для характеристики влияния VEGF на димеризацию KDR (пример 3). Штамм, содержащий pOZ186, обе плазмиды экспрессии слитого белка KDR и pCUP-VEGF обозначают CY592. Дополнительные контрольные штаммы создают трансформацией с использованием обеих плазмид экспрессии слитого белка KDR плюс pCUP или рАСТII плюс pAS2-KDR плюс pCUP-VEGF. Первый штамм (CY595) получают, чтобы изучить димеризацию KDR в отсутствие лиганда, а последний штамм (CY596) служит в качестве негативного контроля. Эти штаммы наносят штрихом на среду для количественного определения (синтетическая полная среда, не содержащая лейцин, триптофан, урацил и аргинин) с циклогексимидом, добавляемым до конечной концентрации 1 микрограмм на мл. Только контрольный штамм CY596 устойчив к циклогексимиду. Индукция репортерного гена UASGAL-CYH в CY592 делает штамм чувствительным к циклогексимиду. Димеризации KDR в отсутствие VEGF (CY592) также достаточно для придания чувствительности к циклогексимиду.
Полагают, что стимуляция димеризации KDR, которая происходит вследствие VEGF-связывания, опосредует ангиогенные эффекты VEGF (N. Vaisman, D. Gospodarowicz and G. Neufeld, J. Biol. Chem. 265:19461-19466, 1990).
Пример Е.
Функциональная экспрессия человеческого рецептора, связанного с белком G.
Обоснование.
Суперсемейство связанных с G-белком рецепторов состоит из большого числа родственных по структуре белков, характеризующихся семью трансмембранными доменами и близкой связью с внутриклеточными GTP-связывающими белками, которые служат для передачи сигналов от рецептора к эффекторному белку. Рецептор рилизинг-фактора гормона роста (GRF) является членом субсемейства рецепторов, связанных с G-белком, в котором основные детерминанты связывания лиганда находятся в единственной соседней области около амино-конца. Взаимодействие GRF/GRFR можно также изучать согласно авторскому изобретению, как показано ниже.
Экспериментальная часть.
кДНК, кодирующую человеческий GRF, сначала амплифицируют полимеразной цепной реакцией (PCR). Олигонуклеотид из 98 оснований, содержащий смысловую нить с кодоном терминации трансляции и сайт ЕсоRI (5'-A-A-T-T-C-G-A-T-A-T-G-C-A-G-A-T-G-C-C-A-T-C-T-T-C-A-C-C-A-A-C-A-G-C-T-A-C-C-G-G-A-A-G-G-T-G-C-T-G-G-G-C-C-A-G-C-T-G-T-C-C-G-C-C-C-G-C-A-A-G-C-T-G-C-T-CC-A-G-G-A-C-A-T-C-A-T-G-A-G-C-A-G-G-T-A-G-G-3') и олигонуклеотид из 98 оснований, содержащий антисмысловую цепь (5'-А-А-Т-Т-С-Т-А-С-С-Т-G-C-T-C-A-T-G-A-TG-T-C-C-T-G-G-A-G-C-A-G-C-T-T-G-C-G-G-G-C-G-G-A-C-A-G-C-T-G-G-C-C-C-A-G-C-A-C-C-T-T-C-C-G-G-T-A-G-C-T-G-T-T-G-G-T-G-A-A-G-A-T-G-G-C-A-T-C-T-G-C-A-T-A-T-C-G-3'), фосфорилируют и аннелируют стандартными методами (Т. Maniatis, E. F. Fritsch and J. Sambrook, Molecular Cloning, Cold Spring Harbor Laboratory Press, 1982). Продукт используют в качестве матрицы в PCR с праймерами, имеющими последовательности (5'-С-T-G-A-А-Т-Т-C-G-A-T-A-T-G-C-A-G-A-T-G-C-C-T-C-3') и (5'-G-A-A-T-T-C-С-Т-А-С-С-Т-G-C-T-C-A-T-G-A-T-G-T-C-3'), получая фрагмент ДНК из 101 пары оснований. Эту кДНК GRF клонируют в вектор pCR (Invitrogen Corp. , San Diego, CA) и выделяют на фрагменте рестрикции EcoRI, затем клонируют в pACTII (пример 1). Фрагмент GRF вырезают из рАСТII и встраивают в pAS1 (Durfee et al., Genes and Devel. 7:555-569, 1993) в виде фрагмента NcoI/BamHI. Последовательности, кодируюющие 127 аминоконцевых аминокислот GRFR свиньи, амплифицируют с помощью PCR, используя праймеры (5'-G-C-C-A-C-C-A-C-C-A-T-G-G-A-C-A-G-C-G-G-G-3') и (5'-G-T-C-G-G-A-T-C-C-C-T-A-G-G-A-G-A-A-G-T-A-G-G-A-T-T-T-С-Т-С-3') с клонируемым рецептором (W. Baumbach, American Cyanamid Co., персональное сообщение; Genbank, LI 1869) в качестве матрицы. Последовательности лигируют в pAS1 на фрагменте NcoI/BamHI, выделяют из этого клона и встраивают в рАСТ в виде фрагмента NcoI/BamHI.
Последовательности GRFR изменяют опосредуемым PCR мутагенезом, замещая остаток аспарагиновой кислоты в положении 60 на глицин. Полагают, что конкретно аспарагиновая кислота необходима для связывания GFR с мышиным GRFR (S. -C. Lin et al., Nature 364:208-213, 1993). Фрагмент амплифицируют, используя вышеуказанный смысловой праймер плюс олигонуклеотид, внедряющий одиночную замену основания GAT Ж.GGТ в кодоне 60. Этот праймер имеет последовательность (5'-С-А-А-C-A-T-С-С-С-А-С-С-С-С-А-G-G-T-С-С-Т-A-G-G-3'). Перекрывающий фрагмент, включающий замену основания, амплифицируют, используя олигонуклеотид (5'-А-С-С-T-G-G-G-G-T-G-G-G-A-T-G-T-T-G-T-G-C-T-G-G-3') и вышеописанный антисмысловой олигонуклеотид. Два PCR-продукта объединяют в конечной PCR с концевыми праймерами, получая интактную ДНК GRFR-D60G. Фрагменты встраивают в pCR, подтверждают анализом нуклеотидной последовательности, вырезают в виде фрагмента NcoI/BamHI и клонируют в pACTII.
Штаммы для анализа получают, трансформируя штамм дрожжей CY770 вышеописанными плазмидами. Штамм CY1012 экспрессируют внеклеточный аминоконцевой домен свиного GRFR в виде слитого белка с доменом активации транскрипции Gal4, a GRF в виде слитого белка с ДНК-связывающим доменом Gal4. Контрольные штаммы CY1023 и CY1024 экспрессируют только один из этих слитых белков, как показано на фигуре Е1. У двух независимых дериватов каждого штамма изучают рост на среде для биоанализа (синтетическая среда, не содержащая лейцин, триптофан и гистидин, дополненная 40 мМ 3-аминотриазола). Только штамм, содержащий оба слитых белка, проявляет прототрофию, что указывает на специфичное взаимодействие между GRFR и GRF-слитыми белками (фигура Е1).
Для дополнительного подтверждения этого результата последовательности GRFR модифицируют с помощью сайт-направленного мутагенеза с целью замены отдельной аминокислоты (D60), как известно, важной для ассоциации с лигандом (S.C. Lin et al., Nature 364: 208-213, 1993). Последовательности, кодирующие D60G-вариант GRFR, клонируют в вектор рАСТII. Два штамма получают, трансформируя плазмиду экспрессии GRFR-D60G плюс плазмида экспрессии GRF, в CY770 или в качестве контроля GRFR-D60G плюс вектор pAS. Эти штаммы называются CY 1037 и CY 1036 соответственно (фиг. Е2). Рост этих штаммов на элективной среде сравнивают с ростом штаммов, экспрессирующих рецептор дикого типа. Только штамм, экспрессирующий рецептор дикого типа (CY1012), проявляет гистидиновую прототрофию (фигура Е2). Наблюдение, что мутация отдельной решающей (важной) аминокислоты в GRFR отменяет ассоциацию с лигандом, иллюстрирует специфичность взаимодействия GRFR дикого типа с лигандом.
Специфичное и обнаруживаемое взаимодействие между GRF и определенной областью GRFR наблюдается в этом примере при применении авторского изобретения. Мы полагаем, что эти результаты демонстрируют применении авторского изобретения для характеристики пептидных лигандов и рецепторов из суперсемейства рецепторов, связанных с G-белком, в особенности то, что мутация отдельной аминокислоты в рецепторе служит примером специфичности взаимодействия лиганд/рецептор, которое может изучаться с помощью авторского изобретения.
Прилагаемая фигура Е1 показывает следующее. Штаммы, экспрессирующие указанные белки, наносят штрихом на среду для анализа (синтетическая среда, не содержащая лейцин, триптофан и гистидин, и дополненная 40 мМ 3-аминотриазола) и инкубируют при 30oС в течение 4 дней. Верхний индекс AD указывает, что аминоконцевая область GRFR экспрессирует в виде слитого белка с доменом активации Gal4; верхний индекс BD указывает, что GRF экспрессирует в виде слитого белка с ДНК-связывающим доменом Gal4. Черточки указывают, что контрольный штамм несет вектор, не содержащий гетерологичных последовательностей. Противоположные квадранты плашки содержат независимо сконструированные, но эквивалентные штаммы.
На прилагаемой фигуре Е2 изображено следующее. Штаммы, экспрессирующие указанные белки, наносят штрихом на среду для анализа (синтетическая среда, в которой отсутствует лейцин, триптофан и гистидин и дополненная 40 мМ 3-аминотриазола) и термостатируют при 30oС в течение 4 дней. Верхний индекс AD указывает, что аминоконцевая область GRFR дикого типа (wt-R) или D60G-мутанта GRFR (mut-R) экспрессирует в виде слитого белка с доменом активации Gal4; верхний индекс BD указывает, что GRF экспрессирует в виде слитого белка с ДНК-связывающим доменом Gal4. Черточки (тире) указывают, что контрольные штаммы несут вектор без гетерологичных последовательностей. Противоположные квадранты плашки содержат независимо сконструированные (созданные), но эквивалентные штаммы.
Пример F.
Функциональная экспрессия молекул клеточной адгезии в модифицированных клетках по изобретению.
Обоснование (предпосылки).
Молекулы клеточной адгезии (слипания клеток) (САМ) представляют собой суперсемейство родственных белков, которые образуют молекулярную основу для клеточной коммуникации. Взаимодействие между молекулами САМ можно изучать и обнаруживать, используя авторское изобретение. Внеклеточные домены двух САМ нематоды Caenorhabditis elegans функционально экспрессируют в модифицированных клетках по авторскому изобретению следующим образом.
Экспериментальная часть.
Последовательности, кодирующие внеклеточные домены двух С. elegans CAM, обозначенных linl2 и lag2, амплифицируют полимеразной цепной реакцией (PCR). Синтезируют праймер смысловой цепи с последовательностью (5'-C-C-C-G-G-G-G-A-T-G-C-G-G-А-Т-С-С-С-Т-A-C-G-А-Т-Т-T-G-3'). Этот РСК-праймер добавляет сайт рестрикции сразу же "выше" (ubstream, в обратном -3',5'-направлении) ATG-инициирующего кодона для linl2. Антисмысловой праймер синтезируют с последовательностью (5'-G-T-C-G-A-C-T-T-A-T-C-C-T-G-T-А-Т-Т-G-T-T-T-C-C-A-G-A-Т-Т-Т-Т-3'). Этот праймер добавляет терминирующий кодон и сайт рестрикции SalI. Последовательности, кодирующие внеклеточный домен linl2, амплифицируют с помощью PCR, используя кДНК клона linl2 и лигируют в вектор pCR (Invitrogen Corp. , San Diego, CA). Затем последовательности linl2 выделяют на фрагменте рестрикции SmaI-SalI и лигируют в плазмиду pAS 1 (Durfee et al. . Genes and Devel. 7:555-569, 1993), расщепляемую теми же фрагментами. Эта плазмида экспрессирует область linl2, слитую с доменом связывания ДНК (ДНК-связывающим доменом) дрожжей Gal4. Область ДНК lag2 амплифицируют при использовании пула кДНК, синтезированные при использовании выделенной м РНК С. elegans с помощью набора для синтеза кДНК, поставляемого GIBCO-BRL (Gaithersburg, MD). Олигонуклеотид синтезируют на основе опубликованной последовательности lag2 (F. Е. Tax, J.J.Yeargers and J.H.Thomas, Nature 368: 150-154. 1994). Смысловой праймер представляет собой (5'-A-C-T-T-C-C-T-C-T-T-A-C-T-C-C-T-C-A-C-C-T-G-3'), а антисмысловой праймер представляет собой (5'-С-С-Т-С-А-С-Т-Т-С-С-Т-С-А-Т-С-А-А-Т-С-Т-Т-С-3'). Эти праймеры амплифицируют 1082 пар оснований фрагмента ДНК, который клонируют в pCR и изучают анализом нуклеотидной последовательности для подтверждения идентичности. Специфичные праймеры PCR предназначены для добавления сайта SmaI к 5'-концу lag2 и терминирующего кодона плюс сайта XhoI к 3'-концу. Этими кодонами являются (5'-C-C-C-G-G-G-G-A-T-G-А-Т-С-G-C-T-Т-А-С-Т-Т-С-С-Т-С-Т-Т-А-3') и (5'-C-T-C-G-A-G-T-T-A-А-А-Т-С-Т-С-С-А-С-G-G-T-A-G-T-T-G-G-G-G-T-3') соответственно. Эти праймеры используют в PCR с первоначальным клоном lag2 в качестве матрицы для амплификации последовательностей, кодирующих внеклеточный домен lag2. PCR-продукт клонируют в PCR-вектор, затем выделяют в виде фрагмента рестрикции SmaI-XhoI. Этот фрагмент клонируют в вектор рАСТII (пример 1), расщепляемый SmaI плюс SalI, что делает возможной экспрессию lag2 в виде слияния с доменом активации транскрипции.
Анализируемые штаммы получают трансформацией штамма дрожжей CY770 с помощью описанной выше плазмиды. Штаммы, экспрессирующие слитые белки как linl2, так и lag2, или в качестве контроля, один из двух слитых белков (один или другой) испытывают на среде для количественного определения (синтетическая среда, не содержащая лейцин, триптофан и гистидин и дополненная 40 мМ 3-аминотриазола) (фиг. F). Стимулированную транскрипцию репортерного гена UASGAL-HIS3, что показано ростом на среде для количественного определения, наблюдают только в штаммах, экспрессирующих слитые белки как linl2, так и lag2. Это открытие демонстрирует, что эти белки САМ могут функционально взаимодействовать в этих модифицированных штаммах.
Прилагаемая фигура 2 изображает следующее. Штаммы, экспрессирующие указанные белки, наносят штрихом на среду для анализа (синтетическая среда, не содержащая лейцин, триптофан и гистидин и дополненная 40 мМ 3-аминотриазола) и инкубируют при 30oС в течение 4 дней. Верхний индекс AD указывает, что внеклеточный домен lag2 экспрессирует в виде слитого белка с доменом активации Gal4; верхний индекс BD указывает, что внеклеточный домен linl2 экспрессирует в виде слитого белка с доменом связывания ДНК Gal4. Черточки указывают, что контрольный штамм несет вектор, не имеющий гетерологичных последовательностей. Два независимых изолята каждого штамма содержатся в указанном квадранте.
Пример Н.
Исследование влияния цистеинового мутагенеза VEGF на его взаимодействие с KDR-белками с помощью модифицированных клеток по авторскому изобретению.
Обоснование (предпосылки).
Образование дисульфидных мостиков часто необходимо для общей структурной целостности белкового лиганда и рецептора. VEGF структурно родственен хорошо описанному лиганду PDGF-B. PDGF-B и родственные белки образуют мотив "цистеиновый узел", который включает несколько цистеиновых мостиков, которые необходимы для должной структурной целостности лиганда и для того, чтобы вызвать ассоциацию лиганда соответствующим ему рецептором. Несколько цистеиновых остатков в VEGF подвергают мутации в остатки серина и экспрессии в штаммах, модифицированных по авторскому изобретению, чтобы оценить влияние на димеризацию KDR.
Экспериментальная часть.
Молекулы мутантного VEGF продуцируют, используя мутагенез, опосредуемый стандартной полимеразной цепной реакцией (PCR). Для осуществления указанных мутаций получают следующие пары олигонуклеотидов:
С51S (Межмолекулярное взаимодействие)
(5'-T-C-C-T-C-T-G-T-G-C-C-C-C-T-G-A-T-G-C-G-3') (#148)
(5'-C-A-C-A-G-A-G-G-A-T-G-G-C-T-T-G-A-A-G-A-3') (#149)
C51S+C60S (Межмолекулярное)
(5'-C-T-C-T-G-T-G-C-C-C-C-T-G-A-T-G-C-G-A-T-G-C-G-G-G-G-G-C-T-G-C-T-C-C-A-A-3') (#150)
(5'-T-G-G-A-G-C-A-G-C-C-C-C-C-G-C-A-T-C-G-C-A-T-C-A-G-G-G-G-C-A-C-C-G-C-G-G-3') (#151)
C57S (Внутримолекулярное и незаменимое)
(5'-C-G-A-T-C-C-G-G-G-G-G-C-T-G-C-T-G-C-A-A-T-3') (#152)
(5'-C-C-G-G-A-T-C-G-C-A-T-C-A-G-G-G-G-C-A-C-A-3') (#153)
С61S (Внутримолекулярное и заменимое)
(5'-G-C-T-C-C-A-A-T-G-A-C-G-A-G-G-G-C-C-T-G-G-3') (#154)
(5'-T-C-A-T-T-G-G-A-G-C-A-G-C-C-C-C-C-G-C-A-T-3') (#155)
Каждый олигонуклеотид используют в сочетании с противоположным концевым олигонуклеотидом из примера C с целью получения PCR-фрагментов с определенной(-ыми) указанной(-ыми) цистеиновой(-ыми) мутацией(-ями). PCR-реакции осуществляют в следующих комбинациях: в комбинации (А) используют олигонуклеотид N148 + антисмысловой концевой олигонуклеотид для получения фрагмента из 280 пар оснований и N149 + смысловой концевой олигонуклеотид для получения фрагмента из 200 пар оснований; эти фрагменты кодируют перекрывающиеся сегменты VEGF с мутацией С51S. PCR проводят для комбинации (В) и используют олигонуклеотид N150 + антисмысловой концевой олигонуклеотид для получения фрагмента из 280 пар оснований и олигонуклеотид N151 + смысловой концевой олигонуклеотид для получения фрагмента из 210 пар оснований. Эти фрагменты кодируют части VEGF с перекрывающимися сегментами, содержащими мутации C51S и C60S. PCR проводят для комбинации (С) и используют олигонуклеотид N 152 + антисмысловой концевой олигонуклеотид для получения фрагмента из 270 пар оснований и олигонуклеотид N153 + смысловой концевой олигонуклеотид для получения фрагмента из 210 пар оснований. Эти фрагменты кодируют перекрывающиеся сегменты VEGF, содержащие мутацию C57S. Наконец, проводят PCR для комбинации (D) и используют олигонуклеотид N154 + антисмысловой концевой олигонуклеотид для получения фрагмента из 250 пар оснований и олигонуклеотид N 155 + смысловой концевой олигонуклеотид для получения фрагмента из 230 пар оснований. Эти фрагменты кодируют участки VEGF с перекрывающимися сегментами, содержащими мутацию C61S.
Вторичную PCR проводят, используя комбинацию (А) продукты с 280 и 200 пар оснований с концевым олигонуклеотидом для обоих для амплификации полноразмерной кДНК, кодирующей VEGF-C51S. Другие три комбинации осуществляют тем же способом. Получают четыре фрагмента кДНК, кодирующих цистеиновые мутантные формы VEGF, в виде фрагментов EcoRI и субклонируют в сайт EcoRI векторов рАСТII и pCUP и подтверждают анализом нуклеотидной последовательности. Конечную ДНК трансформируют в дрожжи литийацетатным методом, получая соответствующие штаммы.
Для анализа влияния цистеинового мутагенеза на гомодимеризацию лиганда VEGF-VEGF клетки-хозяева штамма дрожжей CY770 трансформируют с помощью VEGF-pAS2 плюс каждый мутант VEGF-pACT-II, получая четыре экспериментальных штамма. Штаммы анализируют на функциональное взаимодействие слитых белков немодифицированный VEGF/мутантный VEGF, как показано, наблюдая рост на элективной среде. Штамм, экспрессирующий два слитых белка немодифицированного VEGF, растет интенсивно. Рост замедлен в случае всех штаммов, экспрессирующих цистеиновую мутантную форму белка VEGF. Экспрессия слитого белка C51S мутантного VEGF проявляет некоторый рост, хотя этот рост незначителен по сравнению со штаммом, экспрессирующим два слитых белка немодифицированного VEGF (фигура H1).
Для изучения влияния цистеиновых мутаций на лигандзависимую димеризацию рецептора те же самые мутантные VEGF-белки исследуют в штаммах, совместно коэспрессирующих слитые белки KDR. Клетки-хозяева штамма дрожжей CY770 трансформируют с помощью KDR-pACT-II и KDR-pAS2 (описанных в примере 3) и каждой цистеиновой мутантной формы pCUP-VEGF. Штамм, экспрессирующий слитые белки немодифицированного VEGF с KDR, значительно усиливает рост. Тогда как наблюдается, что штаммы, экспрессирующие KDR-слияния в отсутствие (немодифицированного) VEGF или в присутствии мутантного VEGF, проявляют при сравнении значительно меньший рост, как показано на фигуре Н2.
На прилагаемых фигурах H1 и Н2 показано следующее. Фигура H1. Штаммы, экспрессирующие указанный слитый белок VEGF-pACT в присутствии немодифицированного VEGF-pAS, наносят штрихом на среду для количественного определения (синтетическая среда, не содержащая гистидин, лейцин, триптофан и урацил и дополненная 60 мМ 3-аминотриазола) и инкубируют при 30oС в течение 3 дней.
Фигура Н2. Штаммы, экспрессирующие неслитые белки, немодифицированный или мутантный VEGF при использовании pCUP со слитыми белками KDR, наносят штрихом на среду для количественного анализа (синтетическая среда, не содержащая гистидин, лейцин, триптофан и урацил и дополненная 60 мМ 3-аминотриазола) и инкубируют при 30oС в течение 3 дней.
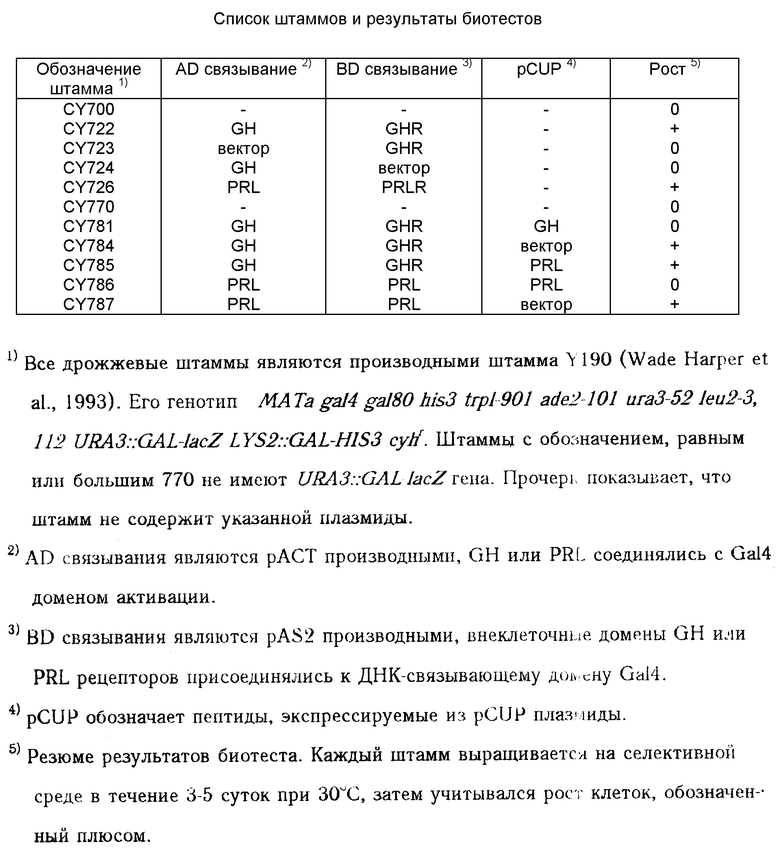
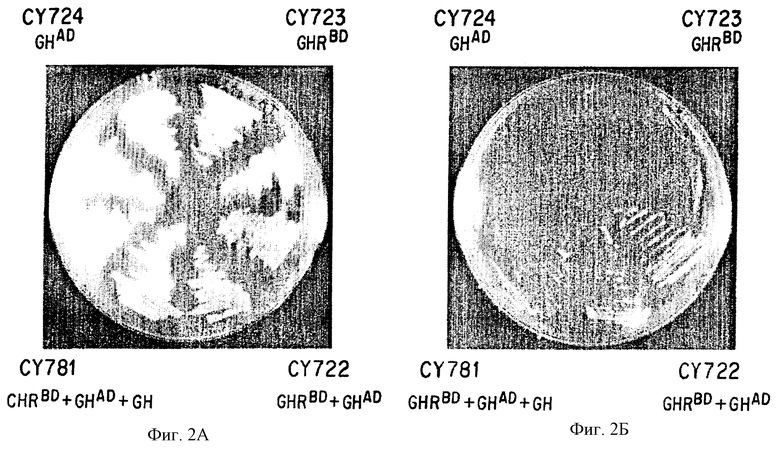
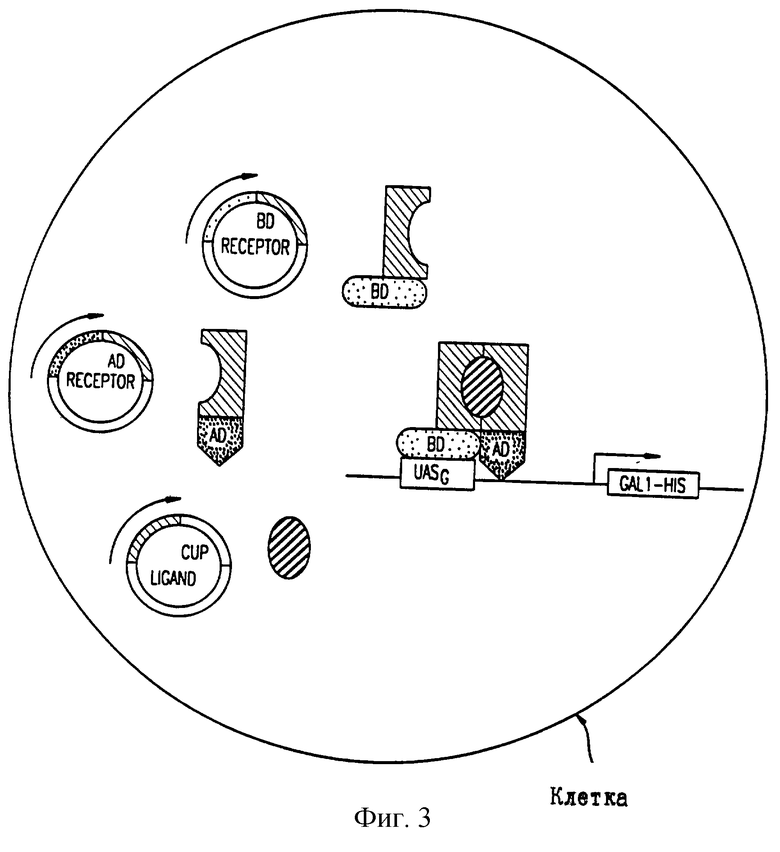
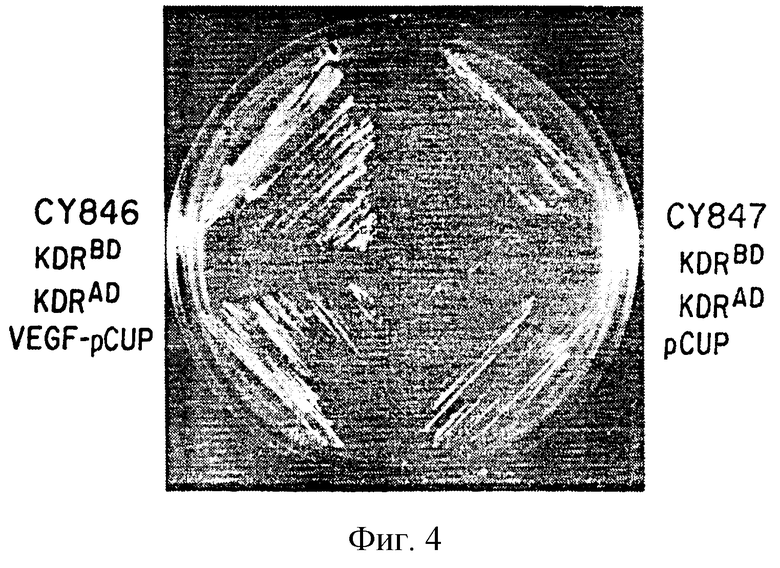
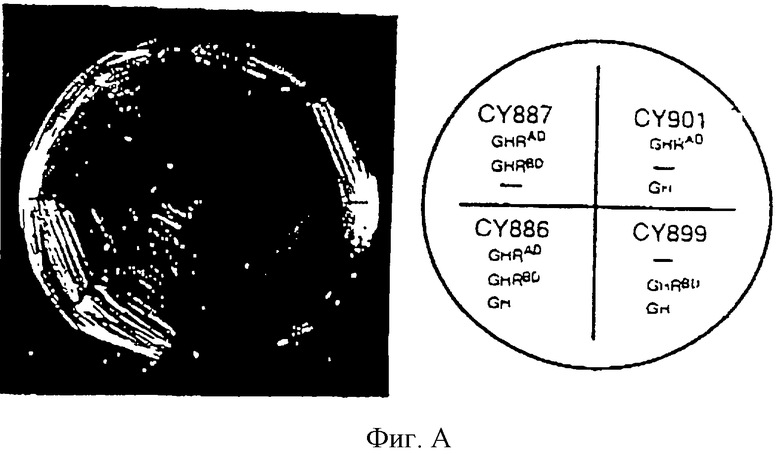
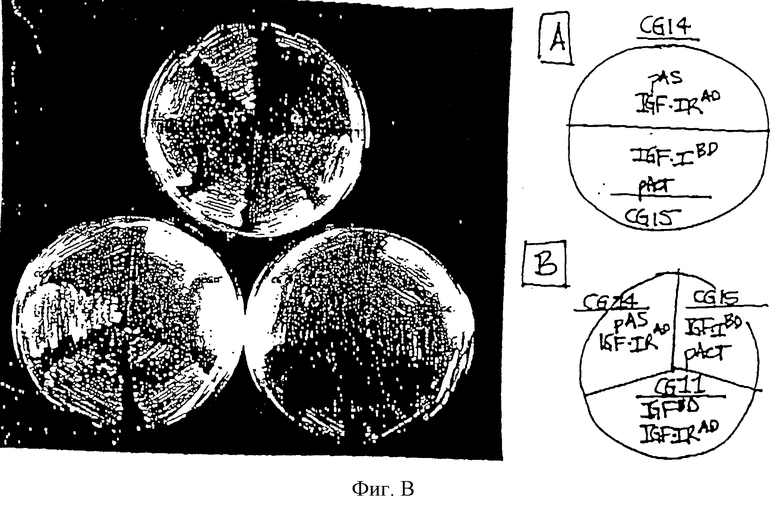
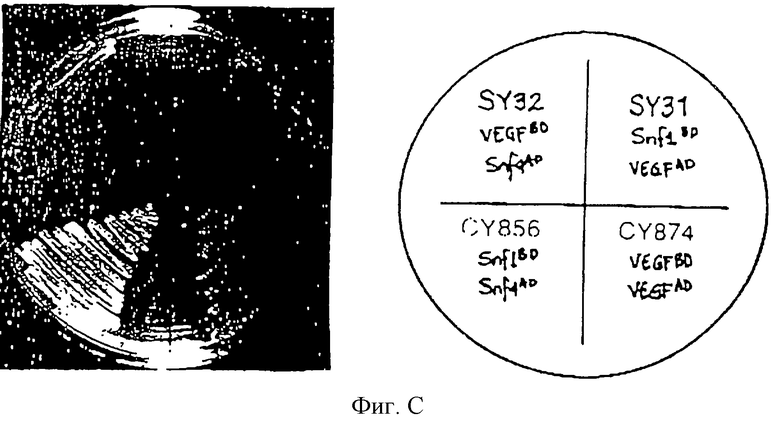
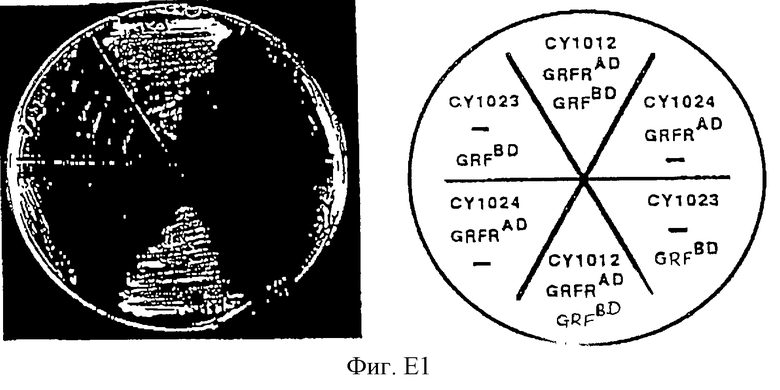
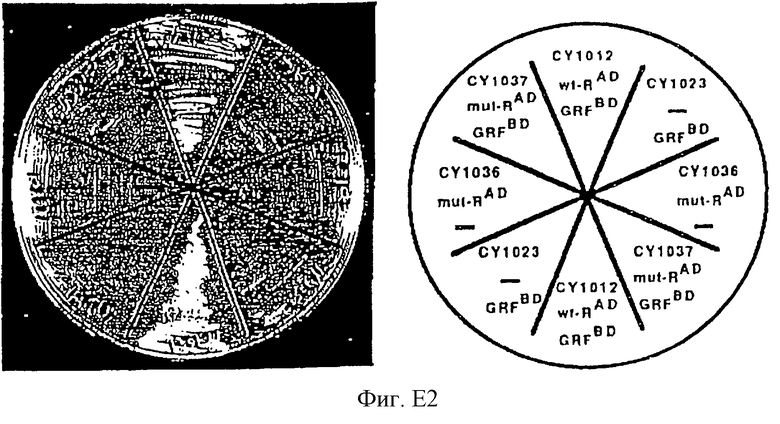
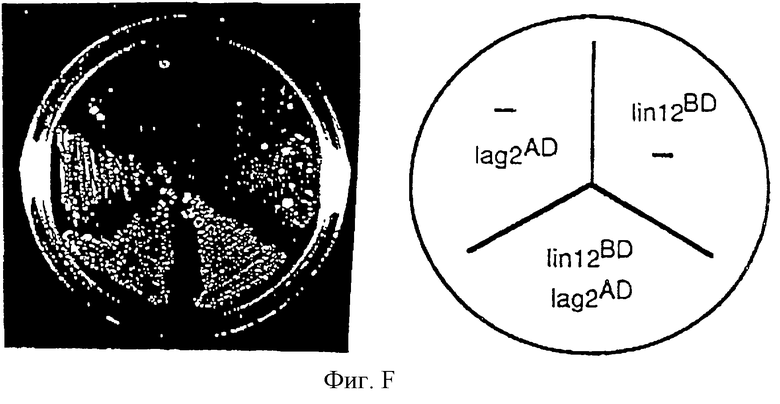
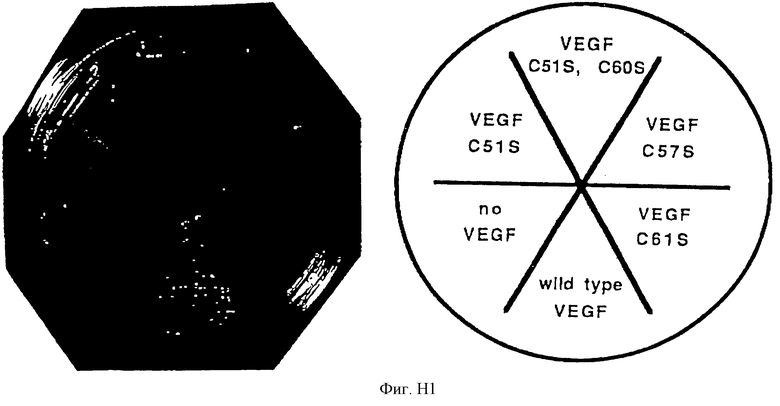
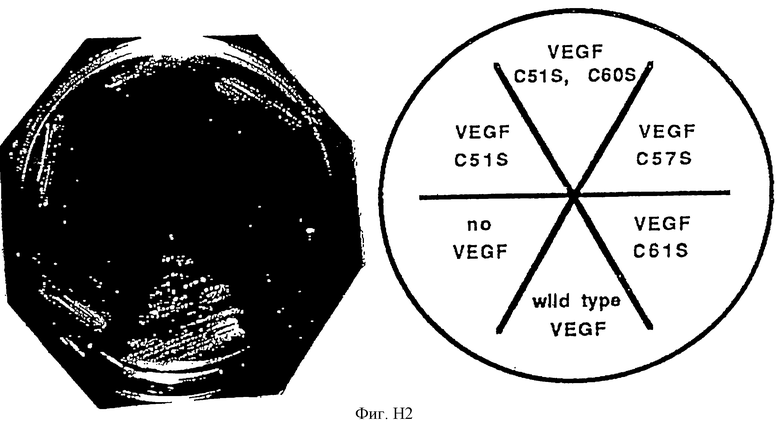
Проводят определение активности гена-репортера при прибавлении тестового образца к модифицированной клетке хозяина в условиях, пригодных для детектирования этой активности в присутствии образца, обладающего взаимодействием связывания в паре пептидного связывания. Активность гена-репортера определяют измерением отобранного фенотипа, который зависит от активности репортера. Проводят наблюдение за изменением в измеряемом фенотипе модифицированной клетки хозяина, в которой ген-репортер эффективно ассоциирован с дрожжевым протеином транскрипциональной активации при прибавлении тестового образца к клетке хозяина. Активность гена-репортера определяют измерением отобранного фенотипа, который зависит от активности репортера. Клетка хозяина при этом может проявить изменение в фенотипе только в присутствии тестового образца, который связывается только с одним из пептидов пары пептидного связывания. Определяют уровень активности гена-репортера модифицированной клетки хозяина при добавлении тестового образца к упомянутой клетке в условиях, подходящих для обнаружения упомянутой активности. Изобретение позволяет открывать соединения, которые могут взаимодействовать как лиганды для специфических рецепторов или трансдукторов. 5 с. и 53 з.п.ф-лы, 12 ил., 1 табл.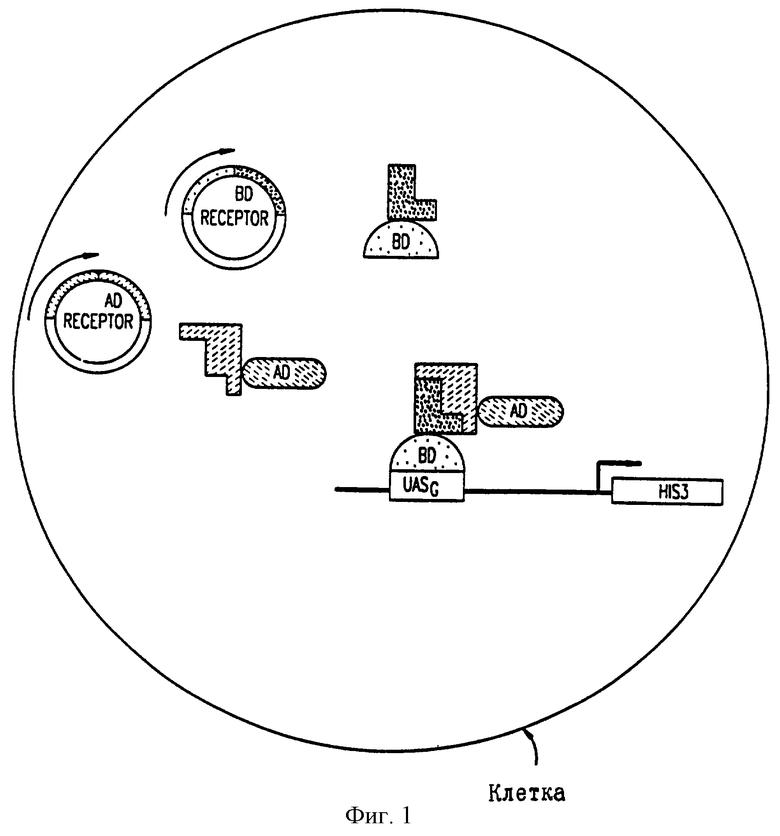
| US 5283173 A, 01.02.1994 | |||
| WO 9409133 A1, 28.04.1994 | |||
| WU et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Cell, 74, Dec | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| VOJTEK A | |||
| et al | |||
| Mammalian Ras Interacts Directly with the Serine/Threonine Kinase Raf, Cell, vol | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| YANG, X., et al | |||
| A protein kinase substrate identified by the two-hybrid system cited in the application, Science, 257, 680-682, (1992). | |||
Авторы
Даты
2003-07-20—Публикация
1995-05-31—Подача