Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при разработке и изготовлении вакцинных препаратов для профилактики парвовирусной инфекции свиней (ПВИС).
ПВИС - контагиозная вирусная болезнь, проявляющаяся клинически только у супоросных свиноматок и характеризующаяся прохолостами, малочисленными пометами, рождением мумифицированных плодов, мертвых и слабых поросят и ранними (в I половине супоросности) абортами.
Связь парвовируса свиней (ПВС) с нарушением воспроизводительной функции свиноматок в естественных условиях впервые была установлена в 1967 г. в Великобритании, однако экспериментально болезнь была воспроизведена через 10 лет.
Болезнь у свиноматок протекает, как правило, без видимых симптомов. Наблюдается лишь нарушение репродуктивной функции. Вирус проникает через плаценту, поражает плоды в I половине супоросности, вызывая их мумификацию и гибель. Клинически болезнь проявляется прохолостами, ранними, в I половине супоросности, абортами и преждевременнми родами. При возникновении болезни в ранее благополучных хозяйствах рождение живых поросят на одну свиноматку в год снижается на 50-60%, в стационарно-неблагополучных хозяйствах - на 10-20%.
Для специфической профилактики ПВИС применяются как инактивированные, так и живые вакцины. В настоящее время основным средством борьбы с ПВИС являются инактивированные вакцины, которыми иммунизируют молодых свиноматок не позже 30-го дня до первого осеменения. Вакцинация создает у свиноматок выраженный иммунитет и предупреждает передачу вируса эмбрионам и плодам (1).
Известно, что все известные изоляты ПВС оказались в антигенном отношении похожими, если не полностью идентичными (2).
При изготовлении инактивированной вакцины против ПВИС единственным требованием к исходному штамму ПВС является хорошее накопление вируса в чувствительной биологической системе, используемой для его культивирования.
В связи с этим задача отбора и изучения эпизоотических изолятов данного возбудителя в целях получения новых высокопродуктивных производственных штаммов ПВС для изготовления вакцинных препаратов остается актуальной.
Известен штамм NADL-2 (коллекция АТСС VR-742) ПВС, используемый для изготовления инактивированной вакцины (3).
Наиболее близким предлагаемому изобретению по совокупности существенных признаков является штамм И-82 ПВС, используемый для изготовления инактивированной вакцины (4).
Общим недостатком известных штаммов является их низкая продуктивность в известных биологических системах культивирования.
В задачу создания настоящего изобретения входило расширение арсенала штаммов ПВС, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления эффективных вакцинных препаратов, создающих напряженный и продолжительный иммунитет у привитых животных.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала новых высокопродуктивных вакцинных штаммов ПВС, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления эффективных вакцинных препаратов.
Указанный технический результат достигнут получением штамма "Вл-94" ПВС. Штамм "Вл-94" является новым, ранее неизвестным. Исходный вирус для получения штамма "Вл-94" выделен во ВНИИ защиты животных в 1994 году при вирусологическом исследовании внутренних органов абортированных (до 15 см длиной) плодов свиноматок, привезенных из свинокомплекса "Владимирский" Владимирской области. Производственный штамм "Вл-94" ПВС получен последовательными пассажами на перевиваемой культуре клеток почки поросенка "Казанская" (ППК).
Полученный штамм депонирован во Всероссийской государственной коллекции штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов МСХ РФ (ВГНКИ) 1 июля 1996 года под регистрационным шифром "Вл-94-ДЕП".
Штамм "Вл-94" ПВС обладает высокой биологической, антигенной и иммуногенной активностью в нативном виде и после инактивации и отличается высокой продуктивностью в чувствительных биологических системах культивирования. Экспериментально подтверждена возможность его использования для приготовления инактивированной эмульсионной вакцины против ПВИС, создающей напряженный и продолжительный иммунитет у вакцинированных животных.
Сущность изобретения пояснена на чертеже, на котором изображена микропанель с результатами исследования гемагглютинирующей активности (ГА-активности) штамма "Вл-94" в реакции гемагглютинации (РГА).
Штамм "Вл-94" ПВС характеризуется следующими признаками и свойствами.
Морфологические свойства
Штамм "Вл-94" ПВС относится к семейству Parvoviridae, роду Parvovirus. Зрелый вирион имеет кубическую симметрию, включает 32 капсомера, 2 или 3 капсидных белка, диаметр вириона около 20 нм, не содержит оболочки и липиды, мол. м. составляет 5,3•106 Д. Вирусный геном представлен 1-нитевой ДНК с мол. м. 1,4 кД, т.е. около 26,5% массы полного вириона, доля гуанин + цитозин составляет 41÷53%. Плавучая плотность в CsCl полного инфекционного вируса, неполного ("пустого") вириона и экстрагированной вирионной ДНК составляет 1,38÷1,395; 1,30÷1,315 и 1,724 г/см3 соответственно. Коэффициент седиментации 110÷122S.
Антигенные свойства
Вирус содержит три полипептида А, В и С с мол. массой 60÷90 кД. Все сравнивавшиеся изоляты ПВС свиней оказались в антигенном отношении похожими, если не полностью идентичными. Их идентичность установлена в РН и РТГА. Вирус обладает выраженной антигенной активностью и индуцирует синтез вируснейтрализующих, комплементсвязывающих и преципитирующих антител, а также антигемагглютинин. Изучение антигенных свойств изолированных индивидуальных вирионных полипептидов возбудителя показало, что антисыворотка к каждому структурному белку нейтрализует инфекционную активность полных вирионов и взаимодействует со всеми тремя структурными белками вируса. Каждый индивидуальный белок взаимодействует с вируснейтрализующими антителами, полученными на введение полного вируса. Вирусспецифические антигенные детерминанты имеются, предположительно, на всех вирионных белках ПВС. Биологический полураспад антител у поросят зависит от их массы, в среднем он составляет от 18 до 20 дней.
Биотехнологические характеристики
Штамм "Вл-94" ПВС хорошо размножается в перевиваемой культуре клеток ППК и накапливается в титре 8,0 lg ТЦД50/см3. Перевиваемая культура клеток СПЭВ нечувствительна к вирусу. Особенностью культивирования и накопления вируса является его зависимость от клеточного деления. Кривая размножения вируса зависит от количества митозов. Он хорошо размножается в делящихся клетках почки плода свиньи при заражении через 48 часов после посадки культуры. Наивысшая концентрация вируса достигается на 2-3 день культивирования. ЦПД характеризуется вакуолизацией и округлением клеток, диффузной грануляцией. При изучении цикла размножения методом иммунофлюресценции было установлено, что антиген обнаруживается в ядре клеток через 6 часов после заражения и накапливается в максимальных количествах к 18-24 часам. Штамм "Вл-94" ПВС предназначен для изготовления инактивированных вакцинных препаратов против ПВИС. Штамм "Вл-94" ПВС является генетически стабильным и сохраняет иммунобиологические свойства на протяжении 10 пассажей (срок наблюдения).
Хемо-генотаксономическая характеристика
Геном ПВС штамма "Вл-94" представлен 1-спиральной линейной молекулой ДНК с мол. м. 1,4 кД. 1-спиральная ДНК состоит примерно из 5 тысяч нуклеотидов и кодирует 4 белка - 3 структурных и 1 неструктурный. На обоих концах ДНК имеются неидентичные, самокомплементарные последовательности нуклеотидов (палиндромы), образующие 2-спиральные шпильки, резистентные к нуклеазе S1; 3'-концевая шпилька состоит из 115÷116 нуклеотидов, 5'-концевая - из 200÷242 нуклеотидов. Шпилечные структуры играют важную роль в репликации ДНК. Гены, кодирующие структурные белки, расположены в 5'-концевой половине, а ген, кодирующий неструктурный белок - в 3'-концевой половине ДНК. В вирионах штамма "Вл-94" содержится минус-ДНК. Вирус штамма "Вл-94" является автономным (недефектным).
Патогенные свойства
Штамм "Вл-94" ПВС патогенен для этого вида животных и апатогенен для хомяков и мышей. У всех зараженных поросят симптомы болезни и патоморфологические изменения обычно отсутствуют, однако обнаруживаются специфические антитела. Вирус выделяют из семенных пузырьков на 7-9 день после заражения. С 12 дня в сыворотке крови животных выявляют антигемагглютинин. У поросят, находившихся в контакте с зараженными животными, так же обнаруживаются специфические антитела, что свидетельствует о контагиозности инфекции. После внутримозгового, орального и интраназального заражения поросят каких-либо определенных воспроизводимых клинических симптомов не наблюдалось. Однако у таких животных удавалось выделить вирус из испражнений, крови и большинства тканей. К 7 дню выделяли специфические антитела. При заражении свиней вирусом из штамма "Вл-94" на разных стадиях беременности наблюдали трансплацентарное инфицирование плодов.
Гемагглютинирующие свойства
Штамм "Вл-94" ПВС агглютинирует эритроциты морской свинки, цыпленка, кошки, крысы, мыши, обезьяны, человека и не агглютинирует эритроциты барана, лошади, свиньи, КРС, собаки, кролика, хомячка и утки. Для определения его ГА-активности используют эритроциты морской свинки, реакцию проводят при 4oС, а в качестве разбавителя применяют физиологический раствор, рН 7,2. ГА-активность в РГА составляла 1:2048 ГАЕ. Вирус не освобождается с эритроцитов при 37-40oС в течение одного часа, однако в щелочном буфере (рН 9,0) он полностью элюирует с них за 30 мин при комнатной температуре. \\62 Физические свойства
Молекулярная масса вирионов составляет 5,5÷6,2 МД, плавучая плотность в градиенте CsCl 1,39÷1,42 г/см3, коэффициент седиментации 110÷122S.
Устойчивость к внешним факторам
Штамм "Вл-94" ПВС устойчив к действию различных физико-химических факторов. Сохраняет инфекционность при рН 3÷9 и 37oС в течение 1,5 ч, однако полностью инактивируется при рН 2 в тех же условиях. Вирус стабилен при 56oС в течение 2 сут, при 70oC - 2 ч и при 80oС инактивируется за 5 мин. Не теряет инфекционность в культуральной жидкости с 20% фетальной сыворотки КРС при 35÷37oС в течение 15 недель. Устойчив при обработке хлороформом, эфиром и фреоном в 10÷50% концентрации в течение 10÷30 мин при комнатной температуре. Вирус резистентен к действию РНК- и ДНК-азы и протеаз (папаина, хемотрипсина, трипсина, пепсина), устойчив к действию ультразвука, инактивируется УФ-лучами, формалином, этиленимином и его производными; β-пропиолактоном, глутаральдегидом. В помещениях вирус сохраняет активность более 4 мес, в свинарниках - до 4÷6 мес.
Дополнительные признаки и свойства
Свободен от контаминации бактериями, грибной микрофлорой, микоплазмами и вирусами.
На основании полученных данных можно утверждать, что штамм "Вл-94" по антигенному и иммунологическому спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным изолятом ПВС. Для снижения его эпизоотической опасности необходима своевременная профилактика вновь возникающих очагов болезни, а для этого необходима высокоактивная и безвредная вакцина.
По мнению заявителя, предлагаемый штамм обладает установленными Патентным законом России признаками патентоспособности "новизна" и "изобретательский уровень".
Сущность предлагаемого изобретения пояснена примерами его исполнения, которые не ограничивают его объем.
Пример 1.
В 1994 году при вирусологическом исследовании внутренних органов абортированных (до 15 см длиной) плодов свиноматок, привезенных из свинокомплекса "Владимирский" Владимирской области, на перевиваемой культуре клеток ППК был выделен ПВС с гемагглютинирующим титром 1:16. В следующих последовательных пассажах на ППК титр ПВС составил 1:64 (2 пассаж), 1:128 (3 пассаж), 1:256 (4 пассаж), 1:1024 (5 пассаж), 1:2048÷1:4096 (6 пассаж).
Для выращивания изолята были испытаны культуры клеток СПЭВ, VIRO, MARC-145 и ВНК-21, однако на некоторых из них не отмечали ЦПД и ГА-активности вируса (ВНК-21, MARS-145), на других проявлялось незначительное ЦПД, однако ГА-активность оставалась на уровне 1:16 (СПЭВ, VIRO). Оптимальные для изолята результаты были получены в течение 3-6 пассажей в 2-3 суточной перевиваемой культуре клеток почки поросенка "Казанская" (ППК), выращенной на питательной среде пристеночной (ПСП). Оптимальными условиями для размножения ПВС на ППК явились поддержание температуры культивирования в пределах 36-37oС и рН 7,2-7,4, а также контакт в течение 50-60 мин вируссодержащей суспензии с монослоем клеток ППК при заражении. Для освобождения ПВС клетки ППК разрушали 3-кратным замораживанием при -20oС и оттаиванием при 37oС. Полученный вирус был подвергнут всестороннему контролю в соответствии с Руководством МЭБ по стандартным диагностическим методам и вакцинам (1996).
Результаты проведенных испытаний показали, что изолят ПВС соответствует требованиям, предъявляемым к производственным штаммам ПВС. Вирус с инфекционной активностью в культуре клеток ППК 7,5 lg ТЦД50/см3 и с ГА-активностью в РГА 1: 2048 заложен на хранение в качестве матровой расплодки под авторским наименованием "Вл-94".
Штамм хранят при -40oС или -70oС в нативном виде во флаконах по 10 см3 под герметично закрытыми пробками и металлическими колпачками. Штамм в нативном виде освежают каждые 12 мес в культуре клеток ППК. Титр вируса во флаконах за 12 мес хранения снижался менее чем на 0,5 lg ТЦД50/см3. При этом стабильно сохраняется активность в РГА и иммуногенная активность.
Пример 2.
Для изготовления эмульсионной инактивированной вакцины используют штамм "Вл-94" ПВС, адаптированный к перевиваемой культуре клеток ППК, выращенной на ПСП, и проявляющий ГА-активность не меньше 1÷1024 ГАЕ и инфекционную активность не меньше 7,5 lg ТЦД50/см3. Для получения вакцины используют выращенную в матрасах культуру клеток ППК с хорошим монослоем 2-3-суточного возраста. Для получения 20 л вируссодержащей суспензии ПВС берут от 110 до 120 матрасов с культурой клеток емкостью 1,5 дм3. После слива ростовой среды в матрасы вносят по 5-7 см3 ПВС матриксной серии. После 40-60 мин инкубирования при (37±2)oC в матрасы вносят по 150-200 см3 поддерживающей среды без сыворотки КРС. Зараженные матрасы помещают в термостат для культивирования при (37±2)oC. Срок культивирования от 48 до 72 ч. Для контроля незараженными оставляют 3 матраса, в которых ростовую среду меняют на 200 см3 поддерживающей среды без сыворотки. Начиная с 24 ч инкубирования, инфицированные и контрольные матрасы ежесуточно микроскопируют. Матрасы, в которых наблюдается ЦПД с поражением до 60% клеточного монослоя (обычно через 48-72 ч), отбирают, 3-кратно замораживают при температуре не выше -20oС и оттаивают при 37oС. Затем вируссодержащий материал очищают от клеточного детрита. Для этого содержимое матрасов сливают в одну емкость и охлажденную вируссодержащую суспензию, соблюдая стерильные условия, освобождают от клеточного детрита центрифугированием при 1000 об/мин в течение 10 мин. Очищенная от детрита суспензия должна иметь вид прозрачной жидкости розовато-вишневого цвета. В очищенную суспензию вносят гентамицин (100 ЕД) и перемешивают 20 мин. Затем из емкости отбирают пробу для лабораторно-производственного контроля на стерильность, инфекционную и ГА-активность вируса. Производственная серия должна иметь ГА-активность не меньше 1÷1024 и инфекционную активность не меньше 7,5 lg ТЦД50/см3. Очищенную вируссодержащую суспензию подвергают инактивации. Инактивацию вируса ведут с помощью 1% водного раствора аминоэтилэтиленимина (АЭЭИ), вносимого до конечной концентрации 0,05÷0,08%. Для этого в суспензию, нагретую до 26-28oС, вносят при постоянном перемешивании раствор АЭЭИ и устанавливают значение рН 7,6-7,8 добавлением в него 5% раствора янтарной кислоты. Инактивацию ведут в термостате при (37±2)oС в течение 20-22 ч с периодическим перемешиванием. По окончании инактивации антигенсодержащую суспензию охлаждают до 4÷6oС, устанавливают значение ее рН в пределах 7,6-7,8 и отбирают пробы антигена для проверки на стерильность, авирулентность и ГА-активность, используя для этого известные специалисту методы. Эмульсионную вакцину готовят путем диспергирования смеси антигенсодержащего материала и масляного адъюванта, содержащего минеральное масло с эмульгатором.
В качестве масляного адъюванта используют препараты фирмы "Сеппик" (Франция): Монтанид ИЗА 70 и Монтанид ИЗА 206. Масляный адъювант и инактивированный антиген смешивают на гомогенизаторе согласно следующим режимам:
1) при использовании Монтанида ИЗА 70 - гомогенизация в течение 4-5 мин при скорости вращения винта 3000 об/мин и температуре 10oС, при этом получают однородную эмульсию белого цвета типа "вода-масло";
2) при использовании Монтанида ИЗА 206 - гомогенизация в течение 3-4 мин при скорости вращения винта 600 об/мин и температуре 30oС. Тип получаемой эмульсии "вода-масло-вода". При изготовлении вакцин антиген соединяют с масляным адъвантом в следующем соотношении: с адъювантом Монтанид ИЗА 70 по меньшей мере 1:2, а с адъювантом Монтанид ИЗА 206 по меньшей мере 1:1 соответственно.
Готовую эмульсионную вакцину собирают в одну стерильную емкость, фасуют в стеклянные флаконы и контролируют в соответствии с техническими условиями.
Для оценки антигенной активности препарата используют количественный метод контроля, с помощью которого определяют количество антигена парвовируса в прививной дозе вакцины (1 см3). Метод заключается в следующем: готовую вакцину деэмульгируют хлороформом в соотношении 1:1, центрифугируют 10 мин при 2000 об/мин. Надосадок исследуют в РГА. Вакцина считается иммуногенной, если ГА-титр выделенного из вакцинного препарата парвовирусного антигена не ниже 1: 256 в прививной дозе 1 см3. В большинстве серий количество антигена равняется 512 ГАЕ, 1024 ГАЕ и 2048 ГАЕ.
Вакцина представляет собой эмульсию белого или белого с розовым оттенком цвета, слегка вязкой консистенции. При хранении вакцины допускается незначительное отслоение минерального масла на поверхности эмульсии. При встряхивании вакцина приобретает однородную гомогенную структуру.
Полученная вакцина имеет оптимальный компонентный состав, мас. %:
Антигенсодержащий материал из штамма "Вл-94" ПВС с инфекционной активностью не меньше 7,5 lg ТЦД50/см3 - 40,0-60,0
АЭЭИ - 0,05÷0,08
Масляный адъювант - До 100,0
Вакцину применяют для профилактической иммунизации свиней против ПВИС. Вакцина способствует образованию активного иммунитета против ПВИС через 21 сут после 2-кратного применения препарата длительностью не менее 6 мес.
Свиноматок, ремонтных свинок и хряков-производителей прививают двукратно с интервалом 20-30 дней за три недели до осеменения. Поросят прививают в 2-2,5-месячном возрасте 2-кратно с интервалом 20-30 дней. Вакцину вводят свиньям внутримышечно за ухом в дозе 1 см3 независимо от возраста животных. Вакцина пригодна для применения в течение 12 мес после изготовления при условии ее хранения в темном помещении при температуре (1-8)oС.
Пример 3.
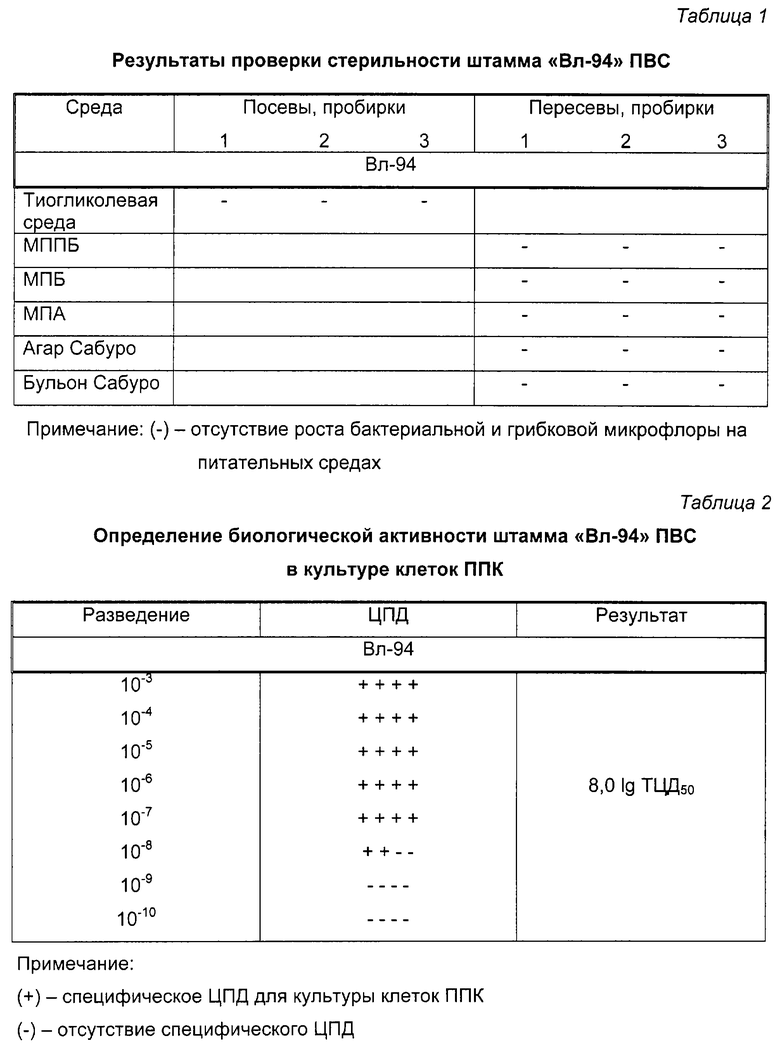
Проведены исследования по проверке стерильности производственного штамма "Вл-94" ПВС (4 пассаж). Для этого из 3 флаконов нативного вируса готовили среднюю пробу и вносили по 1 см3 в три пробирки, содержащие тиогликолевую среду. Одну засеянную пробирку выдерживали в термостате в течение 14 сут при (37±0,5)oC, другую - при комнатной температуре от 21oС до 25oС в течение этого же срока. Третью пробирку выдерживали в течение 7 сут при (37±0,5)oC и затем делали из нее пересевы по 0,5 см3 в каждую пробирку со следующими средами: мясопептонный бульон (МПБ) и агар (МПА), мясопептонный печеночный бульон под вазелиновым маслом (МППБ), агар и бульон Сабуро. Среды МПБ, МПА, МППБ с посевами выдерживали в течение 7 сут при (37±0,5)oC, а агар и бульон Сабуро - при температуре от 21oС до 25oС. Результаты исследований приведены в табл. 1.
Испытания показали, что штамм "Вл-94" (4 пассаж) ПВС не контаминирован бактериальной и грибковой микрофлорой. На всех средах с высевами и пересевами роста бактериальной и грибковой микрофлоры не обнаружено.
Пример 4.
Проведены исследования по проверке биологической активности производственного штамма "Вл-94" ПВС (4 пассаж) титрованием в перевиваемой культуре клеток почки поросенка ППК. Для этого содержимое 3 флаконов штамма "Вл-94" (4 пассаж) смешивали и готовили разведение от 10-3 до 10-10 на среде ПСП.
Из флаконов 0,05 см3 сливали ростовую среду, после чего в 4 пробирки с монослоем культуры клеток ППК вносили по 2 см3 соответствующих разведений вируса. Контакт составлял 40-60 мин. После чего во флаконы вносили ПСП.
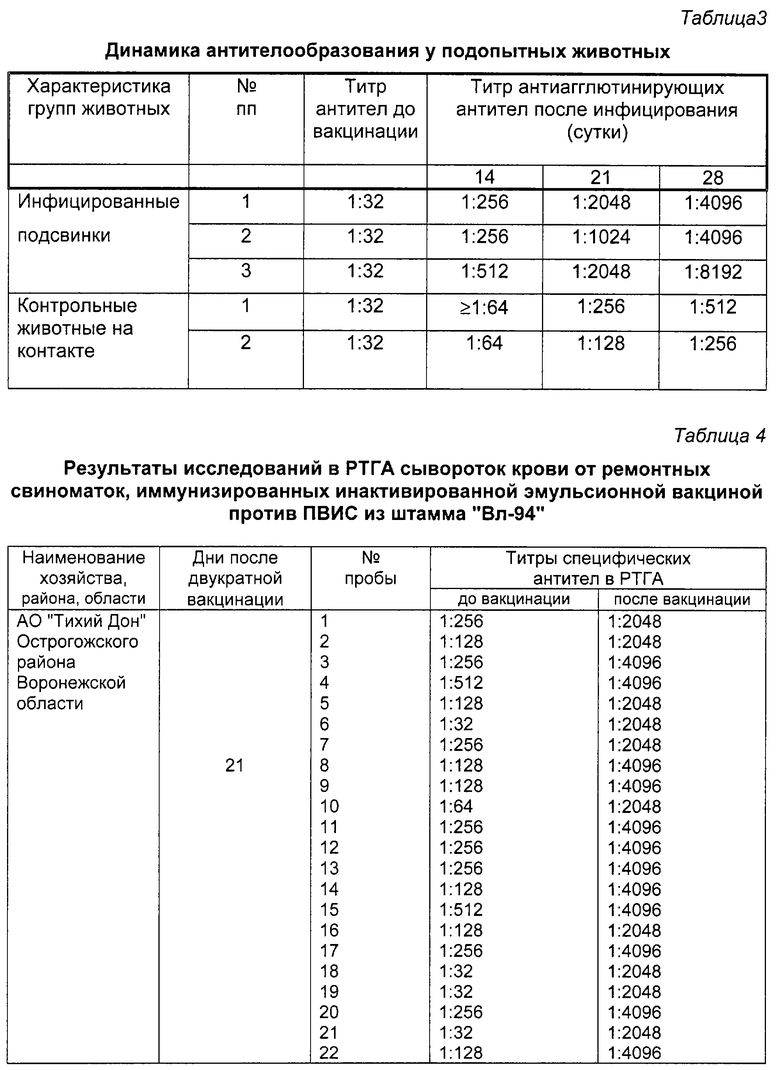
Зараженную и контрольную культуру клеток выдерживали в термостате при 37±2oC в течение 144 ч без замены питательной среды. Титрование вируса в культуре клеток ППК определяли по характерному ЦПД и разрушению монослоя клеток. Микроскопирование монослоя во флаконах проводили ежедневно. В контрольных флаконах (4 шт. ) не отмечали каких-либо деструктивных изменений клеток. Окончательный учет результатов производили на 6 сут. Одновременно просматривали и контрольные флаконы. Результаты титрования считали достоверными при сохранении монослоя в контроле. Результаты исследований представлены в табл. 2. Таким образом, испытания показали, что штамм "Вл-94" 5 пассажа имеет биологическую активность на культуре клеток ППК 8,0 lg ТЦД50/см3.
Пример 5.
Проведены исследования по определению ГА-активности производственного штамма "Вл-94" ПВС. ГА-активность штамма определяли в РГА.
Вирус для исследования брали из усредненной пробы, изготовленной из нативного вируса 3 пенициллиновых флаконов. Вирус титровали в трех повторностях на 96-луночной круглодонной микропанели. В лунки вносили по 50 мкл физраствора рН 7,2÷7,4 и готовили 2-кратные разведения вируса, начиная с 1:2 и до 1:4096. Затем в каждую лунку вносили по 50 мкл 0,6% суспензии эритроцитов морской свинки. Микропанель встряхивали и оставляли на 1-1,5 ч при 4±2oC. ГА-титром штамма ПВС считали наибольшее его разведение, которое вызывало полную агглютинацию эритроцитов. Результаты РГА достоверны, поскольку на микропанели присутствовали контроли:
- контроль специфического парвовирусного антигена с заведомо известным титром;
- контроль эритроцитов морской свинки (в 50 мкл физраствора вносили по 50 мкл 0,6% взвеси эритроцитов).
Результаты испытаний представлены на чертеже микропанели.
Таким образом, испытания показали, что гемагглютинирующий титр штамма "Вл-94" 5 пассажа в трех повторностях составил 1:2048.
Пример 6.
Проведены исследования по проверке специфичности производственного штамма "Вл-94" ПВС. Исследования проводились двумя методами: молекулярным и серологическим. При помощи ПЦР в штамме "Вл-94" выявлен только геном ПВС.
Определение специфичности штамма серологическим методом заключалось в постановке РТГА со специфической свиной сывороткой, полученной на 28 сут после введения штамма "Вл-94" 5 пассажа. Результаты РТГА показали, что специфическая свиная сыворотка подавляла гемагглютинирующие свойства (8 ГАЕ) вируса в титре 1:1024. Задержка гемагглютинации указывает на соответствие типа вируса и взятой (заведомо известной) специфической сыворотки крови. Таким образом, результаты ПЦР и РТГА свидетельствуют о специфичности штамма "Вл-94" ПВС.
Пример 7.
Проведены исследования по проверке иммуногенной активности производственного штамма "Вл-94" ПВС. Для этого из 3 флаконов штамма "Вл-94" (5 пассаж) составляли среднюю пробу и готовили разведение от 10-3 до 10-10 на среде ПСП. Для оценки антигенной активности штамма использовали 5 подсвинков массой 25-30 кг, из них двух подсвинков для контроля, а трем ввели вирус с инфекционной активностью 8,0 lg ТЦД50/см3 в дозе 1 см3 каждому (внутримышечно в область шеи за ухом). За зараженными и контрольными животными вели ежедневное клиническое наблюдение, проводили термометрию. В течение 12 сут как контрольные, так и инфицированные животные оставались клинически здоровыми, температура тела была в пределах нормы. Через 14, 21 и 28 сут после заражения у всех животных отбирали пробы крови. Сыворотки исследовали в РТГА. Результаты исследования сывороток крови представлены в табл. 3. Таким образом, специфические к штамму "Вл-94" антитела выявляли как у зараженных, так и контрольных (на контакте) подсвинков.
Пример 8.
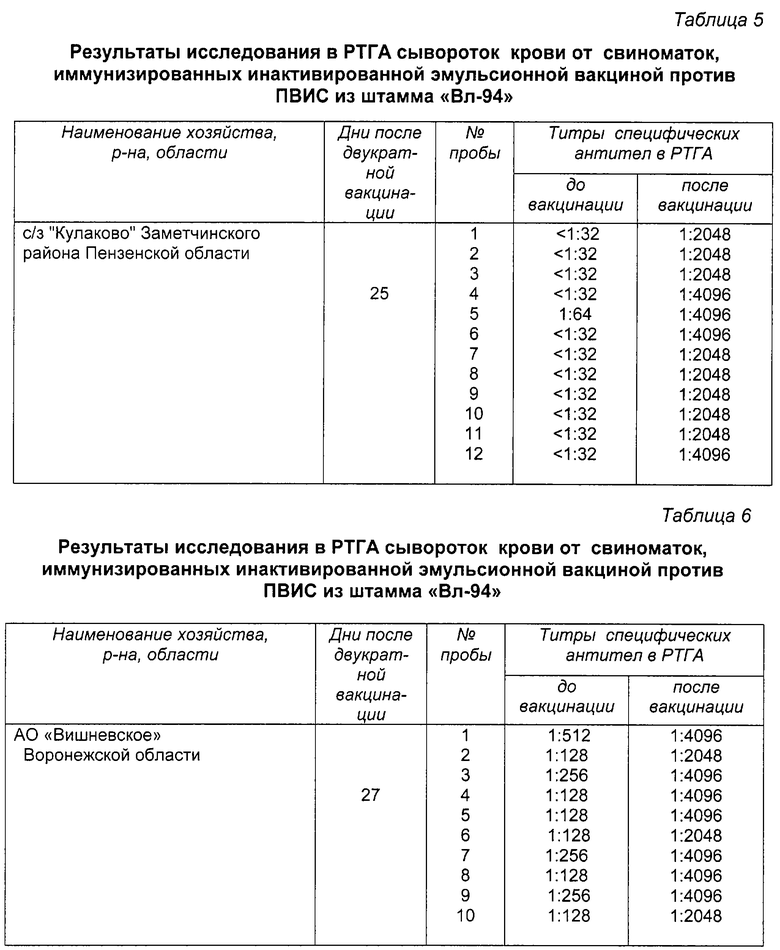
Эффективность инактивированной эмульсионной вакцины против ПВИС из штамма "Вл-94", изготовленной так, как описано в примере 2, проверена в спецхозе АО "Тихий Дон" Острогожского района Воронежской области на ремонтных свинках в количестве 22 голов, привитых упомянутой вакциной двукратно с интервалом 20 дней в дозе 1 см3. Результаты исследования в РТГА сывороток крови от ремонтных свиноматок, иммунизированных этой вакциной, приведены в табл. 4. Опорос ремонтных свинок прошел в установленные физиологические сроки на 114÷116 день супоросности. Получено по 9-10 поросят на одну свиноматку. Поросята имели массу тела 0,9÷1,1 кг, хорошо развиты и с хорошим сосательным рефлексом.
Среди опоросившихся свиноматок наблюдали: количество пометов с мертворожденными поросятами - нет, количество пометов с частично мертворожденными поросятами - нет, количество пометов с патологией различного характера - нет.
Пример 9.
Эффективность инактивированной эмульсионной вакцины против ПВИС из штамма "Вл-94", изготовленной так, как описано в примере 2, проверена в с/з "Кулаковo" Заметчинского района Пензенской области на 12 свиноматках, привитых упомянутой вакциной двукратно с интервалом 20 дней в дозе 1 см3.
Результаты исследований в РТГА сывороток крови от свиноматок, иммунизированных этой вакциной, приведены в табл. 5.
Осложнений после вакцинации не наблюдалось. Эффективность вакцины составила 97%.
Пример 10.
Эффективность инактивированной эмульсионной вакцины против ПВИС из штамма "Вл-94", изготовленной так, как описано в примере 2, проверена в АО "Вишневское" Воронежской области на 10 свиноматках, привитых упомянутой вакциной двукратно с интервалом 20 дней в дозе 1 см3.
Результаты исследований в РТГА сывороток крови от свиноматок, иммунизированных этой вакциной, приведены в табл. 6.
Осложнений после вакцинации не наблюдалось. Эффективность вакцины составила 98%.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемого изобретения следующей совокупности условий:
- штамм "Вл-94" ПВС, воплощающий предлагаемое изобретение, предназначен для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии;
- для предлагаемого изобретения в том виде, как оно охарактеризовано в независимом пункте формулы изобретения, подтверждена возможность его осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- штамм "Вл-94" ПВС, полученный в соответствии с предлагаемым изобретением, расширяет арсенал новых высокопродуктивных штаммов гомологичного вируса, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления эффективных вакцинных препаратов. Следовательно, предлагаемое изобретение соответствует условию патентоспособности "промышленная применимость".
Источники информации
1. Сюрин В.Н. и др. Вирусные болезни животных. М., ВНИТИБП, 1998, 573-584.
2. Ruckenbauer G.M. et al. Can. J. Соmp. Med., 1978, 42, 278.
3. Заявка Франции 2781159, А 61 К 39/23, 21.03.2000 г.
4. Пат. России 1538305, А 61 К 39/295, 15.12.94 г. (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНАКТИВИРОВАННАЯ ЭМУЛЬСИОННАЯ ВАКЦИНА ПРОТИВ ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 2002 |
|
RU2214276C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ЭМУЛЬСИОННОЙ ВАКЦИНЫ ПРОТИВ ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 2002 |
|
RU2214275C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА И ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 2004 |
|
RU2269361C2 |
| ШТАММ № R-72 ВНИИЗЖ ПАРВОВИРУСА СОБАК ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2003 |
|
RU2242994C1 |
| ВАКЦИНА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ | 2002 |
|
RU2236253C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ЭМУЛЬСИОННОЙ ИНАКТИВИРОВАННОЙ ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ | 2002 |
|
RU2236254C2 |
| ШТАММ "СИНЛАК" ВИРУСА PESTIS SUUM ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ | 2001 |
|
RU2180237C1 |
| ШТАММ "КПР-96" ВИРУСА РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И/ИЛИ ВАКЦИННЫХ ПРЕПАРАТОВ | 2005 |
|
RU2295567C1 |
| ВАКЦИНА ПРОТИВ РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2006 |
|
RU2316346C2 |
| ШТАММ "БИСС № 113" ВИРУСА СИНДРОМА СНИЖЕНИЯ ЯЙЦЕНОСКОСТИ - 76 ПТИЦ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ ПРЕПАРАТОВ | 2002 |
|
RU2221865C1 |
Изобретение относится к биотехнологии, в частности к ветеринарной вирусологии. Новый вакцинный штамм "Вл-94" парвовируса свиней (ПВС) обладает высокой иммуногенной активностью. Штамм хорошо размножается в перевиваемой культуре клеток почки поросенка (ППК) и накапливается в титре 8,0 Ig ТЦД50/см3 через 18-24 ч культивирования. Полученный штамм обладает высокой биологической, антигенной и иммуногенной активностью и может быть использован для изготовления эффективных вакцинных препаратов. 1 ил., 6 табл.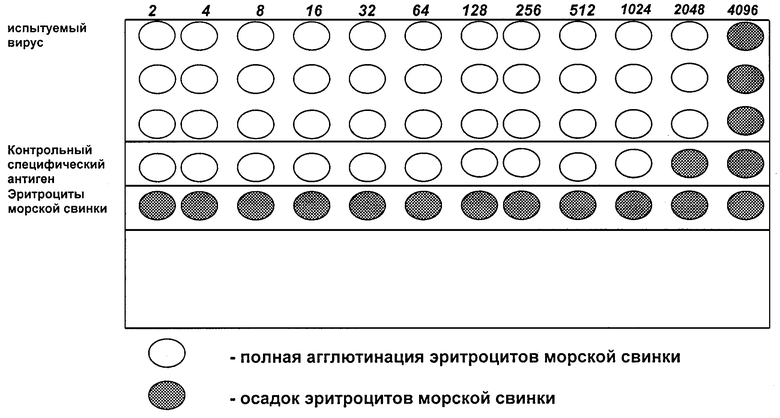
Штамм Parvovirus suum, коллекция ВГНКИ "Вл-94-ДЕП", для изготовления вакцинных препаратов.
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ЛЕПТОСПИРОЗА И ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 1987 |
|
SU1538305A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РАДИАЛЬНОЙ СКОРОСТИ ОБЪЕКТА ПО ВЫБОРКАМ КВАДРАТОВ ДАЛЬНОСТИ | 2021 |
|
RU2781159C1 |
| Способ измерения координаты трека заряженной частицы с помощью проволочной плоской пропорциональной камеры | 1975 |
|
SU562136A1 |
| JP 6217385, 06.08.1987. | |||
Авторы
Даты
2003-09-27—Публикация
2002-02-11—Подача