Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при изготовлении средств диагностики и специфической профилактики парвовирусного энтерита собак (ПВЭС).
ПВЭС - контагиозная болезнь, проявляющаяся рвотой, геморрагическим гастроэнтеритом, миокардитом, лейкопенией, дегидратацией и гибелью щенков моложе пятимесячного возраста.
Заболевание впервые зарегистрировано в Бельгии в 1976 году, затем в США, Канаде, Австралии, Франции, Германии, Великобритании и Швейцарии (1979 г.). В странах СНГ ПВЭС регистрируется с 1980 года. В настоящее время это одна из наиболее широко распространенных инфекционных болезней.
Возбудитель ПВЭС близок по своим свойствам вирусу панлейкопении кошек (ВПЛК). Предполагается, что он может быть мутантной формой этого вируса. ВПЛК близок вирусу энтерита норок (ВЭН), но не идентичен ему, как и возбудитель ПВЭС ВЭН, отличаясь от них по антигенной структуре, гемагглютинирующим свойствам, спектру патогенности для животных и строению генома. Возбудители ПВЭС и панлейкопении кошек различаются менее чем на 1% по нуклеотидной последовательности ДНК, но поражают разных хозяев. Обнаружена антигенная общность всех парвовирусов (у собак, кошек, норок, крыс, свиней, мышей), однако возбудитель ПВЭС четко дифференциируется от парвовирусов кошек и норок. Установлено также различие физической карты геномов этих вирусов.
Заражение первичных и перевиваемых культур клеток кошек и собак показало, что ВПЛК размножается только в кошачьих клеточных культурах, а возбудитель ПВЭС - в культурах клеток как собак, так и кошек.
Наиболее четкую идентификацию возбудителя ПВЭС и дифференциацию его от ВЭН и ВПЛК проводят с помощью моноклональных антител.
Вакцинопрофилактика ПВЭС занимает ведущее место в комплексе противоэпизоотических мер, направленных на борьбу с этим заболеванием. Для профилактики ПВЭС используют гетерологические, аттенуированные или инактивированные вакцины, приготовленные из близкородственных вирусов, выращенных на чувствительных гетеро- или гомологичных биологических системах [1].
Известен штамм CPV-916 (ATCC VR 2006) парвовируса собак (ПВС), выращенный на чувствительных гетеро- или гомологичных культурах клеток и используемый для изготовления вакцинных препаратов [2].
Известен штамм CPVA-BN 80/82 САРМ V-290 ПВС, выращенный на чувствительной гетерологичной культуре клеток и используемый для изготовления вакцинных препаратов [3].
Известен штамм "Риэль" ПВС, выращенный на чувствительной гетерологичной культуре клеток и используемый для изготовления вакцинных препаратов [4].
В связи с тем, что периодически продолжают выделять новые возбудители ПВЭС, отличающиеся по структуре генома, антигенными и иммуногенными свойствами, необходимость поиска, отбора и изучения эпизоотических изолятов ПВС в целях получения новых производственных штаммов для изготовления диагностических и вакцинных препаратов остается актуальной.
В задачу создания настоящего изобретения входило получить новый производственный штамм ПВС, обладающий высокой биологической, антигенной и иммуногенной активностью в нативном (культуральная вирусная суспензия) виде и обеспечивающий изготовление высокоспецифичных диагностических и вакцинных препаратов.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала производственных штаммов ПВС, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления высокоспецифичных диагностических и вакцинных препаратов.
Указанный технический результат достигнут получением штамма №R-72 ВНИИЗЖ ПВС, используемого для изготовления диагностических и вакцинных препаратов.
Штамм №R-72 ВНИИЗЖ является новым, ранее неизвестным. Исходный вирус для получения штамма №R-72 ВНИИЗЖ выделен в 1992 году к.в.н., с.н.с. Старовым С.К. из печени павшей собаки породы Бассет-хаунд в возрасте 1 года, принадлежащей частному владельцу. Штамм адаптирован к первичнотрипсинизированным культурам клеток почки котенка, щенка, эмбриона норки и перевиваемой культуре клеток почки свиньи ППК.
Полученный штамм депонирован во Всероссийской государственной коллекции микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов Министерства сельского хозяйства и продовольствия РФ (ВГНКИ) 15.05.2000 г. под регистрационным №R-72 ВНИИЗЖ.
Указанный штамм по специфичности и активности не уступает другим штаммам возбудителей ПВЭС, штаммам ВЭН и ВПЛК, определяемых с помощью наборов ИФА, выпускаемых фирмой "Нарвак". Кроме того, в РТГА титровали испытуемый вирус с полученными из ВГНКИ сыворотками норок, иммунизированных парвовирусом штамма "Родники". Во всех случаях титры вируса были примерно одинаковыми и составляли 1:128 и 1:256.
Преимуществом предлагаемого штамма является его технологичность:
стабильно высокое накопление вируса в культурах клеток и высокая биологическая, антигенная и иммуногенная активность. Экспериментально подтверждена возможность его использования в составе ассоциированных вакцин.
Сущность изобретения поясняется в конце описания, где представлены нуклеотидные последовательности фрагментов гена VP2 различных штаммов и изолятов возбудителя ПВЭС.
Штамм №R-72 ВНИИЗЖ ПВС характеризуется следующими признаками и свойствами.
Морфологические свойства
Штамм №R-72 ВНИИЗЖ относится к семейству Parvoviridae, роду Parvovirus, виду Parvovirus canine и обладает морфологическими признаками, характерными для парвовируса: форма вириона икосаэдрическая, диаметр 20-25 нм, плавучая плотность 1,38-1,43 г/см3.
В состав вириона входит одноцепочечная линейная молекула ДНК.
Устойчив к эфиру, хлороформу, трипсину и др.
Антигенные свойства
По своим антигенным свойствам штамм №R-72 ВНИИЗЖ ПВС близок вирусу панлейкопении кошек и вирусу энтерита норок, но не идентичен им, отличаясь от них по структуре генома, гемагглютинирующим свойствам и спектру патогенности для животных.
Штамм №R-72 ВНИИЗЖ ПВС имеет родство с парвовирусами крыс, свиней и мышей. Все названные возбудители имеют 80% гомологии рестрикционных участков, в других сайтах имеются различия.
У переболевших и вакцинированных животных образуются антитела, выявляемые в РН, РТГА и РДП.
При иммунизации собак и кроликов живой вирус индуцирует образование вирусспецифических антител, выявляемых в РТГА в разведении 1:256-1:2048 и в РН на культуре клеток ППК в титрах 5,0-7,0 log2.
При определении антигенного соответствия штамма №R-72 ВНИИЗЖ ПВС в ИФА с близкородственными возбудителями энтерита норок штамма "Родники" и панлейкопении кошек использовали диагностический набор фирмы "Нарвак" на основе моноклональных антител. Кроме того, была подтверждена специфичность штамма №R-72 ВНИИЗЖ ПВС в РТГА с сывороткой, полученной от норок, иммунизированных антигеном ВЭН штамма "Родники" производства ВГНКИ.
Было проведено сравнительное исследование первичной структуры гена белка VP2. Сравнительный анализ установленных структур штамма №R-72 ВНИИЗЖ ПВС и других близкородственных вирусов и изолятов: multifel, dan, sample 2, isolate и canvak, предоставленных фирмой "Нарвак", показал замену в 18 и 41 кодоне, которая является значимой и приводит к замене аминокислот аргинина на лизин и аланина на валин.
Биотехнологические характеристики
Штамм №R-72 ВНИИЗЖ ПВС проявляет высокую биологическую, антигенную и иммуногенную активность в нативном, лиофилизированном виде и в виде культуральной вируссодержащей суспензии. Штамм предназначен для изготовления диагностических и вакцинных препаратов при ПВЭС.
Штамм №R-72 ВНИИЗЖ репродуцируется в монослойных культурах клеток (первичнотрипсинизированных культурах клеток почки котенка и щенка и перевиваемой культуре клеток ППК) и в течение 48-96 часов инкубирования накапливается в титре 1:128-1:256 ГАЕ. Сохраняет исходные характеристики при пассировании в чувствительных биологических системах в течение 60 пассажей.
Хемо- и генотаксономическая характеристика
Штамм №R-72 ВНИИЗЖ является ДНК-содержащим вирусом с молекулярной массой 1,5-2 МД, доля Г+Ц составляет 41-53%.
Нуклеиновая кислота представлена одноцепочечной линейной молекулой. Вирион имеет белковую оболочку, состоящую, по одним данным, из трех белков (А, В, С), по другим выявлен 4-й белок Д, который является продуктом ферментативного расщепления более крупного белка. Составлена специфическая эпитопная карта с вариантом последовательностей гена каждого белка у возбудителей парвовирусного энтерита собак, норок и енотов.
Проведено определение первичной структуры участка генома вируса с помощью ПЦР. Результаты исследований представлены на графическом материале. Сравнительный анализ показал, что штамм №R-72 ВНИИЗЖ ПВС отличается от других возбудителей ПВЭС (multifel, dan, sample 2, isolate и canvak) на две аминокислоты и эта замена является существенной.
Физические свойства
Молекулярная масса вириона составляет 5,5-6,2 МД. При электронно-микроскопических исследованиях концентрированного очищенного парвовируса собак штамма №R-72 ВНИИЗЖ обнаружены частицы диаметром 20-25 нм икосаэдрической формы. Плавучая плотность частиц в хлористом цезии составляет 1,38-1,43 г/см3. Коэффициент седиментации 110-122 S.
Устойчивость к внешним факторам
Вирус штамма №R-72 ВНИИЗЖ устойчив к эфиру, хлороформу, трипсину и другим растворителям липидов, стабилен при рН 3,0-9,0, а также к прогреванию при 56°С в течение 1 часа.
Дополнительные признаки и свойства
Иммуногенная активность - иммуногенен в составе живой лиофилизированной вакцины.
Реактогенность - реактогенностью не обладает.
Патогенность - при внутримышечном введении собакам заболевания не вызывает.
Вирулентность - авирулентен для собак при контактном, аэрозольном и парентеральном заражении.
Антигенные свойства - вирус индуцирует у собак образование вируснейтрализующих и гемагглютинирующих антител.
Гемагглютинирующие свойства - гемагглютинирующая активность определяется в РГА с эритроцитами поросенка.
Стабильность биологических свойств. Сохраняет исходные характеристики при пассировании в чувствительных биологических системах в течение 60 пассажей.
Исходя из полученных данных можно утверждать, что штамм №R-72 ВНИИЗЖ по антигенному и иммунологическому спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным вариантом ПВС.
По мнению заявителя, предлагаемый штамм соответствует условиям патентоспособности "новизна" и "изобретательский уровень".
Сущность предложенного изобретения пояснена примерами его использования.
Пример 1.
Получение штамма
Штамм №R-72 ВНИИЗЖ ПВС был изолирован из печени павшей собаки. Подготовку материала проводили общепринятыми методами.
Биологические и вирусологические методы включали адаптацию вируса, выделенного от павшей собаки, к культурам первичнотрипсинизированных и перевиваемых линий клеток. Были использованы первичные культуры клеток почки котенка, щенка и перевиваемые культуры клеток ППК.
Первичные и перевиваемые культуры клеток выращивали на соответствующих питательных средах во флаконах емкостью 50 см3, отмывали от ростовой среды и заражали 10%-ной органной вируссодержащей суспензией (множественность заражения составила 10 ТЦД50 на клетку), приготовленной в растворе Хенкса с 0,5% ГЛА с антибиотиками по стандартной рецептуре. Для удаления микрофлоры и балластных клеточных компонентов суспензию обрабатывали хлороформом в соотношении 1:10 с последующим центрифугированием. После 30 минутного инкубирования при 37°С во флаконы вносили по 5-10 см3 поддерживающей среды и инкубировали при 37°С до появления ЦПД. При наличии ЦПД (округление клеток, повышение их оптической плотности, дегенерация и отделение клеток от стекла) флаконы подвергали замораживанию - оттаиванию, очистке от клеточной взвеси хлороформом и центрифугированию при 3000 об/мин в течение 15 минут. Полученный вируссодержащий материал использовали для последующих пассажей и исследования в РГА, РН и ИФА на наличие вирусного антигена, при этом использовали набор типоспецифических сывороток, полученных из ВГНКИ и фирмы "Нарвак".
Результаты адаптации вируса к различным культурам клеток представлены в таблице 1.
Данные, приведенные в таблице 1, свидетельствуют о хорошей адаптационной активности штамма №R-72 ВНИИЗЖ ПВС к используемым клеточным культурам.
Изолированный с помощью перечисленных методов вирус был исследован в РГА, РН и ИФА с набором диагностикумов на некоторые близкородственные штаммы парвовирусов плотоядных.
Результаты исследований представлены в таблице 2.
Приведенные в таблице 2 результаты свидетельствуют о том, что штамм №R-72 ВНИИЗЖ ПВС является близкородственным к другим возбудителям парвовирусного энтерита плотоядных.
Пример 2.
Получение гипериммунной сыворотки на щенках собак и кроликах
Для гипериммунизации животных использовали вирус штамма №R-72 ВНИИЗЖ, полученный в монослойной культуре клеток ППК. Вируссодержащую суспензию очищали от балластных примесей центрифугированием при 3000 об/мин.
Очищенный вирус концентрировали в 100 раз добавлением 10% полиэтиленгликоля (ПЭГ) ММ 6000.
Концентрированный антиген в объеме 1 см3 вводили внутримышечно кроликам и щенкам собак. Через 21 день иммунизацию повторили и через 21 день провели отбор проб сывороток крови.
Проверку активности сывороток проводили в РТГА с эритроцитами поросенка.
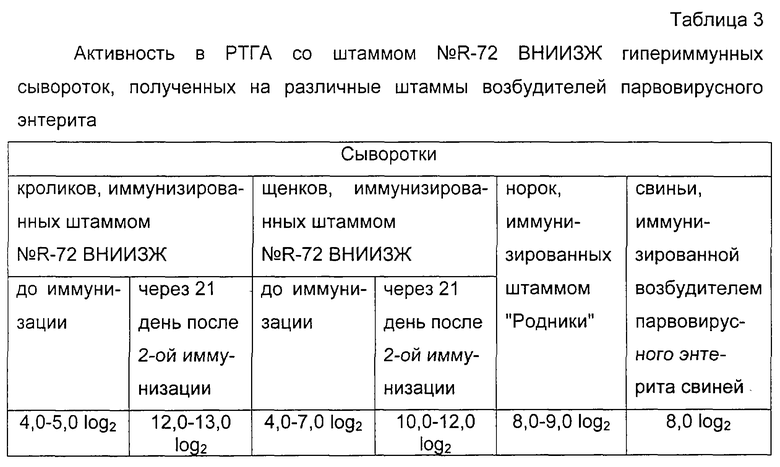
Характеристика сывороток представлена в таблице 3.
Данные таблицы 3 свидетельствуют, что вирус штамма №R-72 ВНИИЗЖ при внутримышечном введении в организм животных вызывает образование специфических антител.
Пример 3.
Приготовление и испытание живой лиофилизированной вакцины
ПВС штамма №R-72 ВНИИЗЖ входит в качестве компонента в ассоциированную вакцину вместе с возбудителем чумы плотоядных штамма "Рокборн". Вакцину готовят из равных объемов возбудителя ПВЭС штамма №R-72 ВНИИЗЖ, выращенного в монослое клеток ППК, и вируса чумы плотоядных, выращенного в монослое клеток Vero. В полученную вируссодержащую жидкость добавляют защитную среду (на 1 л вирусной суспензиии добавляют 150 см3 20%-ного раствора ГЛА, 35 см3 20%-ного раствора желатозы, 60 см3 50%-ного раствора сахарозы). Полученную суспензию расфасовывают в стеклянные флаконы по 1 см3 и подвергают лиофилизации. Полученный препарат в соответствии с ТУ по своим физико-химическим и иммунобиологическим свойствам должен соответствовать требованиям и нормам ТУ:
Внешний вид: сухая масса цилиндрической формы.
Цвет: желтовато-розовый.
Наличие посторонней примеси, трещин флаконов, отсутствие этикеток: не допускается.
Массовая доля влаги: не более 5%.
Растворимость: в пределах 1-2 минут.
Стерильность: не должно быть бактериальной и грибной микрофлоры.
Контаминация микоплазмами: рост микоплазм не допускается.
Безвредность: все животные должны оставаться живыми и здоровыми в течение 14 суток наблюдения после введения двукратной дозы вакцины.
Иммуногенная активность: при постановке РТГА прирост титров антител в сыворотке крови вакцинированных животных должен составлять не менее 2,0 log2.
Пример 4.
Эффективность вирусвакцины против ПВЭС на основе штамма №R-72 ВНИИЗЖ проверена в комиссионном опыте в составе ассоциированной вакцины против ПВЭС, аденовирусного гепатита, бешенства и чумы плотоядных в условиях ФГУ ВНИИ защиты животных.
В составе ассоциированной вакцины были использованы следующие компоненты:
- живой возбудитель чумы плотоядных, штамм "Rockborn", 4-5 пассажей, выращенный в перевиваемой культуре клеток Vero, в титре 4,75-6,75 lg ТЦД50/см3;
- живой возбудитель ПВЭС, штамм №R-72 ВНИИЗЖ, выращенный в перевиваемой линии клеток ППК, титр вируса в РГА 1:164-1:128. (Вируссодержащие материалы в соотношении 1:1 после лиофильного высушивания в объеме 1 см3 вошли в состав компонентов сухой вакцины);
- возбудитель бешенства, штамм "ВНИИЗЖ", выращенный в перевиваемой культуре клеток ПСГК-30, с титром до инактивации димером этиленимина (ДЭИ) 6,5-7,0 lg ТЦД50/см3;
- возбудитель аденовирусного гепатита собак, тип 1, выращенный в перевиваемой культуре клеток ПСГК-30, с титром до инактивации ДЭИ 6,5-7,0 lg ТЦД50/см3. (Суспензии после проверки на авирулентность были объединены в соотношении 1:1, сорбированы на ГОА и после фасовки по 1 см3 вошли в состав компонентов жидкой вакцины).
Готовая вакцина прошла контроль на специфичность, безвредность и иммуногенность.
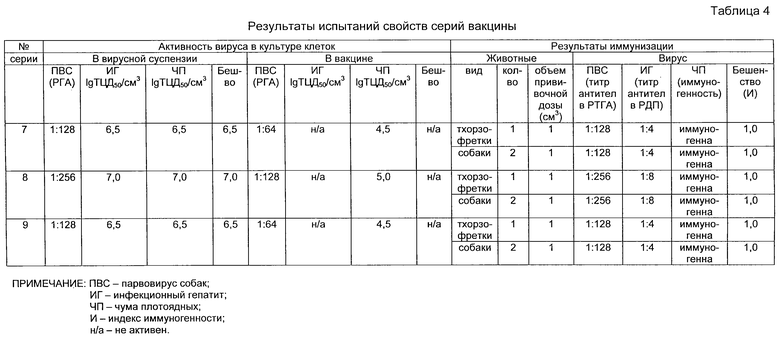
Количественные методы контроля ассоциированной вакцины на лабораторных животных (тхорзофретках и собаках) позволили определить прививную дозу препарата и иммунологические свойства образцов вакцины. Результаты испытаний свойств серий вакцины приведены в таблице 4.
Результаты испытаний показали, что введение ассоциированной вакцины против парвовирусного энтерита, аденовирусного гепатита, бешенства и чумы плотоядных в дозе 1-2 см3 к 21 дню вызывало образование у животных высокого титра специфических антител, что свидетельствовало об иммуногенной активности препарата.
Ассоциированная вакцина была испытана в различных регионах России. Рекламаций с мест применения не поступало.
Пример 5.
Эффективность вирусвакцины против ПВЭС на основе штамма №R-72 ВНИИЗЖ проверена в составе ассоциированной вакцины против ПВЭС, аденовирусного гепатита и чумы плотоядных, а также ассоциированной вакцины против ПВЭС, аденовирусного гепатита, чумы плотоядных и бешенства в условиях Владимирской областной ветеринарной лаборатории в порядке производственной апробации при иммунизации собак. Было использовано 500 доз вакцин. После их применения поствакцинальных осложнений и прорывов иммунитета не наблюдалось.
Пример 6.
Эффективность вирусвакцины против ПВЭС на основе штамма №R-72 ВНИИЗЖ проверена в составе ассоциированной вакцины против ПВЭС, аденовирусного гепатита и чумы плотоядных, а также ассоциированной вакцины против ПВЭС, аденовирусного гепатита, бешенства и чумы плотоядных в условиях Тюменской области в порядке производственной апробации при иммунизации собак. Было использовано около 1500 доз вакцин. После применения указанных препаратов поствакцинальных осложнений и прорывов иммунитета не отмечалось.
Пример 7.
Эффективность вирусвакцины против ПВЭС на основе штамма №R-72 ВНИИЗЖ проверена в составе ассоциированной вакцины против ПВЭС, аденовирусного гепатита и чумы плотоядных. Вакцина в количестве приблизительно 20000 доз применялась в порядке производственной апробации для иммунизации собак в 8 регионах Сибири и Дальнего Востока. После применения указанного препарата поствакцинальных осложнений и прорывов иммунитета не наблюдалось.
Таким образом, приведенная выше информация свидетельствует о выполнении при использовании предлагаемого изобретения следующего ряда условий:
- штамм №R-72 ВНИИЗЖ ПВС, воплощающий предлагаемое изобретение, предназначен для использования в сельском хозяйстве, а именно в ветеринарной вирусологии и биотехнологии;
- для предлагаемого изобретения в том виде, как оно охарактеризовано в независимом пункте формулы изобретения, подтверждена возможность его осуществления с помощью описанных в заявке или известных до даты приоритета средств и методов;
- штамм №R-72 ВНИИЗЖ ПВС, полученный в соответствии с предлагаемым изобретением, обладает высокой специфической, иммуногенной и антигенной активностью и пригоден для изготовления диагностических и вакцинных препаратов.
Следовательно, предлагаемое изобретение соответствует условию патентоспособности "Промышленная применимость".
Источники информации
1. Сюрин В.Н., Самуйленко А.Я. и др. Вирусные болезни животных. - Москва, ВНИТИБП. - С.561-570.
2. Пат. США №4193991; 424-89, 435-238; 18.03.80 г.
3. Авт.свид. ЧССР №252747; А 61 К 39/23, 39/175; 15.10.87 г.
4. Пат. России №2147609; С 12 N 7/00, А 61 К 39/295, 39/23, 39/235, 39/29; 20.04.2000 г.


Изобретение относится к ветеринарии, вирусологии и биотехнологии. Штамм № R-72 ВНИИЗЖ возбудителя парвовирусного энтерита собак (ПВЭС) получен путем многократных последовательных пассажей на чувствительных первичных и перевиваемых культурах клеток. Штамм депонирован во Всероссийской государственной коллекции микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов МСХ и продовольствия РФ (ВГНКИ) 15.05.2000 г. под регистрационным № R-72 ВНИИЗЖ. Вирус штамма № R-72 ВНИИЗЖ продуцируется в первичных культурах клеток почки котенка и щенка и перевиваемых клетках почки свиньи в течение 48-96 часов инкубирования и накапливается в титре 1:256. Штамм № R-72 ВНИИЗЖ сохраняет исходные характеристики при пассировании в культурах клеток в течение 60 пассажей. Штамм обладает высокой биологической, антигенной и иммуногенной активностью и пригоден для изготовления высокоспецифичных диагностических и вакцинных препаратов. 4 табл.
Штамм парвовируса собак сем. Parvoviridae, род Parvovirus, вид Parvovirus canine, коллекция ВГНКИ №R-72 ВНИИЗЖ, для изготовления диагностических и вакцинных препаратов.
| US 4193991 А, 18.03.1980 | |||
| ШТАММ ВИРУСА CANINE PARVOVIRUS "РИЭЛЬ" ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ ПАРВОВИРУСНОЙ ИНФЕКЦИИ ПЛОТОЯДНЫХ И ВАКЦИНЫ "ВЛАДИВАК" ПРОТИВ ВИРУСНЫХ БОЛЕЗНЕЙ ПЛОТОЯДНЫХ НА ЕГО ОСНОВЕ | 1998 |
|
RU2147609C1 |
Авторы
Даты
2004-12-27—Публикация
2003-08-05—Подача