Изобретение относится к макролидным соединениям, включающим макроциклические лактоны, такие как соединения LL -Р28249 α-λ, 23-оксо- или 23-иминопроизводные соединений LL-F28249 α-λ, соединения милбемицина, такие как милбемицин и милбемициноксим, соединения авермектина, такие как абамектин, ивермектин и дорамектин, и их смеси полезны для профилактики и регуляции гельминтоза и инфекций, переносимых клешами и членистоногими эндо- и эктопаразитами теплокровных животных. Подкожная инъекция водных композиций является предпочтительным методом введения таких соединений.
Вакцины применяют для защиты теплокровных животных от различных болезней с помощью подкожной инъекции. Однако не известна композиция вакцины, содержащая макролидное соединение и антигены. Главная причина отсутствия такой смешанной вакцины обусловлена тем, что водные инъецируемые композиции макролидных соединений содержат диспергаторы, которые, как известно, взаимодействуют с белками к влияют на проницаемость внешней мембраны клеток бактерий. Такое взаимодействие может денатурировать или иным образом повреждать белки, такие как антигены.
Патент Великобритании А-2030043 описывает инъецируемые композиции, которые содержат тетрамизол или его левовращающий изомер и вакцину. Однако эта заявка не раскрывает смешанную вакцину, которая включает сложное макролидное соединение. Далее, эта заявка не описывает использование диспергатора - важного компонента водных макролидных инъецируемых композиций.
Следовательно, цель настоящего изобретения - обеспечить стабильные композиции вакцин, содержащие макролидные соединения и антигены. Также целью является обеспечение стабильных композиций макролидных соединений в отсутствие антигена.
Целью изобретения является также обеспечение метода предотвращения или регуляции гельминтоза, инфицирования клещами и членистоногими эндо- и эктопаразитами и микробных и вирусных болезней у теплокровных животных.
Следующей целью настоящего изобретения является обеспечение способа получения стабильных композиций вакцин.
Эти и другие цели и признаки настоящего изобретения станут более очевидными из детального списания изобретения, следуемого далее.
Настоящее изобретение относится к стабильным композициям вакцин. Композиции содержат, на основе массы к объему, около 0,05-2,5% макролидного соединения, около 0,1-6% водорастворимого органического растворителя, около 1-8% диспергатора, 10-50% адъюванта, по меньшей мере один антиген, до примерно 0,1% консерванта и солевой раствор или воду, или их смесь.
Было установлено, что композиции вакцин настоящего изобретения стабильны в присутствии диспергатора и могут храниться в течение длительных периодов времени без потери действенности актигена и макролида.
В соответствии с настоящим изобретением стабильные композиции вакцин содержат макролидное соединение, обозначенное выше, водорастворимый органический растворитель, диспергатор, вспомогательное вещество, по меньшей мере один антиген, возможно, консервант и солевой раствор или воду и их смесь. Изобретение также обеспечивает метод предотвращения или регуляции гельминтоза, инфицирования клещами и членистоногими эндо- и эктопаразитами и заболеваний у теплокровных животных.
Предпочтительные композиции вакцин настоящего изобретения содержат, на основе масса к объему, около 0,1-1% соединения LL-F28249 α-λ, 23-оксо- или 23-иминопроизводного соединения LL-F28249 α-λ, соединения милбемицина, соединения авермектина или их смесь, 0,2-2,5% водорастворимого органического растворителя, 2-7% диспергатора, 20-40% вспомогательного вещества, по меньшей мере один антиген, до примерно 0,1% консерванта и солевой раствор или воду или их смесь.
Макролидные соединения, используемые в изобретении, включают макроциклические лактоны, соединения милбемицина, соединения авермектина и их смеси, описанные ниже.
Макроциклические соединения включают, но не ограничиваются соединениями, описанными в патентах США 5019589, 4886828, 5108992, 5030650 и 5055486, включенных сейчас в рассмотрение.
Предпочтительные макроциклические лактоны включают соединения, обозначенные LL-F28249 α-λ, которые (совместно) выделяют из ферментационного бульона микроорганизма Steptomyces cyaneoqriseus подвида noncyanoqenus, депонированного в NRRL под 15773. Способ получения LL-F28249 α-λ предложен в патенте США 5106994 и его продолжении, патенте США 5169956, включенными здесь в рассмотрение.
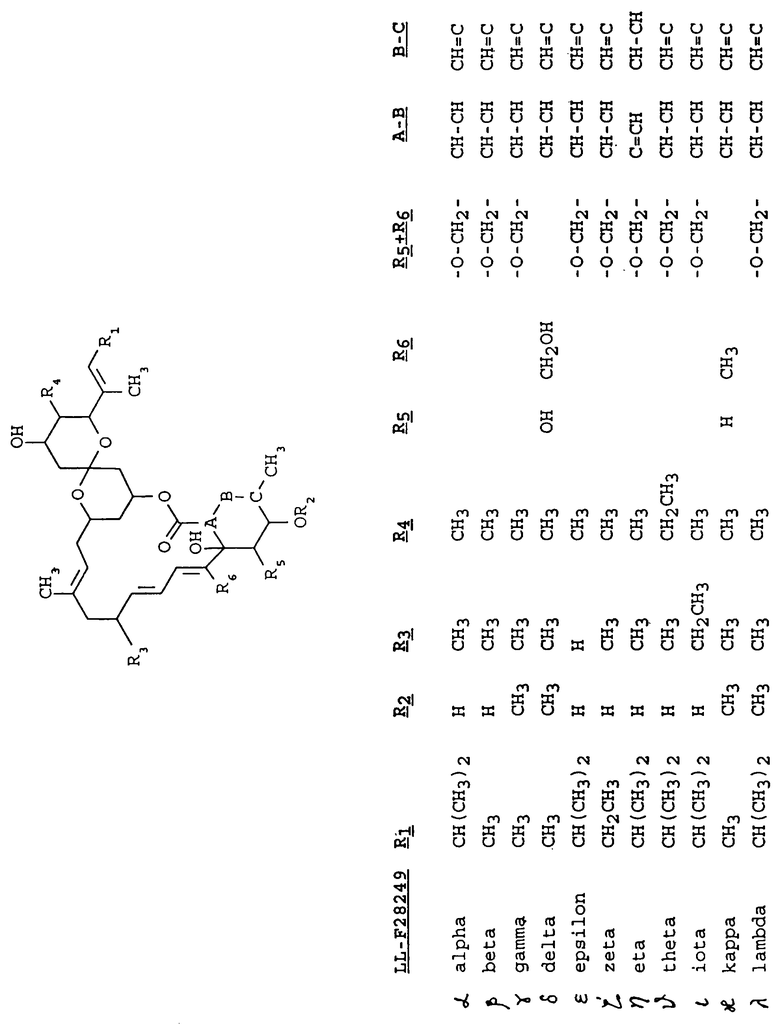
Соединения LL-F28249 α-λ представлены структурной формулой, приведенной в конце описания.
Известны 23-оксо- и 23-иминопроизводные соединений LL-F28249 α-λ используемых в устойчивых композициях вакцин этого изобретения, предложенные в патенте США 4916154, включенные здесь в рассмотрение.
Предпочтительное соединение LL-F28249 α-λ и 23-иминопроизводно соединения LL-F28249 α-λ, используемые в композиции вакцин этого изобретения имеют следующие структурные формулы: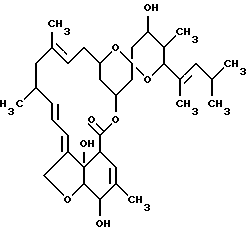
и 23-(О-метилоксим)-LL-F28249 α-λ (моксидектин)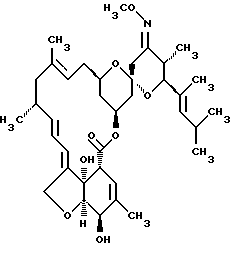
Соединения милбемицина, использующиеся в стабильных композициях вакцин настоящего изобретения, включают милбемицин Д, милбемициноксим и соединения, описанные в патентах США 3950360, 4346171 и 4547520, включенных здесь в рассмотрение, но не ограничиваются ими. Предпочтительными соединениями милбемицина, используемыми в этом изобретении, являются милбемицин Д и милбемициноксим.
Соединения авермектина, используемые в композициях изобретения, включают абамектин, ивермектин, дорамектин и соединения, описанные в патентах CШA 4199569 и 4310519, включенных здесь в рассмотрение, но не ограничиваются ими, причем предпочтительными соединениями являются ивермектин, абамектин и дорамектин. Дорамектин и способ его получения описаны в патенте США 5089480, включенном здесь в рассмотрение.
Антигены, использующиеся в композициях настоящего изобретения, включают антигены, происходящие из бактериальных и вирусных патогенных микроорганизмов теплокровных животных, включая произведенные методом рекомбинантных ДНК, но не ограничиваются ими. Предпочтительные антигены включают Clostridium perfringens типа А, В, С и D, Clostridium septicum, Clostridium tetani, Clostridium chauvoei, Clostridium novyi типа В, Clostridium sordelli, Clostridium haemolytica, Pasteurella, Pasteurella maltocida и Corynebacterium pseudotuberculosis, которые используют для лечения заболеваний, таких как дизентерия ягнят, острая токсемия ягнят (энтеротоксемия), острая токсемия животных (интоксикация крови), столбняк, болезнь "черная ножка", казеозный лимфаденит и пастереллез.
Настоящее изобретение также обеспечивает способ получения стабильных композиций вакцин, который включает:
а) смешивание диспергатора с водой с образованием первого раствора,
б) добавление к первому раствору второго раствора, представляющего собой раствор макролидного соединения, описанного выше, в водорастворимом органическом растворителе, с образованием третьего раствора,
в) добавление третьего раствора к первой суспензии, содержащей по меньшей мере один антиген, адъювант и солевой раствор, с образованием второй суспензии и
г) установление во второй суспензии рН 6-7.
Диспергаторы, используемые в способе настоящего изобретения, включают полиоксиэтилированные моноолеаты полиоксиэтилен сорбитана, такие как моноолеат полиоксиэтилен(20)сорбитана (tweenr 80, Harcros Chemicals), полиоксиэтиленовые спирты, такие как лаурет 9 и кетомакрогол 1000, натрий-лаурилсульфат, диоктилнатрийсульфосукцинат, полиэтиленгликоли и блок-сополимеры α-гидро-ω-гидроксиполи(оксиэтилен)поли(оксипропилен)-поли(оксиэтилена), причем моноолеаты полиоксиэтиленсорбитана, такие как моноолеат полиоксиэтилен(20)сорбитана являются предпочтительными.
Было обнаружено, что теплокровные животные, обработанные композициями вакцин настоящего изобретения (содержащими диспергатор), реагируют на вакцинацию так же, как теплокровные животные, обработанные обычными композициями вакцин. Это совершенно необычный результат, поскольку композиции изобретения содержат диспергатор, который, как полагают, обычно денатурирует или иным образом повреждает антигены.
Далее, найдено, что отсутствует вредное воздействие на биологическую доступность и характеристики макролидного соединения в композициях изобретения.
Водорастворимый органический растворитель используют для солюбилизации макролидного соединения. Водорастворимые органические растворители, использующиеся в настоящем изобретении, включают спирты, такие как бензиловый спирт, этанол и метанол, пропиленгликоли к глицеринформаль, причем бензиловый спирт предпочтителен.
Адьювант изобретения используют для стабилизации антигена. Адъюванты настоящего изобретения включают гидроксид алюминия, алюмокалиевые квасцы, протамин, фосфат алюминия и фосфат кальция, причем гель гидроксида алюминия, такой как TASGELR (Pitman-Moore, New Zealand) предпочтителен.
Во второй суспензии предпочтительно устанавливают рН 6-7 добавлением неорганической кислоты, такой как серная кислота, соляная кислота и бромистоводородная кислота. Эта область значений рН выбрана так, чтобы избежать денатурацию антигенов.
В предпочтительном способе настоящего изобретения перед стадией (г) ко второй суспензии добавляют консервант. Консервант, пригодный для использования в настоящем изобретении, включает тимеросал ([(o-карбоксифенил)тио]этилртуть натриевая соль), формальдегид, фенол, пропиленгликоль, глицерин, эфиры п-гидроксибензойной кислоты, бензойную кислоту и бензоат натрия, причем тимеросал предпочтителен.
В другом предпочтительном способе изобретения стадии (а) и (б) проводят при повышенной температуре (больше 25oС) для гарантии солюбилизации диспергатора, макролидного соединения и водорастворимого органического растворителя.
В способе этого изобретения первый раствор содержит по массе 10-25% диспергатора, второй раствор содержит по массе 20-40% макролидного соединения и первая суспензия содержит по массе 25-75% адъюванта.
Настоящее изобретение обеспечивает стабильную макролидную композицию для парентерального введения. Макролидная композиция содержит на основе масса к объему около 0,05-2,5% макролидного соединения, как определено выше, или их смеси, около 0,1-10% водорастворимого органического растворителя, около 1-8% диспергатора, около 10-50% адъюванта и солевой раствор или воду или их смесь. Предпочтительные макролидные композиции настоящего изобретения содержат на основе масса к объему 0,1-1% соединения LL-F28249 α-λ, 23оксо- или 23-иминопроизводного соединения LL-F28249 α-λ, соединения милбемицина, соединения авермектина или их смеси, около 0,2-2,5% водорастворимого органического растворителя, 2-7% диспергаторе, 20-40% адъюванта, по меньшей мере один антиген, до 0,1% консерванта, солевой раствор или воду или их смесь.
Стабильные макролидные композиции этого изобретения могут быть получены смешиванием раствора макролидного соединения, водорастворимого органического растворителя, диспергатора, адъюванта с водой или солевым раствором.
При парентеральном введении композиции вакцин этого изобретения высокоэффективны для профилактики или регуляции гельминтоза, инфицирования клещами и членистоногими эндо- и эктопаразитами и заболеваний теплокровных животных, таких как овцы, рогатый скот, лошади, свиньи, олени, верблюды, домашняя птица, собаки, кошки и козы. Соответственно, настоящее изобретение обеспечивает метод профилактики или регуляции гельминтоза, инфицирования клещами и членистоногими эндо- к эктопаразитами и заболеваний теплокровных животных, который заключается в парентеральном введении животным эффективного количества композиции вакцины настоящего изобретения.
Гельминтоз - широко распространенное заболевание, находимое у многих животных и вызывающее значительные экономические потери во всем мире. Среди гельминтов наиболее часто встречается группа червей, известных как нематоды. Нематоды находятся в кишечном тракте, сердце, легких, кровеносных сосудах и других тканях организма животных и являются первопричиной анемии, потери веса и нарушения питания у инфицированных животных. Они производят серьезные повреждения стенок и тканей органов, в которых они находятся и, при отсутствии лечения, могут приводить к смерти инфицированных животных.
Нематоды, наиболее часто находимые в качестве инфицирующего фактора у жвачных животных, включают Haemonchus и Ostertagia, обычно присутствующие в сычуге, Cooperia, Trichostrongylus и Nematodirus, обычно присутствующие в кишечном тракте, и Dictyocaulus, находимые в легких. У нежвачных животных важные нематоды включают Тохосаrа и Ancylostoma в кишечнике и Dirofilaria в сердце собак, Ascaris в кишечнике свиней, Ascaridia и Неterakis в кишечнике домашней птицы и большие и маленькие Strongyles у лошадей.
Членистоногие эктопаразиты, обычно инфицирующие теплокровных животных, включают иксодовых клещей, вшей, блох, клещей, падальных мух, эктопаразита Lucilla sp. овец, кусающих насекомых и мигрирующих личинок двукрылых, таких как Нypoderma sp. крупного рогатого скота, Gastrophilus лошадей и Cuterebra sp. грызунов.
Обработка животных с целью предотвращения их инвазии вышеуказанными паразитами или с целью снижения или регуляции распространения этих инфицирующих факторов у животных, следовательно, является важным аспектом настоящего изобретения.
Для лучшего понимания изобретения далее представлены следующие примеры, иллюстрирующие изобретение, не ограничивая его объем.
Пример 1
Получение вакцинных композиций моксидектин/6 в 1.
Композицию моксидектин/6 в 1 вакцине, определяемую как композицию номер 1 в таблице I, получают смешиванием TASGELR(300 мл) с нормальным солевым раствором (332,6 мл), добавлением соответствующих концентратов антигенов в количествах, определенных ниже, добавлением раствора моксидектина (предварительно приготовленного смешиванием 30% мас./мас. раствора моксидектина в бензиловом спирте (7,5 мл) с 17% мас./мас. раствором TWEENR 80 (300 мл) при примерно 37oС, фильтрованием и охлаждением образующегося раствора), добавлением 1,3% мас./мас. раствора тимеросала (7,7 мл) и установлением рН 6,5 серной кислотой.
Концентрат антигена - Количество (мл)
Cl. Septicum - 4,4
Cl. novyi В - 1,8
Cl. tetani - 1,85
Cl. perfringens D - 40,5
Cl. chauvoei - 8,75
С.pseudotuberculosis - 2,5
По этой же методике получены композиции моксидектин/6 в1 вакцине, определенные как композиции номер 2, 3 и 4 в таблице I.
Коммерчески доступные 6 в 1 вакцинах производимые Arthur Webster Pty Limited, Castle Hill, New South Wales, Australia, получают по описанной выше методике, за исключением того, что не используют раствор моксидектина. Вакцины 6 в 1, использованные в следующих примерах, определены как композиция номер 5, 6 и 7 в таблице II.
Пример 2
Анализ подсчета яиц нематодов в фекалиях, сероконверсии в антигены клостридий и веса тела ягнят, обработанных композицией моксидектин/6 в 1 вакцине
В этом опыте используют 185 2-4-месячных кросбредных мериносовых ягнят, которые при отъеме, шестью неделями ранее, получили начальную 6 в 1 вакцинацию (2 мл композиции номер 5 в таблице II). Однократную дозу (2 мл) моксидектина/6 в 1 вакцины (композиция номер 1 в таблице I) вводят 92 ягнятам в 0 день опыта, а 93 ягненка получают однократную дозу (2 кл) вакцины 6 в 1 (композиция номер 5 в таблице II). Оба препарата вводят подкожно в верхнюю часть шеи с правой стороны.
Ягнят взвешивают в 0,13 и 28 день опыта, причем в эти дни из прямой кишки 15 ягнят каждой группы отбирают образца фекалий. У этих же ягнят берут образцы крови в 0 и 28 день.
Образцы фекалий анализируют микроскопией на полное количество яиц нематодов. Объединенные образцы сыворотки анализируют на антитела против экзотоксинов Clostridium septicum, tetani и novyi тип B в тесте нейтрализации сыворотки на мышах. Образцы дня 0 (предварительная обработка) из обеих групп объединяют для анализов на антитела. Результаты суммированы в таблицах III, IV и V.
Как можно видеть из данных таблицы III, моксидектин/6 в 1 вакцине (композиция номер 1) высокоэффективна в регуляции нематод. В группе, получающей только вакцину 6 в 1, количество червей после отъема резко возрастает, в то время как количество яиц в группе, обработанной вакциной моксидектин/6 в 1, падает до низкого уровня в образцах после первой обработки и остается низким в конечных образцах на 28 день. Это является особенно важным открытием, поскольку ягнята, получающие вакцину моксидектин/6 в 1, сохраняют низкий уровень червей несмотря на выпас стадом на том же загрязненном пастбище, что и группа, обработанная группой 6 в 1.
Оказалось, что ягнята, обработанные моксидектином/6 в 1 вакцине, реагируют на вакцинацию так же, как ягнята, обработанные 6 в 1 вакцине (таблица IV).
Пример 3
Оценка количества яиц фекальных нематод к сероконверсии в клостридные антигены у овец, обработанных композицией вакцины моксидектин/6 в 1
В опыте используют 188 суягных мериносовых овец в возрасте 2-5 лет, которые должны ягниться примерно через две недели после начала опыта. Их иммунизировали ежегодно вакциной 6 в 1 (Clanvac, CSL Ltd) и за два месяца до опыта поили левамизолом (Nilverm, Coopers Animal Health).
Овец взвешивают в день 0, когда их средний вес составлял 50,7 кг, и распределяют случайным образом на две группы, Девяносто четыре овцы получают однократную дозу (2 мл) вакцины моксидектин/6 в 1 (композиция номер 2 в таблице I) в день 0 опыта, тогда как 94 овцы получают однократную дозу вакцины 6 в 1 (композиция номер 6 в таблице II). Пятнадцать овец каждой группы метят как контрольных для отбора проб фекалий и крови в дни 0 и 24 опыта и дополнительного отбора фекалий в 15 день. Образцы фекалий и сыворотки испытывают как описано в примере 2.
Так как опыт предпринят в коммерческом хозяйстве, то нельзя выдерживать овец, обработанных вакциной 6 в 1, без нематодной обработки после 24 дня опыта, и этих животных обрабатывают перрорально 7 мл CYDECTINR на овцу (Сyаnаmid Websters, Castle Hill New South Wales, Australia) на 25 день. Животным, получившим обработку вакциной моксидектин/6 в 1 в день 0, больше ничего не вводят. Далее, образцы фекалий отбирают у 15 контрольных овец в дни 38, 52 и 65 опыта и эти образцы испытывают на количество яиц, как описано выше.
Как можно видеть из таблицы VI, обе обработки ведут к увеличению количества антител. Преимущественно, как можно видеть из данных таблицы VII, обработка вакциной моксидектин/6 в 1 предотвращает классический околородовой рост яиц нематод у обработанных овец, даже пасущихся вместе с овцами, обработанными вакциной 6 в 1.
Пример 4
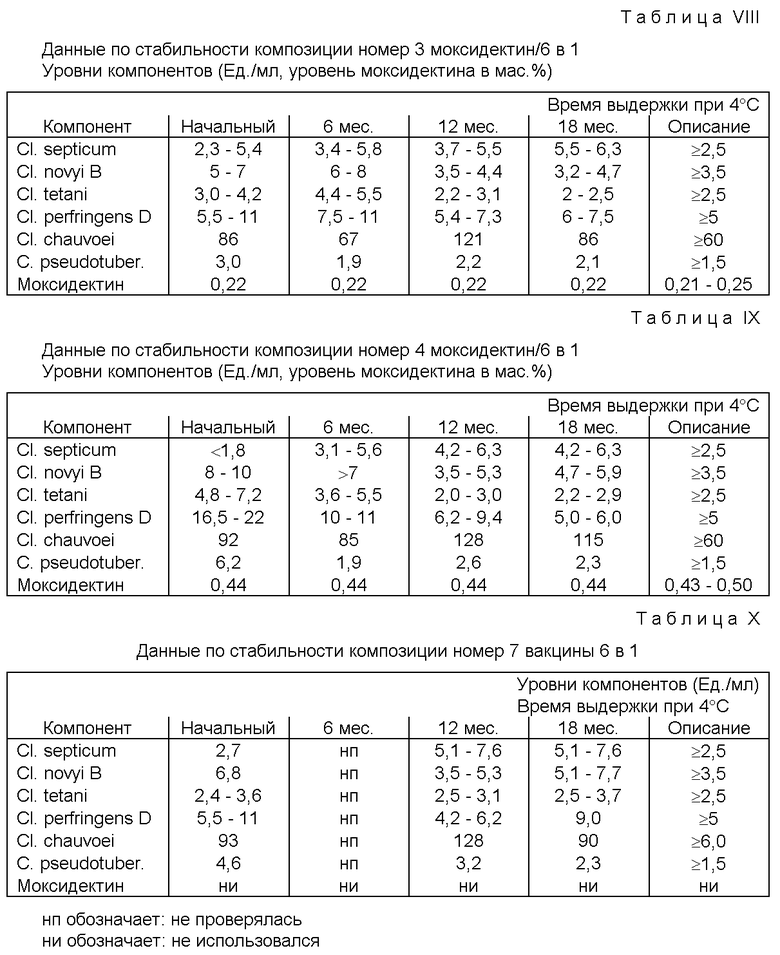
Тесты на стабильность композиций вакцин моксидектин/6 в 1
Уровни моксидектина и активности антигена для двух вакцин моксидектин/6 в 1 (композиции 3 и 4 в таблице I) и активности антигена для обычных вакцин 6 в 1 (композиция номер 7 в таблице II) измеряют после получения и после 6, 12 и 18 месяцев хранения при 4oС. Активности антигена измеряют по методикам анализа, установленным законом и описанным в Британской Фармакопее (Ветеринария), 1977 год. Уровни моксидектина определяют высокоэффективной жидкостной хроматографией. Результаты обобщены в таблицах VIII, IX и X.
Как можно видеть из данных таблиц VIII и IX, активности антигена и уровни моксидектина для композиций 3 и 4 остаются в пределах требований описания. Это особенно удивительное открытие, поскольку все актигенные компоненты являются белками, a TWEENR 80 как известно, денатурирует белки.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПИЛЮЛЬ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ | 1990 |
|
RU2014832C1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ БЕЛОК РЕСПИРАТОРНО-СИНЦИТИАЛЬНОГО ВИРУСА (ВАРИАНТЫ) | 1994 |
|
RU2160119C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА, СПОСОБ ОДНОВРЕМЕННОЙ КОМБИНИРОВАННОЙ ВАКЦИНАЦИИ И СПОСОБ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ | 1993 |
|
RU2121365C1 |
| МАКРОЦИКЛИЧЕСКИЙ ЛАКТОН, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИБИОТИЧЕСКОЙ АКТИВНОСТЬЮ, И ИНСЕКТОАКАРИЦИДНАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2100354C1 |
| СПОСОБ ПОЛУЧЕНИЯ 23-(C-C-АЛКИЛОКСИМОВ)-LL-F-28249 | 1990 |
|
RU2030416C1 |
| БЕНЗИМИДАЗОЛЬНЫЕ АНТИГЕЛЬМИНТНЫЕ КОМПОЗИЦИИ | 2009 |
|
RU2493825C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ В ВИДЕ МИКРОСФЕРИЧЕСКИХ ЧАСТИЦ И КОМПОЗИЦИЯ В ВИДЕ МИКРОСФЕРИЧЕСКИХ ЧАСТИЦ | 1991 |
|
RU2011377C1 |
| ГЕРБИЦИДНАЯ ВОДОРАСТВОРИМАЯ ГРАНУЛИРОВАННАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2152151C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА | 1990 |
|
RU2029783C1 |
| ПЕСТИЦИДНЫЕ АГЕНТЫ С ПОКРЫТИЕМ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ КОМПОЗИЦИИ | 1995 |
|
RU2152152C2 |

Изобретение относится к медицине и ветеринарии, а именно к определенным стабильным композициям вакцин, содержащим макроциклический лактон, соединения милбемицина, соединения авермектина или их смеси, по меньшей мере, один антиген, диспергатор, адъювант, водорастворимый органический растворитель и солевой раствор, или воду, или их смеси. Изобретение также относится к стабильным композициям, описанным выше, макроциклического лактона, соединениям милбемицина, соединениям авермектина или их смесям, но без антигена. Изобретение также относится к способу предотвращения или регуляции гельминтоза, инфицирования клещами и членистоногими эндо- и эктопаразитами и бактериальных и вирусных заболеваний у теплокровных животных парентеральным введением композиций изобретения. Изобретение также относится к способу получения композиций изобретения. Изобретение обеспечивает получение стабильных и эффективных вакцин с длительным сроком хранения. 4 с. и 11 з.п.ф-лы, 10 табл.
| СПОСОБ ПОЛУЧЕНИЯ МАКРОЛИДНЫХ СОЕДИНЕНИЙ | 1987 |
|
RU2024527C1 |
| US 4916153, 10.04.1990 | |||
| US 5314999, 24.05.1994 | |||
| СПОСОБ ЛЕЧЕНИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ | 1991 |
|
RU2050830C1 |
Авторы
Даты
2003-10-10—Публикация
1996-06-28—Подача