Изобретение относится к области органической химии, а именно к способу получения гексахлорэтана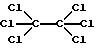 ,
,
который может найти применение в производстве хладона 113, таблеток для дегазации, при отливе алюминиевых деталей, при получении дезодорантов, бактерицидных препаратов, а также для получения дымообразующих смесей.
В промышленности гексахлорэтан производят хлорированием 1,2-дихлорэтана над активированным углем, который служит катализатором. (Промышленные хлорорганические продукты. Под ред. Ошина Л.А., Химия. 1978. 195[1]). Процесс проводят по следующей методике: 1,2-дихлорэтан поступает в испаритель, превращаясь в газ, смешивается с хлором, затем полученная смесь направляется в трубчатый реактор, нагретый до 270-290oС и заполненный активированным углем АГ-3. Хлор обычно подается в 30%-ном избытке по отношению к 1,2-дихлорэтану. В результате реакции образуется сложная смесь хлорсодержащих соединений: НСl, трихлорэтан, тетрахлорэтилен, тетрахлорэтан, гексахлорбутадиен и гексахлорэтан. Выход гсксахлорэтана составляет 17%.
CH2Cl-CH2Cl+Сl2-->ССl3-ССl3+HCl+СНСl= СНСl2+CCl2= CCl2+ССl2= ССl-ССl= ССl2
Недостатками данного метода синтеза гексахлорэтана являются:
1. Низкий выход гексахлорэтана - 17%.
2. Использование газообразного хлора, что требует применения дорогостоящего коррозионно-стойкого оборудования. Кроме того, необходим специальный технологический узел (резервуары, трубопроводы, контрольно-измерительная аппаратура, насосы, защитная зона) для хранения, дозировки, а также для утилизации хлора и хлорсодержащих отходов.
3. Высокая температура реакции (270-290oС) и связанные с этим большие затраты энергии.
4. Низкая селективность реакции, образование побочных трудноразделяемых продуктов.
Известен метод получения гексахлорэтана хлорированием тетрахлорэтилена в присутствии безводного хлорного железа (Промышленные хлорорганические продукты. Под ред. Ошина Л.А., Химия. 1978, 196 [2]). По данному методу в оптимальных условиях (100-110oС, 4 ч, мольное соотношение ([С2Сl4]:[FеСl3]=100: 1) выход гексахлорэтана составляет 40-45%.
ССl2=ССl2+Сl2-->ССl3ССl3
Метод имеет следующие недостатки.
1. Низкий выход гексахлорэтана (40-45%).
2. Использование в качестве реагента высотоксичного и экологически опасного хлора.
3. Сложность аппаратурного оформления процесса, т.к. для хранения, дозировки и утилизации отходов хлора требуется специальное технологическое оборудование из коррозионно-стойких материалов.
Необходимо отметить, что гексахлорэтан был впервые получен из чстыреххлористого углерода, пропусканием его паров через стеклянную трубку, нагретую до 500oС (W.Kolbe // Lieb. Ann. В. 54, S. 14 [3]). Разложение CCl4 протекает неселективно и приводит к получению (наряду с гексахлорэтаном) хлора, дихлорацителена и неидентифицированных продуктов.
Закономерности термического распада ССl4 были исследованы в более поздних трудах (А. Е.Шилов, Р.Д.Сабирова // ДАН СССР. Сер. физ. хим., 1957, Т. 114, 5, с. 1058[4]; А.Е.Шилов, Р.Д.Сабирова // Сер. физ. хим., 1960, т. 34, с. 860[5] ; А.Е.Шилов, Р.Д.Сабирова // Сер. физ. хим., 1959, т. 33, с. 1365 [6] ). Авторы этих работ установили, что высокотемпературный распад CCl4 в интервале температур от 227 до 874К сопровождается образованием хлора, тетрахлорэтилена и гексахлорэтана, выход которого не превышает 1,7%.
CCl4-->ССl3-ССl3+CCl2=CCl2+Cl2
На состав термического разложения CCl4 существенное влияние оказывает материал реактора. Так, Коршак В.В. с сотрудниками исследовали разложение CCl4 в фарфоровой трубке, нагретой до 400-700oС и установили, что основным продуктом реакции является тетрахлорэтилен, а гексахлорэтан образуется в количестве ~10%, а максимальная конверсия CCl4 не превышает 52% (В.В.Коршак, Ю.А.Степихеев, Л.Ф.Вертолатова // ЖОХ, 1947, 17, c. 1626[7]).
Метод получения гексахлорэтана путем термического разложения имеет следующие недостатки.
1. Разложение CCl4 с заметной скоростью протекает при повышенной температуре (400-700oС), следовательно, необходимы большие энергетические затраты.
2. Процесс разложения CCl4 проходит неселективно и приводит к образованию смеси трудноразделяемых продуктов.
3. Низкий выход целевого продукта.
Наиболее близким по технической сущности к данному способу является способ получения ГХЭ (гексахлорэтана) из ЧХУ (четыреххлористого углерода) и алюминия активированного с помощью АОС [патент Англии 790896, 19.02.1958].
Сущность данного способа заключается в том, что в соответствующий реактор с мешалкой помещают 27 частей алюминия. Затем добавляют 150 частей диэтилалюминийхлорида, начинают перемешивание и нагревают до 150oС в течение 1 ч. После этого в реакционный сосуд помещают 1000 частей гептана. Реактор нагревают до кипения, приблизительно до 95oС. В кипящую реакционную смесь в течение 2 ч добавляют 460 частей четыреххлористого углерода. После прохождения реакции реактор охлаждают, реакционную смесь гидролизуют соляной кислотой. Полученный ГХЭ отфильтровывают.
Данный метод имеет очень серьезный недостаток: использование алюминийорганики, что существенно усложняет технологическое оформление процесса.
Предлагается способ получения гексахлорэтана из четыреххлористого углерода, свободного от указанных недостатков.
Сущность метода заключается в получении гексахлорэтана из ССl4 под действием порошкообразного алюминия активированного йодом, взятых в мольном соотношении Al: CCl4=1:8. Активация происходит следующим образом. К навеске алюминия, помещенного в реактор, добавляют несколько кристалликов йода и под аргоном нагревают на спиртовке до полной возгонки йода. Реакцию проводят при небольшом нагревании до 40-50oС, при атмосферном давлении, постепенно добавляя CCl4. Время реакции около 30 мин.
Реакция протекает по схеме:
6СCl4+2Аl-->2АlСl3+3С2Сl6
Избыток CCl4 в данной реакции необходим для того, чтобы уменьшить количество побочных продуктов, которые могут образоваться в результате вовлечения в реакцию гексахлорэтана.
Выход, определенный хроматографически, методом внутреннего стандарта составляет 99%. В качестве побочного продукта наблюдается гексахлорбутадиен в количестве 0,6%.
Предлагаемый метод имеет следующие преимущества/
1. Высокий выход целевого продукта.
2. Доступность исходных реагентов.
3. Образование небольших количеств отходов. Непрореагировавший избыток CCl4 легко вернуть простой перегонкой и снова использовать в реакции. АlСl3, образовавшийся в реакции, можно использовать в качестве катализатора в других процессах.
4. Не требуется высоких температур и повышения давления.
5. Отсутствие такого токсичного и экологически опасного компонента как хлор.
6. Удешевление себестоимости и упрощение технологии за счет уменьшения энерго- и трудозатрат, экологическая безопасность процесса.
Предлагаемый способ поясняется следующим примером.
Пример.
В стеклянный реактор объемом 50 мл помещается 0,32 г (11,8 ммоль) порошкообразного Аl и несколько кристалликов йода. В атмосфере аргона ректор нагревают на спиртовке до полной возгонки йода. Реактор устанавливают на магнитной мешалке, добавляют 10 мл (97,3 ммоль) CCl4. Периодически включая мешалку, проводят перемешивание реакционной массы в течение 30 мин, при температуре 45oС. По окончании реакции реакционная смесь приобретает коричневую окраску. Реакционную смесь гидролизуют водой, затем отделяют органический слой и пропускают его через Аl2О3, затем упаривают его досуха. Двойной перекристаллизацией из этанола получают 2,9 г белого кристаллического порошка (гексахлорэтана), что составляет 81,3% от теоретического выхода.
ИК-спектр (ν, см-1): 760
Элементный анализ (в скобках приведено теоретическое содержание): С= 10,62 (10,13)%:Сl=88,9(89,87)%
Спектр ЯМР 13С (δ, м.д.): 105,15.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРЭТАНА | 2001 |
|
RU2185365C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРЭТАНА | 2020 |
|
RU2741384C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ E3,E8-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]ДЕКАНА И E3,E9-ДИМЕТИЛТРАНСБИЦИКЛО[4.4.0]-ДЕКАНА | 2002 |
|
RU2221764C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИХЛОРАДАМАНТАНА | 2011 |
|
RU2459797C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА, 1- И 4-ХЛОРДИАМАНТАНОВ | 2000 |
|
RU2185364C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОР-3-АЦЕТИЛ- И 1,3-ДИХЛОР-5-АЦЕТИЛАДАМАНТАНОВ | 2000 |
|
RU2197467C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦЕТОФЕНОНА (МЕТИЛФЕНИЛКЕТОНА) | 2002 |
|
RU2237055C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРАДАМАНТАНА | 2011 |
|
RU2486169C2 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ ИЗОМЕРИЗАЦИИ ЭНДОТЕТРАГИДРОЦИКЛОПЕНТАДИЕНА В ЭКЗОТЕТРАГИДРОЦИКЛОПЕНТАДИЕН | 2002 |
|
RU2228325C2 |
| Способ получения гексахлорэтана | 1991 |
|
SU1781198A1 |
Изобретение относится к получению гексахлорэтана, который используют в производстве хладона 113, таблеток для дегазации, при отливе алюминиевых деталей, при получении дезодорантов, бактерицидных препаратов и дымовых смесей. Способ осуществляют путем добавления ССl4 к порошкообразному алюминию в атмосфере аргона. Алюминий предварительно активируют йодом. Мольное соотношение алюминий: ССl4=1:8. Процесс ведут при атмосферном давлении, при температуре 45oС в течение 30 мин. Технический результат - увеличение выхода целевого продукта, снижение количества отходов.
Способ получения гексахлорэтана из четыреххлористого углерода, отличающийся тем, что к порошкообразному алюминию, предварительно активированному йодом, добавляют ССl4 в мольном соотношении 1:8 в атмосфере аргона, при атмосферном давлении, при температуре 45°С в течение 30 мин.
| GB 790896 А, 19.02.1958 | |||
| КОРШАК В.В., СТЕПИХЕЕВ Ю.А., ВЕРТОЛАТОВА Л.Ф | |||
| ЖОХ, 1947, 17, с | |||
| Машина для производства всех процессов тестообразования с применением подогревания при замешивании теста и с расположением аппаратов для выполнения этих процессов, с целью объединения таковых, друг над другом | 1923 |
|
SU1626A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРЭТАНА | 2001 |
|
RU2185365C1 |
Авторы
Даты
2003-11-27—Публикация
2002-06-13—Подача