Ь С



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ утилизации гексахлорбензола | 1987 |
|
SU1467046A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВИНИЛИДЕНХЛОРИДА | 1994 |
|
RU2078071C1 |
| Способ получения 3-хлорфталевого ангидрида и катализатор для его осуществления | 1991 |
|
SU1806139A3 |
| Катализатор для окислительного хлорирования метана | 1987 |
|
SU1502075A1 |
| Катализатор для окисления хлористого водорода в хлор и способ получения хлора | 1985 |
|
SU1326330A1 |
| Способ получения арилированных фталоцианинов | 1988 |
|
SU1623998A1 |
| Способ получения малеинового ангидрида | 1976 |
|
SU1071221A3 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА ОКИСЛЕНИЕМ ХЛОРИСТОГО ВОДОРОДА | 2008 |
|
RU2373139C1 |
| Способ получения нефтяных сульфоксидов | 2017 |
|
RU2668810C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА НИТРАТА ХРОМА (III) | 2016 |
|
RU2639782C1 |
Использование: гексахлорэтан используется в синтезе полиамидов, при выплавке алюминия, при получении дезодорантов, бактерицидных препаратов. Продукт: гекса- хлорэтзн БФ . Реагент 1: тетрахлорэ- тилен; реагент 2: кислород. Условия реакции: в газовой фазе, 260-270°С, катализатор СоСи4Сгб020 5 мас.% (на остальное до 100 мас.%), реакционная смесь имеет состав, мзс.%: тетрахлорэчи- лен 0,1-0,4; кислород 1-8; азот остальное, объемная скорость . Выход до 99,5%. 6 табл.
Изобретение относится к органическому синтезу, в частности, к способам получения гексахлорэтана (ГХЭ) из тетрах- лорэтилена (ТХЭ). Гексахлорэтан используется в процессе синтеза полиамидов, при выплавке алюминия, при получении дезодорантов, бактерицидных препаратов.
Известен способ получения ГХЭ, сущность способа которого заключается в том, что в стеклянную колбу, содержащую ТХЭ, вводят хлор и этилен. Полученную смесь перемешивают в течение двух часов при 81°С. Получают 1595 г жидкости, содержащей 5,5% 1,2-дихлорэтана, 49,6ТХЭ и 44,8% ГХЭ.
К недостаткам известного способа следует отнести использование высоко- токсичного и обладающего сильными коррозионными свойствами хлора. Известный
способ не позволяет вести непрерывный процесс. Кроме этого, в известном способе небольшой выход ГХЭ.
Известен способ получения ГХЭ с применением катализатора, сущность способа которого заключается в том, что загружают ТХЭ, содержащий соединение формулы R1R1C(CN)NC(CN)R2R3 (где R1-R3 алкил или циклогексил) в концентрации 0,001-1 %, и подают хлор при температуре 75-100°С. Реакционную смесь перемешивают до полного поглощения хлора, охлаждают и отделяют кристаллы ГХЭ. Конверсия хлора 99,9%.
К недостаткам известного способа следует отнести применение высокотоксичного и коррозионноспособного хлора, а также необходимость использования сложного органического соединения в качестве катализатора, который необходимо отделять от
VI
О 00
целевого продукта при очистке последнего. Известный способ не позволяет вести непрерывный процесс.
Наиболее близким по технической сущности к данному способу является способ получения ГХЭ .из ТХЭ.
Сущность известного способа заключается в том, что в колонку, с укрепляющей частью и отгонной частью, заполненную насадкой из керамических колец, подают сверху ТХЭ, содержащего 0,01% азобисизо- бутиронитрила. В среднюю часть колонны подают хлор. Пары из верхней части колонны конденсируются в обратном холодильнике и возвращаются в колонну вместе со свежим ТХЭ. Систему поддерживают под избыточным давлением 0,53-2 зтм. После трехчасовой работы из куба колонны выгружают охлажденный твердый ГХЭ. Выход 97-98%.
К недостаткам известного способа следует отнести применение под избыточным давлением высокотоксичного хлора, обладающего также и высококоррозионными свойствами. Кроме этого, в процессе требуется применение сложного органического катализатора азобисизобу- тиронитрила, который расходуется в процессе и который необходимо отделять от целевого продукта. В известном способе требуется очистка получаемого ГХЭ. На проведение процесса требуется длительный промежуток времени. Известный способ не позволяет вести непрерывный процесс.
Целью изобретения является упрощение технологического процесса.
Поставленная цель достигается тем, что гексахлорэтан получают газофазным окислением ТХЭ молекулярным кислородом, причем реакция протекает по суммарному уравнению:
ЗСаСЦ + 202 2СОа + 2C2de
При этом максимальный выход продукта обеспечивается при применении гетерогенного катализатора окисления, состоящего из 5% активной массы эмпирической формулы CoCiMCr5020 на носителе y-MzOz (95яас.%) при температуре 260-270°С, объемной скорости 180 ч и составе реакционной смеси, об.%:
ТХЭ0,1-0,4
Кислород1-8
Пример Процесс окисления ведут на установке проточного типа в реакционной трубке из нержавеющей стали с внутренним диаметром 15 мм и длиной 200 м. В реактор загружают 20 см3 катализатора состава 5 мас.% активной массы CoCrO/i на носителе (95 мае. %).
Катализатор состава 5 мас.% СоСгСм на носителе у-А120з готовят следующим образом.
4,26 г азотнокислого кобальта Co(NOs}2 x х 6Н20 и 1,50 г хромового ангидрида СгОз растворяют в 80 мл воды и в полученный раствор добавляют 51,9 г (100 мл)
. Содержимое упаривают при перемешивании досуха, затем прогревают на воздухе 4 ч при 600°С. Получают катализатор состава 5 мас.% СоСгСм/УА Оз.
Реактор с катализатором нагревают до температуры 260°С и пропускают через него реакционную смесь, содержащую 0,33 об.% ТХЭ, 2 об.% кислорода, остальное - азот. Объемная скорость реакционной смеси составляет 180 (время контакта реакционной смеси с катализатором - 20 с).
Продукты, выходящие из реактора, анализируют методом ГЖХ. На выходе реактора собирают белое твердое вещество с температурой возгонки 187-190°С, Хрома- тографический анализ показал, что этот продукт соответствует гексахлорэтану с содержанием основного вещества 99,9%.
Результаты о составе продуктов реакции, степени превращения ТХЭ, избирательности по ГХЭ и выходе ГХЭ приведены в табл. 1.
П р и м е р 2. Процесс окисления ТХЭ
ведут также, как в примере 1, с тем отличием, что берут катализатор 5 мас,% СоСиСг20а на носителе (95 мас.%). Катализатор готовят следующим образом.
- 2,083 г кобальта азотнокислого Со(Шз)2х х 6Н20 и 0,737 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 1).
1,727 г меди азотнокислой Си(МОз)2Х
х ЗНаО и 0,711 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 2). Растворы 1 и 2 объединяют и добавляют к ним 50,8 г у-А120з. Содержимое упаривают при перемешивании досуха, затем
прогревают на воздухе 4 ч при 600°С. Получают катализатор состава 5 мас.% СоСиСг208/у-А 20з. Результаты представлены в табл. 1.
П я м е р 3. Процесс окисления ТХЭ
ведут -же, как в примере 1, с тем отличием, 4iu берут катализатор 5 мас.% СоСи4Спз020 на носителе у-А.Оз (95 мае. %). Катализатор готовят следующим сбра- зом.
0,833 г кобальта азотнокислого Со(МОз)2х х 6НаО и 0,295 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 1).
2,763 г меди азотнокислой Си(ГМОз)2х х ЗНаО и 1,138 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 2). Растворы 1 и 2 объединяют и добавляют к ним 50,8 г у-А120з. Содержимое упаривают при перемешивании досуха, затем прогревают на воздухе 4 часа при 600°С. Получают катализатор состава 5 мас.% CoCu4Crs020/y-At203. Результаты представлены в табл.1.
П р и м е р 4, Процесс окисления ТХЭ ведут также, как в примере 1, с тем отличием, что берут катализатор 5 мас.% Co4CuCrs020 на носителе y-AlaOs (95 мас.%). Катализатор готовят следующим образом..
3,324 г кобальта азотнокислого Со(МОз)2х х6Н20 и 1,178 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 1),
0,691 г меди азотнокислой Cu(NO3)2x хЗН20 и 0,285 г хромового ангидрида СгОз растворяют в 50 мл воды (раствор 2). Растворы 1 и 2 объединяют и добавляют к ним 50,8 г у-А120з.. Содержимое упаривают при перемешивании досуха, затем про- гревают на воздухе 4 часа при 600°С. Получают катализатор состава 5 мас.% Co4CuCrs020/y-Al203, Результаты представлены в табл,1,
П р и м е р 5. Процесс окисления ТХЭ ведут также, как в примере 1, с тем отличием, что берут катализатор 5 мас.% CuCr04 на носителе у-А120з (95 мас.%). Катализатор готовят следующим образом.
3,450 г меди азотнокислой Си(МОз)2Х х ЗН20 и 1,420 г хромового ангидрида СгОз растворяют в 80 мл воды и в полученный раствор добавляют 50,8 г . Содержимое упаривают при перемешивании досуха, затем прогревают на воздухе 4 часа при 600°С. Получают катализатор состава 5 мас.% СиСгОз/ А Оз.
Результаты представлены в табл. 1.
Изтабл. 1 видно, что наибольший выход ГХЭ, равный 98,2 мол.% наблюдается на катализаторе состава 5 мас.% CoCu4Crs020 на носителе (95 мас.%).
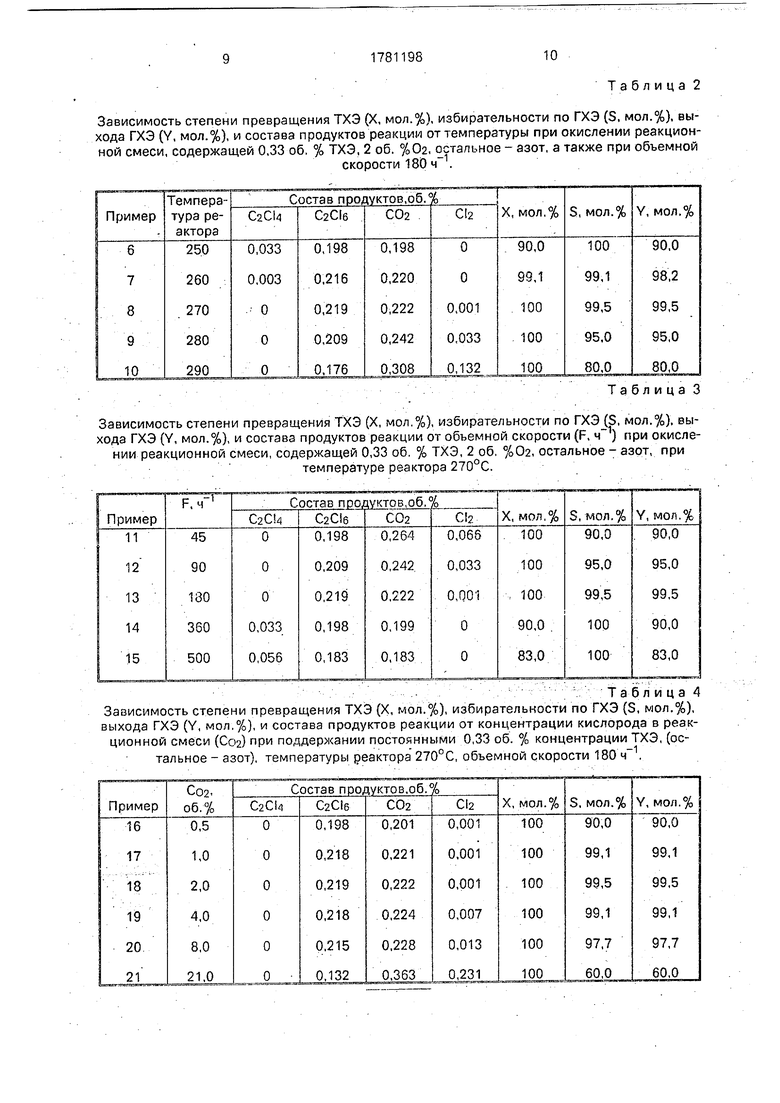
Примеры 6-10. Влияние температуры реактора на процесс окисления ТХЭ.
Процесс ведут, как описано в примере 1, с тем отличием, что берут катализатор 5% СоСи4Сг5020/у-А 20з (95 мас,%) и изменяют температуру реактора от 250 до 290°С. Результаты приведены в табл. 2.
Из табл. 2 видно, что наибольший выход ГХЭ 99,5% наблюдается при температуре 270°С. При температурах реакции больше 270°С в продуктах имеется хлор, причем о дальнейшим повышением температуры реакции его концентрация увеличивается.
Пример 11-15. Влияние объемной скорости реакционной смеси на процесс окисления ТХЭ.
Процесс ведут, как описано в примере 1, с тем отличием, что берут катализатор 5%СоСи4Сг5020/}М120з (95 мас.%) и изменяют объемную скорость реакционной смеси от 45 до 500 , поддерживая постоянными температур-у реактора 270°С и содержание ТХЭ и кислорода, соответственно, 0,33 и 2 об.%.
Результаты приведены в табл. 3.
Из таблицы 3 видно, что наибольший выход ГХЭ 99,5% наблюдается при объемной скорости 180 ,
Уменьшение объемной скорости способствует росту содержания хлора в продуктах реакции, а увеличение объемной скорости приводит к падению степени превращения ТХЭ.
Примеры 16-21. Влияние концентрации кислорода в реакционной смеси на процесс окисления ТХЭ.
Процесс ведут, как описано в примере 1, с тем отличием, что берут катализатор 5%СоСи4Сгб020/у-А120з (95 мас.%) и изменяют концентрацию кислорода от 0,5 об.% до 21 об.% и поддерживают постоянными температуру реактора 270°С, объемную скорость 180 и концентрацию ТХЭ 0,33 об.% (остальное - азот).
Результаты приведены в табл. 4.
Из табл. 4 видно, что наибольший выход ГХЭ 99,5% наблюдается при концентрации кислорода в смеси 2%. Увеличение содерания кислорода по сравнению с указанной величиной приводит к росту в продуктах рекции хлора, а при снижении содержания кислорода ниже 2 об.% начинают наблюать образование смолоподобных продуков.
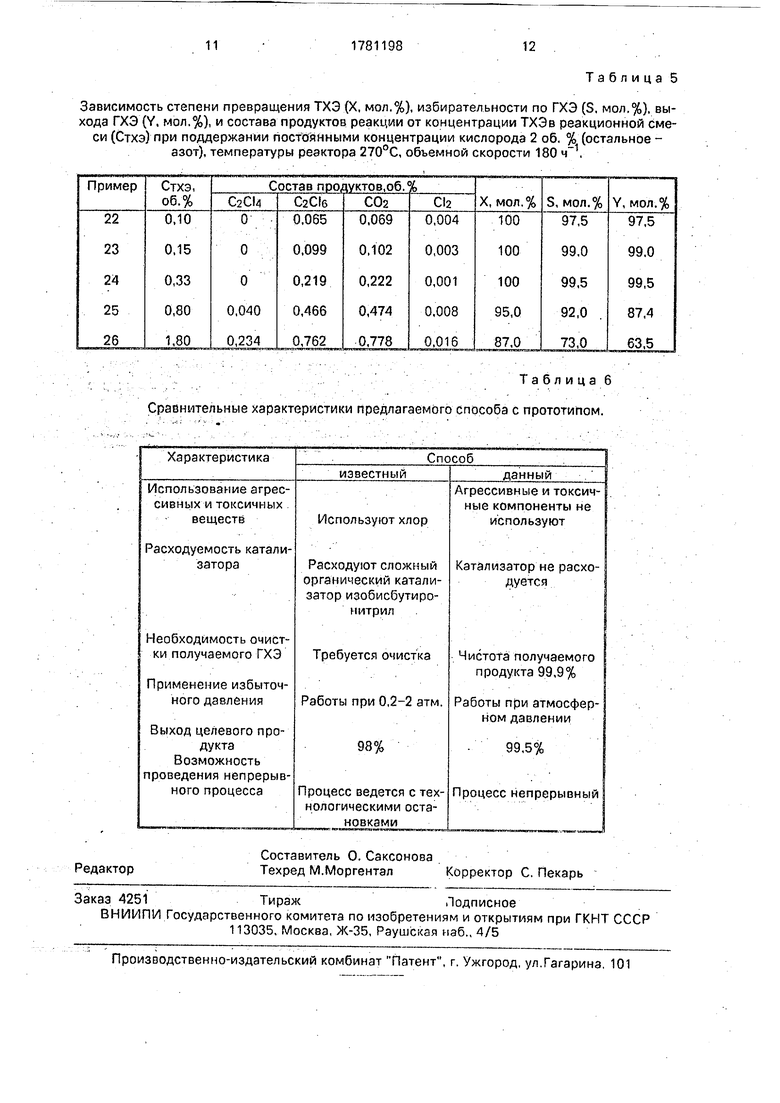
Примеры 22-26. Влияние концентрации ТХЭ в реакционной смеси на процесс го окисления,
Процесс ведут, как описано в примере 1, с тем отличием, что берут катализатор 5% oCu4Crs020/y-Al203(95 мас.%) и изменяют концентрациюТХЭ от 0,10 об.% до 1,8об.% поддерживают постоянными температуру еактора 270°С, объемную скорость 180 ч концентрацию кислорода 2 об.% (остальое - азот).
Результаты приведены в табл. 5.
Из табл. 5 видно, что наибольший выход ГХЭ 99,5% наблюдается при концентрации ТХЭ в реакционной смеси 0,33 об.%. Уменьшение концентрации ТХЭ ниже указанной величины способствует образованию хлора, а увеличение ее ведет к уменьшению степени превращения ТХЭ. а также к образованию неидентифицированных смолоподобных продуктов.
Данные по сравнению приведены в табл, 6.
Как видно из представленной табл. 6, данный способ выгодно отличается от известного способа. Так, данный способ представляет собой более простой непрерывный технологический процесс, в котором не применяется высокотоксичный и коррозионноспособный газ - хлор, не используются аппараты, работающие под давлением.
В данном способе не требуется отделение целевого продукта, чистота которого составляет 99,9%. Хроме этого, в данном
Таблица 1
Зависимость степени превращения ТХЭ (X, мол.%), избирательности по ГХЭ (S, мол.%), выхода ГХЭ
(У, ьюп %}, и состава продуктов реакции от химического состава активной массы катализатора при
окислении реакционной смеси, содержащей 0,33 об.% ТХЭ, 2 об. % кислорода, азот - остальное, при
температуре 260°С и объемной скорости 180 .
способе не расходуется сложный органический катализатор. В данном способе несколько выше выход ГХЭ по сравнению с прототипом (99,5% против 98%). Формула изобретения
Способ получения гексэхлорэтана на основе тетрахлорэтилена в присутствии катализатора при повышенной температуре, отличающийся тем, что, с целью упрощения процесса и повышения выхода целевого продукта, тетрахлорэтилен подвергают газофазному окислению, п качестве катализатора используют гетерогенный ка- тализатор состава, мае. %:
CoCu4Crs020 - 5;
у-А 20з-носитель-остальное, и процесс ведуг при 260-270°С при объемной скорости 180 ч с использованием реакционной смеси состава, мас.%:
тетрахлорэтилен - 0,1-0,4
кислород- 1-8
азот-остальное.
Таблица 2
Зависимость степени превращения ТХЭ (X, мол.%), избирательности по ГХЭ (S, мол.%), выхода ГХЭ (Y, мол.%), и состава продуктов реакции от температуры при окислении реакционной смеси, содержащей 0,33 об. % ТХЭ, 2 об. %02, остальное - азот, а также при объемной
,-1
скорости 180 ч .
Таблица 3
Зависимость степени превращения ТХЭ (X, мол.%), избирательности по ГХЭ (S, мол.%), выхода ГХЭ (Y, мол.%), и состава продуктов реакции от обьемной скорости (F, ) при окислении реакционной смеси, содержащей 0,33 об. % ТХЭ, 2 об, %02, остальное - азот, при
температуре реактора 270°С.
Таблица 4
Зависимость степени превращения ТХЭ (X, мол.%), избирательности по ГХЭ (S, мол.%), выхода ГХЭ (Y, мол,%), и состава продуктов реакции от концентрации кислорода в реакционной смеси (Соа) при поддержании постоянными 0,33 об. % концентрации ТХЭ, (остальное - азот), температуры реактора 270°С, объемной скорости 180 .
из те ст
,-1
.
Таблица 5
Зависимость степени превращения ТХЭ (X, мол.%), избирательности по ГХЭ (S, мол.%), выхода ГХЭ (Y, мол.%), и состава продуктов реакции от концентрации ТХЭв реакционной смеси (Стхэ) при поддержании постоянными концентрации кислорода 2 об. % (остальное - азот), температуры реактора 270°С, объемной скорости 180 ч .
Таблица 6 Сравнительные характеристики предлагаемого способа с прототипом.
Характеристика
известный
Используют хлор
Расходуют сложный органический катализатор изобисбутиро- нитрил
Требуется очистка
Работы при 0,2-2 атм.
98%
Процесс ведется с технологическими остановками
Способ
данный
Агрессивные и токсичные компоненты не используют
Катализатор не расходуется
Чистота получаемого продукта 99,9%
Работы при атмосферном давлении
99,5%
Процесс непрерывный
| СПОСОБ РАЗДАЧИ ТРУБ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2057604C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Устройство станционной централизации и блокировочной сигнализации | 1915 |
|
SU1971A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРЭТАНА | 0 |
|
SU222348A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1992-12-15—Публикация
1991-01-02—Подача