Текст описания в факсимильном виде (см. графическую часть).
| название | год | авторы | номер документа |
|---|---|---|---|
| АГОНИСТЫ АПОЛИПОПРОТЕИНА А-I И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДИСЛИПИДЕМИЕЙ | 1998 |
|
RU2215747C2 |
| АГОНИСТЫ АПОЛИПОПРОТЕИНА А-1 И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ДИСЛИПИДЕМИЧЕСКИХ НАРУШЕНИЙ | 1998 |
|
RU2214831C2 |
| ГЕНОТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ ВВЕДЕНИЯ АГОНИСТОВ АПОЛИПОПРОТЕИНА А-I И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ДИСЛИПИДЕМИЧЕСКИХ НАРУШЕНИЙ | 1998 |
|
RU2222545C2 |
| МИМЕТИКИ АПОЛИПОПРОТЕИНА А-I | 2010 |
|
RU2532222C2 |
| ОБРАЗОВАНИЕ ПЕПТИД/ЛИПИДНОГО КОМПЛЕКСА ПУТЕМ СОВМЕСТНОЙ ЛИОФИЛИЗАЦИИ | 1998 |
|
RU2224506C2 |
| КОНЪЮГАТЫ ИНСУЛИН-ИНКРЕТИН | 2014 |
|
RU2678134C2 |
| Новые производные оксинтомодулина и содержащая их фармацевтическая композиция для лечения ожирения | 2012 |
|
RU2612906C2 |
| Терапевтическое применение глюкагона и включающей его комбинации | 2019 |
|
RU2838895C2 |
| АНТИБАКТЕРИАЛЬНЫЕ ПЕПТИДЫ | 2007 |
|
RU2468033C2 |
| Конъюгат физиологически активного вещества длительного действия и его применение | 2018 |
|
RU2773823C2 |



















































































































































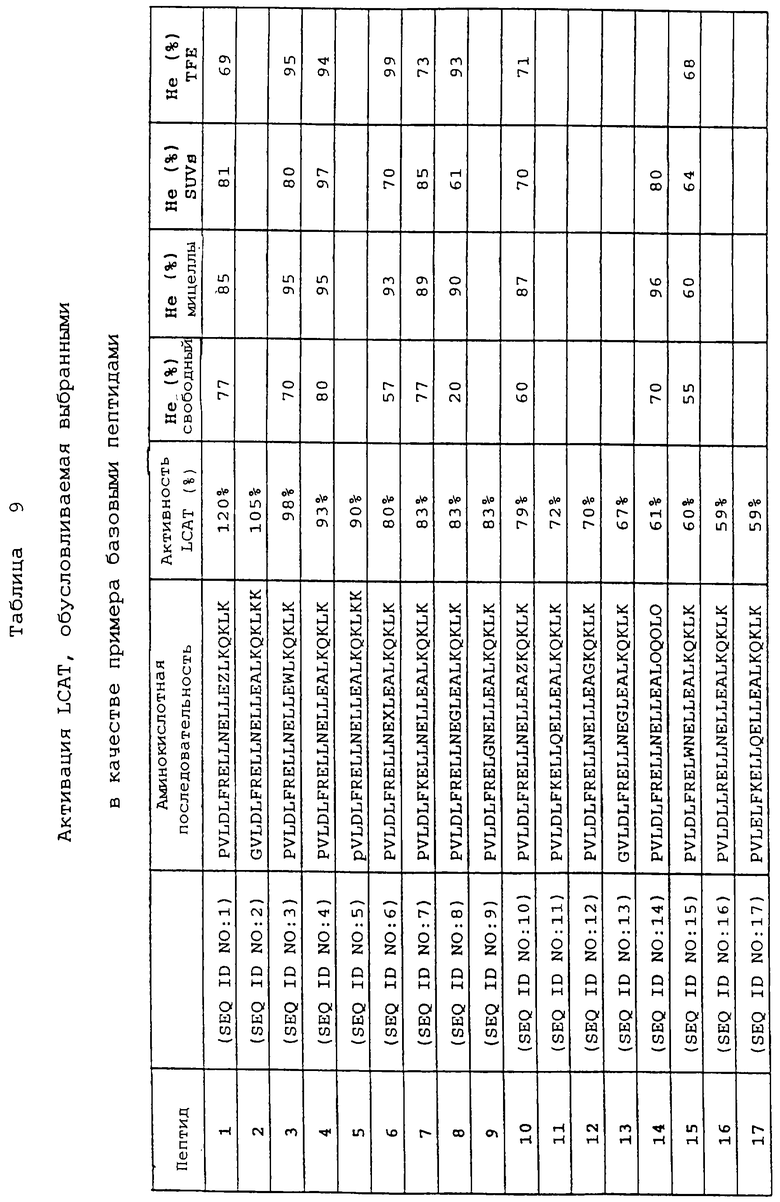
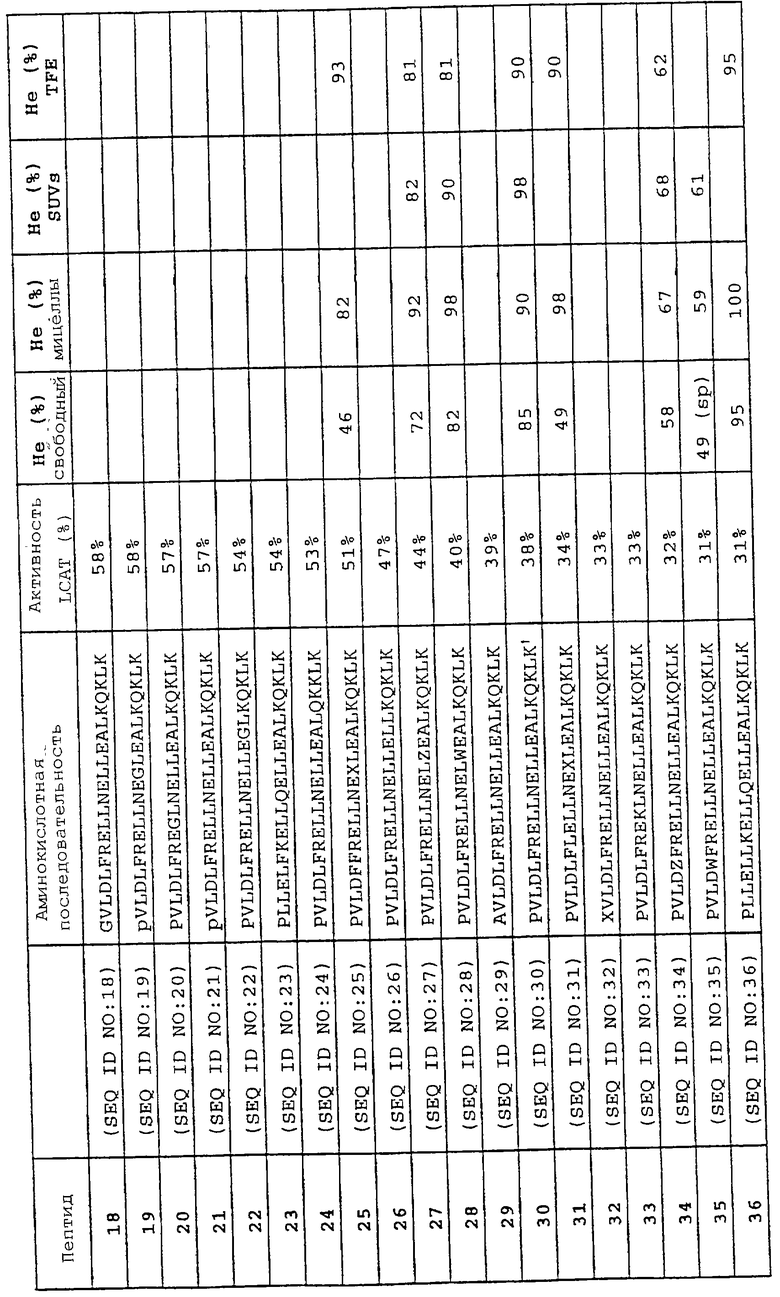
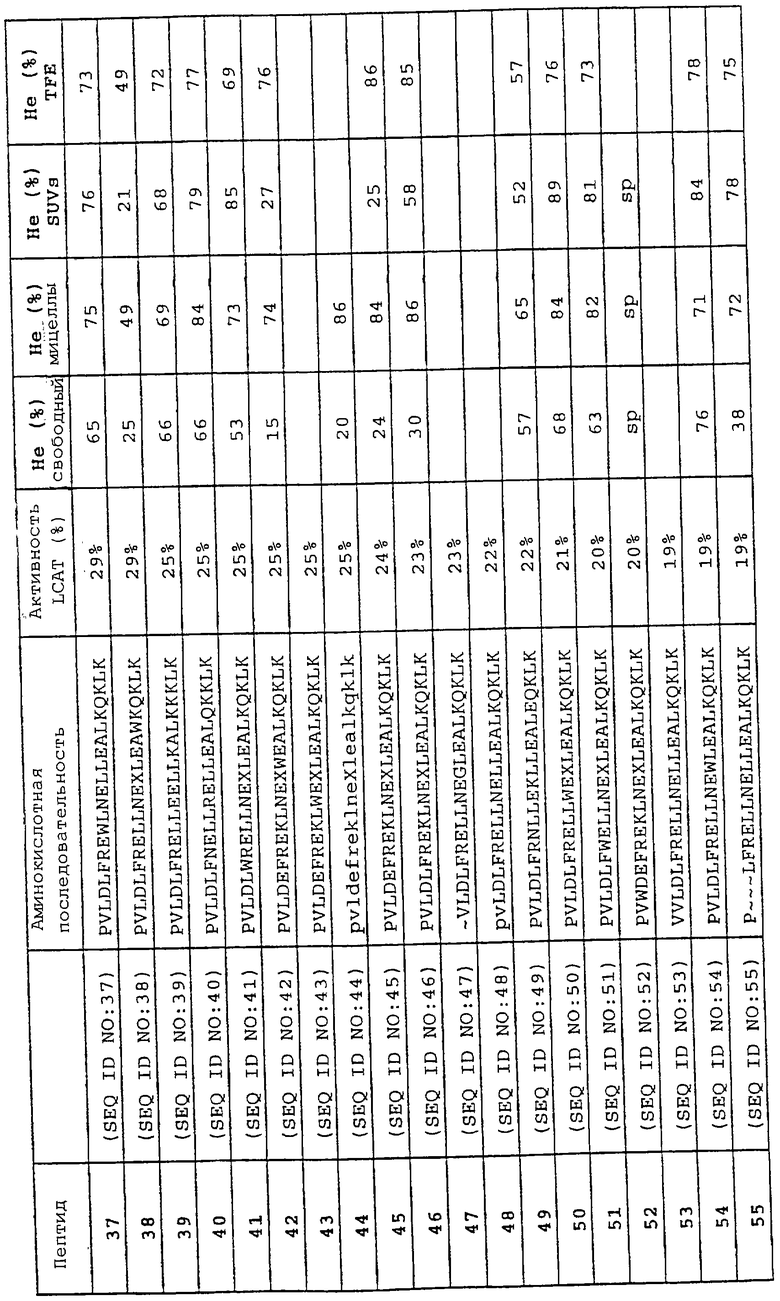
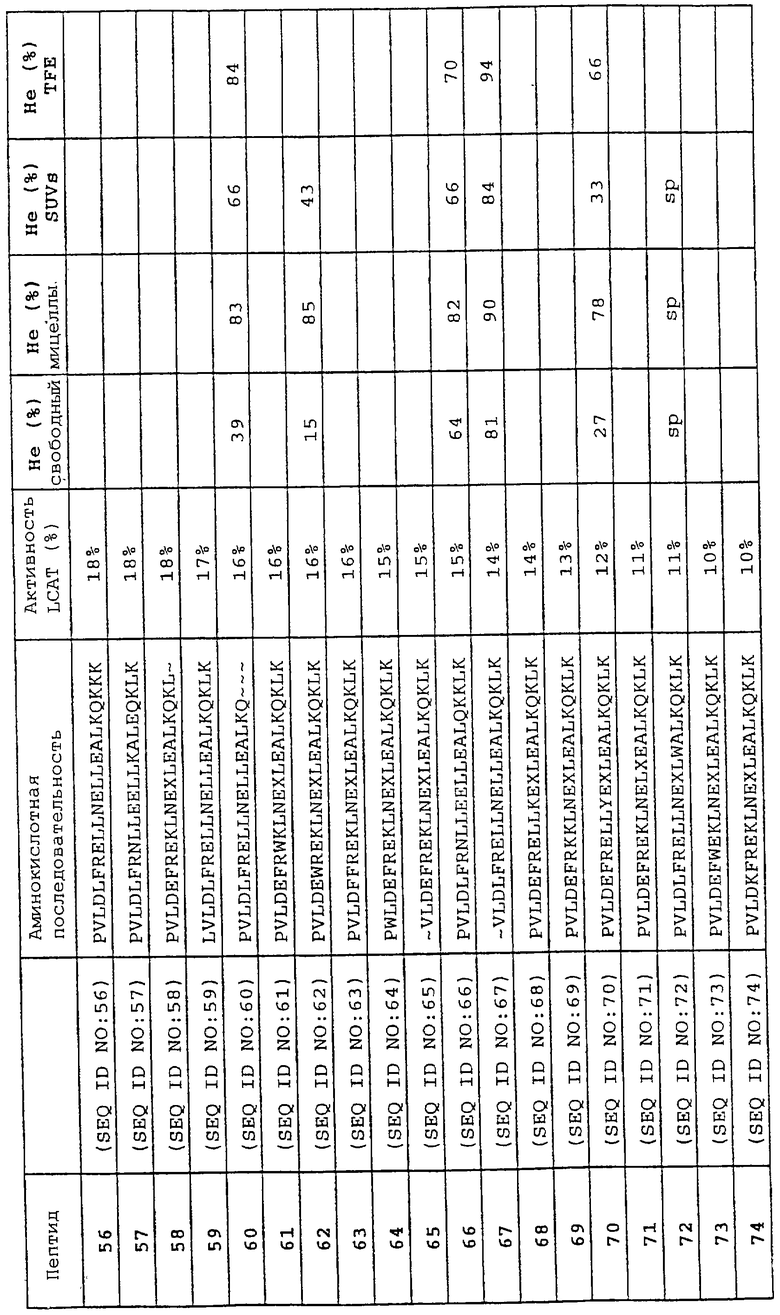
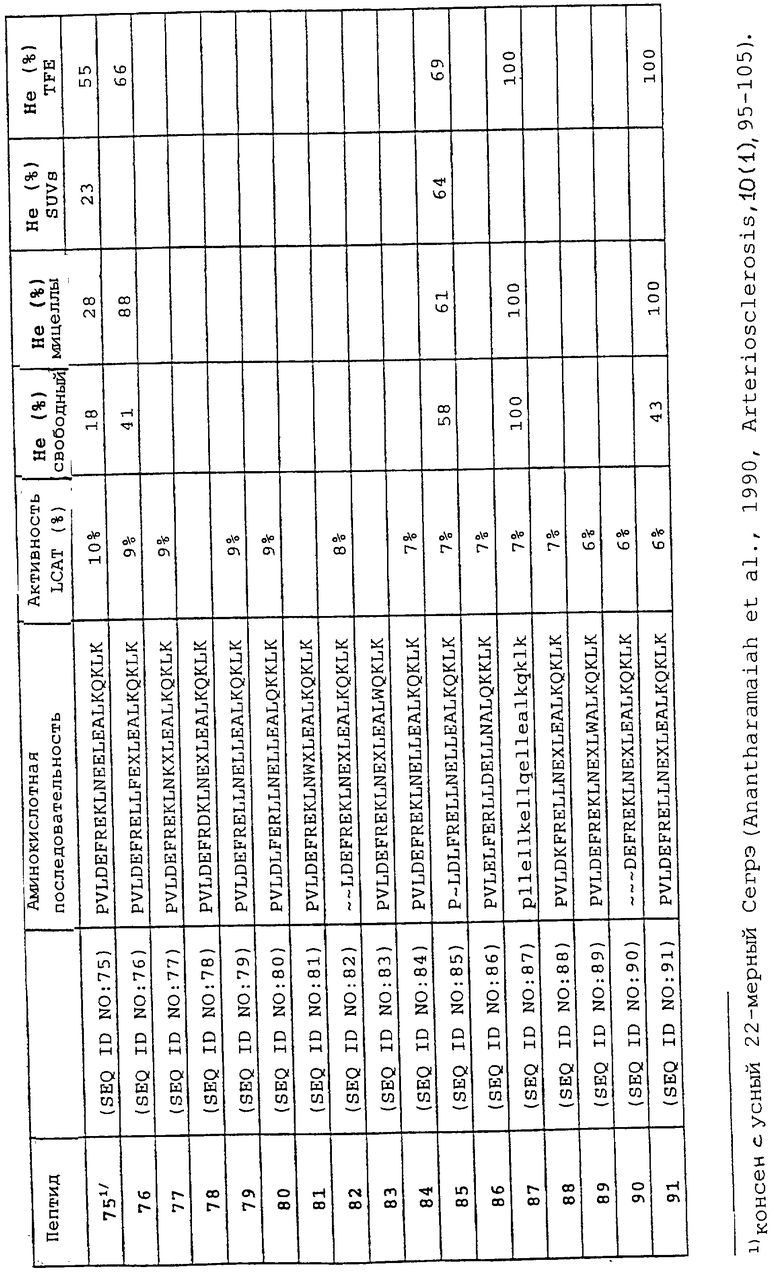
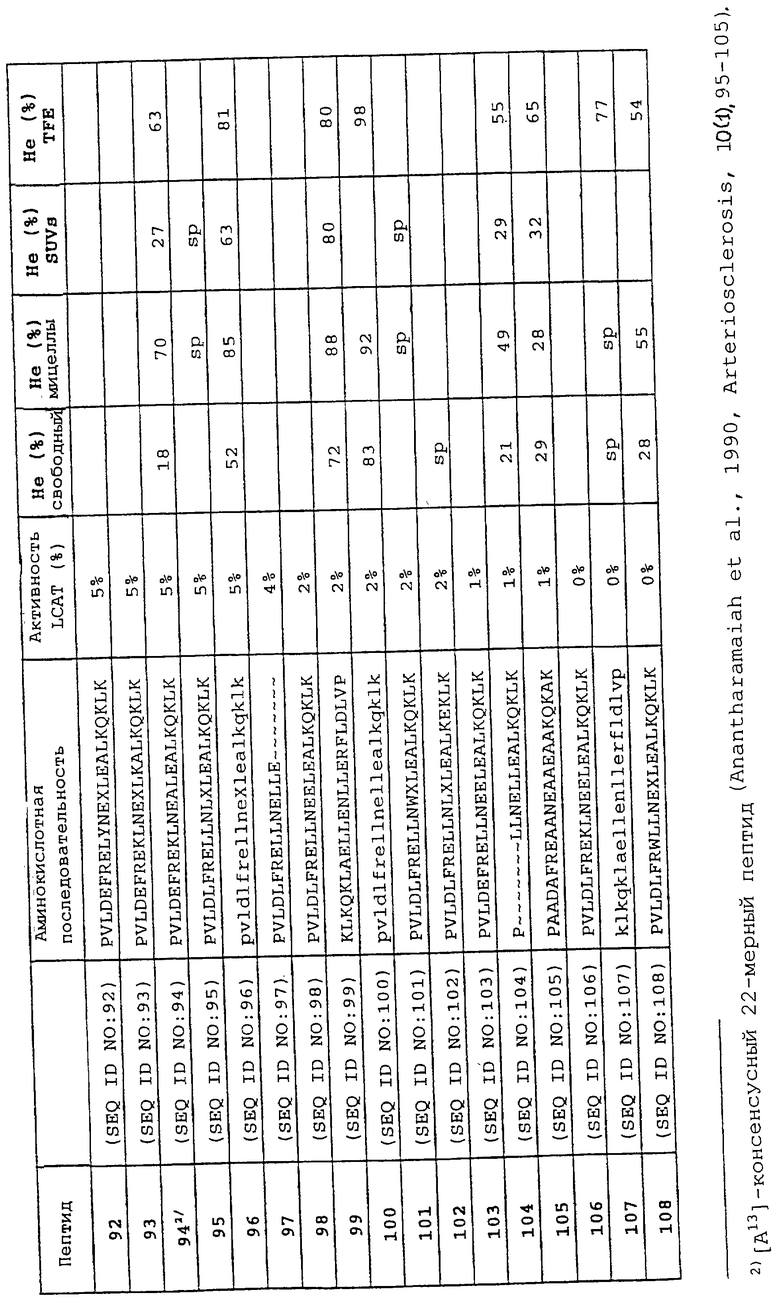
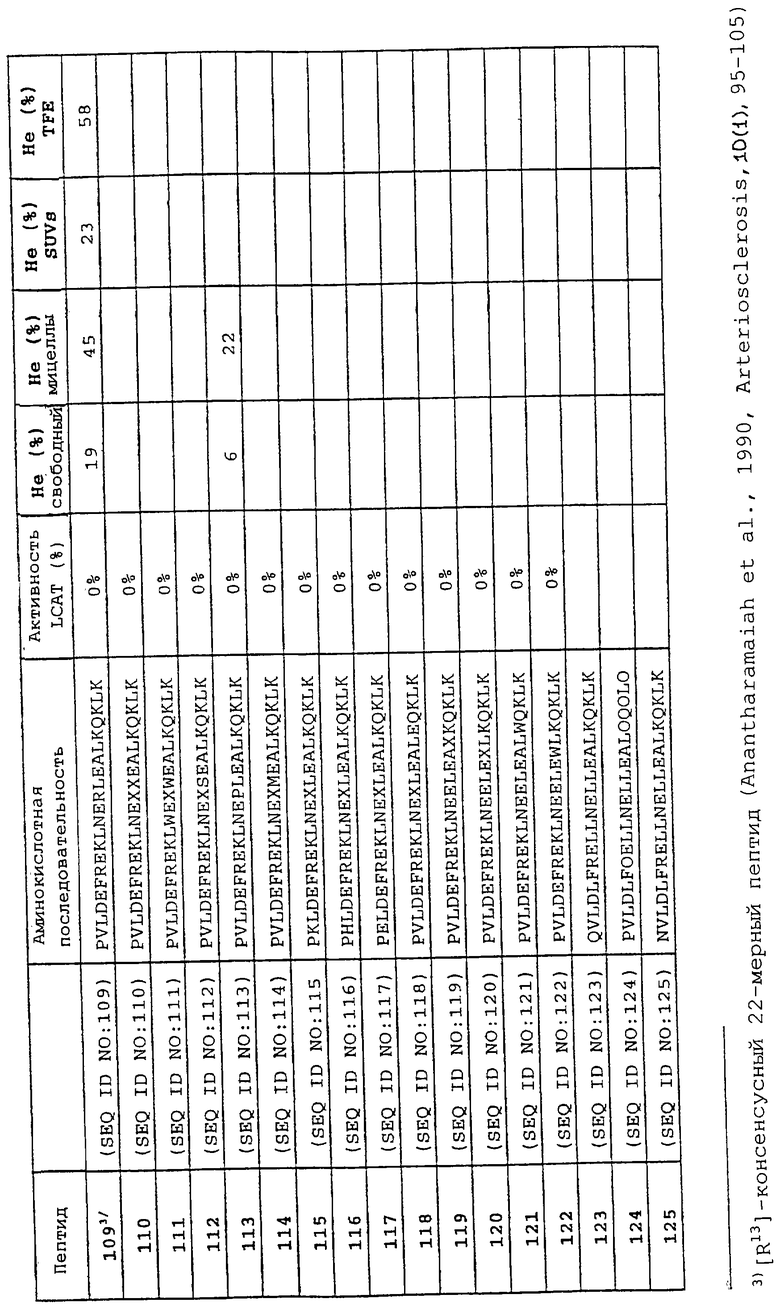
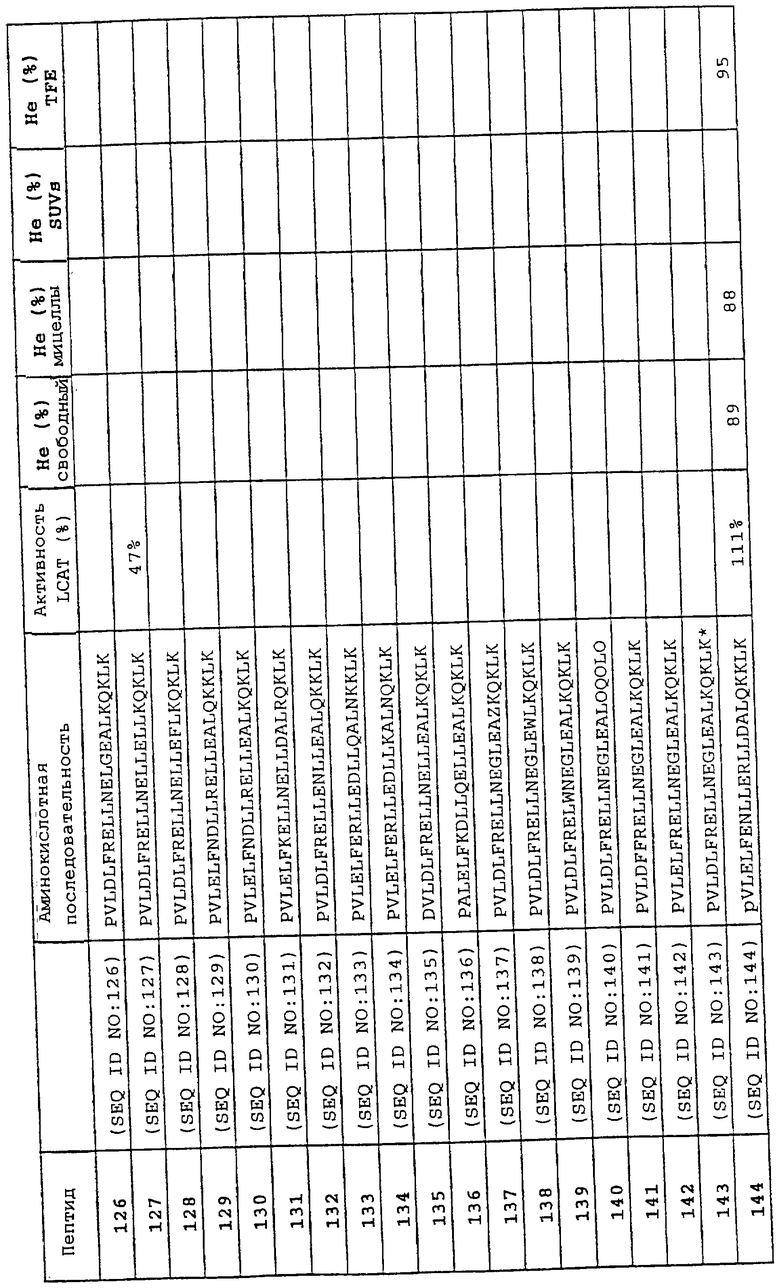
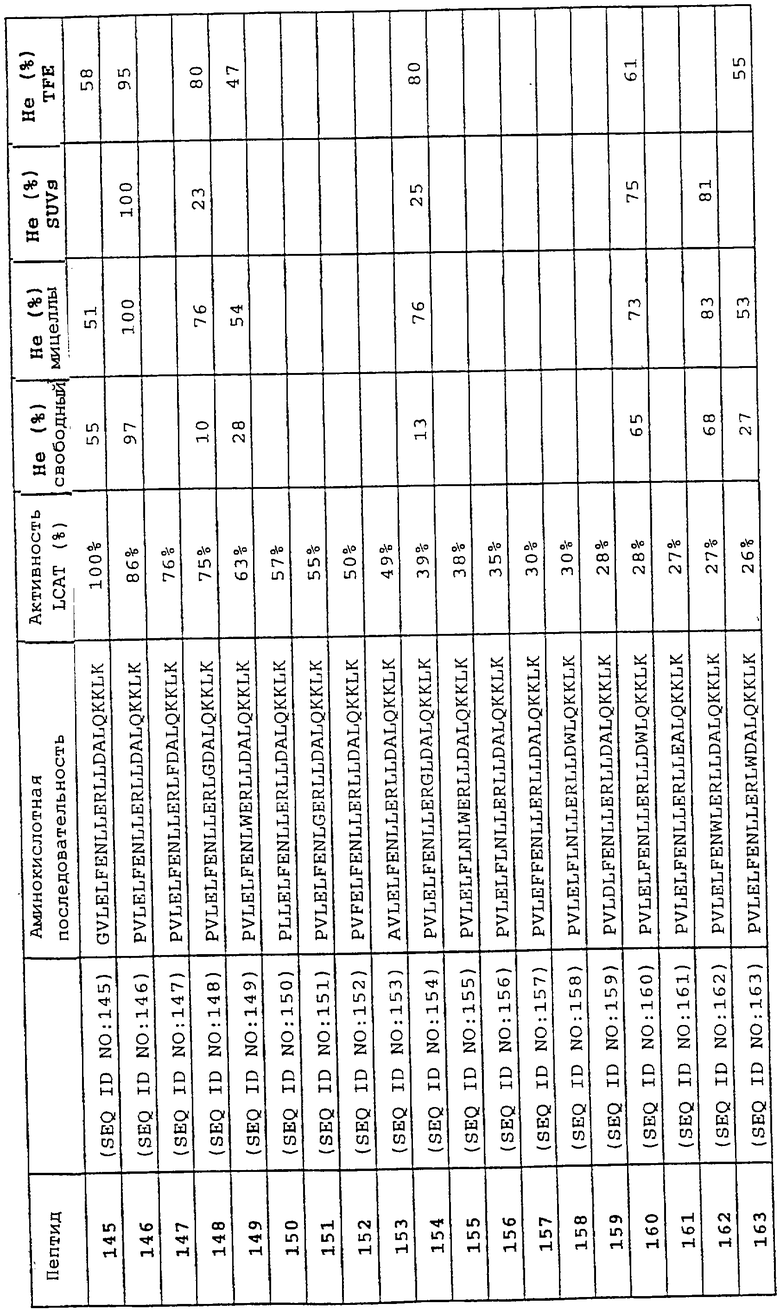
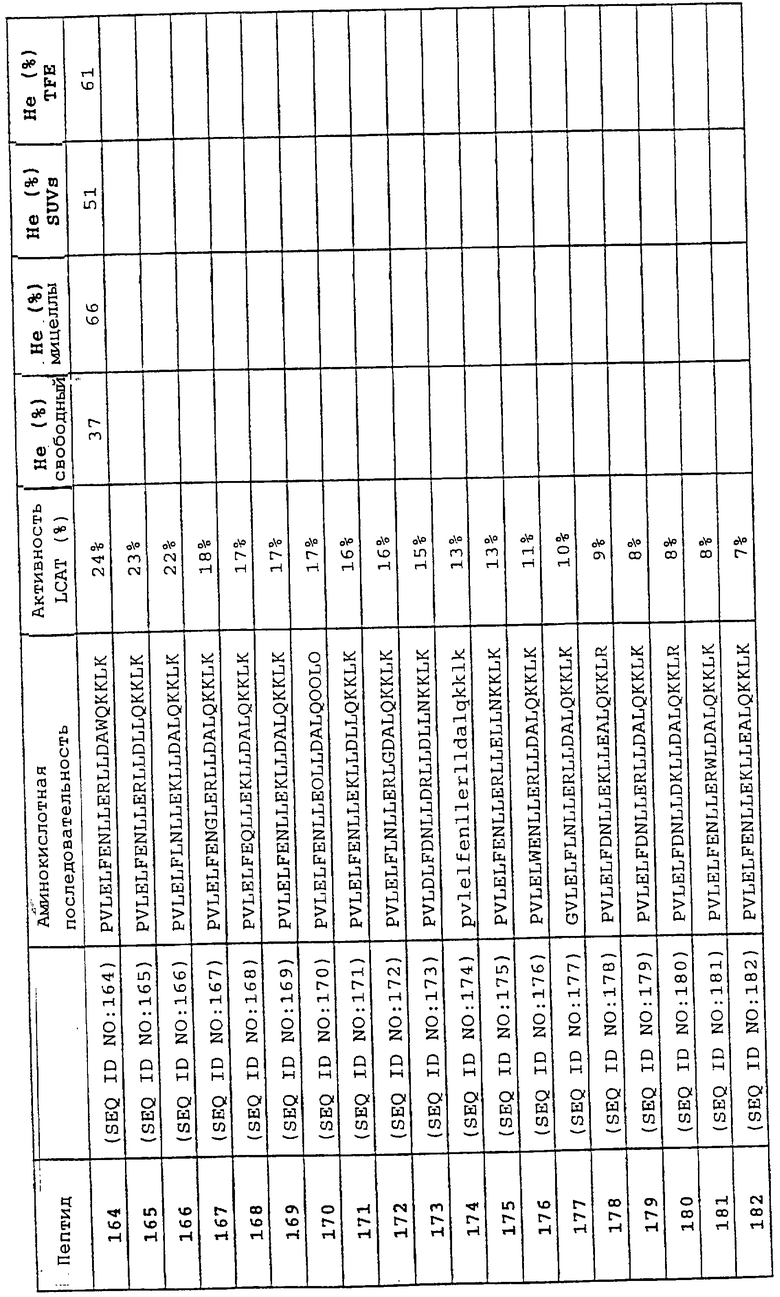
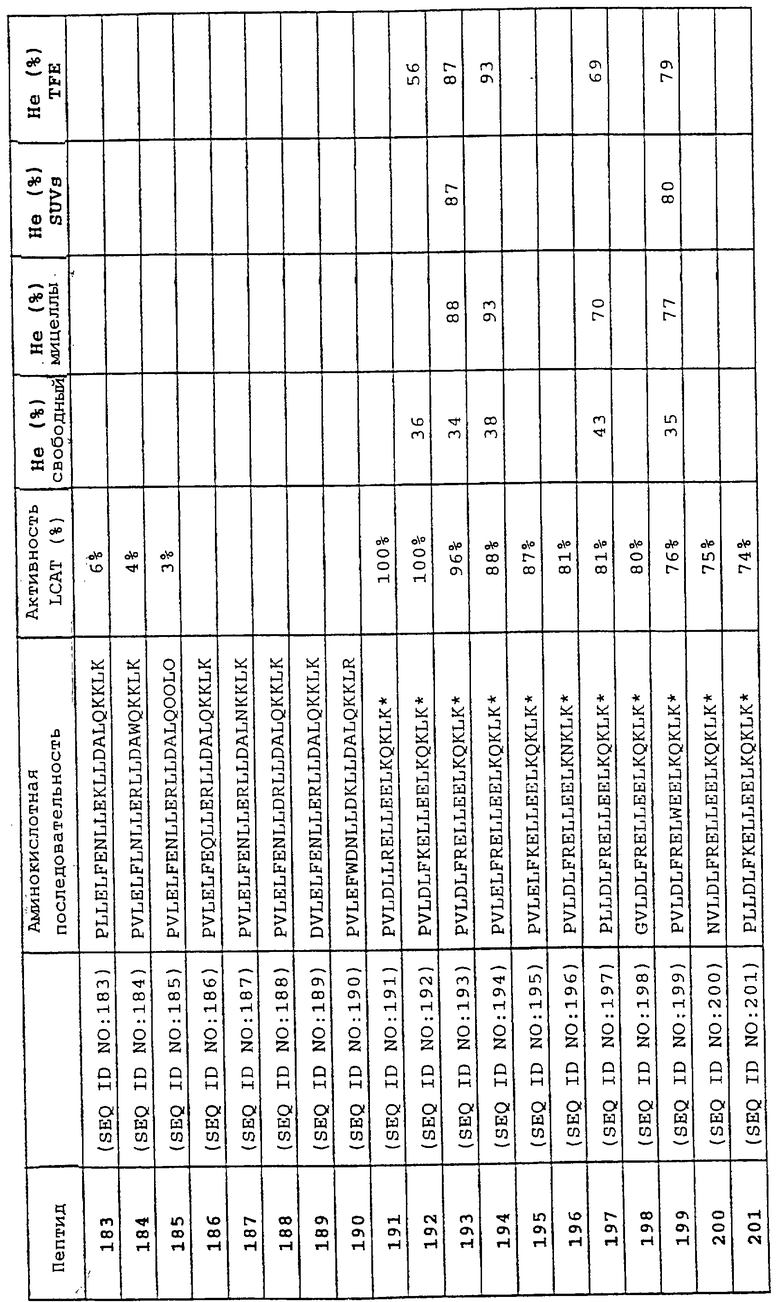
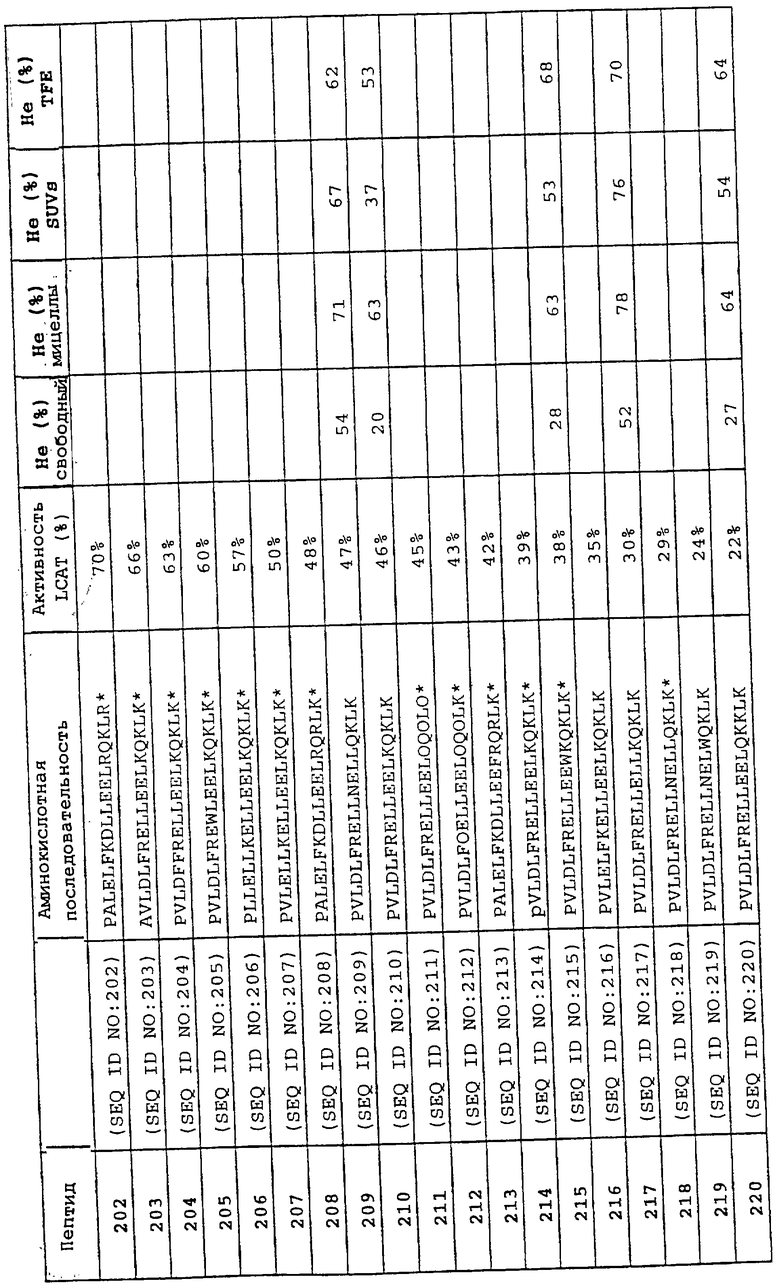















































































































































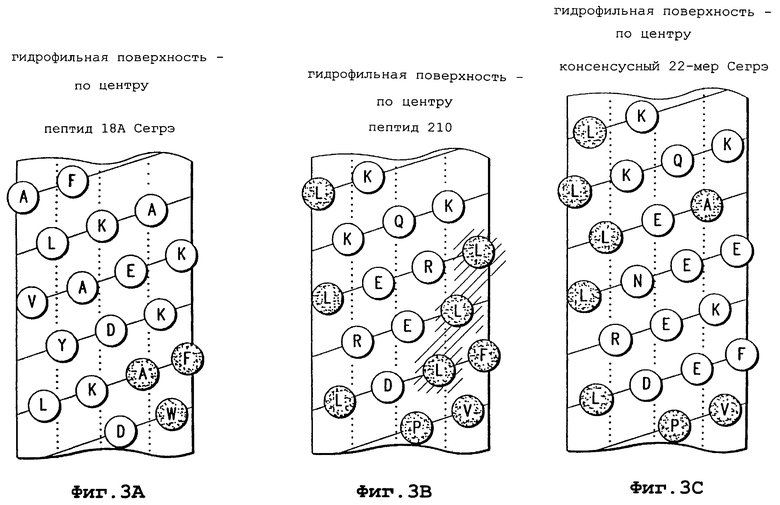
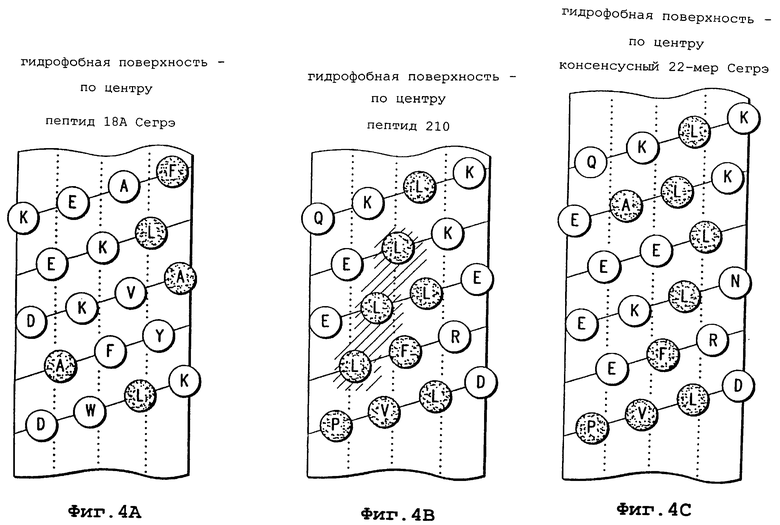
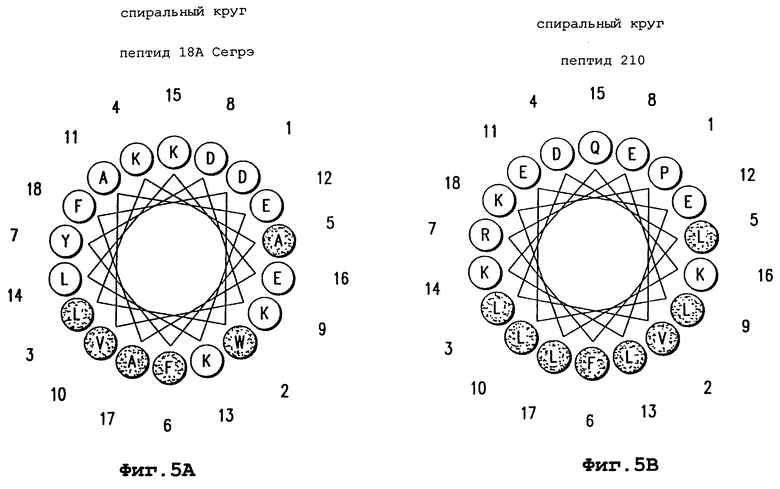
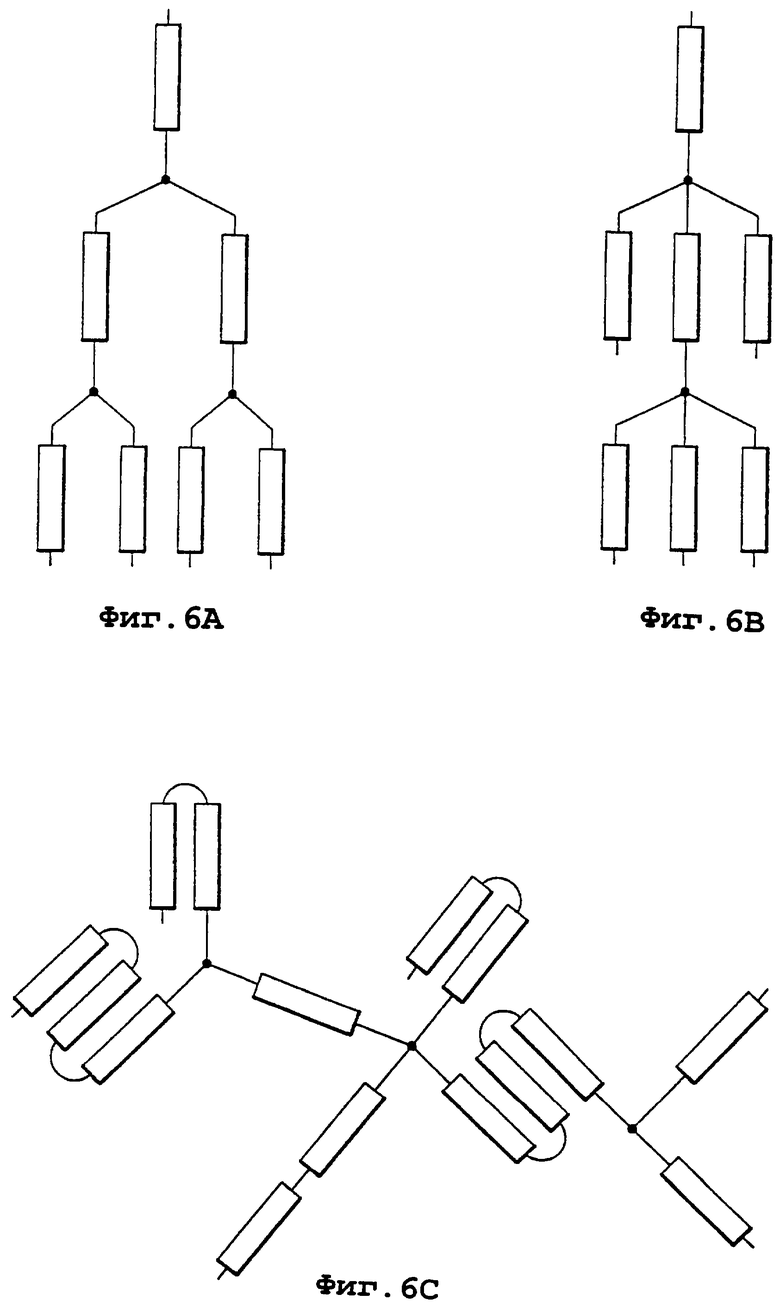
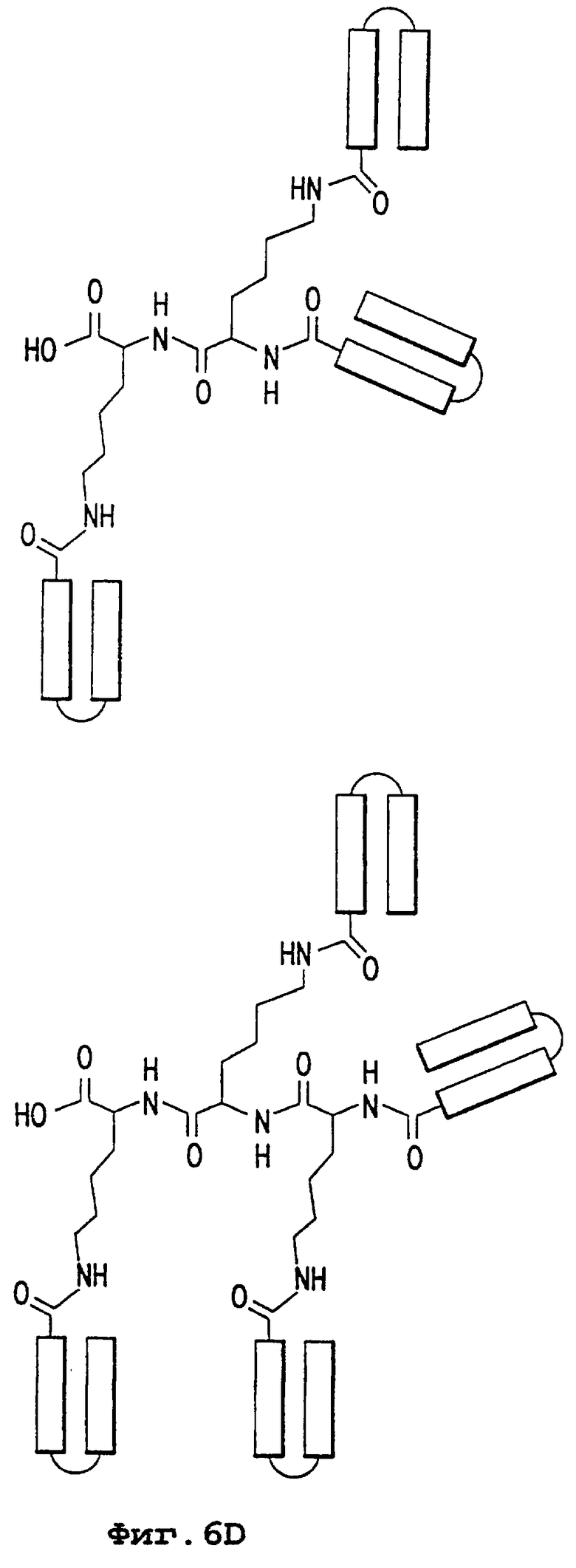
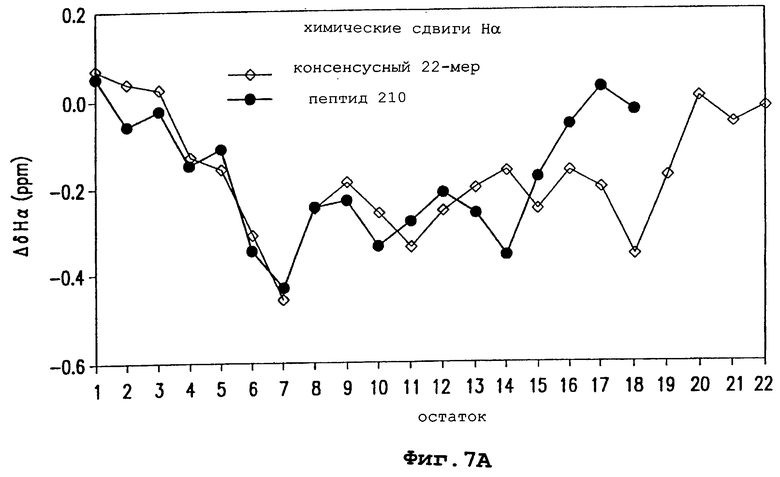
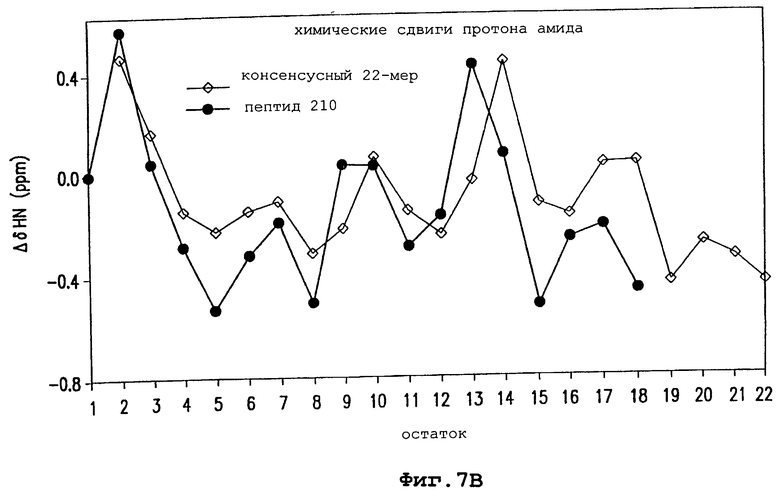
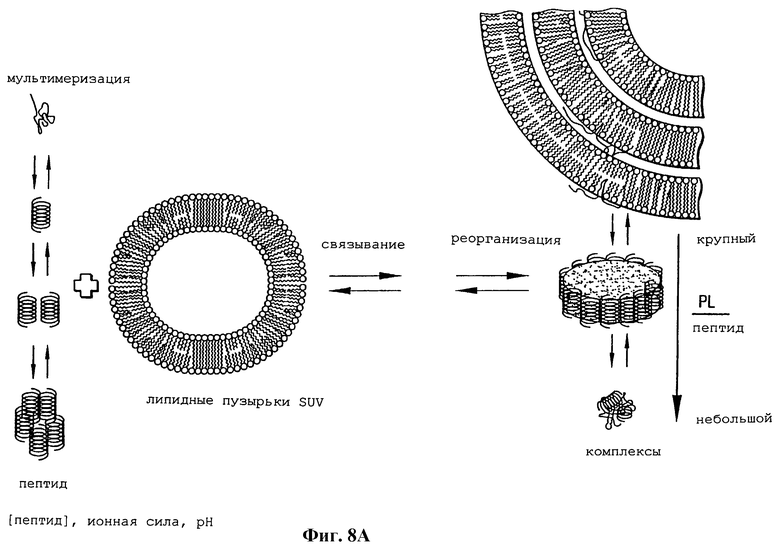
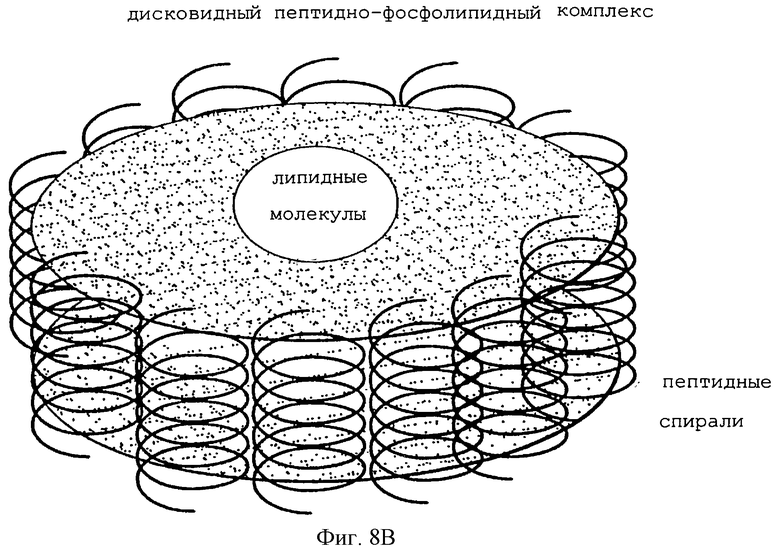
Изобретение относится к области медицинской биотехнологии. Сущность изобретения составляют пептиды и пептидные аналоги, которые имитируют структурные и фармакологические свойства аполипопротеина (АроА-1) человека. Пептиды и пептидные аналоги представляют собой аминокислотные последовательности и мультимерные комплексы с липидами, применимы для лечения различных заболеваний, связанных с дислипидемией. В изобретении описаны фармацевтические композиции и способы лечения на основе имитаторов АроА-1. Технический результат - расширение арсенала средств борьбы с дислипидемией. 8 с. и 44 з.п.ф-лы, 8 ил., 10 табл.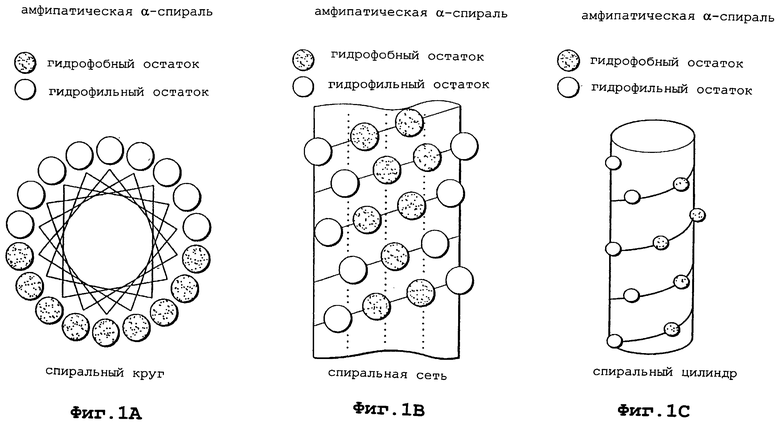
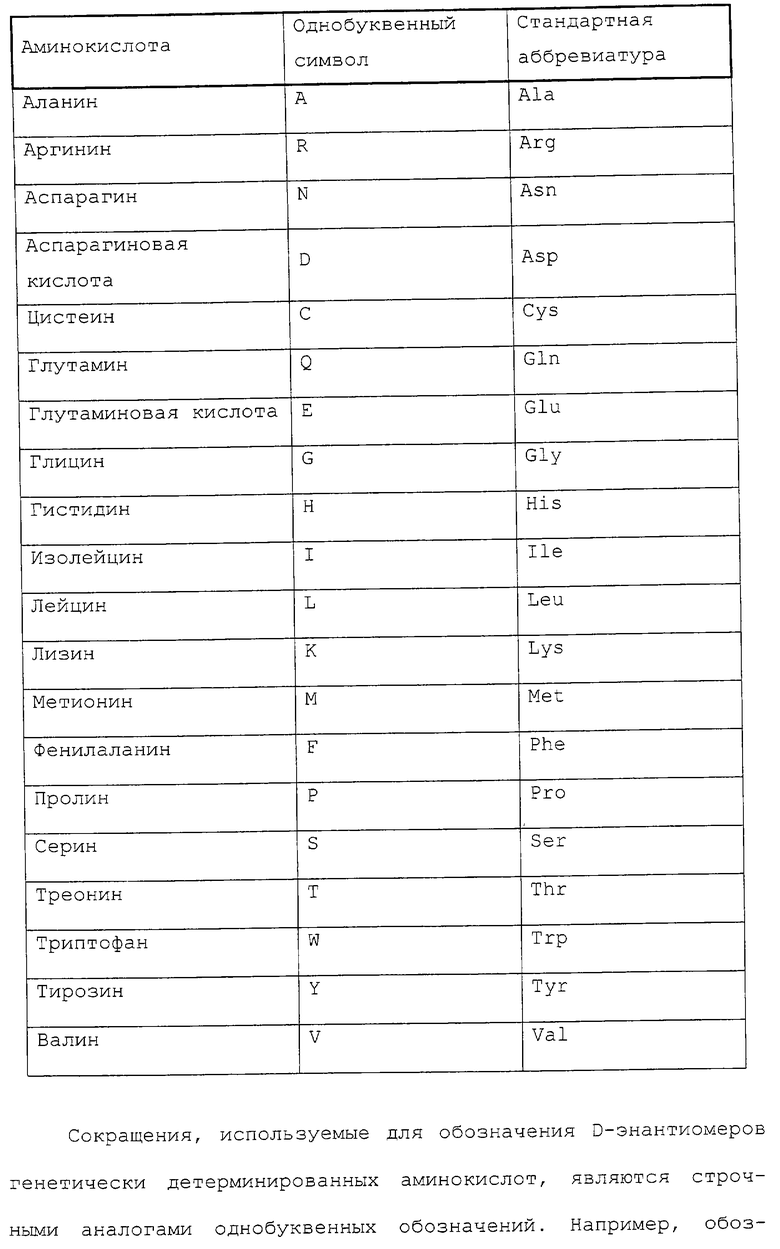
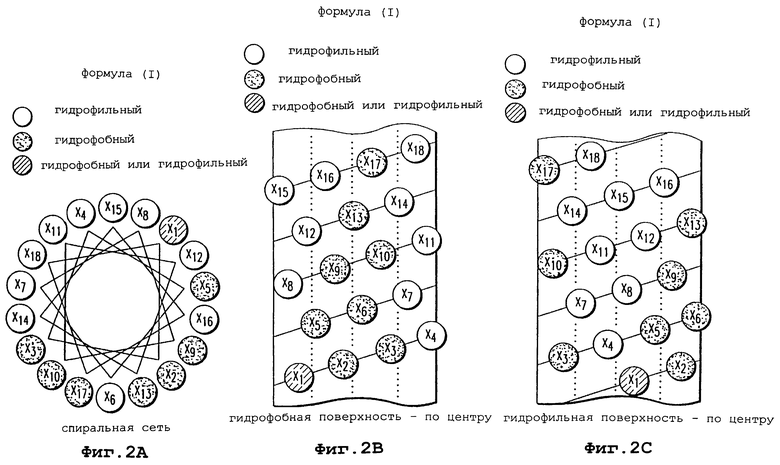
Z1-X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18,
где X1 представлен пролином (Р), аланином (А), глицином (G), аспарагином (N), глутамином (Q) или D-пролином (р);
Х2 - алифатической аминокислотой;
Х3 - лейцином (L);
Х4 - кислой аминокислотой;
X5 - лейцином (L) или фенилаланином (F);
Х6 - лейцином (L) или фенилаланином (F);
Х7 - основной аминокислотой;
X8 - кислой аминокислотой;
Х9 - лейцином (L) или триптофаном (W);
Х10 - лейцином (L) или триптофаном (W);
Х11 - кислой аминокислотой или аспарагином (N);
X12 - кислой аминокислотой;
X13 - лейцином (L), триптофаном (W) или фенилаланином (F);
X14 - основной аминокислотой или лейцином (L);
X15 - глутамином (Q) или аспарагином (N);
X16 - основной аминокислотой;
Х17 - лейцином (L);
X18 - основной аминокислотой;
Z1 - H2N- или RC(O)NH-;
Z2 - -C(O)NRR, -С(О)OR или -С(О)ОН или соответствующей солью;
каждый R независимо друг от друга представлен -Н, C1-C6-алкилом, C1-C6-алкинилом, C1-C6-алкинилом, С5-С20-арилом, C6-C26-алкарилом, 5-20-атомным гетероарилом, 6-26-атомным алкгетероарилом или 1-4-аминокислотным пептидом или пептидным аналогом;
каждый знак "-" между остатками Хn независимо друг от друга обозначает амидную связь, замещенную амидную связь, изостер амида или миметик амида; или (ii) делегированную форму структурной формулы (I), в которой по крайней мере один и вплоть до восьми остатков из X1 - X18 делетированы; или (iii) измененную форму структурной формулы (I), в которой по крайней мере один из остатков X1 - X18 пo консервативному типу заменен на другой остаток.
Х7 - аргинином (R), лизином (К) или орнитином;
X8 - аспарагиновой кислотой (D) или глутаминовой кислотой (Е);
Х11 - аспарагином (N) или глутаминовой кислотой (Е);
X12 - глутаминовой кислотой (Е);
Х14 - лизином (К), аргинином (R) или орнитином;
X15 - глутамином (Q) или аспарагином (N);
X16 - лизином (К), аргинином (R) или орнитином;
X18 - аспарагином (N) или глутамином (Q) и по крайней мере один из остатков X1, X2, Х3, Х5, Х6, Х9, Х10, X13 и X17 заменен по консервативному типу на другой остаток.
Х3 - лейцином (L);
Х4 - аспарагиновой кислотой (D) или глутаминовой кислотой (Е);
Х5 - лейцином (L) или фенилаланином (F);
Х6 - лейцином (L) или фенилаланином (F);
X7 - аргинином (R), лизином (К) или орнитином;
Х8 - аспарагиновой кислотой (D) или глутаминовой кислотой (Е);
Х9 - лейцином (L) или триптофаном (W);
Х10 - лейцином (L) или триптофаном (W);
Х11 - глутаминовой кислотой (Е) или аспарагином (N);
X12 - глутаминовой кислотой (Е);
X13 - лейцином (L), триптофаном (W) или фенил-аланином (F);
X14 - аргинином (R), лизином (К) или орнитином;
X15 - глутамином (Q) или аспарагином (N);
X16 - аргинином (R), лизином (К) или орнитином;
X17 - лейцином (L) и
X18 - аргинином (R), лизином (К) или орнитином.
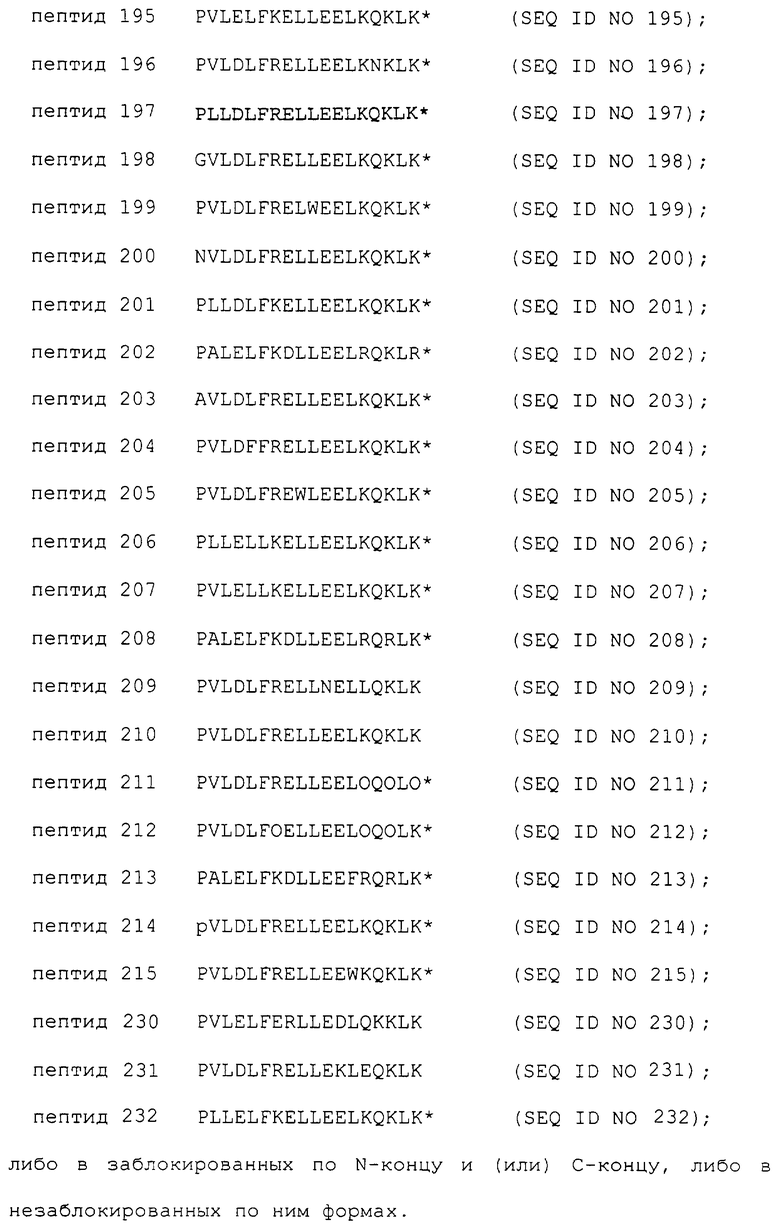
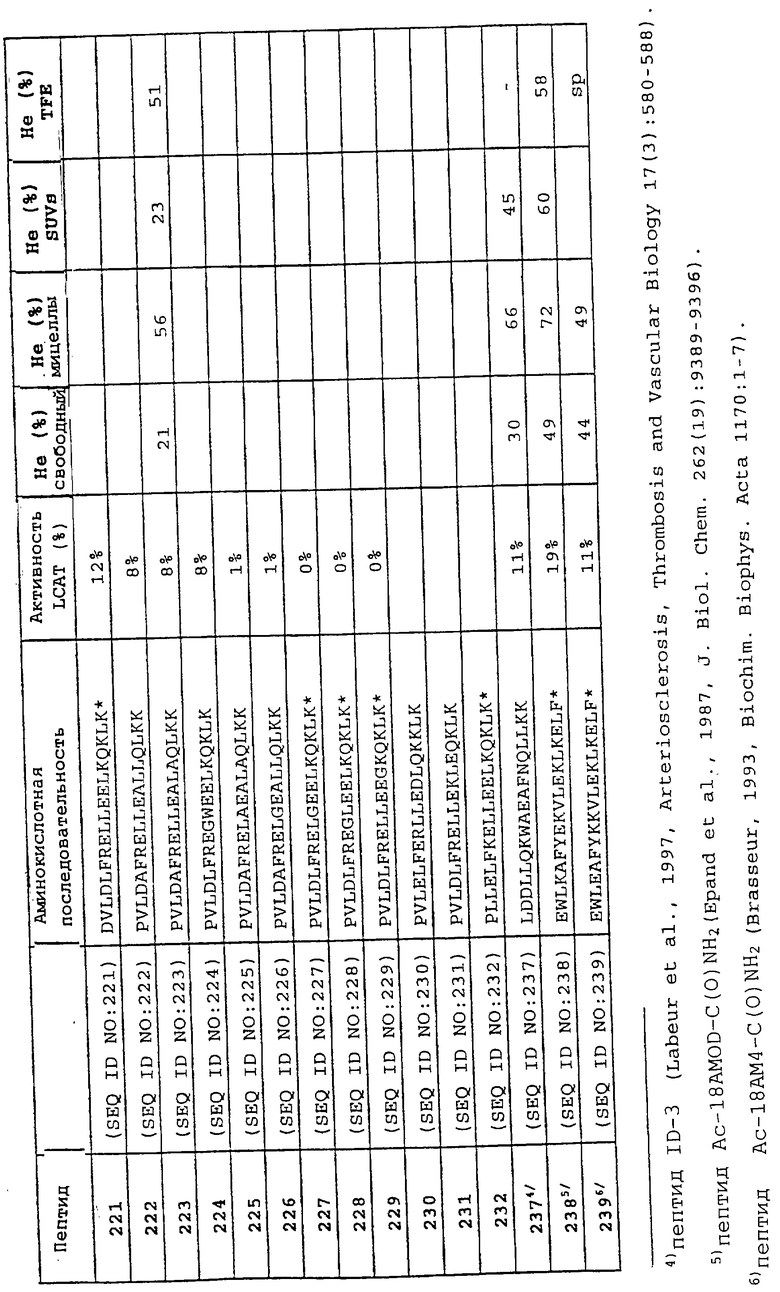
пептид 191 PVLDLLRELLEELKQKLK* (SEQ ID NO 191);
пептид 192 PVLDLFKELLEELKQKLK* (SEQ ID NO 192);
пептид 193 PVLDLFRELLEELKQKLK* (SEQ ID NO 193);
пептид 194 PVLELFRELLEELKQKLK* (SEQ ID NO 194);
пептид 195 PVLELFKELLEELKQKLK* (SEQ ID NO 195);
пептид 196 PVLDLFRELLEELKNKLK* (SEQ ID NO 196);
пептид 197 PLLDLFRELLEELKQKLK* (SEQ ID NO 197);
пептид 198 GVLDLFRELLEELKQKLK* (SEQ ID NO 198);
пептид 199 PVLDLFRELWEELKQKLK* (SEQ ID NO 199);
пептид 200 NVLDLFRELLEELKQKLK* (SEQ ID NO 200);
пептид 201 PLLDLFKELLEELKQKLK* (SEQ ID NO 201);
пептид 202 PALELFKDLLEELRQKLR* (SEQ ID NO 202);
пептид 203 AVLDLFRELLEELKQKLK* (SEQ ID NO 203);
пептид 204 PVLDFFRELLEELKQKLK* (SEQ ID NO 204);
пептид 205 PVLDLFREWLEELKQKLK* (SEQ ID NO 205);
пептид 206 PLLELLKELLEELKQKLK* (SEQ ID NO 206);
пептид 207 PVLELLKELLEELKQKLK* (SEQ ID NO 207);
пептид 208 PALELFKDLLEELRQRLK* (SEQ ID NO 208);
пептид 209 PVLDLFRELLNELLQKLK (SEQ ID NO 209);
пептид 210 PVLDLFRELLEELKQKLK (SEQ ID NO 210);
пептид 211 PVLDLFRELLEELOQOLO* (SEQ ID NO 211);
пептид 212 PVLDLFOELLEELOQOLK* (SEQ ID NO 212);
пептид 213 PALELFKDLLEEFRQRLK* (SEQ ID NO 213);
пептид 214 PVLDLFRELLEELKQKLK* (SEQ ID NO 214);
пептид 215 PVLDLFRELLEEWKQKLK* (SEQ ID NO 215);
пептид 230 PVLELFERLLEDLQKKLK (SEQ ID NO 230);
пептид 231 PVLDLFRELLEKLEQKLK (SEQ ID NO 231);
пептид 232 PLLELFKELLEELKQKLK* (SEQ ID NO 232);
либо в заблокированных по N-концу и(или) С-концу, либо в незаблокированных по ним формах.

или его фармацевтически приемлемая соль,
где независимо друг от друга каждый m=0 или 1;
n=0...10 - целое число;
каждый НН независимо представляет пептид или пептидный аналог по п.1;
каждый LL независимо представляет бифункциональный линкер;
каждый знак "-" независимо обозначает ковалентную связь.
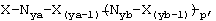
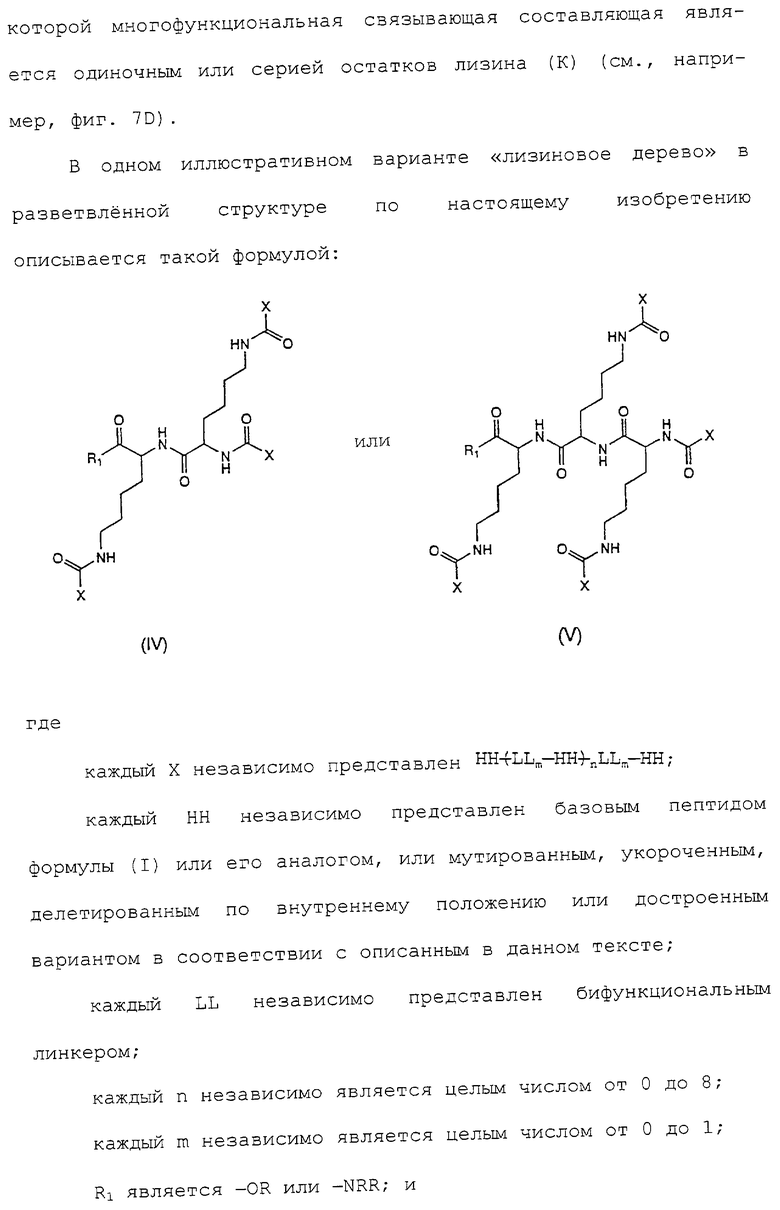
или его фармацевтически приемлемая соль, где каждый Х независимо представлен
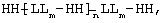
где каждый НН независимо представлен базовым пептидом формулы (I) или его аналогом, или мутированным укороченным, делегированным по внутреннему положению или достроенным вариантом в соответствии с описанным в данном тексте;
каждый LL независимо представлен бифункциональным линкером;
независимо каждый m = 0 или 1;
независимо каждый n = 0...8 - целое число;
Nya и Nyb независимо являются многофункциональной связывающей составляющей, где ya и yb представляют число функциональных групп соответственно в Nya и Nyb;
независимо каждый ya или yb = 3...8 - целое число;
р =0...7 - целое число;
каждый знак “-” независимо обозначает ковалентную связь.
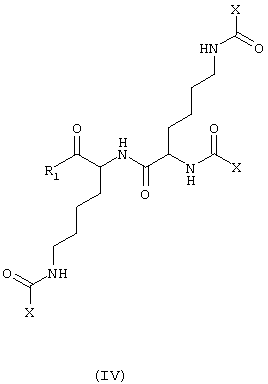
или
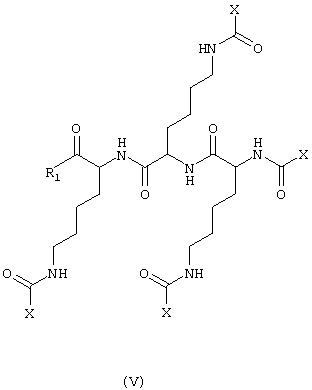
или его фармацевтически приемлемая соль, где каждый Х независимо представлен
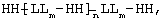
где каждый НН независимо представлен пептидом или пептидным аналогом по п.1; каждый LL независимо - бифункциональным линкером; независимо каждый n = 0 или 1; независимо каждый m = 0...8 - целое число;
R1 является -OR или -NRR, где
каждый R независимо представлен -Н, C1-С6-алкилом, C1-С6-алкенилом, C1-С6-алкинилом, С5-С20-арилом, C6-C26-алкарилом, 5-20-атомным гетероарилом или 6-26-атомным алкгетероарилом.
| US 5545661 A1, 13.08.1996 | |||
| US 5620967 A1, 15.04.1997 | |||
| ОКСОВАНАДИЕВЫЕ КОМПЛЕКСЫ L-ЯБЛОЧНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ | 1996 |
|
RU2101287C1 |
Авторы
Даты
2003-12-27—Публикация
1998-09-28—Подача