Текст описания в факсимильном виде (см. графическую часть).
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕНОТЕРАПЕВТИЧЕСКИЕ СПОСОБЫ ВВЕДЕНИЯ АГОНИСТОВ АПОЛИПОПРОТЕИНА А-I И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ДИСЛИПИДЕМИЧЕСКИХ НАРУШЕНИЙ | 1998 |
|
RU2222545C2 |
| АГОНИСТЫ АПОЛИПОПРОТЕИНА А-I И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДИСЛИПИДЕМИЕЙ | 1998 |
|
RU2215747C2 |
| АГОНИСТЫ АПОЛИПОПРОТЕИНА А-1 И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДИСЛИПИДЕМИЕЙ | 1998 |
|
RU2219941C2 |
| МИМЕТИКИ АПОЛИПОПРОТЕИНА А-I | 2010 |
|
RU2532222C2 |
| Циклические аналоги галанина и пути их применения | 2016 |
|
RU2727013C2 |
| ОБРАЗОВАНИЕ ПЕПТИД/ЛИПИДНОГО КОМПЛЕКСА ПУТЕМ СОВМЕСТНОЙ ЛИОФИЛИЗАЦИИ | 1998 |
|
RU2224506C2 |
| Терапевтическое применение глюкагона и включающей его комбинации | 2019 |
|
RU2838895C2 |
| ДВОЙНЫЕ АГОНИСТЫ GLP1/GIP ИЛИ ТРОЙНЫЕ АГОНИСТЫ GLP1/GIP/ГЛЮКАГОНА | 2013 |
|
RU2652783C2 |
| ПОЛИПЕПТИД, ИМЕЮЩИЙ АНТИБАКТЕРИАЛЬНУЮ АКТИВНОСТЬ И ПРИГОДНЫЙ ДЛЯ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ ЧЕЛОВЕКА | 2010 |
|
RU2434880C1 |
| ПОЛИПЕПТИДЫ АНАЛОГА АМИЛИНА ЧЕЛОВЕКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2839688C2 |
























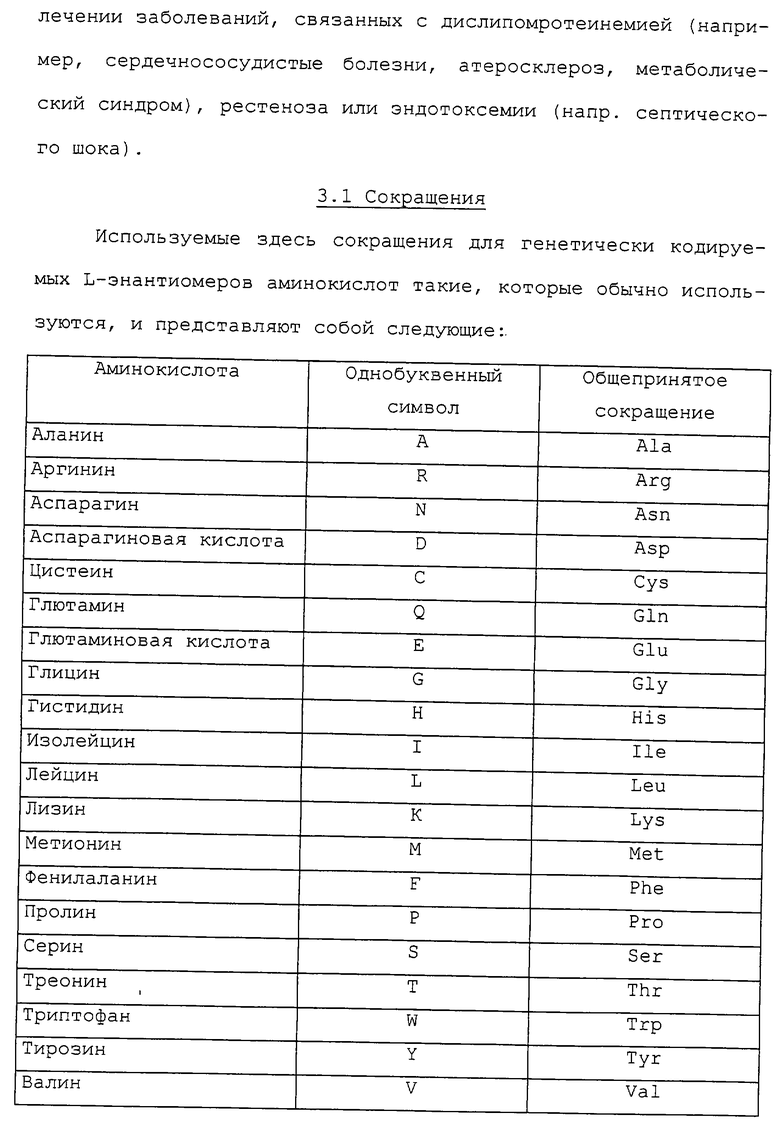
























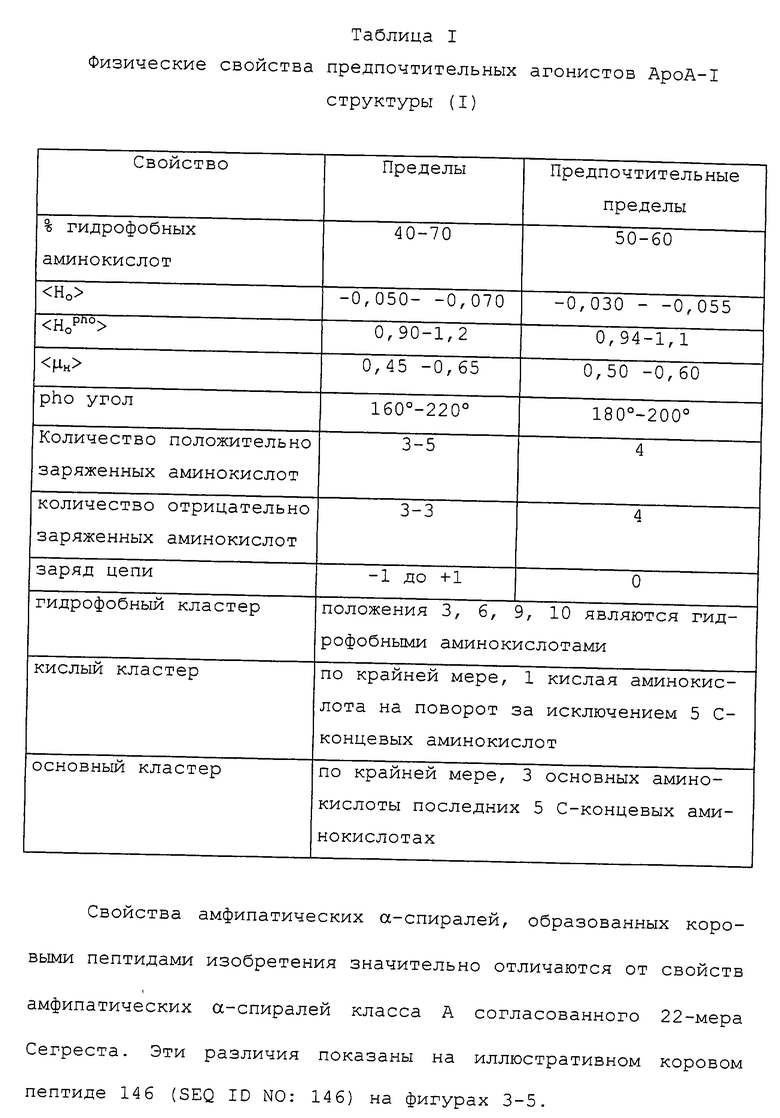
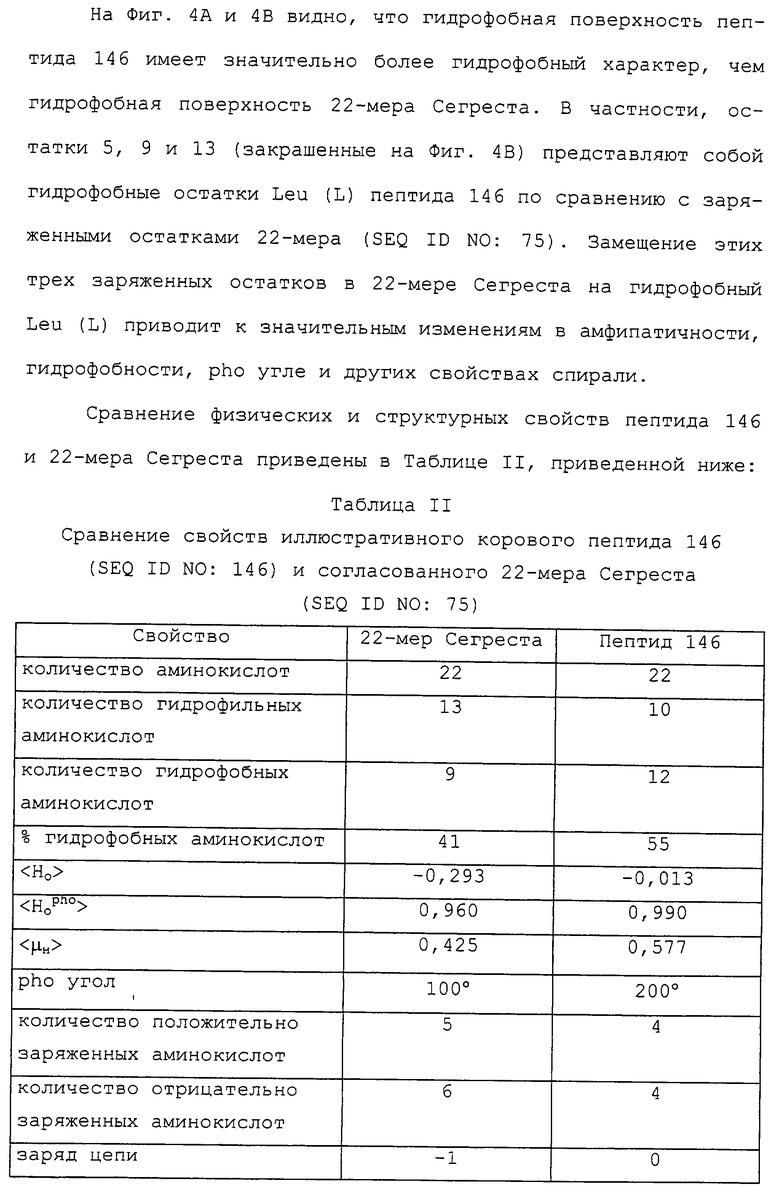







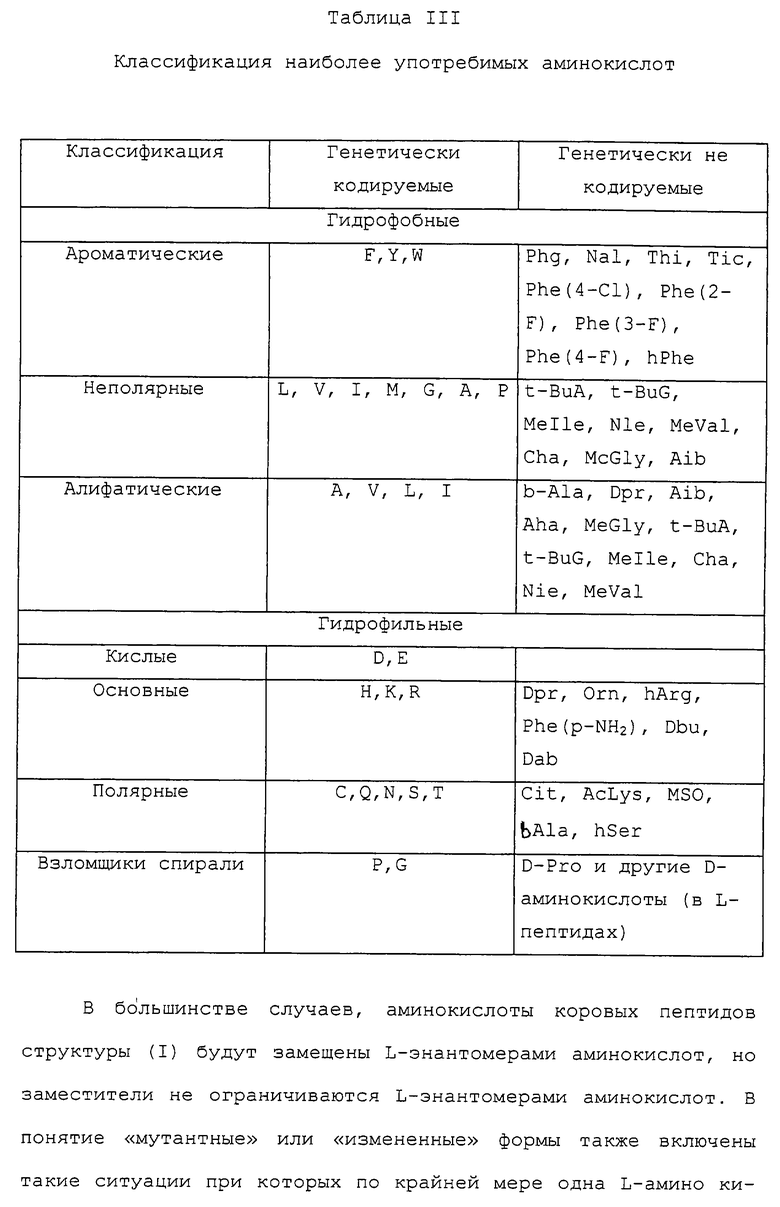












































































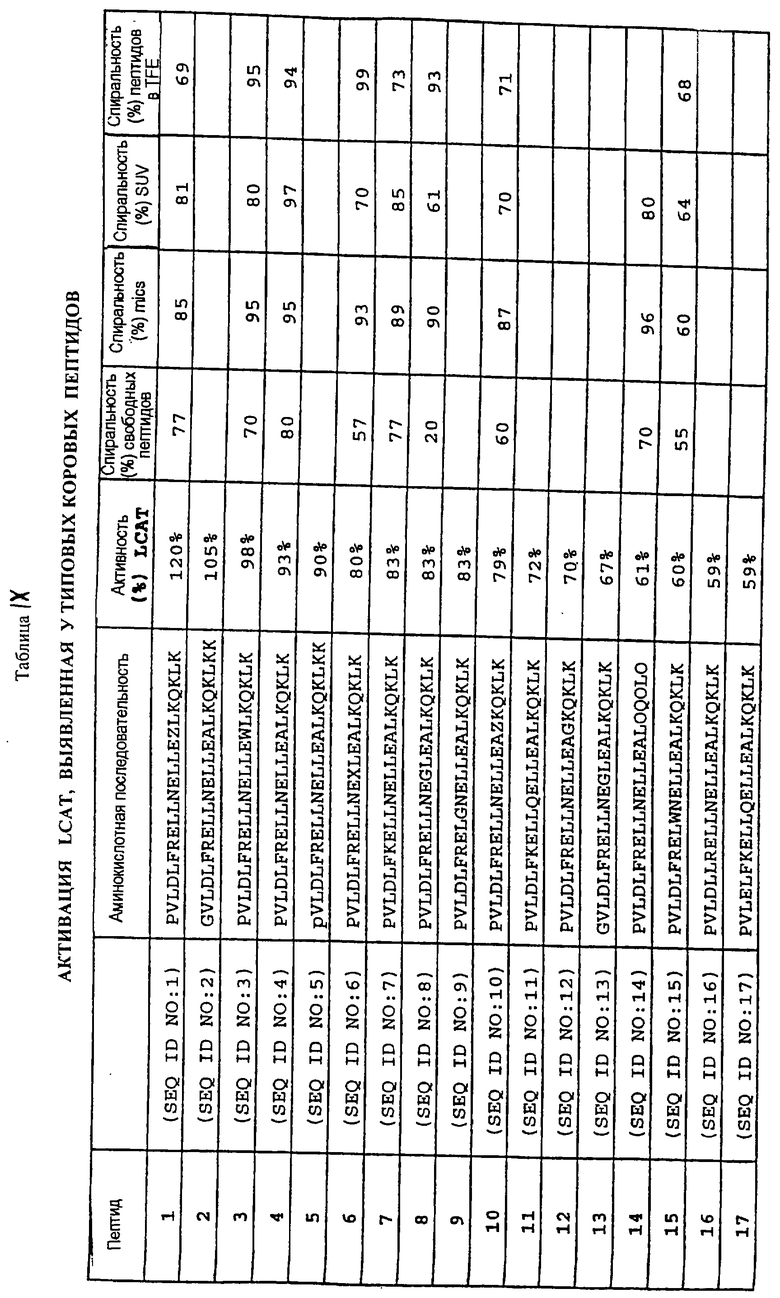
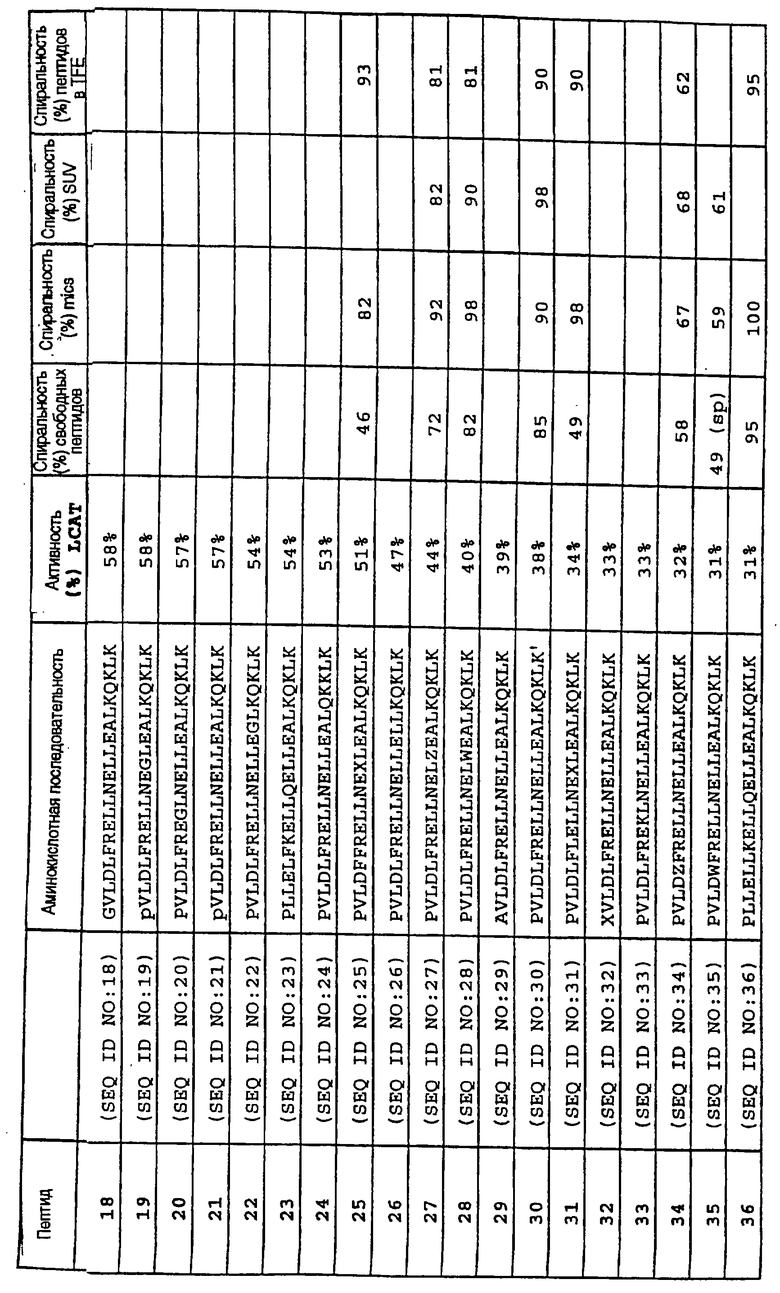
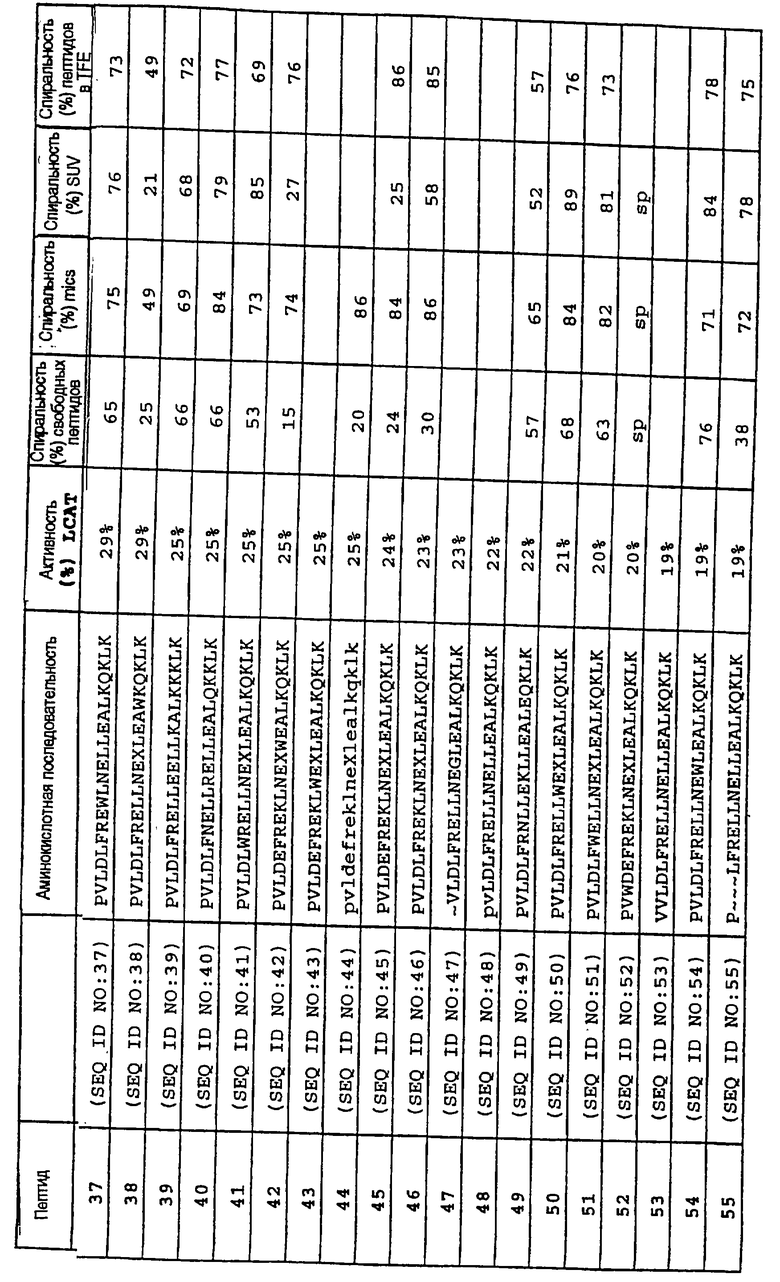
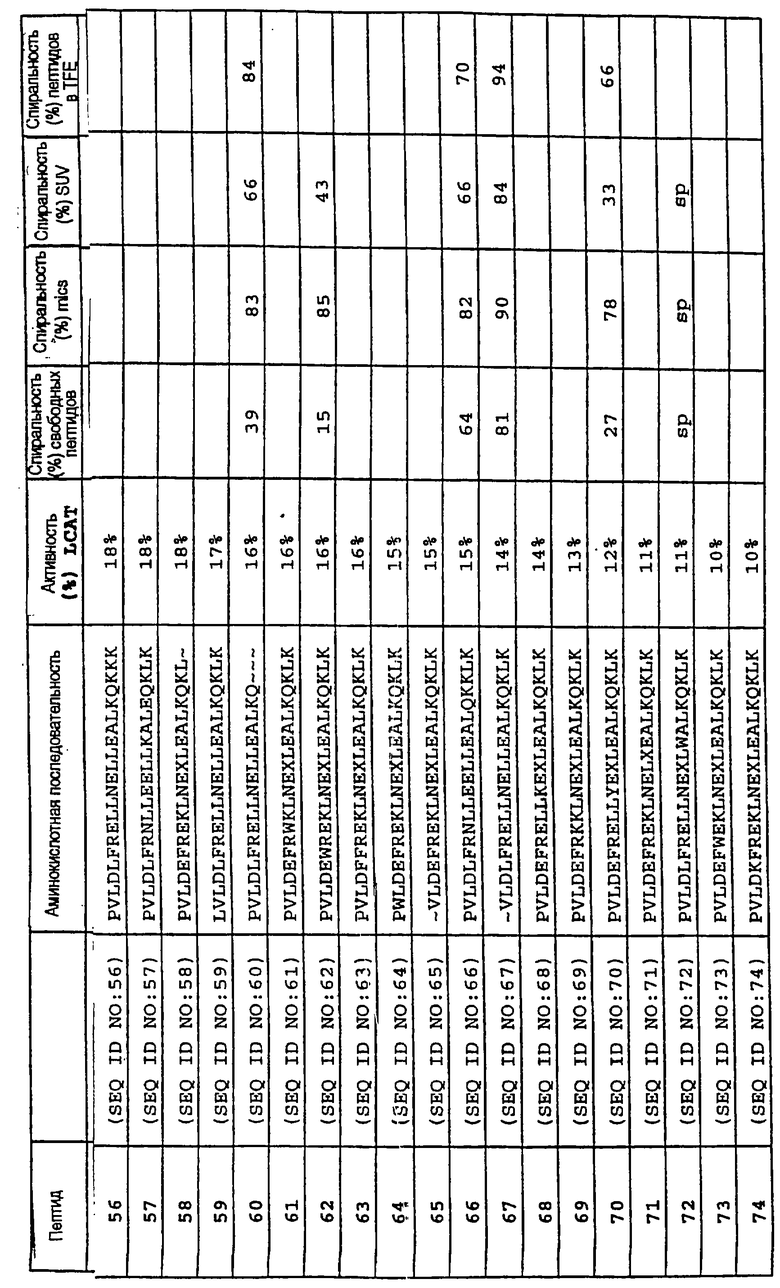
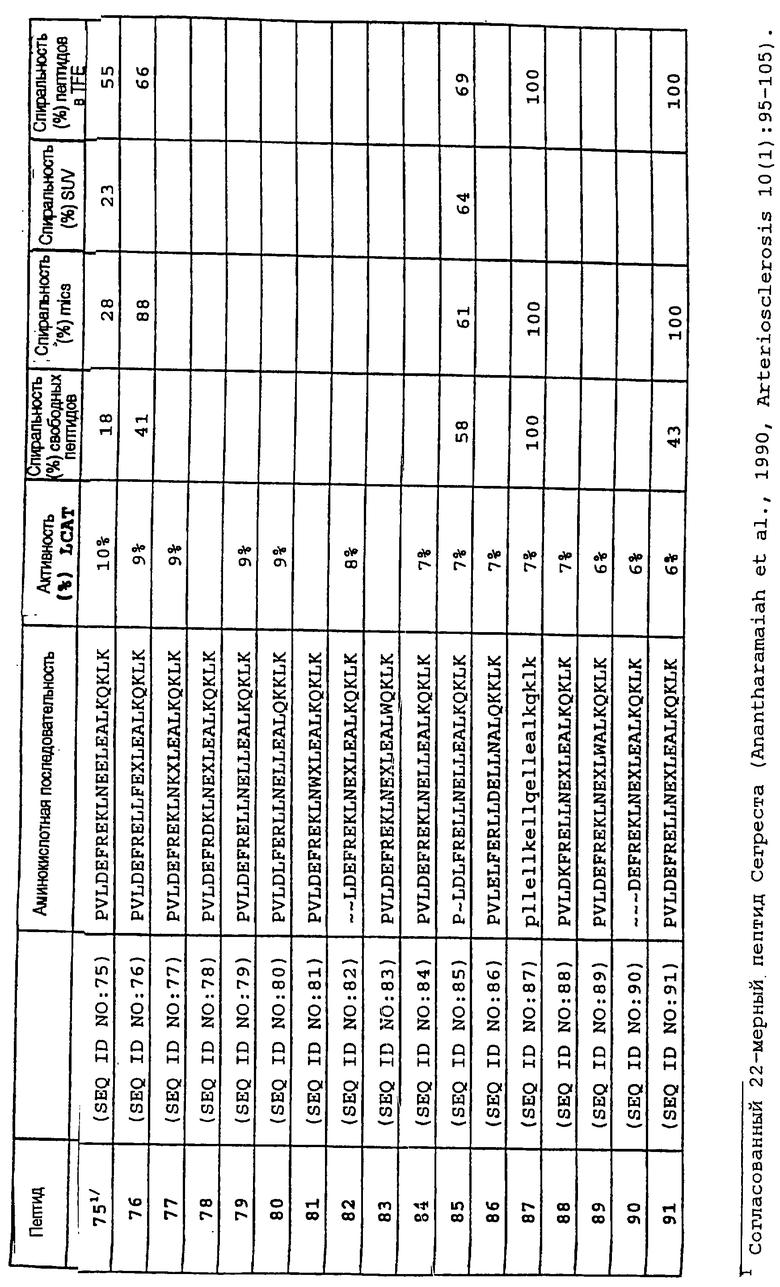
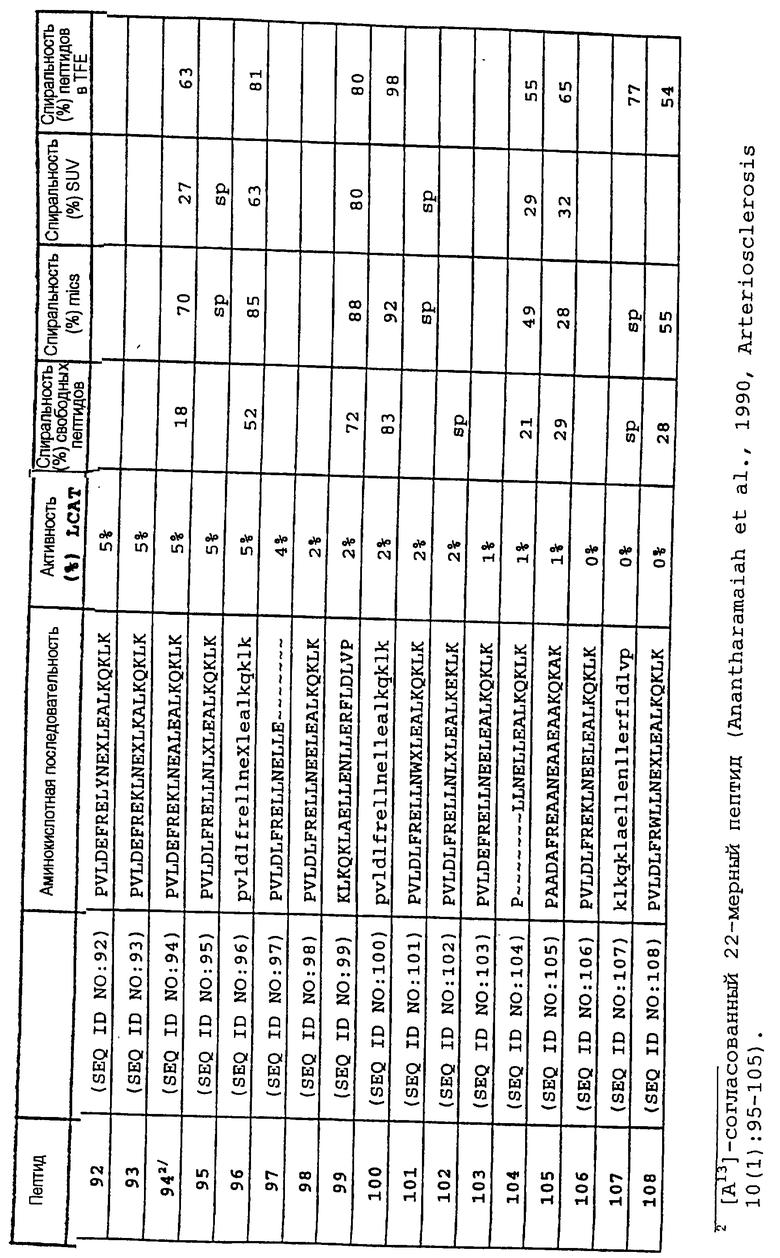
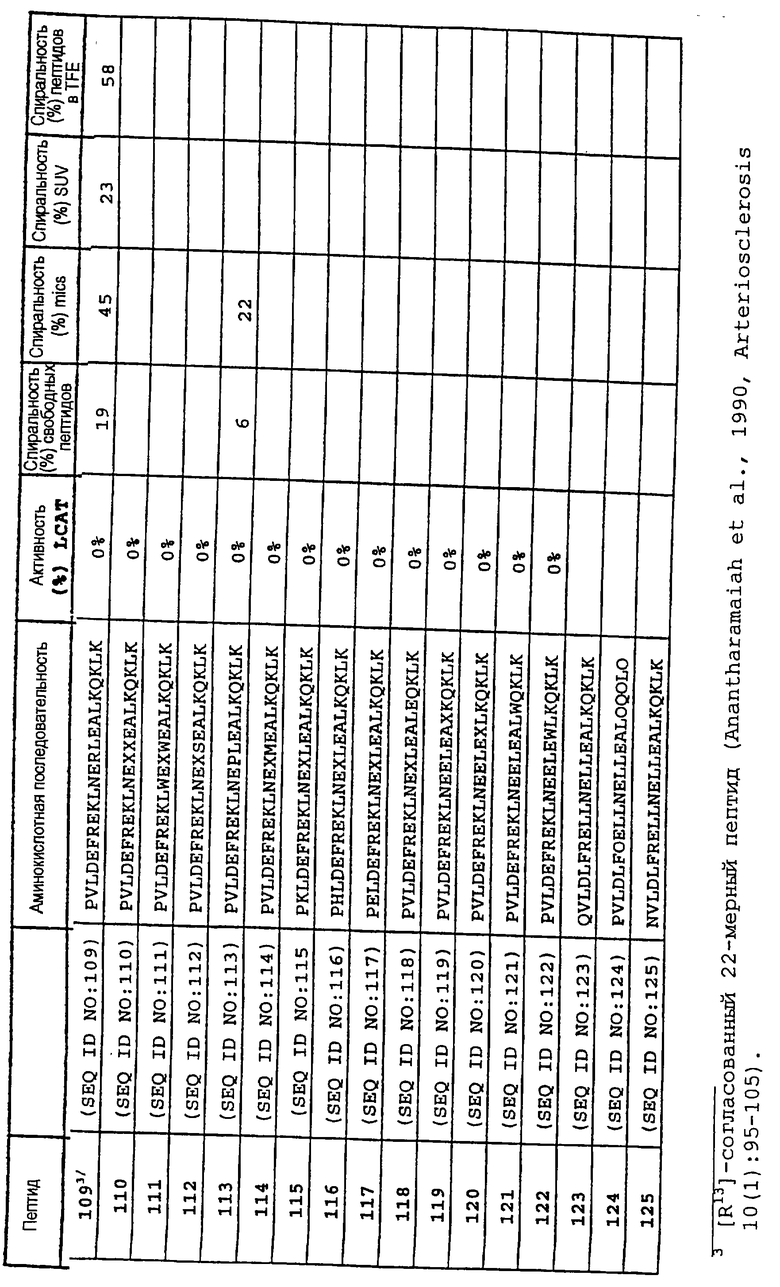
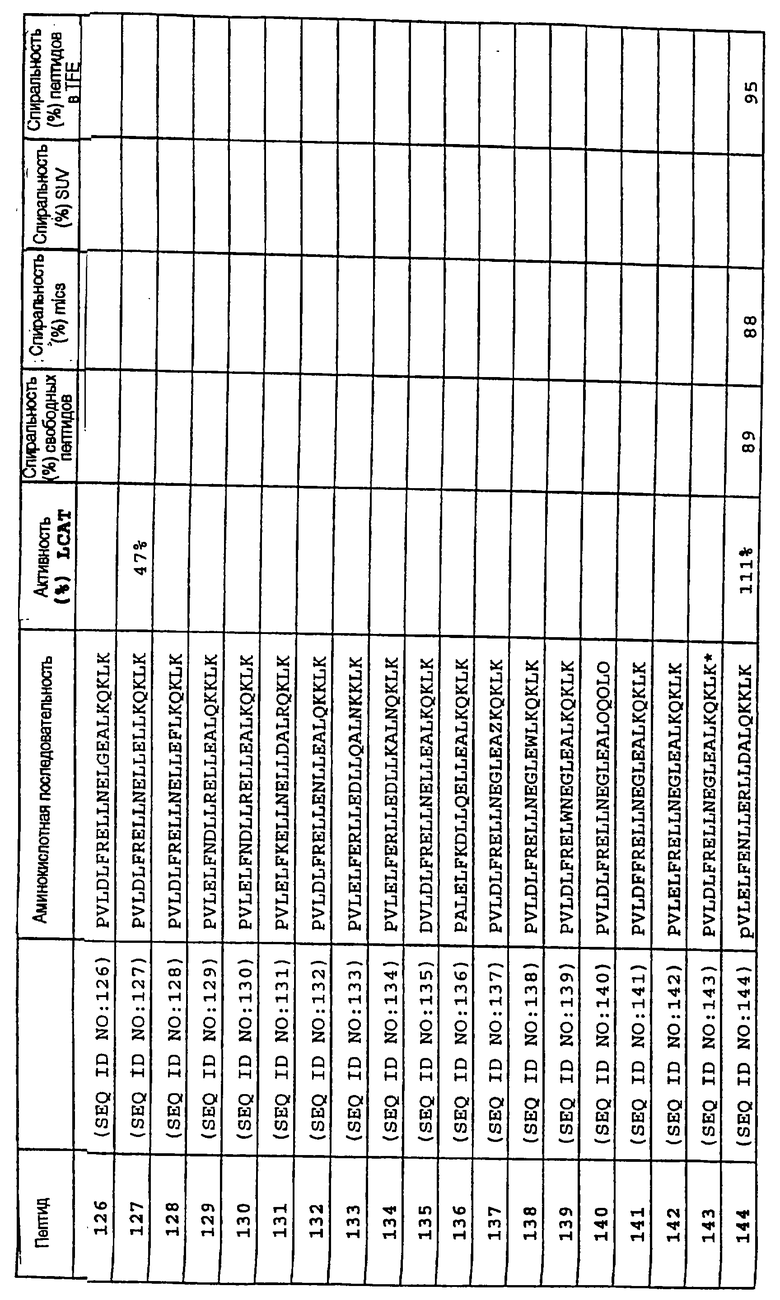
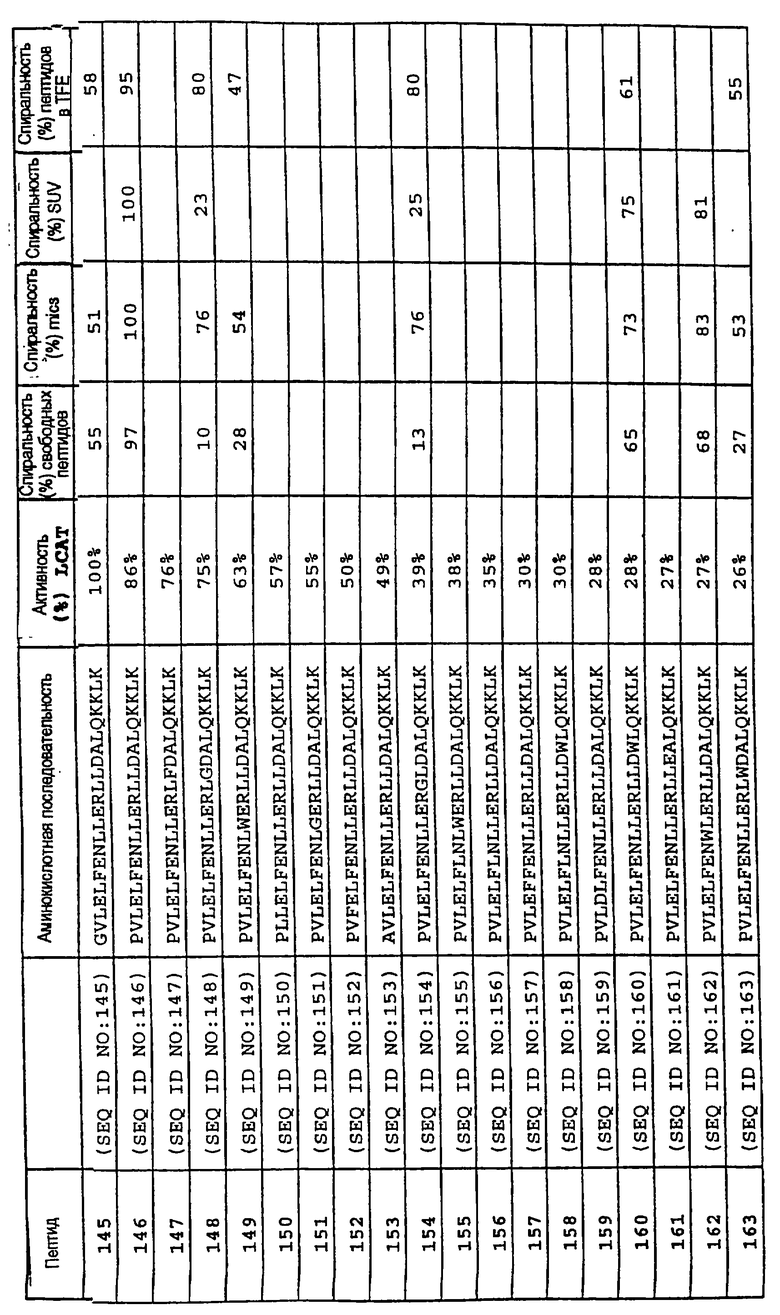

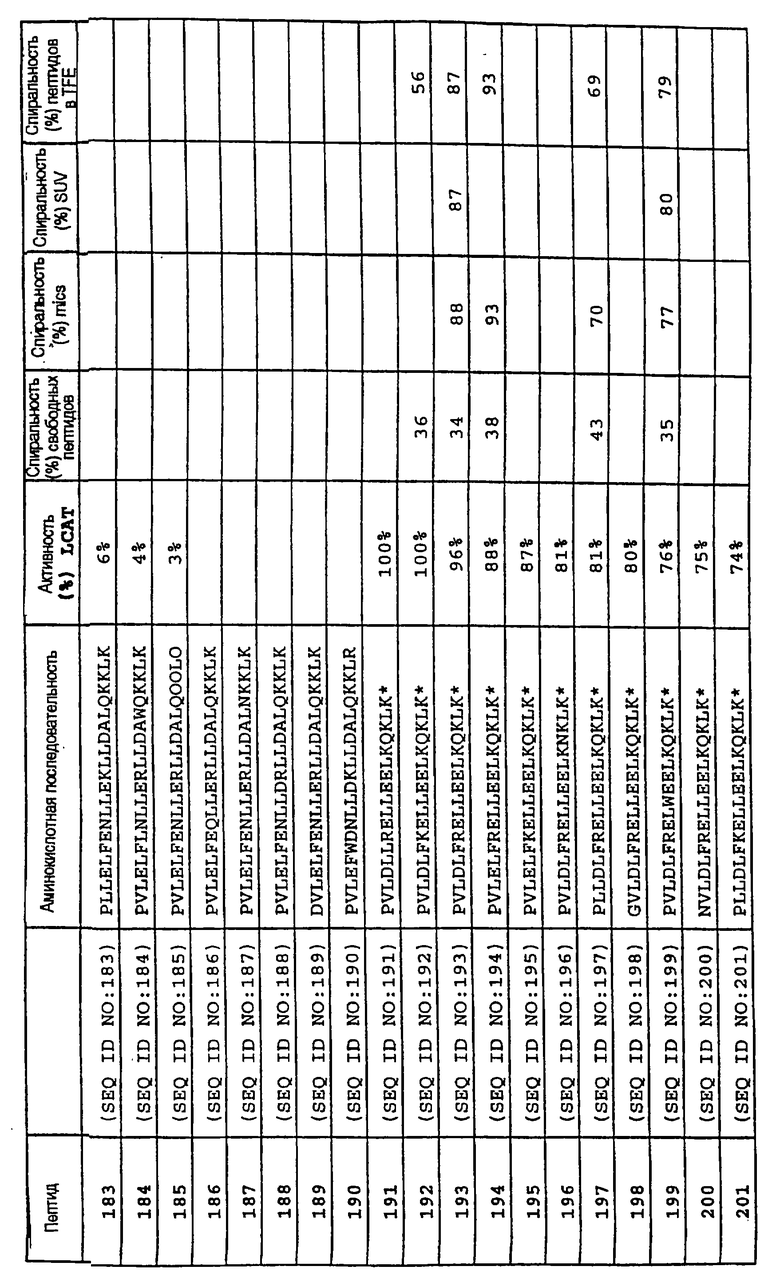
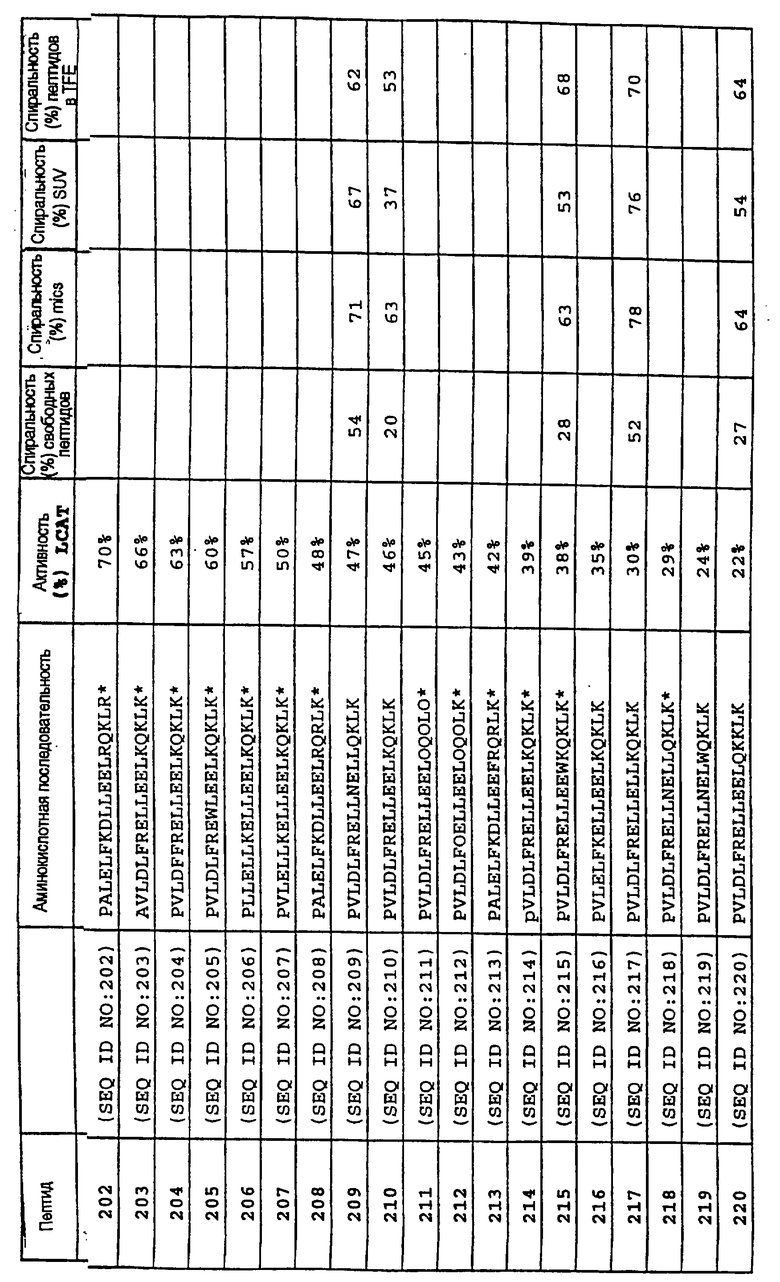
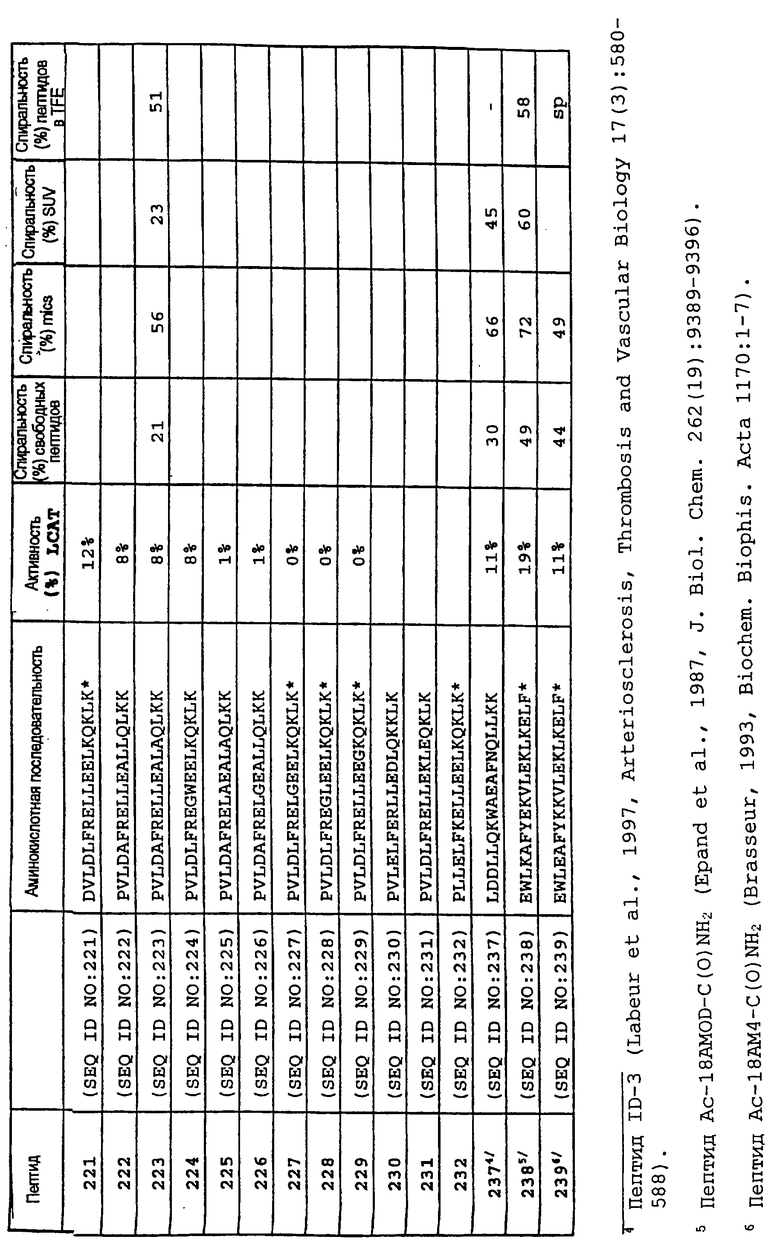
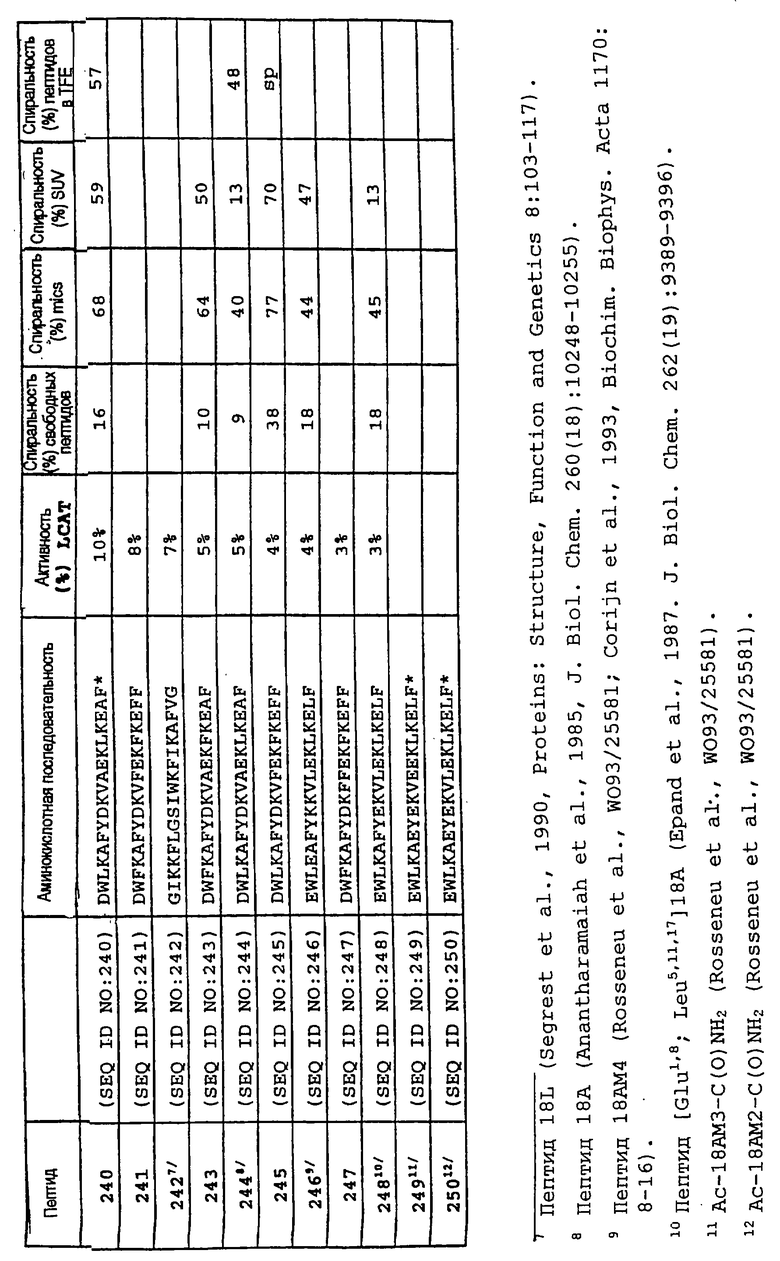
































































































































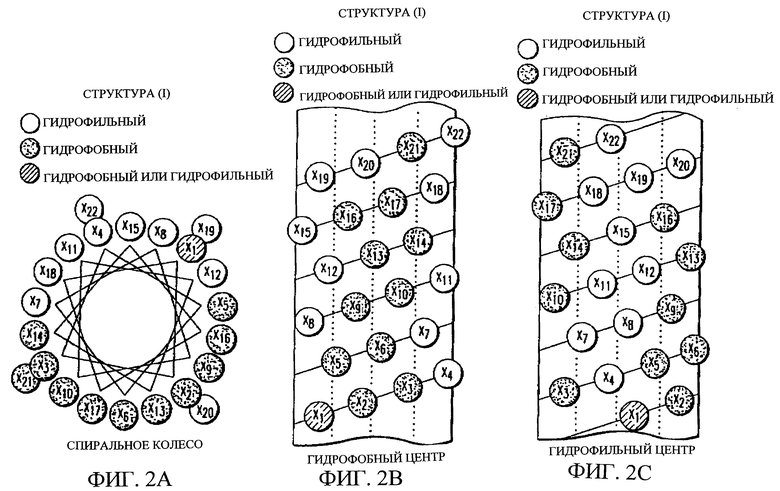
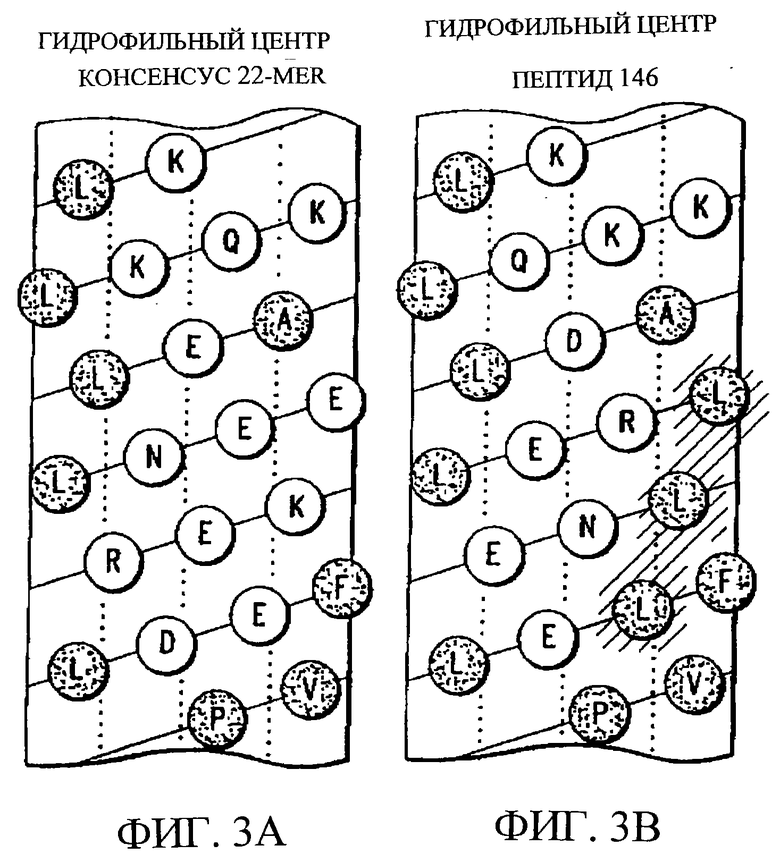
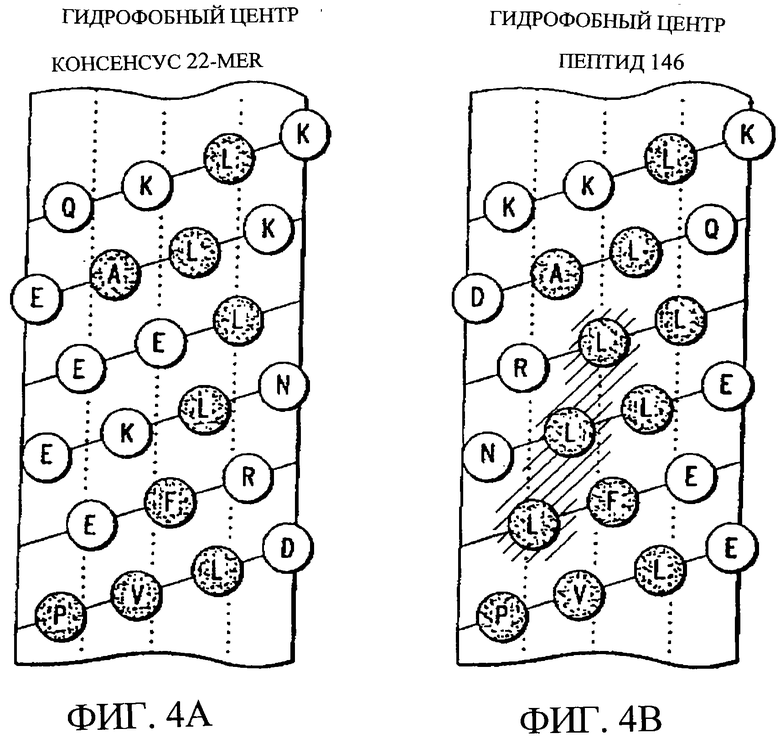
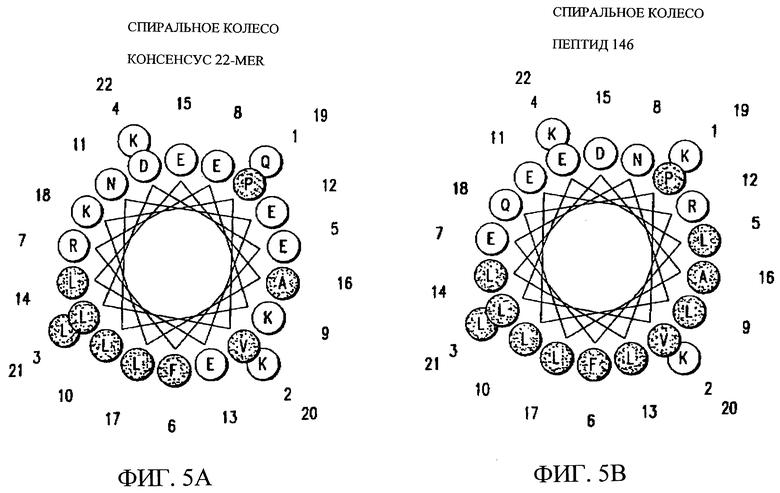
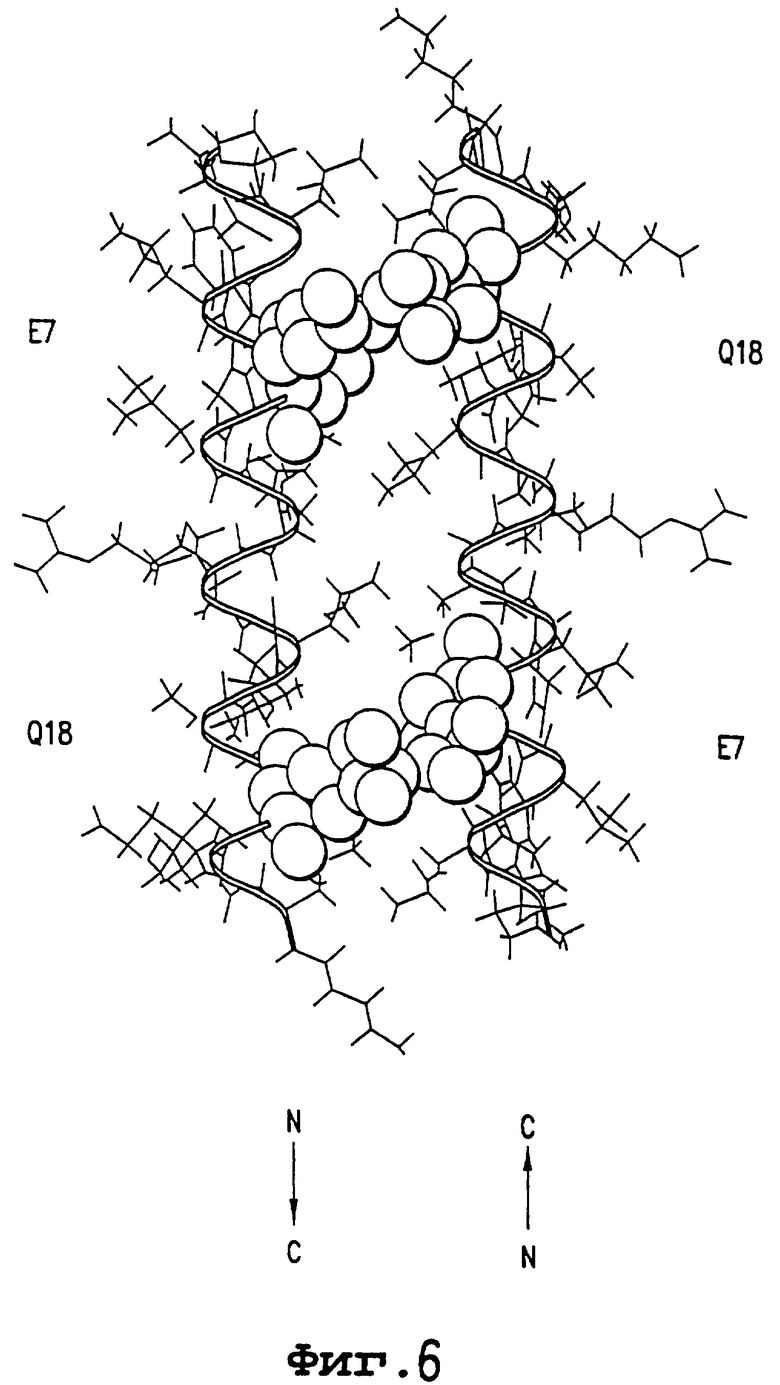
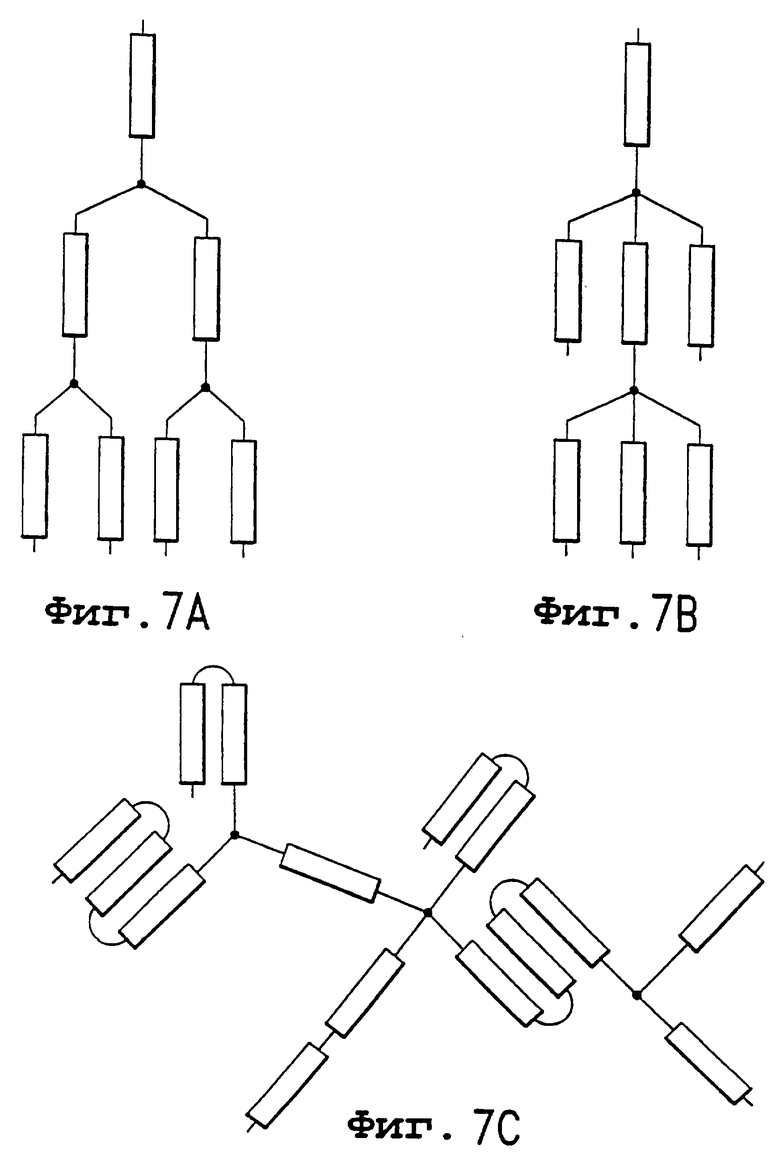
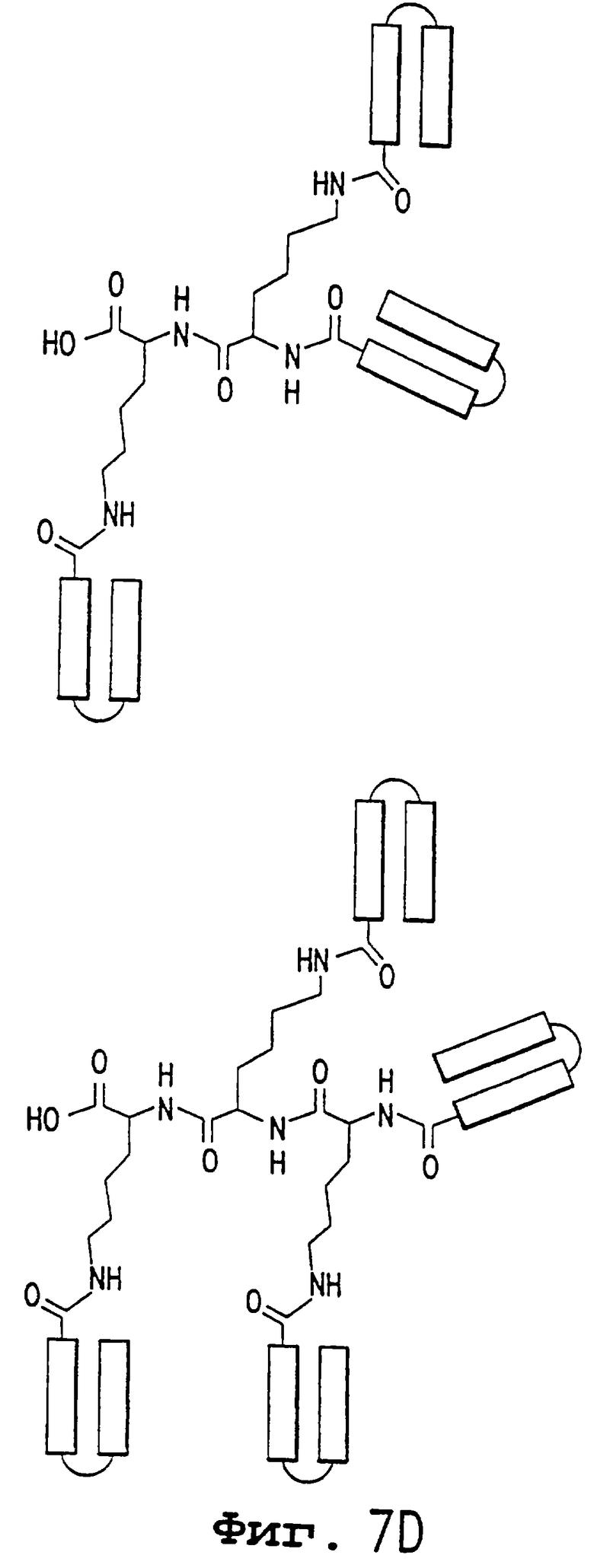
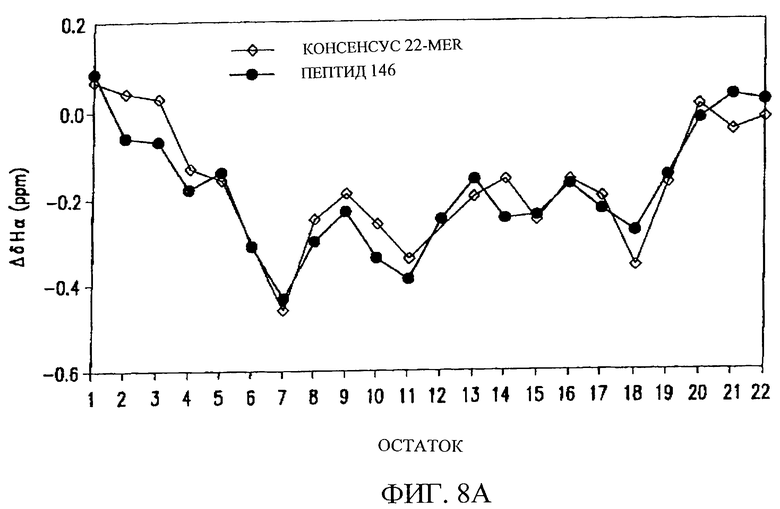
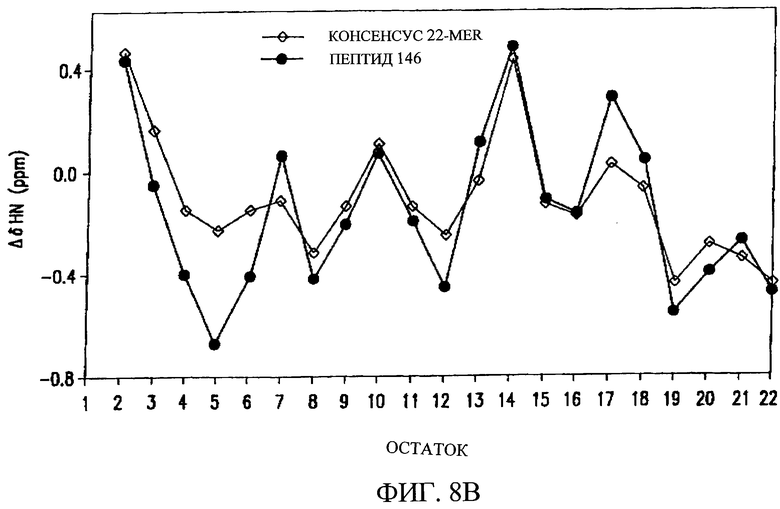
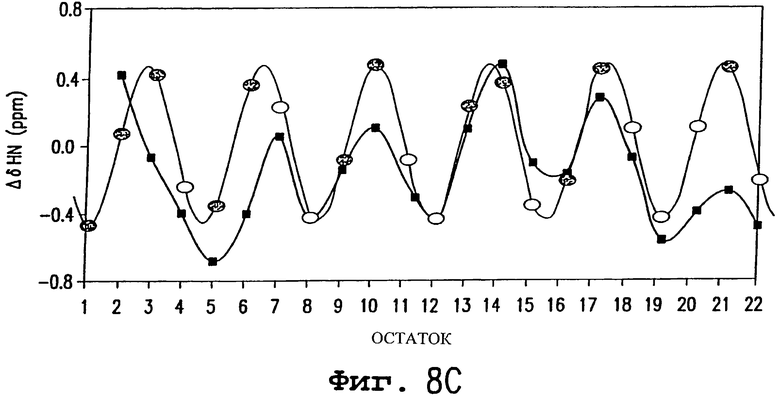
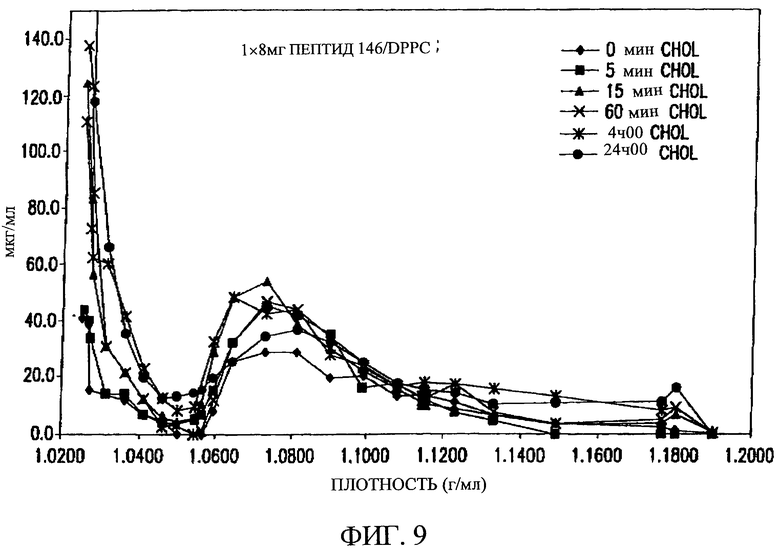
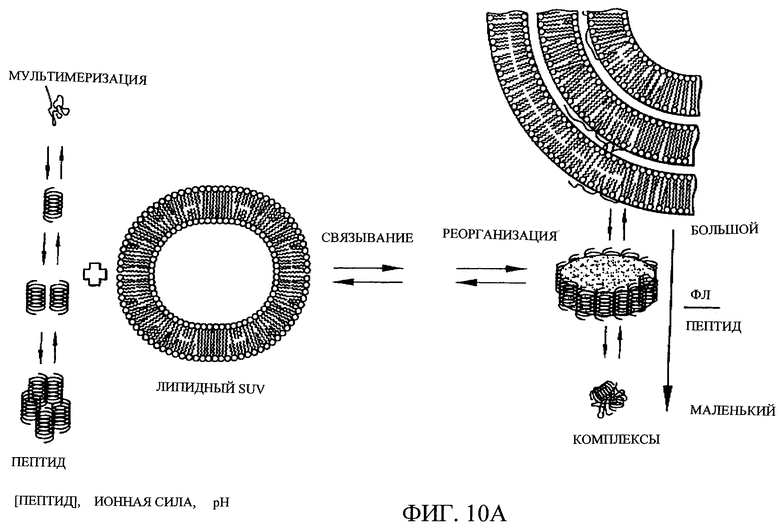
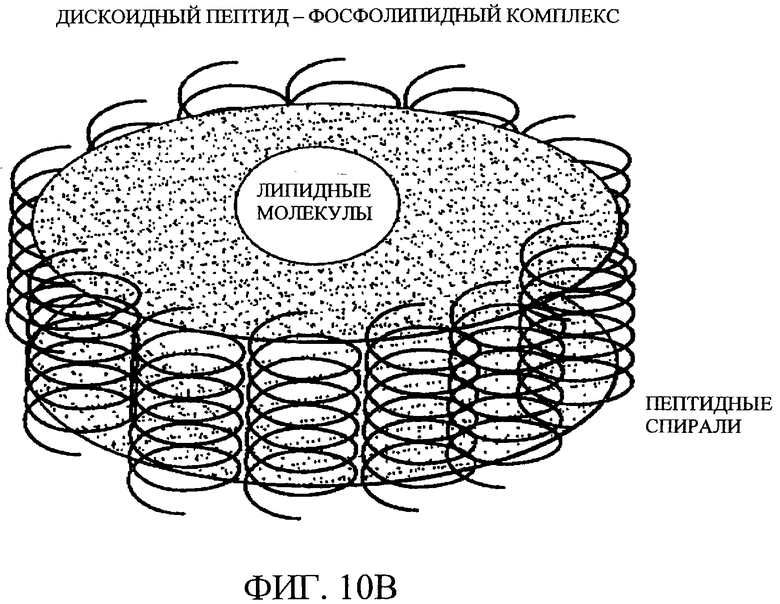

Изобретение относится к медицинской молекулярной биологии. Сущность изобретения составляют новые пептидные последовательности и их аналоги, обладающие свойствами агонистов аполипопротеина А-I (Аро-А-I) путем ввведения их эффективного количества пациенту. Такие пептиды и их аналоги используют для лечения разнообразных нарушений, связанных с дислипидемией. Изобретение содержит сведения о соответствующих химических структурах, различных комплексах таких пептидов, в частности, с липидами, фармацевтических композициях и методах лечения дислипидемических нарушений. Технический результат - расширение арсенала средств терапии различных дислипидемических состояний. 14 с. и 47 з.п.ф-лы, 10 табл., 10 ил.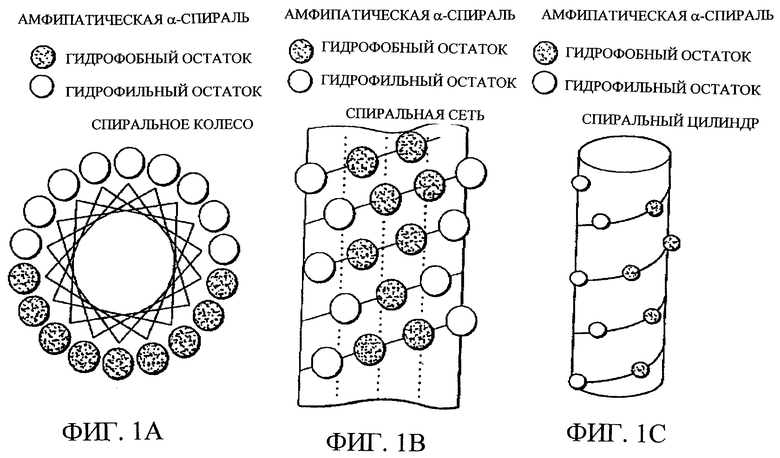
Z1-X1-X2-X3-X4-X5-X6-X7-X8-X9-X10-X11-X12-X13-X14-X15-X16-X17-X18-X19-X20-X21-X22-X23-Z2,
(I)
или его фармацевтически приемлемую соль,
где X1 представляет собой Pro (Р), Ala (A), Gly (G), Gln (Q), Asn (N), Asp (D) или D-Pro (p);
Х2 представляет собой алифатический остаток;
Х3 представляет собой Leu (L) или Phe (F);
Х4 представляет собой Glu (E);
Х5 представляет собой алифатический остаток;
Х6 представляет собой Leu (L) или Phe (F);
Х7 представляет собой Leu (L) или Glu (E);
Х8 представляет собой Asn (N) или Gln (Q);
Х9 представляет собой Leu (L);
Х10 представляет собой Leu (L), Trp (W) или Gly (G);
Х11 представляет собой кислый остаток;
X12 представляет собой Arg (R);
X13 представляет собой Leu (L) или Gly (G);
Х14 представляет собой Leu (L), Phe (F) или Gly (G);
X15 представляет собой Asp (D);
X16 представляет собой Ala (А);
X17 представляет собой Leu (L);
X18 представляет собой Asn (N) или Gln (Q);
X19 представляет собой основный остаток;
X20 представляет собой основный остаток;
X21 представляет собой Leu (L);
X22 представляет собой основный остаток;
Х23 отсутствует или представляет собой основный остаток;
Z1 представляет собой H2N- или RC(O)NH-;
Z2 представляет собой: -C(O)NRR, -С(О)OR, -С(О)ОН, или их соли;
каждый R представляет собой независимо -Н, (C1-С6) алкильную, (C1-С6) алкенильную, (C1-С6) алкинильную, (C5-С20) арильную, (C6-С26) алкарильную группы, 5-20-членную гетероарильную или 6-26-членную алкгетероарильную группу или 1-7-членный пептид или пептидный аналог;
каждый символ "-" между остатками Xn независимо обозначает амидную связь, замещенную амидную связь, изостер амида или амидомиметик;
или ii) делегированная форма структурной формулы (I), в которой по крайней мере от одного до восьми остатков из X1, X2, Х3, X4, X5, Х6, Х7, Х8, X9, Х10, Х11, X12, X13, Х14, X15, X16, X17, X18, X19, X20, X21 и X22 удалены, или iii) модифицированная форма структурной формулы (I), в которой по крайней мере один из остатков X1, X2, Х3, X4, X5, Х6, Х7, X8, Х9, Х10, Х11, X12, X13, Х14, X15, X16, X17, X18, X19, X20, X21, X22 или Х23 консервативно замещены другим остатком.
и ацилированная по N-концу и/или амидированная или этерифицированная по С-концу его форма.
HH-[LLm-HH] n-LLm-HH, (II)
или является фармацевтически приемлемой его солью,
где каждый m представляет собой независимо целое число от 0 до 1;
n представляет собой целое число от 0 до 10;
каждый НН представляет собой независимо пептид или пептидный аналог по п. 1;
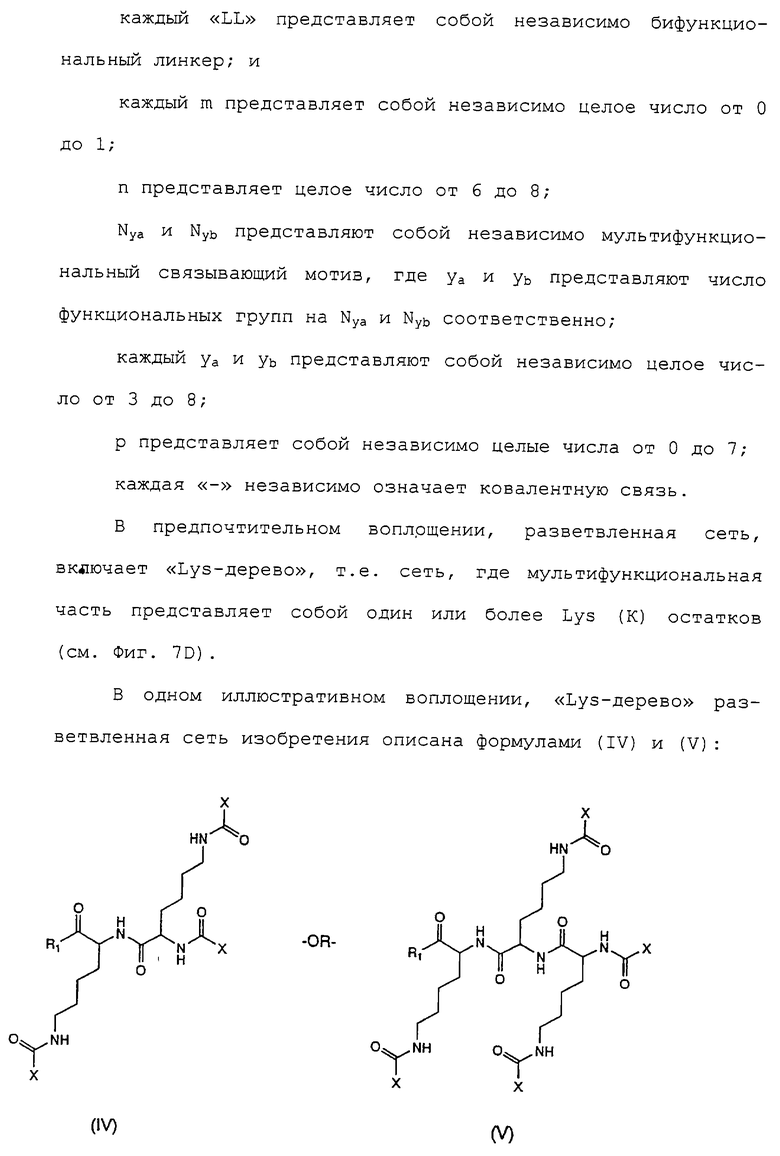
каждый LL представляет собой независимо бифункциональный линкер; и
каждый "-" независимо означает ковалентную связь.
X-Nya-X(ya-1)-(Nyb-X(yb-1))p, (III)
или является фармацевтически приемлемой его солью,
где каждый Х представляет собой независимо HH-[LLm-HH] n-LLm-HH;
каждый НН представляет собой независимо коровый пептид структуры (I) или аналог или мутантную, усеченную, с внутренними делециями или расширенную форму его, как описано здесь;
каждый LL представляет собой независимо бифункциональный линкер;
каждый m представляет собой независимо целое число от 0 до 1;
n представляет собой целое число от 0 до 8;
Nya и Nyb представляют собой независимо мультифункциональный связывающий радикал, где уа и уb представляют число функциональных групп на Nya и Nyb соответственно;
каждый уа и уb представляют собой независимо целое число от 3 до 8;
р представляет собой независимо целое число от 0 до 7;
каждый "-" независимо означает ковалентную связь.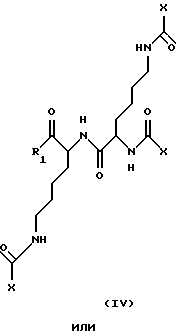
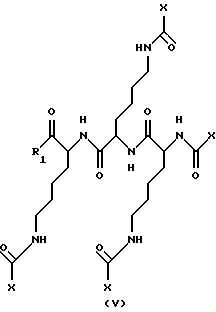
или является фармацевтически приемлемой его солью,
где каждый Х представляет собой независимо НН-[LLm-HH] n-LLm-НН;
каждый НН представляет собой независимо пептид или пептидный аналог по п. 1;
каждый LL представляет собой независимо бифункциональный линкер;
каждый n представляет собой независимо целое число от 0 до 1;
m представляет собой целое число от 0 до 8;
R1 представляет собой -OR или -NRR;
каждый R представляет собой независимо -Н, (C1-C6) алкильную, (C1-C6) алкенильную, (C1-C6) алкинильную, (C5-C20) арильную, (С6-С26) алкарильную группы, 5-20-членную гетероарильную или 6-26-членную алкгетероарильную группу.
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| CORNUT I | |||
| et al | |||
| Application to the novo design..., FEBS Letters, 1994, v | |||
| Способ составления поездов | 1924 |
|
SU349A1 |
| Солесос | 1922 |
|
SU29A1 |
Авторы
Даты
2003-10-27—Публикация
1998-09-28—Подача