Изобретение относится к способу получения алкиленгликолей взаимодействием алкиленоксидов с водой в присутствии каталитической композиции.
Предпосылки изобретения
Алкиленгликоли, в частности моноалкиленгликоли, имеют стабильное промышленное значение. Например, моноалкиленгликоли используются в композициях антифризов в качестве растворителей и в качестве основных материалов при получении полиалкилентерефталатов, например, для волокон или бутылок.
Известно получение алкиленгликолей путем жидкофазного гидролиза алкиленоксидов. Процесс гидролиза осуществляется без катализатора за счет добавления большого избытка воды, например 20 - 25 молей воды на моль алкиленоксида, или осуществляется с меньшим избытком воды в каталитической системе. Считается, что эта реакция является реакцией нуклеофильного замещения, в результате которого происходит раскрытие кольца алкиленоксида, причем вода выполняет роль нуклеофильного агента. Поскольку первоначально образующийся моноалкиленгликоль также действует как нуклеофил, как правило, образуется смесь моноалкиленгликоля, диалкиленгликоля и высших алкиленгликолей. Для того чтобы повысить селективность по моноалкиленгликолю, необходимо подавить вторичную реакцию между первичным продуктом и алкиленоксидом, которая конкурирует с гидролизом алкиленоксида.
Одним из эффективных приемов подавления вторичной реакции является увеличение относительного количества воды, присутствующей в реакционной смеси. Хотя этот прием повышает селективность по моноалкиленгликолю, он создает проблему больших количеств воды, которую необходимо удалять для извлечения продукта.
Были предприняты значительные усилия для того чтобы найти альтернативное решение для повышения селективности реакции без использования большого избытка воды. Обычно эти усилия сосредоточены на подборе более активных катализаторов гидролиза, и были описаны различные катализаторы.
Были исследованы как кислотные, так и щелочные катализаторы гидролиза, в результате чего оказалось, что использование кислотных катализаторов увеличивает скорость реакции без существенного влияния на селективность, тогда как при использовании щелочных катализаторов обычно получают более низкую селективность по моноалкиленгликолю.
Известно, что некоторые анионы, например бикарбонат (гидрокарбонат), бисульфит (гидросульфит), формиат и молибдат, обладают хорошей каталитической активностью с точки зрения конверсии алкиленоксида и селективности по моноалкиленгликолю. Однако, когда соли этих анионов используются в качестве катализатора в гомогенной системе, обработка продукта реакции путем перегонки будет вызывать проблему, поскольку эти соли плохо растворимы в гликоле и имеется тенденция перехода раствора в полутвердое состояние. Соли четвертичного аммония остаются растворенными в гликолевом продукте реакции.
Высокие степени превращения, хорошая селективность и низкое соотношение вода/алкиленоксид можно получить способом, описанным в ЕР-А 0156449 и ЕР-А 0160330 (оба принадлежат фирме Union Саrbide). В соответствии с этими документами гидролиз алкиленоксидов осуществляют в присутствии материала, содержащего металат-анион, который повышает селективность предпочтительно твердого вещества, имеющего электроположительные комплексообразующие центры, которые обладают сродством к металатным анионам. Указанным твердым веществом предпочтительно является анионообменная смола, в частности, сополимер стирол-дивинилбензол. Электроположительные комплексообразующие центры представляют собой, в частности, четвертичный аммоний, протонированный третичный амин или четвертичный фосфоний. Четвертичному фосфонию не приписывается какое-либо конкретное преимущество. Металатные анионы определяются как молибдатный, вольфраматный, метаванадатный, гидропированадатный и пированадатный анионы. Осложнением этого способа является то, что поток продукта, содержащий алкиленгликоль, также содержит значительное количество металатных анионов, вытесненных из электроположительных комплексообразующих центров твердого материала, содержащего металатные анионы. Для того чтобы снизить количество металатных анионов в потоке продукта, содержащем алкиленгликоль, этот поток подвергают контактированию с твердым веществом, имеющим электроположительные комплексообразующие центры, связанные с анионами, которые могут замещаться указанными металатными анионами.
В WO 95/20559 (Shell) описан способ получения алкиленгликолей, в котором алкиленоксид взаимодействует с водой в присутствии каталитической композиции, содержащей твердый материал, имеющий один или более электроположительных центров, которые координированы с одним или более анионами, отличными от металатных или галоидных анионов, например бикарбонат, бисульфит и карбоксилат, при условии, что, когда твердый материал представляет собой анионообменную смолу типа четвертичного аммония, а анион является бикарбонатом, способ осуществляют по существу в отсутствие диоксида углерода. В соответствии с этим документом наличие диоксида углерода в сырье является вредным для каталитической активности смол типа четвертичного аммония с обмененным бикарбонатом.
Как указано выше, в гомогенной системе, а также в гетерогенной системе, могут применяться соли, состоящие из каталитически активных анионов и катионов четвертичного аммония. Действительно, в гетерогенных системах такие ионы четвертичного аммония являются традиционно используемыми катионами большинства анионообменных смол. Недостатком, присущим этим соединениям четвертичного аммония, является их ограниченная термостойкость. При практическом осуществлении способа гидролиза алкиленоксида согласно WO 95/20559 с каталитическими композициями на основе традиционных органических ионообменников с четвертичным аммонием было установлено, что в жестких условиях гидролиза алкиленоксида (высокая температура и/или большой срок эксплуатации) имеется тенденция к ухудшению каталитической активности (селективность и/или степень превращения) и/или характеристики набухания традиционных катализаторов на основе смол.
В патенте США 4160116 (Showa Denko) описан способ получения алкиленгликоля путем гидратации алкиленоксида в присутствии значительного количества диоксида углерода с использованием соли четвертичного фосфония с йодом, бромом или хлором в качестве катализатора.
Сущность изобретения
Настоящее изобретение относится к способу получения алкиленгликолей путем взаимодействия алкиленоксидов с водой в присутствии по меньшей мере одной ионной композиции катиона четвертичного фосфония общей формулы
R1R2R3R4P+,
в которой каждый из R1, R2, R3 и R4 независимо может представлять собой алкильную, циклоалкильную, арильную, алкиларильную или арилалкильную группу, содержащую от 1 до 10 атомов углерода, каждая из которых может нести один или более заместителей или может быть присоединена к полимеру, и аниона, отличного от металата или галогена.
Предпочтительно анион выбирают из группы бикарбоната, бисульфита или производных карбоновой кислоты. Когда анион представляет собой карбоновую кислоту, его предпочтительно выбирают из группы формиата и цитрата.
Обычно диоксид углерода не требуется.
В предпочтительном варианте воплощения настоящего изобретения катион четвертичного фосфония иммобилизуют на твердом носителе, таком как анионообменная смола.
Подробное описание изобретения
Соединения четвертичного фосфония, определенные в изобретении как таковые, являются эффективными в качестве катализаторов гидролиза алкиленоксида в гомогенной жидкой реакционной системе. Однако особые преимущества этих соединений четвертичного фосфония проявляются, когда они применяются в гетерогенной реакционной системе, в которой катионы четвертичного фосфония представляют собой электроположительные центры твердого носителя, как определено в WO 95/20559. В частности, когда твердый носитель является сильно основной (щелочной) анионообменной смолой, основой которой является катион четвертичного фосфония согласно изобретению, образуется каталитическая композиция - с анионом согласно изобретению, - которая является стабильной и сохраняет свою селективность и стабильность в жестких реакционных условиях, а также обладает повышенной стойкостью к набуханию.
В качестве твердого носителя можно использовать любую смолу из большого числа ионообменных смол (ИОС), в частности сильно основные (анионные) ИОС, в которых основными группами являются группы четвертичного фосфония, присоединенные (т. е. адсорбированные, прореагировавшие или привитые) к основной цепи полимера. Подходящие основные цепи полимера включают полимеры и сополимеры с высокой молекулярной массой, например полимеры присоединения и конденсации, включая полиалкилены, полиэфиры, поликарбонаты, полиуретаны, формальдегидные смолы и др. Промышленно доступные ИОС включают смолы на основе полиакрилатных или стирол-дивинилбензольных сополимеров (ПС/ДВБ). Многие из этих ИОС являются чисто органическими полимерами, но также можно удобно использовать смолы на основе диоксида кремния, такие как полисилоксаны. Альтернативные материалы, имеющие электроположительные комплексообразующие центры типа четвертичного фосфония, присоединенные посредством адсорбции, реакции или прививки, включают материалы неорганической природы, такие как углерод, диоксид кремния, диоксид кремния - оксид алюминия, цеолиты, стекло и глины, такие как гидротальцит.
Каталитическая композиция согласно изобретению может быть завершена иммобилизацией каталитически активного аниона на твердом носителе добавлением его водного раствора в суспензию твердого носителя, который может быть необязательно приспособлен в вышеуказанной стадии приготовления. Например, когда твердый носитель представляет собой анионообменную смолу, иммобилизация может быть проведена в одну стадию смешиванием смолы с катализатором в водной среде с последующей промывкой водой или альтернативно, в две стадии, сначала переводя смолу в ее гидроксильную форму обработкой гидроксидом, таким как водный раствор гидроксида натрия, и затем добавляя катализатор.
Алкиленоксиды, используемые в способе изобретения в качестве исходного материала, имеют традиционное определение, то-есть они являются соединениями, имеющими смежную оксидную (эпоксидную) группу в своих молекулах.
Особенно подходящими являются алкиленоксиды общей формулы
в которой радикалы R1-R4 независимо представляют собой атом водорода или необязательно замещенную алкильную группу, содержащую от 1 до 6 атомов углерода. Предпочтительно любая алкильная группа, представленная R1, R2, R3 и/или R4, имеет от 1 до 3 атомов углерода. В качестве заместителей могут присутствовать неактивные фрагменты, такие как гидроксильные группы. Предпочтительно R1, R2 и R3 являются атомами водорода и R4 представляет собой незамещенную С1-С3 алкильную группу, более предпочтительно все радикалы R1, R2, R3 и R4 являются атомами водорода.
Следовательно, примеры подходящих алкиленоксидов включают этиленоксид, пропиленоксид, 1,2-эпоксибутан, 2,3-эпоксибутан и глицидол. Особенное промышленное значение имеют этиленоксид и пропиленоксид.
Как упоминалось выше, выгодно осуществлять гидролиз алкиленоксидов без использования избыточных количеств воды. В способе согласно настоящему изобретению вполне приемлемыми являются количества воды в интервале от 1 до 15 молей на 1 моль алкиленоксида, причем предпочтительными являются количества воды в интервале от 1 до 6 молей на моль алкиленоксида. В способе по изобретению часто достигается уже высокая селективность по моноалкиленгликолю, когда подаются только 4 или 5 молей воды на моль алкиленоксида.
Способ по изобретению может осуществляться в периодическом режиме. Однако предпочтительно, чтобы способ осуществлялся непрерывно, в частности, в крупномасштабном варианте воплощения.
Такой непрерывный способ может быть осуществлен в реакторе с неподвижным слоем катализатора в восходящем или нисходящем потоке. Режим нисходящего потока является предпочтительным.
В реакторе могут поддерживаться изотермические, адиабатические или гибридные условия. Обычно изотермический реактор представляет собой реактор с кожухом или трубчатый реактор, главным образом многотрубчатого типа, в трубках которого содержится катализатор, а охлаждающий агент проходит между трубами. Адиабатический реактор не охлаждается, а поток продукта, покидающий реактор, может охлаждаться в отдельном теплообменнике.
В определенно выбранных условиях каталитическое превращение этиленоксида (ЭО) может быть неполным, в таком случае оставшийся ЭО может гидролизоваться термически в мертвом пространстве реактора ниже слоя катализатора. Поскольку данный термический гидролиз является менее специфичным в отношении моноэтиленгликоля, рекомендуется сокращать до минимума время пребывания жидкости в реакторе. Это может быть достигнуто путем заполнения выходной части реактора внутренней или инертной набивкой для того чтобы уменьшить его объем, и/или путем добавления инертного газа, такого как азот, в исходную реакционную смесь, причем реактор работает в так называемом режиме просачивающегося потока.
Для того чтобы получить соответствующие значения выхода в заданное время, рекомендуется осуществлять способ в условиях повышенной температуры и давления.
Подходящие значения температуры реакции обычно находятся в интервале от 80 до 200oС, причем температура в интервале от 90 до 150oС является предпочтительной. Обычно реакционное давление выбирают в интервале от 200 до 3000 кПа, предпочтительно от 200 до 2000 кПа. В условиях периодического способа выбранное реакционное давление преимущественно получают путем создания повышенного давления инертным газом, таким как азот. При необходимости можно использовать смеси газов, например, в определенных условиях выгодной является смесь диоксида углерода и азота.
Для того чтобы обеспечить любое набухание катализатора в процессе работы, преимущественно объем реактора может быть больше, чем объем размещенного в нем катализатора, например больше на 10 - 70 об.%.
В некоторых случаях, особенно при работе в режиме непрерывного потока, было установлено, что выгодно подвергать по меньшей мере часть, такую как примерно 30-60 вес.%, исходного потока алкиленоксида частичному термическому гидролизу в отсутствие катализатора до завершения каталитического гидролиза. Было обнаружено, что частичный гидролиз, даже в отсутствие катализатора, все еще является достаточно селективным по моноалкиленгликолю, хотя, с другой стороны, этот прием позволяет эффективно сэкономить катализатор.
Время от времени в любом процессе гидролиза оксида этилена может возникнуть проблема, состоящая в наличии небольших количеств аминов и/или фосфинов в качестве примеси в потоке продукта. Когда в качестве твердого носителя каталитического аниона используется сильно основная анионообменная смола согласно настоящему изобретению, ее основными группами являются группы четвертичного фосфония. Было найдено, что в ходе работы небольшие количества фосфинов могут выщелачиваться из смолы в поток продукта. Кроме того, в потоке продукта могут содержаться небольшие количества аминов, которые попадают из ингибиторов коррозии, добавленных в воду, используемую в данном способе. Хотя количество таких аминных и/или фосфиновых загрязнений, попадающих в конечный продукт, обычно является очень малым, они могут влиять на качество конечного продукта, так что может быть желательно поддерживать их содержание ниже определяемого уровня. Например, содержание триметиламина (ТМА) и/или диметиламина (ДМА) в конечном продукте может достигать вплоть до 10 ч. /млн. , хотя рыбный запах ТМА может определяться уже при столь низком содержании, как 1 ч./млрд.
Было найдено, что эффективным средством при удалении аминов и/или фосфинов, которые могут присутствовать в потоке продукта любого обычного процесса, в котором гидролизуется оксид этилена, включая способ настоящего изобретения, является использование защитного слоя, содержащего сильно кислотную ионообменную смолу, которая эффективно улавливает амины или фосфины. Сильно кислотные ионообменные смолы являются смолами сульфонового типа. Примерами промышленно доступных смол являются те, которые известны под торговыми марками Аmberlyst 15, Аmberjet 1500Н, Amberjet 1200Н, Dowex МSС-1, Dоwex 50W, Diаnоn SК1В, Lеwatit VР ОС 1812, Lewatit S 100 МВ и Lеwаtit S 100 G1. Эти сильно кислотные ионообменные смолы доступны в Н+-форме и в солевой форме, такой как Nа+-форма. Когда в защитном слое используется только Н+-форма сильно кислотной смолы, поток продукта после прохождения этого слоя может приобретать кислотность. При использовании смеси сильно кислотной ионообменной смолы в ее Н+-форме и солевой формы имеется то преимущество, что значение рН потока продукта остается близким к нейтральному.
Дополнительным преимуществом сильно кислотного защитного слоя является то, что любое количество оставшегося алкиленоксида, которое может еще присутствовать в потоке продукта, гидролизуется до алкиленгликоля, хотя и с меньшей селективностью по моноалкиленгликолю.
Для того чтобы подготовиться к истощению сильно кислотной ионообменной смолы в ходе работы, выгодно размещать защитный слой в двух или более отдельных емкостях.
Истощенную сильно кислотную ионообменную смолу можно регенерировать посредством обработки кислотой, которая является более сильной, чем группы сульфоновой кислоты в матрице смолы, такой как соляная и серная кислота. Оказалось, что горячая серная кислота с нормальностью 0,1-2 является эффективной.
Следующие ниже примеры будут иллюстрировать изобретение.
Примеры .
1. Приготовление катализаторов
1.1. Гомогенные бикарбонатные катализаторы
Соль четвертичного фосфония и аналогичная соль четвертичного аммония (для сравнения) в гидроксидной форме использовали в качестве предшественников для исследуемых бикарбонатных катализаторов:
- гидроксид тетра-н-бутилфосфония (н-С4Н9)4Р+ОН-;
- гидроксид тетра-н-бутиламмония (н-С4Н9)4N+ОН-.
Эти основания до использования были превращены в бикарбонатные соли перемешиванием в течение ночи под давлением диоксида углерода 1000 кПа:
ОН-+СО2-->НСО3 -/
1.2. Катализаторы на основе сильно основной ИОС
Сильно основную ионообменнуюя смолу типа четвертичного фосфония (трибутилметилфосфонийбромид на полимерном носителе полистирол/1% дивинилбензол от фирмы Fluka, хлоридная форма, обменная емкость 0,9 мг-экв./г) обрабатывали следующим образом для того, чтобы получить бикарбонатный катализатор:
- сухую смолу (25 г) перемешивают в течение 20 ч с 250 мл деминерализованной воды и 18,9 г (10-кратный молярный избыток) бикарбоната натрия (NаНСО3), после фильтрации эту процедуру повторяют три раза,
- после обмена смолу промывают 1200 мл воды в течение 2 ч до отсутствия реакции на хлорид (с помощью АgNО3) в промывной воде.
Сильно основную ионообменную смолу типа четвертичного фосфония (ЕGL-660, монодисперсная сшитая полистирол/дивинилбензольная смола от фирмы Rohm & Нааs, хлоридная форма, обменная емкость 1,7 мг-экв/г) обрабатывают следующим образом для того, чтобы получить формиатный катализатор:
- влажную смолу (100 г, 50 вес.%) суспендируют в стеклянной трубке (60 х 2,5 см), заполненной водой,
- хлорид обменивают обработкой 122,4 г формиата натрия в водном растворе (10-кратный молярный избыток, в 2500 г воды) приблизительно в течение 5 ч при среднечасовой скорости подачи жидкости (СЧСПЖ) 4 л/ч,
- после обмена смолу промывают 1200 мл воды в течение 2 ч при СЧСПЖ 4 л/ч, до отсутствия реакции на хлорид (с помощью АgNО3) в промывной воде.
Сильно основную ионообменную смолу типа четвертичного аммония (торговая марка Аmberjet 4200, монодисперсная сшитая полистирол/дивинилбензольная [ПС/ДВБ] смола от фирмы Rоhm & Нааs, хлоридная форма, обменная емкость 1,4 мг-экв/г) обрабатывают следующим образом для того, чтобы получить бикарбонатный или формиатный катализатор для сравнения:
- влажную смолу (150 мл) суспендируют в стеклянной трубке (60 х 2,5 см), заполненной водой,
- хлорид обменивают обработкой 176,4 г бикарбоната натрия или 151,2 г формиата натрия в водном растворе (10-кратный молярный избыток, в 2500 г воды) приблизительно в течение 5 ч при СЧСПЖ 4 л/ч,
- после обмена смолу промывают 1200 мл воды в течение 2 ч при СЧСПЖ 4 л/ч, до отсутствия реакции на ион хлора (с помощью АgNО3) в промывной воде.
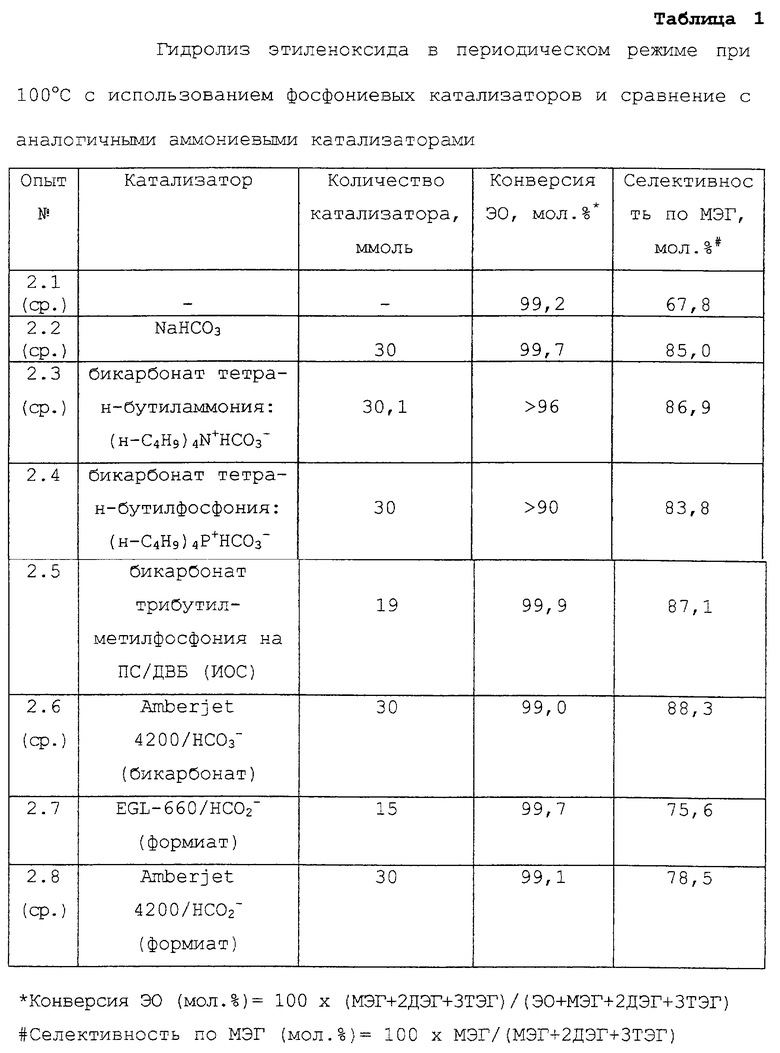
2. Реакция гидролиза этиленоксида при 100oС в периодическом режиме
Автоклав на 250 мл заполняют соответствующим катализатором (30 ммоль) и водой (100 г, 5,55 моль). Газовую "шапку" продувают 3 раза азотом и устанавливают начальное давление азота 1000 кПа. В опытах 2.3 и 2.4 смесь перемешивают в течение ночи при комнатной температуре в атмосфере диоксида углерода. Во всех случаях смесь нагревают до 100oС. При перемешивании (500 об/мин) медленно добавляют этиленоксид (ЭО) (44 г, 1 моль). Реакционную смесь выдерживают в течение 6 ч при реакционной температуре и непрерывном перемешивании. После охлаждения до комнатной температуры (20oС) перемешивание продолжают в течение ночи и в конце опыта отбирают пробу для газо-жидкостной хроматографии (ГЖХ).
В таблице 1 обобщены результаты опытов каталитического гидролиза этиленоксида в периодическом режиме, с точки зрения конверсии ЭО и селективности по моноэтиленгликолю (МЭГ), при использовании катализаторов фосфониевого типа в бикарбонатной форме и результаты сравнительных экспериментов (без катализатора, с NаНСО3, с Amberjet 4200/бикарбонатом и с двумя тетраалкиламмонийбикарбонатными катализаторами).
Эти результаты показывают, что фосфоний/бикарбонатные катализаторы (как гомогенные, так и на полистирол/ дивинилбензольной матрице) имеют весьма привлекательные каталитические свойства по показателю селективности по МЭГ (83,8 и 87,1% соответственно). Эта характеристика очень похожа на характеристику других катализаторов бикарбонатного типа.
3. Испытание стабильности катализатора
Для того чтобы сравнить термическую стабильность соединений четвертичного фосфония с аналогичным соединением четвертичного аммония, эти соединения были исследованы в гидроксидной форме, поскольку такие гидроксиды более чувствительны к термическому разложению, чем соответствующие бикарбонатные формы.
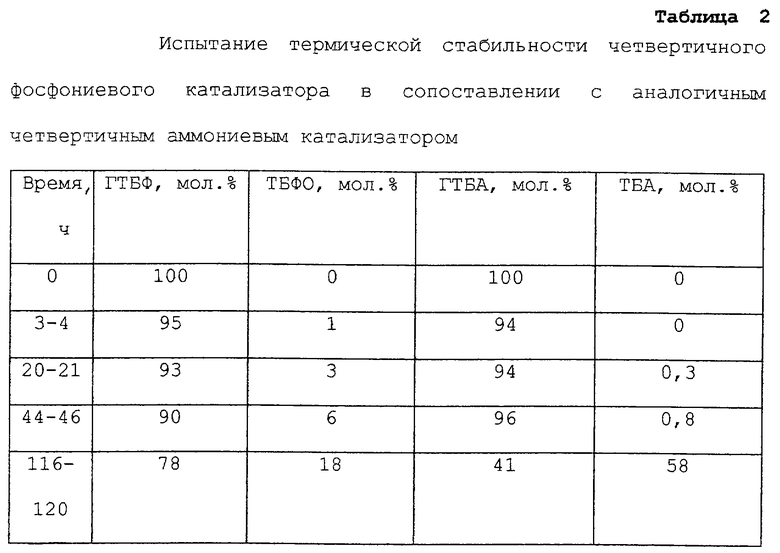
Термическую стабильность гидроксида тетрабутилфосфония (ГТБФ) оценивали и сравнивали с термической стабильностью гидроксида тетрабутиламмония (ГТБА). Данные гидроксиды (в виде 40%-ного водного раствора) выдерживали при 100oС в автоклаве в течение нескольких суток. В определенные моменты времени отбирали пробы для анализа. Разложение четвертичных оснований определяли методом спектроскопии ядерного магнитного резонанса (ЯМР), используя изотоп углерода-13 (13С-ЯМР) для аммониевых соединений и изотоп фосфор-31 (31Р-ЯМР) для фосфониевых соединений.
Анализ методом ЯМР показал, что продуктом термического разложения гидроксида четвертичного аммония (ГТБА) является три-н-бутиламин (ТБА) и что продуктом термического разложения гидроксида четвертичного фосфония (ГТБФ) является три-н-бутилфосфиноксид (ТБФО).
Результаты этих исследований стабильности обобщены в таблице 2.
Эти результаты показывают, что термическая стабильность соединения четвертичного фосфония значительно выше термической стабильности аналогичного соединения четвертичного аммония.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ И КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1999 |
|
RU2233261C2 |
| СПОСОБ ГИДРОЛИЗА АЛКИЛЕНОКСИДОВ С ИСПОЛЬЗОВАНИЕМ ДОБАВКИ, СТАБИЛИЗИРУЮЩЕЙ КАТАЛИЗАТОР | 1999 |
|
RU2230728C2 |
| КАТАЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЯ С РЕЦИКЛОМ РЕАКТОРНОГО ПРОДУКТА | 2001 |
|
RU2267478C2 |
| ТВЕРДЫЙ КАТАЛИЗАТОР, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРЕВРАЩЕНИЯ АЛКИЛЕНОКСИДА В АЛКИЛЕНГЛИКОЛЬ | 2008 |
|
RU2470706C2 |
| КАТАЛИТИЧЕСКИЙ ГИДРОЛИЗ АЛКИЛЕНОКСИДОВ | 1998 |
|
RU2203879C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 1998 |
|
RU2211211C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 2008 |
|
RU2467995C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЯ | 2008 |
|
RU2467996C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 2006 |
|
RU2410370C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 1999 |
|
RU2149864C1 |
Изобретение относится к способу получения алкиленгликолей, в частности моноалкиленгликолей, которые используются в композициях антифризов в качестве растворителей и в качестве основных материалов при получении полиалкилентерефталатов, например, для волокон или бутылок. Способ осуществляется путем взаимодействия алкиленоксида общей формулы  , где R1-R4 независимо представляют собой атом водорода или необязательно замещенную алкильную группу, содержащую от 1 до 6 атомов углерода, с водой в присутствии по меньшей мере одной ионной композиции катиона четвертичного фосфония общей формулы R1R2 R3R4Р+, в которой каждый из R1, R2, R3, R4 независимо может представлять собой алкильную, циклоалкильную, арильную, алкиларильную или арилалкильную группу, содержащую от 1 до 10 атомов углерода, и аниона, выбранного из группы бикарбоната, бисульфита и анионов карбоновых кислот. Способ позволяет проводить процесс без использования большого избытка воды с высокой термической стабильностью четвертичного фосфониевого катализатора. 3 з.п. ф-лы, 2 табл.
, где R1-R4 независимо представляют собой атом водорода или необязательно замещенную алкильную группу, содержащую от 1 до 6 атомов углерода, с водой в присутствии по меньшей мере одной ионной композиции катиона четвертичного фосфония общей формулы R1R2 R3R4Р+, в которой каждый из R1, R2, R3, R4 независимо может представлять собой алкильную, циклоалкильную, арильную, алкиларильную или арилалкильную группу, содержащую от 1 до 10 атомов углерода, и аниона, выбранного из группы бикарбоната, бисульфита и анионов карбоновых кислот. Способ позволяет проводить процесс без использования большого избытка воды с высокой термической стабильностью четвертичного фосфониевого катализатора. 3 з.п. ф-лы, 2 табл.
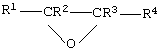
где R1-R4 независимо представляют собой атом водорода или необязательно замещенную алкильную группу, содержащую от 1 до 6 атомов углерода,
с водой в присутствии по меньшей мере одной ионной композиции катиона четвертичного фосфония общей формулы R1R2R3R4P+ в которой каждый из R1, R2, R3, R4 независимо может представлять собой алкильную, циклоалкильную, арильную, алкиларильную или арилалкильную группу, содержащую от 1 до 10 атомов углерода, и аниона, выбранного из группы бикарбоната, бисульфита и анионов карбоновых кислот.
| БРОНИРОВАННАЯ САНИТАРНО-ЭВАКУАЦИОННАЯ СОЧЛЕНЕННАЯ МАШИНА | 1995 |
|
RU2086894C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕНГЛИКОЛЕЙ | 0 |
|
SU267618A1 |
| US 4160116 А, 03.07.1979 | |||
| WO 9520559 A1, 03.08.1995 | |||
| 0 |
|
SU160330A1 | |
Авторы
Даты
2004-01-27—Публикация
1999-12-13—Подача