Изобретение относится к медицинской микробиологии и может быть использовано для профилактики и лечения геморрагического энтероколита.
С середины 90-х годов в мире регистрировались вспышки заболевания геморрагическим энтероколитом (ГЭ), вызываемые энтеропатогенными штаммами Е. coli варианта О157:Н7, продуцирующими веротоксин (ВТЕК). Эти штаммы вызывают геморрагический колит, часто осложненный гемолитическим уремическим синдромом. Летальность при таких вариантах ГЭ составляет от 3 до 7.7%. Традиционная антибиотикотерапия малоэффективна и во многих случаях приводит лишь к ухудшению состояния больных [1, 2, 3].
Известно, что для профилактики, лечения и коррекции микроэкологических нарушений при острых и хронических заболеваниях и дисфункциях желудочно-кишечного тракта используют пробиотики (эубиотики): Бифидумбактерин, Лактобактерин, Колибактерин, Бификол, Биофлор, Биоспорин и др. [4, 5]. Однако до настоящего времени отсутствует достаточная ясность представлений о степени эффективности бактериальной терапии при лечении геморрагических энтероколитов, вызываемых вновь выявленным штаммом Е. coli О157:Н7 [6,7].
Наиболее близким изобретением к патентуемому является способ лечения и профилактики геморрагического энтероколита у скота, вызываемого бактериями штамма Escherichia coli О157:H7. Лечение проводят пробиотиками, выделенными от животных, для этой цели применены: Е. coli 271 АТСС 202020, Е. coli 786 АТСС 202018, Е. coli 797 АТСС 202019 (US 5965128 A, Doyle et al, 12.10.1999; WO 99/08532 A1, 25.02.1999). Однако данные пробиотики могут быть использованы только в ветеринарии и не являются медицинскими лекарственными средствами. В связи с этим изучение лечебной эффективности пробиотиков в практике здравоохранения является актуальным и своевременным. Таким образом, арсенал лекарственных препаратов, используемых при лечении и профилактике геморрагического энтероколита, может быть значительно расширен за счет бактериальных препаратов - колисодержащих пробиотиков, а также пробиотиков других групп микроорганизмов.
Технический результат изобретения состоит в расширении арсенала лекарственных средств, используемых при лечении инфекции, вызываемой энтерогеморрагическими штаммами Escherichia coli О157:Н7.
Технический результат изобретения состоит в том, что в качестве пробиотиков при инфекции, индуцированный в эксперименте на животных, используют препараты на основе штаммов Bacillus subtilis 3 и Bacillus licheniformis 31 или Escherichia coli M-17 или Lactobacteria plantarum 8P-3A, или рекомбинатные штаммы Escherichia coli M-17/p Colap или Escherichia coli M-17 fim H: : Kan/p Colap, которые вводят один раз в сутки в течение 4-5 дней.
Способ по п. 1, отличающийся тем, что препарат "Биоспорин" на основе штаммов Bacillus subtilis 3 и Bacillus licheniformis 31 вводят в дозе 1•106-1•109 КОЕ.
Способ по п.1, отличающийся тем, что препарат "Колибактерин" на основе штамма Escherichia coli М-17 вводят в дозе 1,2•107-1,2•1010 КОЕ.
Способ по п.1, отличающийся тем, что препарат "Биофлор" на основе штамма Escherichia coli М-17 вводят в дозе 2,2•103-3•106 КОЕ.
Способ по п.1, отличающийся тем, что препарат "Лактобактерин" на основе штамма Lactobacteria plantarum 8P-3A вводят в дозе 5•106-5•109 КОЕ.
Способ по п. 1, отличающийся тем, что рекомбинантный штамм Escherichia coli М-17/p Colap вводят в дозе 1•107-1•1010 КОЕ.
Способ по п. 1, отличающийся тем, что рекомбинантный штамм Escherichia coli М-17 fim H::Kan/p Colap вводят в дозе 1•107-1•1010 КОЕ.
Существо изобретения поясняется приведенными ниже примерами и фигурами.
В работе использованы пробиотики, являющиеся фармакопейными препаратами: Колибактерин, Биоспорин, Лактобактерин (производство России), Биофлор (производство Израиля), а так же пробиотические рекомбинантные штаммы Е. coli (не фармакопейные) по окончании инкубации. Упомянутые препараты и штаммы имеют следующие особенности:
- Колибактерин содержит лиофильно высушенную биомассу живых бактерий штамма E.coli M-17;
- в состав Лактобактерина входят лиофильно высушенные живые бактерии штамма Lactobacteria plantarum 8P-3A;
- Биоспорин представляет собой лиофильно высушенную биомассу живых бактерий штамма Bacillus subtilis 3 и Bacillus licheniformis 31;
- Биофлор представляет собой суспензию живых клеток штамма E.coli М-17, растительные экстракты (мяты, свеклы, капусты, петрушки, укропа, чеснока, сои), экстракт прополиса и микроэлементы;
- рекомбинантный штамм Escherichia coli М-17/р Colap (RU 2144954 C1, C 12 N 1/21, A 61 K 35/74, оп. 27.01.2000) (не фармакопейный), обладает повышенной антагонистической активностью и устойчивостью к умеренным дозам антибиотиков пенициллинового ряда по сравнению с исходным штаммом Escherichia coli М-17;
- рекомбинантный штамм Escherichia coli М-17 fim Н:: Kan/p Colap, заявленный в патенте (RU 2144953 C1, C 12 N 1/21, A 61 K 35/74, оп. 27.07.2000) (не фармакопейный), обладает повышенной антагонистической активностью, сниженной способность к колонизации, отличной от первичной интестинальной ниш в мароорганизме и устойчивостью к умеренным дозам антибиотиков пенициллинового ряда по сравнению с исходным штаммом Escherichia coli М-17.
Существо изобретения поясняется опытами in vitro и in vivo.
А. Антагонистическая активность пробиотиков в опыте in vitro
При изучении антагонистической активности пробиотиков в отношении 26 тест-штаммов E. coli О157: H7 в опытах in vitro использовали методику отсроченного антагонизма [8]. Пробиотические препараты (Колибактерин, Лактобактерин, Биофлор, Биоспорин) растворяли 1 мл 0,9% р-ра NaCl на 1 дозу или 1 мл. Рекомбинантные штаммы (Escherichia coli М-17/р Colap, Escherichia coli М-17 fim Н: : Kan/p Colap) выращивали на целлофановой пленке на чашках со средой Гаузе 2 в течение 24 ч при 37oС, затем смывали культуру 0,9% р-ром NaCl и доводили до концентрации 10•109. Использованы 26 тест-штаммов E.coli О157:H7. Тест-штаммы подготавливали аналогично рекомбинантным штаммам.
На подсушенные чашки Петри со средой Гаузе 2 по диаметру петлей 3,5±0,5 мм высевали штрихом пробиотик. Посевы инкубировали в термостате при 37±1oС в течение 72 ч. Затем, отступив на 1 мм от выросшей культуры, перпендикулярным штрихом подсевали тест-штаммы Е. coli О157:H7. Учет результатов проводили через 18 ч инкубирования при 37±1oС. Об антагонистической активности судили по величине зон угнетения роста тест-штаммов, в мм.
Б. Защитная активность пробиотиков в опытах in vivo.
Сущность эксперимента поясняется тремя примерами.
Пример 1
При изучении защитной активности пробиотиков in vivo использовался отобранный в предварительных экспериментах штамм E.coli О157:Н7 212, заражающая однократная доза которого при введении внутрибрюшинно составляла 1•109 КОЕ/0,5 мл.
В предварительных экспериментах по отработке заражающей дозы (LD50) E. coli О157: H17 было установлено, что данная инфекция лучше моделируется на животных с экспериментальным дисбактериозом. Дисбактериоз вызывали, используя методику интрагастрального введения ампиокса [9]. Ежедневно в течение 14 суток для того, чтобы вызвать дисбактериоз животным перорально вводили антибиотик в дозе 4 мг в 0,5 мл один раз в сутки, введение антибиотика прекращали за 1 сутки до введения культуры E.coli О157:Н7 штамма 212. Животные получали пробиотик (Колибактерин или Лактобактерин или Биофлор или Биоспорин или Escherichia coli M-17 fim H:: Kan/p Colap или Escherichia coli М-17/p Colap) per os в двух дозировках (человеческая доза или мышиная доза) 1 раз в сутки параллельно с антибиотиком за 5 дней до заражения. Колибактерин, Лактобактерин и Биоспорин растворяли 0,5 мл 0,9% р-ра NaCl на 1 дозу. "Человеческая" доза жидкого препарата Биофлор содержится в 1 мл. Рекомбинантные штаммы (Escherichia coli М-17/p Colap, Escherichia coli М-17 fim H:: Kan/p Colap) выращивали на целлофановой пленке на чашках со средой Гаузе 2 в течение 24 ч при 37oС, затем смывали культуру 0,9% р-ром NaCl и доводили до необходимой концентрации. "Мышиные" концентрации пробиотиков готовили из человеческих посредством разведений. Таким образом животные получали пробиотики в следующих концентрациях:
Колибактерин - человеческая доза (ч.д.) содержит 1,2•1010 КОЕ/0,5 мл; доза мышиная (м.д.) - 1,2•107 КОЕ/0,5 мл.
Лактобактерин - человеческая доза (ч.д.) содержит 5•109 КОЕ/0,5 мл; доза мышиная (м.д.) - 5•106 KOE/0,5 мл.
Биоспорин - человеческая доза (ч.д.) содержит 1•109 КОЕ/0,5 мл доза мышиная (м.д.) - 1•106 КОЕ/0,5 мл.
Биофлор - человеческая доза (ч.д.) препарата содержит не менее 3•106 КОЕ/0,5 мл; доза мышиная (м.д.) - 2,2•103 КОЕ/0,5мл.
Escherichia coli М-17/p Colap - человеческая доза (ч.д.) содержит не менее 1•1010 КОЕ/0,5 мл; доза мышиная (м.д.) - 1•107 КОЕ/0,5 мл.
Escherichia coli М-17 fim H:: Kan/p Colap - человеческая доза (ч.д.) содержит не менее 1•1010 КОЕ/0,5 мл; доза мышиная (м.д.) - 1•107 КОЕ/0,5 мл.
В экспериментах были использованы беспородные мыши весом 10-15 г. Использованы две контрольные группы животных:
1-я контрольная группа: животные до заражения получали только антибиотик per os;
2-я контрольная группа: животные до и после заражения не получали ни каких препаратов.
Пример II
Аналогичен примеру I (схема эксперимента, дозировки пробиотиков, контрольные группы). Отличен тем, что животные получали пробиотик per os в двух дозировках (человеческая доза или мышиная доза) 1 раз в сутки в течение 5 дней, то есть в течение 2 дней до заражения и 3 дней после.
Пример III
Аналогичен примеру I (схема эксперимента, контрольные группы): животные получали пробиотик per os в одной (человеческой) дозировке 1 раз в сутки, спустя 1 день после заражения, в течение 4 дней.
Полученные результаты статистически обрабатывали параметрическим методом с вычислением средней вариационной величины.
На фиг.1 показана антогонистическая активность пробиотиков по отношению к патогенным штаммам Е.соli О157:Н7. Видно, что средний показатель антагонизма колисодержащих препаратов и рекомбинантных штаммов: Биофлора (23,5±2,50 мм), Колибактерина (24,4±2,80 мм), Escherichia coli М-17 fim H:: Kan/p Colap (23,4±2,8 мм), Escherichia coli М-17/р Colap (28,0±4,1мм) выше, чем у Биоспорина (13,1±2,30 мм), что характеризует их выраженную антагонистическую активность.
Однако следует отметить, что посевная доза Биофлора на четыре порядка ниже посевной дозы Колибактерина и Биоспорина, следовательно, культура Е.соli М-17, входящая в препарат Биофлор, проявляет более выраженную антагонистическую активность.
Были сопоставлены показатели антагонизма in vitro и in vivo, поскольку эффективность пробиотика проявляется именно в условиях живого организма.
На следующие сутки после заражения все выжившие животные были больными, вялыми, глаза закрыты, шерсть всклочена, дрожь в конечностях, диарея.
На вторые сутки животные, получавшие Биофлор и Биоспорин, чувствовали себя лучше, чем остальные мыши, получавшие пробиотики (диарея продолжается, мыши более активные, шерсть еще неопрятна), в 1 и 2 контрольных группах животные чувствовали себя плохо (были вялыми, шерсть всклочена, дрожь в конечностях, диарея).
На третьи сутки животные, получавшие биофлор и биоспорин, чувствовали себя хорошо, в других группах у животных отмечалось улучшение состояния (диарея прекратилась, мыши более активные), кроме 1-й контрольной группы (диарея продолжается, мыши более активные, шерсть еще неопрятна).
На четвертые и пятые сутки животные, получавшие пробиотики, и животные 2-й контрольной группы были практически здоровыми.
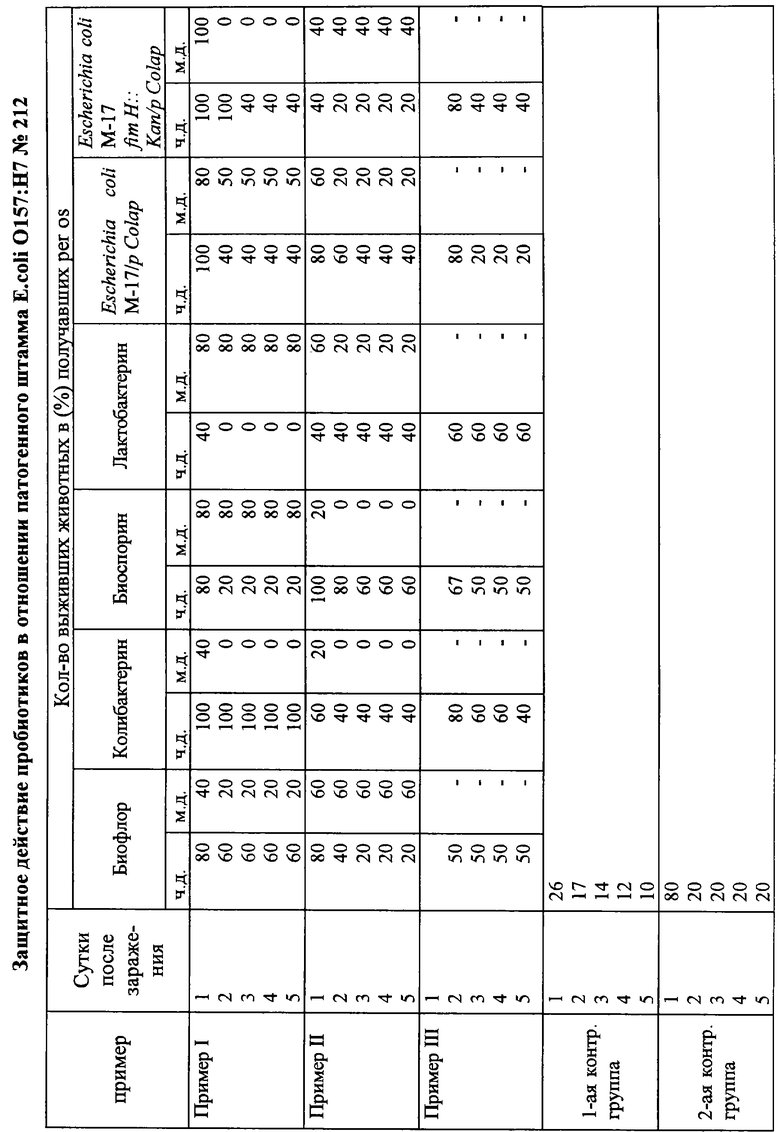
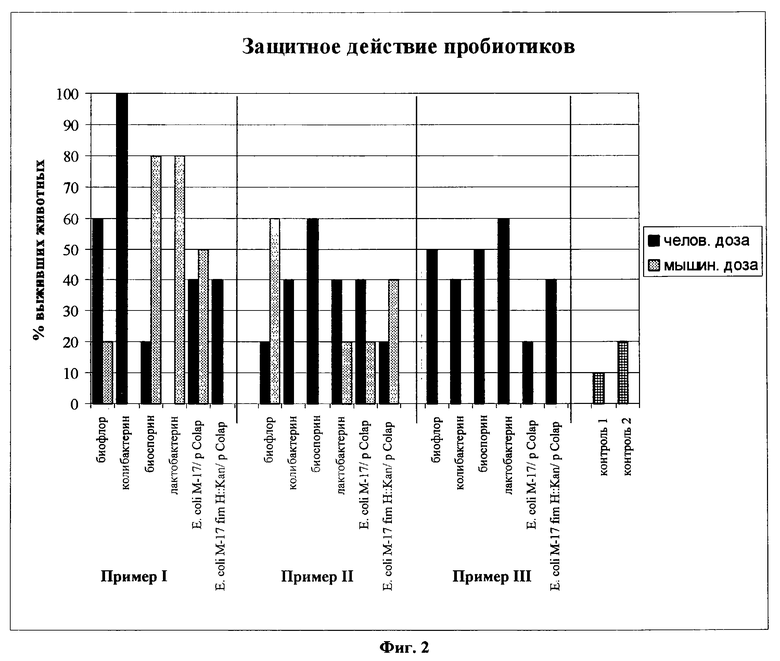
Данные исследований in vivo о защитном действии пробиотиков в отношении патогенного штамма Е.соli О157:Н7 212 представлены в таблице и на фиг.2. Из таблицы видно, что животные, получавшие Биофлор и Биоспорин, быстрее пришли в норму, в связи чем, не исключено, что данные пробиотические препараты обладают антитоксической эффективностью.
Видно, что лучше всего заражение перенесли животные из примера I, получавшие Колибактерин, Биоспорин и Лактобактерин, причем два последних препарата были эффективны в малых дозировках. Животные, получавшие препараты в больших дозировках, выжили в 100% случаев (для Колибактерина) и в 60% (для Биофлора); получавшие рекомбинантный штамм Escherichia coli M-17/p Colap в малой дозировке - в 50% случаев, что, возможно, свидетельствует о профилактической эффективности этих препаратов против инфекции, вызываемой патогенными E.coli О157. Из примера II видно, что эффективной оказалась "мышиная" дозировка Биофлора, тогда как "мышиная" дозировка Колибактерина была не эффективна. В примере III наблюдался 50 - и 60%-ный защитный эффект при приеме Биофлора, Биоспорина и Бактобактерина. Следует отметить, что количество живых микробов в человеческой дозе Биофлора на 4 порядка ниже, чем в Колибактерине, при этом "мышиная" доза Колибактерина превосходила человеческую дозу Биофлора на порядок. Возможно экстракты растительных веществ, входящие в состав Биофлора, стимулируют выработку Е.соli М-17 антибиотических веществ против патогенных Е.соli О157:Н7.
Таким образом, в опытах in vivo все используемые пробиотики были в различной степени эффективны и обладали выраженным профилактическим действием даже в минимальных дозировках.
Из полученных результатов в опытах in vivo и in vitro следует, что при инфекциях, вызываемых Е. соli О157:Н7, применение пробиотиков значительно снижает интоксикацию, обеспечивая протективный и терапевтический эффект.
Список литературы
1. Proulx F, Turgeon JP, Delage G, et al. Randomized controlled trial of antibiotic therapy for Escherichia coli О157:H7 enteritis. J Pediatr. 1992; 121:299-303.
2. Walterspiel JN, Ashkenazi S., Morrow AL., et al. Effect of subinhibitory concentrations of antibiotics on extracellular Shiga-like toxin I. Infection. 1992; 20:25-29.
3. Comite de maladies infectieuses et d'immunisation: Societe canadienne de pediatrie (SCP). L'Escherichia coli О157:H7, les autres colibacilles verotoxinogenes et le syndrome hemolytique et uremique chez l'enfant. de reference: ID95-03.
4. Машковский М.Д. Лекарственные средства, в 2 томах. Харьков, 1997.
5. Mack DR; Michail S.; Wei S.; McDougall L.; Hollingsworth M.A. Probiotics inhibit enteropathogenic E. coli adherence in vitro by inducing intestinal mucin gene expression. Am J Physiol, 276(4 Pt 1):G941-50 1999 Apr.
6. Tachikawa T. ; Seo G.; Nakazawa M.; Sueyoshi M.; Ohishi T.; Joh К. [Estimation of probiotics by infection model of infant rabbit with enterohemorrhagic Escherichia coli О157:H7]. Kansenshogaku Zasshi, 72(12):1300-5 1998 Dec.
7. Takahashi M.; Taguchi H., Yamaguchi H.; Osaki T.; Sakazaki R.; Kamiya S. [Antagonistic interaction between Clostridium butyricum and enterohemorrhagic Escherichia coli О157:H7]. Kansenshogaku Zasshi, 73(1):7-14 1999 Jan.
8. В.Г.Лиходед, M.Ю.Яковлев, Н.В.Лиходед с соавт. Состояние антиэндотоксинового иммунитета при экспериментальном кишечном дисбактериозе у мышей. ЖМЭИ.-1998.- 4.- с. 14-16.
9. И.Г.Чхаидзе, В.Г.Лиходед, M.В.Лиходед с соавт. Корректирующее действие антител при экспериментальном кишечном дисбактериозе. /ЖМЭИ. - 1998. - 14. С.12-14.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ СПЕЦИФИЧЕСКОЙ АКТИВНОСТИ ПРЕПАРАТОВ ПРОБИОТИКОВ РАЗЛИЧНЫХ ЛЕКАРСТВЕННЫХ ФОРМ И ПРОИЗВОДСТВЕННЫХ ШТАММОВ ПО УРОВНЮ ИХ АДГЕЗИВНОЙ АКТИВНОСТИ | 2003 |
|
RU2247570C2 |
| ШТАММ БАКТЕРИЙ Escherichia coli M 17 fimH::kan/p Colap, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 1998 |
|
RU2144953C1 |
| ШТАММ БАКТЕРИЙ Escherichia coli M 17/p Colap, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ПРОБИОТИЧЕСКОГО ПРЕПАРАТА | 1998 |
|
RU2144954C1 |
| БИОПРЕПАРАТ-СУБТИКОЛ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ | 1998 |
|
RU2129432C1 |
| БИОПРЕПАРАТ "ИРИЛИС" НА ОСНОВЕ БАКТЕРИЙ РОДА BACILLUS ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ И ДИСБИОЗА РАЗЛИЧНОЙ ЭТИОЛОГИИ И ШТАММЫ БАКТЕРИЙ BACILLUS SUBTILIS И BACILLUS LICHENIFORMIS, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИЗГОТОВЛЕНИЯ БИОПРЕПАРАТА | 2003 |
|
RU2264454C2 |
| БИОПРЕПАРАТ "ИРИЛИС" ВЕТЕРИНАРНОГО НАЗНАЧЕНИЯ | 2003 |
|
RU2264453C2 |
| ПРОБИОТИК ДЛЯ ПРОФИЛАКТИКИ И КОРРЕКЦИИ ЖЕЛУДОЧНО-КИШЕЧНЫХ ЗАБОЛЕВАНИЙ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ И ПТИЦЫ | 2022 |
|
RU2785174C1 |
| СПОСОБ ЛЕЧЕНИЯ МИКОТИЧЕСКИХ ИНФЕКЦИЙ И ПРЕПАРАТ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2009 |
|
RU2401115C1 |
| Штамм бактерий Escherichia coli С41для получения пробиотического препарата для профилактики колибактериоза сельскохозяйственных животных | 2023 |
|
RU2807738C1 |
| СПОСОБ КОРРЕКЦИИ КИШЕЧНОГО МИКРОБИОЦЕНОЗА | 2014 |
|
RU2562539C1 |
Изобретение относится к медицинской микробиологии и может быть использовано для профилактики и лечения инфекции, вызываемой энтеропатогенными штаммами Escherichia coli. О157: Н7. Способ состоит в том, что при инфекции, индуцированной в эксперименте на животных, используют препараты на основе штаммов Bacillus subtilis 3 и Bacillus licheniformis 31, или Escherichia coli M-17, или Lactobacteria plantarum 8P-3A, или рекомбинантные штаммы Escherichia coli M-17/ p Colap или Escherichia coli M-17 fim H:: Kan/ p Colap, которые вводят один раз в сутки в течение 4-5 дней. Способ обеспечивает протективный и терапевтический эффект при снижении интоксикации организма животного. 6 з.п.ф-лы, 1 табл., 2 ил.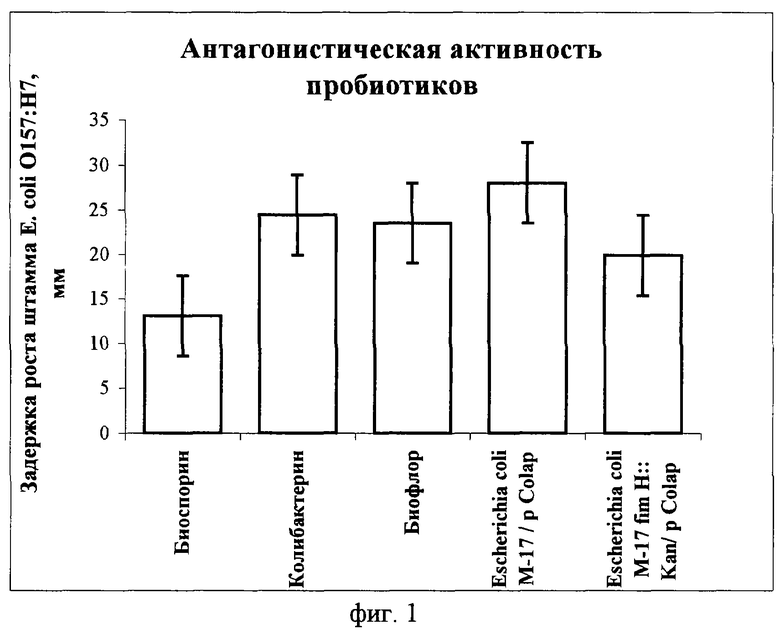
| US 5965128 A, 12.10.1999 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСЛОЖНЕНИЙ У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ С ХРОНИЧЕСКИМ СЕПТИЧЕСКИМ ЭНДОКАРДИТОМ | 1997 |
|
RU2144367C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДИАРЕИ У ДЕТЕЙ С ХРОНИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ ТОНКОЙ КИШКИ | 1997 |
|
RU2138278C1 |
| ГРАЧЕВА Н.М | |||
| и др | |||
| Эффективность нового бактерийного препарата - биоспорин при лечении острых кишечных инфекций | |||
| Журнал микробиологии, эпидемиологии и иммунобиологии, 1996, № 1, с | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
| МАШАРОВА А.А | |||
| и др | |||
| Клиническая эффективность нового эубиотика биофлора при лечении дисбактериоза различного генеза | |||
| Клиническая фармакология и терапия, 1999, 8, № 2, с | |||
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
Авторы
Даты
2004-03-10—Публикация
2000-06-29—Подача