Изобретение относится к области синтеза материалов, которые находят применение в качестве катализаторов тонкого органического синтеза, а именно к усовершенствованному способу получения титан-силикатного катализатора для процессов селективного окисления органических соединений пероксидом водорода.
Органические кислородсодержащие соединения являются ценными продуктами и интермедиатами тонкого органического синтеза. До недавнего времени основным способом их промышленного получения было стехиометрическое, “экологически грязное” окисление такими реагентами, как двуокись марганца, перманганат и бихромат калия, азотная кислота и др. При стехиометрическом окислении используются большие количества дорогих и токсичных окислительных агентов и неизбежно возникают проблемы, связанные с утилизацией токсичных отходов. В последние 10 лет наметилась тенденция замещения традиционных стехиометрических способов каталитическими, которые гораздо более приемлемы как с точки зрения экологии, так и экономики. Наибольший интерес представляют каталитические способы получения кислородсодержащих соединений, основанные на использовании в качестве окислителя молекулярного кислорода и пероксида водорода, поскольку оба эти окислителя являются экологически чистыми и недорогими. Хотя стоимость пероксида водорода выше, чем стоимость кислорода, в малотоннажных процессах тонкого органического синтеза использование первого окислителя часто оказывается предпочтительней, поскольку стоимость технологического оборудования для окисления Н2О2 в целом ниже, чем для окисления кислородом, которое, как правило, ведут при повышенных температурах и давлениях [R.A.Sheldon, J.Dakka. Heterogeneous catalytic oxidations in the manufacture of fine chemicals. Catalysis Today 19 (1994) 215].
Окисление молекулярным кислородом при “комнатных условиях” остается наиболее предпочтительным, однако до сих пор такой процесс представляется не осуществимым. Поэтому все более популярным становится использование второго “зеленого” окислителя - Н2O2, который называют “восходящей химической звездой” и “идеальным окислителем”, поскольку единственным образующимся из него побочным продуктом является вода, а по процентному содержанию кислорода в молекуле Н2О2 стоит на втором месте после молекулярного кислорода. На сегодняшний день лучшими гетерогенными катализаторами для жидкофазного окисления органических соединений пероксидом водорода являются микропористые титан-силикалиты TS-1 и TS-2 [ЕР 100119, B 01 J 29/04, 23.05.89; US 4410501, C 01 B 33/20, 1983; GB 2116974, С 07 С 37/60, 1983]. Процесс окисления фенола H2O2 на TS-1 коммерциализован фирмой Enichem в 1986 году; в настоящее время с помощью этого процесса производится около 10000 тонн в год гидрохинона и пирокатехина. Главным недостатком TS-1 является малый диаметр пор (0.56 нм), что делает невозможным превращения крупных молекул. Имеется целый ряд попыток создания мезопористых молекулярных сит (Ti-MCM-41, Ti-HMS, Ti-MMM и др.), а также аморфных смешанных титан-кремниевых оксидов и их использования в процессах селективного окисления крупных молекул [US 5783167, C 01 B 33/20, 1998; US 5712402, С 07 С 50/02, 1998; US 5855864, C 01 B 033/26, 1999; US 5935895, B 01 J 23/00, 1999; Патент РФ N 2164510, С 07 С 46/06, 2000].
В настоящее время наибольшее число синтезов силикатных и элемент-силикатных мезоструктурированных мезопористых материалов (МСМ-41, МММ и др.) проводят по реакционному пути S+I-, в котором создаются условия для электростатического взаимодействия катионов ПАВ (S+) и анионных форм диоксида кремния (I-) [S.Biz, M.L.Occelli, Catal. Rev.-Sci. Eng, 40(3) (1998) 329; US 5783167, C 01 B 33/20, 1998]. Формирование этих материалов происходит в щелочных средах, при этом, по крайней мере, часть атомов кислорода неорганической стенки материала имеет отрицательный заряд, что обеспечивает взаимодействие с катионом ПАВ. В отличие от электронейтральных SiOH-групп, такие заряженные атомы кислорода не в состоянии образовывать силоксановые связи Si-O-Si при конденсации в процессе гидротермальной обработки и являются причиной возникновения разрывов (понижения электронной плотности) в силикатных стенках, что приводит к блочному типу построения системы, следствием которого является низкая гидролитическая стабильность получаемых материалов [В.Н.Романников, С.Д.Кирик, Л.А.Соловьев, А.Н.Шмаков, А.Ю.Деревянкин, В.Б.Фенелонов, Н.Н.Трухан, О.А.Холдеева, О.Б.Лапина, Е.А.Паукштис. Физико-химические свойства мезопористых мезофазных силикатных материалов, сформированных по механизму S+I-. Кинетика и катализ, 2001, т.42, N6, с.1-10]. В свою очередь следствием низкой гидролитической стабильности является разрушение структуры катализатора в ходе процессов жидкофазного окисления с использованием водного пероксида водорода, приводящее к потери активности катализатора при его многократном использовании [L.Y.Chen, G.К.Chuah, and S.Jaenicke. Ti-containing MCM-41 catalysts for liquid phase oxidaton of cyclohexene with aqueous H2O2 and tert-butyl hydroperoxide. Catal. Lett. 50 (1998) 107; O.A.Kholdeeva, N.N.Trukhan, M.P.Vanina, V.N.Romannikov, V.N.Parmon, 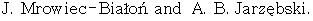 A New Environmentally Friendly Method for the Production of 2,3,5-trimethyl-p-benzoquinone. Catalysis Today, 2002, v.75, N 1-4, p.203]. Имеются попытки дополнительной стабилизации структуры материалов типа MCM-41 с использованием различных химических приемов, в частности путем добавки в процессе синтеза водорастворимых органических и неорганических солей, однако это приводит к потере мезоструктуры и образованию разупорядоченного материала [US 5958368, С 01 В 33/20, 1999].
A New Environmentally Friendly Method for the Production of 2,3,5-trimethyl-p-benzoquinone. Catalysis Today, 2002, v.75, N 1-4, p.203]. Имеются попытки дополнительной стабилизации структуры материалов типа MCM-41 с использованием различных химических приемов, в частности путем добавки в процессе синтеза водорастворимых органических и неорганических солей, однако это приводит к потере мезоструктуры и образованию разупорядоченного материала [US 5958368, С 01 В 33/20, 1999].
Известно формирование силикатных мезоструктурированных материалов при значениях рН, близких к 7 [US 5855864, C 01 B 033/26, 1999], которое в этом случае реализуется по реакционному пути S0I0 через ван-дер-ваальсовское взаимодействие электронейтральных ПАВ и незаряженных силикатных частиц. Однако, как установлено [Р.Т.Tanev, T.J.Pinnavaia, Mesoporous silica molecular sieves prepared by ionic and neutral surfactant templating: A comparison of physical properties. Chem. Mater., 8 (1996) 2068], уровень структурной организованности таких материалов очень низкий и, следовательно, эффективное управление каталитическими свойствами таких систем представляется затруднительным.
Известно формирование силикатных мезоструктурированных материалов в сильно кислых средах при значениях рН, как правило, от 1 и меньше [WO 9937705, C 08 J 9/00, 1999; Р.Т.Tanev, T.J.Pinnavaia. Chem. Mater., 8 (1996) 2068], которое может быть реализовано по реакционному пути S+X-I+, т.е. через электростатическое взаимодействие катионов ПАВ (S+) и электронейтральных частиц диоксида кремния с частично протонированными поверхностными силанольными группами (схематично I+=Н2O+Si(ОН)3), опосредованное через дополнительно введенные анионы (обычно X-=Сl-). В этом случае уровень организованности мезоструктуры и, следовательно, степень управляемости ее свойствами могут быть близки получаемым по простейшему ионному реакционному пути S+I-. Более того, гидростабильность таких материалов оказывается очень высокой [Y.H.Yue, A.Gedeon, J.-L.Bonardet, N.Melosh, J.-B.D'Espinose, J.Fraissard. Direct synthesis of A1SBA mesoporous molecular sieves: characterization and catalytic activities. J. Chem. Soc. Chem. Commun., (1999) 1967], поскольку частицы диоксида кремния, участвующие в формировании мезоструктуры, не содержат в своем составе жестко ионизированных атомов кислорода, препятствующих полной поликонденсации в силикатной стенке.
Таким образом, именно последний из описанных реакционных путей представляется наиболее перспективным для формирования мезоструктурированных каталитических систем на основе элемент-силикатов. Однако сильно кислые среды порождают проблемы, связанные с тем, что при введении гетероэлемента в такие системы [Y.Yue, A.Gedeon, J.-L.Bonardet, N.Melosh, J.-B.D'Espinose, J.Fraissard. Direct synthesis of AlSBA mesoporous molecular sieves: characterization and catalytic activities. J.Chem.Soc. Chem. Commun., (1999) 1967], последний практически не фиксируется в силикатной стенке и легко вымывается в условиях проведения жидкофазных реакций (имеет место так называемый личинг активного компонента). Проведение синтеза в щелочных средах по механизму S+I-, напротив, позволяет получить материал, устойчивый к личингу в условиях жидкофазного окисления пероксидом водорода [Патент РФ N 2164510, С 07 С 46/06, 2000; N.N.Trukhan, V.N.Romannikov, E.A.Paukshtis, A.N.Shmakov, O.A.Kholdeeva. Oxidation of 2,3,6-trimethylphenol over Ti- and V-containing mesoporous mesophase catalysts. Structure-Activity/Selectivity Correlation. J.Catal., 2001, v.202, N1, p.110], однако, как уже говорилось выше, структура силикатной стенки этих материалов разрушается в присутствии воды.
Наиболее близким к настоящему изобретению является способ получения мезопористых силикатных материалов, включающий приготовление водного раствора силиката натрия при рН>9, смешение этого раствора с кислым водным раствором неионного поверхностно-активного вещества (ПАВ) на основе амфифильного блок-сополимера полиоксиэтиленоксида (РЕО) таким образом, что рН смеси находится в пределах от 4 до 10, старение этой смеси при температуре от 0 до 150°С, добавление гетероэлемента и продолжение процесса старения, удаление растворителя и последующее удаление ПАВ экстракцией и/или прокаливанием [US Patent Appl. 20010043901, С 01 В 033/32, 2001].
Получаемые по этому способу материалы имеют разупорядоченную структуру мезопор близкого размера с диаметром от 1.5 до 30 нм, толщиной стенки между соседними порами >0.5 нм, удельной поверхностью 300-1400 м2/г, объемом пор 0.2-3.0 см3/г и обладают термостабильностью, однако об их гидростабильности в [US Patent Appl. 20010043901, С 01 В 033/32, 2001] ничего не сообщается. Согласно имеющимся в литературе представлениям формирование устойчивой к воздействию воды силикатной стенки мезопористого материала может осуществляться только в сильно кислой среде.
Изобретение решает задачу разработки способа приготовления мезопористых мезофазных титан-силикатных материалов, которые будут одновременно термогидростабильными и устойчивыми к вымыванию активного компонента (личингу).
Разработка таких материалов стоит на первом месте в ряду стратегических задач тонкого органического синтеза, ориентированного на использование водного пероксида водорода [W.R.Sanderson. Cleaner Industrial Processes using Hydrogen Peroxide. Pure and Appl. Chem. 72 (2000) 1289; I.W.С.Е.Arends, R.A.Sheldon. Activities and stabilities of heterogeneous catalysts in selective liquid phase oxidations: recent developments. Appl. Catal. A: General. 212 (2001) 175].
Поставленная задача достигается тем, что процесс формирования титан-силикатных мезоструктурированных материалов Ti-MMM-2 проводят в два этапа. На первом этапе готовят смесь, содержащую положительно заряженные гидроксокомплексы кремния, соединение титана и поверхностно-активное вещество (ПАВ), рН поддерживают в диапазоне 0.5-1.5. На втором этапе вводят порцию щелочного раствора таким образом, чтобы рН реакционной смеси поддерживался в диапазоне от 1,5 до 7.0. После этого смесь подвергают гидротермальной обработке, затем продукт отделяют фильтрованием, промывают, сушат и прокаливают.
В качестве соединения титана используют раствор солей титана (III) или (IV) в водной минеральной кислоте или раствор алкоксидов титана в органическом или водно-органическом растворителе или их смеси. В качестве кислоты используют НСl, НВr, Н2SO4, НСlO4, HNO3, Н3РO4 или их смеси. В качестве органического растворителя используют смешивающиеся с водой спирты C1-C12, кетоны, карбоновые кислоты, ацетонитрил.
Часть ионов титана в количестве от 1 до 99 мас.% может быть заменена на гетероэлементы, выбранные из ряда: Аl, В, Ga, Fe; Cr, Zr, Sn, Ge.
В качестве поверхностно-активного вещества используют алкилтриметиламмоний галогениды или гидроксиды общей формулы CnH2n+1(CH3)3NX, где n=12-18; Х=Сl, Вr, ОН, олигомерные алкилполиэтиленоксиды общей формулы CnH2n+1+EOm, где n=12-18; m=2-25, и олигомерные алкилполиэтиленоксиды и полиокси(алкиленоксид) блок-сополимеры или их смеси.
Мольное отношение кремния к титану берут в диапазоне 10-150. Мольное отношение кремния к поверхностно-активному веществу берут в диапазоне 0.2-100.
Гидротермальную обработку проводят при температуре 20-150°С в течение 0.2-120 часов.
Задача решается также способом осуществления процесса жидкофазного селективного окисления органических соединений пероксидом водорода в присутствии мезопористого титан-силикатного катализатора, приготовленного как описано выше.
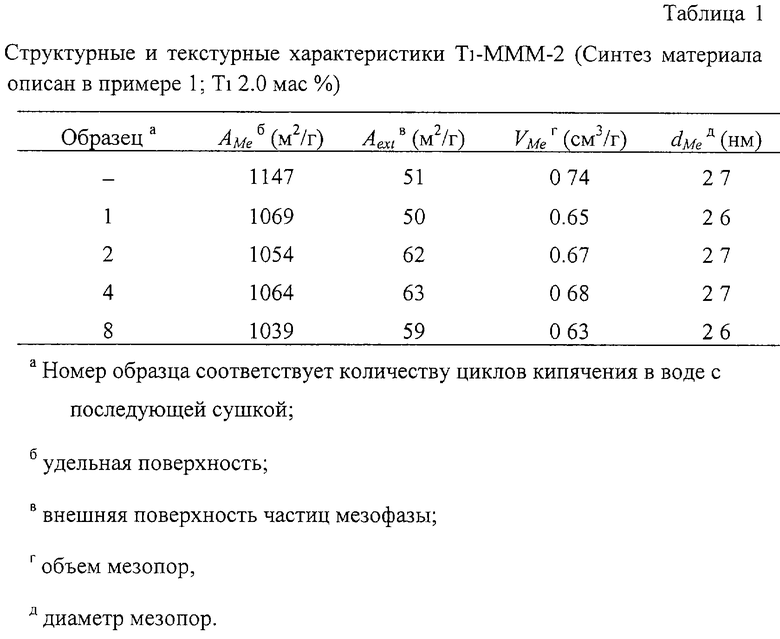
Использование предлагаемого способа позволяет получить организованные мезопористые мезофазные титан-силикатные катализаторы. На Фиг.1 представлено электронно-микроскопическое изображение материала Ti-MMM-2, имеющего диаметр мезопор около 2.5 нм, толщину силикатной стенки 1.0 нм, большую удельную поверхность 1147 м2/г и объем мезопор 0.74 см3/г. Отсутствие разброса по величине диаметра между различными мезопорами подтверждается тем, что область Δ(Р/Ро), в пределах которой происходит капиллярная конденсация азота при 77 К, является очень узкой. На Фиг.2 приведена изотерма адсорбции для Ti-MMM-2. Ti-MMM-2 сохраняют структурные и текстурные характеристики при кипячении в воде в течение нескольких часов. Это подтверждается данными рентгеноструктурного анализа, представленными на Фиг.3 (кривая 1 получена для исходного образца Ti-MMM-2 (2 мас.% Ti), кривая 2 получена для того же образца после его кипячения в воде в течение 6 ч и последующего прокаливания при 600°С). Ti-MMM-2 сохраняет высокую удельную поверхность при циклической обработке в воде (кипячение, сушка). Соответствующие данные по низкотемпературной адсорбции N2 представлены в Таблице 1. Состояние титана в Ti-MMM-2 близко к изолированному, о чем свидетельствует положение максимума (около 210 нм) в УФ-спектре диффузного отражения (Фиг.4). Полученные материалы обладают высокой активностью в реакциях окисления органических субстратов водным пероксидом водорода. В ходе жидкофазной реакции окисления водным пероксидом водорода гетероэлемент не вымывается из силикатной матрицы, катализатор отделяется простой фильтрацией и может быть использован многократно без потери активности. Каталитические свойства получаемых материалов, в первую очередь селективность, можно варьировать, заменяя часть ионов титана на другие гетероэлементы (М, Y), например, М=Аl, В, Ga, Fe, Cr; Y=Zr, Sn, Ge и др.
Предлагаемое изобретение иллюстрируется следующими примерами.
Пример 1. В золь кремниевой кислоты (при соотношении Si:H2O, равном 25, рН~1.1) добавляют раствор сульфата титана (соотношение Ti:Si=0.022). К полученному раствору добавляют ПАВ - (ПАВ: Si=1:0.78 моль) С16Н33N(СН3)3Вr (Lancaster) при тщательном перемешивании и слабом подогреве. Полученную смесь выдерживают при комнатной температуре от 12 до 48 ч, рН смеси 0.9-1.0, после чего добавляют силикат натрия при интенсивном перемешивании, при этом мольное отношение Si/Ti составляет 39. рН раствора доводят до значения 2.5 и конечный продукт подвергают гидротермальной обработке при 50°С в течение 15 мин, затем фильтруют, промывают, высушивают и прокаливают при 600°С в течение 6 ч. Полученный образец Ti-MMM-2 представляет собой мезопористый мезофазный титан-силикат с гексагональной упаковкой унифицированных мезопор диаметром d=2.5 нм и толщиной силикатной стенки h=1.0 нм. Содержание Ti 2.0 мас.%, состояние титана близко к изолированному (λmах=211 нм в УФ-спектре диффузного отражения - Фиг.4). Площадь поверхности катализатора S и объем мезопор ν, оцененные из адсорбционных данных, составляют 1147 м2/г и 0.74 см3/г соответственно. После кипячения в воде в течение 6 ч структура материала сохраняется (Фиг.3, Таблица 1).
Пример 2. Синтез проводят, как в примере 1, но берут мольное отношение Si/Ti, равное 19, в результате чего получают образец Ti-MMM-2, содержащий 4.0 мас.% Ti (λmах=220 нм). Площадь поверхности мезопор S=1131 м2/г, объем мезопор ν=0.69 см3/г, диаметр мезопор d=2.5 нм.
Пример 3. Синтез проводят, как в примере 1, но берут мольное отношение Si/Ti, равное 9, в результате чего получают образец Ti-MMM-2, содержащий 8.0 мас.% Ti (λmах=223 нм). Площадь поверхности мезопор S=933 м2/г, объем мезопор ν=0.65 см3/г, диаметр мезопор d=2.3 нм.
Пример 4. Синтез проводят, как в примере 1, но проводят старение силикатного золя при температуре 40°С в течение 4 ч и затем при комнатной температуре в течение 20 ч, в результате чего получают образец Ti-MMM-2, содержащий 2.0 мас.% Ti (λmах=214 нм). Площадь поверхности мезопор S=1119 м2/г, объем мезопор ν=0.71 см3/г, диаметр мезопор d=2.6 нм.
Пример 5. Синтез проводят, как в примере 1. но вместо 0.018 моль С16Н33N(СН3)3Вr добавляют 0.018 моль С12Н25N(СН3)3Вr, в результате чего получают образец Ti-MMM-2, содержащий 2.0 мас.% Ti (λmах=225 нм). Площадь поверхности мезопор S=671 м2/г, объем мезопор ν=0.3 см3/г, диаметр мезопор d=2.0 нм.
Пример 6. Синтез проводят, как в примере 1, но вместо 0.018 моль С16Н33N(СН3)3Вr добавляют 0.018 моль алкилполиэтиленоксида Brij 56 общей формулы С16Н33ЕО10, в результате чего получают образец, содержащий 2.0 мас.% Ti (λmах=226 нм). Площадь поверхности мезопор S=1072 м2/г, объем мезопор ν=0.66 см3/г, диаметр мезопор d=2.7 нм.
Пример 7. Синтез проводят, как в примере 1, но вместо Ti(SO4)2 используют раствор тетра-изопропоксида титана в этиловом спирте, модифицированный эквимолярным количеством H2SO4, в результате чего получают образец Ti-MMM-2, содержащий 1.8 мас.% Ti (λmах=243 нм). Площадь поверхности мезопор S=980 м2/г, объем мезопор ν=0.58 см3/г, диаметр мезопор d=2.9 нм.
Пример 8. Синтез проводят, как в примере 1, но гидротермальную обработку проводят при 30°С в течение 18 ч, в результате чего получают образец Ti-MMM-2, содержащий 2 мас.% Ti (λmах=218 нм). Площадь поверхности мезопор S=1165 м2/г, объем мезопор ν=0.73 см3/г, диаметр мезопор d=2.4 нм.
Пример 9. Синтез проводят, как в примере 1, но гидротермальную обработку при 100°С в течение 0.5 ч, в результате чего получают образец Ti-MMM-2, содержащий 2 мас.% Ti (λmах=258 нм). Площадь поверхности мезопор S=879 м2/г, объем мезопор ν=0.55 см3/г, диаметр мезопор d=3.1 нм.
Пример 10. Синтез проводят, как в примере 1, но дополнительную порцию силиката натрия вводят в таком количестве, чтобы рН смеси, подвергаемой гидротермальной обработке, был равен 3.0, в результате чего получают образец Ti-MMM-2, содержащий 2.2 мас.% Ti (λmах=243 нм). Площадь поверхности мезопор S=1009 м2/г, объем мезопор ν=0.68 см3/г, диаметр мезопор d=2.6 нм.
Пример 11. Синтез проводят, как в примере 1, но вслед за раствором TiOSO4 вводят такое же количество эквимолярного раствора Аl(SО4)3, в результате чего получают образец Ti-MMM-2, содержащий 2.0 мас.% Ti (λmах=212 нм) и 1.9 мас.% А1. Площадь поверхности мезопор S=1101 м2/г, объем мезопор ν=0.73 см3/г, диаметр мезопор d=2.8 нм.
Пример 12. Синтез проводят, как в примере 1, но полученный материал прокаливают при температуре 540°С, в результате чего получают образец Ti-MMM-2, содержащий 2.0 мас.% Ti (λmах=211 нм). Площадь поверхности мезопор S=1135 м2/г, объем мезопор ν=0.72 см3/г, диаметр мезопор d=2.7 нм.
Пример 13. Синтез проводят, как в примере 1, но дополнительно в реакционную смесь вводят раствор сернокислого алюминия в соотношении Al:Ti, равном 1.0, в результате чего получают образец, содержащий 2.0 мас.% Ti и 2.0 мас.% Al (λmах=212 нм). Площадь поверхности мезопор S=1077 м2/г, объем мезопор ν=0.74 см3/г, диаметр мезопор d=2.6 нм.
Пример 14. Синтез проводят, как в примере 1, но дополнительно в реакционную смесь вводят раствор сернокислого железа в соотношении Fe:Ti, равном 1.0, в результате чего получают образец, содержащий 2.0 мас.% Ti и 2.0 мас.% Fe. Площадь поверхности мезопор S=1213 м2/г, объем мезопор ν=0.87 см3/г, диаметр мезопор d=2.4 нм.
Примеры 15-19 демонстрируют возможность применения полученных мезопористых титан-силикатных материалов в качестве катализаторов в процессах селективного окисления органический соединений водным пероксидом кислорода.
Пример 15. В термостатируемый при 80°С стеклянный реактор, снабженный магнитной мешалкой и обратным холодильником, помещают 41 мг 2,3,6-триметилфенола (ТМФ) (0.30 ммоль), 31 мг прокаленного при 600°С катализатора, синтез которого описан в Примере 1, и 3 мл ацетонитрила. Затем при перемешивании добавляют 140 μл (1.05 ммоль) 28%-ной Н2О2. Смесь интенсивно перемешивают при 80°С. Через 0.3 ч конверсия ТМФ и выход 2.3,5-триметил-1.4-бензохинона (ТМБХ) в расчете на прореагировавший ТМФ, определенные методом ГЖХ, составляют 99 и 82% соответственно. Катализатор отфильтровывают, промывают метанолом, сушат на воздухе и используют повторно. Через 0.5 ч конверсия ТМФ и выход ТМБХ составляют 100 и 81%, соответственно.
Пример 16. Процесс проводят, как в примере 13, но используют вместо 2,3,6-ТМФ 2.6-дитретбутилфенол. Через 2.5 ч конверсия исходного фенола 53%, выход 2,6-дитретбутилбензохинона 80%.
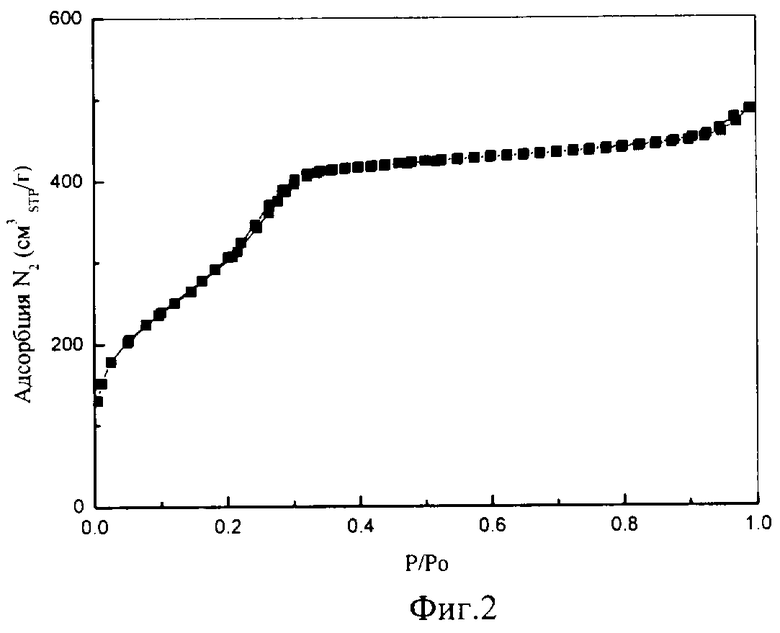
Пример 17. Процесс проводят, как в примере 13, но через 4 мин после начала реакции катализатор отфильтровывают и следят за превращением ТМФ в фильтрате методом ГЖХ. На Фиг.5 показаны кинетические кривые окисления ТМФ H2O; в присутствии Ti-MMM-2 катализатора: кривая 1 - без фильтрования, кривая 2 - катализатор удаляют через 4 мин после начала реакции. Данный пример показывает, что окисление ТМФ является гетерогенным процессом и протекает в матрице катализатора, а не в объеме раствора вследствие вымывания титана.
Пример 18. В термостатируемый при 20°С стеклянный реактор, снабженный магнитной мешалкой и конденсором, помещают 36 μл метилфенилсульфида (МФС) (0.30 ммоль), 14 мг прокаленного при 600°С катализатора, синтез которого описан в примере 1 (содержание Ti в катализаторе - 2.0 мас.%) и 3 мл ацетонитрила. Затем при перемешивании добавляют 46 μл (0.39 ммоль) 28%-ной H2O2. Смесь интенсивно перемешивают при 20°С. Через 35 мин конверсия МФС и выход метилфенилсульфоксида (МФСО), определенные методом ГЖХ, составляют 100 и 78% соответственно. После реакции катализатор отфильтровывают, промывают метанолом, сушат на воздухе при комнатной температуре и используют повторно. Многократное использование катализатора не приводит к потере его активности и селективности (Таблица 2).
Пример 19. В термостатируемый при 50°С стеклянный реактор, снабженный магнитной мешалкой и конденсором, помещают 69 μл (-)-кариофиллена (0.30 ммоль), 14 мг прокаленного при 600°С катализатора, синтез которого описан в примере 1 (содержание Ti в катализаторе 2.0 мас.%) и 3 мл ацетонитрила. Затем при перемешивании добавляют 39 μл (0.33 ммоль) 28%-ной H2O2. Смесь интенсивно перемешивают при 50°С. Через 4 ч конверсия кариофиллена и выход 4.5-моноэпоксида, определенные методом ГЖХ, составляют 75 и 80% соответственно.
Как видно из приведенных примеров, таблиц и рисунков, приготовленные по заявляемому способу мезопористые мезофазные титан-силикатных катализаторы являются одновременно термогидростабильными и устойчивыми к вымыванию активного компонента (личингу).
Полученные катализаторы обладают высокой активностью в реакциях окисления органических субстратов водным пероксидом водорода. В ходе жидкофазной реакции окисления водным пероксидом водорода гетероэлемент не вымывается из силикатной матрицы, катализатор отделяется простой фильтрацией и может быть использован многократно без потери активности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ, КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 2001 |
|
RU2196764C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИ-ТРЕТ-БУТИЛ-П-БЕНЗОХИНОНА | 2016 |
|
RU2654477C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЗОПОРИСТЫХ ЭЛЕМЕНТОСИЛИКАТОВ | 2009 |
|
RU2422361C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЗОПОРИСТЫХ АМОРФНЫХ СМЕШАННЫХ ЭЛЕМЕНТОСИЛИКАТОВ | 2009 |
|
RU2420455C1 |
| КАТАЛИЗАТОР (ВАРИАНТЫ), СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ОЧИСТКИ ЖИДКИХ РАДИОАКТИВНЫХ ОТХОДОВ | 2014 |
|
RU2570510C2 |
| СПОСОБ УСКОРЕННОЙ ГИДРОТЕРМАЛЬНОЙ ОБРАБОТКИ ПРИ СИНТЕЗЕ МЕЗОСТРУКТУРИРОВАННОГО СИЛИКАТНОГО МАТЕРИАЛА ТИПА SBA-15 | 2013 |
|
RU2529549C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ | 2018 |
|
RU2681950C1 |
| Способ получения иерархического железосодержащего силикалита с возможностью регулирования соотношения микромезопор для процесса полного окисления фенола пероксидом водорода | 2022 |
|
RU2803369C1 |
| СПОСОБ ЭПОКСИДИРОВАНИЯ ОЛЕФИНА С ОДНОВРЕМЕННЫМ ПОЛУЧЕНИЕМ ПРЕДШЕСТВЕННИКА НЕЙЛОНА | 2005 |
|
RU2359964C2 |



Изобретение относится к области синтеза материалов, которые находят применение в качестве катализаторов тонкого органического синтеза, а именно к усовершенствованному способу получения титан-силикатного катализатора для процессов селективного окисления органических соединений пероксидом водорода. Изобретение решает задачу разработки способа приготовления мезопористых мезофазных титан-силикатных материалов, которые будут одновременно термогидростабильными и устойчивыми к вымыванию активного компонента (личингу). Поставленная задача достигается тем, что процесс формирования титан-силикатных мезоструктурированных материалов проводят в два этапа. На первом этапе, включающем приготовление смеси, содержащей положительно заряженные гидроксокомплексы кремния, добавление в нее соединения титана и добавление поверхностно-активного вещества (ПАВ) (порядок смешения - произвольный), рН поддерживают в диапазоне 0.5-1.5. На втором этапе проводят введение порции щелочного раствора таким образом, чтобы рН реакционной смеси поддерживался в диапазоне от 1.5 до 7.0, и после этого смесь подвергают гидротермальной обработке, после чего продукт отделяют фильтрованием, промывают, сушат и прокаливают. 5 ил., 2 табл.

| US 20010043901 A1, 22.11.2001 | |||
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
| US 5855864 A, 05.01.1999 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2004-06-10—Публикация
2003-03-17—Подача