Изобретение относится к способу получения замещенных хинонов, в том числе, 2,3,5-триметил-1,4-бензохинона (ТМБХ) - ключевого интермедиата в синтезе витамина Е, широко применяемого в медицинской практике и животноводстве, а также к синтезу катализаторов для этого способа.
Способы получения алкилзамещенных хинонов из соответствующих алкилфенолов делятся на три основные группы: 1) стехиометрическое окисление неорганическими окислителями - соединениями марганца(IV) и хрома(VI), азотной кислотой и др., 2) гомогенное каталитическое окисление в присутствии комплексов переходных металлов и 3) гетерогенное каталитическое окисление в присутствии твердофазных катализаторов, содержащих переходные металлы. При стехиометрическом окислении используются большие количества дорогих и токсичных окислительных агентов, что приводит к возникновению проблем, связанных с утилизацией большого количества токсичных отходов. Поэтому каталитические способы окисления гораздо более приемлемы как с точки зрения экологии, так и с точки зрения экономики. Наибольший интерес представляют каталитические способы получения хинонов из замещенных фенолов, основанные на использовании экологически безопасных окислителей (молекулярного кислорода и пероксида водорода), которые в качестве единственного побочного продукта дают воду [О.А. Kholdeeva, O.V. Zalomaeva, Recent advances in transition-metal catalyzed selective oxidation of phenols and methoxyarenes using environmentally benign oxidants, Coord. Chem. Rev. 306 (2016) 302-330]. Хотя стоимость пероксида водорода выше, чем стоимость кислорода, в малотоннажных процессах тонкого органического синтеза использование первого часто оказывается предпочтительным, поскольку стоимость технологического оборудования для окисления пероксидом водорода ниже, чем для окисления кислородом [R.A. Sheldon, J. Dakka. Heterogeneous catalytic oxidations in the manufacture of fine chemicals. Catalysis Today 19 (1994) 215].
При окислении замещенных фенолов кислородом используют три основных типа гомогенных катализаторов: 1) комплексы кобальта с основаниями Шиффа [L. Schuster, Н. Pommer, DE 1793183 (1968)], 2) галогениды меди [ЕР 0093540, С07С 50/04, 1983; ЕР 0127888 B1, С07С 46/08, 1987] и 3) фосформолибдованадиевые гетерополикислоты H3+nPMo12-nVnO40 (ГПК-n, n=2-6) [SU 1719392, С07С 50/04, 1991; PCT/FR 96/01689, С07С 46/08; RU 2022958, С07С 50/12, 1994; WO 2004/014832]. Катализаторы на основе комплексов кобальта с органическими лигандами (основаниями Шиффа) подвержены окислительной деструкции и имеют низкую производительность. Недостатками каталитических способов, основанных на использовании галогенидов меди, являются высокие (практически стехиометрические) количества катализатора и загрязнение продукта токсичным переходным металлом, а также коррозия аппаратуры. Кроме того, в случае использования хлоридов меди имеет место побочное образование токсичных хлорорганических соединений. Даже применение двухфазных систем вода-органический растворитель [US Pat. 5041572, 1991] не позволяет полностью избежать загрязнения продукта следами переходного металла. В способах, основанных на применении ГПК-n, также используют близкие к стехиометрическим количества катализатора, и продукт загрязняется переходными металлами.
Для окисления замещенных фенолов пероксидом водорода известны системы, основанные на использовании в качестве гомогенного катализатора соединений рутения и железа [Ito S., Aihara K., Matsumoto М. Tetr. Lett. Ruthenium-catalyzed oxidation of phenols with hydrogen peroxide. 24 (1983) 5249; Wienhcfer G., Schrcder K., Mcller K., Junge K., Beller M. Adv. Synth. Catal. 2010, 352, 1615;  , K., Wienhcfer, G., Schrcder, K., Join, В., Junge, K., Beller, M. Chem. Eur. J. 2010, 16, 10300], а также гетерополикислот структуры Кеггина (HnXM12O40, X=Si (n=4), Р (n=3); М=Мо, W) [US 5245059, C07C 50/04, 1993]. В качестве гетерогенных катализаторов могут быть использованы различные мезопористые материалы, содержащие медь [US Patent 6500972 (2002)] и титан [US 5712402, С07С 50/02, 1998; RU 2164510, 2000; 2196764, 2001].
, K., Wienhcfer, G., Schrcder, K., Join, В., Junge, K., Beller, M. Chem. Eur. J. 2010, 16, 10300], а также гетерополикислот структуры Кеггина (HnXM12O40, X=Si (n=4), Р (n=3); М=Мо, W) [US 5245059, C07C 50/04, 1993]. В качестве гетерогенных катализаторов могут быть использованы различные мезопористые материалы, содержащие медь [US Patent 6500972 (2002)] и титан [US 5712402, С07С 50/02, 1998; RU 2164510, 2000; 2196764, 2001].
Недостатками перечисленных выше каталитических систем являются, как правило, недостаточно высокий выход целевого продукта и, соответственно, необходимость затрат на очистку от побочных продуктов, а также низкая эффективность использования окислителя (селективность по пероксиду водорода) вследствие побочного процесса его разложения на катализаторе.
Наиболее близким к данному изобретению является способ окисления замещенных фенолов в хиноны пероксидом водорода в присутствии гомогенного катализатора - алкиламмониевых солей ванадийсодержащего полиоксовольфрамата (Alkm-nHn)[γ-PV2W10O40], Alk=(CkH2k+1)4N, k=4-6; m=5; n=0-2) (Пат. РФ, №2568645, C07C 50/04, B01J 23/22, 20.11.2015). Синтез соединений данного типа описан в [K. Kamata, K. Sugahara, K. Yonehara, R. Ishimoto, N. Mizuno, Chem. Eur. J. 2015, 17, 7549; О.V. Zalomaeva, V.Yu. Evtushok, G.M. Maksimov, R.I. Maksimovskaya, O.A. Kholdeeva, Dalton Transactions, 2017, 46, 5202]. Недостатком данного способа является сложность отделения катализатора от продуктов реакции, поскольку и катализатор и продукты растворены в одной фазе. Кроме того, при использовании гомогенного катализатора возможно загрязнение продукта переходными металлами (W, V).
По способу приготовления катализатора наиболее близким к настоящему изобретению является способ получения композитного гетерогенного катализатора на основе ванадийсодержащего полиоксовольфрамата TBA5-nHn[γ-PV2W10O40], включающий приготовление раствора TBA5-nHn[γ-PV2W10O40] с со-катализаторами TBA4[SiW12O40] и HClO4 и нанесение полученной смеси на Fe2O3 [Wang, Y.; Kamata, K.; Ishimoto, R.; Ogasawara, Y.; Suzuki, K.; Yamaguchi, K.; Mizuno N. Catal. Sci. Technol. 2015, 5, 2602-2615]. Данный тип катализаторов был использован для эпоксидирования алкенов, сульфоксидирования тиоэфиров и гидроксилирования анизола, но не применялся для окисления алкилфенолов в хиноны [Wang, Y.; Kamata, K.; Ishimoto, R.; Ogasawara, Y.; Suzuki, K.; Yamaguchi, K.; Mizuno N. Catal. Sci. Technol. 2015, 5, 2602-2615]. Недостатками указанного способа приготовления катализатора являются сложность технологии синтеза (необходимость использования дополнительного компонента - TBA4[SiW12O40]), использование оксида железа в качестве носителя (на нем может идти непродуктивное разложение пероксида водорода, что приводит к снижению эффективности использования окислителя), уменьшение активности катализатора при повторном использовании, а также неустойчивость полученного данным методом катализатора в полярных растворителях, например, ацетонитриле, применение которых необходимо для процессов окисления алкилфенолов в хиноны.
Задачей данного изобретения является создание эффективного гетерогенного катализатора окисления замещенных фенолов в хиноны, высокотехнологичного способа его приготовления и каталитического способа окисления замещенных фенолов в хиноны с использованием дешевого и экологически чистого окислителя - пероксида водорода.
Технический результат:
- высокая активность и селективность гетерогенного катализатора, не теряющего активность и селективность при многократном использовании,
- способ приготовления катализатора позволяет 1) закрепить активный компонент (ванадийсодержащий полиоксовольфрамат) с сохранением его активности и селективности и 2) получить каталитически активный материал, устойчивый к воздействию полярной реакционной среды, который можно будет использовать многократно без потери каталитических свойств,
- упрощение и удешевление технологии существующих процессов получения хинонов и повышение чистоты продукта за счет исключения образования ядовитых хлорсодержащих побочных продуктов, коррозии аппаратуры и загрязнения продукта переходными металлами.
Задача решается тем, что в качестве гетерогенного катализатора используют тетрабутиламмониевые соли ванадийсодержащего полиоксовольфрамата (ТВА5-nHn[γ-PV2W10O40] (n=1-2), закрепленные на твердом носителе - азотсодержащем углеродном материале, содержание полиоксовольфрамата в катализаторе составляет 5-25 мас. %. Азотсодержащий углеродный материал может представлять собой нанотрубки или нановолокна, содержание азота в носителе 1-5 ат. %.
Задача решается также способом приготовления гетерогенного катализатора, включающего ванадийсодержащий полиоксовольфрамат TBA5-nHn[γ-PV2W10O40], где: n=1-2, для процесса получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода, заключающимся в том, что к раствору полиоксовольфрамата в ацетонитриле добавляют носитель - азотсодержащий углеродный материал и минеральную кислоту, предпочтительно, HClO4, полученный катализатор отделяют фильтрованием от раствора и сушат, в результате чего получают катализатор, который включает ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где: n=1-2, в количестве 5-25 мас. %, закрепленный на твердом носителе - азотсодержащем углеродном материале. Перед процессом нанесения азотсодержащий углеродный материал сушат в вакууме при температуре не выше 100°С.
Задача решается также способом получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода в присутствии катализатора, включающего ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где: n=1-2, в среде ароматического растворителя - ацетонитрила, в качестве катализатора используют описанный выше катализатор, процесс ведут при температуре не ниже 25°С. В качестве ароматических соединений берут замещенные фенолы, такие как, 2,3,6-триметилфенол, 2,6-диметилфенол и 2,6-дитретбутилфенол. Катализатор перед использованием сушат в вакууме при температуре не более 60°С. В качестве окислителя используют водный раствор пероксида водорода с содержанием пероксида водорода не менее 30 мас. %, используют концентрацию субстрата не выше 0.15 М, используют мольное отношение пероксид водорода/субстрат не ниже 2.3, используют мольное отношение субстрат/активный компонент катализатора не ниже 66, катализатор отделяют фильтрованием и используют повторно.
Синтез азотсодержащих углеродных наноматериалов описан в [Suboch, A.N.; Cherepanova, S.V.; Kibis, L.S.; Svintsitskiy, A.D.; Stonkus, O.A.; Boronin, A.I.; Chesnokov, V.V.; Romanenko, A.I.; Ismagilov, Z.R.; Podyacheva O. Yu. Fullerenes, Nanotub. Carbon Nanostructures 2016, 24, 520-530; Shalagina A.E., Ismagilov Z.R., Podyacheva O.Yu., Kvon R.I., Ushakov V.A. Carbon 2007, 45; 1808-1820]. Активный компонент (полиоксовольфрамат) прочно закрепляется на поверхности твердого носителя и не вымывается в процессе жидкофазного окисления пероксидом водорода, катализатор отделяется простым фильтрованием и может быть использован многократно без потери активности и селективности.
Сущность изобретения иллюстрируется нижеследующими примерами, таблицами.
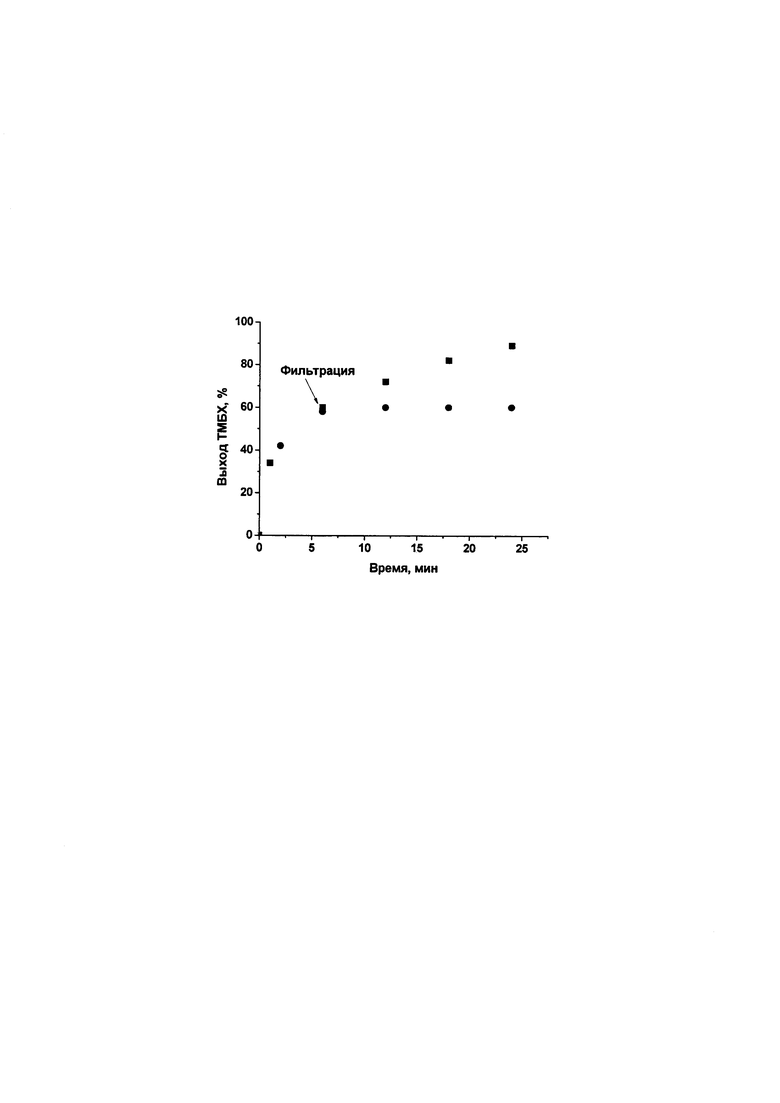
На Фиг. представлены кинетические кривые окисления 2,3,6-триметилфенола Н2О2 в присутствии γ-PV2W10/N-УНТ:  - без фильтрования, • - катализатор отфильтровывали через 6 мин после начала реакции (условия см. в примере 33).
- без фильтрования, • - катализатор отфильтровывали через 6 мин после начала реакции (условия см. в примере 33).
Пример 1.
Перед использованием углеродные нанотрубки с содержанием азота 4.8 ат. % (N-УНТ) сушат в вакууме при 110°С в течение 4 ч. 2.8 микромоль TBA4H[γ-PV2W10O40] (γ-PV2W10) растворяют в 5 мл сухого ацетонитрила и при перемешивании (500 об/мин) добавляют 1 экв. HClO4 (2.8 микромоль). К полученному раствору добавляют 120 мг 4.8% N-УНТ и оставляют на 2 ч при перемешивании. Затем твердое вещество отделяют, промывают ацетонитрилом (3 раза по 5 мл) и сушат на воздухе. Полученный катализатор γ-PV2W10/4.8% N-УНТ содержит 8 мас. % γ-PV2W10 и 4.8 ат. % N. Площадь поверхности катализатора S(BET) 147 м2/г, объем пор 0.53 см3/г, средний диаметр пор 14 нм.
Пример 2. Синтез проводят, как в примере 1, но берут 9.3 микромоль γ-PV2W10 и 9.3 микромоль HClO4, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 25 мас. % γ-PV2W10 и 4.8 ат. % N.
Пример 3. Синтез проводят, как в примере 1, но берут 5.6 микромоль γ-PV2W10 и 5.6 микромоль HClO4, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 15 мас. % γ-PV2W10 и 4.8 ат. % N.
Пример 4. Синтез проводят, как в примере 1, но берут 3.7 микромоль γ-PV2W10 и 3.7 микромоль HClO4, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 10 мас. % γ-PV2W10 и 4.8 ат. % N.
Пример 5. Синтез проводят, как в примере 1, но берут 1.85 микромоль γ-PV2W10 и 1.85 микромоль HClO4, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 5 мас. % γ-PV2W10 и 4.8 ат. % N.
Примеры 1-5 демонстрируют возможный диапазон весового содержания активного компонента (γ-PV2W10) в катализаторе.
Пример 6. Синтез проводят, как в примере 3, но берут N-УНТ с содержанием азота 3.1 ат. %, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 15 мас. % γ-PV2W10 и 3.1 ат. % N.
Пример 7. Синтез проводят, как в примере 3, но берут N-УНТ с содержанием азота 1.8 ат. %, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 15 мас. % γ-PV2W10 и 1.8 ат. % N. Площадь поверхности катализатора S(BET) 132 м2/г, объем пор 0.64 см3/г, средний диаметр пор 19 нм.
Пример 8. Синтез проводят, как в примере 3, но берут углеродные нанотрубки не содержащие азот (УНТ), в результате чего получают катализатор γ-PV2W10/УНТ, содержащий 15 мас. % γ-PV2W10 и 0 ат. % N. Площадь поверхности катализатора S(BET) 145 м2/г, объем пор 0.64 см3/г, средний диаметр пор 15 нм.
Примеры 3 и 6-8 показывают, что варьирование содержания азота в УНТ не влияет на содержание γ-PV2W10 в катализаторе.
Пример 9. Синтез проводят, как в примере 3, но N-УНТ предварительно не сушат, в результате чего получают катализатор γ-PV2W10/N-УНТ, содержащий 6 мас. % γ-PV2W10 и 4.8 ат. % N.
Пример 9 в сравнении с примером 3 показывает, что влажность носителя снижает весовое содержание γ-PV2W10 в катализаторе.
Пример 10. Синтез проводят, как в примере 3, но не добавляют HClO4, в результате чего содержание γ-PV2W10 в полученном материале близко к 0.
Пример 10 в сравнении с примером 3 показывает, что добавление минеральной кислоты HClO4 необходимо для закрепления γ-PV2W10 на УНТ.
Пример 11. Синтез проводят, как в примере 8, но вместо УНТ берут углеродные нановолокна не содержащие азот (УНВ). В результате чего получают катализатор γ-PV2W10/УНВ, содержащий 15 мас. % γ-PV2W10.
Данный пример показывает, что морфология углеродного материала не влияет на содержание γ-PV2W10 в катализаторе.
Пример 12. Синтез проводят, как в примере 11, но берут углеродные нановолокна, содержащие 3 ат. % азота (N-УНВ). В результате чего получают катализатор γ-PV2W10/N-УНВ, содержащий 15 мас. % γ-PV2W10 и 3 ат. % N.
Пример 13. Синтез проводят, как в примере 11, но берут углеродные нановолокна, содержащие 6 ат. % азота (N-УНВ). В результате чего получают катализатор γ-PV2W10/N-УНВ, содержащий 15 мас. % γ-PV2W10 и 6 ат. % N.
Примеры 11-13 показывают, что содержание азота в УНВ также не влияет на содержание γ-PV2W10 в катализаторе.
Пример 14. Синтез проводят, как в примере 13, но берут 2.8 микромоль γ-PV2W10. В результате чего получают катализатор γ-PV2W10/N-УНВ, содержащий 8 мас. % γ-PV2W10 и 6 ат. % N. Площадь поверхности катализатора S(BET) 195 м2/г, объем пор 0.49 см3/г, средний диаметр пор 10 нм.
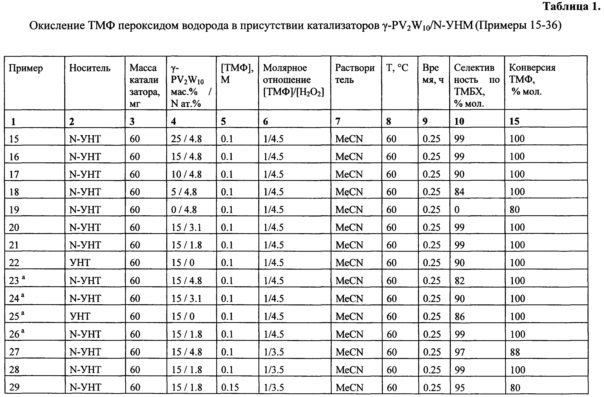
Пример 15. В термостатируемый при 60°С стеклянный реактор, снабженный магнитной мешалкой, помещают 13.6 мг 2,3,6-триметилфенола (ТМФ) (0.1 ммоль), 60 мг высушенного в вакууме при 60°С катализатора γ-PV2W10/N-УНТ, синтез которого описан в примере 2 (весовое содержание γ-PV2W10 25 мас. %, содержание азота 4.8 ат. %) и 1 мл ацетонитрила. Затем при перемешивании добавляют 41 μл (0.45 ммоль) 33% Н2О2. Смесь интенсивно перемешивают при 60°С. Через 0.25 ч конверсия ТМФ и выход 2,3,5-триметил-1,4-бензохинона (ТМБХ) в расчете на прореагировавший ТМФ (селективность), определенные методом ГЖХ, составляют 100 и 99%, соответственно.
Пример 16. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 3 (γ-PV2W10 15 мас. %, содержание азота 4.8 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 99%, соответственно.
Пример 17. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 4 (γ-PV2W10 10 мас. %, содержание азота 4.8 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 90%, соответственно.
Пример 18. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 5 (γ-PV2W10 5 мас. %, содержание азота 4.8 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 84%, соответственно.
Примеры 15-18 показывает, что уменьшение весового содержания γ-PV2W10 ниже 15 мас. % приводит к уменьшению селективности образования целевого продукта.
Пример 19. Процесс проводят как в примере 15, но берут N-УНТ с 4.8 ат. % N, не содержащий γ-PV2W10. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 80 и 0%, соответственно. Данный пример в сравнении с примерами 15-18 показывает, что не содержащий γ-PV2W10 носитель N-УНТ катализирует окисление ТМФ, но процесс не приводит к образованию ТМБХ.
Пример 20. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 6 (γ-PV2W10 15 мас. %, содержание азота 3.1 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 99%, соответственно.
Пример 21. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 7 (γ-PV2W10 15 мас. %, содержание азота 1.8 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 99%, соответственно.
Пример 22. Процесс проводят как в примере 15, но берут катализатор, синтез которого описан в примере 8 (γ-PV2W10 15 мас. %, содержание азота 0 ат. %). Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 90%, соответственно.
Данный пример по сравнению с примерами 15, 20 и 21 показывает, что для достижения селективности 99% необходимо, по крайней мере, 1.8 ат. % азота в носителе.
Пример 23. Процесс проводят как в примере 16, но катализатор не сушат в вакууме перед использованием. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 82%, соответственно.
Пример 24. Процесс проводят как в примере 20, но катализатор не сушат в вакууме перед использованием. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 90%, соответственно.
Пример 25. Процесс проводят как в примере 22, но катализатор не сушат в вакууме перед использованием. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 86%, соответственно.
Примеры 23-25 в сравнении с примерами 16, 20, 22 показывают, что предварительная сушка катализатора необходима для достижения высокой селективности образования целевого продукта.
Пример 26. Процесс проводят как в примере 21, но катализатор не сушат в вакууме перед использованием. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 99%, соответственно.
Данный пример показывает, что сушка катализатора с содержанием γ-PV2W10 15 мас. % и содержанием азота 1.8 ат. % не является критическим параметром, в отличие от катализаторов с другим содержанием азота.
Пример 27. Процесс проводят как в примере 16, но добавляют 33 μл (0.35 ммоль) 33% Н2О2. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 88 и 97%, соответственно.
Данный пример в сравнении с примером 16 показывает, что уменьшение концентрации окислителя приводит к снижению конверсии ТМФ.
Пример 28. Процесс проводят как в примере 21, но добавляют 33 μл (0.35 ммоль) 33% Н2О2. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 100 и 99%, соответственно.
Данный пример в сравнении с примером 21 и 27 показывает, что при использовании катализатора состава γ-PV2W10 15 мас. % и 1.8 ат. % азота возможно снижение концентрации окислителя без снижения конверсии ТМФ поскольку имеет место повышение эффективности использования окислителя с 50% в примере 21 до 80% в данном примере.
Пример 29. Процесс проводят как в примере 28, но берут концентрацию ТМФ 0.15 М. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 80 и 95%, соответственно, а эффективность по перекиси водорода составляет 65%.
Данный пример в сравнении с примером 21 и 28 показывает, что увеличение концентрации ТМФ не приводит к дальнейшему увеличению эффективности использования H2O2.
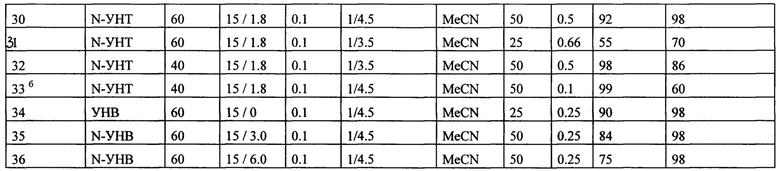
Пример 30. Процесс проводят как в примере 21, но при температуре 50°С. Через 0.5 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 92%, соответственно.
Пример 31. Процесс проводят как в примере 21, но при температуре 25°С. Через 0.66 ч конверсия ТМФ и селективность по ТМБХ составляют 70 и 55%, соответственно.
Примеры 30-31 в сравнении с примером 21 показывает, что снижение температуры приводит к увеличению времени реакции и уменьшению конверсии ТМФ и селективности по ТМБХ.
Пример 32. Процесс проводят как в примере 30, но берут 40 мг катализатора. Через 0.5 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 86%, соответственно.
Пример 33. Процесс проводят как в примере 32, но через 6 мин. после начала реакции катализатор отфильтровывают и следят за превращением ТМФ в фильтрате методом ГЖХ.
Данный пример показывает, что вымывания активного компонента γ-PV2W10 в ходе реакции не происходит и окисление ТМФ является гетерогенным процессом и протекает на поверхности катализатора, а не в объеме раствора.
Пример 34. Процесс проводят как в примере 16, но берут катализатор γ-PV2W10/УНВ, приготовленный как в примере 11. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 90%, соответственно.
Пример 35. Процесс проводят как в примере 16, но берут катализатор γ-PV2W10/УНВ, приготовленный как в примере 12. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 84%, соответственно.
Пример 36. Процесс проводят как в примере 16, но берут катализатор γ-PV2W10/УНВ, приготовленный как в примере 13. Через 0.25 ч конверсия ТМФ и селективность по ТМБХ составляют 98 и 75%, соответственно.
Примеры 36-38 показывают, что увеличение содержания азота в УНВ приводит к уменьшению селективности по ТМБХ.
Пример 37. Процесс проводят как в примере 21, но вместо ТМФ берут 0.1 ммоль 2,6-диметилфенола (ДМФ). Через 0.25 ч конверсия ДМФ и селективность по 2,6-диметилбензохинону составляют 90 и 90%, соответственно.
Пример 38. Процесс проводят как в примере 21, но берут 0.1 ммоль 2,6-ди-трет-бутилфенола. Через 0.25 ч конверсия 2,6-ди-трет-бутилфенола и селективность по 2,6-ди-трет-бутилбензохинону составляют 94 и 90%, соответственно.
Примеры 37-38 показывают, что окисление 2,6-диалкилфенолов в 2,6-диалкил-1,4-бензохиноны протекает с высокой селективностью.
Приведенные примеры показывают, что предлагаемый настоящим изобретением способ получения хинонов является достаточно дешевым, простым в реализации, экологически чистым и позволяет получать целевой продукт с высоким выходом, без примесей хлорсодержащих соединений и переходных металлов.
а) Образцы катализатора не сушили в вакууме перед использованием.
б) Горячее фильтрование (Фиг.)

Условия реакции: 60 мг катализатора γ-PV2W10/N-УНТ (15 мас. % γ-PV2W10, 1.8 ат. % N), концентрация субстрата 0.1, [H2O2]/[субстрат]=1/3.5, время реакции 0.25 ч, 60°С, MeCN.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ | 2014 |
|
RU2568645C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ, КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 2001 |
|
RU2196764C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ТИТАН-СИЛИКАТНОГО КАТАЛИЗАТОРА И СПОСОБ ЖИДКОФАЗНОГО ОКИСЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2003 |
|
RU2229930C1 |
| Способ получения 2,3-диметокси-5-метил-1,4-бензохинона | 2016 |
|
RU2628457C1 |
| Способ получения 2,3,6-триметилбензохинона | 1990 |
|
SU1719392A1 |
| КАТАЛИЗАТОР СИНТЕЗА УГЛЕВОДОРОДОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2422200C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИ-ТРЕТ-БУТИЛ-П-БЕНЗОХИНОНА | 2016 |
|
RU2654477C2 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА ИЗ АММИАКА | 2022 |
|
RU2787379C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-1,4-НАФТОХИНОНА | 2005 |
|
RU2278106C1 |
Изобретение относится к способу получения замещенных хинонов, в том числе 2,3,5-триметил-1,4-бензохинона (ТМБХ) - ключевого интермедиата в синтезе витамина Е, широко применяемого в медицинской практике и животноводстве, а также к синтезу катализаторов для этого способа. Описан катализатор для процесса получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода, включающий ванадийсодержащий полиоксовольфрамат TBA5-nHn[γ-PV2W10O40], где n=1, закрепленный на твердом носителе - азотсодержащем углеродном материале, который представляет собой нанотрубки или нановолокна, содержание полиоксовольфрамата в катализаторе составляет 5-25 мас. %. Способ приготовления указанного гетерогенного катализатора заключается в том, что к раствору полиоксовольфрамата в ацетонитриле добавляют носитель - азотсодержащий углеродный материал, который представляет собой нанотрубки или нановолокна, и минеральную кислоту, полученный катализатор отделяют фильтрованием от раствора и сушат. Также описан способ получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода в присутствии вышеописанного катализатора, включающего ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где n=1, в среде ароматического растворителя – ацетонитрила. Технический результат - создание эффективного гетерогенного катализатора окисления замещенных фенолов в хиноны, высокотехнологичного способа его приготовления и каталитического способа окисления замещенных фенолов в хиноны с использованием дешевого и экологически чистого окислителя - пероксида водорода. 3 н. и 10 з.п. ф-лы, 1 ил., 2 табл., 38 пр.
1. Катализатор для процесса получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода, включающий ванадийсодержащий полиоксовольфрамат TBA5-nHn[γ-PV2W10O40], где n=1, отличающийся тем, что катализатор представляет собой ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где n=1, закрепленный на твердом носителе - азотсодержащем углеродном материале, который представляет собой нанотрубки или нановолокна, содержание полиоксовольфрамата в катализаторе составляет 5-25 мас. %.
2. Катализатор по п. 1, отличающийся тем, что содержание азота в носителе 1-5 ат. %.
3. Способ приготовления гетерогенного катализатора, включающего ванадийсодержащий полиоксовольфрамат TBA5-nHn[γ-PV2W10O40], где n=1, для процесса получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода, отличающийся тем, что к раствору полиоксовольфрамата в ацетонитриле добавляют носитель - азотсодержащий углеродный материал, который представляет собой нанотрубки или нановолокна, и минеральную кислоту, полученный катализатор отделяют фильтрованием от раствора и сушат, в результате чего получают катализатор, который представляет собой ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где n=1, в количестве 5-25 мас. %, закрепленный на твердом носителе - азотсодержащем углеродном материале, который представляет собой нанотрубки или нановолокна.
4. Способ по п. 3, отличающийся тем, что перед процессом нанесения азотсодержащий углеродный материал сушат в вакууме при температуре не выше 100°С.
5. Способ получения замещенных хинонов путем окисления ароматических соединений пероксидом водорода в присутствии катализатора, включающего ванадийсодержащий полиоксовольфрамат ТВА5-nHn[γ-PV2W10O40], где n=1, в среде ароматического растворителя - ацетонитрила, отличающийся тем, что в качестве катализатора используют катализатор по пп. 1, 2 или приготовленный способом по пп. 3, 4.
6. Способ по п. 5, отличающийся тем, что в качестве ароматических соединений берут замещенные фенолы, такие как 2,3,6-триметилфенол, 2,6-диметилфенол и 2,6-дитретбутилфенол.
7. Способ по п. 5, отличающийся тем, что катализатор перед использованием сушат в вакууме при температуре не более 60°С.
8. Способ по п. 5, отличающийся тем, что в качестве окислителя используют водный раствор пероксида водорода с содержанием пероксида водорода не менее 30 мас. %.
9. Способ по п. 5, отличающийся тем, что процесс ведут при температуре не ниже 25°С.
10. Способ по п. 5, отличающийся тем, что используют концентрацию субстрата не выше 0.15 М.
11. Способ по п. 5, отличающийся тем, что используют мольное отношение пероксид водорода/субстрат не ниже 2.3/1.
12. Способ по п. 5, отличающийся тем, что используют мольное отношение субстрат/активный компонент катализатора не ниже 66.
13. Способ по п. 5, отличающийся тем, что катализатор отделяют фильтрованием и используют повторно.
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ | 2014 |
|
RU2568645C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ, КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА | 2001 |
|
RU2196764C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6-ТРИМЕТИЛБЕНЗОХИНОНА И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2164510C1 |
| US 6500972 B2, 31.12.2002 | |||
| US 5712402 A1, 27.01.1998. | |||
Авторы
Даты
2019-03-14—Публикация
2018-03-30—Подача