Изобретение относится к области медицины, а именно к лабораторным методам исследования, и может быть использовано, в частности, для оценки общетоксического действия лекарственных средств на организм.
Известен способ оценки общетоксического действия лекарственных средств, состоящий в исследовании биохимических параметров сыворотки крови, характеризующих функциональное состояние внутренних органов и систем: показатели бромсульфалеиновой пробы, определение содержания общего белка, белковых фракций, общего холестерина сыворотки крови, активности щелочной фосфатазы, трансаминаз, содержание глюкозы крови, желчных кислот, определение креатинина, остаточного азота, мочевины, хлоридов в крови и моче (Изучение “хронической” токсичности. //Методические рекомендации по изучению общетоксического действия фармакологических средств. /Сост. Е.В.Арзамасцев, Т.А.Гуськова, С.С.Либорман, Б.И.Любимов, А.Г.Рудаков, О.Л.Верстакова. - М., 1997. - 10 с.).
Однако способ имеет существенные недостатки, которые ограничивают его использование в практической деятельности лаборатории - потребность в большом количестве исследуемого материала (не менее 2 мл), проведение исследований сыворотки крови в первые часы после ее получения, использование дорогостоящих реактивов.
Известен также способ оценки токсического действия лекарственных средств, основанный на определении ряда гематологических показателей: содержание гемоглобина, количество эритроцитов, лейкоцитов, тромбоцитов, ретикулоцитов, состав лейкоцитарной формулы, скорость свертывания крови, резистентность эритроцитов, гематокрит (Тимофиевская Л.А., Евтушенко Г.Ю. Методы исследования системы крови и кроветворения. //Методы определения токсичности и опасности химических веществ. - М.: “Медицина”, 1970. - с. 219-225). Недостатками этого способа также являются многоэтапность осуществления способа и необходимость использования дорогостоящего оборудования и реактивов.
Наиболее близким к предлагаемому способу является способ оценки токсического действия лекарственных средств, заключающийся в патологоанатомическом исследовании биологических тканей организма (Морфологические исследования. //Гигиенические критерии состояния окружающей среды, 6. - Часть 1. Принципы и методы оценки токсичности химических веществ. - Женева: ВОЗ, 1981. - с. 204-216). Сходство данного способа с предлагаемым заключается в том, что оба они относятся к лабораторным методам исследования и основаны на микроскопическом изучении морфологических параметров полученных образцов.
Недостатками этого способа являются:
- многоэтапность (взятие материала, фиксация, обезвоживание, заливка, приготовление срезов, их окраска);
- длительность исследования (не менее 10 дней с момента взятия материала);
- необходимость использования дорогостоящих, токсичных реактивов и красителей;
- дорогостоящее техническое обеспечение способа.
Предлагаемое изобретение решает основную задачу - упрощение способа. Поставленной задачей было устранение указанных недостатков и создание такого способа диагностики, который позволил бы в короткие сроки на малых объемах биологических жидкостей и экономно установить признаки общетоксического действия лекарственных средств на организм. Это достигается тем, что в способе оценки общетоксического действия лекарственных средств на организм, включающем микроскопическое исследование высушенной сыворотки крови, сыворотку крови интактных животных и животных, получающих исследуемое лекарственное средство, в количестве 20 мкл наносят на поверхность предметного стекла, накрывают покровным стеклом, высушивают при комнатной температуре в течение 48-72 часов, производят сравнительный анализ анизотропных морфотипов и при увеличении в опытных образцах содержания вторичных морфотипов наряду с одновременным снижением числа морфотипов нормы по сравнению с контролем судят о неблагоприятном влиянии на организм исследуемого лекарственного средства, а при наличии в опытных образцах атипичных морфотипов или состояния аморфизации судят о его токсичном действии.
Сыворотка крови является тканью организма, но тканью высокоподвижной за счет слабых межмолекулярных связей между ее элементами. Структуру этих связей можно выявить путем их фиксации - медленная дегидратация.
Изложенная сущность изобретения поясняется фотографиями, где:
Фиг.1 - Базисные морфотипы:
а) сферолиты; б) нитевидные
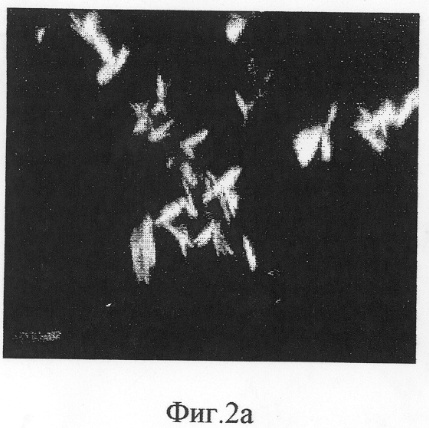
Фиг.2 - Вторичные морфотипы:
а) полиморфные; б) веерные;
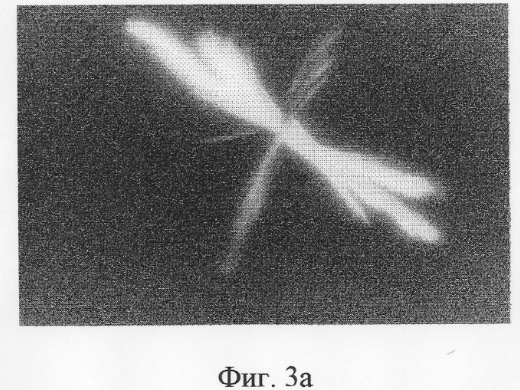
Фиг.3 - Атипичные морфотипы:
а) цветные игольчатые; б) сферолиты с наличием чужеродных вставок; в) состояние аморфизации
Способ осуществляют следующим образом.
Сыворотку крови интактных животных и животных, получающих интрагастрально лекарственное средство, в количестве 20 мкл наносят на поверхность стандартного предметного стекла 75×25 мм, накрывают предметным стеклом 18×18 мм и высушивают при комнатной температуре 18-25°С, относительной влажности воздуха 50-70% в течение 48-72 часов. Предварительно стекла замачивают на 24-48 часов в растворе детергента, затем промывают в проточной воде в течение 10 минут и помещают в смесь Никифорова, состоящую из равных соотношений спирта и эфира на 30 мин. Перед нанесением пробы стекла вытирают сухой безворсовой тканью. Полученные образцы просматривают в поляризованном свете, оценивают форму анизотропных структур, их размеры, цветность, количество, вид морфотипов как базисные, вторичные, атипичные, после чего производят сравнительный анализ опытных и контрольных препаратов. Увеличение содержания вторичных морфотипов при одновременном снижении числа базисных морфотипов в опытных образцах по сравнению с контролем свидетельствует о неблагоприятном влиянии на организм исследуемых лекарственных средств. Появление атипичных форм кристаллов или состояния аморфизации позволяет оценивать лекарственный препарат как препарат токсичного действия.
Предлагаемый способ был успешно апробирован в НИИ по изучению лепры МЗ РФ в течение 2000-2001 г.г. на 350 мышах линии СВА.
Ниже приводятся результаты апробации.
Пример 1
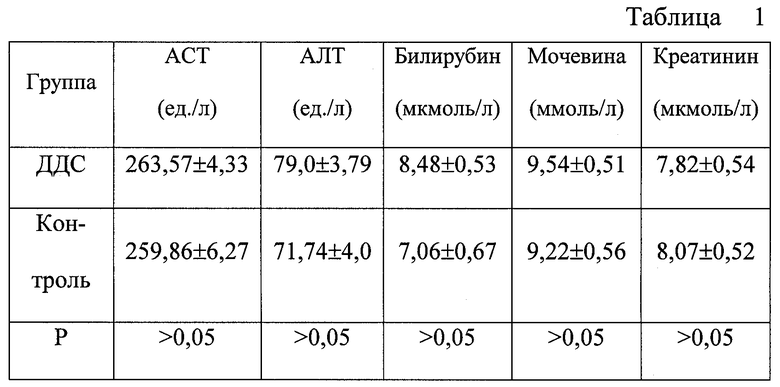
20 мышам линии СВА интрагастрально посредством зонда в дозе 25 мг/кг массы вводили диаминодифенилсульфон (ДДС). Контрольная группа включала интактных животных. По истечении 6 месяцев животных выводили из эксперимента путем декапитации. Производили патоморфологическое исследование внутренних органов (печень, почки), определение биохимических параметров сыворотки крови (ACT, АЛТ, содержание билирубина, креатинина, мочевины), а также оценивали состав морфотипов сыворотки крови.
Микроскопическое строение печени у мышей, получавших ДДС, существенно не отличалось от нормального. В ряде случаев наблюдались гепатоциты с гипертрофированными базофильными ядрами и увеличение количества двуядерных клеток по сравнению с контрольной группой. При гистологическом исследовании ткани почек животных опытной группы патологических изменений не обнаружено.
Согласно данным таблицы 1 количественные показатели биохимических параметров опытной группы не отличались достоверно от контроля, что свидетельствовало об отсутствии токсического действия препарата.
Кристаллограмма сыворотки крови интактных животных была представлена базисными (нитевидные и мелкие сферолиты), а также вторичными (игольчатые и полиморфные) морфотипами. В сыворотке крови животных, получавших ДДС, регистрировались преимущественно базисные морфотипы. На их фоне были обнаружены единичные вторичные морфотипы (таблица 2).
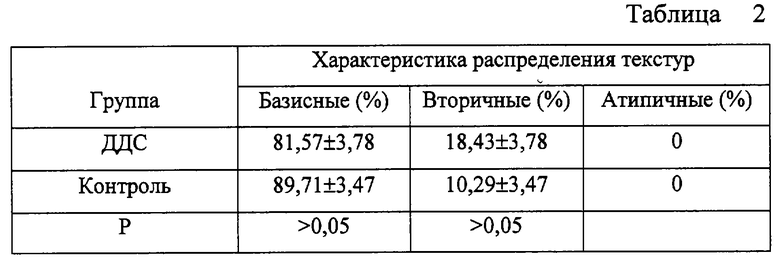
Таким образом, идентичность количественного и качественного состава морфотипов опытной и контрольной групп позволяет сделать вывод, что исследуемое лекарственное средство не является токсичным.
Пример 2
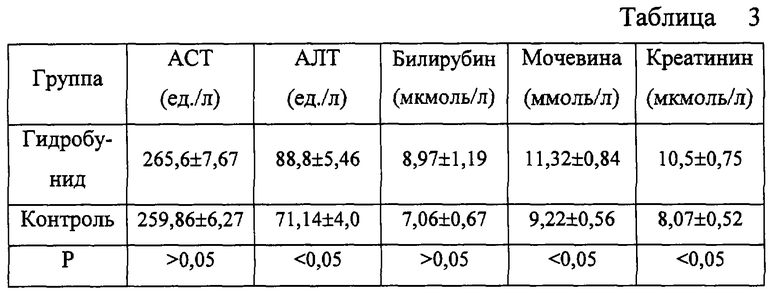
20 мышам линии СВА интрагастрально посредством зонда в течение 6 месяцев ежедневно вводили гидробунид в дозе 40 мг/кг. Контролем служили интактные животные. По окончании эксперимента производили патоморфологическое исследование внутренних органов (печень, почки), определение биохимических, параметров сыворотки крови (ACT, АЛТ, содержание билирубина, креатинина, мочевины), а также оценивали состав морфотипов сыворотки крови.
При гистологическом исследовании ткани печени мышей, получавших гидробунид, отмечались очаговая зернистая дистрофия и некроз единичных гепатоцитов, а также сопутствующая лимфомакрофагальная инфильтрация. При микроскопическом изучении ткани почек мышей опытной группы отмечалась умеренная дистрофия эпителия извитых канальцев.
Согласно результатам биохимических исследований, представленным в таблице 3, количество билирубина в опытной группе превышало аналогичный показатель в контроле, увеличение содержания АЛТ, креатинина и мочевины у животных, получавших лекарственное средство, носило достоверный характер. Полученные данные свидетельствуют о неблагоприятном действии препарата на гепатобилиарную и мочевыделительную системы.
В сыворотке крови интактных животных отмечались базисные и вторичные морфотипы. Состав морфотипов сыворотки крови опытной группы животных был представлен единичными базисными и большим количеством вторичных (таблица 4).
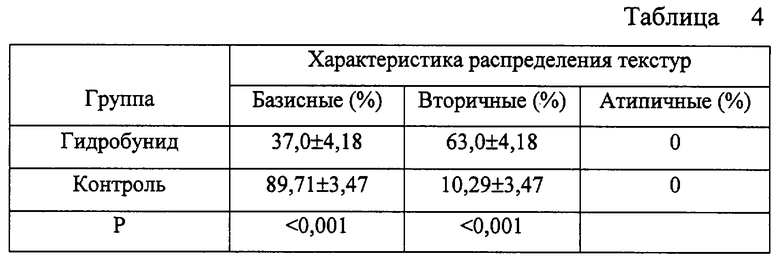
Из представленных данных видно, что увеличение содержания вторичных морфотипов в сыворотке крови при одновременном уменьшении числа базисных по сравнению с контролем служит критерием неблагоприятного влияния лекарственного средства на организм.
Пример 3
20 мышам линии СВА интрагастрально посредством зонда в течение 6 месяцев ежедневно вводили фуразонал в дозе 0,75 г/кг. Контролем служили интактные животные. По окончании эксперимента производили патоморфологическое исследование внутренних органов (печени, почек), определение биохимических параметров сыворотки крови (ACT, АЛТ, содержание билирубина, креатинина, мочевины), а также оценивали состав морфотипов сыворотки крови.
При гистологическом изучении печени наблюдались выраженные изменения: диффузная зернистая дистрофия и некрозы целых групп гепатоцитов, расположенные как в центральных, так и в периферийных отделах печеночной дольки. При микроскопическом изучении ткани почек мышей опытных групп наблюдались воспалительная инфильтрация стромы пирамид лимфоцитами, плазматическими клетками с примесью эозинофилов и некроз эпителия извитых канальцев почки.
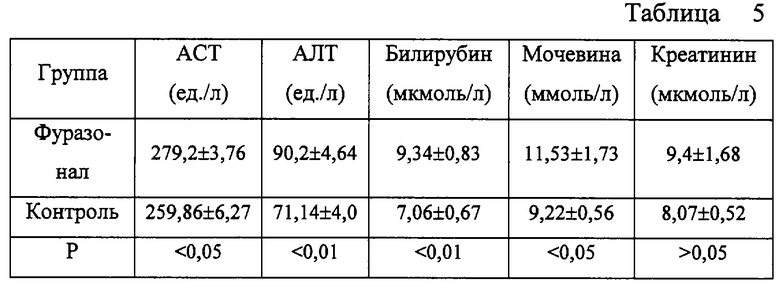
В сыворотке крови животных, получавших фуразонал, отмечалось значительное повышение изучаемых биохимических показателей, достоверным оказалось различие в содержании АЛТ, ACT, билирубина, мочевины, что указывает на наличие побочного действия препарата (таблица 5).
В сыворотке крови интактных животных регистрировались преимущественно базисные морфотипы.
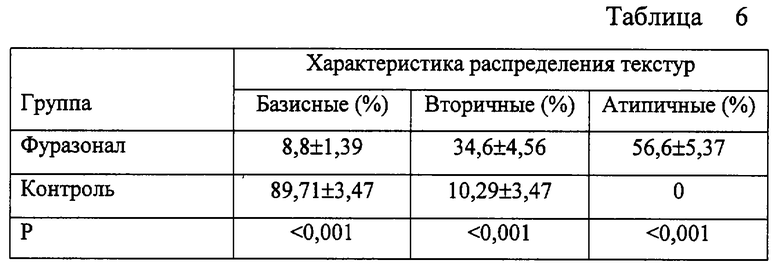
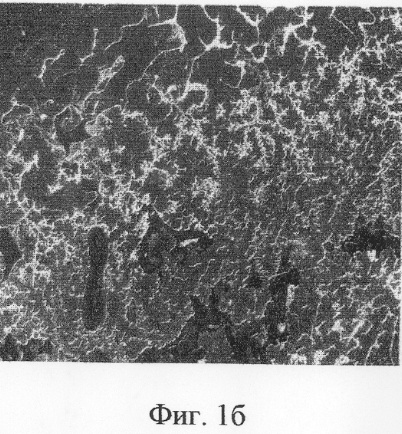
В сыворотке крови опытной группы животных преобладал атипичный состав морфотипов (цветные игольчатые, сферолиты с наличием чужеродных вставок). Также было зарегистрировано незначительное число базисных и вторичных морфотипов (таблица 6).
Появление атипичных морфотипов в сыворотке крови животных, получавших фуразонал, коррелирует с данными патоморфологического исследования внутренних органов и значительными отклонениями биохимических показателей, что свидетельствует о токсичности лекарственного средства.
Пример 4
20 мышам линии СВА интрагастрально посредством зонда в течение 6 месяцев ежедневно вводили комбинацию препаратов: фуразонал в дозе 0,25 г/кг, ДДС в дозе 10 мг/кг и рифампицин в дозе 0,25 г/кг. Контролем служили интактные животные. По окончании эксперимента производили патоморфологическое исследование внутренних органов (печень, почки), определение биохимических параметров сыворотки крови (ACT, АЛТ, содержание билирубина, креатинина, мочевины), а также оценивали состав морфотипов сыворотки крови.
При гистологическом исследовании внутренних органов наблюдались изменения, характерные для токсического гепатита (дистрофия и некроз гепатоцитов, сопутствующая воспалительная реакция).
При микроскопическом исследовании почек наряду с некрозом канальцевого эпителия отмечались отек и клеточная инфильтрация межуточной ткани.
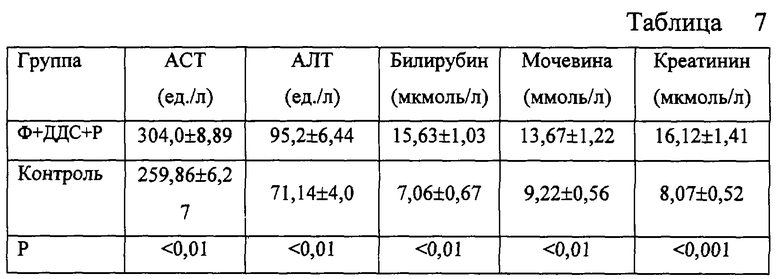
Результаты биохимических исследований, представленные в таблице 7, свидетельствуют о достоверном повышении изучаемых показателей в опытной группе по сравнению с интактными животными, что указывает на наличие токсического действия используемого комплекса лекарственных средств.
При просмотре образцов сыворотки крови животных, получавших указанный комплекс лекарственных средств, в поляризованном свете обнаружено темное изотропное поле (состояние аморфизации), являющееся следствием угнетения структурирования и характеризующее состояние гомеостаза как декомпенсированное.
Таким образом, отсутствие анизотропных структур в сыворотке крови опытных животных коррелирует со значительными отклонениями биохимических показателей от контроля, что свидетельствует о выраженной токсичности используемых лекарственных средств.
Применением предложенного способа по сравнению со способом-прототипом достигается положительный результат, заключающийся в упрощении способа. Способ прост в техническом исполнении и анализе результатов, отсутствует многоэтапность, исключается необходимость оценки комплекса биохимических показателей, способ осуществим с использованием незначительного количества сыворотки крови, что актуально для экспериментальных исследований, возможно использование исследуемого материала через год после хранения при -18°С. Способ экономичен, не требует наличия специализированной лаборатории, использования дорогостоящей аппаратуры, реактивов, красителей.
Предлагаемый способ может быть рекомендован к использованию в морфологических, биохимических, микробиологических лабораториях научно-исследовательских учреждений.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ПРОТИВОЛЕПРОЗНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2003 |
|
RU2242761C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО "КАРСИЛИН" | 2002 |
|
RU2205637C1 |
| Способ оценки эффективности применения лекарственного препарата "Лаеннек" на фармакологической модели неалкогольной жировой болезни печени с перегрузкой железом у экспериментальных животных | 2024 |
|
RU2837019C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АДАПТОГЕННОЙ И ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2013 |
|
RU2516886C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИБРИДНОГО ПРОИСХОЖДЕНИЯ ОСЕТРОВЫХ РЫБ | 2003 |
|
RU2257053C2 |
| АНАЛЬГЕТИЧЕСКОЕ, ЖАРОПОНИЖАЮЩИЕ И ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО "ПЕНТАБУФЕН" | 2002 |
|
RU2222322C1 |
| Средство, проявляющее гепатопротекторную, липидрегулирующую, противоишемическую и нейротропную активность | 2018 |
|
RU2705575C1 |
| Применение пентааминокислотных производных фуллеренов в качестве антиоксидантов и антидиабетических средств | 2016 |
|
RU2669341C2 |
| СПОСОБ ЛЕЧЕНИЯ АЛКОГОЛИЗМА | 1990 |
|
RU2007171C1 |
| СРЕДСТВО С ПАНКРЕО- И ГЕПАТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ ДЛЯ ПАРЕНТЕРАЛЬНОГО ВВЕДЕНИЯ | 2017 |
|
RU2662324C1 |



Изобретение относится к области медицины, а именно к лабораторным методам исследования. Сущность способа: проводят микроскопическое исследование сыворотки крови, для чего сыворотку крови интактных животных и животных, получающих исследуемое лекарственное средство, в количестве 20 мкл наносят на поверхность предметного стекла, накрывают покровным стеклом, высушивают при комнатной температуре в течение 48-72 часов, производят сравнительный анализ анизотропных морфотипов и при увеличении в опытных образцах содержания вторичных морфотипов наряду с одновременным снижением числа морфотипов нормы по сравнению с контролем судят о неблагоприятном влиянии на организм исследуемого лекарственного средства, а при наличии в опытных образцах атипичных морфотипов или состояния аморфизации судят о его токсичном действии. Способ прост в техническом исполнении, экономичен, не требует дорогостоящего оборудования и реактивов. 7 табл., 3 ил.

Способ оценки общетоксического действия лекарственных средств на организм, включающий микроскопическое исследование сыворотки крови, отличающийся тем, что сыворотку крови интактных животных и животных, получающих исследуемое лекарственное средство, в количестве 20 мкл наносят на поверхность предметного стекла, накрывают покровным стеклом, высушивают при комнатной температуре в течение 48-72 ч, производят сравнительный анализ анизотропных морфотипов и при увеличении в опытных образцах содержания вторичных морфотипов наряду с одновременным снижением числа морфотипов нормы по сравнению с контролем судят о неблагоприятном влиянии на организм исследуемого лекарственного средства, а при наличии в опытных образцах атипичных морфотипов или состояния аморфизации судят о его токсичном действии.
| МОРФОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ | |||
| Гигиенические критерии состояния окружающей среды, 6 | |||
| Ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Принципы и методы оценки токсичности химических веществ | |||
| - Женева: ВОЗ, 1981, с | |||
| Ротационный фильтр-пресс для отжатия торфяной массы, подвергшейся коагулированию, и т.п. работ | 1924 |
|
SU204A1 |
| СПОСОБ СЕРТИФИКАЦИИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1995 |
|
RU2124202C1 |
| Способ определения токсичности водорастворимых веществ | 1989 |
|
SU1656454A1 |
| Способ определения токсичности биологически активных веществ | 1979 |
|
SU991302A1 |
| WO 9961910 A1, 02.12.1999. | |||
Авторы
Даты
2004-07-10—Публикация
2002-11-04—Подача