Изобретение относится к медицине, в частности, к лекарственным средствам, обладающим анальгетическим, жаропонижающим и противовоспалительным действием, и может быть использовано при различных состояниях, сопровождающихся болевым синдромом - головной болью, миалгией, невралгией, артралгией и ряде других заболеваний.
В повседневной практике в качестве анальгетических, жаропонижающих и противовоспалительных средств широко используют ненаркотические анальгетики и нестероидные противовоспалительные препараты. К первым относятся антипирин, амидопирин, анальгин, фенацетин, парацетамол, а также композиции, содержащие перечисленные лекарственные вещества, например, цитрамон-П, включающий ацетилсалициловую кислоту, парацетамол, кофеин, лимонную кислоту и какао (М. Д. Машковский "Лекарственные средства", изд. 13, Торсинг, Харьков, 1997, т. 1, с.164), зарубежные комбинированные препараты: Колдрекс, Солпадеин, Панадол-экстра (там же, с.162-164), Пенталгин ICN, содержащий анальгина и парацетамола по 0,3 г, кофеина 0,05 г, кодеина 0,008 г и фенобарбитала 0,01 г (РЛС России, Энциклопедия лекарств, 1999, 6-ое изд., с.850-851).
Ко вторым относятся ацетилсалициловая кислота и ее производные, бутадион, ибупрофен, ортофен, индометацин, напроксен, пироксикам, кетопрофен (М.Д. Машковский "Лекарственные средства", изд. 13, Торсинг, Харьков, 1997, т.1, с.165-175).
Известно средство, обладающее анальгетическим действием, содержащее в качестве активного вещества калия 2,4-дихлорбензоат и вспомогательные вещества (патент RU 2101011, 1994).
Известна болеутоляющая композиция, содержащая в качестве активного компонента кетопрофен в смеси с его энантиомерами (патент RU 2125873, 1992). В патенте RU 2134577, 1992 описана фармацевтическая композиция, содержащая ибупрофен, стабилизатор и вспомогательные вещества, композиция используется как болеутоляющее средство и может быть выполнена в форме шипучих таблеток.
Известна твердая нешипучая прессованная дозированная форма ибупрофена, включающая ибупрофеновый лекарственный ингредиент и носитель (патент RU 2182000, 1996).
Широкое применение находят также композиции, содержащие одновременно ненаркотические анальгетики и нестероидные противовоспалительные препараты, например, пенталгин-Н, содержащий анальгин, напроксен, кофеин и фенобарбитал при определенном соотношении компонентов (РЛС России, Энциклопедия лекарств, 1999, 6-ое изд., с.851). Пенталгин-Н является наиболее близким к заявленному по техническому результату и составу и принят за прототип. Ненаркотические анальгетики и нестероидные противовоспалительные препараты вызывают ряд побочных эффектов: аллергические реакции, угнетение кроветворения, а нестероидные противовоспалительные препараты, кроме того, эрозиво-язвенные поражения ЖКТ, диспептические расстройства, боли в эпигастрии.
Задачей настоящего изобретения является создание анальгетического, жаропонижающего и противовоспалительного лекарственного средства, обладающего высоким терапевтическим эффектом и низкой токсичностью.
Поставленная задача решается тем, что предложено анальгетичечское, жаропонижающие и противовоспалительное средство, содержащее анальгин, ибупрофен, кофеин, кодеин и фенобарбитал при следующем содержании ингредиентов на 1 таблетку, мг:
Анальгин - 300
Ибупрофен - 200
Кофеин - 50
Кодеин - 8
Фенобарбитал - 10
Вспомогательные вещества - До массы таблетки 768
Технический результат, получаемый при использовании изобретения, выражается в повышении терапевтического эффекта и снижении нежелательных побочных эффектов.
Заявленное средство (таблетки "Пентабуфен") получают путем прямого прессования смеси активных субстанций со вспомогательными веществами, с предварительным брикетированием; кодеина фосфат вводят тритурацией с частью анальгина.
Пример 1
Заявленное средство имеет следующий состав, мг на 1 таблетку:
Анальгин - 150
Ибупрофен - 150
Кофеин - 40
Кодеин - 8
Фенобарбитал - 5
Вспомогательные вещества - До массы таблетки 768 мг
Пример 2
Заявленное средство имеет следующий состав, мг на 1 таблетку:
Анальгин - 300
Ибупрофен - 200
Кофеин - 50
Кодеин - 8
Фенобарбитал - 10
Вспомогательные вещества - До массы таблетки 768
Пример 3
Заявленное средство имеет следующий состав, мг на 1 таблетку:
Анальгин - 400
Ибупрофен - 300
Кофеин - 75
Кодеин - 10
Фенобарбитал - 25
Вспомогательные вещества - До массы таблетки 768
Экспериментально подтверждено, что именно заявленный качественный и количественный состав композиции обеспечивает достижение заявленного технического результата.
Были проведены испытания заявленного средства:
1. Изучение токсичности.
2. Изучение специфической (анальгетической, жаропонижающей и противовоспалительной) активности.
Так как все действующие компоненты данного препарата хорошо изучены и с успехом применяются в медицине как отдельно, так и в различных сочетаниях, токсикологисечкие исследования были проведены в следующем объеме:
1. Изучение токсичности субстанции пентабуфена при однократном введении различным видам лабораторных животных.
2. Исследования токсичности готовой лекарственной формы пентабуфена (таблетки) на кроликах в 4-недельном эксперименте.
Изучение специфической активности заявленного средства "Пентабуфен" было проведено в сравнительном аспекте с известными и широко используемыми препаратами Пенталгин ICN и Пенталгин-Н, поскольку все три композиции содержат ненаркотические анальгетики и нестероидные противовоспалительные средства, а именно Пенталгин ICN содержит в качестве нестероидного противовоспалительного средства парацетамол, Пенталгин-Н-напроксен и заявленный препарат Пентабуфен-ибупрофен, причем известно, что парацетамол обладает слабой, а напроксен и ибупрофен - примерно одинаковой противовоспалительной активностью.
1. Изучение токсичности субстанции пентабуфена при однократном введении различным видам лабораторных животных
Исследования были выполнены в соответствии с "Методическими рекомендациями по изучению общетоксического действия фармакологических средств" (1998).
Токсичность субстанции пентабуфена изучали на белых беспородных мышах обоего пола с массой тела 18-20 г и белых беспородных крысах, самцах и самках (масса тела 180-200 г), при однократном внутрибрюшинном и внутрижелудочном способах введения.
Лабораторные животные получены из питомника "Крюково" и содержались в виварии ВНИИ лекарственных и ароматических растений в соответствии с принятыми санитарными нормами (нормальный световой и температурный режим, свободный доступ к воде, сбалансированный по питательности гранулированный корм и т.д.). Все животные прошли двухнедельный карантин в условиях вивария.
Субстанцию пентабуфена вводили в виде 0,1-30% водных растворов, подогретых до 45-50oС в объеме 0,1-0,7 мл на животное.
Длительность наблюдений за мышами и крысами составляла 10-14 дней. Отмечали реакцию на окружающие раздражители, двигательную активность, внешний вид, а в случаях летального исхода фиксировали клиническую картину и число погибших мышей и крыс.
Определение параметров токсичности пентабуфена при однократном внутрибрюшинном и внутрижелудочном способах введения проверено с использованием метода Дейхмана и Лебланка (1943) - определение ориентировочной среднесмертельной дозы, и метода пробит-анализа по Литчфилду и Уилкоксону (М.Л.Беленький, 1963).
При внутрибрюшинном введении пентабуфена мышам в дозах от 50 до 100 мг/кг признаков интоксикации не наблюдалось.
С увеличением дозы до 120-150 мг/кг у мышей через 3-5 мин отмечалось беспокойство, через 8-10 мин двигательное возбуждение, груминг. Через 15-20 мин у животных отмечалась отдышка, цианоз ушных раковин и хвоста. Позднее (через 2-3 ч) симптомы возбуждения сменялись угнетением ЦНС.
С дальнейшим увеличением дозы до 160-170 мг/кг у животных наблюдалось дыхание Чейн-Стокса, клонико-тонические судороги и гибель отдельных мышей, наступавшая в первые 2-3 ч.
Клиническая картина острой интоксикации пентабуфеном у белых беспородных крыс при внутрибрюшинном введении существенно не отличалась от вышеописанной у мышей, однако гибель животных от доз, близких к среднесмертельным, наступала в конце первых суток после введения препарата.
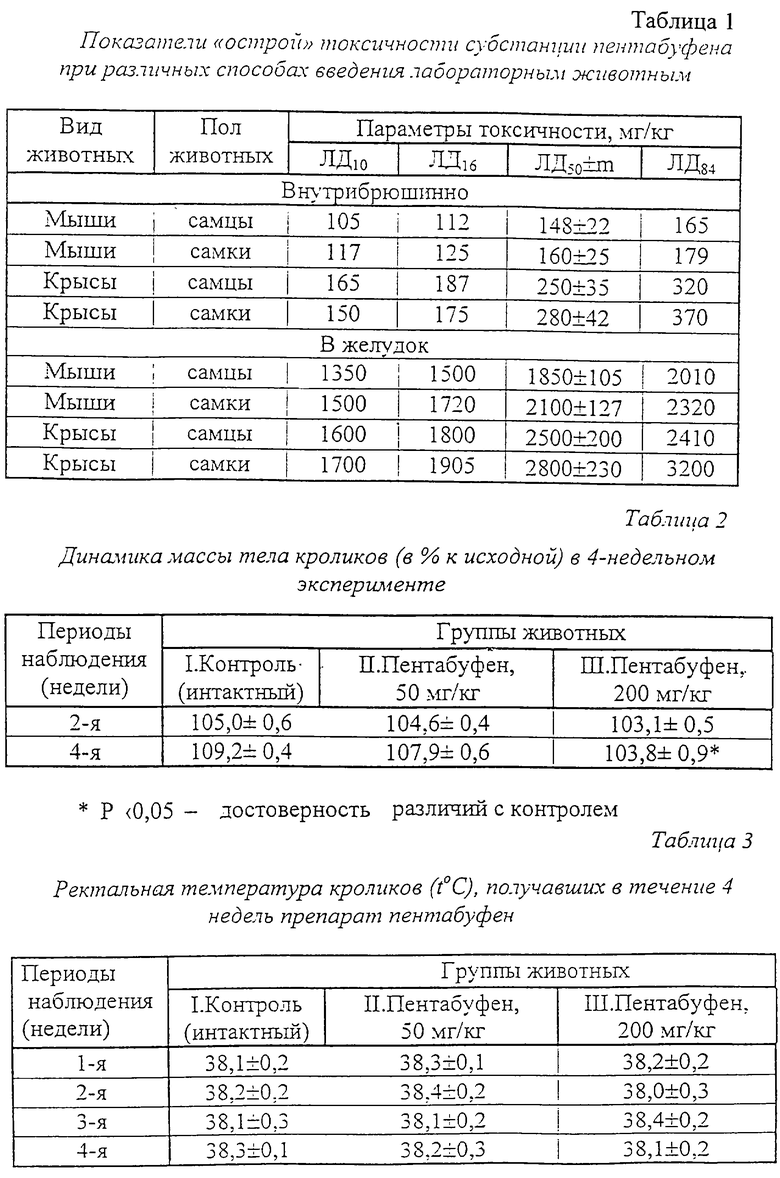
По параметрам LD50 мыши оказались более чувствительными к действию препарата, однако статистически достоверных различий в показателях среднесмертельных доз для мышей и крыс установлено не было (таблица 1).
При введении пентабуфена в желудок мышам и крысам в широком диапазоне доз от 500 до 1300 мг/кг признаков острого отравления у животных отмечено не было. Увеличение доз до 2000-2500 мг/кг вызывало у животных картину острой интоксикации, существенно не отличающуюся от описанной выше, однако симптомы отравления были менее выражены и проявлялись в более поздние сроки после введения препарата. Гибель мышей и крыс при введении пентабуфена в дозах, близких к среднесмертельным, отмечалась в течение двух суток.
Анализ данных, представленных в таблице 1, свидетельствует о том, что показатели LD50 при введении субстанции пентабуфена в желудок мышам и крысам возрастают примерно в 10 раз по сравнению со среднесмертельными дозами препарата при внутрибрюшинном введении. Отмечена некоторая тенденция к увеличению чувствительности самцов мышей и крыс под воздействием препарата.
Таким образом, проведенные исследования показали, что по параметрам LD50 при однократном внутрибрюшинном и внутрижелудочном способах введения мышам и крысам обоего пола пентабуфен следует отнести к IV классу токсичности - малотоксичным веществам (по классификации токсичности, принятой в РФ и ВОЗ, К. К.Сидоров, 1973).
2. Исследование токсичности препарата пентабуфен на кроликах в 4-недельном эксперименте
Изучение токсичности готовой лекарственной формы пентабуфена - таблетки (0,57 г по сумме действующих веществ) проведено на 15 кроликах-самцах породы Шиншилла с первоначальной массой 2,5-3,0 кг. Животные были разделены на 3 группы по 5 кроликов в каждой: I группа контроль (интактная), II - группа пентабуфен, 50 мг/кг; III - группа пентабуфен, 200 мг/кг массы тела.
Максимальная из испытанных доз препарата в 20 раз превышала терапевтическую, рекомендованную для человека (10 мг/кг).
Препарат вводили кроликам ежедневно, внутрь, один раз в день в течение 4 недель. Таблетки пентабуфена при помощи роторасширителя помещали на корень языка кроликам, а затем водой, струйно, мягким зондом смывали препарат.
Во время эксперимента у кроликов отмечали общее состояние, двигательную активность, аппетит, динамику массы тела, состояние шерстного покрова, реакцию на внешние раздражители. Перед началом эксперимента у животных брали кровь для определения некоторых фоновых показателей (число эритроцитов, лейкоцитов, содержание гемоглобина). В течение всего эксперимента регулярно проводили термометрию.
Через 2 и 4 недели после начала введения препарата исследовали морфологический состав периферической крови (общее количество лейкоцитов, эритроцитов, тромбоцитов, содержание гемоглобина, гемограммы), биохимические показатели (общий белок, общий и прямой билирубин, общий холестерин, общие липиды, мочевина, глюкоза), а также активность некоторых ферментов сыворотки крови (щелочная фосфатаза, аланин- и аспартаттрансаминазы).
В конце хронического эксперимента была проведена бромсульфалеиновая проба (Й.Тодоров, 1968).
Кровь у кроликов брали из краевой вены уха в количестве 2,0-2,5 мл.
Для определения состояния сердечно-сосудистой системы кроликов на 4-й неделе на полиграфе "Салют" снимали электрокардиограммы во II стандартном отведении.
Общее количество лейкоцитов, эритроцитов, тромбоцитов в периферической крови животных определяли на автоматическом счетчике клеток "Пикоскель", гемоглобин - гемиглобинцианидным методом, гемограмму - на окрашенных по Романовскому-Гинзе мазках крови (А.А.Кудрявцев и Л.А.Кудрявцева, 1974, В.В. Меньшиков, 1987).
Активность сывороточных ферментов - аланин- и аспартаттрансаминаз, а также общего и прямого билирубина, общих липидов, мочевины и глюкозы определяли с помощью биохимических наборов фирмы "Диаком-Синтэко" (Россия); общий белок сыворотки крови - рефрактометрически на приборе RL-2, общий холестерин - применяя биохимический набор фирмы "Новохол" (Россия), щелочную фосфатазу с помощью набора фирмы "LANCHEMA".
После окончания эксперимента и эвтаназии животных методом воздушной эмболии определяли коэффициенты массы и проводили патогистологическое исследование внутренних органов кроликов.
Все цифровые данные, полученные в эксперименте, обрабатывались методом вариационной статистики с применением критерия "t" Стьюдента.
Как показали проведенные исследования, пентабуфен при длительном применении не влиял на общее состояние и поведение животных. У них сохранился гладкий шерстный покров, был хороший аппетит. Животные адекватно реагировали на внешние раздражители. Под действием пентабуфена в максимальной дозе - 200 мг/кг у кроликов на 4-й неделе было отмечено статистически достоверное снижение массы тела (таблица 2).
Ни в одной из групп не было отмечено гибели животных.
Пентабуфен, в условиях хронического эксперимента, не влиял на ректальную температуру кроликов, которая на протяжении всего опыта находилась на уровне 38,0-38,4oС (таблица 3).
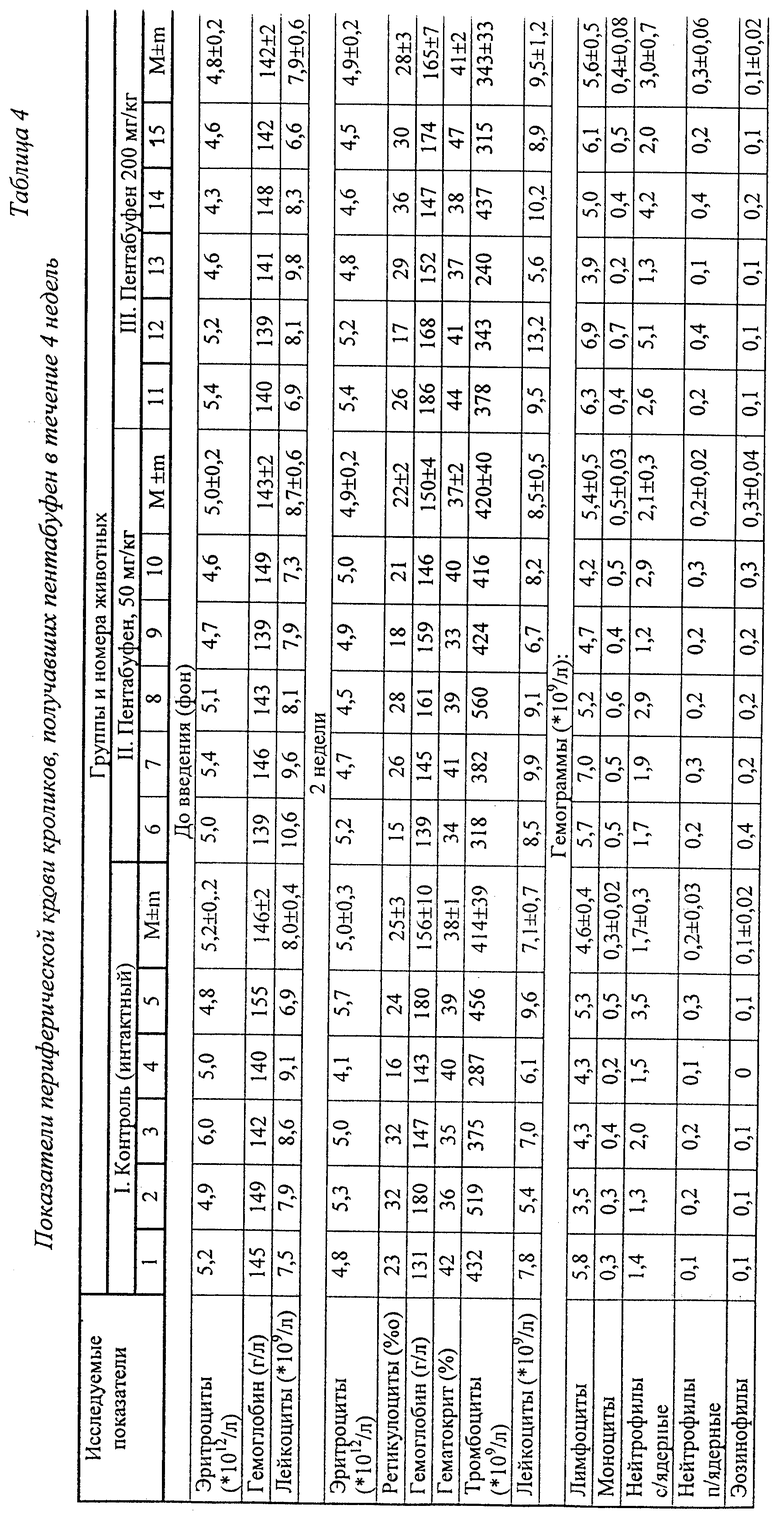
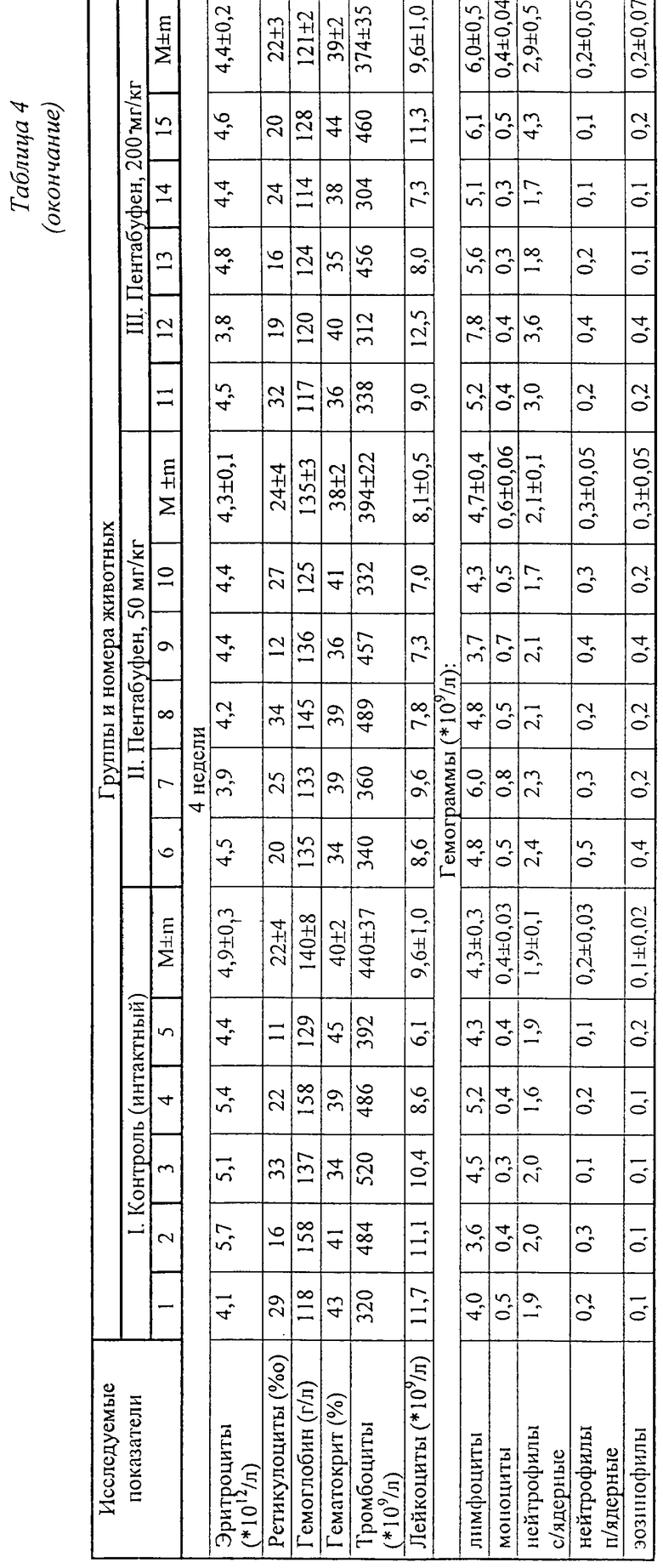
Длительное введение пентабуфена в испытанных дозах не влияло на морфологический состав периферической крови. При подсчете гемограмм, как видно из таблицы 4, количество различных форменных элементов крови - лимфоцитов, моноцитов, гранулоцитов во всех экспериментальных группах существенно не различалось. В мазках крови не обнаружено каких-либо патологически измененных клеток. Число эритроцитов, лейкоцитов, тромбоцитов и количество гемоглобина у опытных и контрольных кроликов также не выходило за границы физиологической нормы во все периоды исследований.
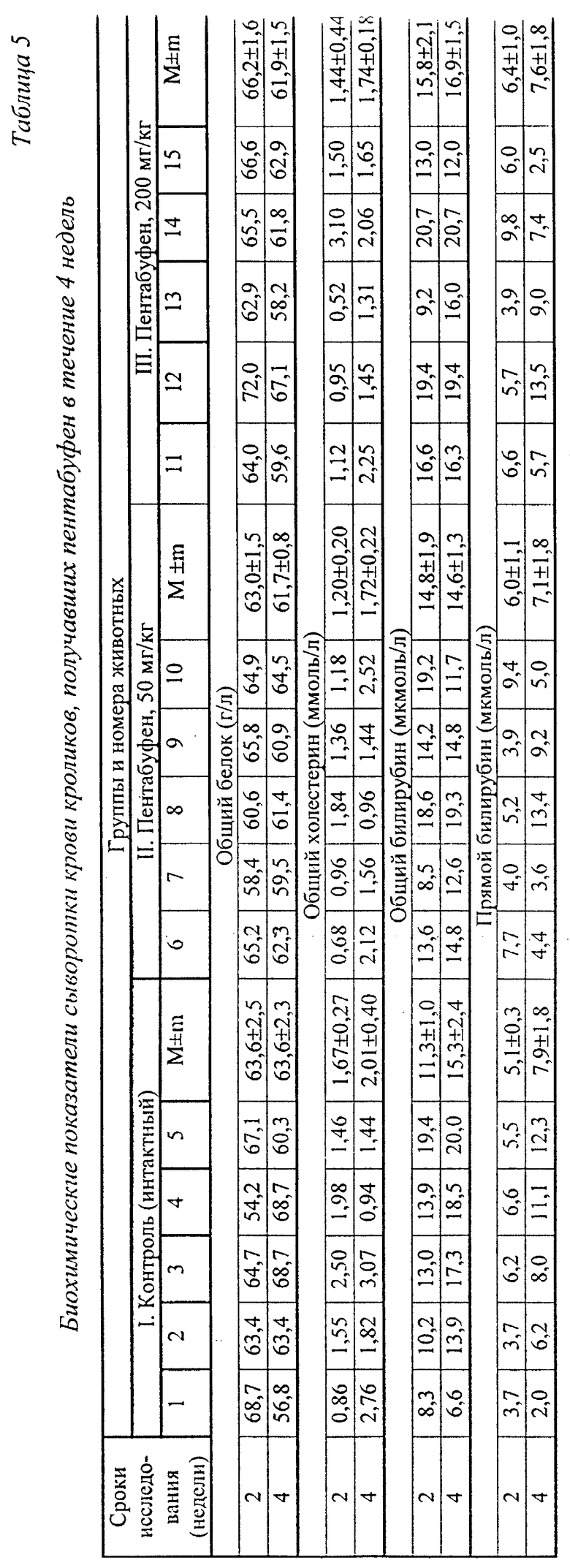
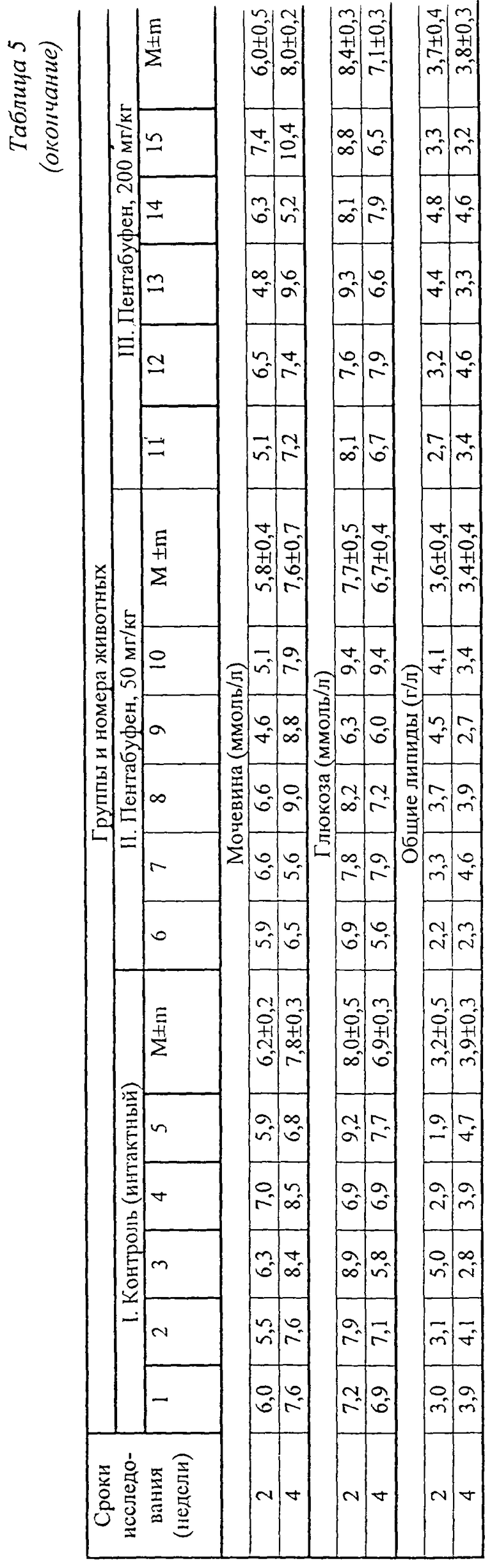
Как показали биохимические исследования сыворотки крови (общий белок, общий холестерин, общий и прямой билирубин, общие липиды, глюкоза и мочевина), введение пентабуфена кроликам в течение месяца не вызывало изменений указанных показателей по сравнению с контролем (таблица 5).
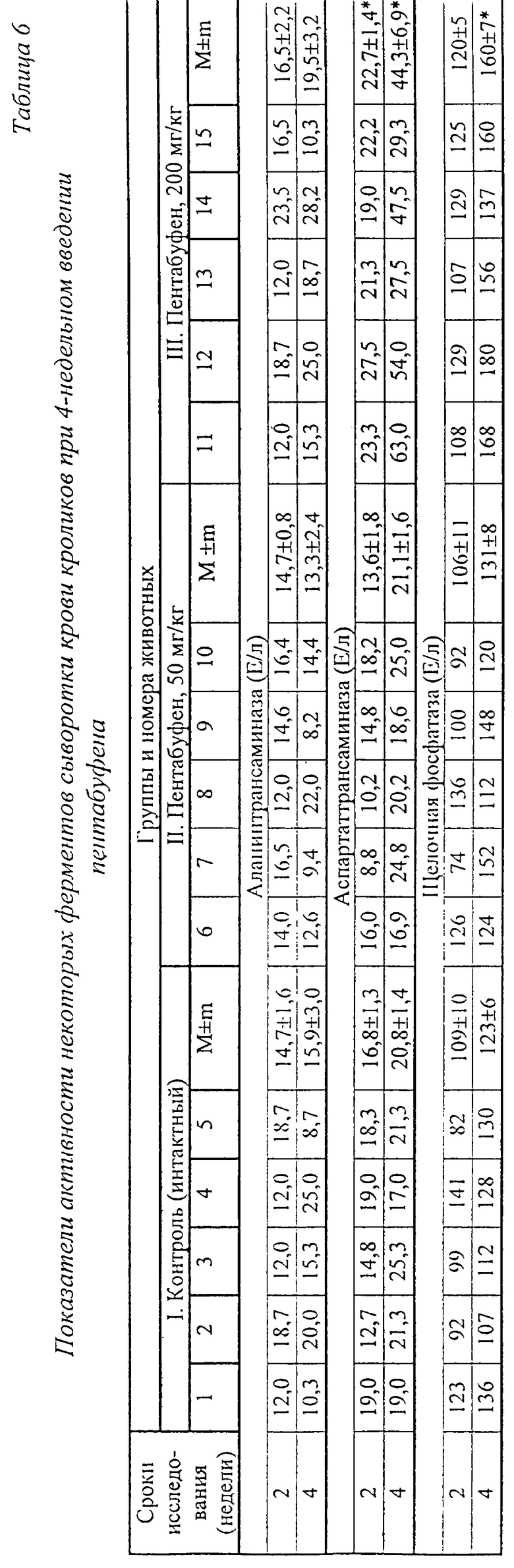
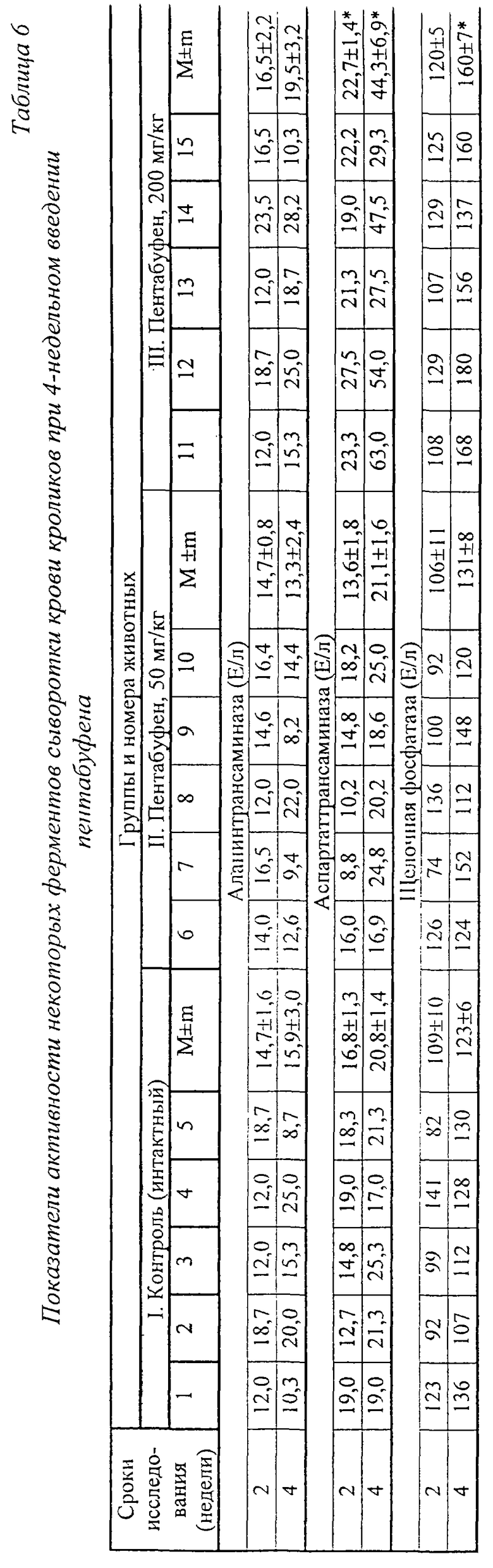
При исследовании некоторых ферментов сыворотки крови кроликов, получавших пентабуфен в дозах 50 и 200 мг/кг, установлено достоверное увеличение показателей активности аспартаттрансаминазы на 2 и 4-и неделях опыта и щелочной фосфатазы на 4-й неделе эксперимента, что может характеризовать повреждающее действие исследуемого препарата на функциональное состояние печени. Активность аланинтрансаминазы у кроликов опытных групп не отличалась от показателей в контроле (таблица 6).
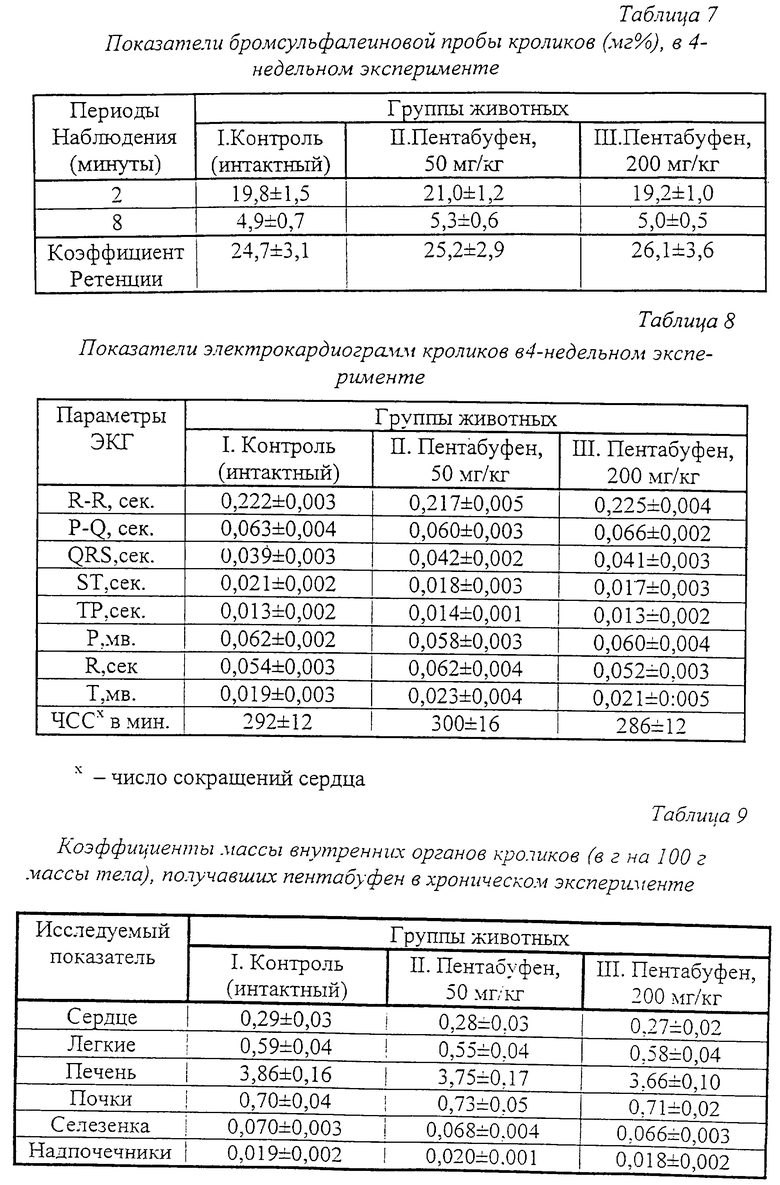
Для изучения действия препарата на экскреторную функцию печени была проведена бромсульфалеиновая проба (таблица 7).
Как видно из таблицы 7, пентабуфен в испытанных дозах не влиял на выделение красителя из организма экспериментальных животных, как в динамике через 2 и 8 мин, так и по коэффициенту ретенции, что свидетельствует об отсутствии влияния препарата на экскреторную функцию печени.
Под воздействием пентабуфена существенно не изменилось и состояние сердечно-сосудистой системы, о чем судили по записи электрокардиограмм во II стандартном отведении на 4-й неделе эксперимента (таблица 8).
После завершения опыта и эвтаназии животных были определены коэффициенты массы внутренних органов кроликов. Как видно из таблицы 9, у животных всех экспериментальных групп коэффициенты массы внутренних органов практически не различались.
После окончания эксперимента было проведено макро- и микроскопическое исследование внутренних органов животных.
При вскрытии животных обеих групп и визуальном исследовании внутренних органов каких-либо патологических изменений не определялось.
Изучение специфической активности заявленного препарата
Эксперименты по оценке анальгетической активности выполнены в соответствии с Методическими Рекомендациями, одобренными Фармакологическим государственным комитетом Минздрава России "Экспериментальное изучение препаратов, предлагаемых для клинических испытаний в качестве обезболивающих средств преимущественно центрального действия и их антагонистов" (Ведомости Фармакологического Комитета, 1998, 3, 30-31).
Эксперименты по оценке анальгетической активности выполнены в соответствии с Методическими Рекомендациями по экспериментальному (доклиническому) изучению нестероидных противовоспалительных фармакологических веществ, одобренными Фармакологическим Комитетом Минздрава СССР и утвержденными Управлением по внедрению новых лекарственных средств и медицинской техники 20.11.82.
Об анальгезирующей активности изучаемых препаратов судили по изменению выраженности болевой реакции при различных видах болевого раздражения.
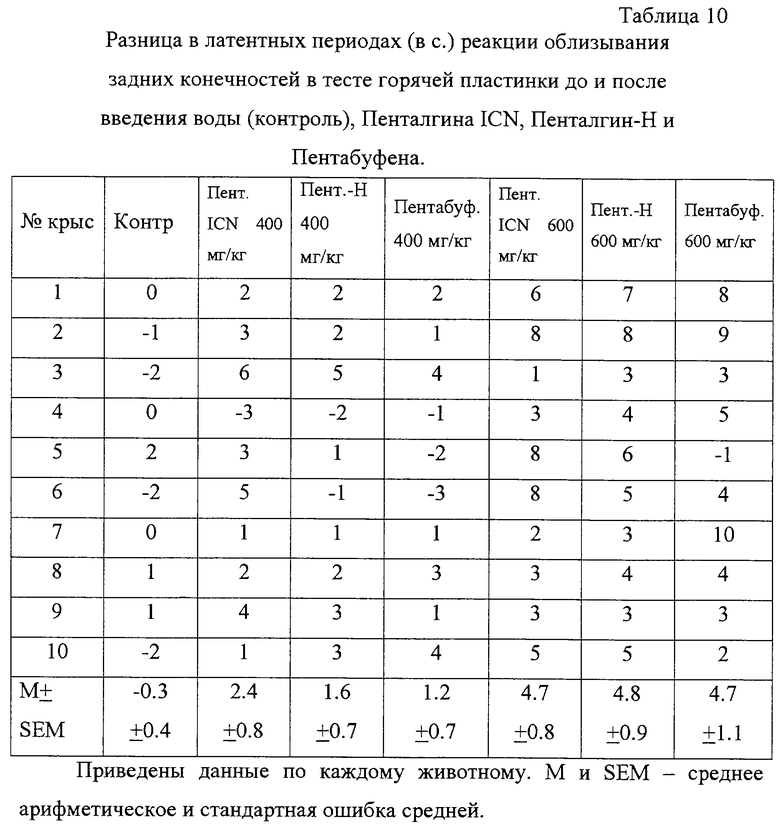
а. Оценка реакции на контактно-болевое раздражение проводилась на самцах беспородных белых крыс (масса 180-220 г). Крысы помещались на металлическую пластинку, с постоянной температурой 55oС, поддерживаемой с помощью термостата. Определялась исходная болевая чувствительность данной крысы по латентному времени начала облизывания задних лапок после помещения крыс на горячую пластинку. Затем экспериментальные животные случайным образом разделялись на четыре группы по 10 крыс в каждой. Крысам первой группы за 30 мин до повторного тестирования перорально вводили воду из расчета 0,2 мл/100 г массы, животным второй группы за 30 мин до повторного тестирования - Пенталгин ICN, животным третьей группы за 30 мин до повторного тестирования - Пенталгин-Н, животным четвертой группы за 30 мин до повторного тестирования - Пентабуфен. Анальгетический эффект оценивали по разнице латентного периода реакции облизывания задних конечностей до и после введения исследуемого препарата и воды. Пенталгин ICN, Пенталгин-Н и Пентабуфен вводились в дозах 400 и 600 мг/кг. Каждая из четырех групп в этом и всех нижеописанных тестах состояла из 10 животных.
Данные приведены в таблице 10.
Как следует из данных, представленных в таблице 10, Пенталгин ICN, Пенталгин-Н и Пентабуфен проявляют анальгетическое действие во всех использованных тестах на анальгетический эффект. В тесте горячей пластинки они в 4-8 раз увеличивают интервал между помещением животных на горячую пластинку и возникновением двигательной реакции животных на температурное раздражение. Статистически достоверных различий между изученными препаратами по тесту горячей пластинки не выявлено.
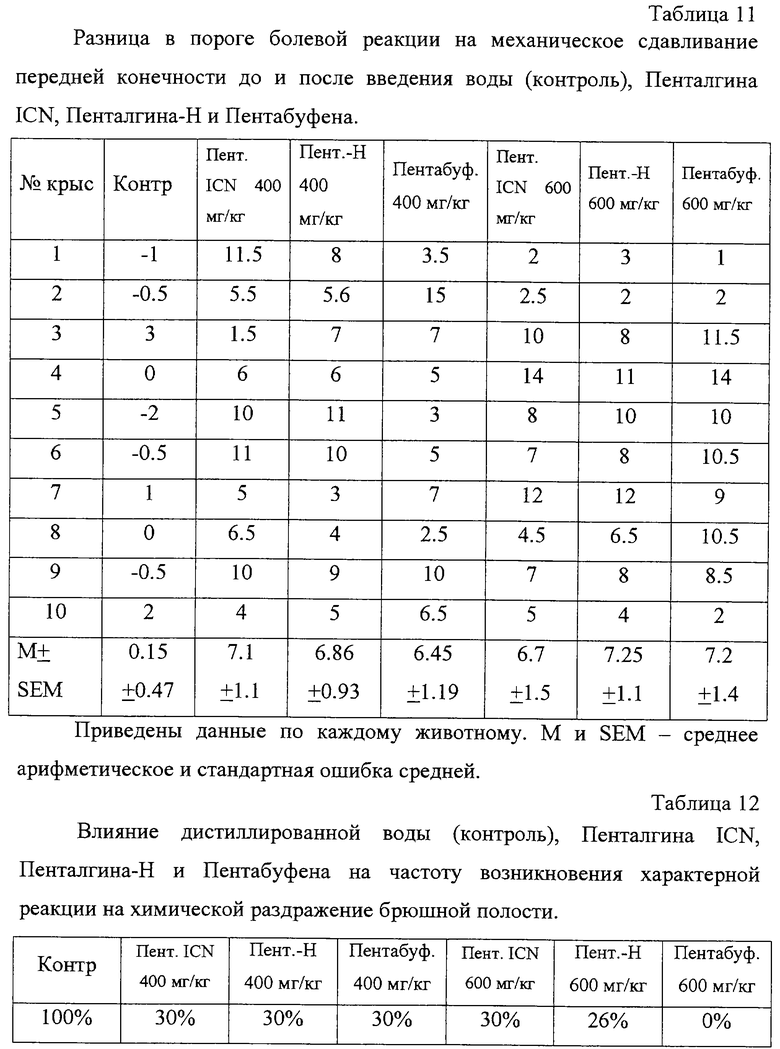
б. Влияние препаратов на чувствительность к механическому раздражению оценивалось в тесте с механическим сдавливанием передней конечности. Опыты выполнены на самцах беспородных белых крыс (масса 180-220 г). Сдавливание лапы осуществлялось с помощью Аналгезиметра фирмы Hugo Basil (Италия). Появление боли фиксировалось по писку животного. Степень нарастания порога болевой реакции (выражаемая в изменении у данного животного силы сдавливания конечности после воздействия препарата или воды) характеризует выраженность анальгетического действия препарата. Разделение животных на экспериментальные группы и режим введения препаратов аналогичны описанным выше для теста горячей пластинки.
Данные об эффективности изученных препаратов на модели механического воздействия представлены в таблице 11. Из нее следует, что все три изученных препарата обладают выраженным анальгетическим действием. Они увеличивают пороговую силу механического раздражения, при котором возникает ответная реакция крыс (вокализация) на болевое раздражение в 40-45 раз.
в. Влияние изучаемых препаратов на чувствительность животных к химическому раздражению оценивали в опытах на самцах беспородных белых крыс, которым внутрибрюшинно вводили 3% раствор уксусной кислоты из расчета 300 мг/кг массы тела. Эксперименты проведены на четырех группах крыс: крысах, которым, за 30 мин до введения раствора уксусной кислоты перорально вводился Пенталгин ICN, которым за 30 мин до введения раствора уксусной кислоты перорально вводился Пенталгин-Н, и крысах, которым за 30 мин до введения раствора уксусной кислоты вводили Пентабуфен. Изучаемые препараты исследовались в двух дозах: 400 и 600 мг/кг. Эффективность препаратов оценивалась по уменьшению числа животных, демонстрирующих развитие характерной болевой реакции (распластывание на полу клетки и прижимание задней половины тела к полу) по сравнению с контрольной группой. Данные представлены в таблице 12.
Как следует из данных, представленных в таблице 12, изученные препараты в дозе 400 мг/кг вызывают одинаково выраженное снижение числа животных, реагирующих на химическое раздражение брюшной полости. При использовании препаратов в дозе 600 мг/кг выявлено, что Пентабуфен проявляет более выраженный анальгетический эффект, чем Пенталгин ICN и Пенталгин-Н.
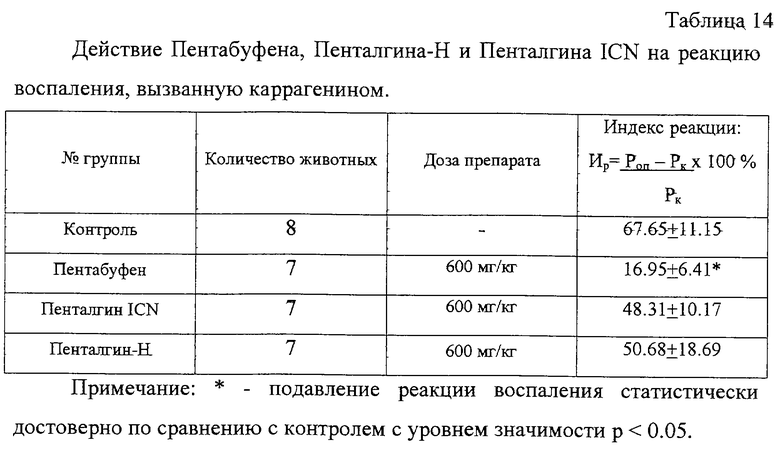
Сравнение противовоспалительной активности Пенталгина ICN и Пентабуфена проводились на основе изучения их антиэкссудативных свойств с использованием модели каррагенинового отека стопы крыс, которая в настоящее время является наиболее распространенной и детально изученной (M.T.Buckley et al. Drugs, 1990, 39; 86-109; J.Jiang et al. Pharmacological Research, 1997, 36, 309-314; A. S. Lages et al. Bioorganic Medicinal Chemistry Letters, 1998, 8, 183-188).
В опытах использовали самцов беспородных белых крыс массой 170-200 г. Животным контрольной группы за 60 мин до введения каррагенина вводили per os дистиллированную воду, животным опытных групп за 60 мин до введения каррагенина вводили per os Пенталгин ICN или Пенталгин-Н или Пентабуфен в дозе 600 мг/кг. Затем животным контрольной и опытных групп в правую подушечку задней стопы вводили 0,1 мл 1% раствора каррагенина (Sigma), в левую контрольную лапу - 0,1 мл растворителя (стерильного физиологического раствора). В течение 5 последующих часов с интервалом в 60 мин микрометром замеряли отек стоп задних конечностей у животных всех экспериментальных групп. Через 6 ч, сразу после забоя животных местную воспалительную реакцию оценивали по разнице массы опытной (Роп) и контрольной (Pk) лап (Методические материалы по экспериментальному и клиническому испытанию иммуномодулирующего действия фармакологических средств, стр. 13, 1984). Обе лапы отрезали по выступу костей ниже сочленения мало- и большеберцовой кости и выше пяточного сустава. Индекс реакции вычисляли для каждого животного по формуле: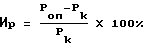
Данные представлены в таблицах 13 и 14. Как следует из данных таблицы 13, Пентабуфен вызывает значительное и статистически достоверное подавление реакции воспаления на каррагенин. Противовоспалительное действие Пенталгина-Н и Пенталгина ICN было менее выраженным через 3 ч после введения каррагенина, введение Пентабуфена вызывало через 3 ч подавление экссудативного отека в 1,8 раза по сравнению с контролем, Пенталгин-Н - 1,4 раза, Пенталгина ICN - 1,3 раза. В конце опыта Пентабуфен практически полностью подавлял воспалительную реакцию у всех животных. Как следует из данных, представленных в таблице 14, увеличение массы стоп Пентабуфен подавлял на 75% по сравнению с контролем, Пенталгин-Н - 30%, Пенталгин ICN - на 25%.
Таким образом, предлагаемое анальгезирующее, жаропонижающее и противовоспалительное средство, по результатам экспериментальных исследований, показало более высокую, чем Пенталгина ICN и Пенталгин-Н специфическую активность и низкую токсичность.

Изобретение относится к медицине, а именно к созданию анальгетических, жаропонижающих и противовоспалительных средств. Изобретение заключается в том, что предложенное анальгетическое, жаропонижающее и противовоспалительное средство включает анальгин, кофеин, кодеин и фенобарбитал при определенном соотношении ингредиентов. Изобретение обеспечивает повышение специфической активности и снижение токсичности. 1 з.п.ф-лы, 14 табл.
Анальгин 300
Ибупрофен 200
Кофеин 50
Кодеин 8
Фенобарбитал 10
| РЛС России | |||
| Энциклопедия лекарств, 1999, 6 изд.-е, с | |||
| Приспособление для подачи коробок в машинах для наполнения коробок | 1925 |
|
SU851A1 |
| НЕНАРКОТИЧЕСКОЕ АНАЛЬГЕТИЧЕСКОЕ НЕСТЕРОИДНОЕ ПРОТИВОВОСПАЛИТЕЛЬНОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2157190C2 |
Авторы
Даты
2004-01-27—Публикация
2002-09-18—Подача