Изобретение относится к биотехнологии, в частности к генетической инженерии, и представляет собой сконструированную in vitro рекомбинантную плазмидную ДНК, содержащую ДНК процессированной формы фермента органофосфатгидролазы, trc-промотор Escherichia coli и синтетический участок - усилитель трансляции, обуславливающие биосинтез фермента органофосфатгидролазы, а также штамм Escherichia coli - продуцент этого белка.
Органофосфатгидролаза (ОРН) (арилдиалкилфосфатаза, параоксоназа, фосфотриэстераза, ЕС 3.1.8.1) - фермент, катализирующий гидролиз эфирной связи в триэфирах фосфорной кислоты - является металлзависимым ферментом и содержит по два иона Zn2+ или Со2+ на субъединицу. Фермент в разной степени способен катализировать гидролиз Р-O, P-F и P-S связей в триэфирах фосфорной кислоты [Ефременко Е.Н., Сергеева B.C. Органофосфатгидролаза - фермент, катализирующий деградацию фосфорсодержащих отравляющих веществ и пестицидов // Известия АН. Сер. Хим., №10, с.1743-1749 (2001)]. Показано, что органофосфатгидролаза не содержит гликозидных остатков [Munnecke D.M. Enzymic detoxification of waste organophosphate pesticides // J. Agric. Food Chem., V.28, p.105-111 (1980)].
Биологическая роль фермента заключается в деградации фосфорорганических нейротоксинов, таких как параоксон, паратион, кумафос, малатион и т.д.
Рекомбинантная органофосфатгидролаза находит широкое применение в лабораторных исследованиях. На основе этого фермента изготовляются различные биосенсоры, а также изучаются возможности оптимизации условий гидролиза фосфорорганических соединений [Mulchandani P., Chen W., Mulchandani A. Flow injection amperometric enzyme biosensor for direct determination of organophosphate nerve agents // Environ. Sci. Technol., V.35, p.2562-2565 (2001); Simonian A.L., Efremenko E.N., Wild J.R. Discriminative detection of neurotoxins in multi-component samples // Anal. Chemica Acta, V.444, p.179-186 (2001)].
Ген ОРН первоначально был выделен из обитающих в загрязненных пестицидами почвах бактериальных клеток Pseudomonas diminuta и Flavobacterium sp. [Munnecke D.M. Enzymic detoxification of waste organophosphate pesticides // J. Agric. Food Chem., V.28, p.105-111 (1980); Mulbry W.W., Karns J.S., Kearney P.C., Nelson J.O, McDaniel C.S., Wild J.R. Identification of a plasmid-borne parathion hydrolase gene from Flavobacterium sp. by southern hybridization with opd from Pseudomonas diminuta // Appl. Environ Microbiol, V.51, p.926-930 (1986); Dave K.I., Miller L.L., Wild J.R. Characterization of organophosphorus hydrolases and the genetic manipulation of the phosphotriesterase from Pseudomonas diminuta // Chem. - Biol. Interact., V.87, p.55-68 (1993)].
Природные штаммы, обладающие органофосфатгидролазной активностью, не могут быть рассмотрены в качестве продуцентов данного фермента ввиду крайне низких уровней его синтеза в клетках (0,0085 мг белка из 1 г клеток).
Была предпринята попытка создания продуцента ОРН на основе культуры тканей личинок насекомых (клетки sf9, Spodoptera frugiperda), которые были инфицированы рекомбинантным бакуловирусом А5В, несущим ген ОРН [Dumas D.P., Caldwell S.R., Wild J.R., Raushel E.M. Purification and properties of the phosphotriesterase from Pseudomonas diminuta // J. Biol. Chem., V.264, p.19659-19665 (1989)]. Для накопления фермента внутри клеток их культивирование проводили в течение 4 суток при конечном накоплении 5-6 г/л клеточной биомассы. Последующее выделение ОРН позволило получить авторам этого продуцента 2,7 мг белка из 8 г клеток, что означает получение 0,34 мг белка из 1 г клеток.
Низкий выход фермента, длительная процедура накопления биомассы, многостадийность процесса очистки белкового препарата, включающая 4 стадии различных типов хроматографии, свидетельствуют об очевидной невозможности технологической реализации процесса получения ОРН с использованием указанного продуцента.
Известны попытки конструирования эффективных генно-инженерных продуцентов ОРН на основе клеток микроорганизмов.
Ген ОРН был клонирован из Flavobacterium sp.(ATTC 27551) в клетках Streptomyces lividans, фермент был очищен до гомогенного состояния. Авторы разрабатывали способы увеличения выхода внеклеточной ОРН из рекомбинантных клеток Streptomyces lividans. Для этого использовались богатые питательные среды, содержащие 85 г/л триптона и 60 г/л глюкозы, с подпиткой культуры во время ее ферментации (по 0,57 л раствора, содержащего 133 г/л глюкозы и 167 г/л триптона) [Payne G.F., DelaCruz N., Copella S.J. Improved production of geterologous protein from Streptomyces lividans // Appl. Microbiol. Biotechnol., V.33, p.395-400 (1990)]. Для обеспечения эффективной секреции ОРН из клеток Streptomyces lividans была создана генетическая конструкция, в которой нативную сигнальную последовательность β-галактозидазы из Streptomyces заменили на сигнальную последовательность из Flavobacterium. Это привело к увеличению содержания ОРН во внеклеточной культуральной жидкости до 25 мг/л при наличие в среде 10 г/л клеток, что означает, что выход фермента составлял 2,5 мг внеклеточного белка из 1 г клеток.
При этом секретируемый фермент составлял 2% от всех секретируемых в среду клеточных белков, что приводило к серьезным технологическим трудностям и увеличению числа стадий при его выделении. Дополнительные сложности в процесс очистки внеклеточного фермента вносила богатая по своему белковому составу питательная среда. Секретируемый белок содержал дополнительную сигнальную последовательность, удаление которой требовало проведения дополнительной стадии обработки белка.
Для создания продуцента рекомбинантной ОРН в ряде работ были использованы клетки E.coli.
Для создания генно-инженерного штамма, обладающего ОРН активностью, клетки E.coli трансформировали плазмидой рJK33, содержащей ген ОРН [Omburo G.A., Kuo J.M., Mullins L.S., Raushel F.M. Characterization of the zinc binding site of bacterial phosphotriesterase // J. Biol. Chem., V.267, p.13278-13283 (1992)]. Использованная плазмида обеспечивала внутриклеточный синтез модифицированного белка ОРН, в котором первые 33 были заменены на 5 следущих аминокислот: Met-Ile-Thr-Asn-Ser-. Синтезируемый фермент накапливался в растворимом виде в клетках, при этом его выход после очистки и выделения в гомогенном состоянии составил 298 мг из 160 г клеток, что означает, что удельный выход был 1,87 мг белка из 1 г клеток.
Для накопления необходимого количества биомассы требовалось длительное культивирование клеток (38 часов), а для индукции синтеза фермента необходимо было применение высокой концентрации дорогостоящего индуктора - изопропил-β-D-тиогалактопиранозида (ИПТГ) - 1 мМ. Последние два фактора определяли экономическую неэффективность этого продуцента.
Наиболее близким к заявляемому техническому решению (прототипом) является генно-инженерная конструкция и штамм для получения органофосфатгидролазы, предложенные авторами изобретения (United States Patent No.5589386; кл. C 12 S 13/00; C 12 N 15/00; C 12 N 01/20; C 12 N 01/14, 1996). Для реализации способа гидролиза фосфорорганических соединений авторами прототипа предлагаются сконструированные экспрессионные плазмиды с термоиндуцибельным промотором для получения ОРН и ее метионинового аналога, синтез которого кодируется ДНК последовательностью ОРН с делецией 29 аминокислот с N-конца последовательности, которыми трансформируют клетки E.coli, Bacillus и Streptomyces. Предлагаемые в прототипе плазмиды pCMS75 (ATCC №67778) и pCMS77 (ATCC №67779), трансформированные в клетки E.coli Fm5, позволяют получать наибольшее количество ОРН, причем в случае плазмиды pCMS77 фермент синтезируется в виде телец включения. Суммарная активность клеточного экстракта E.coli (pCMS75) в 10 раз выше, чем активность клеточного экстракта E.coli (pCMS77). В данном прототипе предлагается метод гидролиза ингибиторов холинэстеразы, состоящих из фосфорорганических соединений, заключающийся в том, что проводится обработка этих ингибиторов выделенной и очищенной зрелой формой ОРН и ее аналогом, не содержащим инициирующего аминокислотного остатка метионина. Удельная активность ОРН, выраженная в ед/мг белка, увеличивается в случае продуцирования ее микроорганизмами при их культивировании в среде, содержащей более чем 0,15 мМ, но не больше 3,0 мМ любого из металлов, выбранного из ряда: кобальт, цинк или смеси кобальта с цинком. Заявленный в прототипе метод позволяет гидролизовать следующие ингибиторы холинэстеразы: диизопропилфторфосфат, изопропилметилфторфосфат и пинаколилметилфторфосфат.
В тексте прототипа не указан выход фермента из 1 г клеток, но приведена его максимальная удельная активность, которая составляет 1000 ед/мг белка.
Недостатками конструкции pCMS77 является преимущественное накопление фермента в неактивном нерастворимом состоянии в составе телец включения, а также технологические сложности, связанные с использованием термоиндуцибельного промотора и требующие изменения температурного режима ведения процесса в ходе культивирования.
Предлагаемое изобретение решает задачу создания генно-инженерной конструкции и штамма клеток, которые обеспечивают получение значительных количеств активной растворимой формы органофосфатгидролазы в цитоплазме клеток путем индуцибельного синтеза фермента с помощью индуктора ИПТГ.
Поставленная задача решается путем конструирования рекомбинантной плазмидной ДНК рТrсТЕ-ОРН, кодирующей индуцибельный синтез фермента органофосфатгидролазы, и штамма Escherichia coli DH5α/pTrcTE-OPH, обеспечивающего синтез этого белка с уровнем экспрессии, позволяющим получать не менее 12 мг очищенного белка из 1 г влажной биомассы.
Индуцибельный высокий уровень синтеза целевого полипептида обеспечивается тем, что предлагаемая плазмида рТrсТЕ-ОРН отличается от известной наличием trc-промотора Е.coli и синтетического усилителя трансляции гена 10 бактериофага Т7.
Рекомбинантная плазмидная ДНК рТrсТЕ-ОРН, кодирующая фермент органофосфатгидролазу, характеризуется следующими признаками:
имеет молекулярную массу 3,46 Md (5,243 т.п.о.);
кодирует аминокислотную последовательность фермента органофосфатгидролазы;
состоит из Cla I/Hind III - фрагмента ДНК плазмиды pTrcTE-Lep (Патент RU 2185438 С2, кл. С 12 N 15/12, 1/21, 2002) длиной 4,682 т.п.о., содержащего trc-промотор Е.coli, синтетический усилитель трансляции TREN гена 10 бактериофага Т7, ген blа β-лактамазы, определяющий устойчивость трансформированных плазмидой рТrсТЕ-ОРН клеток к ампициллину, и участок ori инициации репликации; а также из ДНК фермента органофосфатгидролазы длиной 1,011 т.п.о., фланкированного сайтами рестрикции Cla I и Hind III;
содержит: trc-промотор Е.coli, уникальные сайты узнавания рестрикционными эндонуклеазами, имеющими следующие координаты: Nco I - 265, Есо М - 270, Крn I - 286, Xba I - 340, Cla I - 377, Hind III - 1389.
Особенностью предложенной плазмидной конструкции является наличие trc-промотора Е.coli, контролирующего синтез ДНК фермента ОРН, а для усиления трансляции используется синтетический усилитель трансляции, что в совокупности обеспечивает индуцибельный синтез целевого белка с надежной регуляцией и высоким выходом, достигаемым при малых концентрациях индуктора.
Для получения штамма-продуцента фермента органофосфатгидролазы трансформируют компетентные клетки Escherichia coli DH5α рекомбинантной плазмидой рТrсТЕ-ОРН.
Полученный штамм Escherichia coli DH5α/рTrcTE-OPH характеризуется следующими признаками.
Морфологические признаки. Клетки мелкие палочковидной формы, грамотрицательные, неспороносные, 1×3-5 мкм, подвижные.
Культуральные признаки. При росте на агаризованной среде LB (Состав среды LB: триптон - 10,0 г/л; дрожжевой экстракт - 5,0 г/л; NaCl - 5,0 г/л; и 1,7% бактоагара) колонии круглые, гладкие, полупрозрачные, блестящие, серые, край ровный, диаметр колоний 1-3 мм; консистенция пастообразная. Рост в жидкой среде LB (триптон - 10,0 г/л; дрожжевой экстракт - 5,0 г/л; NaCl - 5,0 г/л) характеризуется ровным помутнением с образованием легкого осадка.
Физико-биохимические признаки. Клетки растут при температуре 4-42°С при оптимуме рН 6,8-7,2. В качестве источника азота используют как минеральные соли в аммонийной форме, так и органические соединения в виде пептона, триптона, дрожжевого экстракта, аминокислот. В качестве источника углерода используют аминокислоты, глицерин, углеводы.
Устойчивость к антибиотикам. Клетки проявляют устойчивость к ампициллину (до 200 мкг/мл), обусловленную наличием в плазмиде гена β-лактамазы.
Штамм Е.coli DH5α/рTrcTE-OPH обеспечивает индуцибельный синтез фермента органофосфатгидролазы с высоким содержанием растворимой формы фермента в цитоплазме, что позволяет получать не менее 12 мг очищенного белка из 1 г влажной биомассы. В данном штамме достигается более высокий выход растворимой формы целевого белка при использовании небольших количеств индуктора. При этом в процессе индукции не требуется изменение температурного режима культивирования клеток. Совокупность перечисленных свойств штамма Е.coli DH5α/рTrcTE-OPH делает получение рекомбинантной органофосфатгидролазы высокотехнологичным процессом.
Полученный штамм депонирован в коллекции культур микроорганизмов Института биоорганической химии им. М.М.Шемякина - Ю.А.Овчинникова Российской Академии Наук под номером 25.
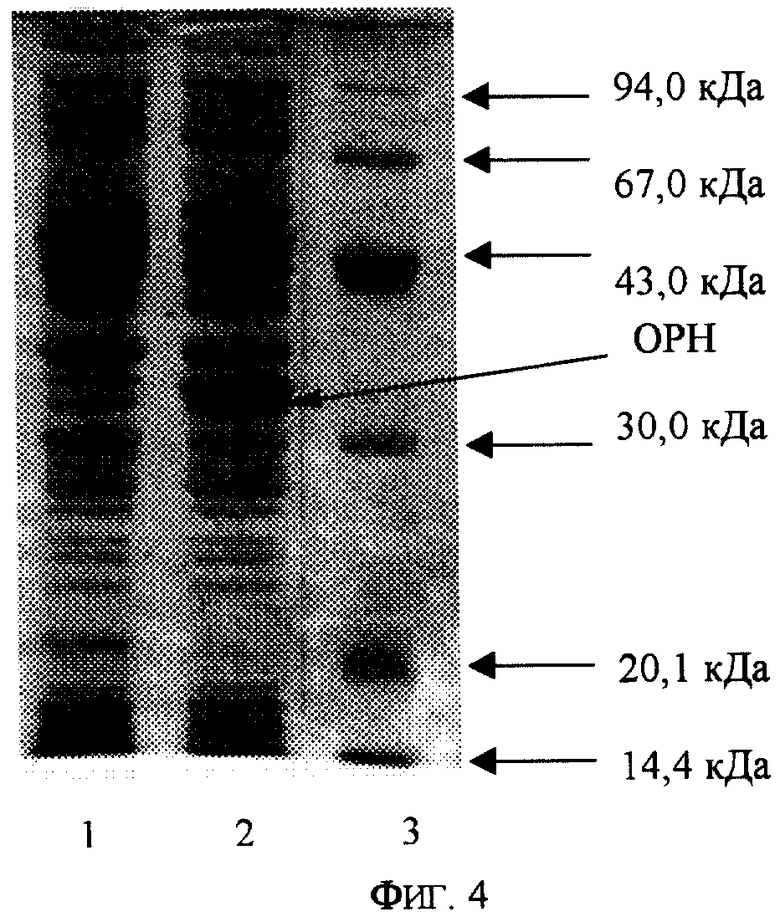
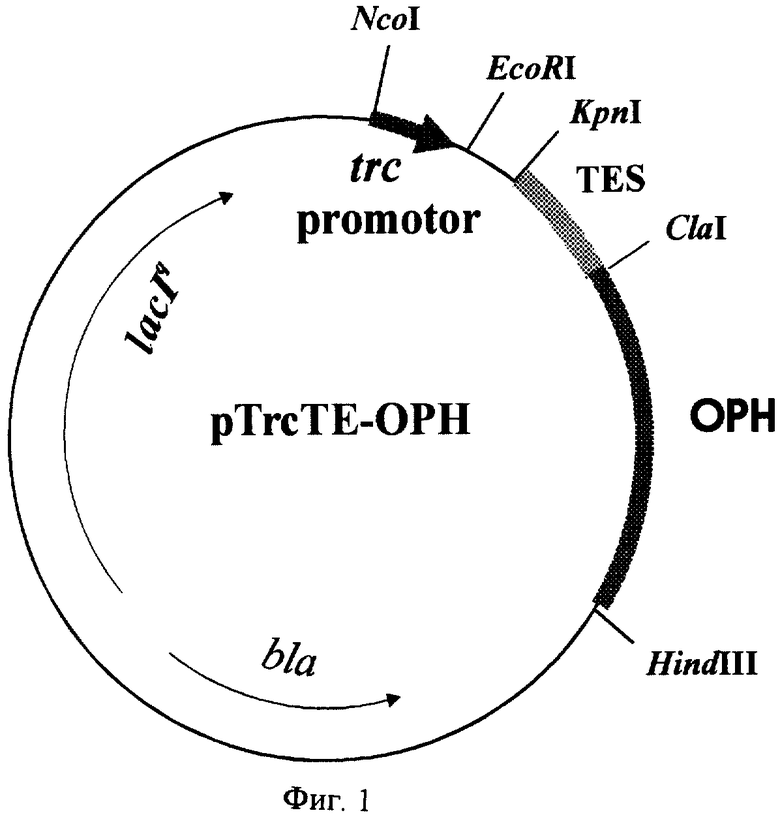
На фиг.1 представлена физическая карта рекомбинантной плазмиды рТrсТЕ-ОРН; на фиг.2 - нуклеотидная последовательность ДНК фермента органофосфатгидролазы с прилегающими регуляторными элементами: trc - промотор (1-30 п.о.), усилитель трансляции TREN (93-186 п.о.), ген органофосфатгидролазы (190-1201 п.о.); инициирующий и терминирующий кодоны подчеркнуты, в рамки взяты сайты рестриктаз: Есо RI, Cla I и Hind III; на фиг.3 - аминокислотная последовательность фермента органофосфатгидролазы, кодируемого рекомбинантной плазмидой рТrсТЕ- ОРН; на фиг.4 - электрофореграмма лизатов клеток штамма-реципиента Е.coli DH 5α (дорожка 1), штамма-продуцента Е.coli DH5α/рTrcTE-OPH (дорожка 2), белковых стандартов молекулярного веса (дорожка 3) в 10%-ном полиакриламидном геле (стрелкой указан фермент органофосфатгидролаза).
Изобретение иллюстрируется следующими примерами.
Пример 1. Конструирование рекомбинантной плазмидной ДНК рТrсТЕ-ОРН.
Культуру Pseudomonas diminuta VKM В-1297 объемом 100 мл центрифугируют 15 мин 3000 об/мин и осадок ресуспендируют в 10 мл ТЕ буфера (50 мМ Tris-HCl, pH 8,0, 5 мМ ЭДТА). После этого добавляют 1 мл раствора лизоцима (10 мг/мл). Суспензию замораживают при -70°С, инкубируют на водяной бане при 20°С до полного оттаивания клеток и выдерживают во льду 1 ч для разрушения клеточных стенок бактерий. Добавляют 2 мл 0,5% раствора SDS, содержащего 0,4 М ЭДТА и 2 мл раствора протеиназы К (1 мг/мл). Инкубируют 1 ч при 60°С, проводят фенольную экстракцию, после чего осаждают ДНК этиловым спиртом. Осадок растворяют примерно в 1 мл ТЕ буфера (50 мМ Tris-HCl, pH 7,5, 1 мМ ЭДТА).
Добавляют РНКазу А до концентрации 50 мкг/мл, инкубируют 2 ч при 4°С, осторожно перемешивая. Повторяют фенольную экстракцию, переосаждают ДНК этанолом, растворяют осадок в 1 мл ТЕ буфера.
Полученную ДНК из Pseudomonas diminuta VKM В-1297 используют для амплификации методом полимеразной цепной реакции гена органофосфатгидролазы. Для этого к 5 мкл раствора ДНК (10 нг/мкл) прибавляют по 100 пмоль праймера FOR-Cla с нуклеотидной последовательностью СТТ ССА TCG АТА TGA GAG GAT CGC АТС и 100 пмоль праймера REV-Hind с нуклеотидной последовательностью ССА САА AGC TTC ATG ACG CCC GCA AGG ТС, 8 мкл смеси, содержащей 2,5 мМ каждого из дезоксинуклеозидтрифосфатов, 10 мкл 10-кратного буфера (100 мМ трис-HCl, рН 8,8, 500 мМ КСl, 15 мМ MgCl2), 2 ед. Taq ДНК-полимеразы и воду до 100 мкл. Полимеразную цепную реакцию (ПЦР) проводят в следующем режиме: денатурация - 1 мин, 94°С; отжиг - 1 мин., 55°С; достройка - 1 мин 30 с, 72°С; количество циклов - 35. Праймер FOR-Cla представляет собой 27-звенный олигонуклеотид, в состав которого входят сайт узнавания рестриктазы Cla I, стартовый ATG-кодон и 13 нуклеотидов 5'-области ДНК органофосфатгидролазы. Праймер REV-Hind представляет собой 29-звенный олигонуклеотид, содержащий сайт узнавания рестриктазы Hind III, а также последовательность, комплементарную стоп-кодону гена органофосфатгидролазы и прилегающим 15 нуклеотидам кодирующей области.
Реакционную смесь после прохождения ПЦР экстрагируют равным объемом хлороформа, после чего осаждают этиловым спиртом. После центрифугирования и высушивания ДНК растворяют в 20 мкл 10 мМ триса-HСl, 1мМ ЭДТА (рН 8,0).
Амплифицированную ДНК (5 мкл) обрабатывают 10 ед. рестриктазы Cla I и 15 ед. рестриктазы Hind III (Fermentas, Литва) в течение 1 ч при 37°С в 20 мкл буферного раствора, содержащего 33 мМ трис-ацетата (рН 7,9), 10 мМ ацетата магния, 66 мМ ацетата калия, и из полученного гидролизата выделяют фрагменты ДНК органофосфатгидролазы длиной 1,011 т.п.о. (Cla I - Hind III фрагмент) переносом их из 1,5%-ного агарозного геля на DEAE-мембрану NA-45.
Плазмидную ДНК pTrcTE-Lep длиной (5 мкг) размером 4,682 т.п.о., содержащей trc-промотор и усилитель трансляции TREN бактериофага Т7, обрабатывают 10 ед. рестриктазы Cla I и 15 ед. рестриктазы Hind III в течение 2 ч при 37°С в 30 мкл буферного раствора, содержащего 33 мМ трис-ацетата (рН 7,9), 10 мМ ацетата магния, 66 мМ ацетата калия, и из полученного гидролизата выделяют векторную часть плазмидной ДНК длиной 4,232 т.п.о. переносом ее из 0,8%-ного агарозного геля на DEAE-мембрану NA-45.
Cla I - Hind III фрагмент ДНК фермента ОРН длиной 1,011 т.п.о. (0,02 мкг) и 0,05 мкг векторной части плазмидной ДНК pTrcTE-Lep длиной 4,232 т.п.о. соединяют при помощи лигазной реакции в течение 3 ч при 10°С в 15 мкл раствора, содержащего 40 мМ трис-НСl (рН 7,8), 10 мМ MgCl2, 10 мМ дитиотреитола, 0,5 мМ аденозинтрифосфата и 2 ед. Вейса Т4 ДНК-лигазы.
Реакционную смесь (5 мкл) используют для трансформации 200 мкл компетентных клеток XL-1 Blue. 1/10 клеток, использованных для трансформации, высевают на LB-агар, содержащий 75 мкг/мл ампициллина. Из выросших клонов выделяют плазмидную ДНК, содержащую фрагмент ДНК фермента ОРН.
Окончательно структуру рекомбинантной ДНК рТrсТЕ-ОРН подтверждают определением нуклеотидной последовательности в области встроенной ДНК фермента органофосфатгидролазы.
Пример 2. Получение штамма-продуцента фермента органофосфатгидролазы.
Рекомбинантной плазмидной ДНК рТrсТЕ-ОРН трансформируют компетентные клетки Escherichia coli DH5α [F- (Ф80dΔ(lacZ)M15) recA1 endA1 gyrA96 thi1 hsdR17(r
Пример 3. Выделение, очистка и исследование свойств рекомбинантного фермента органофосфатгидролазы.
Для накопления биомассы клеток используют жидкую питательную среду ТУYЕ (триптон - 12,0 г/л, дрожжевой экстракт - 24,0 г/л, глицерин - 4,0 мл/л, КН2РO4 - 6,95 г/л, К2НРO4 × 3Н2O - 12,54 г/л, рН среды 7,0), в которую добавляют СоСl2 × 6Н2О до концентрации 237 мг/л. Перед посевом клеток в среду добавляют раствор ампициллина (концентрация в среде 100 мкг/мл).
Для получения инокулята производят посев культуры петлей с чашек Петри в 20 мл среды LB. 12-часовой инокулят вносят в колбу, содержащую 100 мл полноценной питательной среды, культуру выращивают при 30°С и постоянном перемешивании (200 об/мин) до тех пор, пока оптическая плотность при длине волны 540 нм не достигнет 0,6, после чего добавляют ИПТГ до концентрации 0,2 мМ. Клетки культивируют в течение 21 ч. Полученную биомассу отделяют центрифугированием (5000 g, 15 мин), взвешивают и ресуспендируют в 10 мМ фосфатном буфере, рН 7,0 (массовое соотношение биомасса:буфер - 1:5). Клетки разрушают обработкой ультразвуком (частота 44 кГц) 4 раза по 45 с, между обработками биомассу выдерживают в течение 1 мин во льду. Осадок отделяют центрифугированием (15000 g, 30 мин). К супернатанту добавляют 10% раствор сульфата стрептомицина в 25 мМ TRIS буфере, рН 7,0 (соотношение объемов супернатанта и раствора сульфата стрептомицина - 1:9), выпавший осадок отделяют центрифугированием (15000 g, 30 мин). К супернатанту добавляют сульфат аммония до его конечной концентрации 45% (258 мг/мл раствора белка), затем образовавшийся осадок отделяют центрифугированием (15000 g, 40 мин). Ресуспендируют осадок, содержащий ОРН, в 40 мл фосфатного буфера (10 мМ, рН 7,0). Полученный раствор подвергают диализу против 2 л 10 мМ фосфатного буфера, рН 6,9. Раствор, содержащий ОРН, наносят на 100 мл колонку с SP-сефарозой (Pharmacia) (скорость нанесения 0,5 мл/мин), уравновешенной тем же фосфатным буфером (рН 6,9), затем через колонку пропускают градиент раствора КСl (от 0 до 0,5 М в фосфатном буфере, рН 6,9).
Полученные фракции, содержащие ОРН, объединяют и подвергают диализу против 50 мМ трис-НСl буфера, (рН 8,3), затем наносят на 10 мл колонку с DEAE (Pharmacia), предварительно уравновешенную тем же буфером.
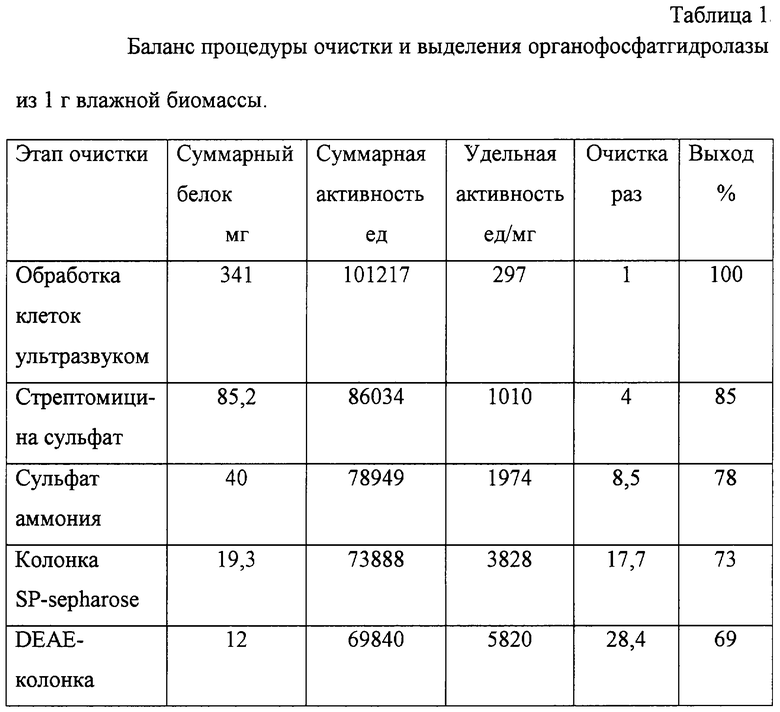
В процессе очистки из 1 г влажной биомассы получают 12 мг высокоочищенного фермента со средней удельной активностью 5820 ед/мг белка. Выход фермента составляет 69% от исходного количества ОРН, синтезированного клетками (табл.1).
За скоростью исследуемой реакции следят спектрофотометрически на спектрофотометрах, снабженных термостатируемыми кюветными отделениями, по накоплению продукта 4-нитрофенолят аниона (ε=17000 моль-1см-1, рН 9,0, λ=405 нм). Для определения каталитической активности органофосфатгидролазы в водных растворах используют 0,05 М CHES буфер (рН 9,0). В качестве субстрата используют 1 мМ водные растворы параоксона, паратиона и метил-паратиона.
Каталитическую реакцию инициируют внесением в кювету с буфером и субстратом раствора органофосфатгидролазы в 10 мМ фосфатном буфере (рН 7,0). Концентрация фермента в кювете составляет 10-10-10-9 М.
За единицу ферментативной активности принимают такое количество фермента, которое необходимо для того, чтобы гидролизовать 1 мМ субстрата за 1 мин при рН 9,0 и 20°С.
Расчет скоростей ферментативной реакции проводят по начальным линейным участкам кинетических кривых (Vo=tgα). Максимальную скорость ферментативной реакции (Vm) и константу Михаэлиса (Km) определяют с использованием двойных обратных координат 1/vo-1[S] (Лайнуивера-Берка).
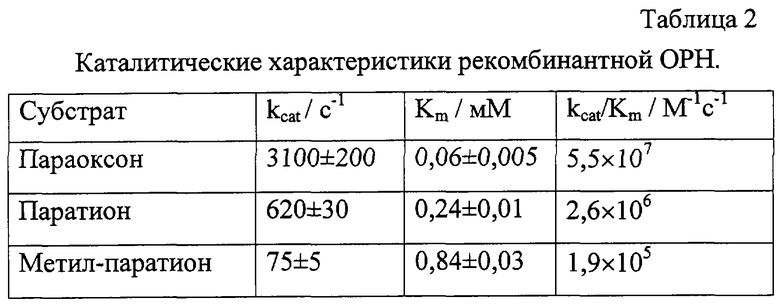
Кинетические характеристики рекомбинантной органофосфатгидролазы приведены в табл.2. рН-оптимум действия фермента составляет 9,0.
Таким образом, заявляемое техническое решение представляет собой плазмиду уникальной конструкции для микробного синтеза ОРН и штамм E.coli, обеспечивающий экспрессию данной плазмиды, позволяющий получить полипептид со свойствами, идентичными свойствам природной ОРН, и обеспечивающий супервысокий выход растворимого высокоактивного фермента (не менее 12 мг из 1 г влажной биомассы) в течение довольно короткого периода времени (21 ч). Биосинтез полипептида индуцируется добавлением в среду невысоких концентраций ИПТГ (0,2 мМ), при этом не требуется изменения температурных условий культивирования клеток. Предлагаемое решение позволяет получать ОРН в виде растворимого белка с высокой активностью и в таком количестве, которые более чем в 5 раз превосходят все известные аналоги и решение, заявленное в прототипе. Все это позволяет значительно повысить технологичность и экономичность процесса получения высокоактивного рекомбинантного фермента органофосфатгидролазы.
Рекомбинантный фермент может быть использован для приготовления наборов для аналитического определения фосфорорганических соединений, а также для производства препаратов на основе ОРН, предназначенных для деградации фосфорорганических соединений.


Изобретение относится к биотехнологии, в частности к генетической инженерии. Оно представляет собой сконструированную in vitro рекомбинантную плазмидную ДНК, содержащую ДНК процессированной формы фермента органофосфатгидролазы (ОРН), trc-промотор Escherichia coli и синтетический участок - усилитель трансляции, обуславливающие биосинтез фермента ОРН, а также штамм Escherichia coli - продуцент этого белка. Рекомбинантный фермент может быть использован для производства препаратов на основе ОРН, предназначенных для деградации фосфорорганических соединений, а также для их аналитического определения. Изобретение решает задачу создания генно-инженерной конструкции и штамма клеток, которые обеспечивают получение значительных количеств активной растворимой формы органофосфатгидролазы в цитоплазме клеток путем индуцибельного синтеза фермента. Поставленная задача решается путем конструирования рекомбинантной плазмидной ДНК pTrcTE-OPH, кодирующей индуцибельный синтез ОРН и штамма Escherichia coli DH5α/pTrcTE-OPH, обеспечивающего синтез этого белка с уровнем экспрессии, позволяющим получать до 12 мг очищенного белка из 1 г влажной биомассы. Индуцибельный высокий уровень синтеза целевого полипептида обеспечивается тем, что предлагаемая плазмида pTrcTE-OPH отличается от известной наличием trc-промотора Е.coli и синтетического усилителя трансляции гена 10 бактериофага Т7. 2 н.п. ф-лы, 2 табл., 4 ил.
| CN 1376789, 30.10.2002 | |||
| US 5552313, 03.09.1996 | |||
| US 5589386, 31.12.1996. |
Авторы
Даты
2004-07-20—Публикация
2002-11-26—Подача