Родственные заявки
Данная заявка заявляет приоритет предварительных заявок на патенты США с регистрационными номерами 60/138851; 60/138854 и 60/139323, каждая из которых была подана 11 июня 1999 года. Каждая из этих заявок включена, таким образом, в качестве ссылки.
Область изобретения
Данное изобретение в общем относится к введению андрогенов женщинам. Таким образом, данное изобретение включает в себя области фармацевтических наук и медицины.
Предпосылки изобретения
Известно, что функциональный уровень андрогенных гормонов у женщин стимулирует сексуальное здоровье и сексуальную активность, ощущения благополучия, максимизирует массу и функцию мышц и ингибирует разрежение костной массы (остеопороз). Далее, функциональный уровень андрогенных гормонов может стимулировать сердечно-сосудистое и коронарное здоровье, уменьшать болезненность молочной железы, снижать вазомоторную нестабильность, модулировать иммунную функцию, усиливать некоторые познавательные способности, улучшать здоровье мочеполовых путей, уменьшать побочные действия, связанные с пополнением эстрогена, и обеспечивает прямые нейрозащитные эффекты.
На достижение у женщин функциональных уровней андрогенных гормонов, например тестостерона, могут влиять концентрации в сыворотке связывающего половые гормоны глобулина (SHBG). SHBG является белком, продуцируемым печенью, который связывает половые гормоны, такие как тестостерон и эстрадиол в крови. SHBG-связанные половые гормоны обычно являются “нефункциональными”, т.е. неспособными проявлять биологическое действие при рецепторах половых гормонов в тканях-мишенях и/или подвергаться клиренсу из крови.
Применение перорально вводимых эстрогенов повышает уровни SHBG в сыворотке. Уровни SHBG в сыворотке повышаются также в различных условиях, например при гипертиреоидизме и беременности, и под влиянием некоторых других лекарственных средств, например противосудорожных средств. Повышенные уровни SHBG изменяют уровни андрогенных гормонов и дозы, необходимые для достижения функциональных уровней.
Данное изобретение обеспечивает способы, композиции и наборы для достижения функциональных уровней андрогенных стероидов у женщин с повышенными уровнями SHBG и, следовательно, улучшения их здоровья.
Сущность изобретения
Таким образом, данное изобретение обеспечивает способ и набор для улучшения здоровья женщины, которая имеет повышенный или существенно повышенный уровень связывающего половые гормоны глобулина (SHBG). Кроме того, данное изобретение обеспечивает способ и набор для улучшения здоровья у женщины, принимающей перорально дополнительное количество эстрогена. Далее, данное изобретение обеспечивает способ и набор для улучшения здоровья у женщины, нуждающейся в дополнительном пероральном предоставлении эстрогена.
В одном аспекте такие способы включают в себя непероральное введение андрогенного стероида в количестве, достаточном для обеспечения терапевтического эффекта в присутствии повышенных или существенно повышенных уровней SHBG. В другом аспекте такие способы включают в себя непероральное введение андрогенного стероида в количестве, достаточном для обеспечения терапевтического эффекта в присутствии перорального введения эстрогена. Еще в одном варианте такие способы включают в себя совместное введение эффективного количества перорально вводимого эстрогена и количества неперорально вводимого андрогенного стероида, которое является достаточным для обеспечения терапевтического эффекта в присутствии перорально вводимого эстрогена.
Примеры конкретных андрогенных стероидов, которые могут быть использованы, включают в себя, но не ограничиваются ими: тестостерон, метилтестостерон, андростендион, адреностерон, дегидроэпиандростерон, оксиметолон, флуоксиместерон, метандростенолон, тестолактон, прегненолон, 17α-метилнортестостерон, норэтандролон, дигидротестостерон, даназол, оксиметолон, андростерон, нандролон, станозолол, этилэстренол, оксандролон, боластерон и местеролон, пропионат тестостерона, ципионат тестостерона, фенилацетат тестостерона и энантат тестостерона, ацетат тестостерона, буциклат тестостерона, гептаноат тестостерона, деканоат тестостерона, капрат тестостерона, изокапрат тестостерона, их изомеры и производные и их комбинации.
Вводимое количество андрогенного стероида может быть измерено в соответствии с несколькими различными параметрами. В одном аспекте количество вводимого андрогенного стероида может быть количеством, достаточным для достижения терапевтического эффекта, эквивалентного уровню общего тестостерона в сыворотке от приблизительно 15 до приблизительно 1000 нг/дл. В другом аспекте данного изобретения количество вводимого андрогенного стероида может быть количеством, достаточным для достижения терапевтического эффекта, эквивалентного уровню свободного тестостерона в сыворотке от приблизительно 0,5 до приблизительно 30 пг/мл. В дополнительном аспекте данного изобретения количество вводимого андрогенного стероида может быть количеством, достаточным для достижения терапевтического эффекта, эквивалентного уровню биодоступного тестостерона в сыворотке от приблизительно 1 до приблизительно 70 нг/дл. Еще в одном аспекте данного изобретения количество вводимого андрогенного стероида может быть количеством, достаточным для достижения терапевтического эффекта, эквивалентного дозе тестостерона по меньшей мере около 50 мкг/день.
Примеры конкретных эстрогенов, которые могут быть использованы в связи со способом данного изобретения, включают в себя, но не ограничиваются ими: 17β-эстрадиол, 17α-эстрадиол, конъюгированный лошадиный эстрадиол, этерифицированный эстроген, микронизированный эстрадиол, сульфат натрий-эстрогена, этинилэстрадиол, эстрон, тиболон, селективные модуляторы рецептора эстрогена (SERM), фитоэстрогены, их изомеры и производные и их комбинации. В одном аспекте данного изобретения количество вводимого эстрогена может быть дозой, достаточной для достижения терапевтического эффекта, эквивалентного дозе конъюгированного лошадиного эстрогена от около 0,2 до около 3,0 мг/день.
Различные формы неперорального введения андрогена могут быть использованы в соответствии со способами данного изобретения, в том числе, но не только: местное введение или парентеральное введение или их комбинация. В одном аспекте формы местного введения включают в себя, без ограничения, трансдермальную, или трансмукозную, или сублингвальную формы введения или их комбинации. В другом аспекте парентеральные формы введения включают в себя, без ограничения, внутримышечную инъекцию, или подкожную имплантацию, или их комбинацию.
Прогестин может совместно вводиться с андрогенным стероидом и эстрогеном, если желательно. В одном аспекте введение прогестина может быть количеством, достаточным для обеспечения эндометриальной безопасности во время введения эстрогена. В другом варианте введение прогестина может быть количеством, достаточным для обеспечения эффективной контрацепции.
Имеется много индикаторов улучшенного здоровья, которые могут встречаться как результат способа данного изобретения. Особо следует отметить, без ограничения ими, восстановление, усиление, улучшение или профилактику характеристик, таких как половое влечение, частоту половой активности, стимуляцию половых органов, способность достижения оргазма, удовольствие во время половой активности, жизненную энергию, чувство благополучия, настроение и чувство эмоционального здоровья (благополучия), застенчивость, познавательные способности, массу и функцию мышц, состав тела, минеральную плотность костей, состояние кожи и волос, лобковых волос, атрофию мочеполовых путей, сухость влагалища, сухие глаза, здоровье в аутоиммунных состояниях, вазомоторную нестабильность, болезненность молочной железы, симптомы предменструального синдрома и их комбинации.
Краткое описание графических материалов
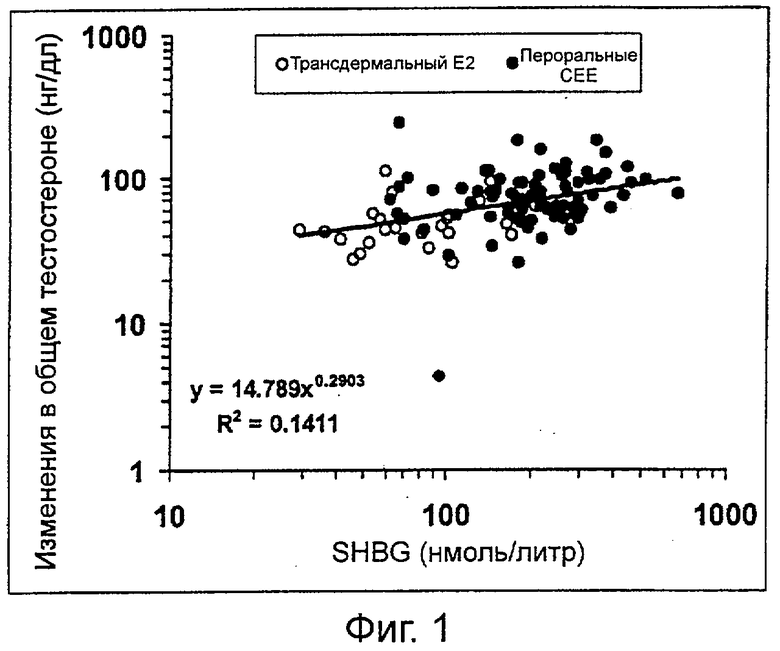
Фиг.1 показывает изменение в уровне общего тестостерона в зависимости от базового уровня (фона) SHBG во время нанесения чрескожного (трансдермального) пластыря с тестостероном (номинальная доставка 300 мкг/день) пациентам, одновременно получающим трансдермально эстрадиол или перорально конъюгированные лошадиные эстрогены.
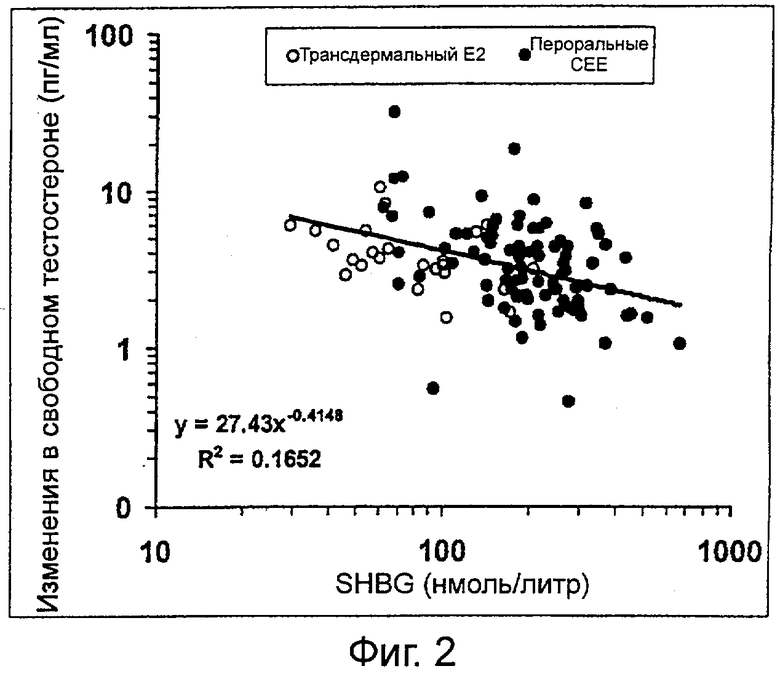
Фиг.2 показывает изменение в уровне свободного тестостерона в зависимости от базового уровня (фона) SHBG во время нанесения чрескожного (трансдермального) пластыря (номинальная доставка 300 мкг/день) пациентам, одновременно получающим трансдермально эстрадиол или перорально конъюгированные лошадиные эстрогены.
Подробное описание
А. Определения (дефиниции)
В описании и в формуле данного изобретения будет использована следующая терминология.
Формы единственного числа с неопределенными артиклями (“a”, “an”) и с определенным артиклем (“the”) включают в себя множественные ссылки, если контекст ясно не дает иное указание. Так, например, ссылка на “трансдермальный пластырь” включает в себя ссылку на один или несколько таких трансдермальных пластырей, а ссылка на “an estrogen” (эстроген) включает в себя ссылку на один или несколько таких эстрогенов.
“Половые гормоны” обозначают любой гормон, который влияет на рост или функцию репродуктивных органов или на развитие вторичных половых признаков. В одном аспекте половые гормоны включают в себя, но не ограничиваются ими, андрогены, эстрогены, прогестины и другие гормоны, которые известны в данной области.
“Андрогенный стероид”, или “андроген”, обозначает стероид, природный или синтетический, который проявляет его биологическое или фармакологическое действие прежде всего посредством связывания с рецепторами андрогенов. Примеры включают в себя, но не ограничиваются ими: тестостерон, метилтестостерон, андростендион, адреностерон, дегидроэпиандростерон, оксиметолон, флуоксиместерон, метандростенолон, тестолактон, прегненолон, 17α-метилнортестостерон, норэтандролон, дигидротестостерон, даназол, андростерон, нандролон, станозолол, этилэстренол, оксандролон, боластерон и местеролон, пропионат тестостерона, ципионат тестостерона, фенилацетат тестостерона и энантат тестостерона, ацетат тестостерона, буциклат тестостерона, гептаноат тестостерона, деканоат тестостерона, капрат тестостерона, изокапрат тестостерона, а также их сложные эфиры, производные, пролекарства и изомеры.
“Тестостерон” обозначает соединение, имеющее названия IUPAC (17β)-17-гидроксиандрост-4-ен-3-он и Δ4-андростен-17β-ол-3-он, а также их изомеры. Тестостерон находится в списке в Merck Index, entry no. 9322, at page 1569, 12th ed. (1996).
“Эстроген” и “эстрогенный гормон” обозначает любое вещество, природное или синтетическое, которое проявляет его биологическое или фармакологическое действие прежде всего посредством связывания с рецепторами эстрогенов. Примеры включают в себя, но не ограничиваются ими: 17β-эстрадиол, 17α-эстрадиол, эстриол, эстрон и фитоэстрогены. Эти эстрогены могут быть дериватизованы или модифицированы для образования, например, конъюгированных лошадиных эстрогенов, этерифицированных эстрогенов, этинилэстрадиола и т.д. Примеры этерифицированных эстрогенов включают в себя, но не ограничиваются ими: эстрадиол-3,17-диацетат, эстрадиол-3-ацетат, эстрадиол-17-ацетат, эстрадиол-3,17-дивалерат, эстрадиол-3-валерат, эстрадиол-17-валерат. Также включены селективные модуляторы рецептора эстрогена (SERMS), например ралоксифен, доступный под товарным названием Evista® из Eli Lilly, и т.п. Эстрогены могут также присутствовать в виде солей (например, в виде сульфата натрий-эстрогена), изомеров или пролекарств.
Включены также фитоэстрогены, которые являются происходящими из растений эстрогенами. Изофлавоны являются одной из главных форм фитоэстрогенов и имеют общую дифенольную структуру, которая сходна со стуктурой сильных синтетических эстрогенов, таких как диэтилстильбэстрол и гексэстрол. Основные изофлавоны, найденные в людях, включают в себя, но не ограничиваются ими, генистеин, диадзеин и эквол.
“Пероральные эстрогены” обозначают любой эстроген, который находится в дозированной лекарственной форме, пригодной для перорального введения. Конъюгированные лошадиные эстрогены, этерифицированные эстрогены и микронизированный эстрадиол являются примерами пероральных эстрогенов. Коммерчески доступные пероральные эстрогенные продукты включают в себя конъюгированные лошадиные эстрогены, доступные под товарным названием Премарин® из Wyeth-Ayerst Laboratories, этерифицированные эстрогены, доступные под товарным названием Эстратаб® из Solvay Pharmaceuticals, и микронизированный 17β-эстрадиол, доступный под товарным названием Эстрасе® из Bristol Meyers Squibb.
“Прогестин”, или “прогестерон”, обозначают любое вещество, природное или синтетическое, которое проявляет биологическое или фармакологическое действие первично посредством связывания с рецепторами прогестина. Примеры включают в себя, но не ограничиваются ими: прогестерон, ацетат медроксипрогестерона, норэтиндрон и ацетат норэтиндрона, их эфиры, производные, пролекарства и изомеры. Прогестин может быть введен женщине для достижения нескольких эффектов. Примеры, без ограничения, включают в себя обеспечение эндометриальной безопасности во время сопутствующего введения эстрогена и обеспечение эффективной контрацепции. Хотя количество прогестина, необходимое для достижения таких эффектов, может варьироваться от женщины к женщине, способы определения подходящих и эффективных количеств прогестина для достижения описанных цели или эффекта хорошо известны специалистам с обычной квалификацией в данной области.
“Связывающий половые гормоны глобулин”, или “SHBG”, также известный как связывающий половые гормоны белок (SHBP) и связывающий тестостерон-эстрадиол глобулин (TeBG), обозначает сывороточный белок, который связывает различные половые гормоны с высокой аффинностью (см. таблицу 1; из Dunn et al., Transport of Steroid Hormones: Binding of 21 Endogenous Steroides to Both Testosterone-Binding Globulin and Corticosteroid-Binding Globulin in Human Plasma, J. Clinical Endocrinology and Metabolism, Vol. 53:58-67 (1981)). Представленные константы аффинности связывания (К-величины) для конкретных половых гормонов и SHBG приведены в таблице 1 следующим образом (заимствовано из Dunn et al., 1981).
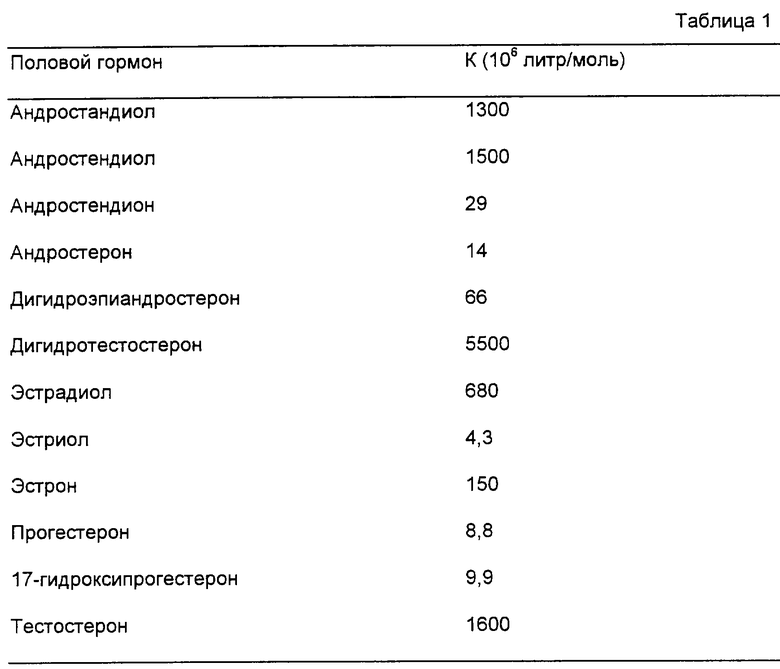
Для целей данной заявки константы аффинности связывания SHBG, превышающие приблизительно 1×106 литр/моль, свидетельствуют о высокой аффинности связывания.
Структура и предполагаемые функции SHBG были описаны и охарактеризованы. См., например, Rosner et al., Sex Hormone-Binding Globulin Mediates Sreroid Hormone Signal Transduction at the Plasma Membrane, J. Steroid Biochem. Mol. Biol. Vol. 69:481-5 (1999); Petra, P.H. The plasma Sex Steroid Binding Protein (SBP or SHBG). A Critical Review of Recent Developments on the Structure, Molecular Biology and Function, J. Steroid Biochem. Mol. Biol. Vol. 40:735-53 (1991). Различные способы использовали для количественного определения концентраций SHBG, в том числе осаждение сульфатом аммония, гель-фильтрацию, равновесный диализ, покрытый декстраном уголь и радиоиммуноанализ. См., например, Khan et al., Radioimmunoassay for Human Testosterone-Estradiol-Binding Globulin, J. Clinical Endocrinology and Metabolism. Vol. 54:705-710 (1982). При помощи валидизированного моноклонального иммуно-радиометрического анализа (Endocrine Sciences, Calabassas Hills, CA) было обнаружено, что средний сывороточный уровень SHBG в здоровых предклимактерических женщинах равен 84 нмоль/л, а нормальный диапазон равен 36-185 нмоль/л. Известно, что сывороточные уровни SHBG повышаются в женщинах, получавших пероральные, эстрогены, эстрогенсодержащие пероральные контрацептивы, кломифен, тамоксифен, ралоксифен, фенитоин и натрий-валпроат, а также в женщинах, которые являются беременными, гипертиреоидными, имеют хроническое заболевание печени и ВИЧ-инфекцию. См., например, Bond et al., Sex Hormone Binding Globulin in Clinical Perspective, Acta. Obstet. Gynecol. Scand. Vol. 66:255-262 (1987); Miller et al., Transdermal Testosterone Administration in Women with Acquired Immunodeficiency Syndrome Wasting: A Pilot Study, J. of Clinical Endocrinology and Metabolism. Vol. 83:2717-2725 (1998).
“Введение” обозначает способ, при помощи которого лекарственное средство предоставляется субъекту. Введение может быть выполнено различными путями, хорошо известными в данной области, такими как пероральные и непероральные способы.
“Пероральное введение” может достигаться проглатыванием, разжевыванием или сосанием пероральной дозированной лекарственной формы, содержащей лекарственное средство. “Непероральное введение” обозначает любой способ введения, в котором лекарственная композиция не обеспечена в твердой или жидкой пероральной дозированной форме, причем такая твердая или жидкая пероральная дозированная лекарственная форма традиционно предназначена для высвобождения и/или доставки лекарственного средства в основном в желудочно-кишечном тракте за пределами ротовой полости и/или щечного кармана. Такие твердые дозированные формы включают в себя общепринятые таблетки, капсулы, каплетки и т.д., которые по существу не высвобождают лекарственное средство во рту или в полости рта.
Понятно, что многие пероральные жидкие дозированные лекарственные формы, такие как растворы, суспензии, эмульсии и т.д., и некоторые пероральные твердые дозированные формы могут высвобождать некоторую часть лекарственного средства во рту или в ротовой полости во время проглатывания этих готовых форм. Однако, вследствие их очень короткого транзитного времени при прохождении через рот или полость рта, высвобождение лекарственного средства из этих готовых форм во рту или полости рта рассматривается как минимальное или несущественное. Таким образом, буккальные пластыри, адгезивные пленки, подъязычные таблетки и лепешки, которые предназначены для высвобождения лекарственного средства во рту, являются непероральными композициями для данных целей.
Таким образом, термин “непероральные” включает в себя парентеральные, местные, ингаляционные, имплантированные, глазные, назальные и вагинальные или ректальные композиции и введения. Далее, имплантируемые композиции должны быть включены в термин “непероральные”, независимо от физического местоположения имплантата.
“Парентеральное” введение может достигаться инъекцией лекарственной композиции внутривенно, внутриартериально, внутримышечно, внутриоболочечно или подкожно и т.д.
“Локальная (местная) композиция” означает композицию, в которой лекарственное средство может быть помещено для прямого нанесения на поверхность кожи и из которой высвобождается эффективное количество лекарственного средства. Примеры локальных композиций (т.е. композиций для местного применения) включают в себя, но не ограничиваются ими, мази, кремы, гели, трансдермальыне пластыри, спреи, вагинальные кольца и пасты. “Трансдермальный” (чрескожный) обозначает способ введения, который облегчает перенос лекарственного средства через поверхность кожи, в котором трансдермальную композицию наносят на поверхность кожи.
Трансдермальное введение может выполняться наложением, намазыванием, накатыванием, прикреплением, выливанием, прижиманием, втиранием и т.д. трансдермального препарата на поверхность кожи. Эти и другие способы введения хорошо известны в данной области.
“Трансдермальная система доставки”, “трансдермальные пластыри” или просто “пластыри” обозначают приспособление для доставки типа матрикса или резервуара с жидкостью, которое используют для трансдермальной (чрескожной) доставки определенных доз вещества на протяжении конкретного периода нанесения.
Одним примером трансдермального пластыря для введения андрогенного стероида в соответствии с данным изобретением является пластырь типа матрикса, который содержит герметическую подкладку, которая является непроницаемой для андрогенных стероидов и определяет лицевую или верхнюю поверхность пластыря, и твердый или полутвердый слой матрикса, состоящий из гомогенной смеси гормона, полимерного чувствительного к давлению адгезивного (липкого) носителя и необязательных одного или нескольких усилителей проникновения через кожу. Имеющие матрикс пластыри известны в области трансдермальной доставки лекарственных средств. Примерами, без ограничения, имеющих адгезивный матрикс трансдермальных пластырей являются пластыри, описанные или цитируемые в Патентах США №№5122383 и 5460820, которые включены таким образом в качестве ссылки в их полном виде.
Другим примером трансдермального пластыря для введения андрогенного стероида в соответствии с данным изобретением является пластырь типа системы с резервуаром для жидкости (LRS), которая содержит андроген и другие необязательные ингредиенты, такие как усилитель проникновения, в несущем наполнителе. Несущий наполнитель содержит жидкость желаемой вязкости, такую как гель или мазь, которую готовят для заключения в резервуар, имеющий непроницаемую подкладку и проницаемую мембрану для контакта с кожей, или мембранный адгезивный слоистый материал, обеспечивающий диффузионный контакт между содержимым резервуара и кожей. Для применения отделяемый герметизирующий высвобождение слой удаляют и пластырь прикрепляют к поверхности кожи. LRS-пластыри известны в области трансдермальной доставки лекарственного средства. Неограничительными примерами LRS-трансдермальных пластырей являются пластыри, описанные или цитируемые в Патентах США №№4849224, 4983395, которые включены таким образом в качестве ссылки в их полном виде.
Термины “кожа”, “поверхность кожи”, “дерма”, “эпидермис” и подобные термины используются здесь взаимозаменяемо и относятся не только к наружной коже субъекта, содержащей эпидермис, но также к поверхностям слизистых оболочек, на которые может быть введена лекарственная композиция. Примеры поверхностей слизистых оболочек включают в себя респираторные (в том числе назальные и легочные), оральные (рот и щечная поверхность во рту), вагинальную, интроитальную (поверхность отверстий (входов в канал или полый орган, например, влагалище)), губную и ректальную поверхности. Таким образом, термин “трансдермальная” включает в себя также “трансмукозная”.
“Совместное введение” (“ко-введение”) и аналогичные термины обозначают введение множественных веществ одному индивидууму, одновременно или последовательно. Так, при ссылке на эстроген и андроген этот термин включает в себя любую ситуацию, при которой женщины принимают пероральный эстроген и непероральный андроген. Этот термин не подразумевает, что эстроген и андроген должны вводиться в одно и то же время. Скорее, до тех пор, пока женщина получает пероральный эстроген, введение неперорального андрогена будет находится в пределах данного определения “совместное введение”. Должно быть понятно, что эстроген и андроген не должны предоставляться в виде единого продукта или посредством идентичного пути для “совместного введения”.
Термины “готовая форма” или “композиция” используются здесь взаимозаменяемо. Термины “фармацевтическое вещество” и “лекарственное средство” используются также взаимозаменяемо для обозначения фармацевтически активного вещества или композиции. Эти термины данной области хорошо известны в областях фармацевтики и медицины.
“Общий уровень в сыворотке”, “общий уровень в крови” и “эндогенный уровень в сыворотке” относятся к общим уровням в сыворотке андрогена или эстрогена, включающим в себя как белоксвязанный, так и свободный андроген или эстроген. Некоторые белки, такие как альбумин, связывают андроген или эстроген с низкой аффинностью, так что эти половые гормоны являются функциональными (биодоступными) (т.е. проявляют их известный или предполагаемый эффект). В противоположность этому, некоторые белки, такие как SHBG, связывают андроген или эстроген с высокой аффиностью, делая их нефункциональными. Специалисту в данной области известно, как измерить и охарактеризовать эти типы связывания. См., например, Dunn et al.
Таким образом, термин “общий уровень тестостерона в сыворотке” относится к сумме: (1) свободного тестостерона; (2) тестостерона, который слабо связан с сывороточными белками, такого как альбумин-связанный тестостерон; и (3) тестостерона, который прочно связан с сывороточными белками высокой аффинности, такого как SHBG-связанный тестостерон.
Термин “белок-связанный” включает в себя все типы связывания с белком.
Общий сывороточный тестостерон может быть измерен известными способами анализа, такими как радиоиммуноанализ (РИА). См., например, процедуру РИА, используемую Endocrine Sciences, Inc. (Calabassas Hills, CA). Эта процедура основана на РИА, опубликованном Furuyama et al., Radioimmunoassay for Plasma Testosterone, Steroids, 1970; 16:415-428. Сообщалось, что с использованием данного способа анализа нормальный диапазон уровней общего сывороточного тестостерона, измеренного в здоровых предклимактерических женщинах согласно Endocrine Sciences, Inc., был 14-54,3 нг/дл (Miller et al., 1998).
“Уровень эндогенного свободного тестостерона”, или “уровень физиологического свободного тестостерона”, будет относиться к уровню свободного тестостерона (FT), который обычно обнаруживается во взрослых женщинах без симптомов, связанных с недостаточностью тестостерона и/или избытком тестостерона, и/или симптомов несбалансированных эстрогена/андрогена.
“Биодоступный”, “сывороточный биодоступный” и подобные термины относятся к андрогену или эстрогену, который не связан с SHBG. Таким образом, андроген, который является “свободным” (несвязанным) или “слабо связанным” с сывороточным альбумином (легко диссоциируемым от него) рассматривается как биодоступный для тканей. Вследствие высокой связывающей способности (ненасыщаемости) альбумина в отношении тестостерона сывороточная концентрация альбумин-связанного тестостерона будет, как правило, пропорциональна концентрации свободного тестостерона. Коэффициент пропорциональности соответствует произведению константы связывания альбумин-тестостерон (3,6×104 л/моль) и концентрации сывороточного альбумина (выраженной в моль/л). См. Vermeulen et al., A Critical Evalution of Simple Methods for the Estimation of Free Testosterone in Serum, J. of Clinical Endocrinology and Metabolism. Vol. 84:3666-3672 (1999). Поскольку концентрация сывороточного альбумина поддерживается в пределах относительно узкого диапазона (например, 4-5 г/дл; 5,8×10-4 7,6×10-4 моль/л), коэффициент пропорциональности равен приблизительно 22. Как следствие этой зависимости, концентрация биодоступного тестостерона может быть приблизительно в 23 раза выше, чем концентрация свободного тестостерона, независимо от концентраций общего тестостерона и SHBG.
Концентрацию биодоступного тестостерона обычно измеряют с использованием способа осаждения сульфатом аммония. См., например, Nankin et al. Daytime Titers of Testosterone, LH, Estrone, Estradiol and Testosterone-Binding Protein: Acute Effects of LH and LH-Releasing Hormone in Men, J. Clinical Endocrinology Metabolism. Vol. 41:271-81 (1975). Сообщалось, что с использованием этого способа нормальный диапазон уровней биодоступного тестостерона, измеренных в здоровых предклимактерических женщинах согласно Endocrine Sciences, Inc., был 1,6-12,7 нг/дл или приблизительно 2-13 нг/дл.
“Свободный”, “несвязанный” или подобные термины относятся к андрогену или эстрогену, который не присоединен ни к какому белку, такому как SHBG или альбумин. Таким образом, андроген или эстроген, который не связан с белком, считается “свободным”.
В качестве неограничительного примера термины, такие как “свободный тестостерон”, “несвязанный тестостерон”, “свободный сывороточный тестостерон”, относятся к тестостерону в сыворотке, который не связан с белком. Уровни сывороточного свободного тестостерона могут быть измерены различными лабораторными способами, в том числе равновесным диализом, ультрафильтрацией, аналогичным РИА-способом и расчетом из уровней общего тестостерона, SHBG и альбумина. См., например, Winters et al. The Analog Free Testosterone Assay: Are the Results in Men Clinically Useful? Clinical Chemistry. Vol. 44:2178-2182 (1998); см. также Vermeulen et al. (1999). Считается, что в настоящее время способ равновесного диализа обеспечивает наиболее точные результаты. См. Mathor et al., Free Plasma Testosterone Levels During the Normal Menstrual Cycle, J. Endocrinol. Invest. Vol. 8:437-41 (1985). Сообщалось, что с использованием этого способа нормальный диапазон уровней свободного тестостерона, измеренных в здоровых предклимактерических женщинах согласно Endocrine Sciences, Inc., был 1,3-6,8 пг/мл или приблизительно 2-7 пг/мл.
Термин “женщина” обозначает женскую особь человека, которая получает пользу от добавления андрогена или эстрогена любым путем. В одном аспекте женщина может быть менопаузальной вследствие возраста, оофорэктомии или овариальной недостаточности. В другом аспекте эта женщина может получать пероральные эстрогены для благоприятных эффектов, например для предупреждения или задержки рарефикации костной массы (остеопороза), для предупреждения или задержки изменений в липидах крови, которые в противном случае предрасполагают эту женщину к сердечно-сосудистому заболеванию. Еще в одном варианте эта женщина может проявлять недостаточность или дисбаланс эстрогенных и андрогенных гормонов. Еще в одном варианте эта женщина может принимать пероральные эстрогены для контрацепции.
“Улучшение здоровья” обозначает уменьшение, улучшение или предупреждение встречаемости и/или интенсивности симптомов, связанных с недостаточночтью андрогенных стероидов. Примеры таких симптомов включают в себя, но не ограничиваются ими: половую дисфункцию, которая может проявляться в утрате полового влечения, уменьшенной чувствительности к сексуальной стимуляции, пониженной возбудимости и способности к оргазму, пониженную жизненную энергию, пониженное настроение, уменьшенное чувство благополучия, повышенную застенчивость, потерю мышечной массы и функции, неблагоприятный состав тела, т.е. отношение массы тощих мышц к жирным мышцам, поредение и потеря лобковых волос, атрофию мочеполовых путей, сухие и ломкие волосы волосистой части головы (скальпа), сухую кожу, сниженные познавательные способности, сухость глаз, аутоиммунные явления и их комбинацию.
Увеличения и уменьшения в присутствии и тяжести таких симптомов могут быть определены с использованием различных устройств, известных в данной области, для оценки каждого конкретного симптома. Например, половая функция у женщин может быть оценена с использованием анкет самооценки, таких как Brief Index of Sexual Functioning for Women, (Taylor et al., 1994); Derogatis Interview for Sexual Functioning, Derogatis, L., The Derogatis Interview for Sexual Functioning (DISF/DISF-SR): an introductory report, J. Sex. Marital Ther. Winter 23(4):291-304 (1997) и других анкет, таких как Derogatis et al., Psychological assessment measures of human sexual functioning in clinical Trials, Int. J. Impot. Res., May 10 Suppl. 2:S13-20 (1998); а также с использованием способов исследования кровоснабжения половых органов (Laan, 1998). Массу мышц, состав тела и минеральную плотность костей обычно измеряют с использованием рентгеновской абсорбциометрии с двойной энергией (DEXA). Настроение, чувство благополучия и нейрокогнитивную функцию можно измерить с использованием Beck Depression Inventory (Beck et al., 1961), психологического общего индекса благополучия (Dupuy, 1984) и батареи тестов нейрокогнитивной функции. Синдром сухих глаз может быть оценен при помощи тестов для функции слезоотделения, например осмоляльности, объема, скорости истечения, теста Ширмера, с использованием препаратов искусственных слез и с использованием субъективных анкет. См., например, Mathers et al. Menopause and Tear Function: The Influence of Prolactin and Sex Hormones on Human Tear Production, Cornea. Vol. 17:353-8 (1998). Иммунная функция может быть оценена по титрам циркулирующих аутоантител, по числу CD4+ и CD8+ лимфоцитов и по симптоматологии конкретных аутоиммунных нарушений, например системной красной волчанки, ревматоидного артрита, и т.д.
“Повышенная”, в применении в связи с уровнями SHBG, обозначает сывороточную концентрацию SHBG, измеренную в конкретной женщине, которая является более высокой, чем средняя величина для здоровой предклимактерической женщины, сообщенная клинической лабораторией, в которой измеряют уровень SHBG. Например, величина, полученная с использованием методологии иммунорадиометрического анализа Endocrine Sciences, Inc., рассматривалась бы как повышенная, если бы она была больше 84 нмоль/л. “Существенно повышенный” уровень SHBG обозначает концентрацию SHBG в сыворотке в конкретной женщине, которая больше, чем верхний предел нормального диапазона для здоровой предклимактерической женщины, сообщенный клинической лабораторией, в которой измеряют этот уровень SHBG. Например, величина, полученная с использованием методологии иммунорадиометрического анализа Endocrine Sciences, Inc., рассматривалась бы как существенно повышенная, если бы она была больше 185 нмоль/л. В связи с различными способами, используемыми для измерения SHBG в различных лабораториях клинических стандартов, и соответствующими вариациями в средних величинах и нормальных диапазонах, сообщаемых ими, определения повышенных величин SHBG, приведенные выше, применимы к любому валидизированному способу с правильно определенными нормальными диапазонами.
“Эффективное количество” обозначает количество вещества, которое является достаточным для достижения его предполагаемой цели или его предполагаемого эффекта. Различные биологические факторы могут влиять на способность доставляемого вещества выполнять его предполагаемую задачу. Таким образом, “эффективное количество” может зависеть от таких биологических факторов. В качестве примера, без ограничения, женщина, имеющая уровень сывороточного SHBG 225 нмоль/л, может нуждаться в более высокой дозе тестостерона для достижения предполагаемого эффекта, чем женщина, имеющая уровень сывороточного тестостерона 100 нмоль/л. Таким образом, хотя дозы тестостерона в таких женщинах будут варьироваться, каждая доза должна рассматриваться как “эффективное количество” до тех пор, пока она позволяет достичь желаемый эффект. Определение “эффективного количества” находится вполне в рамках обычной квалификации в данной области.
Многочисленные оценки могут быть использованы для измерения достижения желаемых эффектов в случае доставки андрогенов и эстрогенов, которые хорошо известны в данной области. Такие оценки могут выполняться врачом или другим квалифицированным медицинским персоналом и могут включать в себя физическое обследование, анализы крови и т.д.
“Терапевтический эффект” обозначает желаемый результат, который достигается до какой-либо степени. В контексте добавления андрогенов и эстрогенов, представленного в данной патентной заявке, ряд желаемых результатов называют “улучшением здоровья”. В одном аспекте терапевтические эффекты могут быть достигнуты доставкой “эффективного количества” вещества, способного приводить к желательному результату до выбранной степени. Хотя достижение терапевтических эффектов может быть измерено врачом или другим квалифицированным медицинским персоналом с использованием оценок, известных в данной области, понятно, что индивидуальные вариация и ответная реакция на лечение могут делать достижение терапевтических эффектов субъективным решением.
Концентрации, количества, растворимости и другие цифровые данные могут быть представлены здесь в формате диапазонов. Должно быть понятно, что такой формат диапазонов используется лишь для удобства и краткости и должен интерпретироваться гибко, чтобы включать в себя не только цифровые величины, точно указанные как границы диапазона, но также включать в себя все индивидуальные цифровые величины или поддиапазоны, заключенные в данном диапазоне, как если бы каждая цифровая величина и каждый поддиапазон были точно названы.
Например, диапазон концентраций 0,5-15 пг/мл должен интерпретироваться как включающий в себя не только точно названные границы концентраций 0,5 пг/мл и 15 пг/мл, но также как включающий индивидуальные концентрации в этом диапазоне, такие как 0,5 пг/мл, 0,7 пг/мл, 1,0 пг/мл, 5,2 пг/мл, 11,6 пг/мл, 14,2 пг/мл, и поддиапазоны, такие как 0,5-2,5 пг/мл, 4,8-7,2 пг/мл, 6-14,9 пг/мл, и т.д. Эта интерпретация должна применяться независимо от ширины диапазона или от описываемых характеристик.
В. Изобретение
Недавнее исследование показало, что андрогены и, в частности, тестостерон вносят существенный вклад в здоровье и благополучие женщины. В одном аспекте Ebert et al. Патент США 5460820 описывают композицию и способ для введения тестостерона трансдермально с использованием пластыря в качестве системы доставки. Эти композиции и способы поддерживают общие уровни тестостерона в сыворотке крови в “физиологическом диапазоне” между приблизительно 15 и 80 нг/дл при трансдермальном введении приблизительно 50-500 мкг/день тестостерона из тестостеронового матрикса. Считается, что непероральная доставка андрогенов является более безопасной для печени и обеспечивает более длительную доставку, чем пероральные способы, так как избегаются эффекты метаболизма первого прохождения. С другой стороны, пероральная доставка эстрогенов делает возможным улучшенный профиль сывороточных липидов. Однако было обнаружено, что указанные выше общие уровни сывороточного тестостерона для женщин могут не быть точным индикатором терапевтически эффективных уровней тестостеронов у женщин с повышенными или существенно повышенными уровнями SHBG, например, у женщин, получающих пероральные эстрогены.
Известно, что связывание тестостерона с SHBG уменьшает транспорт тестостерона к андроген-чувствительным тканям, например тканям, экспрессирующим рецепторы андрогенов. Известно также, что такое связывание уменьшает скорость метаболического клиренса тестостерона как у мужчин, так и у женщин. См., например, Vermeulen et al. Metabolic Clearance Rate and Interconversion of Androgens and the Influence of the Free Androgen Fraction, J. Clinical Endocrinology and Metabolism. Vol. 48:320-326 (1979); Longcope et al. Free Estradiol, Free Testosterone and Sex Hormone-Binding Globulin in Perimenopausal Women, J. Clinical Endocrinology and Metabolism. Vol. 64:513-518 (1987). Вследствие влияния уровней SHBG на связывание и клиренс тестостерона, сывороточные уровни общего, свободного и биодоступного андрогена, которые достигаются введением андрогена конкретному индивидууму, будут зависеть от уровня SHBG этого индивидуума. Однако влияние уровней SHBG на полученные сывороточные уровни андрогена не могут быть точно предсказаны на основании имеющихся в настоящее время знаний, и необходимы экспериментальные данные.
Для обеспечения таких данных выполняли фармакокинетические исследования в трех группах хирургически менопаузальных женщин (т.е. женщин в менопаузе вследствие хирургического вмешательства), которым вводили 300 мкг/день тестостерона в виде трансдермального пластыря с содержащим тестостерон матриксом дважды в неделю в течение 7 дней. Одна группа не получала эстрогеновой заместительной терапии (ERT) в течение по меньшей мере одного месяца, вторая группа получала трансдермально эстрадиол (Е2) в дозе 0,1 мг/день, а третья группа получала пероральные конъюгированные лошадиные эстрогены (СЕЕ) в дозе 1,25 мг/день. Измерения уровня SHBG, полученные перед наложением пластыря, и уровней общего и свободного тестостерона, полученные до и во время второго 3,5-дневного периода применения пластыря, были выполнены Endocrine Sciences. Полученные данные по гормонам (среднее ± SEM (стандартная ошибка среднего)) для этих трех групп хирургически менопаузальных женщин, участвующих в этом клиническом испытании, суммированы в таблице 2 ниже.
Следует отметить, что нормальный диапазон для уровней SHBG является 36-185 нмоль/л при использовании анализа Endocrine Sciences. Далее, изменения в уровнях общего тестостерона и свободного тестостерона представляют собой средние по времени изменения от изменения от базовых уровней во время 3,5-дневного применения пластыря.

Как показано в таблице 2, средний уровень SHBG в группе с пероральным эстрогеном был приблизительно в 2,5 раза большим, чем в других группах, и превышал верхнюю границу нормального диапазона. Уровни SHBG в группе с трансдермальным эстрогеном были сравнимы с уровнем у женщин, которые не получали эстрогеновой заместительной терапии (ERT). Среднее увеличение в уровнях общего тестостерона во время применения пластыря, т.е. усредненное по времени изменение от базовой линии, было приблизительно на 30% более высоким в группе с пероральным эстрогеном, в сравнении с двумя другими группами.
В противоположность среднему увеличению в уровне свободного сывороточного тестостерона в группе с пероральным эстрогеном было приблизительно на 40% более низким, чем в двух других группах. Эти результаты показывают, что посредством снижения клиренса тестостерона повышенные уровни SHBG приводят к увеличению общих сывороточных уровней тестостерона, полученному во время трансдермального введения тестостерона. Однако несмотря на повышение общих сывороточных уровней уровни свободного сывороточного тестостерона и, в результате, уровни биодоступного сывороточного тестостерона уменьшаются повышенными уровнями SHBG, предположительно вследствие увеличенного связывания тестостерона SHBG. Эти открытия являются новыми и неожиданными и не могли быть предсказаны на основании более ранних исследований.
В качестве дальнейшей иллюстрации этих новых действий SHBG на уровни тестостерона индивидуальные приращения общего сывороточного тестостерона и свободного сывороточного тестостерона, полученные во время трансдермального введения 300 мкг/в день тестостерона хирургически менопаузальным женщинам, получающим трансдермальный или пероральный эстроген, наносили на график против индивидуальных уровней SHBG на фиг.1 и 2 соответственно. Как изображено на логарифмических шкалах, приращения в общем сывороточном тестостероне становятся большими с увеличением уровней SHBG, тогда как приращения в свободном тестостероне становятся меньшими по мере увеличения уровней SHBG.
Для дополнительной иллюстрации нового и неожиданного влияния повышенных уровней SHBG на непероральное введение тестостерона таблица 3 ниже обеспечивает оценки скорости доставки тестостерона, необходимой для достижения конкретного увеличения в свободном тестостероне (FT), которые были получены как функция уровня SHBG с использованием уравнения регрессии степенного типа, приведенного на фиг.2. Как показано в таблице 3, необходимая скорость доставки для достижения конкретного увеличения (изменения) FT увеличивается заметно по мере увеличения уровня SHBG. Например, скорость доставки, необходимая для достижения увеличения 15 пг/мл в пациенте, уровень SHBG которого равен 700 нмоль/л, оценивается как 2484 мкг/день, причем эта величина по существу превышает величину, описываемую в предыдущем уровне техники.
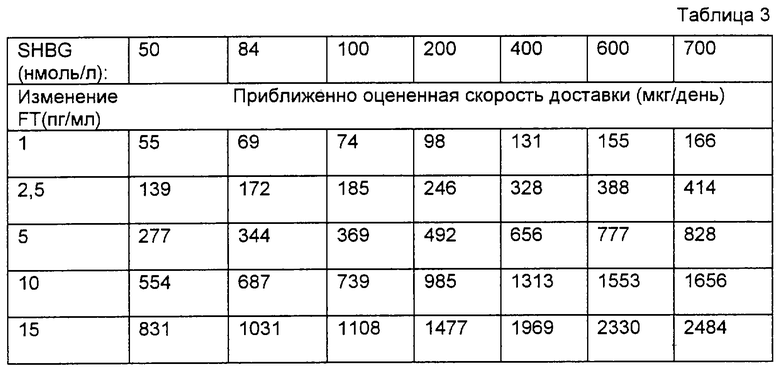
Для скоростей доставки, приведенных выше, изменения в общем уровне тестостерона (нг/дл), соответствующие желаемому изменению в уровне свободного тестостерона и конкретному уровню SHBG, могут быть предсказаны при помощи уравнения регрессии степенного типа, показанного на фиг.1. Таблица 4 ниже обеспечивает иллюстрацию таких предсказаний. Как показано в таблице 4, изменения в уровне общего тестостерона, соответствующие конкретному изменению в уровне свободного тестостерона, увеличиваются заметно по мере увеличения уровня SHBG. Например, в случае, соответствующем изменению в свободном тестостероне 15 пг/мл в пациенте, уровень SHBG которого равен 700 нмоль/л (т.е. скорость доставки 2484 мкг/день), предсказанное увеличение в общем тестостероне равно 820 нг/дл.

Должно быть понятно, что при экстраполяции результатов и предсказаний таблиц 2, 3 и 4 относительно фактического пациента следует прибавить базовый уровень тестостерона пациента (т.е. уровень общего или свободного тестостерона перед лечением) к ожидаемому изменению в уровне тестостерона вследствие лечения. Для индивидуумов с базовыми уровнями, которые являются субнормальными, конечные уровни гормонов, полученные в результате лечения, будут близки к самому изменению.
Приведенные выше новые результаты и предсказания указывают на то, что введение андрогенов женщинам, принимающим пероральные эстрогены, или женщинам, которые обычно имеют повышенные уровни SHBG, будет давать уровни свободного и/или биодоступного тестостерона, которые будут значимо более низкими в сравнении с женщинами, которые принимают непероральные эстрогены или которые имеют низкие или нормальные уровни SHBG. Кроме того, женщины, находящиеся на терапии с пероральным эстрогеном, или женщины с повышенными уровнями SHBG, будут нуждаться в дозах андрогенов, которые могут превышать дозы, ранее считающиеся оптимальными у женщин с нормальными уровнями SHBG. Кроме того, введение таких доз будет давать уровни общего сывороточного тестостерона, превышающие обычно признаваемые нормальные диапазоны. Следует также отметить, что для некоторых терапевтических применений, например краткосрочных применений андрогенов, желательные терапевтические уровни свободного и/или биодоступного тестостерона могли бы также быть более высокими, чем соответствующие нормальные физиологические диапазоны. Таким образом, данное изобретение обеспечивает способы, композиции и наборы для введения андрогенного стероида для улучшения здоровья женщины в условиях, когда уровни SHBG этой женщины являются повышенными.
С. Различные аспекты
В одном аспекте данное изобретение представляет способ и набор для введения половых гормонов, таких как андрогены и эстрогены, женщинам. В другом аспекте данное изобретение представляет способ и набор для неперорального введения андрогенных стероидов женщине, имеющей повышенные уровни SHBG, для ослабления симптомов, связанных с недостаточностью андрогенных гормонов. Еще в одном аспекте данное изобретение обеспечивает способ и набор для неперорального введения андрогенных стероидов женщине, которая получает пероральное добавление эстрогена. В следующем аспекте данное изобретение обеспечивает способ и набор для совместного введения (ко-введения) перорально вводимого эстрогена и неперорально вводимого андрогенного стероида. Было обнаружено, что эти способы и наборы для введения эстрогенов и/или андрогенных стероидов применимы в улучшении здоровья, сексуальной функции и благополучия.
В одном аспекте данного изобретения андроген может быть введен в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню свободного тестостерона от приблизительно 0,5 до приблизительно 30 пг/мл. В другом аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню свободного тестостерона, от приблизительно 1 до приблизительно 15 пг/мл. В другом аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню свободного тестостерона от приблизительно 1,3 до приблизительно 6,8 пг/мл, или от приблизительно 2 до приблизительно 7 пг/мл. Еще в одном аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню свободного тестостерона от приблизительно 3 до приблизительно 10 пг/мл.
В одном аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню биодоступного тестостерона от приблизительно 1 до приблизительно 70 нг/дл. В другом аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню биодоступного тестостерона от приблизительно 2 до приблизительно 35 нг/дл. Еще в одном аспекте данного изобретения, андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню биодоступного тестостерона от приблизительно 2 до приблизительно 13 нг/дл.
В одном аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню общего тестостерона от приблизительно 15 до приблизительно 1000 нг/дл. В другом аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню общего тестостерона от приблизительно 85 до приблизительно 1000 нг/дл. В следующем аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного сывороточному уровню общего тестостерона от приблизительно 100 до приблизительно 1000 нг/дл.
В одном аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного дозе тестостерона по меньшей мере приблизительно 50 мкг/день. В другом аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного дозе тестостерона от приблизительно 75 до приблизительно 3000 мкг/день. В следующем аспекте данного изобретения андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного дозе тестостерона от приблизительно 600 до приблизительно 3000 мкг/день. Еще в одном аспекте андроген может вводиться в дозе, достаточной для достижения терапевтического эффекта, эквивалентного дозе тестостерона от приблизительно 700 до приблизительно 3000 мкг/день.
Одним из непероральных способов доставки для дозы андрогена является местное введение. Композиции для местного введения могут включать в себя усилитель (усилители) проникновения в кожу для повышения уровня поступления в кожу андрогенов. Примеры, без ограничения, усилителей проникновения в кожу, которые могут быть использованы, описаны или цитируется в Патентах США №5122383 и 5153997, описания которых, которые относятся к усилителям проникновения в кожу, включены таким образом в качестве ссылки. Далее индекс усилителей проникновения описан David W. Osborne and Jill J. Henke в их публикации в Интернете, озаглавленной Skin Penetration Enhancers Cited in the Technical Literature, которая может быть найдена по веб-адресу (по адресу всемирной компьютерной сети), известному как pharmtech.com/technical/osborne/osborne.htm, которая включена таким образом в качестве ссылки. Эффективное количество усилителя может быть включено в фармацевтически приемлемый носитель. Различные носители могут быть пригодны в зависимости от типа желаемой композиции доставки. В качестве примера, без ограничения, в случае необходимости трансдермального пластыря с адгезивным матриксом носителем может быть адгезив. В другом аспекте, когда желательным является пластырь системы резервуара с жидкостью (LRS), носителем может быть гель, крем, мазь, лосьон или другая подходящая готовая форма, известная в данной области.
Трансдермальные пластыри для трансдермальной доставки андрогенных стероидов могут быть изготовлены общепринятыми способами, используемыми в области устройств трансдермальной доставки лекарственных средств. Например, андрогены, носитель и усилители могут быть смешаны в желаемых пропорциях с образованием гомогенной смеси и включены в трансдермальное устройство. Различные способы известны в данной области для изготовления различных типов трансдермальных устройств, таких как пластыри с адгезивным матриксом и пластыри с системой резервуара с жидкостью (LRS).
Кроме трансдермальных тестостероновых пластырей, другие непероральные системы для доставки андрогенов включают в себя, но не ограничиваются ими: внутримышечные инъекции эфиров тестостеронов, подкожные имплантаты конденсированного тестостерона и препараты для местного применения тестостерона, метилтестостерона и других андрогенов. Устройства и способы для этих непероральных применений хорошо известны в данной области.
Необходимость в пополнении половых гормонов, таких как эстроген и андрогенные стероиды, должна определяться врачом или другим профессионалом в области медико-санитарной помощи на основе мониторинга признаков и симптомов недостаточности половых гормонов или на основе необходимости фармакологического вмешательства в состояния, которые являются чувствительными к гормональной терапии. Не каждая женщина будет проявлять одни и те же симптомы, и может быть так, что уровни половых гормонов могут быть даже в пределах принятых физиологических диапазонов, но, на основании других факторов, например на основании повышенного уровня SHBG, пополнение половых гормонов может быть все еще необходимым.
Симптомы субфункциональных уровней андрогенов, в том числе тестостерона, могут включать в себя, но не ограничиваются ими: сексуальную дисфункцию, которая может проявляться в потере полового влечения, пониженной чувствительности к сексуальной стимуляции, пониженной возбудимости и способности к оргазму; пониженную жизненную энергию; подавленное настроение; пониженное чувство благополучия; повышенную застенчивость; потерю массы и функции мышц; неблагоприятный состав тела, т.е. отношение массы “тощих” мышц к массе "жирных" мышц; поредение и потерю лобковых волос; атрофию мочеполовых путей; сухие и ломкие волосы волосистой части головы (скальпа); сухую кожу; уменьшенные когнитивные способности; сухие глаза; аутоиммунные явления или их обострение и их комбинацию.
Женщины, которые принимают пероральные эстрогены, могут также получать пользу от андрогенной терапии, так как она может уменьшать болезненность молочной железы, которая может иметь место при применении эстрогена. Благодаря известным антипролиферативным действиям на ткани молочной железы андрогены могут также снижать риск развития рака молочной железы, связанный с применением эстрогена. Таким образом, крайне желательно, если не обязательно, чтобы добавление тестостерона для пациента женского пола было основано на диагнозе врача, который прописывает способ применения, дозу и продолжительность лечения.
При совместном введении с андрогенными стероидами эстроген, например конъюгированный лошадиный эстроген, может вводиться перорально в диапазоне доз между приблизительно 0,2 и 3,0 мг/день. Эта доза может быть скорректирована в соответствии с индивидуальными потребностями женщины и активностью вводимого эстрогена. Доза пероральных эстрогенов может приниматься в виде единственной суточной дозы или в виде двух или более меньших количеств. В идеале для женщин, которые испытывают вазомоторные симптомы, используется самая низкая эффективная доза эстрогена для контроля вазомоторной нестабильности. Более низкие дозы могут быть использованы в случае женщин, которые не страдают вазомоторными симптомами, но будут получать пользу от других преимуществ для здоровья, таких как преимущества в отношении сердечно-сосудистой деятельности и в отношении костей. В случае перорального контрацептивного применения этинилэстрадиол обычно предоставляется циклически в режиме 21 день с этинилэстрадиолом, 7 дней с плацебо.
В одном аспекте данное изобретение обеспечивает способ и набор для введения прогестина с андрогеном и эстрогеном. Известно, что прогестины вводят женщинам для защиты против гиперплазии эндометрия. Прогестины являются также незаменимыми активными ингредиентами многих пероральных контрацептивных препаратов. В соответствии с одним аспектом данного изобретения прогестины могут вводиться любым способом, известным в данной области, в соответствии с потребностью индивидуума. Количество прогестина, которое является эффективным в достижении желаемой цели, может варьироваться от женщины к женщине. Способы определения эффективного количества прогестина, т.е. количества, достаточного для достижения желательного терапевтического эффекта, хорошо известны специалистам с обычной квалификацией в данной области.
На основании приведенных выше доз и лабораторных тестов специалист в данной области может легко определить, какое количество конкретного андрогенного стероида или производного тестостерона вводить для получения желательных уровней андрогенного стероида в сыворотке, которые могут быть достигнуты с использованием более чем одного андрогенного стероида или одной формы тестостерона. Важным является, чтобы доза андрогенного стероида или производного тестостерона была достаточной для получения пользы для женщины-реципиента без введения слишком высокой дозы. Введение подходящих уровней доз для получения оптимального отношения риска/пользы находится вполне в пределах обычной квалификации в данной области.
В вариантах, содержащихся в следующих далее примерах, дозу приблизительно 50-3000 мкг/день андрогенного стероида вводят женщине, принимающей пероральный эстроген в режиме эстрогеновой заместительной терапии (ERT) или в виде контрацептива. Дозы в этом диапазоне являются достаточными для получения терапевтического ответа. Однако эта доза, наиболее подходящая для конкретной женщины, может быть определена эмпирически (например, варьированием доставляемой дозы и оценкой полученных действий на либидо, сексуальную функцию, настроение, общее ощущение благополучия и т.д.). Таким образом, вследствие природной изменчивости в чувствительности к гормонам точная доза является не такой решающей, как получение достигнутого физиологического ответа для конкретного пациента, который может соответствовать уровню общего тестостерона в сыворотке от приблизительно 15 до приблизительно 400 нг/дл или уровню свободного тестостерона в сыворотке от приблизительно 0,5 до приблизительно 15 пг/мл.
Следующие примеры предназначены только для иллюстрации различных аспектов описанного здесь изобретения и не предназначены для ограничения каким-либо образом объема заявленного изобретения. Другие аспекты данного изобретения, которые считаются эквивалентными с точки зрения специалистов с квалификацией в данной области, также находятся в рамках данного изобретения.
Пример 1
В хирургически менопаузальных женщинах в возрасте 20-55 лет пероральный эстроген и трансдермальный тестостерон вводили следующим образом. Эстроген состоял из конъюгированного лошадиного эстрогена (таблетки Премарина®) в суточной дозе 0,625-2,5 мг. Трансдермальный тестостерон вводили с использованием трансдермального пластыря, имеющего матрикс, который накладывали на живот дважды в неделю и который имел скорость доставки 300 мкг/день. Продолжительность совместного введения (ко-введения) была 12 недель. Спустя 12 недель эта схема лечения улучшала сексуальную функцию, настроение и чувство благополучия в сравнении с введением только конъюгированного лошадиного эстрогена.
Было обнаружено, что сывороточные уровни гормонов при этой схеме лечения согласно Endocrine Sciences (Calabassas Hills, CA) находились в следующих диапазонах: общий тестостерон (15,5-254,3 нг/дл), свободный тестостерон (1,7-33,7 пг/мл), биодоступный тестостерон (2,3-71 нг/дл), эстрадиол (5-280 пг/мл) и эстрон (8-410 пг/мл). Уровни связывающего половые гормоны глобулина находились в диапазоне от 62,7 до 563 нмоль/л, причем в 92% случаев они были повышенными и в 48% случаев они были существенно повышенными в соответствии с определениями “повышенные” и “существенно повышенные”, приведенными здесь. Следует отметить, что 73% женщин на схеме лечения с пероральным эстрогеном и трансдермальным тестостероном достигали уровней общего тестостерона более 80 нг/дл, верхней границы нормального диапазона, обычно признаваемого в данной области. В противоположность этому 78% имели уровень свободного тестостерона ниже 6,8 пг/мл (верхней границы нормального диапазона для Endocrine Sciences) и 97% имели уровень свободного тестостерона ниже 15 пг/мл, который находится в пределах рассматриваемого здесь терапевтически приемлемого диапазона. Подобным образом 68% женщин имели уровень биодоступного тестостерона ниже 12,7 нг/дл (верхней границы нормального диапазона для Endocrine Sciences) и 97% имели уровень биодоотупного тестостерона ниже 35 нг/дл, который находится в пределах рассматриваемого здесь терапевтически приемлемого диапазона.
Пример 2
Комбинация андрогенного соединения и эстрогенного соединения может быть введена женщинам, которые являются природно менопаузальными, в соответствии со следующей схемой лечения.
Андроген: местное введение тестостерона в подходящем несущем наполнителе, таком как крем или мазь, который необязательно содержит усилитель проникновения, необходимый для достижения желаемых уровней тестостерона в сыворотке. Содержащий андроген крем может содержать цетиловые зфиры, цетиловый спирт, белый воск, глицерилмоностеарат, моностеарат пропыленгликоля, метилстеарат, бензиловый спирт, лаурилсульфат натрия, глицерин и минеральное масло. Каждый грамм этого крема содержит приблизительно 400 мкг тестостерона. Около 1 г этого крема наносят на кожу или на живот при отходе ко сну. Достигаемые концентрации в сыворотке свободного тестостерона могут находиться в диапазоне 0,5-15 пг/мл, а достигаемые концентрации общего тестостерона могут быть в диапазоне 30-250 нг/дл.
Для регуляции количества вводимого тестостерона может использоваться отмеряющее дозу устройство. Коррекции дозы могут быть произведены либо на основе облегчения симптомов, например восстановленного либидо, либо для достижения желаемых концентраций свободного тестостерона в сыворотке. Диапазоны для облегчения симптомов могут варьироваться между 1-20 пг/мл свободного тестостерона в сыворотке.
Эстрогенное соединение: пероральные таблетки конъюгированных лошадиных эстрогенов могут предоставляться при исходной дозе 0,625 мг/день. При необходимости дозы могут быть увеличены до 1,25 мг/день для лучшего контроля симптомов или могут быть уменьшены до 0,3 мг/день при затухании вазомоторных симптомов для сохранения преимуществ для костей и липидов сыворотки.
У женщин, которые имеют интактную матку, важно, чтобы в сыворотке присутствовало достаточное количество прогестерона для исключения эндометриальной гиперплазии, которая может быть результатом не встречающей сопротивления эстрогеновой заместительной терапии.
Преимущества комбинированной гормональной схемы лечения могут быть замечены пациентом в пределах первых 6 недель введения, но могут иметь место вариабельные ответные реакции. Обычно гормоны вводят в течение продолжительного времени для поддержания здоровья.
Пример 3
Андрогенное соединение и эстрогенное соединение могут вводиться женщинам, которые являются постклимактерическими, для облегчения признаков и симптомов, связанных с хрупкостью, такой как потеря костной и мышечной массы и функции, пониженные когнитивные способности и пониженная энергия.
Андроген: внутримышечная инъекция 150 мг энантата тестостерона один раз в месяц. Энантат тестостерона может быть приготовлен таким образом, что он содержит 200 мг на мл в кунжутном масле. Для обеспечения 150 мг энантата тестостерона инъецируемая доза должна быть 0,75 мл.
Эстроген: пероральные эстрогены предоставляются в диапазоне 0,3-3,0 мг/день.
Введение выполняют до тех пор, пока преимущества лечения являются желательными и считаются полезными по мнению предписывающего врача.
Пример 4
Андрогенное соединение и эстрогенное соединение могут вводиться женщинам с преждевременной недостаточностью яичников, например женщинам, функция яичников которых перманентно приостанавливается до возраста 40 лет.
Андроген: метилтестостерон может предоставляться посредством буккального пути при дозе 1 мг/день для достижения улучшения сексуальной функции, которая является равным образом эффективной относительно улучшения, производимого тестостероном при сывороточных уровнях приблизительно 50-300 нг/дл. Буккальная таблетка может быть двухслойной таблеткой, состоящей из слоя лекарственного средства и биоадгезивного слоя (по 50 мг каждый). Композиция лекарственного слоя (в мас.%) может представлять собой 2% метилтестостерона, 0,75% стеарата магния, 0,1% FD&C желтого №6, 24% Klucel HXF и 73,15% маннита. Композиция биоадгезивного слоя (в мас.%) может представлять собой 69,25% полиэтиленоксида, 30% карбомера 934Р и 0,75% стеарата магния. Адгезивную сторону таблетки прикладывают к десне верхней челюсти, а сторона с лекарственным средством обращена к накрывающей десну буккальной слизистой оболочке. Лекарственное средство абсорбируется трансмукозно (через слизистую оболочку) по мере растворения таблетки на протяжении времени. Таблетку можно применять один раз в день после завтрака.
Эстроген: Estrace®, Bristol-Myers Squibb Co., пероральный микронизированный (измельченный) продукт в форме таблетки, может вводиться в дозе 2 мг/день для облегчения менопаузальных симптомов и предотвращения разрежения кости (остеопороза).
Кроме того, прогестин, такой как ацетат медроксипрогестерона, может вводиться перорально в дозе 5 мг/день в течение последних десяти дней каждого месяца для индукции отделения эндометрия.
Хотя эти примеры направлены прежде всего на доставку андрогенного стероида для обеспечения его пополнения, основанного на определении необходимости этого, это введение должно проводиться совместно с пероральным введением эстрогенных композиций.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ КОНЦЕНТРАЦИИ ТЕСТОСТЕРОНА И РОДСТВЕННЫХ СТЕРОИДОВ У ЖЕНЩИН | 2001 |
|
RU2286787C2 |
| ТРАНСДЕРМАЛЬНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АКТИВНЫЕ АГЕНТЫ | 2010 |
|
RU2639087C2 |
| СПОСОБ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ ВНЕМАТОЧНОЙ ПРОЛИФЕРАЦИИ ЭНДОМЕТРИАЛЬНОЙ ТКАНИ, ОБУСЛОВЛЕННЫХ ЕЮ ХРОНИЧЕСКОЙ БОЛИ В ОБЛАСТИ ТАЗА И НЕПРОХОДИМОСТИ ФАЛЛОПИЕВЫХ ТРУБ | 2000 |
|
RU2255759C2 |
| ВОССТАНОВЛЕНИЕ ТОНИЧЕСКОЙ СЕКРЕЦИИ ЭСТРОГЕНА ИЗ ЯИЧНИКОВ ДЛЯ ПРОДОЛЖИТЕЛЬНЫХ СХЕМ ЛЕЧЕНИЯ | 1995 |
|
RU2181598C2 |
| ПРЕРЫВИСТАЯ ГОРМОНОЗАМЕСТИТЕЛЬНАЯ ТЕРАПИЯ НИЗКИМИ ДОЗАМИ ЭСТРОГЕНА | 2000 |
|
RU2245713C2 |
| НОВАЯ ВСПОМОГАТЕЛЬНАЯ ТЕРАПИЯ ДЛЯ ПРИМЕНЕНИЯ В СПОСОБЕ ЛЕЧЕНИЯ РАКА ПРОСТАТЫ | 2018 |
|
RU2758386C2 |
| СИСТЕМЫ С РЕГУЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ И НИЗКИМИ ДОЗАМИ АНДРОГЕНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ С ПОМОЩЬЮ ЭТИХ СИСТЕМ | 1992 |
|
RU2142276C1 |
| МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ СЕЛЕКТИВНОГО МОДУЛЯТОРА РЕЦЕПТОРОВ ЭСТРОГЕНОВ В КОМБИНАЦИИ С ПРЕДШЕСТВЕННИКАМИ ПОЛОВЫХ СТЕРОИДНЫХ ГОРМОНОВ | 1999 |
|
RU2246947C2 |
| ПРЕПАРАТ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ ДЕФИЦИТА АНДРОГЕНОВ У ЖЕНЩИН, СОДЕРЖАЩИЙ ЭНТОМОЛОГИЧЕСКИЕ ПРОТЕИНЫ | 2015 |
|
RU2577225C1 |
| КОМПОЗИЦИИ ДЛЯ ПЕРСОНАЛИЗИРОВАННОЙ КОНТРАЦЕПЦИИ | 2018 |
|
RU2796919C2 |
Данное изобретение обеспечивает композиции, способы и применение для улучшения здоровья женщины, имеющей повышенные или существенно повышенные уровни связывающего половые гормоны глобулина (SHBG) и получающей пероральное добавление эстрогена, посредством неперорального введения эффективного количества андрогенного стероида. Далее, данное изобретение обеспечивает композиции, способы и применение для совместного введения (ко-введения) эффективного количества перорально вводимого эстрогена и эффективного количества неперорально вводимого андрогенного стероида для женщин, нуждающихся в пополнении эстрогена. Изобретение обеспечивает достижение функциональных уровней андрогенных стероидов у женщин с повышенными уровнями SHBG и, следовательно, улучшение их здоровья. 2 н. и 29 з.п. ф-лы, 4 табл., 2 ил.
| US 5855920 А, 05.01.1999 | |||
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| ЧУВСТВИТЕЛЬНАЯ К ДАВЛЕНИЮ СИСТЕМА ТРАНСДЕРМАЛЬНОЙ ДОСТАВКИ ЛЕКАРСТВА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1992 |
|
RU2124340C1 |
Авторы
Даты
2004-08-27—Публикация
2000-06-09—Подача