Изобретение относится к медицине и медицинской промышленности, в частности к области получения лекарственных средств бионормализующего действия на основе плацентарных тканей.
Под бионормализующим действием препарата понимается его способность при применении в медицине с лечебной и профилактической целью устранять или предотвращать причины патологического состояния организма человека и животных и тем самым обеспечить решение следующих проблем:
- достижение положительного терапевтического эффекта (полное выздоровление) или стойкой ремиссии, независимо от вида и причины патологии без нежелательных побочных эффектов;
- сокращение сроков лечения и обеспечение гарантированного улучшения состояния здоровья и продления активного образа жизни;
- предотвращение преждевременного развития заболеваний, связанных с работой во вредных условиях труда, стрессами, физическими, термическими и другими перегрузками за счет профилактического применения препарата;
- решение геронтологической проблемы.
Практически все известные к настоящему времени лекарственные средства относятся к разряду средств симптоматического действия, т.е. они в той или иной степени устраняют отдельные симптомы заболевания, такие как повышенная температура, артериальная гипертензия, насморк, кашель и др. Наиболее характерно это проявляется при лечении хронических и особенно хронически запущенных патологий, таких как заболевания опорно-двигательной системы (остеоартрозы, полиартриты, болезнь Бехтерева), а также различных заболеваний, являющихся следствием травматического воздействия на плод во время родов (детский церебральный паралич), перенесенных травм черепа, переломов конечностей и позвоночника.
Особое значение приобретает проблема лечения таких заболеваний, как инсульты, инфаркты, огнестрельные ранения. В тот же разряд следует отнести заболевания, связанные с иммунодефицитом (хронические воспалительные процессы различных органов и тканей, особенно урогенитальные), онкологические процессы и др.
Применение известных лекарственных средств при указанных выше и многих других патологических процессах обеспечивает в лучшем случае устранение отдельных симптомов заболевания, которое, как правило, носит временный характер. При этом известно, что все лекарственные средства, относящиеся к классу ксенобиотиков, проявляя терапевтический эффект, оказывают одновременно токсическое действие на другие системы или органы. Конечный баланс такого лечения имеет нулевое или отрицательное значение. Это связано с тем, что с помощью известных лекарственных средств в большинстве случаев невозможно устранить причину заболевания - патологического состояния, являющегося следствием нарушенного по тем или иным причинам метаболизма (обмена веществ и энергии между клеткой и окружающей средой).
Не меньшее значение приобретает вопрос профилактики таких заболеваний, т.к. с помощью известных лекарственных средств пока невозможна разработка радикальной системы продления жизни человека в активной форме.
Известны препараты белковой природы типа интерлейкинов, нейропептидов и другие, полученные методом генной инженерии или выделяемые из различных субстратов организма человека с применением афинной хроматографии и клональных антител, которые в той или иной степени можно отнести к лекарственным средствам бионормализующего действия (Состояние и перспективы разработки лекарственных средств с использованием методов биотехнологии в капиталистических странах: Обзорная информация в сб. "Экономика в медицинской и микробиологической промышленности. - М.: ВНИИСЭНТИ НПО "Медбиоэкономика", 1989, №1/2, 84 с.). Однако эти препараты имеют весьма существенные недостатки, а именно:
- трудоемкая и очень сложная технология получения и соответственно неоправданно высокие затраты;
- быстрая экзо- и особенно эндогенная инактивация препарата, вследствие чего наблюдается кратковременное фармакологическое действие и появление нежелательных побочных эффектов.
Наиболее близким к заявляемому является лекарственное средство бионормализующего действия, полученное на основе плацентарных тканей и описанное в патенте Российской Федерации №2036650 от 09.06.1995 г.
Однако лекарственное средство по указанным авторским свидетельствам, получившее название "Амниоцен", характеризуется нежелательными побочными эффектами, в результате чего, например, оно было исключено в 2000 г. из реестра лекарственных средств Российской Федерации.
В основу настоящего изобретения поставлена, в частности, задача создания лекарственного средства бионормализующего действия, содержащего продукты, полученные из плацентарных тканей, с высокой степенью окисления и стабильностью свойств.
Поставленная выше задача решается тем, что в состав лекарственного средства бионормализующего действия, содержащего продукты, полученные из плацентарных тканей, входят полипептиды в количестве 3,5-7,0 мас.%, аминокислоты в количестве 50-60 мас.%, аминосахариды в количестве 4-5 мас.% и гексуроновые кислоты в количестве 8-9 мас.%, причем указанные продукты находятся в окисленной водорастворимой форме, остальное - полисахариды и неорганические соли.
Указанные продукты представляют собой полученные путем окислительно-гидролитической модификации биополимеров плаценты водорастворимые предшественники макромолекул в более высокой степени окисления, чем естественные продукты биохимических реакций, протекающих в организме человека. Окислительно-гидролитическая модификация биополимеров плаценты означает не что иное, как перевод их в метаболическое состояние. Степень окисления продуктов модификации биополимеров плацентарных тканей по кислороду, определяемая расчетно-аналитическим путем, в 2 раза выше, чем у естественных эндорегуляторов, образующихся в организме человека за счет окисления белков соединительной ткани ферментами пролингидроксилазы или лизингидроксилазы и последующего гидролиза. А с учетом образования связей азот-хлор, степень окисления увеличивается более чем в 3 раза. Вследствие этого заявляемое лекарственное средство обладает высоким бионормализующим действием или, иными словами, является эффективным бионормализатором.
Следующим усовершенствованием лекарственного средства в соответствии с изобретением является то, что в качестве плацентарных тканей используются последы человека и сельскохозяйственных животных. Это позволяет существенно расширить сферу применения данного лекарственного средства и объем его выпуска.
Высокая фармакотерапевтическая эффективность заявляемого препарата как бионормализатора установлена при исследованиях на лабораторных животных (мыши, крысы, кролики, собаки), в процессе клинических испытаний на людях и в результате постклинического применения. Ниже приводятся результаты до клинического, клинического и постклинического применения заявляемого препарата.
Иммунотропное действие
Оценка иммунотропной активности заявляемого препарата определена по стандартным методикам, рекомендованным Всемирной организацией здравоохранения (ВОЗ). Специфическая фармакологическая (иммунологическая) активность проверена в модельных системах, количественно характеризующих действие испытуемого препарата на основные звенья иммунитета. Эксперименты были поставлены на морских свинках, крысах линии Вистар, беспородных мышах и мышах линий СВА, С57В1 (CBAXC57B1)Г1. Проверено влияние заявляемого препарата на клеточный и гуморальный иммунный ответ (фагоцитарная активность, влияние на исход генерализованной синегнойной инфекции, на систему комплемента, на кооперацию Т- и В-лимфоцитов, на реакцию “трансплантат против хозяина”, на реакцию гиперчувствительности замедленного типа, на гуморальный ответ). В качестве препаратов сравнения были использованы известные лекарственные средства, такие как левамизол, Т-активин, циклофосфамид, нуклеат натрия, амниоцен, пирогенал.
По результатам испытаний заявляемый объект значительно превосходит по активности вышеуказанные препараты и только по некоторым тестам проявляет такую же активность, как Т-активин. Наиболее характерным показателем, характеризующим иммунотропную (иммуномодулирушую) активность любого лекарственного средства, является оценка его влияния на реакцию гиперчувствительности замедленного типа (ГЗТ). В опытах по индукции ГЗТ у сублетально облученных мышей (ионизирующее излучение существенно нарушает иммунологическую компетентность организма, подавляя проявление ГЗТ) заявляемый препарат вводили подкожно 5-кратно в суммарной дозе 4,0 и 6,0 мг/кг, начиная со следующего дня после облучения. Как видно из представленной ниже табл.1, обработка животных в дозе 4 мг/кг повышает гиперчувствительность реакции на 30% по отношению к облученным мышам контрольной группы. При дозе 6,0 мг/кг индекс реакции практически достигает уровня группы необлученных животных, что доказывает возможность защиты организма при радиационном воздействии.
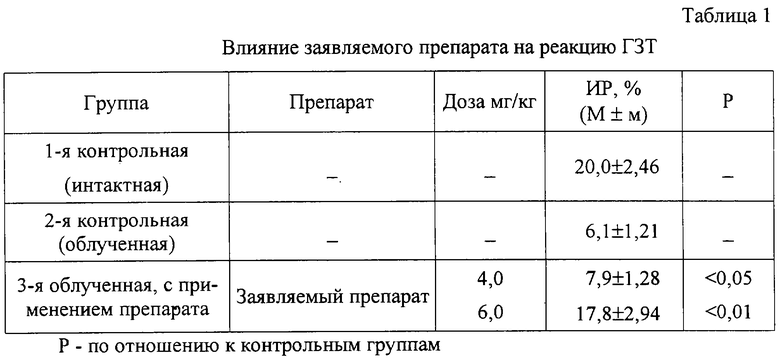
Хондропротекторное действие
В качестве препаратов сравнения для оценки активности заявляемого препарата по способности восстанавливать хрящевую ткань были выбраны известные препараты хондропротекторы, такие как румалон, мукартрин и артепарон. Оценка хондропротекторных свойств произведена на стандартной модели посттравматического артроза тазобедренного сустава у крыс, который развивается после нанесения дефекта в виде круглого отверстия диаметром около 2 мм, проходящего через суставной хрящ в субхондральную область. Нанесение такого дефекта приводит к развитию посттравматического артроза. Для испытания активности заявляемого препарата и препаратов сравнения были выбраны дозы: 0,01; 0,03; 0,06; 0,1; 0,3; 0,5; 1,0 мл/кг массы животных. Оценка эффективности хондропротекторного действия производилась по специально разработанной шкале (в баллах). Максимальная оценка 12 баллов, которая соответствует полному рассасыванию соединительной ткани и восстановлению хрящевой ткани. Результаты оценки в баллах:
Румалон 7,6
Мукартрин 8,4
Артепарон 8,9
Заявляемый препарат 11,8
Противовоспалительное действие
Данный вид действия проверен на модели экспериментальной гранулемы на крысах. В качестве препаратов сравнения были использованы лекарственные средства, получаемые на основе плаценты человека - ПДС (плацента денатурированная суспендированная) и амниоцен. Препараты вводились подкожно одновременно с операцией. Результаты испытаний представлены в табл.2.
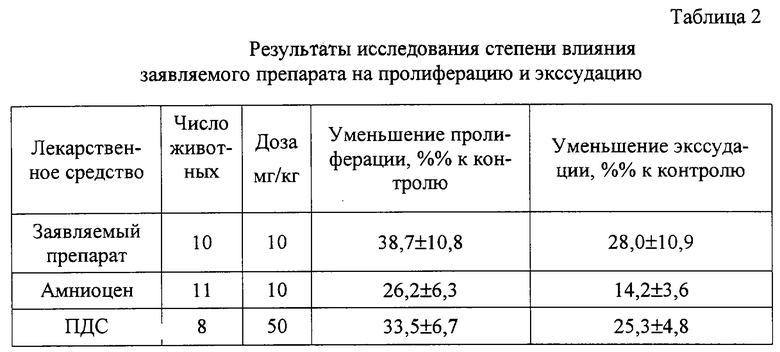
Рассасывающее действие
Рассасывающее действие изучено на модели спаечного процесса, возникающего у небеременных самок крыс в результате дозированной травмы маточного рога. Результаты опытов представлены в табл.3.
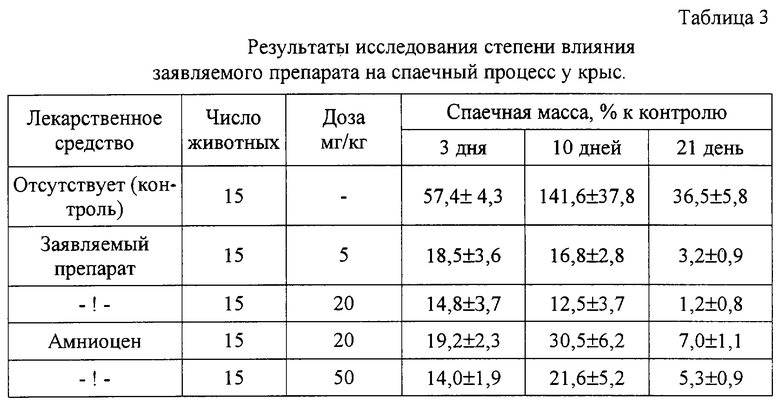
Репаративное действие
Данный вид фармакологического действия установлен на стандартной модели с полнослойным дефектом кожи на мышах, которым вводили заявляемый препарат в дозах 5-10 мг/кг. Под влиянием препарата срок заживления по сравнению с контролем сокращается с 17 дней до 10. Аналогичный эффект оказывает препарат из плаценты амниоцен только в дозе 75 мг/кг. При этом существенным преимуществом применения заявляемого препарата является отсутствие рубцов в процессе заживления.
Антиоксидантное действие
Антиоксидантное действие заявляемого препарата установлено при перекисном окислении липидов, эффективность которого превосходит практически в 10 раз аскорбиновую кислоту. Данный факт имеет существенное значение при практическом использовании заявляемого препарата в онкологии.
Фертильное действие
В процессе исследования заявляемого препарата на мутагенные свойства (на модели доминантных летальных мутаций) обнаружено увеличение фертильности и плодовитости опытных животных по сравнению с контролем. На стадии зрелых сперматозоидов наблюдается значительное снижение постимплатационной гибели, что хорошо согласуется с литературными данными об антимутагенном действии препаратов из плаценты.
Адаптогенное действие
Данный вид действия в процессе создания новых лекарственных средств приобретает одно из самых актуальных направлений поиска, т.к. это может дать возможность влиять на физиологические процессы при физических, термических, химических перегрузках, особенно для предотвращения отравлений, ожогов, повышения выносливости организма и т.д. В процессе исследования заявляемого препарата установлено, что предварительная обработка животных (мыши) в течение 7 суток в условно-терапевтической дозе (0,1 мл/кг) предотвращает гибель животных от токсической дозы ядовитых веществ (стрихнин), летального облучения, инфицирования синегнойной палочкой.
Антистрессовое действие
Антистрессовое действие заявляемого препарата исследовано на основе многомерных методов оценки состояния различных компонентов устойчивости к эмоциональному стрессу у крыс (поведенческий и висцеральный компоненты). В результате данных исследований установлено, что заявляемый препарат обладает способностью повышать устойчивость к эмоциональному стрессу, т.е. предупреждать развитие функциональных расстройств высшей нервной деятельности, общего иммунитета и метаболических нарушений сердечной деятельности. Наиболее эффективной оказалась доза 30 мкл на 100 г массы крысы, что соответствует дозе 2 мл на 1 инъекцию у человека.
Лактогенное действие
В процессе практического применения заявляемого препарата в ветеринарии установлено, что при агалактии у свиноматок заявляемый объект приводит к восстановлению процесса лактации.
Антикоагулянтное действие
В процессе исследования степени влияния заявляемого препарата на свертываемость крови установлено, что в дозе 1,5 мг/кг при месячном введении проявляется антикоагулянтное действие, которое исчезает через 30 дней после окончания введения препарата. Данный факт может иметь существенное практическое значение при лечении предынфарктных и постинфарктных состояний.
Заявляемый препарат в полном объеме исследован на острую и хроническую токсичность в соответствии с методами, рекомендованными ВОЗ.
Острая токсичность
Проверка заявляемого препарата на острую токсичность проведена на мышах путем постепенного (двойного) увеличения дозы препарата, начиная с 10 мг/кг массы животных до 100 г/кг. В максимально допустимой дозе (100 г на 1 кг массы) животные не гибнут, что доказывает абсолютную безвредность препарата. В высоких дозах, превышающих условно-терапевтическую в 5000 раз, естественно, животные проявляют гиподинамию, апатию, вялость, но восстанавливают свою активность через 3-4 дня без признаков отравления.
Хроническая токсичность
Исследование хронической токсичности заявляемого препарата проведено в соответствии с рекомендациями ВОЗ на трех группах животных (крысы, кролики и собаки) в течение 6-месячного ежедневного введения препарата в дозах, превышающих условно-терапевтическую в 10, 20, 50 и 100 раз. После 6-месячного введения препарата 50% животных забивали для оценки степени влияния заявляемого препарата на органы и ткани, а остальных животных реабилитировали в течение 1 месяца и затем снова забивали для сравнительной оценки патологического влияния препарата.
В результате исследования внутренних органов животных после 6-месячного введения препаратов в указанных выше дозах ни одно из животных не погибло. Обнаруженные изменения в легких, мозге и почках после месячной реабилитации восстанавливались полностью, что подтверждает безвредность заявляемого препарата (высокую биодоступность и биосовместимость).
Результаты клинических испытаний
Клинические испытания заявляемого препарата проведены в три стадии. Первая фаза - добровольцы (30 человек), которым внутримышечно вводился 2% раствор заявляемого лекарственного средства в воде, в течение 10 дней. Токсического воздействия и других побочных эффектов не установлено. Вторая фаза (90 человек) - определение терапевтической дозы при применении препарата в качестве противовоспалительного и обезболивающего средства при остеоартрозах (как одно из наиболее перспективных направлений биологического действия препарата).
Третья фаза - исследование, проведенное в трех клиниках г. Москвы с общим количеством больных 156 человек (мужчины и женщины в возрасте от 18 до 78 лет) с диагнозом остеоартрозы различной этиологии и тяжести. Основным клиническим проявлением остеоартроза является болевой синдром, оценка которого производилась по специально разработанной шкале в баллах по 5-балльной системе как до лечения, так и после лечения. Заявляемый препарат вводился парентерально и внутрисуставно, доза 2 мл, вначале через день (10 инъекций), затем ежедневно (20 инъекций). Каждый больной получал по 60 мл препарата. Субъективная оценка эффективности применения показала, что у 58 человек боли значительно уменьшились (37%), у 42 человек (27%) - полностью исчезли, у 33 человек (21%) исчезли боли полностью в коленных суставах и значительно снизились в тазобедренных суставах. У всех больных увеличился объем движений, в том числе при ходьбе по лестнице. У 12 больных, поступивших в стационар на костылях, появилась возможность передвигаться самостоятельно. Побочных эффектов в процессе испытании не установлено.
Постклинические испытания заявляемого препарата показали высокий эффект при многих патологических состояниях, что доказывает его бионормализующее действие. Ниже приведены примеры таких испытаний.
Пример 1
Больной Л,. 33 года. Диагноз - последствия детского церебрального паралича (спастика правой кисти и всей руки, двигательная гиподинамия). После лечения заявляемым препаратом в течение одного года в сочетании с физиотерапевтическими методами также с применением заявляемого препарата достигнуто практически полное выздоровление. Больной стал писать, чистить картофель и выполнять другие мелкие движения с высокой точностью. Начал бегать, плавать. Применение известных лекарственных средств в течение предыдущих 30 лет не дало положительных результатов.
Пример 2. Применение заявляемого препарата в детской и подростковой психоневрологической практике
Терапевтическая коррекция психических и неврологических синдромов, сформировавшихся вследствие раннего органического поражения центральной нервной системы, закрытых черепно-мозговых травм и нейроинфекции у детей и подростков оставалась до применения заявляемого препарата трудно разрешимой проблемой. При использовании для этих целей заявляемого препарата в течение 25-30 дней в сочетании с физиотерапевтическими методами в Украинском НИИ охраны здоровья детей и подростков достигнут высокий стойкий терапевтический эффект (95,3%). У остальных больных отмечено существенное улучшение состояния здоровья.
Пример 3. Применение заявляемого препарата при токсоплазмозе
Токсоплазмоз - зоотропная паразитарная болезнь, характеризующаяся полиморфной клинической картиной, латентным, острым и хроническим течением при приобретенной или врожденной инфекции. Токсоплазмоз, как правило, не поддается эффективному лечению, и болезнь приобретает затяжной хронический характер. Применением заявляемого препарата при лечении токсоплазмоза по данным фирмы "Бактерии" при Днепропетровской медицинской академии доказана высокая фармакотерапевтическая эффективность, характеризующаяся в большинстве случаев полным выздоровлением.
Пример 4. Применение заявляемого препарата при хронических нарушениях мозгового кровообращения
По результатам лечения больных с диагнозом инсульт, независимо от давности, полученных в поликлинике №3, г. Харьков, установлено полное рассасывание гематомы мозга, образовавшихся спаек и других патологических дефектов. В конечном итоге восстановление утраченной двигательной функции и речи. Продолжительность лечения зависела от степени тяжести и давности патологического состояния.
Пример 5. Эффективность лечения урогенитальной инфекции
Применение заявляемого препарата в урологической практике при лечении таких заболеваний, как хламидиоз, уроплазмоз и других, особенно при их комбинации дает высокий терапевтический эффект. По результатам, полученным в урологической клинике при Харьковском медицинском университете, достигнут положительный эффект в 94,7% случаев.
Пример 6. Применение заявляемого препарата в кардиологии
На базе поликлиники №6 г. Харькова проведено лечение более 200 больных с сердечно-сосудистой недостаточностью (постинфарктное состояние, стенокардия, миокардит и др.). У абсолютного большинства больных получен стойкий терапевтический эффект, особенно при стенокардии и постинфарктном состоянии.
Пример 7. Применение заявляемого препарата при лечении травм и заболеваний опорно-двигательной системы
По результатам лечения больных с заболеваниями опорно-двигательного аппарата различной этиологии, проведенных на базе поликлиники №6 г. Харькова, достигнут положительный эффект практически в 100% случаев.
Пример 8. Применение заявляемого препарата в гинекологической практике
Высокая эффективность лечения таких гинекологических заболеваний, как эндометриты, диффузионные фибромиомы, аднекситы, поликистоз, воспаление придатков и др. показано на результатах его применения в гинекологических учреждениях г. Харькова.
Высокая эффективность заявляемого препарата установлена также в онкологии, офтальмологии, хирургии и других отраслях медицины. Препарат разрешен к медицинскому применению.
Известны способы получения препаратов на основе продуктов плаценты в окисленном состоянии. По способу, описанному в а.с. СССР №948001, плаценту обрабатывают хлором. По способу, описанному в А.С. СССР №1392684, обработка производится диоксидом хлора.
Наиболее близким к заявляемому способу получения лекарственного средства бионормализующего действия является способ по патенту Российской Федерации №2036650, опубл. 09.06.95 г., бюлл. №16, в соответствии с которым окисление измельченной плаценты производится хлоритом натрия в солянокислой среде.
Однако все указанные способы обработки плаценты не обеспечивают бионормализующего действия получаемого препарата из-за сравнительно невысокой степени окисления входящих в его состав продуктов и постоянно меняющегося состава готового продукта, т.к. процесс окисления оказывается неуправляемым.
В основу настоящего изобретения относительно способа получения описанного лекарственного средства бионормализующего действия поставлена задача усовершенствования известного способа с тем, чтобы путем введения новых реагентов и новых условий его осуществления добиться более высокой степени окисления готового продукта при стабильности его состава и тем самым получить лекарственное средство бионормализующего действия.
Поставленная задача решается тем, что известный способ, включающий окислительно-гидролитическую модификацию плацентарных тканей кислородными соединениями хлора, усовершенствуют следующим образом: процесс окислительно-гидролитической модификации проводят хлористой кислотой в присутствии модифицирующих добавок.
Указанные модифицирующие добавки обеспечивают необходимую селективность процесса окислительно-гидролитической модификации. Это дает возможность получать лекарственное средство с требуемой степенью окисления ингредиентов за счет образования связей углерод - кислород, азот - кислород, сера - кислород, а также азот - хлор путем замещения атома водорода в амидогруппе (пептидная связь) или в свободной аминогруппе.
В конкретном варианте реализации способа процесс модификации проводят при соотношении ткань/хлористая кислота 1:(0,1-1,5) при температуре 18-45°С.
В еще одном конкретном варианте реализации способа в соответствии с изобретением в качестве модифицирующих добавок используют органические соединения никеля или кобальта.
Продолжительность процесса обработки до требуемой степени окисления (по содержанию кислорода и хлора) зависит от температуры и колеблется от 2 до 40-45 суток.
Ниже приводятся примеры конкретного выполнения заявляемого способа.
Пример 9
Плаценту, заготавливаемую в родильных домах в замороженном виде, измельчают, отмывают от крови, полученную суспензию загружают в стеклянный реактор, снабженный мешалкой и змеевиком для нагрева или охлаждения, добавляют предварительно приготовленную смесь в эквивалентных количествах натриевой соли аминокислоты (предпочтительно лизин) и модификатора - хлорида кобальта или никеля – в соотношении по массе ткань/модификатор 1:(0,001-0,1), затем загружают 5% раствор хлористой кислоты при массовом соотношении ткань/кислота 1:(0,1-1,5) и выдерживают в течение 1-45 суток до требуемой степени окисления. Степень окисления определяют по процентному массовому содержанию кислорода и хлора в продуктах реакции и сравнивают с этими же показателями в исходном продукте. Содержание по массе кислорода в готовом продукте по сравнению с исходным сырьем должно быть больше в 1,8-2,1 раза. Содержание общего хлора - свободного и органически связанного - должно находиться в пределах 8,0-20 мас.% в пересчете на сухое вещество.
Полипептидную фракцию в виде водного раствора отделяют от осадка, подвергают очистке путем фильтрации, нейтрализуют щелочным агентом и переводят в инъекционную лекарственную форму известными методами.
Пример 10
В условиях примера 9 вместо хлористой кислоты используют хлорит натрия в присутствии эквивалентного количества соляной кислоты. Основным действующим веществом (окислителем) в данном случае является хлористая кислота, которая выделяется при обработке хлорида натрия соляной кислотой. Соотношение окислитель/ткань плаценты по массе в пересчете на хлорид натрия 1:(0,15-1,8). Целевой продукт выделяют аналогично примеру 9. В данном случае в качестве модифицирующей добавки применяют просто кобальтхлорид в тех же соотношениях.
Пример 11
В условиях примера 9 обработку измельченных тканей плаценты производят диоксидом хлора при соотношении ткань/диоксид хлора 1:(0,1-0,9) по массе. Действующим веществом в данном случае также является хлористая кислота, которая образуется при взаимодействии СlО2 с водой. В качестве модифицирующей добавки в данном случае предпочтительнее смесь натриевой соли лизина и хлорида кобальта. Выделение целевого продукта осуществляют аналогичным образом.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯТОР ПРОЦЕССОВ ОБМЕНА ВЕЩЕСТВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2377250C2 |
| РЕГУЛЯТОР РОСТА И РАЗВИТИЯ РАСТЕНИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2352116C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОГЕННОГО СТИМУЛЯТОРА | 1991 |
|
RU2036650C1 |
| БИОГЕННЫЙ СТИМУЛЯТОР ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 1991 |
|
RU2036651C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1996 |
|
RU2133615C1 |
| БЕЛКОВО-ПОЛИПЕПТИДНЫЙ КОМПЛЕКС, ОБЛАДАЮЩИЙ ТКАНЕСПЕЦИФИЧЕСКИМ РЕГЕНЕРАТИВНО-РЕПАРАТИВНЫМ И ОМОЛАЖИВАЮЩИМ ДЕЙСТВИЕМ НА КОЖНУЮ ТКАНЬ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2485133C2 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЭНДОМЕТРИТА У КОРОВ И СВИНОМАТОК | 2003 |
|
RU2253466C1 |
| БИОКОНЦЕНТРАТ ИЗ ПЛАЦЕНТЫ | 2003 |
|
RU2246308C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ТКАНЕВОГО ПРЕПАРАТА | 1999 |
|
RU2148408C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСТИМУЛЯТОРА "ПОМ" ИЗ ПЛАЦЕНТЫ КОРОВ | 1989 |
|
SU1730762A1 |
Изобретение относится к медицине и медицинской промышленности, в частности к области получения лекарственных средств бионормализующего действия на основе плацентарных тканей человека или сельскохозяйственных животных. Способ заключается в том, что плацентарную ткань измельчают, отмывают от крови, к суспензии добавляют раствор хлористой кислоты при соотношении по массе ткань/хлористая кислота 1:(0,1-1,5) и модифицирующие добавки, обеспечивающие селективность процесса, причем окислительно-гидролитическую модификацию плацентарных тканей проводят при температуре 18-45°С. Лекарственное средство содержит в своем составе полипептиды в количестве 3,5-7,0 мас.%, аминокислоты в количестве 50-60 мас.%, аминосахариды в количестве 4-5 мас.% и гексуроновые кислоты в количестве 8-9 мас.%, причем указанные продукты находятся в окисленной водорастворимой форме, остальное - полисахариды и неорганические кислоты. Технический результат: повышение бионормализующего действия за счет создания лекарственного средства с высокой степенью окисления и стабильностью свойств. 2 н. и 2 з.п.ф-лы, 3 табл.
| СПОСОБ ПОЛУЧЕНИЯ БИОГЕННОГО СТИМУЛЯТОРА | 1991 |
|
RU2036650C1 |
| АЛЛОГЕННЫЙ ПРЕПАРАТ ПЛАЦЕНТЫ ЧЕЛОВЕКА, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫМ, РЕПАРАТИВНЫМ, АНТИМИКРОБНЫМ, РАНОЗАЖИВЛЯЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2137486C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ПЛАЦЕНТЫ | 1992 |
|
RU2033797C1 |
| US 4054648 А, 18.10.1977 | |||
| СПОСОБ МОДЕЛИРОВАНИЯ ЭЛЕКТРОЭНЕРГЕТИЧЕСКИХСИСТЕМ | 0 |
|
SU285370A1 |
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
Авторы
Даты
2004-09-10—Публикация
2002-09-27—Подача