Настоящее изобретение относится к способу получения соединений 4,4 -дигалоген-о-гидроксидифенила формулы
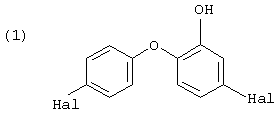
где Hal обозначает атом галогена,
и к использованию этих соединений для защиты органических веществ и объектов от микроорганизмов.
Получение соединений 4,4’-дигалоген-о-гидроксидифенила обычно осуществляют диазотированием и последующим гидролизом 2-амино-4,4-дихлордифенилового эфира (соединение формулы (1))
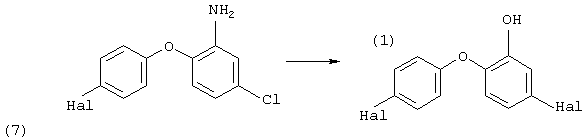 (см. патент US 3506720). Аналогичные способы описаны в источниках: Synthesis, 1986, № 10, p. 868-870.
(см. патент US 3506720). Аналогичные способы описаны в источниках: Synthesis, 1986, № 10, p. 868-870.
Однако выход, получаемый данным методом получения, является неудовлетворительным, так как различные химические реакции могут проходить одновременно.
Поэтому целью настоящего изобретения является создание экономичного способа получения соединений 4,4-дигалоген-о-гидроксидифенила, при котором подавляются нежелательные сопутствующие реакции.
Эта цель достигается в соответствии с настоящим изобретением за счет проведения трехстадийной реакции, причем на 1-й стадии а) алкоксифенол формулы (6) галогенируют (a1), при этом полученное галоидзамещенное соединение фенола формулы (5) подвергают взаимодействию с п-дигалогенфенолом формулы (4b) в присутствии меди и/или медных солей с получением соединения дифенилового эфира формулы (2) (a2), после чего искомое соединение дифенилового эфира формулы (1) получают расщеплением эфира (а3), или b) алкоксифенол формулы (6) подвергают взаимодействию с галогенфенолом формулы (4b) с получением соединения формулы (3) (b1), после чего это соединение галогенируют (b2) и полученное соединение дифенилового эфира формулы (2) подвергают расщеплению эфира с получением искомого соединения дифенилового эфира формулы (1) (b3) в соответствии со следующей схемой реакции:
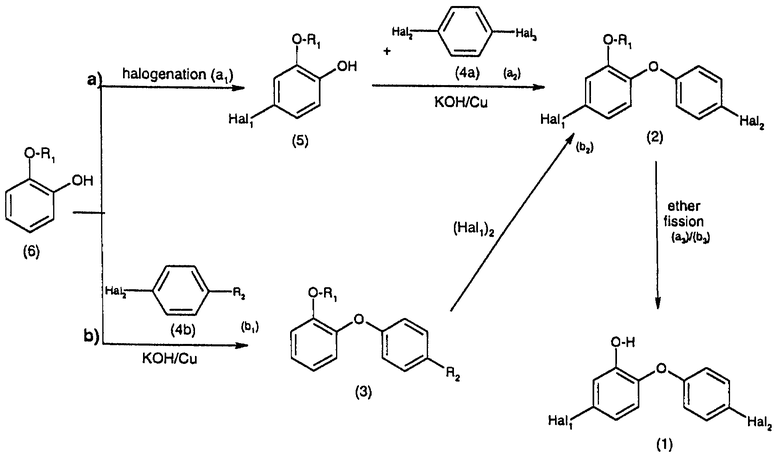
На вышеприведенной схеме:
R1 обозначает С1-С3-алкил;
R2 обозначает водород, хлор или бром;
Hal1, Hal2 – хлор;
Hаl3 - бром.
С1-С5-Алкил является разветвленным или неразветвленным алкилом, таким как метил, этил, пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, 2-этилбутил или н-пентил.
На вышеприведенной схеме реакции:
R1 обозначает предпочтительно С1-С4-алкил, более предпочтительно метил;
Hal1, Hal2 обозначает хлор;
Наl3 обозначает бром.
Галоидирование алкоксифенола формулы (6) в соединение фенола формулы (5) предпочтительно осуществляют с использованием газообразного хлора или сульфурилхлорида в присутствии органического растворителя, например ароматического, алифатического или циклоалифатического углеводорода, предпочтительно с изомерной смесью толуола или ксилола, при температуре реакции в диапазоне от -10 до 70°С, предпочтительно от 25 до 35°С. Полученный таким образом неочищенный продукт формулы (5) отделяют от реакционной смеси нейтрализацией с помощью карбоната натрия или карбоната калия или с помощью воздуха, пропускаемого через реакционную смесь, после чего неочищенный продукт формулы (5) собирают перегонкой при пониженном давлении.
Взаимодействие галоидзамещенного соединения фенола формулы (5) с соединением дигалогена формулы (4а) (реакция (а2)) и взаимодействие соединения фенола формулы (6) с соединением дигалогена формулы (4b) (реакция (b1)) обычно осуществляют при температуре реакции в диапазоне от 120 до 200°С, предпочтительно от 130 до 170°С. Такая температура необходима для того, чтобы фенольное соединение формулы (5) и соединение дигалогена формулы (4а) или (4b) присутствовали в стехиометрическом отношении, тогда как гидроокись щелочи должна присутствовать в количестве меньшем, чем эквимолярное количество (от 20 до 80% от теоретического).
Используемые медные катализаторы предпочтительно являются солями меди, традиционно используемыми для синтеза Ульмана, например окись меди (II), окись меди (I), карбонат меди, карбонат основной меди, хлорид меди (I), хлорид меди (II), бромид меди (I), бромид меди (II) или сульфат меди.
Дополнительные подробности относительно стадии 1b реакции можно найти в DE-OS-2,242,519.
Расщепление эфира (реакция а3/b3)) обычно осуществляют путем обработки А1С13 в инертном органическом растворителе, например петролейном эфире или бензоле, либо нагревания с бромистоводородной кислотой или смесями бромистоводородной кислоты и уксусной кислоты. Время реакции для этой стадии может варьироваться от 0,5 до 10 часов, тогда как температура составляет от 40 до 110°С.
Предпочтителен путь реакции а) (=а1/а2/а3) в соответствии со следующей схемой:
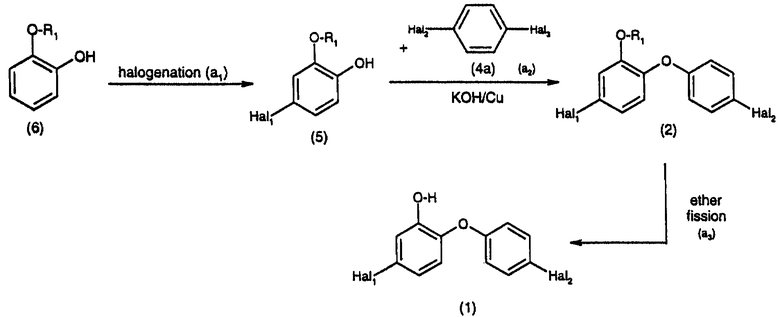
Соединения 4,4’-дигалоген-о-гидроксидифенила, полученные в соответствии с настоящим изобретением, нерастворимы в воде, но растворимы в разбавленном растворе гидроокиси натрия и растворе гидроокиси калия и во всех органических растворителях. Благодаря этим предварительным условиям растворимости они имеют весьма универсальное применение для борьбы с микроорганизмами, в частности бактериями, и для защиты органических веществ и объектов от микроорганизмов. Эти соединения могут наноситься, например, на человеческую кожу и руки, а также на твердые предметы в разбавленном или неразбавленном виде вместе, например, со смачивающими веществами или диспергаторами, например, в форме мыла или синтетического детергента, для дезинфекции и очистки.
Следящие примеры, не ограничивающие объем изобретения, иллюстрирует его более подробно.
Пример 1. Первая стадия реакции
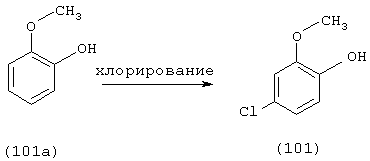
124 г о-метоксифенола и 200 мл сухого толуола помещают в четырехгорлую колбу, снабженную смесителем, конденсатором и капельной воронкой.
148 г сульфурил хлорида добавляют по каплям, перемешивая, в течение примерно 1 часа, при этом температуру реакционной смеси поддерживают на уровне 20-25°С. По завершении добавления перемешивание продолжают при комнатной температуре в течение 2 часов, после чего реакционную смесь переносят в делительную воронку, встряхивают с 50 мл порциями 5% раствора карбоната натрия, промывают 50 мл воды и сушат в присутствии сульфата натрия. Затем сульфат натрия удаляют фильтрацией и хлорированный реакционный продукт подвергают перегонке при пониженном давлении. Это приводит к получению 144 г 2-метокси-4-хлорфенола, имеющего температуру плавления от 128 до 134°С при давлении 1999,8 Па.
Выход: 90,8% от теоретического.
Пример 2. 2-я стадия реакции
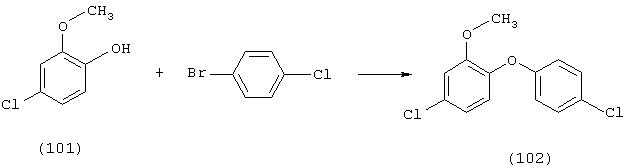
198,3 г 4-хлор-2-метоксифенола (соединение формулы (101)) помещают в сосуд вместе с 209 г изомерной смеси ксилола и полученную смесь нагревают до температуры 80°С и загружают 27,5 г КОН (80 мас.%). Эту смесь затем нагревают до температуры 145°С и 9,5 мл воды отделяют в водяном сепараторе в течение свыше 2 часов.
После охлаждения до температуры 100°С последовательно добавляют 1 г карбоната основной меди и 239,4 г 4-бромхлорбензола. После перемешивания в течение 2,5 часа при температуре 144-150°С смесь охлаждают до комнатной температуры и образовавшийся бромид калия удаляют фильтрацией.
Затем растворитель и выделенные вещества удаляют под вакуумом. Перегонка в вакууме масляного насоса приводит к получению 67,6 г желтоватого масла, которое быстро твердеет. Перекристаллизация из петролейного эфира приводит к получению неочищенного продукта формулы (102) в виде бесцветных кристаллов, имеющих температуру плавления 72-73°С.
Пример 3
Повторяют пример 2, однако используют 294 г 1,4-дихлорбензола вместо 239,4 г 4-бромхлорбензола. По истечении 5 часов реакции при температуре 148°С и еще 19 часов при температуре 141°С и обработки соединение формулы (102) получают с выходом 44 г.
Пример 4. Расщепление эфира (3-я стадия реакции)
Схема реакции:

5,3 г дифенилового эфира формулы (102) помещают в суспензию в 50 мл петролейного эфира при температуре 80-110°С, после чего в эту суспензию загружают при комнатной температуре 6 г безводного хлорида алюминия и нагревают до 80°С. Эту температуру поддерживают, тщательно перемешивая суспензию, в течение 1,5 часа до завершения расщепления эфира. В реакционную смесь добавляют 100 мл 2 н. раствора хлористоводородной кислоты, перемешивают 15 минут при температуре около 70°С и подвергают фазовому разделению. Фазу растворителя осветляют теплой фильтрацией, и продукт вначале кристаллизуют при температуре 25°С, а затем в течение 1 часа при температуре 5°С, после чего сушат с получением 2,3 г беспримесного белого кристаллического продукта формулы (103), имеющего температуру плавления 73-74°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 4,4'-ДИХЛОР-О-ГИДРОКСИДИФЕНИЛОВОГО ЭФИРА | 1999 |
|
RU2220946C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДЗАМЕЩЕННЫХ СОЕДИНЕНИЙ ГИДРОКСИДИФЕНИЛА | 1998 |
|
RU2193549C2 |
| ГАЛОГЕНИДЫ ГАЛОГЕНСУЛЬФОНИЛБЕНЗОЙНОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ФЕНИЛСУЛЬФОНИЛМОЧЕВИН | 2003 |
|
RU2330027C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКОКСИФЕНОЛА И АЛКОКСИГИДРОКСИБЕНЗАЛЬДЕГИДА | 2013 |
|
RU2628525C2 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ПОДАВЛЕНИЯ РОСТА СОРНЯКОВ | 2000 |
|
RU2259359C2 |
| Способ получения динитропроизводных дифениловых и трифениловых эфиров | 2017 |
|
RU2671581C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКОКСИГИДРОКСИБЕНЗАЛЬДЕГИДА, В СУЩЕСТВЕННОЙ СТЕПЕНИ СВОБОДНОГО ОТ АЛКИЛАЛКОКСИГИДРОКСИБЕНЗАЛЬДЕГИДА | 2013 |
|
RU2648044C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ - ПРОИЗВОДНОГО СЛОЖНОГО ГИДРОКСИЭФИРА И ЭПОКСИДНЫЕ СМОЛЫ, ПОЛУЧЕННЫЕ ИЗ НЕГО | 2001 |
|
RU2276158C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕН-О-ГИДРОКСИДИФЕНИЛОВЫХ СОЕДИНЕНИЙ И АЦИЛЬНЫЕ СОЕДИНЕНИЯ | 1998 |
|
RU2191770C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАМЕТИЛЬНЫХ ПРОИЗВОДНЫХ ДИФЕНИЛОВОГО ЭФИРА | 2016 |
|
RU2643519C1 |
Настоящее изобретение относится к способу получения 4,4'-дихлор-о-гидроксидифенилового эфира формулы (1), где Hal1 и Hal2 – хлор.
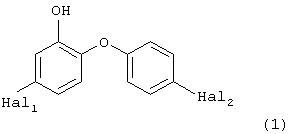
Способ включает галогенирование алкоксифенола формулы (6), где R1 обозначает С1-С5-алкил (стадия a1).
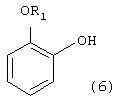
При этом стадию (a1) осуществляют с использованием элементарного хлора или сульфурилхлорида в присутствии органического растворителя, выбранного из ароматического, алифатического или циклоалифатического углеводорода; взаимодействие полученного галоидзамещенного фенола формулы (5)
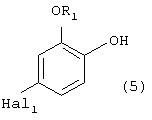
где R1 и Hal1 как указано выше, с п-дигалогенбензолом формулы (4а)
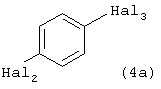
где Hal2 - хлор, Hal3 - бром, в присутствии меди и/или медных солей в качестве катализатора и гидроксида щелочного металла, взятого в количестве от 20 до 80 мас.% от теоретического количества исходных компонентов, с получением соответствующего дифенилового эфира формулы (2)
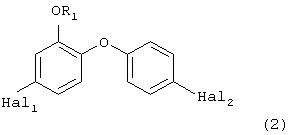
где R1, Hal1 и Hal2 - как указано выше (стадия а2), с последующим расщеплением полученного дифенилового эфира формулы (2) (стадия а3). Способ позволяет получать 4,4'-дихлор-о-гидроксидифениловый эфир без побочных реакций, что является экономически выгодным. 1 з.п. ф-лы.
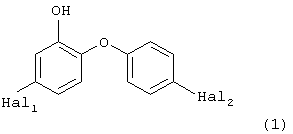
где Hal1 и Hal2 - хлор, включающий галогенирование алкоксифенола формулы (6)
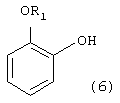
где R1 обозначает С1-С5-алкил (стадия a1),
при этом стадию (a1) осуществляют с использованием элементарного хлора или сульфурилхлорида в присутствии органического растворителя, выбранного из ароматического, алифатического или циклоалифатического углеводорода; взаимодействие полученного галоидзамещенного фенола формулы (5)
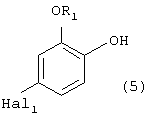
где R1 и Hal1 как указано выше, с парадигалогенбензолом формулы (4а)
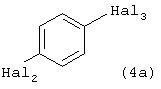
где Hal2 - хлор, Наl3 - бром,
в присутствии меди и/или медных солей в качестве катализатора и гидроксида щелочного металла, взятого в количестве 20-80 мас.% от теоретического количества исходных компонентов с получением соответствующего дифенилового эфира формулы (2)
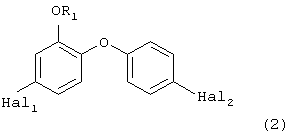
где R1, Hal1 и Hal2 как указано выше (стадия а2),
с последующим расщеплением полученного дифенилового эфира формулы (2) (стадия а3).
| YEAGER G.W | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Synthesis, 1995, №1, p.28-30 | |||
| OLAH G.A | |||
| et al | |||
| Способ получения морфия из опия | 1922 |
|
SU127A1 |
| Regioselective para Halogenation of Phenols, Phenol Ethers and Anilines with Halodimethylsulfonium Halides | |||
| US 3651151 A, 21.03.1972 | |||
| СПОСОБ ПРЕДОТВРАЩЕНИЯ КОМКОВАНИЯ САХАРНОГО ПЕСКА | 2003 |
|
RU2242519C1 |
| NILSSON C.A | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Chemosphere | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| HUMPPI T | |||
| Preparation of Polychlorinated Phenoxyphenols as Model Compounds of Impurities in Technical Chlorophenol Formulations | |||
| Synthesis, 1985, №10, p.919-924.EP 0857711 A1, 12.08.1998.DE 3723994 A1, 04.02.1988.CH 428759 A, 31.07.1967.SU 455936 A, 05.01.1975. | |||
Авторы
Даты
2004-09-27—Публикация
1999-09-27—Подача