Предлагаемое изобретение относится к нитропроизводным фенилововых эфиров, а именно к способам получения динитродифениловых и динитротрифениловых эфиров, которые применяются в качестве исходных соединений при получении полиимидных матриц, используемых при получении высокотермостойких композиционных материалов, клеев и покрытий, применяемых в авиационной и аэрокосмической отраслях, в судо- и автомобилестроении, при производстве строительных материалов.
Производные фенилового эфира имеют следующую общую структурную формулу:
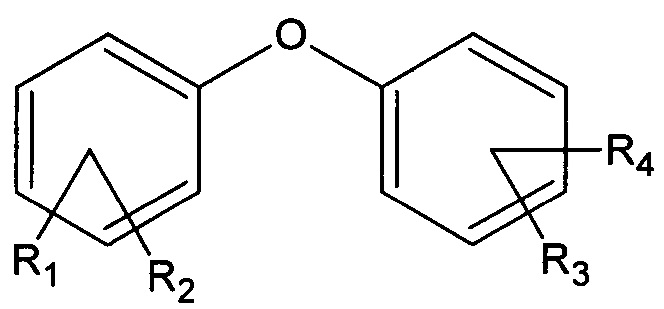
где R1, R2, R3, R4 - различные функциональные заместители.
Среди известных методов получения данных соединений особое внимание при анализе достигнутого уровня техники уделяется изучению метода синтеза, в основе которого лежит реакция Ульмана.
Известно, что под реакцией Ульмана подразумевается метод получения двух- и многоядерных ароматических соединений, проводимый в присутствии меди или ее соединений и осуществляемый разными вариантами, а именно:
- гомосочетанием арилгалогенидов или гетероарилгалогенидов согласно следующей реакции:

- арилированием фенолов, аминов, амидов, тиофенолов, сульфиновых кислот согласно следующей реакции:

Получение производных дифениловых эфиров, основанное на гетерофазной реакции Ульмана, проводится при определенных условиях. Реакция Ульмана обычно проводится в присутствии катализаторов. Чаще всего в качестве катализатора в реакции конденсации Ульмана применяются: металлическая медь и ее соли, а именно, дихлорид меди (II) (CuCl2), хлорид меди (I) (CuCl), сульфат меди (II) (CuSO4), диацетат меди (II) (Cu(СН3СОО)2), карбонат меди (II) (CuCO3), медные соли алкилнафталинсульфокислот, алкилдифенилдисульфокислот и фенолов, а также комплексные соединения двухвалентной меди состава (C5H5N)2CuCl2 [Грагеров И.П., Касухин Л.Ф. ИССЛЕДОВАНИЕ МЕХАНИЗМА РЕАКЦИЙ УЛЬМАНА // Журнал органической химии. - 1969. - Т. 5. - №.1-6. - С. 3].
Реакцию Ульмана обычно осуществляют при нагревании в инертном растворителе. Выявлено, что наличие электроноакцепторных заместителей, находящихся в орто-положении в арилгалогениде, заметно активируют прохождение реакции. [Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 425-28; Fan ta P.Е., "Synthesis", 1974, №1, р. 9-21. Перевод В.В. Жданкина].
Известно, что исходные фенольные компоненты часто вводят в виде солей, при этом более активными, по-видимому, являются калиевые соли. Их употребляют чаще фенолятов натрия [Lewis Е.A. et al. Atomic-scale insight into the formation, mobility and reaction of Ullmann coupling intermediates // Chemical Communications. - 2014. - T. 50. - №.8. - C. 1006-1008].
Примером конкретного осуществления реакции Ульмана для получения производных фенилового эфира может служить известный способ получения одного из тетраметильных производных дифенилового эфира, а именно, 1,4-бис(3',4'-диметилфенокси)бензола. Данный способ осуществляют реакцией Ульмана с использованием в качестве исходных продуктов диметилзамещенного фенола (ксилола) и диметилзамещенного галогенбензола (дибромбензола) (SU 236483, С07С 63/00, 1976).
1,4-бис(3',4'-Диметилфенокси)бензол, согласно цитируемому патенту, получают следующим образом. Сначала смешивают ксилол, диметилбромбензол, гидроксид калия при их мольном соотношении, соответственно равном 4:1:2 и нагревают полученную смесь в течение 1 часа до 110°С, затем добавляют порошок активированной металлической меди и нагревают в течении 6-ти часов при 250°С. После этого реакционную массу охлаждают до комнатной температуры и подвергают полученный продукт многостадийной обработке, для чего его промывают многократно водой, отфильтровывают на воронке Бюхнера, перегоняют под вакуумом, собирая фракции воды и непрореагировавшего бромбензола, полученный осадок подвергают перекристаллизаци в этаноле. Выделяют продукт с 47% выходом (в расчете на бромбензол).
Результаты применения реакции Ульмана в известных способах проведения реакции Ульмана для получения динитропроизводных фенилового эфира весьма удовлетворительны, поскольку выход продуктов реакции в них очень низок.
Среди динитропроизводных фенилового эфира наибольшую известность получил 4,4'-оксидинитробензол (бис(п-нитрофениловый эфир), имеющий следующую структурную формулу:
 ,
,
а также 1,4-бис(п-нитрофенокси)бензол, имеющий следующую структурную формулу:

Синтез данного соединения может быть осуществлен либо конденсацией гидрохинона с галогеннитробензолом, либо парадигалогенбензола с пара-нитрофенолом.
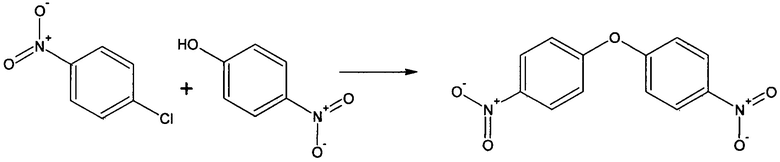
Одним из известных методов получения динитродифениловых эфиров является метод, основанный на реакции взаимодействия галогеннитрофенилового соединения с основанием. К данному методу, например, относится известный способ получения нитропроизводного дифенилового эфира реакцией п-нитрохлорбензола с п-нитрогидроксибензолом в среде диметилсульфоксида в присутствии карбоната калия [Li, Feng; Wang, Quanrui; Ding, Zongbiao; Tao, Fenggang; Organic Letters; vol. 5; nb. 12; (2003); p. 2169-2171; Li, Feng; Meng, Qingqing; Chen, Huansheng; Li, Zhiming; Wang, Quanrui; Tao, Fenggang; Synthesis; nb. 8; (2005); p. 1305-1313]. Известен способ получения нитропроизводного дифенилового эфира из данных соединений, осуществляемый в присутствии катализаторов - фторида калия на гидроксиде алюминия и в присутствии эфира 18-краун-6 в ацетонитриле [Sawyer, J. Scott; Schmittling, Elisabeth A.; Palkowitz, Jayne A.; Smith III, William J.; Journal of Organic Chemistry; vol. 63; nb. 18; (1998); p. 6338-6343].
Механизм получения данного соединения по данному методу синтеза приведен ниже:

К данному методу относится известный способ получения динитродифенилового эфира, в котором процесс изготовления симметричного динитродифенилового эфира из о- или п-нитрохлорбензола или о- или п-нитрофторбензола осуществляется в среде органического растворителя, диметилацетамиде, при температуре 150-210°С в присутствии калиевой соли жирной карбоновой кислоты, содержащей от 2 до 20 атомов углерода или калиевой соли ароматической карбоновой кислоты, содержащей от 7 до 12 атомов углерода или натриевого или калиевого карбоната, фторида калия [US 4558164, МПК С07С 79/35; С07С 41/01, 10.12.85] В основе данного способа лежит следующая реакция:
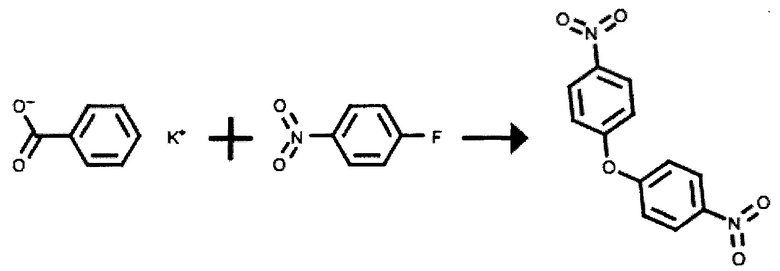
Известно, что в качестве исходных галогендинитробензолов могут быть использованы как хлорпроизводные (хлорнитробензол), так и фторпроизводные (фторнитробензол), и бромпроизводные (бромнитробензол). Так, в способе, описанном в американском патенте [US 4700011, МПК С07С 43/275, 13.10.1987] в качестве хлорпроизводных используются следующие соединения: о-хлорнитробензол, п-хлорнитробензол, 2,5-дихлорнитробензол, 3,4-дихлорнитробензол, 2-хлор-5-этилнитробензол, 5-хлор-2-нитроанизол, а бромпроизводных - бромнитробензол. При этом динитродифениловые эфиры данным способом получают реакцией перечисленных галогеннитрофениловых соединений с основаниями, в качестве которых используются органические и неорганические соединения, например, нитрофеноляты щелочных металлов, гидроокиси щелочных и щелочноземельных металлов, карбонаты, бикарбонаты, нитриты, динатрийфосфаты. Реакция осуществляется при температуре от 150-250°С, молярном избытке галогеннитрофенилового соединения и предпочтительно при использовании оснований в виде концентрированных 45-50%-ных водных растворов. Молярное соотношение реагентов, галоген-нитрофенильного соединения с основанием, составляет по меньшей мере 1,15:1. Реакцию по данному изобретению проводят в реакционной среде, содержащей органический растворитель, способный растворять галогеннитрофенильное соединение, органические растворители включают алифатические амиды, органические сульфоны и сульфоксиды, такие как диэтилсульфоксид и диметилсульфоксид. Сырой динитрофениловый эфир очищают экстракцией в неводном растворителе, например, диметилацетамиде. [US 4700011, МПК С07С 43/275; С07С 79/35, 13.10.87].
Недостатком данного метода является использование водных растворов оснований. Скорость этерификации, наблюдаемая в отсутствие воды, обычно вдвое превышает скорость, наблюдаемую в присутствии воды. Удаление воды из реакционной системы способствует улучшению выхода продуктов и уменьшению образования побочных продуктов.
Среди известных способов проведения реакции Ульмана для получения динитропроиздодных соединений выход продуктов реакции очень низок.
Как видно из рассмотренных аналогов, динитропроизводные фениловых эфиров, как дифениловых, так и трифениловых, в частности 4,4'-оксидинитробензол и 1,4-бис(п-нитрофенокси)бензол, в известных способах получают с низкими выходами, а сам процесс получения занимает большое количество времени.
Для расширения ассортимента нитропроизводных дифенилового эфира, получаемых реакцией Ульмана, а также для повышения эффективности процесса их получения и повышения чистоты получаемых веществ предлагается способ получения динитропроизводных дифениловых и трифениловых эфиров, осуществляемый реакцией взаимодействием замещенного фенола, выбранного из группы пара-нитрофенол и гидрохинон, с пара-хлорнитробензолом в среде органического растворителя в атмосфере инертного газа при повышенной температуре в присутствии катализатора с последующим выделением целевого продукта, при этом реакцию взаимодействия замещенного фенола с пара-хлорнитробензолом проводят в среде апротонного органического растворителя при мольном соотношении исходных фенолов к пара-хлорнитробензолу, равном 1:1 или 1:2 или 2:1, и в присутствии прокаленного карбоната калия, иодида меди (I) и краун-эфиров, взятых в количествах, соответствующих их мольному соотношению к фенолам, соответственно равному: (1-4:1) - для карбоната калия, (0,05-0,1:1) - для иодида меди (I) и (0,001-0,01:1) - для краун-эфиров, причем реакция взаимодействия замещенных фенолов с пара-хлорнитробензолом осуществляется при дозированном трехкратном введении в реакционную массу на каждом этапе по 1/3 от рассчитанного общего веса каждого реагента, выбранного из группы: карбонат калия, иодид меди (I) и краун-эфир, при следующем временном режиме внесения этих компонентов: первую 1/3 часть этих трех реагентов вводят на начальном этапе, через 4-8 часов проведения реакции при кипении в среде апротонного растворителя вводят вторую 1/3 часть, еще через 4-8 часов осуществления реакции в том же режиме вводят последнюю 1/3 часть всех трех реагентов и кипятят реакционную массу при перемешивании еще 4-8 часов, после чего осуществляют выделение целевого продукта, включающее охлаждение реакционной массы, разбавление ее водой и обработку 50%-ной серной кислотой, экстракцию толуолом, обработку толуольных фракций насыщенным хлоридом натрия, сушку над хлористым кальцием и вакуумную перегонку.
В качестве краун-эфира используют соединения из группы: 15-краун-5, бензо-15-краун-5, 18-краун-6, дибензо-18-краун-6, 21-краун-7, дибензо-21-краун-7, 24-краун-8, дибензо-24-краун-8.
Предлагаемый способ осуществляется реакцией Ульмана с использованием в качестве исходных реагентов фенолов (пара-нитрофенола и гидрохинона) и галогенбензолов (пара-хлорнитробензола), и в присутствии катализаторов межфазового переноса.
Предлагаемый способ отличается от прототипа выбором исходных продуктов (замещенных фенолов), их количественными соотношениями, а также выбором катализаторов и их количественными соотношениями.
В качестве исходных продуктов в предлагаемом способе используется: пара-хлорнитробензол

и, в зависимости от получаемого динитрофенилового эфира, а именно динитродифенилового или динитротрифенилового, используются следующие замещенные фенолы:
пара-нитрофенол

и гидрохинон
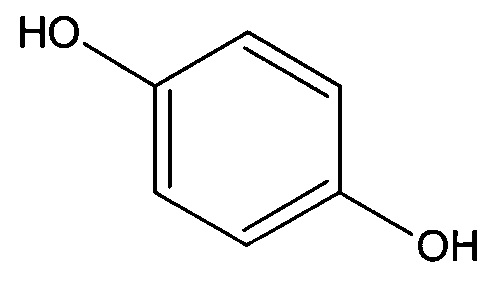
В качестве исходных продуктов в предлагаемом способе в качестве фенола используется не только пара-нитрофенол, как в ряде аналогов, но и гидрохинон.
При этом для получения производных дифенилового эфира в качестве замещенного фенола используется пара-нитрофенол, а для получения производных трифенилового эфира используется гидрохинон.
Предлагаемый способ, в отличие от прототипа, осуществляется в присутствии каталитической смеси, содержащей иодид меди (I) и краун-эфир. Высокие выхода реакций достигаются именно за счет введения в реакцию катализатора межфазного переноса - краун-эфира в комплексе с иодидом меди. В качестве краун-эфира могут быть использованы соединения, выбранные из группы:
15-краун-5
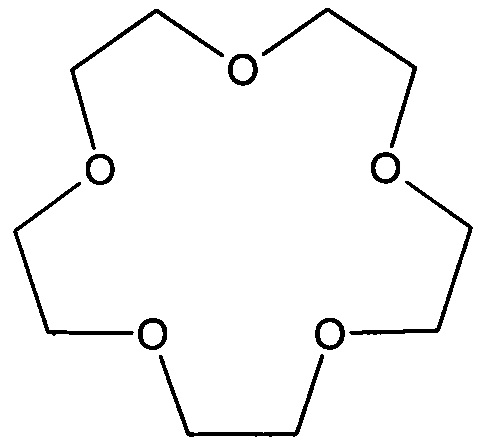
Бензно-15-краун-5
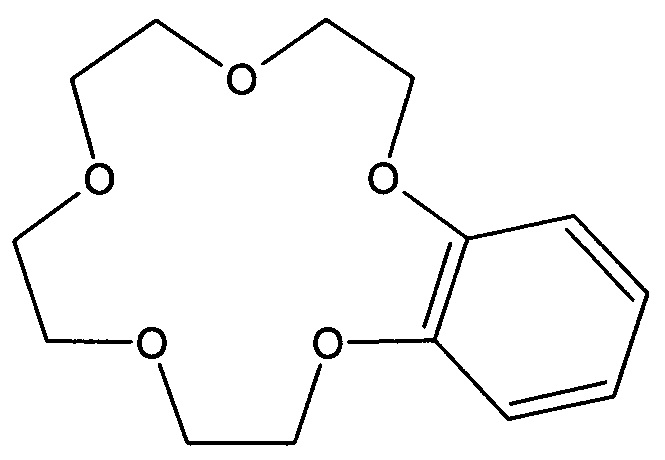
18-краун-6
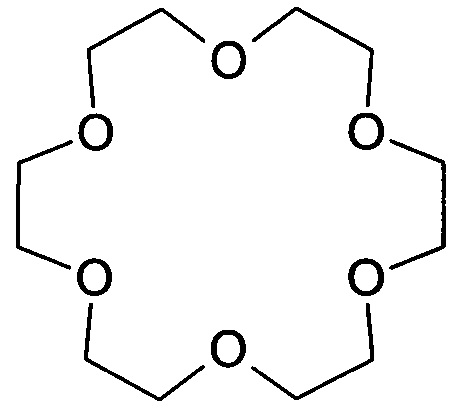
Дибензо-18-краун-6

21-краун-7
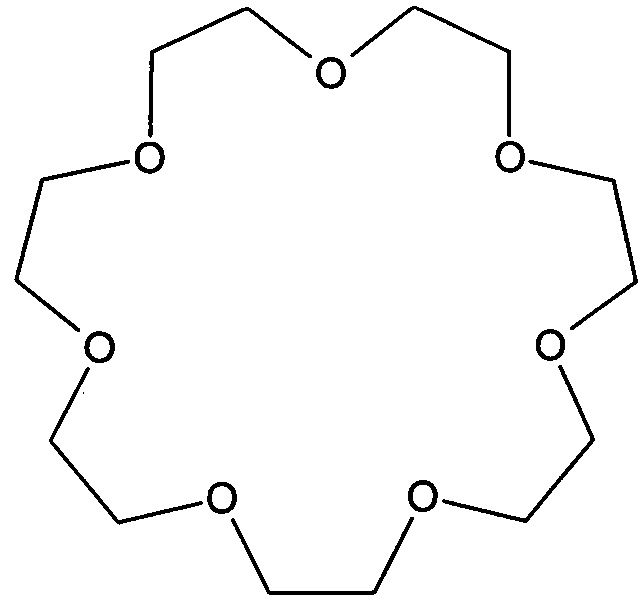
Дибензо-21 -краун-7

24-краун-8
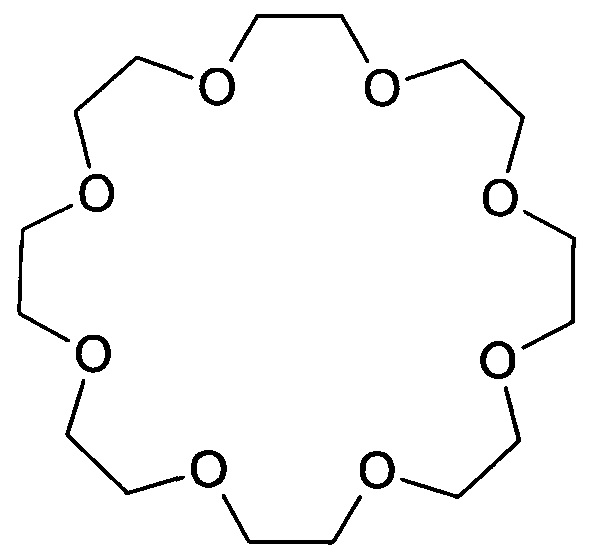
Дибензо-24-краун-8

Использование краун-эфиров является необходимым условием проведения рассматриваемой гетерогенной реакции, поскольку они - краун-эфиры, являясь катализаторами межфазного переноса, способствуют увеличению выхода конечных продуктов по сравнению с прототипом и другими аналогами.
Реакция Ульмана в способе - прототипе и в предлагаемом способе проводится в присутствии калийсодержащего соединения, но в способе - прототипе (US 4700011) это гидроксид калия, используемый в количестве 0,5 мольных эквивалента по отношению к исходному фенолу, а в предлагаемом способе это прокаленный карбонат калия, используемый в количестве, составляющем 1-4 мольных эквивалента по отношению к количеству исходного свободного фенола. Именно замена гидроксида калия, являющегося сильным основанием, на калиевую соль - карбонат калия приводит к снижению количества образующихся побочных продуктов, а значит и к повышению чистоты конечных продуктов.
Существенное отличие предлагаемого способа от прототипа состоит в том, что в новом способе используют смесь сразу двух катализаторов: иодида меди (I) и краун-эфира. Существенное влияние оказывают и выбранные количества используемых катализаторов: (0,05-0,1 мольных эквивалента) - для иодида меди (I) и (0,001-0,01 мольных эквивалента) - для краун-эфира, по отношению к количеству исходного свободного фенола. В то время как в способе-прототипе (US 4700011) в качестве катализатора используется активированная порошкообразная металлическая медь (в количестве 0,08 мольных эквивалента по отношению к исходному фенолу). Использование такого суммарного катализатора повышает эффективность процесса синтеза. К тому же использование иодида меди (I) позволяет избежать стадии активирования медного катализатора, которая необходима при применении порошкообразной меди. Особенность предлагаемого способа заключается и в применении дополнительно к соединению меди в качестве катализатора краун-эфиров, выбранных из группы известных, перечисленных ниже соединений.
Отличие предлагаемого способа от прототипа состоит и в том, что в предлагаемом способе процесс проводится в апротонном органическом растворителе, например, N-метилпирролидоне, диметилформамиде, предпочтительно пиридине, что понижает температуру проведения реакции, и что, в свою очередь, снижает количество побочных реакций, а также облегчает аппаратурное оформление работы.
Экспериментальные исследования показали, что существенное влияние на процесс оказывает выбранный способ внесения исходных соединений, а именно поэтапное дозированное введение карбоната калия, иодида меди (I) и краун-эфира. Для этого до начала процесса конденсации необходимое рассчитанное количество карбоната калия, иодида меди (I) и краун-эфира разделяют каждый по отдельности на три равные части и затем в колбу (реактор) вводят первую часть этих трех реагентов и выдерживают по отработанной схеме в течение 4-8 часов, затем к реакционной массе не прекращая перемешивание при кипении добавляют вторую часть карбоната калия, иодида меди (I) и краун-эфира и продолжают процесс синтеза в тех же условиях в течение еще 4-8 часов и затем добавляют третью порцию карбоната калия, иодида меди (I) и краун-эфира и реакционную массу кипятят при перемешивании в течение еще 4-8 часов, после чего охлаждают и подвергают дальнейшей обработке. Учитывая тот факт, что протекающая реакция является гетерофазной, такое поэтапное дозированное смешение реагентов препятствует загрязнению поверхностей твердых реагентов (основания -карбоната калия) и катализатора (иодида меди (I), что способствует повышению выхода реакции по сравнению с аналогами и повышению чистоты получаемых соединений. Для дальнейшего выделения конечных продуктов проводятся последовательные стадии обработки реакционной массы: охлаждение реакционной массы, разбавление ее водой и обработка 50-%-ной серной кислотой, экстракция органическим растворителем - толуолом, сушка и вакуумная перегонка толуолом, обработка толуольных фракций насыщенным хлоридом натрия, сушка над хлористым кальцием и вакуумная перегонка. Данные стадии осуществляются известными химическими методами.
Ниже приводятся примеры, иллюстрирующие данное изобретение.
Пример 1 (получение 1,4-бис(п-нитрофенокси)бензола).
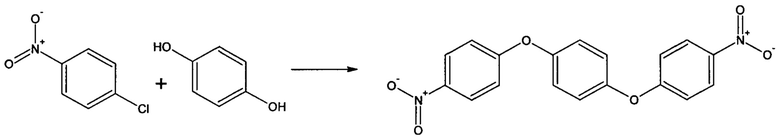
В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 10 г (0,09 моль) гидрохинона, 28,6 г (0,18 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 16,56 г (0,12 моль) прокаленного карбоната калия, 0,57 г (0,003 моль) иодида меди (I), 0,08 г (0,0003 моль) 18-краун-6 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 16,56 г (0,12 моль) прокаленного карбоната калия, 0,57 г (0,003 моль) иодида меди (I), 0,08 г (0,0003 моль) 18-краун-6, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 16,56 г (0,12 моль) прокаленного карбоната калия, 0,57 г (0,003 моль) иодида меди (I), 0,08 г (0,0003 моль) 18-краун-6, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (100 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 2 мм рт.ст. Получают 20,6 г 1,4-бис(п-нитрофенокси)бензола (выход 65%)
Пример 2 (получение 1,4-бис(п-нитрофенокси)бензола).

В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 10 г (0,09 моль) гидрохинона, 28,6 г (0,18 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 4,14 г (0,03 моль) прокаленного карбоната калия, 0,285 г (0,0015 моль) иодида меди (I), 0,0108 г (0,00003 моль) дибензо-18-краун-6 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 4,14 г (0,03 моль) прокаленного карбоната калия, 0,285 г (0,0015 моль) иодида меди (I), 0,0108 г (0,00003 моль) дибензо-18-краун-6, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 4,14 г (0,03 моль) прокаленного карбоната калия, 0,285 г (0,0015 моль) иодида меди (I), 0,0108 г (0,00003 моль) дибензо-18-краун-6, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (100 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 2 мм рт.ст. Получают 18,7 г 1,4-бис(п-нитрофенокси)бензола (выход 59%).
Пример 3 (получение 4,4'-оксидинитробензола).
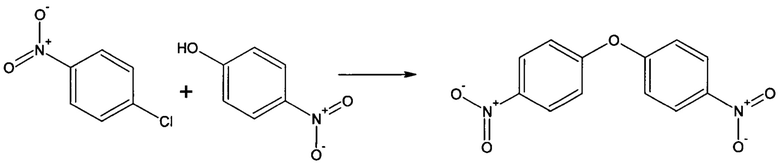
В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 20 г (0,14 моль) пара-нитрофенола, 22,6 г (0,14 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,142 г (0,00046 моль) 21-краун-7 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,142 г (0,00046 моль) 21-краун-7, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,142 г (0,00046 моль) 21-краун-7, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (100 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1,5 мм рт.ст. Получают 14,07 г 4,4'-оксидинитробензола (выход 75%).
Пример 4 (получение 4,4'-оксидинитробензола).
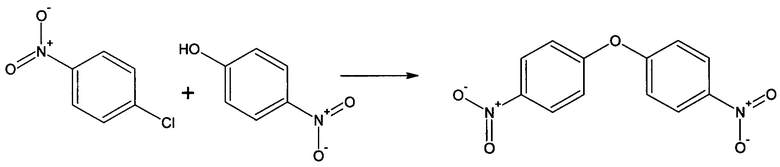
В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 20 г (0,14 моль) пара-нитрофенола, 22,6 г (0,14 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,101 г (0,00046 моль) бензо-15-краун-5 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,101 г (0,00046 моль) бензо-15-краун-5, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,101 г (0,00046 моль) бензо-15-краун-5, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (150 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1 мм рт.ст. Получают 16 г 4,4'-оксидинитробензола (выход 85%).
Пример 5 (получение 4,4'-оксидинитробензола).
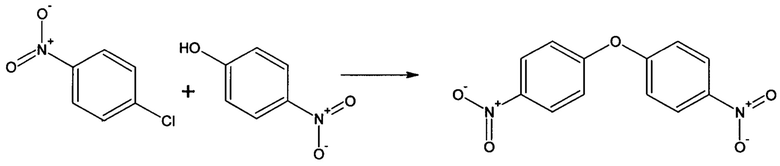
В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 20 г (0,14 моль) пара-нитрофенола, 11,3 г (0,07 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,0184 г (0,000046 моль) дибензо-21-краун-7 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,0184 г (0,000046 моль) дибензо-21-краун-7, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 25,7 г (0,18 моль) прокаленного карбоната калия, 0,87 г (0,0046 моль) иодида меди (I), 0,0184 г (0,000046 моль) дибензо-21-краун-7, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (150 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1 мм рт.ст. Получают 15 г 4,4'-оксидинитробензола (выход 80%).
Пример 6 (получение 4,4'-оксидинитробензола).

В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 10 г (0,07 моль) пара-нитрофенола, 22,6 г (0,14 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 12,85 г (0,09 моль) прокаленного карбоната калия, 0,435 г (0,0023 моль) иодида меди (I), 0,05 г (0,00023 моль) 15-краун-5 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 12,85 г (0,09 моль) прокаленного карбоната калия, 0,435 г (0,0023 моль) иодида меди (I), 0,05 г (0,00023 моль) 15-краун-5, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 12,85 г (0,09 моль) прокаленного карбоната калия, 0,435 г (0,0023 моль) иодида меди (I), 0,05 г (0,00023 моль) 15-краун-5, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (150 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1 мм рт.ст. Получают 15,6 г 4,4'-оксидинитробензола (выход 83%).
Пример 7 (получение 4,4'-оксидинитробензола).
В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 10 г (0,07 моль) пара-нитрофенола, 22,6 г (0,14 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 12,85 г (0,09 моль) прокаленного карбоната калия, 0,435 г (0,0023 моль) иодида меди (I), 0,103 г (0,00023 моль) дибензо-24-краун-8 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 4 г (0,029 моль) прокаленного карбоната калия, 0,42 г (0,002 моль) иодида меди (I), 0,103 г (0,00023 моль) дибензо-24-краун-8, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 4 г (0,029 моль) прокаленного карбоната калия, 0,42 г (0,002 моль) иодида меди (I), 0,103 г (0,00023 моль) дибензо-24-краун-8, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (150 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1 мм рт.ст. Получают 16,9 г 4,4'-оксидинитробензола (выход 90%).
Пример 8 (получение 4,4'-оксидинитробензола).

В трехгорлую круглодонную колбу объемом 250 мл, снабженную механической мешалкой, обратным холодильником, вводом и выводом инертного газа, загружают 10 г (0,07 моль) пара-нитрофенола, 22,6 г (0,14 моль) пара-хлорнитробензола, 100 мл пиридина и при перемешивании добавляют 12,85 г (0,09 моль) прокаленного карбоната калия, 0,435 г (0,0023 моль) иодида меди (I), 0,096 г (0,00023 моль) 24-краун-8 нагревают до кипения и кипятят. Через 8 часов добавляют (не прекращая перемешивание при кипении) вторую порцию 4 г (0,029 моль) прокаленного карбоната калия, 0,42 г (0,002 моль) иодида меди (I), 0,096 г (0,00023 моль) 24-краун-8, спустя еще 8 часов добавляют (не прекращая перемешивание при кипении) третью порцию 4 г (0,029 моль) прокаленного карбоната калия, 0,42 г (0,002 моль) иодида меди (I), 0,096 г (0,00023 моль) 24-краун-8, кипятят при перемешивании еще 8 часов и охлаждают до комнатной температуры.
К реакционной смеси прибавляют 200 мл воды и полученную массу выливают в 250 мл 50% раствора серной кислоты, экстрагируют 3 раза по 150 мл толуолом. Объединенные органические фракции промывают насыщенным раствором хлорида натрия (150 мл) и высушивают над хлоридом кальция (20 г). Отгоняют при вакууме 10 мм рт.ст растворитель. Остаток перегоняют в вакууме 1 мм рт.ст. Получают 13 г 4,4'-оксидинитробензола (выход 70%).
Таким образом, новый способ позволяет получать динитропроизводные ди- и трифениловых эфиров с более высокими выходами и более чистыми по сравнению с ранее известными способами проведения реакции Ульмана.
Ниже приводятся результаты физико-химических анализов (измерение температуры плавления, 1Н ЯМР и элементного анализа), подтверждающие структуру полученных соединений:
Пример 1
Тпл.=230-231°С.
1Н ЯМР (300 МГц, DMSO d6) (м.д.): 8,29 (м, 2Н); 8,26 (м, 2Н); 7,32 (с, 4Н); 7,22 (м, 2Н); 7,19 (м, 2Н);
Элементный анализ: C18H12N2O6 Вычислено, %: С: 61,37, Н: 3,43, N: 7,95. Найдено, %: С:61,4; Н: 3,3, N: 8,0.
Пример 2
Тпл.=230-231°С.
1Н ЯМР (300 МГц, DMSO d6) (м.д.): 8,29 (м, 2Н); 8,25 (м, 2Н); 7,33 (с, 4Н); 7,23 (м, 2Н); 7,20 (м, 2Н);
Элементный анализ: C18H12N2O6 Вычислено, %: С: 61,37, Н: 3,43, N: 7,95. Найдено, %: С:61,2; Н: 3,5, N: 7,9.
Пример 3
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,25 (м, 2Н); 8,22 (м, 2Н); 7,12 (м, 2Н); 7,09 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.1; Н: 3.15, N: 10,9.
Пример 4
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,27 (м, 2Н); 8,24 (м, 2Н); 7,14 (м, 2Н); 7,11 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.2; Н: 3.2, N: 11,0.
Пример 5
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,25 (м, 2Н); 8,22 (м, 2Н); 7,11 (м, 2Н); 7,08 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.3; Н: 3.3, N: 10,7.
Пример 6
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,26 (м, 2Н); 8,23 (м, 2Н); 7,12 (м, 2Н); 7,09 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.4; Н: 3.1, N: 10,9.
Пример 7
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,25 (м, 2Н); 8,22 (м, 2Н); 7,13 (м, 2Н); 7,10 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.5; Н: 3.0, N: 10,7.
Пример 8
Тпл.=143-144°С.
1Н ЯМР (300 МГц, DMSO d6) 8,24 (м, 2Н); 8,21 (м, 2Н); 7,11 (м, 2Н); 7,07 (м, 2Н)
Элементный анализ. C12H8N2O5 Вычислено, %: С: 55,39, Н: 3.10, N: 10,77. Найдено, %: С: 55.0; Н: 3.25, N: 10,9.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАМЕТИЛЬНЫХ ПРОИЗВОДНЫХ ДИФЕНИЛОВОГО ЭФИРА | 2016 |
|
RU2643519C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДОВ АРОМАТИЧЕСКИХ ТЕТРАКАРБОНОВЫХ КИСЛОТ | 2017 |
|
RU2682170C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДА 4,4´-БИНАФТИЛ-1,1´,8,8´-ТЕТРАКАРБОНОВОЙ КИСЛОТЫ ИЗ ГАЛОГЕНАЦЕНАФТЕНОВ | 2017 |
|
RU2671579C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС- И ТРАНС-ИЗОМЕРОВ ДИНИТРОДИБЕНЗО-18-КРАУН-6 | 2017 |
|
RU2658921C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛИДИНОНА | 1972 |
|
SU348002A1 |
| Способ получения 2,3,11,12-дибензо-1,4,7,10,13,16-гексаоксациклооктадека-2,11-диена | 1980 |
|
SU958421A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИИМИДНЫХ СОПОЛИМЕРОВ, СОДЕРЖАЩИХ КРАУН-ЭФИРНЫЕ И ПОЛИСИЛОКСАНОВЫЕ ФРАГМЕНТЫ | 2016 |
|
RU2644152C1 |
| ПРОИЗВОДНЫЕ ДИБЕНЗО[D, G][1,3]ДИОКСОЦИНА И ДИБЕНЗО-[D,G][1,3,6]ДИОКСАЗОЦИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ НЕЙРОГЕННОГО ВОСПАЛЕНИЯ, НЕЙРОПАТИИ И РЕВМАТОИДНОГО АРТРИТА | 1996 |
|
RU2178790C2 |
| Способ получения 6-или 8-оксизамещенных 2,2,4-триметил-1,2-ди или 1,2,3,4-тетрагидрохинолинов | 1986 |
|
SU1384582A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРИМЕТИЛОВОГО ЭФИРА ФОСФОНУКСУСНОЙ КИСЛОТЫ | 2013 |
|
RU2527977C1 |
Изобретение относится к способу получения динитропроизводных дифениловых и трифениловых эфиров. Способ осуществляется реакцией взаимодействия замещенного фенола с пара-хлорнитробензолом в среде органического растворителя в атмосфере инертного газа при повышенной температуре в присутствии катализатора с последующим выделением целевого продукта. Способ характеризуется тем, что реакцию взаимодействия пара-хлорнитробензола с замещенным фенолом, выбранным из группы пара-нитрофенол и гидрохинон, проводят в среде апротонного органического растворителя при мольном соотношении исходных фенолов к пара-хлорнитробензолу, равном 1:1, или 1:2, или 2:1, в присутствии прокаленного карбоната калия, иодида меди (I) и краун-эфиров, взятых в количествах, соответствующих их мольному соотношению к фенолам, соответственно равному (1-4:1) - для карбоната калия, (0,05-0,1:1) - для иодида меди (I) и (0,001-0,01:1) - для краун-эфиров. Реакцию взаимодействия замещенных фенолов с пара-хлорнитробензолом осуществляют при дозированном трехкратном введении в реакционную массу на каждом этапе по 1/3 от рассчитанного общего веса каждого из перечисленных реагентов - карбоната калия, иодида меди (I) и краун-эфира - при следующем временном режиме внесения этих компонентов: первую 1/3 часть этих трех реагентов вводят на начальном этапе, через 4-8 ч проведения реакции при кипении в среде апротонного растворителя вводят вторую 1/3 часть, еще через 4-8 ч осуществления реакции в том же режиме вводят последнюю 1/3 часть всех трех реагентов и кипятят реакционную массу при перемешивании еще 4-8 ч. После этого осуществляют выделение целевого продукта, включающее охлаждение реакционной массы, разбавление ее водой и обработку 50%-ной серной кислотой, экстракцию толуолом, обработку толуольных фракций насыщенным хлоридом натрия, сушку над хлористым кальцием и вакуумную перегонку. Предлагаемый способ позволяет получать динитропроизводные дифениловых и трифениловых эфиров с более высокими выходами. 2 з.п. ф-лы, 8 пр.
1. Способ получения динитропроизводных дифениловых и трифениловых эфиров, осуществляемый реакцией взаимодействия замещенного фенола с пара-хлорнитробензолом в среде органического растворителя в атмосфере инертного газа при повышенной температуре в присутствии катализатора с последующим выделением целевого продукта, отличающийся тем, что реакцию взаимодействия пара-хлорнитробензола с замещенным фенолом, выбранным из группы пара-нитрофенол и гидрохинон, проводят в среде апротонного органического растворителя при мольном соотношении исходных фенолов к пара-хлорнитробензолу, равном 1:1, или 1:2, или 2:1, и в присутствии прокаленного карбоната калия, иодида меди (I) и краун-эфиров, взятых в количествах, соответствующих их мольному соотношению к фенолам, соответственно равному (1-4:1) - для карбоната калия, (0,05-0,1:1) - для иодида меди (I) и (0,001-0,01:1) - для краун-эфиров, причем реакция взаимодействия замещенных фенолов с пара-хлорнитробензолом осуществляется при дозированном трехкратном введении в реакционную массу на каждом этапе по 1/3 от рассчитанного общего веса каждого из перечисленных реагентов - карбоната калия, иодида меди (I) и краун-эфира - при следующем временном режиме внесения этих компонентов: первую 1/3 часть этих трех реагентов вводят на начальном этапе, через 4-8 ч проведения реакции при кипении в среде апротонного растворителя вводят вторую 1/3 часть, еще через 4-8 ч осуществления реакции в том же режиме вводят последнюю 1/3 часть всех трех реагентов и кипятят реакционную массу при перемешивании еще 4-8 ч, после чего осуществляют выделение целевого продукта, включающее охлаждение реакционной массы, разбавление ее водой и обработку 50%-ной серной кислотой, экстракцию толуолом, обработку толуольных фракций насыщенным хлоридом натрия, сушку над хлористым кальцием и вакуумную перегонку.
2. Способ по п.1, отличающийся тем, что в качестве краун-эфира используют соединения из группы 15-краун-5, бензо-15-краун-5, 18-краун-6, дибензо-18-краун-6, 21-краун-7, дибензо-21-краун-7, 24-краун-8, дибензо-24-краун-8.
3. Способ по п.1, отличающийся тем, что в качестве апротонного растворителя используют предпочтительно пиридин.
| C | |||
| PARADISI ET AL., Anion Activation in the Synthesis of Ethers from Oxygen Anions and 1-Chloro-4-nitrobenzene, J | |||
| ORG | |||
| CHEM., 1983, Vol | |||
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| КОВШЕВОЙ ТРАНСПОРТЕР | 1925 |
|
SU3022A1 |
| J | |||
| S | |||
| SAWYER ET AL., Synthesis of Diaryl Ethers, Diaryl Thioethers, and Diarylamines Mediated by Potassium Fluoride-Alumina and 18-Crown-6: Expansion of Scope and Utility, J | |||
| ORG | |||
| CHEM., 1998, Vol | |||
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Соединительное приспособление для труб | 1925 |
|
SU6338A1 |
| W.-Q | |||
| ZHANG ET AL., Thermal transition behaviors, solubility, and mechanical properties of wholly aromatic para-, meta-poly(ether-amide)s: effect on numbers of para-aryl ether linkages, RSC ADVANCES, 2016, 6, 84284-84293 | |||
| US 4700011 A, 13.10.1987 | |||
| Способ получения диангидрида 3,4,3,4трифенилдиоксидтетракарбоновой кислоты | 1967 |
|
SU236483A1 |
Авторы
Даты
2018-11-02—Публикация
2017-12-28—Подача