Изобретение относится к области медицины, в частности к иммунологии. Содержание растворимых HLA-DR молекул является важным показателем в трансплантационной иммунологии. Содержание растворимых HLA-DR антигенов в сыворотке крови существенно повышается при ревматоидном артрите (Claus et al.//Cell Immunol, 2000, V.206, №2, Р.85-100; Verbruggen et al.//Tissue Antigens, 2000, V.56, №5, Р.436-440), аутоиммунном гепатите (Hagihara et al.//Autoimmunity, 1999, V.31, №2, Р.85-93). Отмечается прогностическое значение уровня молекул sHLA-DR в сыворотке крови больных гепатитом С при терапии интерфероном альфа (Hosoi et al.//Tokai. J. Exp. Clin. Med., 2000, v.25, №3, p.117-124). Известна корреляция между сывороточным уровнем sHLA-DR и активностью множественного склероза (Ott et al.//Tissue Antigens, 1998, v.51, №3, p.301-304). Таким образом, сывороточный уровень растворимых HLA-DR антигенов может применяться как прогностический показатель течения заболеваний различной природы.
Известны некоторые способы определения растворимых форм HLA-DR антигенов:
1) Метод ингибиции антител на основе микролимфоцитотоксической пробы, заключающийся в следующем: к тестовой моноспецифической антисыворотке добавляют различные исследуемые на HLA-DR образцы жидкости, после инкубации вносят лимфоциты, содержащие HLA, соответствующие антителам антисыворотки. Далее проводят микролимфоцитотоксический тест с применением комплемента (см. Terasaki P.J., Mc Glelland J.D. // Nature, 1964, v.204, p.998-1000; модификация Рагимов А.А. // Иммунология, 1982, №3, с.34-36). Однако этот способ имеет довольно низкую чувствительность, т.к. оценку интенсивности цитотоксической реакции производят по проценту гибели клеток.
2) Метод скоростной нефелометрии, основанный на зависимости скорости взаимодействия HLA-антигенов с моноклональными антителами от концентрации HLA-молекул (см. Коненков В.И., Наумов Ю.Н., Прокофьев В.Ф.//Иммунология, 1987, №6, с.61-63). Но при этом способе требуется дорогостоящее оборудование для регистрации изменения мутности исследуемых растворов (нефелометр).
Наиболее близким к предлагаемому изобретению является иммуноферментный метод определения растворимой формы HLA-DR молекул (см. Hausmann S., Claus R., Buchwald S., Kohler H., Hausmann D., Falk U., Wegener S.//J.Immunoassay, 1996, 17, 257-75). В данном способе иммунологические планшеты сорбируют HLA-DR-специфичными моноклональными антителами BL-Ia/5 при 4°С, затем инкубируют с образцами сыворотки и стандартом при 37°С в течение 90 мин. Следующий этап - последовательная инкубация с HLA-DR-специфичными моноклональными антителами L243 (1 ч), стрептавидином, конъюгированным с пероксидазой (30 мин) и о-фенилендиамином в качестве субстрата (30 мин). Реакцию останавливают серной кислотой, измеряют оптическую плотность при 492 нм и переводят по калибровочной кривой в нг. Этот способ характеризуется высокой чувствительностью и простотой постановки, но из-за применения моноклональных антител иностранного производства довольно дорог. Однако опосредованная связь вторых антител и фермента снижает специфичность реакции.
Целью изобретения является удешевление способа с сохранением высокой чувствительности и специфичности.
Сущность изобретения заключается в том, что для определения растворимых форм молекул HLA-DR в качестве первых антител применяют поликлональные антитела против поверхностных антигенов мононуклеарных клеток человека, а в качестве вторых антител используют HLA-DR-специфичные моноклональные антитела МКА ИКО-1, полученные в Онкологическом центре РАМН, конъюгированные непосредственно с пероксидазой хрена.
Способ определения растворимых HLA-DR молекул с помощью твердофазного иммуноферментного анализа осуществляют следующим образом.
Поликлональные антитела против поверхностных антигенов мононуклеарных клеток человека выделяют с помощью сульфата аммония и ионообменной хроматографии на ДЕАЕ-целлюлозе и сорбируют в разведении 1:1000 по 100 мкл в лунки полистироловых планшетов для иммуноферментного анализа в течение 16-18 ч при 4-8°С. После отмывания не связавшихся антител в лунки вносят образцы исследуемых сывороток. Планшеты инкубируют при комнатной температуре в течение 16-18 ч с последующим отмыванием не связавшихся белков. Затем лунки планшетов обрабатывают рабочим раствором очищенных моноклональных антител МКА ИКО-1, конъюгированных с пероксидазой хрена (Иммунологические методы /Под ред. Г. Фримеля, с.438) в разведении 1:400 и инкубируют в течение 1 часа при 37°С. После отмывки не связавшихся меченых антител в лунки планшетов вносят субстрат: на 10 мл цитратного буфера - 3 мг о-фенилендиамина с последующей инкубацией в течение 15-20 мин при комнатной температуре. Реакцию останавливают внесением 0,5 М H2SО4. Снимают показания с помощью иммуноферментного фотометра. Концентрацию растворимых HLA-DR антигенов оценивают, переводя единицы оптической плотности в условные единицы (U/ml) по калибровочному графику с использованием стандарта, представляющего собой хранящиеся при -60°С образцы сыворотки крови, содержащие растворимые HLA-DR в одних и тех же концентрациях.
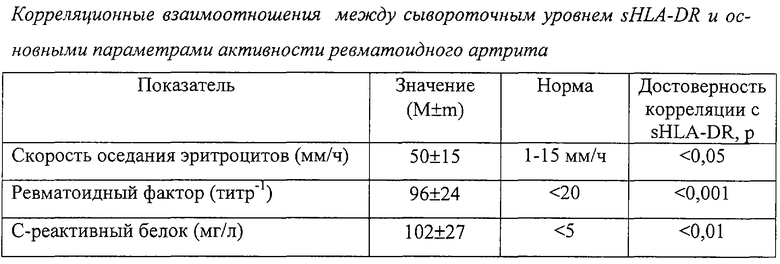
Оптимальные концентрации поликлональных антител для сорбции планшетов определяли, измеряя оптическую плотность при различных разведениях от 1:100 до 1:1500. Максимальная разница между опытным и фоновым значениями наблюдалась при тысячекратном разведении поликлональных антител (см. фиг. 1А). Наиболее эффективную концентрацию моноклональных антител, конъюгированных с пероксидазой хрена, также определяли, используя разведения конъюгата от 1:50 до 1:800. Оптимальным явилось разведение в 400 раз (чертеж, В).
Пример практического применения
При исследовании уровня растворимой формы HLA-DR молекул в сыворотке крови 198 здоровых доноров было показано, что ее содержание в норме составляет 115,9±14,61 U/ml. Образцы сыворотки были получены также от 22 пациентов с ревматоидным артритом (18 женщин и 4 мужчины). Средний возраст больных составил 44,2±2,3 года, средняя продолжительность болезни 7,7±1,6 года. У одного больного установлена II рентгенологическая стадия заболевания, у остальных - II-III стадии. Активность заболевания у 6 больных соответствовала I, у остальных - II-III степени. Ревматоидный фактор был обнаружен у 18 больных. В исследованной группе было выявлено статистически достоверное увеличение сывороточного содержания sHLA-DR, средний уровень которого составил 227±19 U/ml (р<0,01). Была отмечена достоверная корреляция между сывороточным уровнем sHLA-DR и параметрами активности заболевания пациентов: скоростью оседания эритроцитов, ревматоидным фактором, С-реактивным белком (см. таблицу). Таким образом, определение сывороточной концентрации sHLA-DR молекул позволяет судить об активности течения ревматоидного артрита.
К достоинствам разработанного метода относится простота в применении, отсутствие сложной аппаратуры, дорогостоящих реактивов, высокая специфичность, возможность определять минимальные концентрации вещества (нанограммы/мл). Конъюгирование вторых антител непосредственно с ферментом позволяет сократить этап работы.
В связи с тем, что молекулы главного комплекса гистосовместимости играют центральную роль в иммунном ответе, определяя выраженность реакции иммунной системы индивида на каждое антигенное воздействие, исследование уровня растворимой формы HLA-DR антигенов в сыворотке человека важно как диагностический и прогностический маркер течения различных заболеваний вирусной, аутоиммунной и другой природы, а также при трансплантации различных органов.
Способ разработан и осуществлен в лаборатории молекулярной иммунологии бактериальных и вирусных инфекций НИИ эпидемиологии и микробиологии им. акад. И.Н.Блохиной, г. Н. Новгород.
Изобретение относится к области медицины, в частности к иммунологии. Сущность изобретения состоит в том, что на твердом носителе проводят иммобилизацию специфических антител на твердом носителе, последовательную инкубацию с исследуемой сывороткой и пероксидазным конъюгатом, при этом в качестве первых антител используют поликлональные антитела против поверхностных антигенов мононуклеарных клеток человека, а в качестве вторых антител применяют HLA-DR специфичные моноклональные антитела ИКО-1, конъюгированные с пероксидазой хрена. 2 з.п. ф-лы, 1 табл., 1 ил.
| HAUSMANN S | |||
| et al | |||
| Influence of anticoagulants on the level of soluble HLA class I and class II antigens measured in blood samples | |||
| Journal of immunology, 1996, 17(3), p.257-275 | |||
| HAUSMANN S | |||
| et al | |||
| Quantitation of soluble HLA-DR antigens in human serum and other body fluids | |||
| Beitr Infusionsther Transfusionsmed, 1994, 32, p.281-287 | |||
| КОНЕНКОВ В.И | |||
| и др | |||
| Уровень экспрессии HLA-антигенов I и II классов на поверхностной мембране субпопуляций лимфоцитов периферической крови здоровых людей | |||
| - Иммунология, 1987, №6, с.61-63. |
Авторы
Даты
2004-09-27—Публикация
2002-06-10—Подача