Настоящее изобретение относится к новым фармацевтическим применениям фторированных триазолов.
Более конкретно настоящее изобретение относится к новым фармацевтическим применениям соединений формулы I
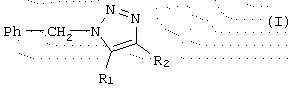
где Ph обозначает ортофторированный фенильный радикал, который может быть дополнительно замещен 1 или 2 атомами галогена, выбранными из атомов фтора и хлора, R1 обозначает водород, карбамоил, N-(С2-С5)алканоилкарбамоил или N,N-ди(С1-С4)алкилкарбамоил, и R2 обозначает карбамоил, N-(C2-С5)алканоилкарбамоил или N,N-ди(С1-С4)алкилкарбамоил.
Соединения формулы I, а также метод их получения являются известными, например, они описаны в европейском патенте 199262. В этом патенте также описано применение соединений формулы I для лечения судорог различного происхождения, например, при эпилепсии. В то же время европейский патент 199262 не содержит сведений о лечении невропатической боли, аффективных расстройств, расстройств внимания.
При создании настоящего изобретения неожиданно было установлено, что соединения формулы I могут применяться для лечения невропатической боли, аффективных расстройств, включая биполярные расстройства настроения, а также расстройства внимания.
Активность соединений формулы I при лечении невропатической боли может быть продемонстрирована, например, на описанных ниже моделях невропатической боли с использованием крыс и морских свинок:
Крыс линии Wistar или морских свинок линии Dunkin Hartley подвергают анестезии энфураном (для морских свинок - в N2O:O2) и выделяют левый седалищный нерв и частично перевязывают нитью. Эта процедура вызывает механическую гипералгезию, которая развивается в течение 2-3 дней и сохраняется в течение по крайней мере 4 недель. С использованием аналгезиметра измеряют пороговые значения стимула в виде давления для реакции отдергивания лапы. Определяют пороговые значения механического стимула как для ипсилатеральной (с наложенной лигатурой), так и для контралатеральной (без лигатуры) лапы до опыта и затем через 6 ч после введения лекарственного средства или носителя. Для каждого момента времени рассчитывают реверсирование гипералгезии. В опытах используют группы животных по 6 особей в каждой. Статистический анализ результатов измерений пороговых значений стимула для реакции отдергивания проводят с использованием дисперсионного анализа (ANOVA) после HSD-теста Turkey.
На моделях с использованием крыс соединения формулы I вызывают существенное реверсирование невропатической механической гипералгезии при введении в дозах от приблизительно 10 до приблизительно 300 мг/кг перорально. Например, при применении 1-(2,6-дифторфенил)метил-1Н-1,2,3-триазол-4-карбоксамида максимальное реверсирование невропатической механической гипералгезии, составляющее 30%, достигается через 3 ч после введения этого соединения в дозе 10 мг/кг перорально.
На моделях с использованием морских свинок соединения формулы I вызывают существенное реверсирование невропатической механической гипералгезии при введении в дозах от приблизительно 3 до приблизительно 100 мг/кг перорально. Например, при применении указанного выше карбоксамида максимальное реверсирование невропатической механической гипералгезии, составляющее 60%, достигается через 3 ч после введения этого соединения в дозе 30 мг/кг перорально.
Активность соединений формулы I при лечении невропатической боли может быть продемонстрирована в клинических опытах, например, в описанном ниже исследовании, предназначенном для оценки эффективности соединения в отношении лечения хронической боли у пациентов, страдающих диабетической невропатией:
Пациентов случайным образом разделяют на группы в соотношении 1:1, которым вводят соединение или плацебо в дозе 2400 мг/день.
Исследование включает фазу предварительного случайного отбора (1 неделя) и фазу двойного опыта вслепую (5 недель). Фаза двойного опыта вслепую включает три периода: однонедельный период увеличения дозы (период "титрования"), трехнедельный период выдерживания и однонедельный завершающий период.
В течение 1-недельной фазы предварительного случайного отбора оценивают степень приемлемости пациентов. Пациентов, удовлетворяющих всем критериям включения/исключения, случайным образом распределяют по группам, которым вводят в ходе фазы двойного опыта вслепую либо соединение, либо плацебо. В течение 1-недельного периода "титрования" дозу тестируемого соединения повышают от 800 мг/день (вводимой дважды в день) до 2400 мг/день (вводимой дважды в день). Пациенты, прошедшие 1-недельный период "титрования", переходят к 3-недельному периоду выдерживания. Пациенты, прошедшие 3-недельный период выдерживания, или для которых лечение, предусмотренное методом двойного опыта, вслепую прерывается до его окончания, переходят к 1-недельному завершающему периоду. После перехода к завершающему периоду полностью прекращается введение исследуемого лекарственного средства. В ходе фазы двойного опыта вслепую получают серийные оценки эффективности и безопасности.
120 амбулаторных больных мужского и женского пола возрастом 18-65 лет, имеющих клинический диагноз сахарный диабет (типа I или II) и историю боли, связанной с диабетической невропатией, в течение периода времени от 6 месяцев до 3 лет до начала опыта, случайным образом распределяют в соотношении 1:1 на группы, которым вводят соединение или плацебо.
В качестве основного параметра эффективности используют общий балл, полученный на основе краткой формы опросника МакГилла (McGill) для изучения боли (SF-MPQ). В качестве вспомогательных параметров эффективности используют средние за каждую неделю баллы оценки степени боли (ежедневный дневник пациента по оценке боли) от начала случайным образом назначенного типа обработки до конца периода выдерживания, использование экстренных лекарственных средств в течение периода "титрования" и выдерживания и средний балл серьезности боли в течение завершающего периода (рецедив боли).
Общий SF-MPQ-балл оценки боли по окончании периода выдерживания анализируют с помощью ковариационного анализа для оценки влияния обработки на баллы, полученные по окончании обработки, с использованием исходного (базового) общего SF-MPQ-балла боли в качестве ковариации. Средние еженедельные оценки степени боли анализируют с помощью ковариационного анализа с учетом повторных измерений, используя номер недели, когда производилась обработка, и средний балл оценки степени боли, полученный на фазе предварительного случайного отбора, в качестве ковариации. Использование экстренных лекарственных средств в течение фазы двойного опыта вслепую анализируют с помощью теста Кохрана-Мантеля-Хенсцеля с поправкой на среднее значение. Средний балл серьезности боли в течение завершающего периода (рецедив боли) анализируют с помощью ковариационного анализа, используя оценку влияния обработки на средний балл степени боли в течение завершающего периода в сочетании со средним баллом степени боли в течение фазы предварительного случайного отбора в качестве ковариации.
В данном исследовании было установлено, что введение соединений формулы I, в частности, 1-(2,6-дифторфенил)метил-1Н-1,2,3-триазол-4-карбоксамида, в течение периода выдерживания и завершающего периода приводит к статистически достоверному уменьшению оценок степени боли по сравнению с плацебо.
Таким образом, соединения формулы I могут применяться для лечения невропатической боли и связанной с ней гипералгезии, включая невралгию тройничного нерва и невралгию при опоясывающем лишае, диабетическую невропатическую боль, каузалгию и синдромы деафферентации, такие как разрыв плечевого сплетения.
Эффективность соединений формулы I в отношении лечения аффективных расстройств и расстройств внимания может быть продемонстрирована, например, с помощью описанных ниже тестов, которые применяют для выявления лекарственных средств, обладающих потенциальными растормаживающими поведение и/или социотропными действиями, которые, как считается, влияют на возвращение из состояния ухода от общества, что является основной причиной депрессии и связанных с ней психиатрических состояний.
а) Тест с использованием закрытой наполовину платформы
Этот тест проводят в основном следуя методу, описанному в Psychopharmacology, 89:31-37, 1986.
Группам животных, включающим по 12 самцов мышей линии OF-1, за 1 ч до начала опыта с использованием платформы вводят носитель или тестируемую субстанцию. Устройство состоит из прозрачной платформы, в которой просверлены 25 расположенных на одинаковом расстоянии друг от друга отверстий диаметром 1 см. Платформу разделяют на две одинаковые половины высотой по 15 см, одна половина имеет вертикальные стенки, вторая половина не имеет стенок. Вся платформа находится на ножках высотой 15 см. Посередине проведена линия от края одной стенки до края противоположной стенки. Эксперимент состоит в том, что мышь помещают на среднюю линию и регистрируют ее поведение в течение 5 мин, когда она исследует платформу. В частности, регистрируют средние частоты и продолжительности элементов (типов) поведения и проводят статистические сравнения с использованием "Н"-теста Крускала-Уоллиса, после чего проводят парные сравнения между контрольной группой и группами, подвергнутыми обработке, с использованием U-теста Манна-Уитни. Назначенные вероятности (р≤0,05) рассчитывались с использованием двух параметров.
Соединения формулы I, вводимые в дозах приблизительно от 0,3 до приблизительно 10 мг/кг перорально, вызывают существенное усиление исследовательского поведения, такого как вытянутая "внимательная" поза, поднятие головы и продвижение вперед, при нахождении на открытой половине платформы, при этом в закрытой части платформы уменьшается частота стационарных элементов, таких как неподвижное сидение и неактивное поведение.
б) Тест с использованием мыши-гостя
Этот тест проводят, в основном следуя методу, описанному в Triangle, 21:95-105, 1982 и в J. Clin. Psychiatry, 55: 9 (приложение В), 4-7, 1994.
Группе мышей "гостей" вводят субстанцию или носитель за 1 ч до приведения их в контакт на 6 минут с необработанными агрессивными, содержащимися по отдельности в нейтральных клетках мышами (хозяевами). Каждая группа состоит из 8 мышей. Социальный кофликт записывается на видеопленку и наблюдатель регистрирует наличие и продолжительность более 60 элементов поведения, включающих как несоциальные, так и социальные формы из репертуара (набора) типов поведения животного. Регистрируются частота, продолжительность и при необходимости последовательность элементов. Для каждой категории регистрируют средние частоты и продолжительности элементов поведения, и проводят статистические сравнения с использованием "Н"-теста Крускала-Уоллиса, после чего проводят парные сравнения между контрольной группой и группами, подвергнутыми обработке, с использованием U-теста Манна-Уитни. Назначенные вероятности (р≤0,05) рассчитывались с использованием двух параметров.
Соединения формулы I, вводимые в дозах приблизительно от 1 до приблизительно 10 мг/кг перорально, вызывают существенное усиление несоциального поведения и исследовательского социального поведения у подвергнутых обработке мышей-гостей, при этом уменьшается защитная амбивалентность, прекращаются бегство и избегание.
Благодаря тому, что они обладают растормаживающей поведение (типа анксиолитической/антидепрессантной) и социотропной активностями, соединения формулы I могут применяться при лечении аффективных расстройств, включая биполярные расстройства настроения, например маниакально-депрессивных психозов, экстремальных психотических состояний, например мании, шизофрении, и чрезмерных перепадов настроения, когда требуется стабилизация поведения. Кроме того, соединения показаны для ADHD (гиперактивные расстройства дефицита внимания) и других расстройств внимания, например аутизма, состояний страха, общего состояния страха и агорафобии, а также состояний поведения, характеризующихся избеганием общества, например негативными симптомами.
В предпочтительной группе соединений формулы I, которые могут применяться согласно изобретению, Ph обозначает ортофторфенил, 2,5-дифторфенил, 2,6-дифторфенил или 2-хлор-6-фторфенил, R1 обозначает водород или карбамоил и R2 обозначает карбамоил. Наиболее предпочтительным соединением является 1-(2,6-дифторфенил)метил-1Н-1,2,3-триазол-4-карбоксамид.
Для перечисленных выше показаний пригодная доза должна, конечно, варьироваться в зависимости, например, от используемого соединения, хозяина, пути введения и природы и серьезности состояния, подлежащего лечению. Однако в целом удовлетворительные результаты для животных могут быть получены при введении суточной дозы приблизительно от 1 до приблизительно 50 мг/кг веса тела животного. Для крупных млекопитающих, например людей, показанная суточная доза составляет от приблизительно 50 до приблизительно 3500 мг соединения по изобретению, которое удобно вводить, например, в виде разделенных доз до четырех раз в день.
Соединения формулы I могут вводиться любым общепринятым методом, например перорально, например, в форме таблеток или капсул или парентерально, например, в форме растворов или суспензий для инъекций.
Настоящее изобретение также относится к фармацевтическим композициям, включающим соединение формулы I в сочетании с по крайней мере одним фармацевтическим носителем или разбавителем, предназначенным для применения при лечении невропатической боли. Такие композиции могут быть приготовлены общепринятым методом. Стандартные дозируемые формы могут содержать, например, от приблизительно 10 до приблизительно 1500 мг соединения формулы I.
Например, таблетки, каждая из которых содержит 50 мг, или филмтаблетки, каждая из которых содержит 100 мг 1-(2,6-дифторфенил) метил-1Н-1,2,3-триазол-4-карбоксамида, могут быть получены согласно методу, описанному в примерах 15 и 16 ЕР 199262.
Кроме того, изобретение относится к применению соединения формулы I для изготовления фармацевтической композиции, предназначенной для лечения невропатической боли и аффективных расстройств и расстройств внимания.
Кроме того, изобретение относится к способу лечения невропатической боли и аффективных расстройств и расстройств внимания у пациента, нуждающегося в таком лечении, который предусматривает введение такому пациенту терапевтически эффективного количества соединения формулы I.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОГИДРОКСИКАРБАМАЗЕПИН ДЛЯ ПРИМЕНЕНИЯ В ПОЛУЧЕНИИ ЛЕКАРСТВЕННОГО СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ АФФЕКТИВНОГО И СВЯЗАННОГО С ВНИМАНИЕМ РАССТРОЙСТВА И НЕВРОПАТИЧЕСКОЙ БОЛИ | 2002 |
|
RU2353365C2 |
| ПРОИЗВОДНОЕ ПИРРОЛИДИНАЦЕТАМИДА ИЛИ ЕГО КОМБИНАЦИЯ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ ЦНС | 2000 |
|
RU2261093C2 |
| АНТАГОНИСТЫ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ (MGLUR5) ДЛЯ ЛЕЧЕНИЯ БОЛИ И СОСТОЯНИЯ ТРЕВОГИ | 1999 |
|
RU2232017C2 |
| ИНГИБИТОРЫ ЦИСТАТИОНИН-Г-ЛИАЗЫ (CSE) | 2013 |
|
RU2640418C2 |
| ЛИГАНДЫ СИГМА-РЕЦЕПТОРОВ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ БОЛИ, ВЫЗВАННОЙ ХИМИОТЕРАПИЕЙ | 2010 |
|
RU2543382C2 |
| НОВОЕ ПРОФИЛАКТИЧЕСКОЕ И/ИЛИ ЛЕКАРСТВЕННОЕ СРЕДСТВО ПРОТИВ НЕВРОПАТИЧЕСКОЙ БОЛИ | 2008 |
|
RU2462459C2 |
| КОМПОЗИЦИИ (-)-E-10-OH-NT И СПОСОБЫ ИХ СИНТЕЗА И ПРИМЕНЕНИЯ | 2008 |
|
RU2469715C2 |
| ЭСЛИКАРБАЗЕПИНА АЦЕТАТ И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2005 |
|
RU2417085C2 |
| НОВОЕ ПРИМЕНЕНИЕ ОБЪЕДИНЕННЫХ АГОНИСТОВ 5-HT И ИНГИБИТОРОВ ОБРАТНОГО ЗАХВАТА СЕРОТОНИНА | 2001 |
|
RU2302243C2 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ТРАДИПИТАНТОМ | 2018 |
|
RU2797248C2 |
Изобретение относится к химико-фармацевтической промышленности и касается применения фторированых триазолов формулы I для лечения боли и аффективных нарушений и расстройств внимания. Вещества обладают повышенной эффективностью и биодоступностью. 4 с. и 1 з.п. ф-лы
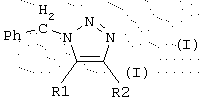
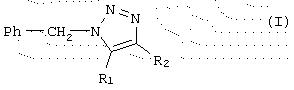
где Ph обозначает ортофторированный фенильный радикал, который может быть дополнительно замещен 1 или 2 атомами галогена, выбранными из атомов фтора и хлора;
R1 обозначает водород, карбамоил, N-(С2-С5)алканоилкарбамоил или N,N-ди(С1-С4)алканоилкарбамоил, и R2 обозначает карбамоил, N-(C2-С5)алканоилкарбамоил или N,N-ди(С1-С4)алкилкарбамоил,
в качестве лекарственного средства для лечения невропатической боли и аффективных расстройств и расстройств внимания.
| 0 |
|
SU199262A1 | |
| US 4789680 A, 06.12.1988 | |||
| ПРОИЗВОДНЫЕ ДЕКАГИДРОИЗОХИНОЛИНОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1993 |
|
RU2117661C1 |
Авторы
Даты
2004-10-27—Публикация
2000-02-28—Подача