Изобретение относится к медицине и касается применения полиуронидных кислот или их солей в качестве средств заместительной терапии заболеваний, связанных с нарушением метаболических процессов, в частности реакций конъюгации с глюкуроновой кислотой. К такого рода заболеваниям можно отнести гемолитическую болезнь, печеночную кому, печеночно-клеточную недостаточность, гепатиты, желтухи и др.
Существенное место в метаболизме различных веществ в организме принадлежит конъюгационным механизмам. Различные вещества конъюгируют с различными эндогенными соединениями (глюкуроновая, серная кислоты и др.). Конъюгация с глюкуроновой кислотой является наиболее важным механизмом конъюгации у человека и включает два основных этапа: биосинтез коферментного комплекса глюкуроновой кислоты и перенос с этого комплекса глюкуронидной части на инактивируемое вещество. Примером такой конъюгации может служить конъгация билирубина:
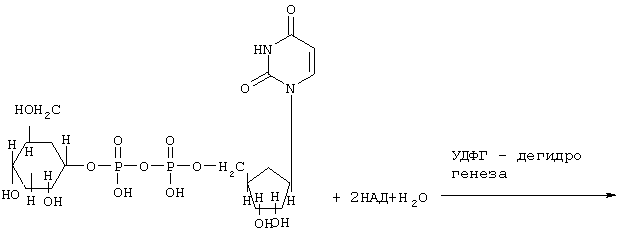 Уридиндифосфат-α-D-глюкоза (УДФГ)
Уридиндифосфат-α-D-глюкоза (УДФГ)
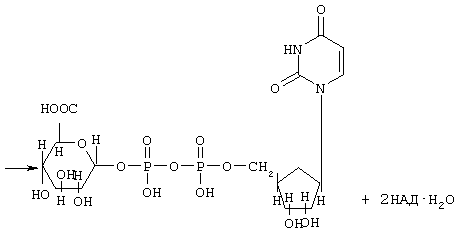
Уридиндифосфат-α-D-глюкороновая кислота
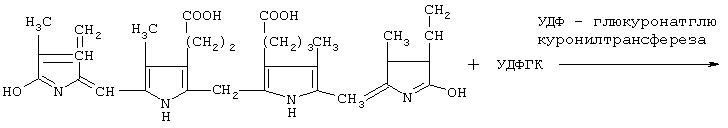
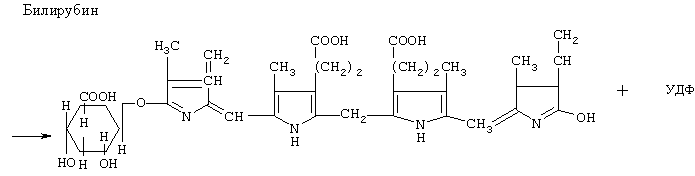
Глюкуронид билирубина (р-конфигурация) (Василенко Ю.К. Биологическая химия. - М.: ВШ, 1978. - С.370-371; Балаховский С.Д., Балаховский И.С. Методы химического анализа крови. - М.: Медгиз, 1953. - С.588).
Важная физиологическая роль образования глюкуронидов (гликозидов β-D-глюкуроновой кислоты) связана с тем, что эта реакция является одной из основных реакций конъюгации, ведущих к обезвреживанию и выведению лекарственных и токсичных веществ и некоторых метаболитов. К ним относятся как многие нормальные метаболиты (билирубин, стероиды, тироксин и др.), так и чужеродные вещества (продукты метаболизма микрофлоры кишечника, лекарственные средства, химические загрязнения окружающей среды). В основе патогенеза гемолитической болезни новорожденных лежит недостаточность глюкуронилтрансферазы, катализирующей образование глюкуронида билирубина, т.е. той формы билирубина, которая выводится из организма; в результате этой энзимопатии билирубин накапливается в крови и тканях. Патогенез симптомов печеночно-клеточной недостаточности и печеночной комы связан с отравлением организма токсичными веществами вследствие нарушения механизма реакций обезвреживания в печени, в частности реакций образования глюкуронидов (Большая медицинская энциклопедия. - М.: Сов. Энциклопедия, 1976. - Т.4. - Изд.3. - С.325).
β-Д-Глюкуроновая кислота является эндогенным веществом, т.е. веществом, образующимся в организме человека, в результате ферментативного окисления глюкозы.
Из лекарственных препаратов, содержащих глюкуроновую кислоту, известен только один препарат - хонсурид (Chonsuridum) - препарат, получаемый из трахей крупного рогатого скота (Машковский М.Д. Лекарственные средства: В 2-х т. - Т.2. - 10-е изд., стер. - М.: Медицина, 1986. - С.156). Действующим веществом хонсурида является хондроитинсерная кислота, построенная из молекул N-ацетилгалактозамин-6-сульфата и глюкуроновой кислоты. Данное средство близко к заявляемому и выбрано за прототип. Недостатками данного препарата являются: 1) невозможность его применения для реакций конъюгации, способствующих обезвреживанию и выделению различных метаболитов из организма, т.к. в хондроитинсульфате глюкуроновая кислота связана с N-ацетилгалактозамин-6-сульфатом очень прочной β(1→4)-гликозидной связью, а для участия в реакции конъюгации глюкуроновая кислота должна быть связана в УДФГК (комплекс с макроэргической связью); 2) невозможность применения хонсурида внутрь, т.к. он наряду с гиалуроновой кислотой участвует в построении основного вещества соединительной ткани.
По химической структуре родственными глюкуроновой кислоте соединениями являются полиурониды: пектины, альгинаты. Пектины представляют собой биополимеры, состоящие из остатков D-галактуроновой кислоты, соединенных между собой α(1→4)-гликозидными связями. Полигалактуроновая кислота частично этерифицирована метанолом, что способствует растворению пектина в воде (Комиссаренко С.Н., Спиридонов В.Н. Пектины - их свойства и применение. Обзор. / Растит. ресурсы, 1998. - Т.34. - Вып.1. - С.111-119). Альгиновые кислоты представляют собой гетерополиурониды, молекулы которых построены из остатков β-D-маннуроновой и α-L-гулуроновой кислот, связанных в линейные цепи 1-4-гликозидными связями. Т.к. альгиновые кислоты мало растворимы в воде, а их натриевые соли легко растворимы в воде, то чаще всего используются последние (Хим. энциклопедия. - М.: Науч. изд-во “Большая Российская энциклопедия”, 1998. - Т.1. - С.192-193). Химические формулы мономеров полиуронидов (Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М.: Медицина, 1985. - С.352-354, 375-376) приведены ниже:
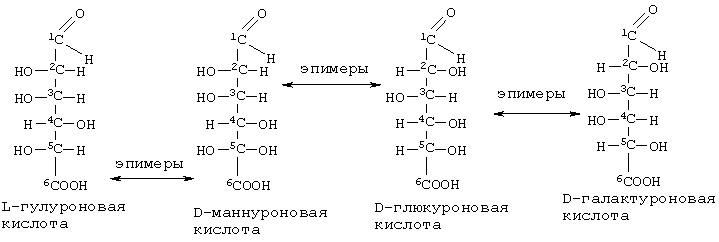
Как видно из приведенных химических формул гексуроновых кислот, глюкуроновая и галактуроновые кислоты являются эпимерами по гидроксильной группе у С4; глюкуроновая и маннуроновая кислоты - эпимеры по гидроксильной группе у С2, а гулуроновая и маннуроновая кислоты - эпимеры по гидроксилу у С5.
Однотипное строение упомянутых выше гексуроновых кислот позволило предположить возможность замены глюкуроновой кислоты в реакциях конъюгации на другие уроновые кислоты или их соли экзогенного происхождения. В качестве конъюгирующих веществ нами были выбраны свекловичный пектин (СП) со степенью этерификации полигалактуроновой кислоты 40,4% и альгинат натрия (АН), выделенный из ламинарии сахаристой.
Цель изобретения - изучение возможности применения растительных полиуронидов в качестве конъюгирующих веществ вместо глюкуроновой кислоты при нарушении биосинтеза или обмена последней в организме человека.
Известны различные факторы, препятствующие протеканию реакций конъюгирования с глюкуроновой кислотой: а) блокирование ионами тяжелых металлов глюкуроновой кислоты, глюкозо-1-фосфата (исходное вещество для синтеза УДФГ). Соединения тяжелых металлов блокируют функциональные группы (карбоксильные, сульфгидрильные, фосфорные, аминные и др.) биомолекул, образуя соединения, лишенные многих физико-химических и биологических свойств, нарушая тем самым метаболизм вообще и глюкуронидную конъюгацию, в частности (Неотложная помощь при острых отравлениях. Справочник по токсикологии. / Под ред. С.Н.Голикова. - М.: Медицина, 1978. - С. 214-215); б) ингибирование фермента УДФ-глюкуронилтрансферазы и других ферментов ионами тяжелых металлов, парахлормеркуриебензоатом (Большая медицинская энциклопедия), что тормозит перенос глюкуронидной части с УДФГК на инактивируемое вещество и вызывает отравление организма токсичными веществами вследствие накопления последних в крови и тканях; в) генетические дефекты ферментов (Биохимия человека. / Марри Р., Греннер Д., Мейес П., Родуэлл В. - М.: Мир, 1993. - В 2-х т. - Т.1. - 382 с.).
Поставленная цель достигается тем, что сначала создается модель нарушения метаболических процессов путем ежедневного перорального введения белым крысам-самцам раствора ацетата свинца (II) в дозе 45 мг/кг в течение недели, а затем ежедневно перорально в течение трех месяцев животным вводится раствор СП или АН в дозе 500 мг/кг. У животных на протяжении всего эксперимента изучалось содержание гексуроновых кислот и билирубина (нормального метаболита для организма человека) в сыворотке крови и моче. Для выявления влияния экзогенных полиуронидов на метаболизм ксенобиотиков, в частности аспирина, животным после недельного введения ацетата свинца (II) и месячного введения полисахаридов ежедневно в течение недели после еды перорально вводят аспирин в дозе 30 мг/кг в виде взвеси с водой объемом 5 мл. В качестве сравнения служила группа интактных животных.
Содержание гексуроновых кислот в биологическом материале определено после кислотного гидролиза биосубстрата по реакции с карбазолом в сернокислой среде путем измерения светопоглощения окрашенного в розово-малиновый цвет продукта реакции при длине волны 530 нм (Методы исследований в профпатологии (биохимические). Руководство для врачей. / Архипова О.Г., Шацкая М.М., Семенова Л.С. и др. / Под ред. О.Г.Архиповой. - М.: Медицина, 1988. - 203 с.).
Обнаружение билирубина в моче проведено по пробе Розина, основанной на образовании из билирубина под действием иода биливердина, окрашенного в зеленый цвет (Строев Е.А., Макарова В.Г. Практикум по биологической химии. - М.: ВШ, 1986. - С.188).
Количественное содержание прямого билирубина в сыворотке крови определено методом разведения, основанным на взаимодействии диазореактива с билирубином в самой разбавленной сыворотке крови (Балаховский С.Д., Балаховский И.С. Методы химического анализа крови. - М.: Медгиз, 1953. - С.586).
Содержание оксибензойной кислоты (аспирина) в биологических жидкостях определено методом кислотно-основного титрования (Государственная фармакопея СССР. - М.: Медицина, 1968. - Х изд. - Ст.3).
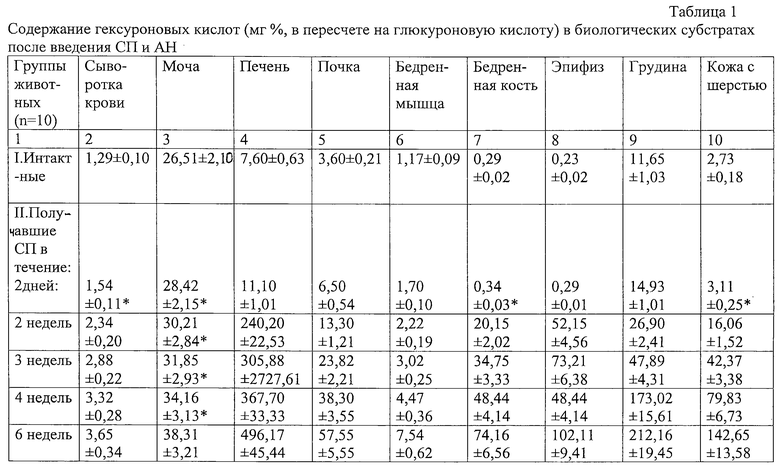
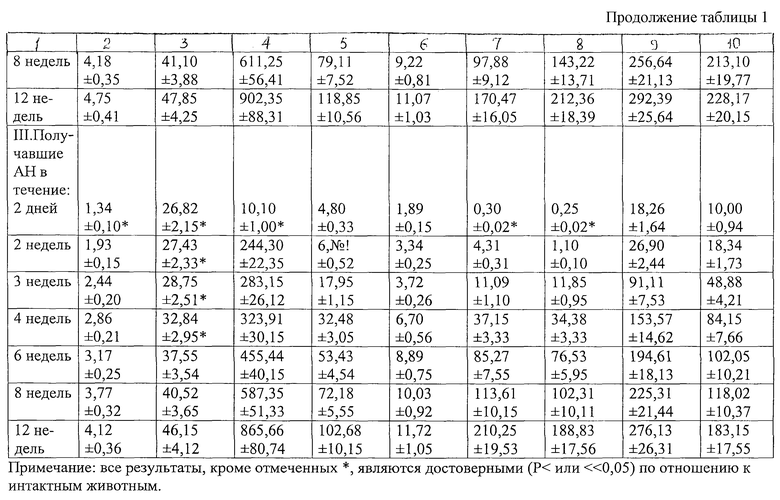
Предварительно (до создания модели нарушения метаболических процессов) было изучено влияние СП и АН на уровень гексуроновых кислот в различных биологических системах и органах животных. Полученные результаты приведены в таблице 1 (см. в конце описания).
Приведенные в таблице 1 данные свидетельствуют о том, что в результате перорального введения животным СП и АН уровень гексуроновых кислот во всех биосубстратах повышается: наиболее быстро он повышается в сыворотке крови и мягких тканях, медленно - в костной ткани. Увеличение содержания гексуроновых кислот, особенно в сыворотке крови, в печени позволяет предположить возможность участия вводимых полиуронидов в метаболических процессах.
При определении наличия билирубина в моче по пробе Розина в каждой группе животных на протяжении всего периода исследования реакция на билирубин была отрицательной, что свидетельствовало о нормальном протекании метаболических процессов в печени.
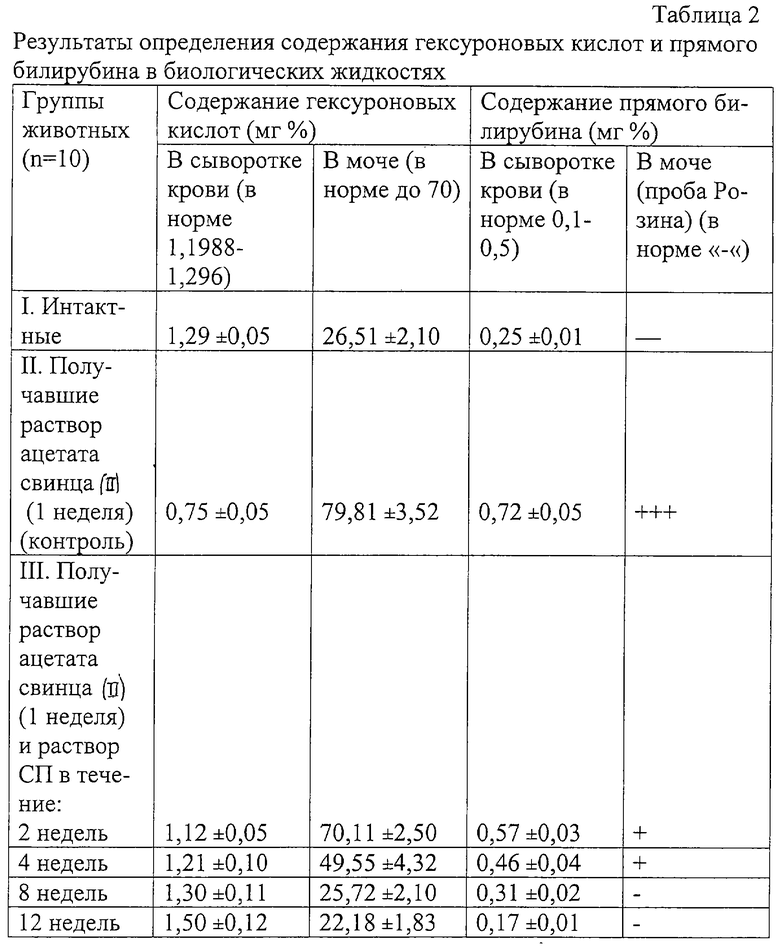
Для создания модели нарушения метаболических процессов белым крысам-самцам линии Вистар массой 170-220 г вводили ежедневно в течение 7 дней перорально раствор ацетата свинца (II) в дозе 45 мг/кг массы тела (в пересчете на свинец), а затем растворы СП или АН в дозах по 500 мг/кг массы тела ежедневно в течение 12 недель. Периодически в крови и моче определяли содержание гексуроновых кислот (в пересчете на глюкуроновую кислоту) и билирубина. Полученные результаты приведены в таблице 2.
Результаты, приведенные в таблице 2, показывают, что после введения животным раствора ацетата свинца (II) в крови и моче увеличивается содержание билирубина, при этом содержание гексуроновых кислот в крови падает, а в моче - растет. По-видимому, это можно объяснить тем, что под влиянием свинца происходит блокирование трансфераз, катализирующих перенос глюкуронидной части с УДФГК на билирубин, т.е. введение свинца нарушает синтез глюкуронида-билирубина, поэтому и в крови, и в моче содержание несвязанного билирубина растет. По этой же причине увеличивается и содержание глюкуроновой кислоты в виде уридиновых коферментов в моче. Уменьшение содержания глюкуроновой кислоты в крови, возможно, происходит за счет связывания ионами свинца карбоксильных групп уроновой кислоты или фосфатных групп глюкозо-1-фосфата на стадии синтеза УДФГ.
На фоне свинцовой патологии последующий длительный прием полиуронидных препаратов приводит к исчезновению в моче билирубина (после 8 недель приема полисахаридов) и уменьшению его содержания в крови до нормальных величин (после 4-х недель приема). При этом содержание гексуроновых кислот в сыворотке крови и моче нормализуется после 4-недельного приема полиуронидов. Благоприятное действие полиуронидных препаратов на метаболизм, в частности билирубина, по-видимому, можно объяснить вовлечением мономерных фрагментов введенных полиуронидных препаратов в процесс конъюгации.
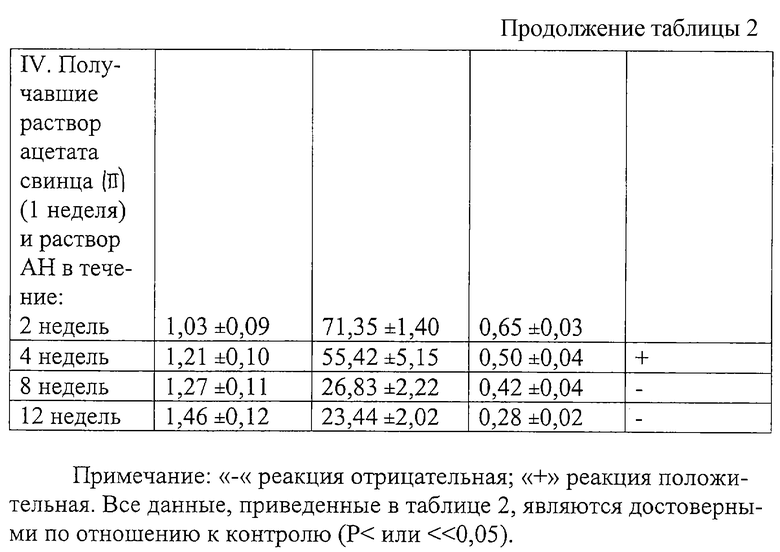
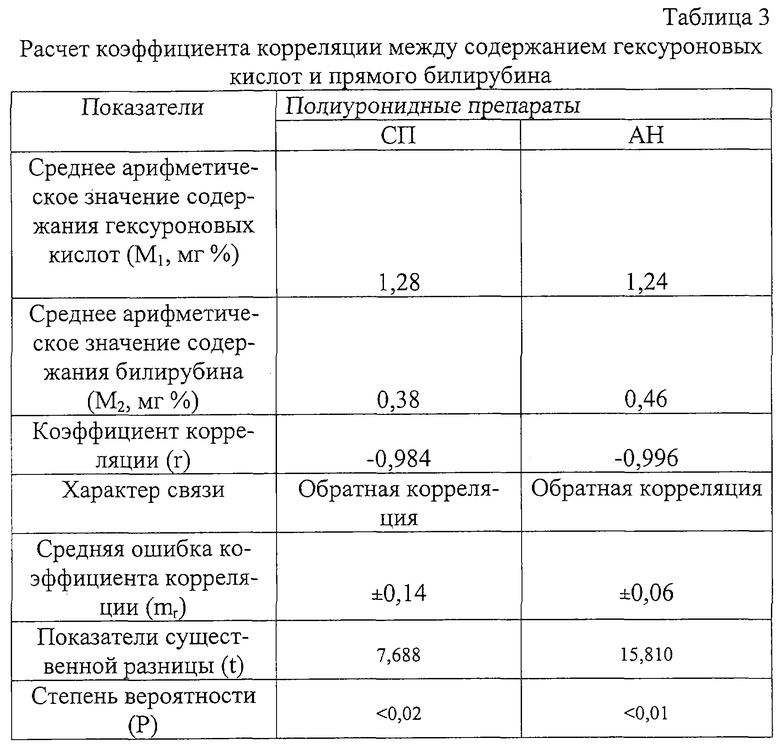
Для установления связи между содержанием гексуроновых кислот и прямого билирубина в сыворотке крови, а также для установления характера зависимости и количественного выражения достоверности связи вычислен коэффициент корреляции (r) между двумя указанными признаками по известной методике (Асатиани B.C. Новые методы биохимической фотометрии. - М.: Наука, 1965. - С. 507-510). Расчет коэффициента корреляции между содержанием гексуроновых кислот и прямого билирубина в сыворотке крови после введения полиуронидных препаратов приведен в таблице 3.
Данные таблицы 3 показывают, что между содержанием гексуроновых кислот после введения полиуронидов и прямого билирубина в сыворотке крови существует связь. Отрицательное значение коэффициента корреляции указывает на обратную корреляцию между рассматриваемыми признаками. Значения коэффициента, очень близкие к единице, свидетельствуют о высокой вероятности наличия связи между показателями в обоих случаях применения полисахаридов.
Установленные степени вероятности показывают, что между содержанием гексуроновых кислот после дачи полиуронидных препаратов и содержанием прямого билирубина в рассматриваемых случаях существует статистически достоверная обратная зависимость. Это подтверждает правильность предположения, что уменьшение содержания билирубина в сыворотке крови явилось следствием увеличения содержания уроновых кислот за счет введения полиуронидных препаратов.
Наряду с нормальными метаболитами, к числу которых относится билирубин, предпринята попытка изучения связи между содержанием гексуроновых кислот после приема полиуронидов и содержанием какого-либо ксенобиотика, метаболизирующегося в организме путем глюкуронидной конъюгации. В качестве такого ксенобиотика был выбран аспирин. В печени он образует конъюгат с глюкуроновой кислотой (Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М.: Медицина, 1985. - С.376).
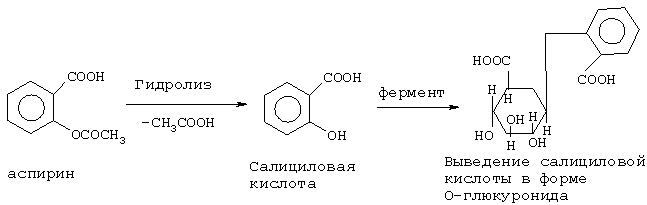
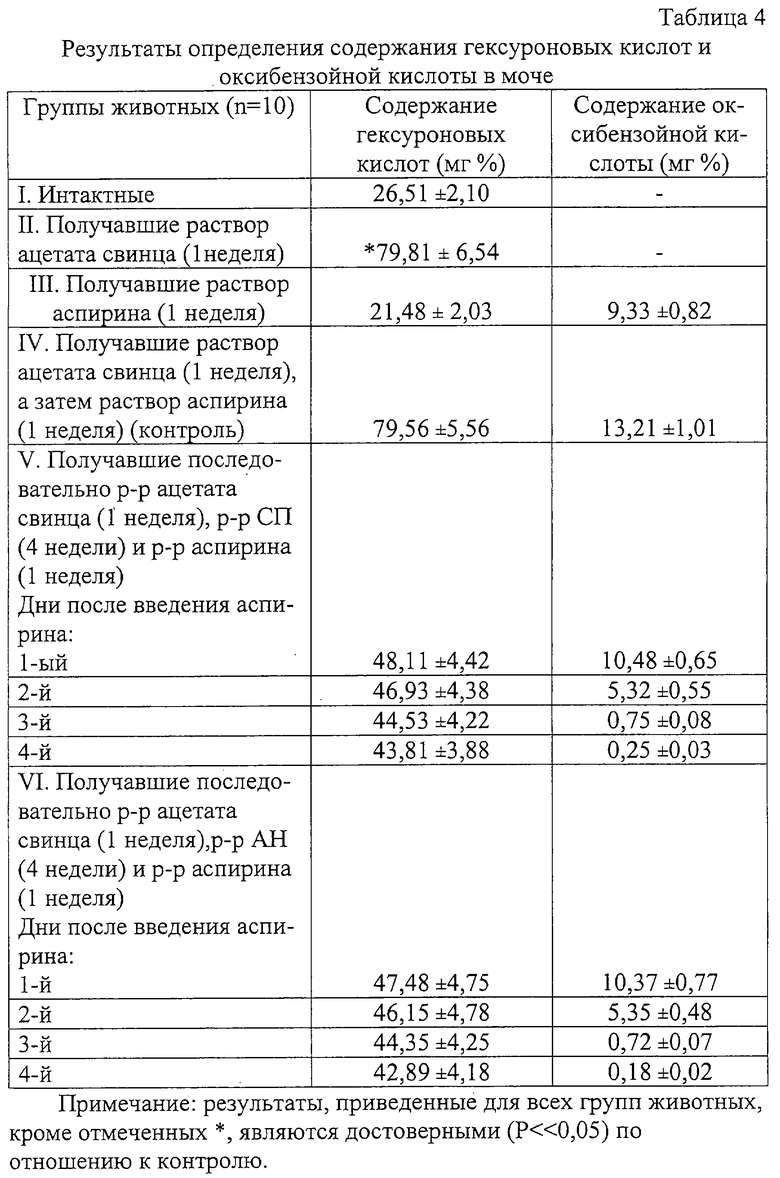
Сначала была создана модель нарушения метаболических процессов путем перорального введения в течение одной недели белым крысам самцам раствора ацетата свинца (II) (как и в вышеописанном случае). Затем на фоне свинцовой патологии одной группе животных перорально в течение недели ежедневно (после еды) вводили с помощью зонда порошок аспирина из расчета 30 мг/кг массы тела в виде взвеси в 5 мл воды. Двум другим группам животных после недельного введения свинца перорально в течение 4-х недель ежедневно вводили растворы СП или АН в дозах по 500 мг/кг массы тела и только потом вводили аспирин (аналогично первой группе животных). В моче животных определяли содержание оксибензойной кислоты методом кислотно-основного титрования (Государственная фармакопея СССР. - М.: Медицина, 1968. - Х изд. - Ст.3). Результаты количественного определения содержания оксибензойной кислоты в моче животных представлены в таблице 4.
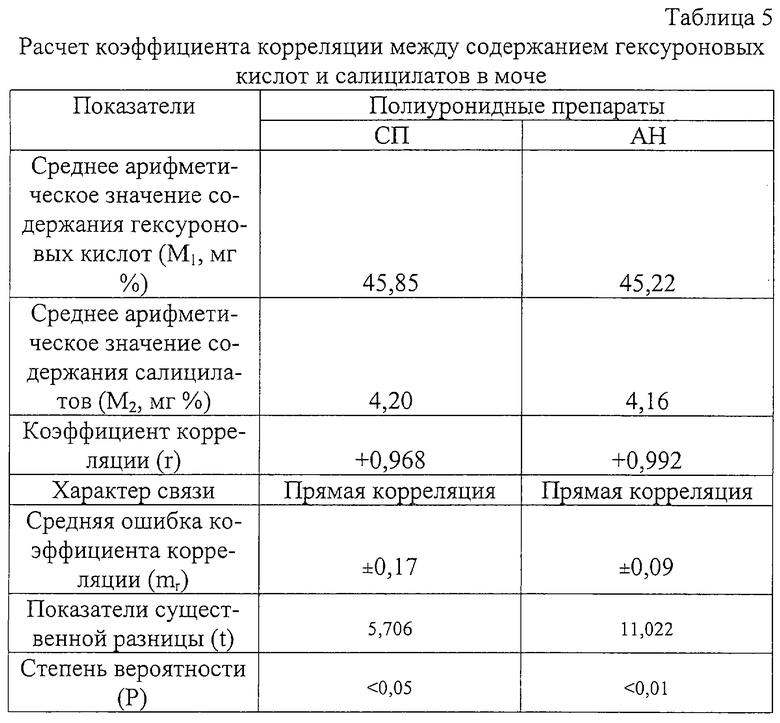
Данные таблицы 4 показывают, что в результате введения аспирина на фоне свинцовой патологии, когда нарушены метаболические процессы, в моче увеличивается содержание свободной, неконъюгированной, оксибензойной кислоты, т.к., по-видимому, из-за ингибирования ионами свинца фермента трансферазы уронидная составляющая не переносится с УДФГК на инактивируемое вещество (салицилаты), что ведет к повышенному содержанию гексуроновых кислот в моче. Предположительно, глюкуроновая кислота заблокирована ионами свинца и не может участвовать в конъюгации метаболитов. Введение аспирина на фоне свинцовой патологии и длительного приема полиуронидов свидетельствует о нормализации метаболических процессов: с уменьшением содержания салицилатов уменьшается и содержание гексуроновых кислот в моче. Чтобы определить наличие связи между двумя признаками (содержание гексуроновых кислот и салицилатов в моче после введения аспирина на фоне свинца и полиуронидов) рассчитан коэффициент корреляции. Результаты расчета приведены в таблице 5.
Данные таблицы 5 показывают, что между содержанием гексуроновых кислот (после введения полиуронидов) и содержанием салицилатов в моче существует связь. Положительное значение коэффициента корреляции указывает на прямую корреляцию между рассматриваемыми показателями. В случае введения АН коэффициент корреляции практически составляет 1 (0,992), что свидетельствует о высокой степени вероятности наличия зависимости между показателями. Это подтверждает правильность предположения, что уменьшение содержания оксибензойной кислоты (салицилатов) в моче явилось следствием уменьшения содержания уроновых кислот за счет введения полисахаридов.
Наряду с эндогенным конъюгирующим веществом - глюкуроновой кислотой - после приема полисахаридных препаратов в биологических органах и системах появляются другие уроновые кислоты (галактуроновая, маннуроновая, гулуроновая). Можно предположить, что либо эти другие уроновые кислоты выполняют такую же роль конъюгирующих веществ, как и глюкуроновая кислота, либо происходит превращение экзогенных уроновых кислот в глюкуроновую, как это наблюдается при ферментативных превращениях, происходящих в растениях (Кретович В.Л. Биохимия растений. - М.: ВШ, 1980. - С.193):
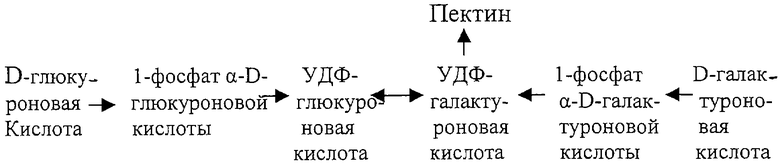
Второе предположение менее вероятно из-за возможного отсутствия соответствующих ферментов в человеческом организме.
Наряду с описанным выраженным биологическим действием применение СП и АН безвредно для человека, т.к. оба полисахарида являются компонентами пищевых продуктов и биосовместимы с организмом.
Изучение “острой” токсичности СП и АН проведено методом Кербера (Сидоров К.К. Методы определения острой токсичности и опасности химических веществ (токсикометрия). - М.: Медицина, 1970) на 20 белых крысах-самцах массой 180-220 г путем перорального введения 5 мл раствора СП или АН в дозе 3500 мг/кг веса тела. После одноразового введения за время наблюдения (в течение 14 дней) гибели животных не отмечалось, что позволило определить LD50 при пероральном введении >3500 мг/кг (для обоих полисахаридов). Согласно классификации токсических веществ (Сидоров К.К., 1970) оба исследованных полисахарида относятся к группе малотоксичных веществ.
Заявляемый способ поясняется следующими примерами.
Пример 1
Навеску ацетата свинца (II) массой 3,5313 г растворяют в 100 мл воды путем перемешивания колбы с раствором на магнитной мешалке, затем раствор количественно переносят в мерную колбу вместимостью 250 мл. Для подавления гидролиза ионов свинца (II) и ацетат ионов к полученному раствору прибавляют несколько капель 0,1 моль/л раствора уксусной кислоты до исчезновения мути. Затем раствор доводят водой до метки. 1 мл приготовленного раствора ацетата свинца (II) содержит 9 мг ионов свинца (II).
Опыты проводили на 60 половозрелых белых крысах-самцах линии Вистар массой 180-220 г, разделенных на 6 групп по 10 животных в каждой. Первая группа животных - интактные - служила сравнением. Остальным группам (II-VI) животных ежедневно в течение 7 дней перорально (с помощью зонда) вводили раствор ацетата свинца (II) объемом 1 мл в дозе 45 мг/кг (в пересчете на свинец). II группа животных служила контролем. Затем III-VI группам животных ежедневно перорально вводили раствор свекловичного пектина (объемом 5 мл) в дозе 500 мг/кг в течение 2 недель (III группа), 4 недель (IV группа), 8 недель (V группа) и 12 недель (VI группа).
Для приготовления раствора пектина отвешивали навеску СП массой 10 г, переносили в коническую колбу вместимостью 1 л и добавляли 500 мл воды, т.е. готовили 2% раствор СП. Для набухания и растворения пектина в воде раствор оставляли на сутки при комнатной температуре.
Все животные в течение эксперимента находились на стандартном режиме питания. У животных всех групп изучали содержание гексуроновых кислот (в пересчете на глюкуроновую кислоту) в сыворотке крови и моче карбазольным методом (Методы исследований в профпатологии (биохимические)...), наличие прямого билирубина в моче по пробе Розина (Строев Е.А., Макарова В.Г. и др.) и содержание прямого билирубина в сыворотке крови (Балаховский С.Д. и др.).
Для получения мочи крысам с помощью зонда вводили внутрижелудочно по 5 мл воды, затем животных отсаживали на сутки в мочесборник. Собранную мочу перед анализом фильтровали через бумажный фильтр.
Для отбора крови животных декапитировали. Собранную кровь отстаивали в холодильнике для отделения сыворотки.
Полученные результаты биохимического анализа биологических жидкостей приведены в таблице 2. Вероятность различий результатов по отношению к контролю не превышает 0,05, что находится в пределах нормы и свидетельствует о статистической достоверности данных.
Пример 2
Проводят аналогично примеру 1, но вместо 2% раствора СП используют 2% раствор альгината натрия (АН).
Для приготовления 2% раствора АН отвешивают навеску АН массой 10 г, помещают в коническую колбу вместимостью 1 л, прибавляют 500 мл воды и раствор перемешивают до растворения АН.
Полученные результаты биохимического анализа сыворотки крови и мочи на содержание гексуроновых кислот и прямого билирубина приведены в таблице 2. Полученные результаты статистически достоверны.
Пример 3
Растворы ацетата свинца (II) и СП готовили как описано в примере 1.
Опыты проводили на 50 крысах-самцах линии Вистар, разделенных на 5 групп по 10 животных в каждой. Первая группа - интактные животные. Остальным группам (II-V, кроме III) животным в течение недели ежедневно перорально вводили раствор ацетата свинца (II) объемом 1 мл, в дозе 45 мг/кг (в пересчете на свинец). Затем IV группе (на фоне свинцовой патологии; контроль) и III группе животных в течение недели ежедневно с помощью зонда после еды перорально вводили порошок аспирина из расчета 30 мг/кг массы тела в виде взвеси в 5 мл воды. Далее V группе животных (на фоне свинцовой патологии) ежедневно перорально вводили 2% раствор СП объемом 5 мл в дозе 500 мг/кг в течение 4-х недель и затем взвесь аспирина объемом 5 мл в дозе 30 мг/кг в течение 1 недели ежедневно после еды.
У животных всех групп по окончании опыта, а у V группы ежедневно в течение 4-х дней после введения аспирина изучали содержание в моче гексуроновых кислот (в пересчете на глюкуроновую кислоту) карбазольным методом (Методы исследований в профпатологии (биохимические)...) и оксибензойной кислоты методом кислотно-основного титрования (Государственная фармакопея СССР...).
Полученные результаты биохимических исследований статистически достоверны и приведены в таблице 4.
Пример 4
Проводят аналогично примеру 3, но вместо 2% раствора СП используют 2% раствор АН (его приготовление описано в примере 2).
Результаты биохимических исследований приведены в таблице 4.
Таким образом, кислые полисахариды, предлагаемые в качестве конъюгирующих веществ, обеспечивают следующий положительный эффект:
1) при введении в организм интактных животных кислых полисахаридов (СП, АН) содержание гексуроновых кислот в биосистемах увеличивается; в мягких тканях увеличение наступает раньше, чем в костной ткани. Увеличение содержания уроновых кислот в сыворотке крови, печени, моче дает возможность предположить участие вводимых полиуронидов вместе с глюкуроновой кислотой в процессах метаболизма, в частности глюкуронидной конъюгации.
2) В результате недельного введения ацетата свинца (II) нарушаются метаболические процессы: содержание гексуроновых кислот в сыворотке крови уменьшается в 1,7 раза, а в моче - увеличивается в 3 раза; содержание свободного билирубина (нормального для организма метаболита) в сыворотке крови увеличивается в 2,9 раза, в моче также появляется билирубин. Возможно, это связано с тем, что ионы свинца (II) блокируют функциональные группы как глюкозо-1-фосфата, УДФ-глюкуроновой кислоты, так и фермента - трансферазы, катализирующей перенос уронидной части с УДФГК на билирубин, в результате чего не образуется конъюгат глюкуронид-билирубин и билирубин в свободном виде находится в моче и в крови. Частично, из-за блокирования ионами свинца (II), УДФ-глюкуроновая кислота не может конъюгировать билирубин. Последующий длительный прием СП и АН нормализует метаболические процессы: после 4 недель приема полисахаридов в сыворотке крови и моче нормализуется содержание гексуроновых кислот, что приводит к нормализации содержания билирубина в крови, а после 8 недель приема полиуронидных препаратов билирубин в моче не обнаруживается. Благоприятное действие полиуронидов на метаболизм билирубина, обычно выводимого из организма в виде конъюгатов с глюкуроновой кислотой, по-видимому, можно объяснить образованием конъюгатов билирубина с кислыми полисахаридами, вводимыми в организм при недостатке глюкуроновой кислоты.
3) Установлена обратная зависимость между содержанием гексуроновых кислот, вводимых в виде СП и АН, и билирубина в сыворотке крови. Коэффициенты корреляции соответственно для СП и АН составляют -0,984 и -0,996, это свидетельствует о высокой степени вероятности наличия связи между содержанием гексуроновых кислот и билирубина в крови.
4) Установлено благоприятное действие СП и АН на метаболизм не только нормальных метаболитов, но и на метаболизм ксенобиотиков, в частности аспирина. Введение животным аспирина на фоне свинцовой патологии способствует увеличению содержания в моче неконъюгированной оксибензойной кислоты и глюкуроновой кислоты в сравнении с моделью без патологии соответственно в 1,4 и 3,7 раза. Если аспирин вводить после недельного приема свинца и 4-х недельного приема полисахаридных препаратов, то метаболические процессы соответствуют норме. Следовательно, полисахаридные препараты включаются вместо глюкуроновой кислоты в цикл конъюгации с аспирином, при этом в моче снижаются и содержание гексуроновых кислот, и содержание аспирина.
5) Установлена прямая зависимость между содержанием гексуроновых кислот, вводимыми в виде СП и АН, и содержанием оксибензойной кислоты (аспирина). Коэффициенты корреляции соответственно для СП и АН составляют +0,968 и +0,992, что доказывает с высокой степенью вероятности наличие прямой корреляции между указанными признаками.
6) Кислые полисахариды (СП, АН) умеренно растворимы в воде и поэтому могут вводиться в организм в виде растворов, в т.ч. и инъекционных. Растворы, обладая антимикробным действием, стабильны (Пекто. Натуральный бактерицидный энтеросорбент. / Погорельская Л.В., Трякина И.П., Бунов С.В. Методические рекомендации. - М., 2000. - 16 с.).
7) Являясь компонентами пищевых продуктов (СП получают из отжимов сахарной свеклы, АН - из слоевищ морской капусты) и будучи биосовместимыми с организмом человека, СП и АН характеризуются LD50>3500 мг/кг при пероральном введении.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения и применения биологически активной добавки на основе протеогликанов и гликозаминогликанов | 2019 |
|
RU2738448C2 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ДЕТОКСИЦИРУЮЩЕЙ АКТИВНОСТЬЮ | 2001 |
|
RU2191590C1 |
| СПОСОБ ЛЕЧЕНИЯ РАННИХ СТАДИЙ ОСТЕОАРТРОЗА КОЛЕННОГО СУСТАВА | 2008 |
|
RU2367447C1 |
| Гепатопротекторное средство | 2017 |
|
RU2635762C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГЕПАТОЗАЩИТНЫМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ, И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2009 |
|
RU2406496C1 |
| ГЕПАТОПРОТЕКТОРНОЕ СРЕДСТВО "КАРСИЛИН" | 2002 |
|
RU2205637C1 |
| ПРОДУКТ, СОДЕРЖАЩИЙ ГЛЮКОМАННАН, КСАНТАНОВУЮ КАМЕДЬ И АЛЬГИНАТ ДЛЯ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКИХ НАРУШЕНИЙ | 2011 |
|
RU2553348C2 |
| СПОСОБ ПОДГОТОВКИ БЕРЕМЕННОЙ К РОДАМ | 1992 |
|
RU2014839C1 |
| КОМПЛЕКСНЫЙ АНТИБАКТЕРИАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЖИВОТНЫХ | 2014 |
|
RU2554797C1 |
| СПОСОБ ДИАГНОСТИКИ ВНУТРИУТРОБНОЙ ИНФЕКЦИИ НОВОРОЖДЕННЫХ | 2002 |
|
RU2231791C2 |
Изобретение относится к медицине и касается применения полиуронидных кислот или их солей в качестве средств заместительной терапии заболеваний, связанных с нарушением метаболических процессов, в частности реакций конъюгации с глюкуроновой кислотой (почечная кома, печеночно-клеточная недостаточность, гепатиты, желтухи и др.). Средство заместительной терапии, содержащее уроновые кислоты, отличающееся тем, что в качестве уроновых кислот содержит полигалактуроновую кислоту со степенью этерификации 40,4% (свекловичный пектин) или производную натриевых солей полиманнуроновой и полигулуроновой кислот (альгинат натрия). Средство способствует эффективной защите больных с нарушением метаболических процессов. 5 табл.
Средство заместительной терапии, содержащее уроновые кислоты, отличающееся тем, что в качестве уроновых кислот содержит полигалактуроновую кислоту со степенью этерификации 40,4% (свекловичный пектин) или производную натриевых солей полиманнуроновой и полигулуроновой кислот (альгинат натрия).
| RU 94026096 A1, 10.09.1996 | |||
| ШЕВЦОВА О.И | |||
| и др | |||
| Эффекты препаратов низкоэтерифицированного пектина и альгината кальция при остром токсическом гепатите | |||
| // Человек и лекарство, 1998, №5, с | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| МАЛОВ A.M | |||
| и др | |||
| Эффективность сочетанного применения пектина и альгината натрия при хронической интоксикации ртутью в эксперименте | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Индукционная катушка | 1920 |
|
SU187A1 |
| ШЕВЦОВА О.И | |||
| Влияние альгината кальция и пектина на перекисное окисление липидов при токсическом гепатите | |||
| // Год | |||
| конф | |||
| Ин-та биол | |||
| моря ДВО РАН, 1999, с | |||
| Кулисный парораспределительный механизм | 1920 |
|
SU177A1 |
Авторы
Даты
2004-11-20—Публикация
2003-04-08—Подача