Изобретение относится к области медицины, в частности к иммунологии, и может быть использовано для диагностики аутоиммунного процесса и последующего влияния на данное звено патогенеза за счет возможности выяснения наличия или отсутствия атопического механизма среди других механизмов аутоагрессии, направленный на орган мишень.
От столь разных подходов меняется и терапевтическая тактика. Если речь идет о чужеродных аллергенах, то есть о классической аллергии, то один из закономерных методов лечащего врача - устранение антигенов, предотвращение контакта с ними больного, их уничтожение и наоборот, если речь идет об аутоиммунном процессе, то целью врача становится защита антигена, так как им является необходимый орган.
В настоящее время для определения аутоантител используют различные по чувствительности и специфичности методы, которые не позволяют верифицировать атопический механизм от других механизмов аутоагрессии (см RU 2173464 С1, 10.09.2001).
Наиболее близким аналогом к заявляемому способу является способ определения уровня аутоантител, в котором проводят выявление взаимодействия аутоантигенов с аутоантителами, идентификацию и определение уровня циркулирующих аутоантител осуществляют с помощью меченого конъюгата фирмы Amersham (биотинилированные человеческие анти-IgG и авидин-пероксидаза) методом твердофазного иммуноферментного анализа (см. Сидорик Л.Л. и др. Иммунный ответ на некоторые внутриклеточные антигены у больных дилатационной кардиомиопатией (http://www.rql.kiev.ua/cardio j/2000/3/ryabenko.htm. 1999 год).
Способ позволяет решать задачу по определению аутоантител, где в качестве конъюгата использовались конъюгаты к антителам классов, считающихся классическими для аутоиммунных синдромов, но не позволяет верифицировать атопическое звено патогенеза аутоагрессии на страдающий орган - мишень за счет определения уровня антигенспецифического IgE.
Целью настоящего изобретения является разработка неиновазивного способа, позволяющего верифицировать атопический компонент аутоагрессии на страдающий орган - мишень. Разработанный способ реализуется за счет определения уровня антигенспецифического IgE и позволяет реально влиять на течение аутоиммунного процесса. Это достигается тем, что для определения уровня циркулирующих аутоантител в биологических жидкостях проводят выявление взаимодействия аутоантигенов с аутоантителами с помощью конъюгата, в кчестве которого используют меченые для последующей идентификации антитела, комплементарные эпсилон-цепям иммуноглобулина Е производства ЦНИРРИ, Санкт-Петербург, РФ. Методика получения антител приведена в публикации Bohn A, Konig W. Generation of monoclonal murine anti-DNP-IgE, IgM and IgG1 antibodies: biochemical and biological characterization // Immunology. 1982 Oct; 47(2):297-3H.
Способ осуществляют следующим образом.
Проводят определение циркулирующих аутоантител IgE класса в биологических жидкостях (крови, лимфе, слюне, ликворе, сперме, желчи, моче, эксудате, отечной жидкости, жидкости глазной камеры и др.) с помощью предварительно меченых для последующей идентификации антител, комплементарных эпсилон-цепям IgE. Для этого используют поликлональные и моноклональные анти-IgE-антитела, входящие в конъюгат, в котором в качестве метки может быть использован флюоресцирующий в ультрафиолетовом свете краситель, изотоп, выявляемый радиометрией и т.д., в зависимости от метода используемого для определения уровня аутоантител.
На первом этапе исследования происходит специфическое связывание аутоантигенов (белков органов-мишеней аутоиммунного процесса) с аутоантителами класса IgE, циркулирующими в исследуемой биологической жидкости. Возникают комплексы антиген-антитело, которые затем выявляют с помощью вышеупомянутого идентифицируемого конъюгата, афинно взаимодействующего с антителами класса IgE, выступающими в данном случае в качестве антигена. Снятие результата реакции осуществляют с помощью высокочувствительных приборов, позволяющих количественно выявить меченый конъюгат и, следовательно, искомые аутоантитела IgE определяемой антигенспецифичности.
Примеры конкретного выполнения способа
Пример 1
1. Больная 72 лет. Госпитализирована на период с 19.11. по 9.01.02 с диагнозом: " Хронический вирусный гепатит В, НВеАв(+), НВ сог (+). Обострение. ИБС. Общий атеросклероз. Диффузный нетоксический зоб. Эутиреоз". За время курации наблюдалась фазовость как в динамике самочувствия больной, так и в характере течения основных гепатологических синдромов. Так, самочувствие больной последовательно ухудшалось до 03.12, после чего тенденция поменялась на противоположную. Основной биохимический маркер синдрома цитолиза - активность фермента АлАТ вначале планомерно возрастала от 1102 е/л 20.11 до 1111 е/л 23.11, затем столь же планомерно снижалась до 397 е/л 04.12 (норма - 11-40 е/л).
Билирубинемия - биохимический маркер синдрома желтухи в динамике первой фазы демонстрировал периоды повышения с незначительным снижением концентрации билирубина (также 23-24.11). В целом, однако, показатель возрастал от 20.11 (376 мкмоль/л) до 3.12 (510 мкмоль/л), а затем планомерно снижался до 199 мкмоль/л 04.01.
Нам трудно указать фактор, повлиявший на перелом тенденции в динамике цитолиза и транзиторном спаде концентрации билирубина 23 - 24.11. Природа же феномена смены фаз в динамике самочувствия и синдрома желтухи очевидна: именно 03.12 больной проводилась повторная процедура плазмофореза. Столь рельефное влияние указанной терапии на состояние пациентки косвенно подтверждает антителозависимый механизм развития ее заболевания. Подтверждение этому мы находим в данных иммунологических исследований.
Кровь для них изымалась 21.11 и 5.01, т.е. соответственно в фазе подъема и спада активности основных гепатологических синдромов, а также на фоне ухудшения и улучшения субъективного самочувствия больной. Уровень циркулирующихся аутоантител определяли твердофазным иммуноферментным анализом с помощью конъюгата, который содержит антитела, комплементарные эпсилон-цепям иммуноглобулина Е. Полученные данные показали, что в вышеобозначенных фазах патологического процесса уровень аутоантител достоверно различен. Для общих антител он составляет в оптической плотности 0,777 и 1,129 для антител класса IgE - 1,483; 0,913 соответственно. Это свидетельствует о том, что у данного больного в патогенезе хронического вирусного заболевания печени имеется аутоиммунный процесс, преимущественно опосредованный не общепринятыми для подобных процессов классами антител, а антигенспецифическими антителами класса IgE.
Пример 2
Больная 43 лет. Госпитализирована на период с 20.05 по 10.06 с диагнозом: “Хронический вирусный гепатит В, HBsAg+, цирротическая стадия, декомпенсация. Портальная гипертензия, отечно-асцитический синдром. Геморрагический синдром. Хронический холецистит, обострение”. По словам районного инфекциониста (лечащий врач), настоящая госпитализация связана с нарастающим в течение недели асцитом, слабостью, одышкой.
В дальнейшем за время госпитализации состояние средней тяжести констатировалось у обследуемой до 26.05 включительно; с 27.05 и до дня выписки (10.06) оно оценивалось как удовлетворительное или относительно удовлетворительное.
Давая общую оценку состояния и самочувствия больной за время госпитального наблюдения, необходимо отметить, что тяжесть ее состояния обуславливалась в основном проявлениями синдрома портальной гипертензии.
Действительно, билирубинемия с момента поступления больной на госпитальном наблюдении не превышала верхней границы области среднетяжелого течения (классификация рижского гепатологического центра, 1984), а затем неуклонно снижалась. Эта динамика не в полной мере отражает динамику тяжести состояния больной.
В еще меньшей степени динамика тяжести отражалась в данных биохимии синдрома цитолиза но АлАТ. Этот параметр колебался около 60 ед/л с волнообразной динамикой самочувствия больной.
Между тем динамика проявлений клинического синдрома портальной гипертензии (слабость, асцит, одышка) послужили причиной и для госпитализации, и для выписки пациентки: по факту исчезновения слабости и одышки, уменьшения асцита дальнейшее пребывание пациентки на госпитальном наблюдении было “признано нецелесообразным (9.06, осмотр заведующего отделением)”. Больная выписана 10.06. Районный инфекционист, наблюдавший больную до госпитализации, также отмечает общее улучшение ее состояния. По данным УЗИ органов брюшной полости от 3.06 имеет место формирование микронодулярного цирроза печени с портальной гипертензией IV.
Таким образом, в отличие от предыдущего случая гепатологический ауто-иммунный процесс может повлиять в основном на тяжесть течения синдрома портальной гипертензии. Было проведено определение уровня циркулирующих аутоантител радиоиммунным методом с помощью конъюгата, который содержит антитела, комплементарные эпсилон-цепям иммулоглобулина Е. При этом уровни антител к f-протеину как общих, так и принадлежащих классу IgE достоверно различны и составляют 1,025; 0,94 и 0,185; 0.09 соответственно. Полученные данные свидетельствуют о том, что у данной больной в патогенезе хронического вирусного заболевания печени имеется аутоиммунный процесс наряду с общепринятыми для подобных процессов классами антител, опосредованный антигенспецифическими антителами класса IgE.
Пример 3
Больной 19 лет. Обследовался и лечился амбулаторию. В течение октября 2002 года наблюдался на поликлиническом отделении городскою гепатологического центра с основным диагнозом: “Хронический вирусный гепатит В. HBsAg +. HBeAg +. PCR HBV +.” Кровь для иммунологических исследований изымалась 11.10.02 и 23.10.02. В анамнезе у больного (декабрь 2001 года) госпитальное лечение в гепатологическом центре по поводу впервые выявленного вирусного гепатита В с последующим наблюдением у районного инфекциониста по месту жительства и в поликлиническом отделении гепатологического центра. До августа 2002 года у пациента сохранялась цитолитическая активность с цифрами АлАТ, в 3-4 раза превышающими нормальные. На момент настоящего обследования у больного пальпаторно отмечалась неярко выраженная гепатомегалия (+1 см).
Анализируя данные биохимического обследования, мы пришли к очевидному выводу, что у больного на момент наблюдения имел место равномерный рост патологической активности показателей, маркирующих активность основных гепатологических синдромов, таких как синдром желтухи и цитолитический синдром. Указанному равномерному росту биохимических показателей соответствует также неярко выраженная клиническая активность, проявляющаяся нетяжелой гепатомегалией. То есть и по клиническим, и по лабораторным данным есть основания говорить об обострении хронического вирусного заболевания печени. Проведенные иммунологическое исследование биологической жидкости желчи заявленным способом показали, что этому обострению соответствует и, очевидно, в немалой степени обуславливает его рост интенсивности аутоиммунного гепатологического синдрома, проявляющийся соответствующим колебанием уровня антител к f-протеину общих и циркулирующих аутоантител класса IgE, при этом оптическая плотность составляет 0,355: 0,525 и 0,155: 0.365 соответственно. Полученные данные свидетельствуют о том, что у данного больного в патогенезе хронического вирусного заболевания печени имеется аутоиммунный процесс наряду с общепринятыми для подобных процессов классами антител, опосредованный антигенспецифическими антителами класса IgE.
В целом из клинических случаев №№1-3 очевидна актуальность исследования уровня циркулирующих аутоантител в сыворотке крови на разных этапах и при различных ведущих синдромах изучаемого заболевания у разных статистических групп больных (госпитализированные и амбулаторные больные, больные с впервые выявленным диагнозом и с обострением ранее диагностированного заболевания и т.д.).
Приведенные примеры свидетельствуют о том, что данный способ определения уровня циркулирующих аутоантител в биологических жидкостях (в частности, в крови и желчи больных) может быть использован в диагностике аутоиммунного процесса и, кроме того, реально влиять на данное звено патогенеза. Научная и практическая медицина в течение десятилетий имела дело с IgE-индуцированными эффекторами анафилаксии. Перенесение методов, выработанных для борьбы с ними, в сферу лечения аутоиммунных компонентов патогенеза при заболеваниях различной этиологии может оказать существенную помощь в их эффективной терапии.
Для более широкой апробации метода было также исследовано 10 образцов другой биологической жидкости, конкретно отечной жидкости больных, скончавшихся от хронического вирусного гепатита В (см. таблицу).
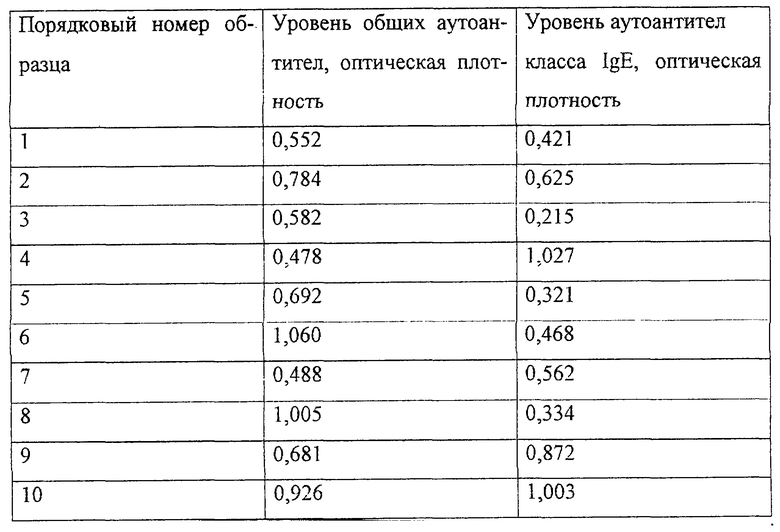
Полученные данные свидетельствуют о том, что определение уровня циркулирующих аутоантител в биологических жидкостях позволяют привязать уровень антител класса IgE к имеющемуся у пациента патологическому процессу и вычленить в патогенезе данного процесса атопический механизм.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ АУТОАНТИТЕЛ, СПЕЦИФИЧНЫХ К F-ПРОТЕИНУ ПЕЧЕНИ ЧЕЛОВЕКА, В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ЧЕЛОВЕКА, СОДЕРЖАЩИХ СПЕЦИФИЧНЫЕ АУТОАНТИТЕЛА | 2003 |
|
RU2236686C1 |
| СПОСОБ ОЦЕНКИ АУТОИММУНИТЕТА К АНТИГЕНУ ПЕЧЕНИ ЧЕЛОВЕКА | 2005 |
|
RU2293335C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ВИРУСНОГО ЭНЦЕФАЛИТА | 2003 |
|
RU2235328C1 |
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННЫХ ПОРАЖЕНИЙ ПЕЧЕНИ У БОЛЬНЫХ ХРОНИЧЕСКИМИ ГЕПАТИТАМИ | 2003 |
|
RU2247387C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ДИФФУЗНЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2001 |
|
RU2243011C2 |
| СПОСОБ ВЫЯВЛЕНИЯ АУТОАНТИТЕЛ В СЫВОРОТКЕ КРОВИ, АССОЦИИРОВАННЫХ С АУТОИММУННЫМ ПОЛИГЛАНДУЛЯРНЫМ СИНДРОМОМ I ТИПА, НА ГИДРОГЕЛЕВОМ БИОЧИПЕ | 2021 |
|
RU2781976C2 |
| АГЕНТЫ, УМЕНЬШАЮЩИЕ КОЛИЧЕСТВО В-КЛЕТОК, ТАКИЕ КАК АНТИТЕЛА ПРОТИВ CD20 ИЛИ ИХ ФРАГМЕНТЫ, ДЛЯ ЛЕЧЕНИЯ СИНДРОМА ХРОНИЧЕСКОЙ УСТАЛОСТИ | 2009 |
|
RU2519229C2 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЭКССУДАТИВНЫХ РЕАКЦИЙ, РАЗВИВАЮЩИХСЯ В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ ПОСЛЕ ИМПЛАНТАЦИИ ИСКУССТВЕННОГО ХРУСТАЛИКА | 2008 |
|
RU2381775C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2014 |
|
RU2566723C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНДЕКСА АВИДНОСТИ АУТОАНТИТЕЛ В СЫВОРОТКЕ КРОВИ ЧЕЛОВЕКА НА ГИДРОГЕЛЕВЫХ БИОЧИПАХ | 2023 |
|
RU2818115C1 |
Изобретение относится к области медицины, в частности к иммунологии, и может быть использовано для диагностики аутоиммунного процесса. Сущность способа состоит в том, что проводят определение уровня циркулирующих аутоантител в биологических жидкостях путем выявления взаимодействия аутоантигенов с аутоантителами, последующую идентификацию и определение уровня циркулирующих аутоантител с помощью меченого конъюгата, при этом в качестве конъюгата используют анти-IgE антитела, комплементарные эпсилон-цепям иммуноглобулина Е, конъюгированные с меткой для последующей идентификации. Техническим результатом является разработка способа, обеспечивающего высокую чувствительность и специфичность. 1 табл.
Способ определения уровня циркулирующих аутоантител в биологических жидкостях, включающий выявление взаимодействия аутоантигенов с аутоантителами и последующую идентификацию и определение уровня циркулирующих аутоантител с помощью меченого конъюгата, отличающийся тем, что в качестве конъюгата используют анти-IgE-антитела, комплементарные эпсилон-цепям иммуноглобулина Е, конъюгированные с меткой для последующей идентификации.
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АУТОАНТИТЕЛ К ЛИПОПРОТЕИДАМ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ КРОВИ | 1997 |
|
RU2137134C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАТАЛИТИЧЕСКИХ АУТОАНТИТЕЛ И СПОСОБ ДИАГНОСТИКИ СИСТЕМНЫХ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ С ИХ ИСПОЛЬЗОВАНИЕМ | 2000 |
|
RU2173464C1 |
| Autoantibodies to immunoglobuline | |||
| Vol ed F.Shakib, Monogr in allergy, Vol 2b, Basel ect, Rarges, 1989, p.270-274. | |||
Авторы
Даты
2004-11-20—Публикация
2003-04-14—Подача