Изобретение относится к медицинской промышленности и касается иммуномодулирующего препарата ″ОЛЕТИМ″ и способа его получения.
Известны препараты Т-активин (тактивин), тималин и тимоптин полипептидной природы, выделенные из тимуса крупного рогатого скота и обладающие иммуномодулирующим действием [1].
Т-активин применяется при иммунодефицитных состояниях, нормализует количественные и функциональные показатели Т-системы иммунитета, стимулирует продукцию лимфокинов, в том числе интерферона, а также другие показатели клеточного иммунитета.
Тималин обладает способностью стимулировать иммунологическую реактивность организма, регулирует количество Т- и В-лимфоцитов, стимулирует реакцию клеточного иммунитета и фагоцитоз, усиливает процессы регенерации и кроветворения в случае их угнетения.
Тимоптин по действию аналогичен Т-активину.
Препараты, полученные из тимуса, обладающие иммуномодулирующей активностью, содержат различное количество биологически активных полипептидов различной молекулярной массы (ММ). Так, ММ полипептидов Т-активина находится в пределах от 1,5 до 6,0 кД, MM полипептидов тимоптина находится в пределах от 1,5 до 10 кД.
Способы получения различных иммуномодулирующих препаратов из тимуса включают гомогенизацию исходного сырья, автолиз при пониженных температурах или предварительное обезжиривание, или экстрагирование активных веществ и их очистку с применением чередования различных этапов очистки, включающих фракционирование сернокислым аммонием, ультрафильтрационных и хроматографических методов [2, 3].
Наиболее близкими к заявленному изобретению являются иммуномодулирующий препарат и способ его приготовления из тимуса северного оленя [4, 5].
Способ получения иммуномодулирующего препарата включает измельчение исходного сырья до гомогенной массы, выделение активных веществ экстрагированием в 0,9% растворе натрия хлорида, денатурирование термолабильной фракции нагреванием экстракта и удаление из него термолабильной фракции белков, очистку экстракта от сопутствующих примесей с использованием ультрафильтрационных мембран, задерживающих вещества вначале с молекулярной массой (ММ) более 10,0 кД, а затем более 1,0 кД, разбавление задержанной фракции и добавление в нее стабилизирующего вещества Д-маннита, фильтрацию раствора через стерилизующий фильтр, розлив стерильного раствора во флаконы и лиофилизацию содержимого флаконов [4].
К недостаткам рассматриваемого способа получения препарата следует отнести:
- использование в качестве экстрагента натрия хлорида, не позволяющего полностью экстрагировать биологически активные пептиды (БАП) из измельченной ткани;
- потерю ценного БАП, обладающего иммуномодулирующими свойствами, при удалении из экстракта ультрафильтрацией на мембране, задерживающей вещества с молекулярной массой более 1,0 кД;
- энергоемкость процесса получения препарата из-за использования лиофильного оборудования для высушивания конечного продукта;
- форма выпуска препарата в виде лиофильно высушенного порошка, требующего растворения перед введением, а следовательно, затрат времени на подготовку препарата перед его введением, а следовательно, и увеличение возможности контаминации препарата.
Задачей изобретения является: увеличить выход комплекса БАП; повысить активность иммуномодулирующего препарата, а также разработать инъекционную форму полученного препарата, не требующую дополнительных затрат на ее подготовку перед использованием.
Сущность изобретения.
Иммуномодулирующее средство (препарат ″ОЛЕТИМ″) представляет собой комплекс БАП с молекулярной массой от 10,0 до 0,5 кД, выделенный из тимуса северного оленя и содержащий: тимусный фактор X, тимопоэтины 1 и 2, α1-тимозин, тимусный гуморальный фактор, гемостатический тимусный гормон и сывороточный тимусный фактор, обладающий иммуномодулирующими свойствами, выраженными в обеспечении созревания Т-лимфоцитов, увеличении количества иммуноглобулинов классов lgG, lgM, в усилении бактериальной и фагоцитарной активности макрофагов.
Способ получения препарата ″ОЛЕТИМ″ заключается в том, что тимус северного оленя измельчают до гомогенного состояния, выделение активных веществ проводят экстрагированием гомогената водно-солевым раствором, денатурируют термолабильные вещества нагреванием экстракта в течение 10-20 минут при температуре 70-90°С и удаляют их из экстракта, а очистку экстракта осуществляют последовательной ультрафильтрацией сначала через мембраны, задерживающие вещества с молекулярной массой 10 кД, а затем ультрафильтрат очищают с использованием ультрафильтрационных мембран, задерживающих вещества с молекулярной массой 0,5 кД.
Оптимальный вариант способа заключается в выделении активных веществ экстрагированием водно-солевым раствором, содержащим 5,5 г/л натрия хлорида и 0,42 г/л калия хлорида.
Предложенный иммуномодулирующий препарат ″ОЛЕТИМ″, полученный предложенным способом, применяют в виде инъекционной формы, полученной путем разбавления препарата ″ОЛЕТИМ″ раствором нипагина до содержания в 1 мл.: белка 30-150 мкг и нипагина 0,40-0,60 мг.
Изобретение реализуется следующим образом.
Комплекс биологически активных пептидов (препарат ″ОЛЕТИМ″) из тимуса северного оленя получают измельчением тимуса до гомогенного состояния, выделением активных веществ путем экстрагирования гомогената водно-солевым раствором, содержащим 5,5 г/л натрия хлорида и 0,42 г/л калия хлорида, денатурированием термолабильных веществ нагреванием, удалением коагулята из экстракта и отделением из экстракта биологически активных веществ вначале на мембране, задерживающей вещества с молекулярной массой 10,0 кД, а затем на мембране, задерживающей вещества с молекулярной массой 0,5 кД.
Комплекс биологически активных пептидов с молекулярной массой от 10,0 до 0,5 кД представляет собой иммуномодулирующее средство (препарат ″ОЛЕТИМ″), в состав которого входят такие вещества, как тимусный фактор Х (ММ 9,6 кД), тимопоэтины 1 и 2 (MM 5,5 кД), α1-тимозин (ММ 3,1 кД), тимусный гуморальный фактор (ММ 3,2 кД), гемостатический тимусный гормон (ММ 2,0 кД) и сывороточный тимусный фактор (ММ 0,86 кД), которые оказывают иммуномодулирующее действие на Т-системы иммунитета.
Приготовление инъекционной формы (препарата ″ОЛЕТИМ″) осуществляют путем разбавления полученного комплекса биологически активных пептидов с молекулярной массой 10,0-0,5 кД раствором нипагина до содержания в 1мл: белка 30-150 мкг и нипагина 0,40-0,60 мг.
Затем раствор подвергают стерилизующей фильтрации через мембраны вначале с размером пор 0,45, а затем 0,22 мкм. Полученный стерильный раствор разливают в ампулы по 1-5 мл или во флаконы по 5-10 мл. Ампулы запаивают, а флаконы укупоривают резиновыми пробками, околпачивают алюминиевыми колпачками и обкатывают алюминиевые колпачки на флаконах.
Заявленное изобретение иллюстрируется следующими примерами.
Пример 1. 1,0 кг тимуса, измельченного на волчке с диаметром решетки 3 мм, гомогенизируют в течение 2 минут в 1,5 л водно-солевого раствора, содержащего 5,5 г/л натрия хлорида и 0,42 г/л калия хлорида. Гомогенат заливают 4,5 л водно-солевого раствора и при постоянном перемешивании проводят экстрагирование БАП в течение 1 часа. Экстракт центрифугируют в течение 60 минут при 2500 об/мин. Преципитат декантируют, а супернатант сливают в экстрактор с рубашкой для подачи острого пара (теплоносителя).
При постоянном перемешивании со скоростью мешалки 90 об/мин осуществляют подогрев супернатанта в течение 15 минут до температуры 70°С. При этой температуре супернатант выдерживают в течение 10 минут, далее подачу острого пара прекращают и включают подачу в рубашку реактора охлаждающего раствора. При постоянном перемешивании охлаждают супернатант до температуры 4°С и, после достижении этой температуры, подачу охлаждающего раствора прекращают, мешалку отключают, а супернатант подвергают центрифугированию в течение 45 минут при 2500 об/мин и температуре 4°С. Жировую пленку, образовавшуюся на фугате, и коагулят декантируют, а супернатант осветляют фильтрацией.
Осветленный фильтрат пропускают через мембраны, задерживающие вещества с молекулярной массой более 10,0 кД. Задержанную фракцию утилизируют, а ультрафильтрат пропускают через мембраны, задерживающие вещества с молекулярной массой более 0,5 кД. Ультрафильтрат утилизируют, а в задержанной фракции, представляющей собой комплекс БАП, определяют содержание белка по Лоури. Выход БАП в пересчете на сухое вещество составляет 1,8 г на 1 кг исходного сырья.
По полученным результатам анализа рассчитывают количество воды для инъекций, необходимое для разбавления задерживаемой фракции до концентрации по белку 30-50 мкг/мл. Затем 1/3 часть (от рассчитанного количества) воды для инъекций подогревают до температуры 70°С и в нее добавляют нипагин. Растворение нипагина осуществляют при постоянном перемешивании в течение 20 минут.
В чистый реактор с мешалкой помещают комплекс БАП и при перемешивании со скоростью 100 об/мин к ней добавляют приготовленный раствор нипагина до содержания 0,40-0,60 мг на 1 мл разбавленного раствора. Перемешивание продолжают в течение 15 минут, а затем приготовленный раствор подвергают стерилизующей фильтрации через мембраны с размером пор 0,45 мкм и далее с размером пор 0,22 мкм.
Полученный стерильный раствор с содержанием белка 30-40 мкг/мл и нипагина 0,45 мг/мл разливают в ампулы по 1-5 мл или во флаконы по 5-10 мл. Ампулы запаивают, а флаконы укупоривают резиновыми пробками, околпачивают алюминиевыми колпачками и обкатывают последние на флаконах.
Пример 2. 1,0 кг тимуса, измельченного на волчке с диаметром решетки 5 мм, гомогенизируют в течение 5 минут в 1,5 л охлажденного до 5°С водно-солевого раствора, содержащего 5,5 г/л натрия хлорида и 0,42 г/л калия хлорида. Гомогенат заливают 4,5 л водно-солевого раствора и при постоянном перемешивании проводят экстрагирование БАП в течение часов. Экстракт центрифугируют в течение 60 минут при 2500 об/мин. Преципитат декантируют, а супернатант сливают в экстрактор с рубашкой для подачи острого пара (теплоносителя).
При постоянном перемешивании со скоростью 120 об/мин осуществляют подогрев супернатанта в течение 45 минут до температуры 90°С. При этой температуре супернатант выдерживают в течение 20 минут, далее прекращают подачу острого пара и включают подачу в рубашку реактора охлаждающего раствора. При постоянном перемешивании с той же скоростью мешалки супернатант охлаждают до температуры 10°С и, после достижении этой температуры, подачу охлаждающего раствора прекращают, мешалку отключают, а супернатант подвергают центрифугированию в течение 60 минут при 2500 об/мин и температуре 10°С. Жировую пленку, образовавшуюся на фугате, и коагулят декантируют, а супернатант осветляют фильтрацией.
Осветленный фильтрат пропускают через мембраны, задерживающие вещества с молекулярной массой более 10,0 кД. Полученную задержанную фракцию утилизируют, а ультрафильтрат пропускают через мембраны, задерживающие вещества с молекулярной массой более 0,5 кД. Ультрафильтрат утилизируют, а в задерживаемой фракции определяют содержание белка по Лоури. Выход БАП составляет 1,85 г на 1 кг исходного сырья.
По полученным результатам анализа рассчитывают количество воды для инъекций, необходимое для разбавления задерживаемой фракции до концентрации по белку 100-150 мкг/мл. Затем 1/3 часть (от рассчитанного количества) воды для инъекций подогревают до температуры 90°С, и в нее добавляют нипагин, чтобы в конечном растворе концентрация нипагина составила 0,60 мг на 1 мл разбавленного раствора. Растворение нипагина осуществляют при постоянном перемешивании в течение 40 минут, после чего в раствор вводят оставшуюся часть воды для инъекций.
В чистый реактор с мешалкой помещают комплекс БАП и при перемешивании со скоростью 150 об/мин к ней добавляют приготовленный раствор нипагина до содержания 0,60 мг на 1 мл разбавленного раствора. Перемешивание продолжают в течение 30 минут, а затем приготовленный раствор подвергают стерилизующей фильтрации через мембраны с размером пор 0,45 мкм и далее с размером пор 0,22 мкм.
Полученный стерильный раствор, имеющий содержание белка 100-150 мкг/мл и нипагина 0,60 мг/мл, разливают в ампулы по 1-5 мл или во флаконы по 5-10 мл. Ампулы запаивают, а флаконы укупоривают резиновыми пробками, околпачивают алюминиевыми колпачками и обкатывают последние на флаконах.
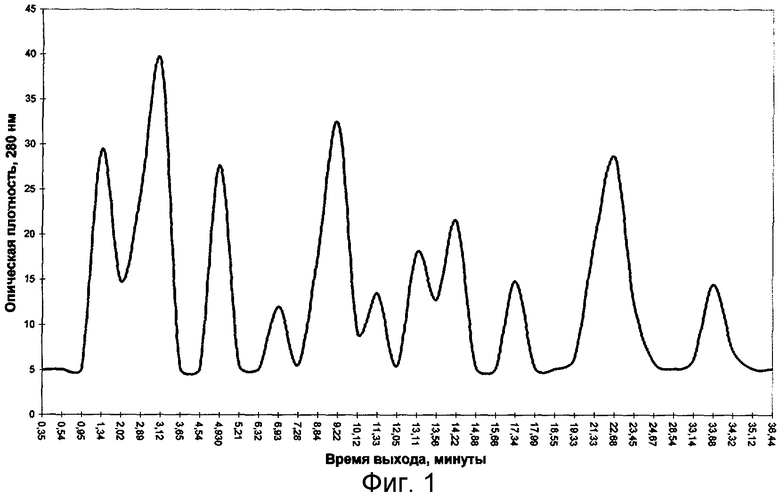
Состав препарата ″ОЛЕТИМ″ по молекулярной массе определяют методом высокоэффективной жидкостной хроматографии (ВЭЖХ) (фиг.1). При проведении ВЭЖХ, по времени выхода фракций из колонки, устанавливают наличие в комплексе БАП идентифицированных веществ с определенной молекулярной массой (тимусный фактор X, тимопоэтины 1 и 2, α1-тимозин, тимусный гуморальный фактор, гемостатический тимусный гормон и сывороточный тимусный фактор). Из фиг.1 следует: пик, по времени выхода соответствующий 33 минуте, идентифицируется как сывороточный тимусный фактор, пик, по времени выхода соответствующий 20 минуте, идентифицируется как гемостатический тимусный гормон, а пик, соответствующий по времени выхода 2 минуте, - как тимусный фактор X.
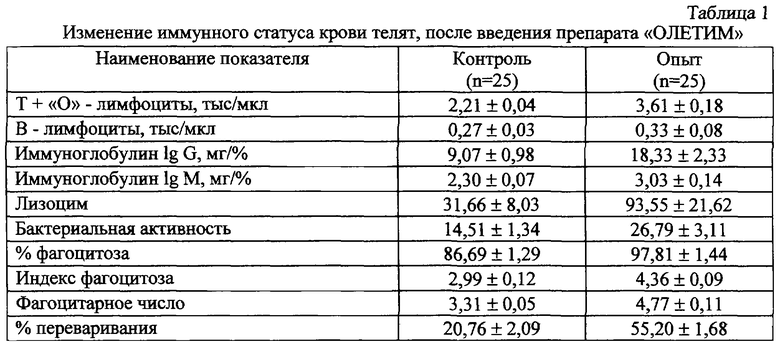
Влияние комплекса БАП на иммунологический статус крови было проверено на телятах в возрасте 6 месяцев. Изменения показателей иммунного статуса крови телят через 2 недели после введения препарата ″ОЛЕТИМ″ по сравнению с контрольной партией представлены в таблице 1. При этом оценку иммунологического статуса проводили по стандартным методикам [6].
Результаты испытаний (табл.1) показали, что после введения телятам комплекса БАП с молекулярной массой от 10,0 до 0,5 кД в крови наблюдается достоверное увеличение количества Т+″О″-лимфоцитов и иммуноглобулинов классов lgG и lgM, бактериальной и фагоцитарной активностей и существенное увеличение показателя переваривания. Кроме того, выявлена некоторая тенденция к увеличению показателя В-лимфоцитов.
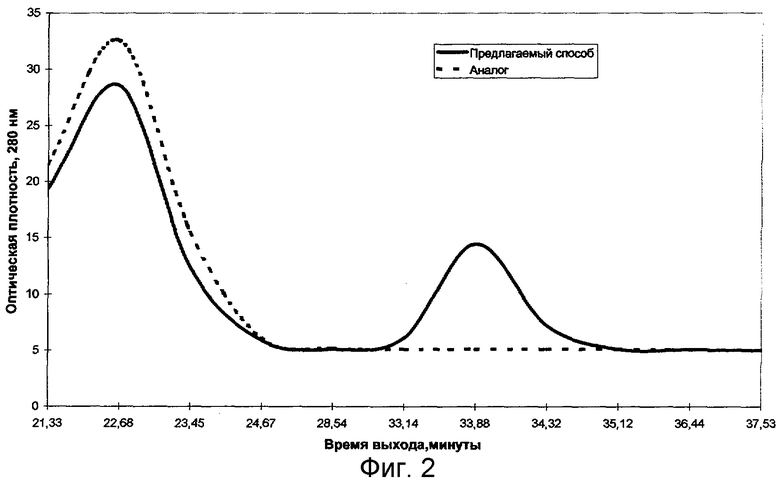
Результаты анализа ВЭЖХ полученной инъекционной формы по сравнению с известным препаратом по содержанию веществ с ММ менее 2,0 кД представлены на фиг.2. Из фиг.2 следует, что в полученной композиции присутствует полипептид с молекулярной массой между 0,8 и 0,9 кД. Данный пик был идентифицирован как сывороточный тимусный фактор.
Сравнение биологической активности полученного препарата и известного проведено на мышах линии BALB/C с возрастной инволюцией тимуса в возрасте 15 месяцев. Сравнительные показатели биологической активности препаратов по показателям количества ядросодержащих клеток (ЯСК) тимуса и индекса стимуляции (ИС) при введении препаратов мышам в равных дозах представлены в таблице 2. Показатель ИС представляет собой отношение среднего количества ЯСК в тимусе мышей с возрастной инволюцией, получивших препарат, к этому показателю у мышей контрольной группы.
Результаты испытаний показали, что показатель биологической активности, определенный как ИС, у препарата ″ОЛЕТИМ″ на 40% выше, чем у препарата по прототипу.
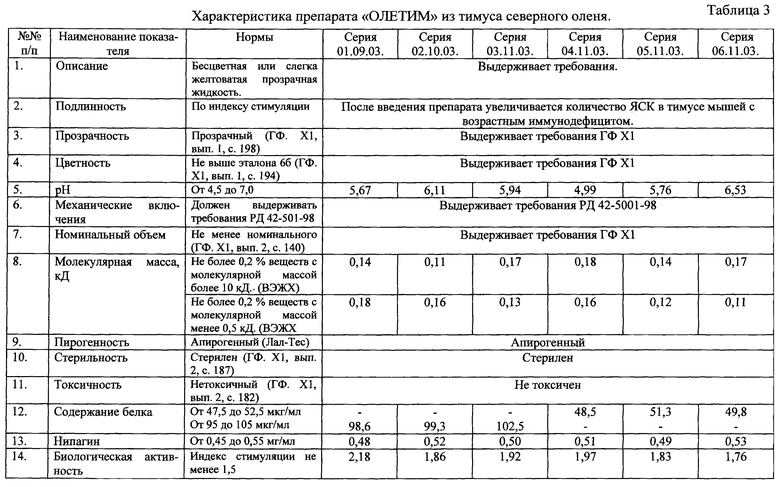
Характеристика препарата ″ОЛЕТИМ″ из тимуса северного оленя представлена в таблице 3.
Из таблицы 3 следует, что все серии препарата ″ОЛЕТИМ″, наработанные как в дозе (по белку) 100 мкг/мл, так и 50 мкг/мл, по таким его показателям, как внешний вид, прозрачность, цветность, рН, содержание белка и нипагина, соответствуют нормам, предусмотренным проектом ФПС на данный препарат. Показатель биологическая активность препарата, выраженный как индекс стимуляции, во всех наработанных сериях препарата, соответствовал нормам и колеблется от 1,76 (серия 06.11.03) до 2,18 (серия 01.09.03).
Указанный препарат может быть применен для лечения Т-системы иммунитета, вызванной вирусными и бактериальными инфекциями, а также для восстановления нарушений иммунной системы, вызванных стрессовыми состояниями. Препарат индуцирует пролиферацию и дифференцировку предшественников Т-лимфоцитов в зрелые иммунокомпетентные клетки, нормализует взаимодействия Т- и В-лимфоцитов (опосредованно), активизирует фагоцитарную функцию нейтрофилов и восстанавливает ряд других показателей, характеризирующих напряженность клеточного иммунитета. Препарат может применяться для лечения как человека, так и животных.
Источники информации
1. Машковский М.Д., Лекарственные средства, М., из-во: ООО ″Новая Волна″, 2001, т. №2, стр.190-191.
2. SU, №1218521 А1, 30.06.1994 г.
3. RU, №2112523 С1, 10.06.1998 г.
4. RU, №2205013 С1, 27.05.2003 г.
5. Матвеев Ю.А. Разработка технологии получения и исследования свойств иммуномодулирующего препарата из тимуса северного оленя, автореферат дис. на соискание ученой степени к.б.н., Щелково, 2001 г.
6. Емельяненко П.А., Грызлова О.И. и др. Методические указания по тестированию естественной резистентности телят, М., Московская ветеринарная академия им. К.И. Скрябина, 1980.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ИММУНОМОДУЛИРУЮЩЕГО ПРЕПАРАТА ИЗ ТИМУСА СЕВЕРНОГО ОЛЕНЯ | 2001 |
|
RU2205013C1 |
| ПОЛИПЕПТИДНЫЙ ПРЕПАРАТ ИЗ БУРСЫ КУР, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2000 |
|
RU2180592C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОСТИМУЛИРУЮЩИХ ТИМУСНЫХ ПОЛИПЕПТИДОВ | 1989 |
|
SU1737798A1 |
| МЕМБРАННЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА НА ОСНОВЕ ПЕПТИДОВ ТИМУСА ТЕЛЯТ | 2016 |
|
RU2648468C1 |
| Препарат для лечения заболеваний дыхательных путей у лошадей и способ его применения | 2017 |
|
RU2691110C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОМОДУЛЯТОРА | 2003 |
|
RU2257904C2 |
| БИОЛОГИЧЕСКИ АКТИВНОЕ СРЕДСТВО, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРЕПАРАТ, СОДЕРЖАЩИЙ УКАЗАННОЕ СРЕДСТВО, И СПОСОБ ИСПОЛЬЗОВАНИЯ ПРЕПАРАТА | 1992 |
|
RU2041717C1 |
| БИОЛОГИЧЕСКИ АКТИВНОЕ СРЕДСТВО, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРЕПАРАТ, СОДЕРЖАЩИЙ УКАЗАННОЕ СРЕДСТВО, И СПОСОБ ИСПОЛЬЗОВАНИЯ ПРЕПАРАТА | 1992 |
|
RU2041715C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВОЙ ПИЩЕВОЙ ДОБАВКИ | 1996 |
|
RU2075944C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНА ИЗ ПРИРОДНОГО ИСТОЧНИКА И ИНСУЛИН | 2003 |
|
RU2251426C1 |
Изобретение относится к медицинской промышленности и касается иммуномодулирующего препарата "ОЛЕТИМ", способа его получения и его инъекционной формы. Препарат "ОЛЕТИМ" характеризуется тем, что он представляет собой комплекс биологически активных пептидов (БАП) с молекулярной массой от 10,0 до 0,5 кД, выделенный из тимуса северного оленя, обладающий иммуномодулирующими свойствами, выраженными в обеспечении созревания Т-лимфоцитов, увеличении количества иммуноглобулинов классов IgG, IgM и усилении бактериальной и фагоцитарной активностей макрофагов. Способ получения препарата "ОЛЕТИМ" характеризуется тем, что тимус северного оленя измельчают, выделение активных веществ проводят экстрагированием гомогената водно-солевым раствором, денатурированием термолабильных веществ нагреванием, удалением коагулята, отделением биологически активных веществ вначале на мембране, задерживающей вещества с молекулярной массой 10,0 кД, а затем на мембране, задерживающей вещества с молекулярной массой 0,5 кД. Инъекционная форма характеризуется тем, что средство, полученное по заявленному способу, разбавляют раствором нипагина до содержания в 1 мл: белка 30-150 мкг. Преимущество изобретения заключается в разработке инъекционной формы. 3 с.п.ф-лы, 3 табл., 2 ил.
| СПОСОБ ПРИГОТОВЛЕНИЯ ИММУНОМОДУЛИРУЮЩЕГО ПРЕПАРАТА ИЗ ТИМУСА СЕВЕРНОГО ОЛЕНЯ | 2001 |
|
RU2205013C1 |
| ПЕПТИДСОДЕРЖАЩАЯ ФРАКЦИЯ ИЗ СЕЛЕЗЕНКИ МЛЕКОПИТАЮЩИХ, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2033796C1 |
| RU 2002428 C1, 15.11.1993 | |||
| ПРЕПАРАТ С ИММУНОМОДУЛИРУЮЩИМИ СВОЙСТВАМИ | 1995 |
|
RU2102988C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОМОДУЛЯТОРОВ | 1998 |
|
RU2149006C1 |
Авторы
Даты
2004-11-27—Публикация
2003-12-17—Подача