Изобретение относится к области ветеринарной вирусологии и биотехнологии, может быть использовано для разработки и изготовления средств диагностики и специфической профилактики парвовирусного энтерита собак и контроля антигенной и иммуногенной активности вакцин против данного заболевания.
Парвовирусный энтерит является одним из самых распространенных кишечных заболеваний собак вирусной этиологии в мире. Данная инфекция характеризуется обезвоживанием, геморрагическим энтеритом, миокардитом, лейкопенией. Возбудителем парвовирусного энтерита собак является ДНК-содержащий вирус, принадлежащий к семейству Parvoviridae, роду Protoparvovirus, виду Carnivore protoparvovirus 1 [1-3]. Вирус парвовирусного энтерита собак 2 типа (Canine parvovirus - CPV-2) был открыт в 1978 году в США и быстро распространился по всему миру [3]. CPV-2 рассматривают как вариант вируса панлейкопении кошек (FPV), который в результате мутации приобрел 6 аминокислотных изменений в капсиде, позволивших вирусу также заражать собак [4]. Через несколько лет после своего появления CPV-2 дал начало первому антигенному варианту, названному CPV-2a, а затем в 1984 году появился и второй антигенный вариант - CPV-2b. В 2000 году был обнаружен третий антигенный вариант - CPV-2c. Эти три варианта по-разному распространены по всему миру и практически полностью заменили исходный вариант, оставшийся лишь в некоторых вакцинах. Несмотря на антигенные различия, все сероварианты дают перекрестные реакции в реакции торможения гемагглютинации (РТГА) [1, 5, 6]. CPV-2 устойчив к воздействию дезинфицирующих средств, эфиру, хлороформу, а также к воздействиюнеблагоприятных условий окружающей среды и способен существовать вне хозяина в течение 12 месяцев и дольше [7]. Все эти факторы способствуют сохранению и циркуляции вируса парвовирусного энтерита в популяции собак по всему миру, особенно в странах, где вакцинация применяется недостаточно широко. Согласно руководству по вакцинации собак и кошек Международной ветеринарной ассоциации мелких домашних животных (WSAVA - the World Small Animal Veterinary Association) вакцины против парвовирусного энтерита относятся к базовым («core») вакцинам, которые должны получать все собаки независимо от обстоятельств (они обеспечивают защиту от заболеваний, опасных для жизни животных) [8]. Однако, несмотря на широкое распространение и огромный выбор вакцин для собак, заболеваемость парвовирусным энтеритом во всем мире по-прежнему чрезвычайно высока. В связи с этим вопрос о необходимости разработки средств вакцинопрофилактики, обеспечивающих надежную защиту от новых штаммов парвовирусного энтерита собак, не теряет актуальности.
В настоящее время наиболее известны следующие производственные штаммы вируса парвовирусного энтерита собак, которые применяются для производства средств специфической профилактики против данной болезни.
Известен штамм парвовируса "Геркулес" для приготовления вакцины [9], выделенный от больного тигра, который культивируют на монослое клеток перевиваемой линии почки котенка CRFK.
Известен штамм «№2312» [10], выделенный в 1988 г. из фекалий больных собак с диарейным синдромом, который адаптирован к перевиваемой культуре клеток почки собаки (МДСК). Вирус размножается в эпителиальных клетках тонкого отдела кишечника и на уровне 60-85 пассажа не вызывает заболевания у 8-14 недельных щенков при пероральном, подкожном и внутримышечном введении.
Известны штаммы «С 154» [11], «SP99» [12], «NL-35-D» [13], «ОР - 1/81» [14] входящими в состав импортных/зарубежных вакцин.
Тенденция к ежегодному росту случаев заболеваний парвовирусомсобак может свидетельствовать о недостаточной эффективности зарубежных вакцин против штаммов, циркулирующих в популяции собак на территории РФ.
Наиболее близкими предполагаемому изобретению по совокупности существенных признаков являются штаммы «Геркулес» и «№2312» вируса парвовирусного энтерита собак. Однако данные штаммы выделены до 2000 года. Периодически продолжают выделять новые возбудители парвовирусного энтерита свиней, отличающиеся по структуре генома, антигенными и иммуногенными свойствами, необходимость поиска, отбора и изучения эпизоотических изолятов CPV-2 в целях получения новых производственных штаммов для изготовления диагностических и вакцинных препаратов остается актуальной.
Задача, на решение которой направлено настоящее изобретение, входило получить новый производственный штамм CPV-2, обладающий высокой биологической, антигенной и иммуногенной активностью в нативном (культуральная вирусная суспензия) виде и обеспечивающий изготовление высокоспецифичных диагностических и вакцинных препаратов.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала производственных штаммов CPV-2, обладающих высокой биологической, антигенной и иммуногенной активностью и пригодных для изготовления высокоспецифичных диагностических и вакцинных препаратов.
Указанный технический результат достигнут получением штамма «Арчи» вируса парвовирусного энтерита собак, используемого для изготовления биопрепаратов для диагностики и специфической профилактики парвовирусного энтерита собак.
Штамм «Арчи» является новым, ранее неизвестным. Изолят вируса парвовирусного энтерита собак, послуживший источником для получения штамма «Арчи», был выделен из патологического материала, полученного от погибшего беспородного щенка, который содержался в приюте длябезнадзорных животных на территории г. Гусь-Хрустальный Владимирской области в 2021 г.
Штамм «Арчи» вируса парвовирусного энтерита собак депонирован во Всероссийской государственной коллекции экзотических типов вируса ящура и других патогенов животных ФГБУ «ВНИИЗЖ» под регистрационным номером: №454 - деп / 23-4 - ГКШМ ФГБУ «ВНИИЗЖ».
Преимуществом предлагаемого штамма является его технологичность: стабильно высокое накопление вируса в культурах клеток и высокая биологическая, антигенная и иммуногенная активность. Экспериментально подтверждена возможность использования штамма «Арчи» вируса парвовирусного энтерита собак для изготовления средств диагностики и специфической профилактики парвовирусного энтерита собак.
Для получения штамма «Арчи» вируса парвовирусного энтерита собак, обладающего оптимальными биотехнологическими свойствами, использовали перевиваемую культуру клеток почки кошки (CRFK). В результате проведения серии последовательных пассажей в данной культуре клеток из ранее выделенного изолята был получен штамм «Арчи» вируса парвовирусного энтерита собак, имеющий необходимые биотехнологические свойства и пригодный для изготовления диагностических препаратов и препаратов специфической профилактики данного заболевания. Штамм адаптирован к перевиваемой культуре клеток почки кошки (CRFK), что позволяет в промышленных масштабах получать вирусный материал штамма «Арчи» вируса парвовирусного энтерита собак с титрами гемагглютинирующей активности не менее 7,0 log2 НА.
Идентификация и филогенетическое родство штамма «Арчи».
Проводили генетическую идентификацию полученного вируса и сравнительный анализ последовательности ДНК с помощью реакции амплификации. Для идентификации и филогенетического анализа осуществляли секвенирование по Сенгеру.
Редактор выравнивания последовательностей BioEdit использовался дляанализа необработанных последовательностей. Выравнивания, содержащие полногеномные последовательности, были построены с использованием программы Clustal_W. Эволюционная история была выведена с использованием критерия максимального правдоподобия, основанного на 3 параметрах классической модели Tamura. Дерево было нарисовано в масштабе, с длиной ветвей, измеренной в количестве замен на сайт. Эволюционный анализ был проведен в MEGA7. Выравнивание аминокислотных последовательностей проводили с использованием Clustal X.
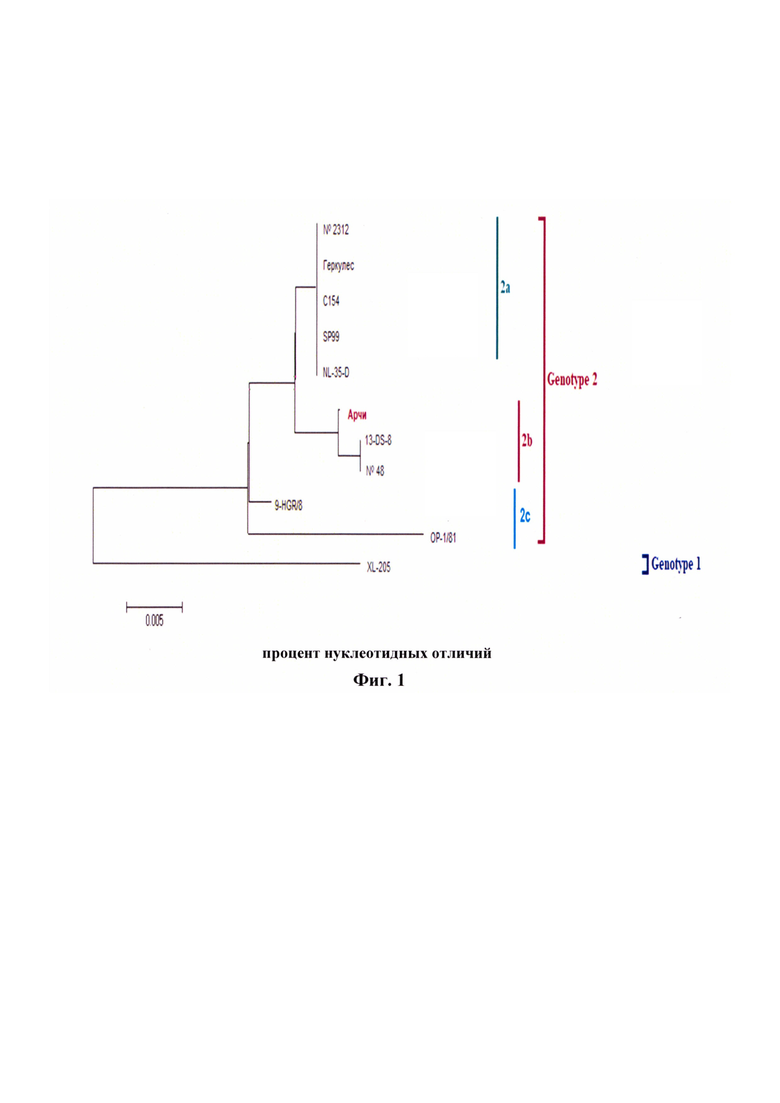
Дендрограмма основана на сравнении нуклеотидных последовательностей VP2-гена ДНК CPV. Штамм «Арчи» имеет большое количество нуклеотидных отличий от других заявленных штаммов и относится к геногруппе 2b.
Сущность изобретения отражена на графических изображениях:
Фиг. 1 - Филогенетическое древо для VP2-гена CPV штамма «Арчи».
Сущность изобретения пояснена в перечне последовательностей, в котором:
SEQ ID NO: 1 представляет последовательность нуклеотидов VP2-гена ДНК CPV штамма «Арчи»;
SEQ ID NO: 2 представляет последовательность аминокислот белков для VP2-гена ДНК CPV штамма «Арчи».
Штамм «Арчи» вируса парвовирусного энтерита собак характеризуется следующими признаками и свойствами.
Морфологические признаки
Штамм «Арчи» вируса парвовирусного энтерита собак относится к семейству Parvoviridae, роду Protoparvovirus, виду Carnivore protoparvovirus 1 и обладает морфологическими признаками, характерными для представителей парвовирусов: безоболочечные вирусы с одноцепочечной ДНК и икосаэдрическим капсидом, диаметр 20-25 нм, плавучая плотность 1,38-1,43 г/см3.
Антигенные свойства
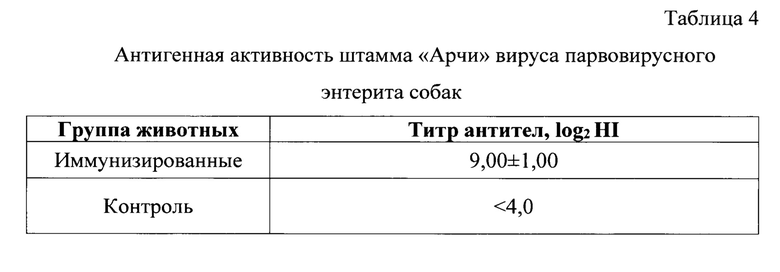
Антигенно CPV-2 родственен парвовирусу песцов (BFP), вирусу энтерита норок (MEV) и панлейкопении кошек (FPV) [1]. Антитела, которые образуются у переболевших животных в сыворотках крови, выявляются в реакции торможения гемагглютинации (РТГА). Инокуляция в организм животного штамма «Арчи» вируса парвовирусного энтерита собак сопровождается образованием антител в крови в титре 9,00±1,00 log2 НА у кроликов.
Устойчивость к внешним факторам
Вирус высокоустойчив к фенолу, эфиру, хлороформу, кислотам, трипсину, 0,2%-ному раствору дезоксихолата натрия, рН 3,0. При нагревании до 56°С активен и течение 60 мин. Хорошо сохраняется в 50%-ном глицерине, забуференном до рН 7,2. Переносит двукратное размораживание и оттаивание.
Дополнительные признаки и свойства:
Реактогенность - реактогенными свойствами не обладает;
Патогенность - патогенен для естественно-восприимчивых животных.
Безвреден для кроликов, морских свинок, белых мышей при внутримышечном и подкожном заражении.
Антигенные свойства - вирус индуцирует у собак образование вируснейтрализующих и гемагглютинирующих антител.
Стабильность - сохраняет исходные биологические свойства при пассировании в чувствительных биологических системах в течение 5 пассажей (срок наблюдения) на перевиваемой культуре клеток CRFK.
Контаминация бактериями, грибами, микоплазмами и посторонними вирусами - штамм «Арчи» не контаминирован бактериями, грибами, микоплазмами и посторонними вирусами.
Условия хранения
При хранении штамма в замороженном состоянии при температуре -70±5°С допустимая длительность хранения без освежения составляет 12 мес., а при хранении в лиофилизированном состоянии при той же температуре - 10 лет.
Биотехнологические характеристики
Штамм «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак репродуцируется в перевиваемой культуре клеток почки кошки (CRFK). Инфицированная вирусом культура клеток (CRFK) инкубируется в термостате при температуре (37,5±0,5)°С в течение 120 ч. Репродукция вируса в культуре клеток CRFK не сопровождается специфическим цитопатическим действием. Биологические свойства характеризовали путем определения гемагглютинирующей активности вируса каждого пассажа методом РГА. При культивировании вируса гемагглютинирующая активность штамма «Арчи» составляет не ниже 7 log2 НА. Исходные характеристики сохраняются при пассировании в чувствительных биологических системах в течение не менее 5 пассажей (срок наблюдения).
Гено- и хемотаксономическая характеристики
Геном штамм «Арчи» CPV имеет размер приблизительно 4200-4300 п. н. В результате проведения его картирования определили, что участок ДНК в диапазоне 1…2007 п. н. кодирует два неструктурных белка NS1 и NS2. Структурный белок VP1 кодируется участками в диапазонах 2014…2044 и 2117…2514 п. н., a VP2 - 2515…4269 п.н. [3]. Штамм «Арчи» CPV принадлежит 2b-генотипу (фиг. 1).
Исходя из полученных данных можно утверждать, что штамм «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак по антигенному и иммунологическому спектрам является оригинальным, в таксономическом отношении новым, ранее неизвестным вариантом CPV.
По мнению заявителя, предлагаемый штамм соответствует условиям патентоспособности «новизна» и «изобретательский уровень».
Сущность предлагаемого изобретения пояснена примерами его использования, которые не ограничивают объем изобретения.
Пример 1. Получение штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак
Проводили биологические и вирусологические методы, которые включали адаптацию вируса, выделенного из патологического материала, полученного от погибшего щенка, к культуре клеток CRFK. Для выделения вируса, вирусную суспензию вносили на освобожденный от ростовой среды монослой перевиваемой культуры клеток почки кошки (CRFK) и экспонировали в течение 60 мин. при температуре (37,0±0,5)°С. Затем вносили поддерживающую среду ПСС (или аналог) с добавлением 2% фетальной сыворотки крови КРС и антибиотиков (стрептомицин 100 мкг/см3 и пенициллин 100 ЕД/см3). Инфицированную культуру инкубировали при температуре (37,0±0,5)°С в течение 120 ч, затем замораживали при минус (45,0±5,0)°С. Полученный вируссодержащий материал использовали для последующих пассажей. После каждого пассажа с помощью РГА определяли гемагглютинирующую активность вируса. По истечении 5 суток культуральные флаконы с вирусным материалом замораживали в низкотемпературном холодильнике при температуре минус (45,0±5,0)°С. После цикла заморозки и разморозки вирусного материала при комнатной температуре производили его сбор с последующим отбором проб для исключения микробной контаминации и повторным определением гемагглютинирующей активности вируса методом РГА. Результаты адаптации вируса к перевиваемой линии клеток почки кошки CRFK представлены в таблице 1. Гемагглютинирующая активность вируса при репродукции в культуре клеток CRFK составила 8,40±1,52 log2HA. Данные, приведенные в таблице 1, свидетельствовали о хорошей адаптационной активности штамма «Арчи» вируса парвовирусного энтерита собак к данной клеточной культуре.
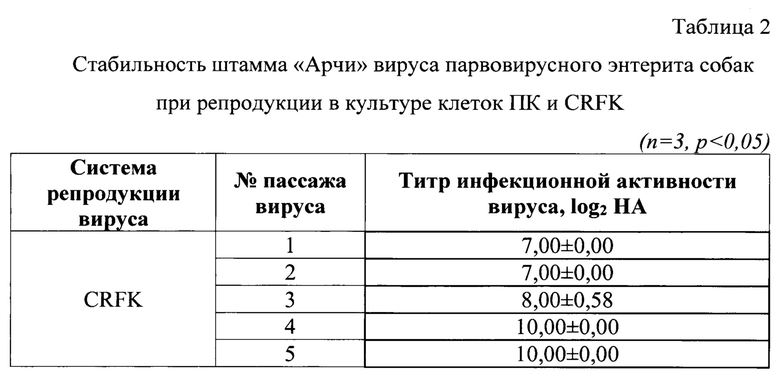
Пример 2. Контроль стабильности биологической активности штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак
Контроль стабильности биологической активности штамма определяли в течение 5 последовательных пассажей в культуре клеток CRFK. Результаты изучения стабильности биологической активности штамма «Арчи» в течение 5 пассажей представлены в таблице 2. В ходе проведенных исследованийустановлено, что штамм «Арчи» вируса парвовирусного энтерита собак в течение 5 последовательных пассажей в культуре клеток CRFK проявлял стабильную биологическую активность, которая находилась в пределах от 7,00±0,00 log2 до 10,00±0,00 log2HA.
Пример 3. Получение антигена вируса парвовирусного энтерита собак штамма «Арчи»
Для приготовления антигена в культуру клеток CRFK, выращенную в культуральных флаконах с площадью рабочей поверхности 300 см2, предварительно слив с них ростовую среду, вносили вируссодержащий материал в количестве 30,0 см3 с гемагглютинирующей активностью не ниже 7,00 log2HA. Флаконы помещали на один час в термостат при температуре (37,0±0,5)°С для контакта клеток культуры с вирусом. После этого вносили поддерживающую среду ПСС (или аналог) с добавлением 2% сыворотки крови КРС. Инфицированную культуру инкубировали при (37,0±0,5)°С в течение 120 ч, затем замораживали при минус (45,0±5,0)°С. Стерильный инфицированный монослой дезагрегировали с рабочей поверхности флаконов путем его разморозки при температуре (20±2)°С и периодического встряхивания. По окончании разморозки интенсивным встряхиванием остатки монослоя удаляли с рабочей поверхности, затем соблюдая условия асептики инфицированную суспензию собирали в общую емкость. Из собранного материала отбирали пробу для контроля. Контроль вирусного материала штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак осуществляли по показателю отсутствия контаминации грибами, бактериями и микоплазмами. Контроль контаминации грибами и бактериями вирусного материала штамма «Арчи» вируса парвовирусного энтерита собак проводили по ГОСТ 28085 [15]. Контроль контаминации микоплазмами осуществляли в соответствии с требованиями ГФ XIV, том II, с. 2997-3008 (ОФС.1.7.2.0031.15) [16]. Вируссодержащий материал с гемагглютинирующей активностью не ниже 7,00 log2 НА использовали для изготовления вакцинных и диагностических препаратов.
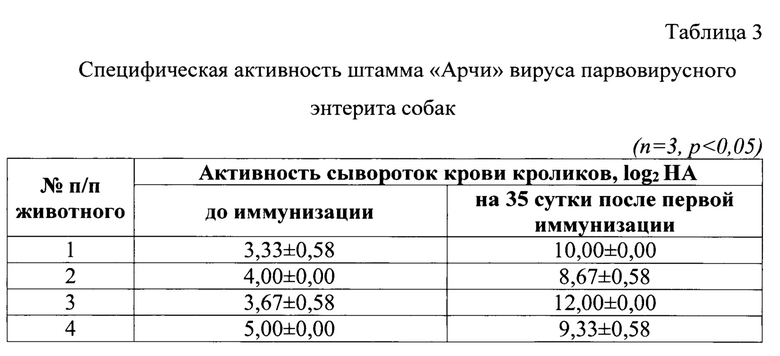
Пример 4. Получение гипериммунной сыворотки против антигена парвовирусного энтерита собак штамма «Арчи»
Штамм «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак использовали для получения высокоактивной гипериммунной сыворотки, предназначенной для оценки иммунобиологических свойств вируса парвовирусного энтерита собак. Для гипериммунизации животных применяли антиген вируса парвовирусного энтерита собак штамма «Арчи», полученный по методике, указанной в примере 3. Кроликов иммунизировали в дозе 1,0 см3 внутримышечно двукратно с интервалом 7 дней, отбор крови производили на 35 сутки после первой иммунизации. Полученную сыворотку крови исследовали на наличие антител против антигена вируса парвовирусного энтерита собак штамма «Арчи». Титр антител определяли в реакции торможения гемагглютинации (РТГА). Данные, представленные в таблице 3, свидетельствуют, что способом, описанным в примере 4, получены высокоактивные гипериммунные сыворотки со специфической активностью 8,67-12,00 log2 НА в РТГА.
Пример 5. Изучение антигенной активности штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак на кроликах
Для изучения антигенной активности штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак использовали вируссодержащий материал с биологической активностью равной 10,0 log2 НА. Подопытным кроликам в количестве 5 голов вводили вируссодержащий материал в среднюю часть бедра в дозе 1,0 см3 однократно. Кроликов в количестве 5 голов оставили в качестве контроля. Титр антител к антигену вируса парвовирусного энтерита собак в сыворотках крови кроликов определяли через 21 сутки после второй иммунизации в РТГА по общепринятой методике.
Результаты исследований антигенной активности штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак представлены в таблице 4, из которой следует, что титр антител уиммунизированных кроликов составил 9,00±1,00 log2 НА.
Пример 6. Определение патогенности штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита для собак
Патогенность штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак изучали на естественно восприимчивых животных (беспородные щенки в возрасте 2-3 мес). Животных разделили на две группы по 4 головы в каждой - подопытную и контрольную. Подопытным щенкам вводили внутрибрюшинно вируссодержащую культуральную жидкость в объеме 2,0 см3 с титром инфекционной активности 10,0 log2 НА. Животным контрольной группы вводили внутрибрюшинно 0,9% раствор хлорида натрия в объеме 2,0 см3. На 2-3 сутки после заражения у всех животных подопытной группы наблюдали характерные клинические признаки парвовирусного энтерита собак: снижение активности, отказ от корма, диарею, дегидратацию организма. Через 3-4 дня наблюдалась гибель подопытных животных. Специфичность заболевания животных, павших после заражения подтверждена исследованиями биоматериала методом ПЦР.
Таким образом, штамм «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак, полученный в соответствии с предлагаемым изобретением, обладает высокой биологической, антигенной активностью, пригоден как антиген для изготовления вакцин, определения их иммуногенной активности, а также диагностикумов, и расширяет арсенал новых отечественных производственных штаммов вируса парвовирусного энтерита собак.
Источники информации, принятые во внимание при составлении описания изобретения к заявке на выдачу патента Российской Федерации на изобретение «Штамм Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак для изготовления биопрепаратов для диагностики и специфической профилактики парвовирусного энтерита собак».
1. Алипер Т. И., Непоклонов Е. А., Мухин А. Н. и др. Диагностика и профилактика инфекционных болезней кошек и кошек: руководство для практикующих ветеринарных врачей. Под ред. Т.И. Алипера. М.: ЗооВетКнига; 2017. 300 с.
2. Mazzaferro Е.М. Update on Canine Parvoviral Enteritis. Vet. Clin. North Am. Small Anim. Pract. 2020 Nov; 50(6): 1307-1325. doi: 10.1016/j.cvsm.2020.07.008. Epub 2020 Sep 2. PMID: 32891439; PMCID: PMC7467068.
3. Chen В., Zhang X., Zhu J., Liao L., Bao E. Molecular Epidemiological Survey of Canine Parvovirus Circulating in China from 2014 to 2019. Pathogens. 2021 May 11;10(5):588. doi: 10.3390/pathogensl0050588. PMID: 34064982; PMCID: PMC8150379.
4. Truyen U., Parrish C.R. Canine and feline host ranges of canine parvovirus and feline panleukopenia virus: distinct host cell tropisms of each virus in vitro and in vivo. J Virol. 1992 Sep;66(9):5399-408. doi: 10.1128/JVI.66.9.5399-5408.1992. PMID: 1323703; PMCID: PMC289096.
5. Decaro N., Buonavoglia C. Canine parvovirus post-vaccination shedding: interference with diagnostic assays and correlation with host immune status. Vet. J. 2017;221:23-24.
6. Decaro N., Buonavoglia C., Barrs V.R. Canine parvovirus vaccination and immunisation failures: Are we far from disease eradication? Vet Microbiol. 2020 Aug;247:108760. doi: 10.1016/j.vetmic.2020. 108760. Epub 2020 Jun 15. PMID: 32768213; PMCID: PMC7295477.
7. Greene C.E., Decaro N. Canine viral enteritis. In: Greene C.E., editor. Infectious Diseases of the Dog and Cat. 4th ed. St. Louis: Elsevier Saunders; 2012. pp.67-80.
8. WSAVA Руководство по вакцинации собак и кошек. - URL: https://wsava.org/ (дата обращения 22.06.2023 г. ).
9. Пат. 2 150 296 Российская Федерация, МПК A61K 39/295 (2006.01). Вакцина "Биовак" против чумы плотоядных, парвовирусного энтерита, инфекционного гепатита, аденовироза и лептоспироза собак [Текст]/ Сулимов А.А., Колышкин В.М., Уласов В.И., Бирюкова Т.А.; заявитель и патентообладатель ТОО «Биоцентр». - №98117482/13; заявл. 1998.09.18; опубл. 2000.06.10.
10. Патент RU №2546247, МПК A61K 39/295(2006.01), А61Р 31/12(2006.01). Вакцина против чумы, аденовирусных инфекций, парвовирусного и коронавирусного энтеритов, лептоспироза и бешенства собак / Непоклонов Е.А., Алипер Т.И., Мусиенко М.И., Соболева Г.Л., Мухин А.Н.; заявитель и патентообладатель АНО «НИИ ДПБ». - №2013126074/10; заявл. 2013.06.06; опубл. 2015.04.10.
11. Нобивак DHPPi. - URL: https://www.vidal.ru/veterinar/nobivak-dhppi-29976/дата обращения 22.06.2023 г.).
12. Дюрамун Макс 5-CvK/4L. - URL: https://www.vidal.ru/veterinar/duramune-max-5-cvk-41-28028.
13. Вангард Плюс 5 L4 CV. -URL: https://www.vetlek.ru/directions/?id=1001
14. Биокан DHPPi+LR. -URL: https://www.vidal.ru/veterinar/biokan-dhppilr-29742.
15. ГОСТ 28085-13 «Средства лекарственные биологические для ветеринарного применения. Метод бактериологического контроля стерильности».
16. ГФ XIV, т. 2, с. 2997-3008 Испытания на присутствие микоплазм (ОФС.1.7.2.0031.15).

--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3" fileName="CPV Archy.xml"
softwareName="WIPO Sequence" softwareVersion="2.1.2"
productionDate="2023-07-13">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>0</ApplicationNumberText>
<FilingDate>2023-07-13</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>524</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>0</ApplicationNumberText>
<FilingDate>2023-07-13</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">ФГБУ "Федеральный центр охраны
здоровья животных" (ФГБУ "ВНИИЗЖ")</ApplicantName>
<ApplicantNameLatin>FGBI "ARRIAH"</ApplicantNameLatin>
<InventorName languageCode="ru">Галкина Татьяна
Сергеевна</InventorName>
<InventorNameLatin>Galkina Tatiana Sergeevna</InventorNameLatin>
<InventionTitle languageCode="ru">Штамм «Арчи» вируса парвовирусного
энтерита собак для изготовления биопрепаратов для диагностики и
специфической профилактики парвовирусного энтерита
собак</InventionTitle>
<SequenceTotalQuantity>2</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>414</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..414</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>genomic DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q1">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>CPV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>ggtactaactttggttatataggagttcaacaagataaaagacgtggtg
taactcaaatgggaaaaacaaactatattactgaagctactattatgagaccagctgaggttggttatag
tgcaccatattattcttttgaggcgtctacacaagggccatttaaaacacctattgcagcaggacggggg
ggagcgcaaacagatgaaaatcaagcagcagatggtgatccaagatatgcatttggtagacaacatggtc
aaaaaactaccacaacaggagaaacacctgagagatttacatatatagcacatcaagatacaggaagata
tccagaaggagattggattcaaaatattaactttaaccttcctgtaacagatgataatgtattgctacca
acagatttttttcct</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>138</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..138</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>CPV</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>GTNFGYIGVQQDKRRGVTQMGKTNYITEATIMRPAEVGYSAPYYSFEAS
TQGPFKTPIAAGRGGAQTDENQAADGDPRYAFGRQHGQKTTTTGETPERFTYIAHQDTGRYPEGDWIQNI
NFNLPVTDDNVLLPTDFFP</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
Изобретение относится к области биотехнологии и касается нового штамма «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак семейства Parvoviridae, рода Protoparvovirus, депонированный во Всероссийской государственной коллекции экзотических типов вируса ящура и других патогенов животных ФГБУ «ВНИИЗЖ» под регистрационным номером: №454 - деп/23-4 - ГКШМ ФГБУ «ВНИИЗЖ». Представленный штамм репродуцируется в перевиваемой культуре клеток почки кошки (CRFK). В CRFK в течение 120 часов инкубирования титр инфекционной активности вируса достигает значений 10,00±0,00 log2 НА, сохраняя исходные характеристики при пассировании в клеточной культуре на протяжении 5 пассажей. Представленный штамм может быть использован для изготовления биопрепаратов для диагностики и специфической профилактики парвовирусного энтерита собак и для контроля антигенной активности вакцин против данного заболевания. 1 ил., 4 табл., 6 пр.
Штамм «Арчи» вируса Carnivore protoparvovirus 1 парвовирусного энтерита собак семейства Parvoviridae, рода Protoparvovirus, депонированный во Всероссийской государственной коллекции экзотических типов вируса ящура и других патогенов животных ФГБУ «ВНИИЗЖ» под регистрационным номером: №454 - деп / 23-4 - ГКШМ ФГБУ «ВНИИЗЖ», для изготовления биопрепаратов для диагностики и специфической профилактики парвовирусного энтерита собак.
| ВАКЦИНА "БИОВАК" ПРОТИВ ЧУМЫ ПЛОТОЯДНЫХ, ПАРВОВИРУСНОГО ЭНТЕРИТА, ИНФЕКЦИОННОГО ГЕПАТИТА, АДЕНОВИРОЗА И ЛЕПТОСПИРОЗА СОБАК | 1998 |
|
RU2150296C1 |
| ВАКЦИНА ПРОТИВ ЧУМЫ, АДЕНОВИРУСНЫХ ИНФЕКЦИЙ, ПАРВОВИРУСНОГО И КОРОНАВИРУСНОГО ЭНТЕРИТОВ, ЛЕПТОСПИРОЗА И БЕШЕНСТВА СОБАК | 2013 |
|
RU2546247C2 |
| DECARO N | |||
| et al | |||
| Canine parvovirus post-vaccination shedding: interference with diagnostic assays and correlation with host immune status | |||
| Vet | |||
| J | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2024-04-12—Публикация
2023-08-22—Подача