Изобретение относится к биотехнологии, в частности к средствам специфической профилактики чумы плотоядных, инфекционного гепатита, аденовироза, парвовирусного энтерита и лептоспироза собак (гексаканивак). Для профилактики этих болезней у собак используют моно- и ассоциированные вакцины.
Для профилактики чумы, инфекционного гепатита, аденовирусных инфекций и парвовирусного энтерита у собак применяют ассоциированную вакцину "Тетравак" (авт.св. СССР по заявке N 4953741/13).
Однако эта вакцина не создает иммунитета к лептоспирозу, приобретающему все большую распространенность среди собак и протекающему с тяжелой клиникой и нередко гибелью животных. Отсутствие лептоспир в вакцине требует дополнительного проведения вакцинации собак поливалентной вакциной ВГНКИ против лептоспироза животных (авт.св. СССР N 828459, 1979) или концентрированной вакциной против лептоспироза животных (патент СССР по заявке N 4890614, 1990). Обе эти вакцины содержат лептоспиры четырех серологических групп, две из которых практически не вызывают лептоспироза собак и предназначены для специфической профилактики лептоспироза животных других видов. Кроме того, наличие в поливалентных вакцинах 28-30% гидроокиси алюминия у собак вызывает нежелательные побочные явления.
Целью изобретения является вакцина для специфической профилактики чумы плотоядных, инфекционного гепатита, аденовироза, парвовирусного энтерита и лептоспироза собак, характеризующаяся высокой антигенной и иммуногенной активностью и безвредностью.
Цель достигается тем, что в вакцине сбалансированы в антигенном и иммуногенном отношении вирусные и бактериальные антигены: в качестве антигенов чумы культуральная вирусная суспензия штамма Distemper canine "ЭПМ" с титром инфекционной активности 103-104 ТЦД50/0,5см3, в качестве антигенов аденовируса инактивированная культуральная вирусная суспензия штамма Mammaliadenovirus Adenovirus canis 2 "Ада" с титром инфекционной активности 104,5-105 ТЦД50/см3, в качестве антигенов парвовируса инактивированная культуральная вирусная суспензия штамма Virus panleucopenia felline "Ганнибал" с титром инфекционной активности 104-105 ИД50/см3 и активностью в РГА 1:64-1:256 ГАЕ/см3, в качестве антигенов лептоспир серогруппы Canicola штамм ВГНКИ-3, в качестве антигенов лептоспир серогруппы Icterohaemorrhagiae штамм ВГНКИ-2 в равном соотношении при концентрации 300-500 млн. клеток/0,2 см3, а также желатоза, сорбит, раствор Хенкса, белок сыворотки крови при следующем соотношении компонентов, об.
Вирусная суспензия штамма
Distemper canine "ЭПМ" с
титром инфекционной актив-
ности 103-104 ТЦД50/0,5см3 15,2-19,0
Инактивированная вирусная
суспензия штамма Mammali-
adenovirus Adenovirus canis 2
"Ада" с титром инфекционной
активности 104,5-105
ТЦД50/см3 11,8-15,0
Инактивированная вирусная
суспензия штамма Virus
panleucopenia felline "Ганни-
бал" с титром инфекционной
активности 104-105 ИД50/см3
и с активностью в РГА
1:64-1:256 ГАЕ/см3 24,3-30,4
Смесь антигенов из штаммов
лептоспир серогрупп Canicola
ВГНКИ-3 и Icterohaemorrhagiae
ВГНКИ-2, взятых в равном
соотношении при концентра-
ции 300-500 млн. клеток/
/0,2 см3 фосфатного буфера 9,2-10,6
Гидроокись алюминия 4,8-5,6
25%-ный раствор желатозы 8,5-11,3
50%-ный раствор сорбита 2,8-3,8
Белок сыворотки крови 3,3-5,5
Дистиллированная вода 1,2-1,8
Раствор Хенкса Остальное
П р и м е р 1. Получают инактивированную культуральную вирусную суспензию штамма Mammaliadenovirus adenovirus canis 2 "Ада".
Для выращивания культуры клеток используют первично-трипсинизированную культуру клеток почек собак 1,3-месячного возраста. В качестве ростовой среды применяют среду, содержащую 35-40% 0,5%-ного гидролизата лактальбумина на растворе Хенкса, по 0,25% среды 199 и "Игла", 10% сыворотки крови крупного рогатого скота и антибиотики (пенициллин 100 ЕД/см3 и стрептомицин 10 мг на 1 см3 среды). В качестве поддерживающей используют среду, содержащую 30% 0,5%-ного ГЛАЭ и 70% среды 199.
При получении вируса культуру клеток в матрасах со сформировавшимся монослоем заражают штаммом "Ада" в дозе 1,0-0,001 ТЦД50/см3, затем осуществляют его адсорбцию в течение 1 ч при температуре 37оС. После добавления поддерживающей среды вирус инкубируют в термостате при 37оС до накопления титра инфекционной активности 104,5-105 ТЦД50/см3. После трехкратного замораживания при -20-40оС и оттаивания при 37оС полученную вируссодержащую культуральную суспензию сливают в одну емкость, добавляют 0,2% формалина для инактивации вируса.
Получают инактивированную культуральную вирусную суспензию штамма Virus panleucopenia felline "Ганнибал".
Первично-трипсинизированную культуру клеток почки котенка заражают при посеве в матрасы нативным ультрафильтратом вируса штамма "Ганнибал" с титром в РГА не ниже 1:16384 ГАЕ/см3 и инфекционной активностью для культуры клеток почки котенка 104-105 ИД50/см3. Вирус разводят раствором Хенкса 1:50-1:100 и в каждый матрас вносят по 5-7 см3. Инкубацию инфицированной культуры клеток проводят при 37оС в питательной среде, содержащей 26% среды "Игла" и 34% ГЛАЭ на растворе Хенкса, 32% среды 199 на растворе Хенкса и 8% сыворотки крупного рогатого скота. На 9-10-е сутки матрасы с культурой клеток замораживают при -20-40оС. После оттаивания при комнатной температуре проводят сбор вируссодержащей жидкости. Сливы вируссодержащей жидкости объединяют и определяют гемагглютинирующую активность в РГА, которая должна быть не ниже 1: 64-1: 256 ГАЕ/см3. Для инактивации вируса к общему объему вирусных сборов добавляют 0,2% формалина.
Получают культуральную вирусную суспензию штамма Distemper canine "ЭПМ".
Вирус чумы плотоядных выращивают в первично-трипсинизированной культуре клеток эмбрионов японских перепелов в ростовой среде, состоящей из 0,5%-ного ГЛА на растворе Хенкса, 25-30% среды 199 и 8-10% сыворотки крупного рогатого скота с добавлением антибиотиков. Вирус вносят в суспензию клеток и выращивают ролерным способом при 37оС. Через 4-6 сут ростовую среду сливают, а культивирование продолжают в поддерживающей среде, включающей 60-70% среды 199 и 30-40% 0,5% -ного ГЛА на растворе Эрла с добавлением антибиотиков. После полного развития ЦПД вируссодержащую культуральную жидкость сливают, замораживают при температуре минус 10-20оС, оттаивают при комнатной температуре и объединяют с 1%-ным сливом (инфекционная активность полученного вируса чумы плотоядных для культуры клеток эмбрионов японских перепелов должна быть 103-104 ТЦД50/0,5см3).
Штаммы лептоспир серогрупп Canicola ВГНКИ-3 и Icterohaemorrhagiae ВГНКИ-2 выращивают раздельно на буферно-сывороточной среде до накопления 70-100 млн. микробных клеток, добавляют формалин до 0,24-0,26%-ной концентрации. Суспензию лептоспир смешивают 1:1, концентрируют ультрафильтрацией до 300-500 млн/см3 микробных клеток.
К инактивированному парвовирусному компоненту добавляют 3%-ный раствор гидрата окиси алюминия. Смесь выдерживают в течение 2 сут при комнатной температуре, после чего удаляют 1/3 надосадочной жидкости и добавляют столько же инактивированного аденовирусного компонента, 3%-ный раствор гидрата окиси алюминия и инактивированную суспензию лептоспир. Полученную смесь тщательно перемешивают и после отстаивания определяют количество остаточного формальдегида, для нейтрализации которого в нее добавляют 2-3% от общего объема растворенного на дистиллированной воде метабисульфита натрия. Общий объем смеси доводят раствором Хенкса до 100 л.
В объединенную смесь сборов суспензии вируса чумы плотоядных добавляют стабилизатор для лиофилизации, в качестве которого используют 25%-ный раствор желатозы и 50%-ный раствор сорбита, тщательно перемешивают на шуттель-аппарате и добавляют антибиотики гентамицин, мономицин или канамицин из расчета 20 мг/см3. Смесь охлаждают до 5-10оС в течение 5-7 ч, расфасовывают в стерильные стеклянные флаконы и лиофилизируют.
Ассоциированную вакцину получают путем разведения сухого компонента, содержащего культуральную вирусную суспензию штамма Distemper canine "ЭПМ" с титром инфекционной активности 103-104 ТЦД50/0,5см3, в жидком растворе, состоящем из инактивированных культуральных вирусных суспензий из штаммов Mammaliadenovirus Adenovirus canis 2 "Ада" и Virus panleucopenia felline "Ганнибал" и бактериальной суспензии штаммов лептоспир Canicola ВГНКИ-3 и Icterohaemorrhagiae ВГНКИ-2. Получают три серии вакцины против чумы плотоядных, инфекционного гепатита, аденовироза, парвовирусного энтерита и лептоспироза собак (гексаканивак) при следующем соотношении компонентов, об.
серия 1 серия 2 серия 3 Вирусная суспензия штамма Distemper canine "ЭПМ" с титром инфекционной активности 103-104 ТЦД50/0,5см3 15,2 17,0 19,0
Инактивированная вирус- ная суспензия штамма Mammaliadenovirus Adenovirus canis 2 "Ада" с титром инфекционной активности 104,5-105 ТЦД50/см3 11,8 13,5 15,0
Инактивированная вирусная суспензия штамма Virus panleuco- penia felline "Ганнибал" с титром инфекционной активности 104-105 ИД50/см3 и с активностью в РГА 1:64-1:256 ГАЕ/см3 24,3 28 30,4
Смесь антигенов из штаммов лептоспир серо- групп Canicola ВГНКИ-3 и Icterohaemor- rhagiae ВГНКИ-2, взятых в равном соотношении при концентрации 300-500 млн. клеток/0,2 см3 фосфатного буфера 9,2 9,6 10,6
Гидроокись алюминия 4,8 5,2 5,6
25%-ный раствор
желатозы 8,5 9,5 11,3
50%-ный раствор сорбита 2,8 3,2 3,8
Белок сыворотки крови 3,3 4,4 5,5
Дистиллированная вода 1,2 1,5 1,8
Раствор Хенкса Остальное
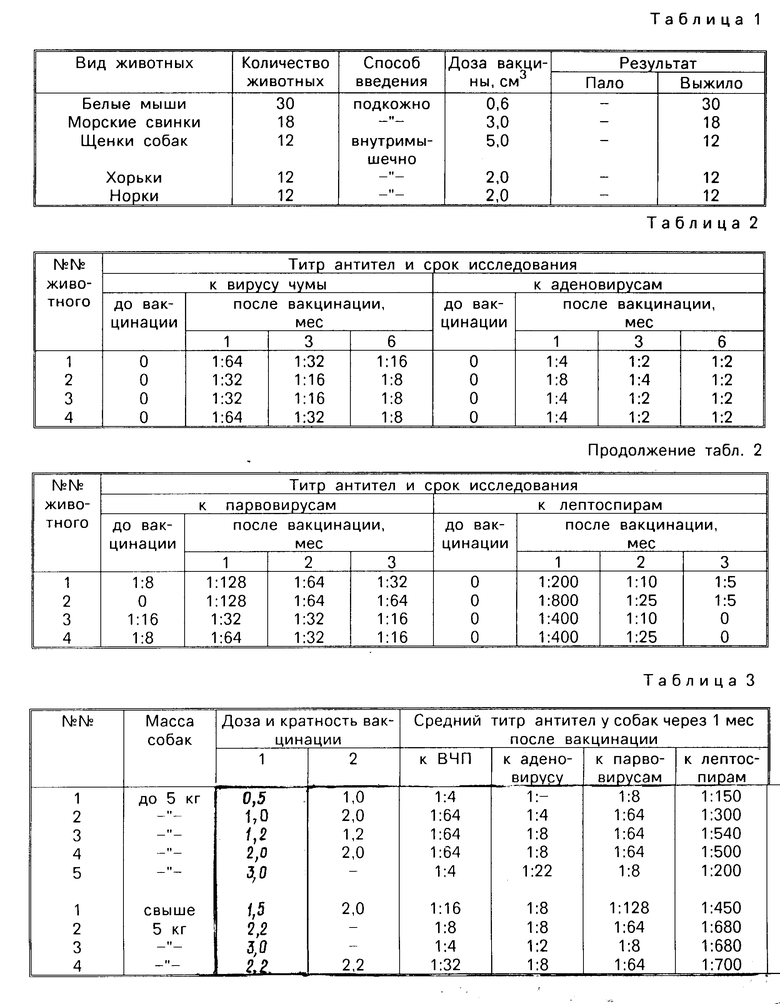
П р и м е р 2. Изучают безвредность вакцины против чумы плотоядных, инфекционного гепатита, аденовироза, парвовирусного энтерита и лептоспироза собак трех серий на белых мышах массой 14-16 г, морских свинок массой 300-350 г, щенках собак двухмесячного возраста, хорьках трехмесячного возраста, норках четырехмесячного возраста при введении различных доз вакцины. Суммарные результаты контроля представлены в табл. 1.
Вакцина "Гексаканивак" безвредна для животных. Животные оставались клинически здоровыми в течение 21 дн наблюдения после вакцинации.
П р и м е р 3. Оценку иммуногенной активности вакцины против чумы плотоядных, инфекционного гепатита, аденовироза, парвовирусного энтерита и лептоспироза собак "Гексаканивак" серии 2 проводят на щенках собак массой до 5 кг. Животных вакцинируют однократно и двукратно в различных дозах.
Активность вводимого животным препарата оценивают посредством изучения динамики накопления специфических антител в сыворотке крови собак, определяемых в следующих серологических реакциях: в реакции нейтрализации в культуре клеток японских перепелов к вирусу чумы плотоядных, в реакции диффузионной преципитации в агаровом геле к возбудителям аденовирозов плотоядных, в реакции торможения гемагглютинации к возбудителю парвовирусного энтерита собак и в реакции микроагглютинации к возбудителям лептоспироза. Результаты представлены в табл. 2.
Из табл. 2 следует, что вакцина "Гексаканивак" у щенков собак вызывает напряженный иммунитет к вирусу чумы плотоядных, к адено- и парвовирусам, а также к лептоспирам.
П р и м е р 4. Определяют оптимальную дозу вакцины "Гексаканивак" серии 2 для щенков собак массой до 5 кг и собак массой свыше 5 кг. Животных вакцинируют разными дозами вакцины одно- и двукратно с интервалом 7-10 дн. Результаты представлены в табл. 3.
Уровень изучения специфических антител в сыворотке крови собак, а также степень выраженности поствакцинальной реакции (табл. 3) свидетельствуют о том, что оптимальной дозой вакцины для щенков массой до 5 кг является двукратное введение вакцины в дозе по 1,2 см3 с интервалом между инъекциями 7-10 дн, а для собак массой свыше 5 кг однократное в дозе 2,2 см3.
Иммунизацию собак проводят за 1 мес до вязки и не менее, чем через 14 дн после иммунизации против других инфекций. Щенят прививают с восьминедельного возраста. Вакцину вводят подкожно в область лопатки или внутримышечно с внутривенной поверхности бедра собакам массой до 5 кг по 1,2 см3, массой более 5 кг по 2,2 см3. Щенкам собак через 7-10 дн вакцину вводят повторно в той же дозе. Собак в возрасте 1 г и более вакцинируют ежегодно однократно в тех же дозах.
Использование предложенной вакцины в ветеринарной практике позволит повысить эффективность проводимых мероприятий по профилактике инфекционных болезней собак.
Использование: в биотехнологии, ветеренарной вирусологии и микробиологии. Сущность изобретения: вакцина содержит сбалансированные в антигенном и иммуногенном отношении вирусные и бактериальные антигены: в качестве антигенов чумы культуральную вирусную суспензию штамма Distemper canine "ЭПМ", в качестве антигенов аденовируса инактивированную культуральную вирусную суспензию штамма Mammaliadenovirus Adenovirus canis 2 "Ада", в качестве антигенов парвовируса инактивированную культуральную вирусную суспензию штамма Virus panleucopenia Felline "Ганнибал", в качестве антигенов лептоспир серогруппы Canicola ВГНКИ-3, в качестве антигенов лептоспир серогруппы - Jcterohaemorrhagial ВГНКИ-2, в качестве одъюванта- гидроокись, алюминия и белок сыворотки крови, в качестве стабилизатора -растворы желатозы и сорбита. Вакцина позволяет создать иммунитет высокой напряженности как к вирусным, так и к бактериальному компонентам. Использование вакцины в ветеринарной практике позволит снизить до минимума материальный ущерб, наносимый указанными болезнями. 3 табл.
ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ ЧУМЫ, ИНФЕКЦИОННОГО ГЕПАТИТА, АДЕНОВИРОЗА, ПАРВОВИРУСНОГО ЭНТЕРИТА И ЛЕПТОСПИРОЗА СОБАК, включающая вирусную суспензию штамма Distemper canine "ЭПМ" с титром инфекционной активности 103 104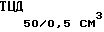 инактивированную вирусную суспензию штамма Mammaliadenovirus Adenovirus canis-2 "Ада" с титром инфекционной активности 104,5 105,0
инактивированную вирусную суспензию штамма Mammaliadenovirus Adenovirus canis-2 "Ада" с титром инфекционной активности 104,5 105,0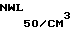 инактивированную вирусную суспензию штамма Virus panleucopenia felline "Ганнибал" с титром инфекционной активности 104 105
инактивированную вирусную суспензию штамма Virus panleucopenia felline "Ганнибал" с титром инфекционной активности 104 105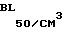 и с активностью в РГА 1 64 1 256 ГАЕ/см3, смесь антигенов из штаммов лептоспир серогрупп Canocola ВГНКИ-3 и Icterohaemorrhagiae ВГНКИ-2, взятых в равном соотношении при концентрации 300 500 млн клеток/0,2 см3 фосфатного буфера, гидроокись алюминия, 25% -ный раствор желатозы, 50%-ный раствор сорбита, белок сыворотки крови, дистиллированную воду, раствор Хенкса при следующем соотношении компонентов, об.
и с активностью в РГА 1 64 1 256 ГАЕ/см3, смесь антигенов из штаммов лептоспир серогрупп Canocola ВГНКИ-3 и Icterohaemorrhagiae ВГНКИ-2, взятых в равном соотношении при концентрации 300 500 млн клеток/0,2 см3 фосфатного буфера, гидроокись алюминия, 25% -ный раствор желатозы, 50%-ный раствор сорбита, белок сыворотки крови, дистиллированную воду, раствор Хенкса при следующем соотношении компонентов, об.
Вирусная суспензия штамма Distemper canine "ЭПМ" с титром инфекционной активности 103 104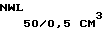 15,2 19,0
15,2 19,0
Инактивированная вирусная суспензия штамма Mammaliadenovirus Adenovirus canis-2 "Ада" с титром инфекционной активности 104,5 105,0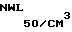 11,8 15,0
11,8 15,0
Инактивированная вирусная суспензия штамма Virus panleucopenia felline "Ганнибал" с титром инфекционной активности 104 105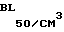 и с активностью в РГА 1 64 1 256 ГАЕ/см3 24,3 30,4
и с активностью в РГА 1 64 1 256 ГАЕ/см3 24,3 30,4
Смесь антигенов из штаммов лептоспир серогрупп Canicola ВГНКИ-3 и Icterohaemorrhagiae ВГНКИ-2, взятых в равном соотношении при концентрации 300 500 млн клеток/0,2 см3 фосфатного буфера 9,2 10,6
Гидроокись алюминия 4,8 5,6
25%-ный раствор желатозы 8,5 11,3
50%-ный раствор сорбита 2,8 3,8
Белок сыворотки крови 3,3 5,5
Дистиллированная вода 1,2 1,8
Раствор Хенкса Остальное
| Аналогов в патентной и научно-технической литературе не обнаружено. |
Авторы
Даты
1995-10-20—Публикация
1992-07-01—Подача