Область техники
Настоящее изобретение направлено, главным образом, на промежуточные соединения, полезные при получении соединений, которые полезны в терапии. Более конкретно, настоящее изобретение относится к промежуточным соединениям, полезным при получении класса конденсированных полициклических алкалоидов. Изобретение относится также к способам получения конденсированных полициклических алкалоидов и их аналогов, и производных.
Предшествующий уровень техники
Существующие в природе молекулы, проявляющие потенциально целебные фармакологические свойства, можно выделить из объектов окружающей среды, таких, как морские, растительные или микробные источники. Одним из примеров таких молекул является общий класс соединений, известных как ламелларины. Эти полиароматические алкалоиды выделяются из морских источников и они имеют конденсированную структуру. Было показано, что ламелларины С и D вызывают ингибирование деления клетки в пробе оплодотворенного морского ежа, тогда как ламелларины I, К и L все проявляют сопоставимую и значительную цитотоксичность против клеточных линий Р388 и А549 в культуре. Недавно было показано, что ламелларин N проявляют активность в клеточных линиях рака легких, действуя как яд микротрубочек типа IV. Более того, было также показано, что эти соединения обладают цитотоксичной активностью по отношению к клеткам, устойчивым к большому числу лекарственных средств, а также эффективностью в качестве нетоксичных модуляторов фенотипа, устойчивого к большому числу лекарственных средств, и, следовательно, предоставляют привлекательный потенциальный источник хемотерапевтических агентов.
Однако возможная клиническая полезность ламелларинов сильно ограничена скромными количествами, получаемыми в природе, а также трудностями, связанными с их выделением.
Соответственно, значительная активность была направлена на развитие синтетеического пути для этого класса молекул и подходы к этим молекулам включали в себя последовательную двойную циклизацию 1,3,4-триарил-2,5-дикарбоксизамещенного пиррольного кольца (Steglich et al., Angew. Chem., Int. Ed. Ing., 1997, 36, 155) и протекающее через N-илид образование пиррольного кольца для введения в молекулу пиррольной и лактонной частей (Banwell et al., Chem. Commun., 1997, 2259; Ishibashi et al., Tetrahedron, 1997, 53, 5951).
В данный момент настоящее изобретение предоставляет альтернативный способ через синтетическое промежуточное соединение, который допускает введение ряда моделей замещения и потенциально открывает доступ к большому числу ламеллариновых соединений и аналогов, содержащих конденсированное полициклическое-пиррольное ядро.
Описание изобретения
Соответственно, в первом аспекте изобретение относится к способу получения соединения формулы (II):
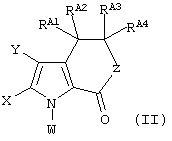
включающему стадию проведения внутримолекулярной циклизации соединения формулы (I):
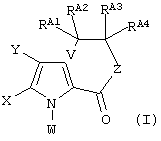
где:
RA1-A4 каждый независимо выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидрокси, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкенокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамидо, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано; или
RA2 и RA3 могут необязательно вместе образовывать связь, a RA1 и RA4 являются определенными выше, или вместе с атомом углерода, с которым они связаны, образуют необязательно замещенную карбоциклическую или гетероциклическую группу; или
RA2 и RA3 вместе с атомом углерода, с которым они связаны, образуют необязательно замещенную насыщенную или ненасыщенную карбоциклическую или гетероциклическую группу; или
RA1RA2C-CRA3RA4 образуют необязательно замещенную арильную группу или ароматическую гетероциклическую группу;
У выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидрокси, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкенокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамида, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано;
W и Х такие, как определено для У, или вместе с атомами азота и углерода, с которыми они связаны, образуют насыщенную или ненасыщенную азотосодержащую гетероциклическую группу, которая необязательно может быть замешена или необязательно конденсирована с насыщенной или ненасыщенной карбоциклической группой, арильной группой или гетероциклической группой;
V является атомом галогена или атомом водорода;
Z представляет собой -(СН2)n-U-(CH2)о-, где U выбирают из СН2, NH или гетероатома, а n и о независимо равны 0, 1, 2 или 3.
Во втором аспекте настоящее изобретение предоставляет промежуточное соединение, полезное при получении соединений формулы (II), где упомянутое промежуточное соединение имеет формулу (I):
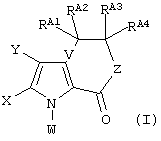
где:
RA1-A4 каждый независимо выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидроксила, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкекокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамидо, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано; или
RA2 и RA3 могут необязательно вместе образовывать связь, и RA1 и RA4 являются определенными выше, или вместе с атомами углерода, с которыми они связаны, образуют необязательно замешенную карбоциклическую или гетероциклическую группу; или
RA2 и RA3 вместе с атомом углерода, с которым они связаны, образуют необязательно замещенную насыщенную или ненасыщенную карбоциклическую или гетероциклическую группу; или
RA1RA2C-CRA3RA4 образуют необязательно замещенную арильную группу или ароматическую гетероциклическую группу;
У выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидрокси, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкенокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамида, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано;
W и Х такие, как определено для У, или вместе с атомами азота и углерода, с которыми они связаны, образуют насыщенную или ненасыщенную азотсодержащую гетероциклическую группу, которая необязательно может быть замещена или необязательно конденсирована с насыщенной или ненасыщенной карбоциклической группой, арильной группой или гетероциклической группой;
V представляет собой атом галогена или атом водорода;
Z является -(CH2)n-U-(CH2)о-, где U выбирают из CH2, NH или гетероатома, а n и о независимо равны 0, 1, 2, или 3.
Следующий аспект настоящего изобретения относится к соединениям формулы (II), определенным выше, полученным по описанным здесь способам.
Использованный здесь термин “алкил” обозначает полностью насыщенные, неразветвленные, разветвленные или циклические углеводородные остатки. Если число атомов углерода не указано, этот термин предпочтительно относится к C1-20алкилу или циклоалкилу. Примеры неразветвленного и разветвленного алкила включают в себя метил, этил, пропил, изопропил, бутил, изобутил, вторбутил, третбутил, амил, изоамил, вторамил, 1,2-диметилпропил, 1,1-диметилпропил, гексил, 4-метилпентил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 1,1-диметилбутил, 2,2-диметилбутил, 3,3-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 1,2,2-триметилпропил, 1,1,2-триметилпропил, гептил, 5-метоксигексил, 1-метилгексил, 2,2-диметилпентил, 3,3-диметилпентил, 4,4-диметилпентил, 1,2-диметилпентил, 1,3-диметилпентил, 1,4-диметилпентил, 1,2,3-триметилбутил, 1,1,2-триметилбутил, 1,1,3-триметилбутил, октил, 6-метилгептил, 1-метилгептил, 1,1,3,3-тетраметилбутил, нонил, 1-, 2-, 3-, 4-, 5-, 6- или 7-метилоктил, 1-, 2-, 3-, 4- или 5-этилгептил, 1- 2- или 3-пропилгексил, децил, 1-, 2-, 3-, 4-, 5-, 6-, 7- или 8-метилнонил, 1-, 2-, 3-, 4-, 5- или 6-этилоктил, 1-, 2-,3- или 4-пропилгептил, ундецил, 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8- или 9-метилдецил, 1-, 2-, 3-, 4-, 5-, 6- или 7-этилнонил, 1-, 2-, 3-, 4- или 5-пропилоктил, 1-, 2- или 3-бутилгептил, 1-пентилгексил, додецил, 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8-, 9- или 10-метилундецил, 1-, 2-, 3-, 4-, 5-, 6-, 7- или 8-этилдецил, 1-, 2-, 3-, 4-, 5- или 6-пропилнонил, 1-, 2-, 3- или 4-бутилоктил, 1-2-пентилгептил и т.п. Примеры циклического алкила включают в себя моно-или полициклические алкильные группы, такие как циклопропильная, циклобутильная, циклопентильная, циклогексильная, циклогептильная, циклооктильная, циклононильная, циклодецильная и т.п.
Использованный здесь термин “алкенил” обозначает группы, образованные из неразветвленных, разветвленных или циклических углеводородных остатков, содержащих, по меньшей мере, одну двойную углерод-углеродную связь, включая этиленоподобные моно-, ди- или полиненасыщенные алкильные или циклоалкильные группы, определенные выше. Если число томов углерода не указано, этот термин относится к C1-20алкенилу. Примеры алкенила включают в себя винил, аллил, 1-метилвинил, бутенил, изобутенил, 3-метил-2-бутенил, 1-пентенил, циклопентенил, 1-метилциклопентенил, 1-гексенил, 3-гексенил, циклогексенил, 1-гептенил, 3-гептенил, 1-октенил, циклооктенил, 1-ноненил, 2-ноненил, 3-ноненил, 1-деценил, 3-деценил, 1,3-бутадиенил, 1,4-пентадиенил, 1,3-циклопентадиенил, 1,3-гексадиенил, 1,4-гексадиенил, 1,3-циклогексадиенил, 1,4-циклогексадиенил, 1,3-циклогептадиенил, 1,3,5-циклогептатриепил и 1,3,5,7-циклооктатетраенил.
Использованный здесь термин “алкинил” обозначает группы, полученные из неразветвленных, разветвленных или циклических углеводородных остатков, содержащих, по меньшей мере, одну тройную углерод-углеродную связь, включая этиноподобные моно-, ди- или полиненасыщенные алкильные или циклоалкильные группы, определенные выше. Если число атомов углерода не указано, этот термин относится к C1-20алкинилу. Примеры включают в себя этинил, 1-пропинил, 2-пропинил, и изомеры бутинила, и изомеры пентинила.
Термины “алкокси”, “алкенокси” и “алкинокси” означают соответственно алкильную, алкенильную и алкинильную группы, определенные выше, в случае их связывания через кислород.
Термин “галоген” означает фтор, хлор, бром или йод.
Термин “арил” означает одинарные, полиядерные, сопряженные и конденсированные остатки ароматических углеводородных циклических систем. Примеры арила включают в фенил, дифенил, трифенил, тетрафенил, нафтил, тетрагидронафталил, антраценил, дигидроантраценил, бензантраценил, дибензантраценил, фенантренил, флуоренил, пиренил, иденил, азуленил, хризенил.
Термин “гетероциклический” означает моно- или поликарбоциклическую группу, включая арильную, в которой, по меньшей мере, один атом углерода заменен на гетероатом, предпочтительно, выбранный из азота, серы или кислорода. В случае, когда моно- или поликарбоциклическая группа, в которой, по меньшей мере, один атом углерода, заменен на гетероатом, представляет собой арильную группу, ее называют ароматической гетероциклической группой.
Подходящие гетероциклические группы включают в себя N-содержащие гетероциклические группы, такие, как ненасыщенные 3-6-членные гетеромоноциклические группы, содержащие от 1 до 4 атомов азота, например, пирролил, пирролинил, имидазолил, имидазолинил, пиразолил, пиридил, пиримидинил, пиразинил, пиридазинил, триазолил или тетразолил;
насыщенные 3-6-членные гетеромоноциклические группы, содержащие от 1 до 4 атомов азота, например, пирролидинил, имидазолидинил, пиперидил, пиразолидинил или пиперазинил;
конденсированные насыщенные или ненасыщенные гетероциклические группы, содержащие от 1 до 5 атомов азота, такие, как индолил, изоиндолил, индолинил, изоиндолинил, индолизинил, изоиндолизилил, бензимидазолил, хинолил, изохинолил, индазолил, бензотриазолил, пуринил, хиназолинил, хиноксалинил, фенантрадинил, фенантролинил, фталазинил, нафтиридинил, циннолинил, птеридинил, перимидинил, или тетразолопиридазинил;
насыщенные 3-6-членные гетеромоноциклические группы, содержащие от 1 до 3 атомов кислорода, такие, как тетрагидрофуранил, тетрагидропиранил, тетрагидродиоксинил;
ненасыщенную 3-6-членную гетеромоноциклическую группу, содержащую атом кислорода, такую, как пиранил, диоксинил или фурил;
конденсированные насыщенные или ненасыщенные гетероциклические группы, содержащие от 1 до 3 атомов кислорода, такие, как бензофуранил, хроменил или ксантенил;
ненасыщенную 3-6-членные гетеромоноциклическую группу, содержащую от 1 до 2 атомов серы, такую, как тиенил или дитиолил;
ненасыщенную 3-6-членную гетеромоноциклическую группу, содержащую от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, такую, как оксазолил, оксазолинил, изоксазолил, фуразанил или оксадиазолил;
насыщенную 3-6-членную гетеромоноциклическую группу, содержащую от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, такую, как морфолинил;
ненасыщенную конденсированную гетероциклическую группу, содержащую от 1 до 2 атомов кислорода и от 1 до 3 атомов азота, такую, как бензоксазолил или бензоксадиазолил;
ненасыщенную 3-6-членную гетеромоноциклическую группу, содержащую от 1 до 2 атомов серы и от 1 до 3 атомов азота, такую, как тиазолил, тиазолинил или тиадиазоил;
насыщенную 3-6-членную гетеромоноциклическую группу, содержащую от 1 до 2 атомов серы и от 1 до 3 атомов азота, такую, как тиазолидинил; и
ненасыщенную конденсированную гетероциклическую группу, содержащую от 1 до 2 атомов серы и от 1 до 3 атомов азота, такую, как бензотиазолил или бензотиадиазолил.
Термин “ацил” относится к остатку карбоновой кислоты, в котором ОН заменена группой, например, определенной для W, Х и У, и может, в частности, означать карбамоил, алифатическую ацильную группу или ацильную группу, содержащую ароматическое кольцо, называемую ароматическим ацилом, или гетероциклическое кольцо, называемую гетероциклическим ацилом, предпочтительно, C1-20ацилом. Примеры подходящего ацила включают в себя карбамоил; неразветвленный или разветвленный алканоил, такой, как формил, ацетил, пропаноил, бутаноил, 2-метилпропаноил, пентаноил, 2,2-диметилпропаноил, гексаноил, гептаноил, октаноил, нонаноил, деканоил, ундеканоил, додеканоил, тридеканоил, тетрадеканоил, пентадеканоил, гексадеканоил, гептадеканоил, октадеканоил, нонадеканоил и икозаноил; алкоксикарбонил, такой, как метоксикарбонил, этоксикарбонил, третбутоксикарбонил, третпентилоксикарбонил и гептилоксикарбонил; циклоалкилкарбонил, такой, как циклопропилкарбонил, циклобутилкарбонил, циклопентилкарбонил и циклогексилкарбонил; алкилсульфонил, такой, как метилсульфонил и этилсульфонил; алкоксисульфонил, такой, как метоксисульфонил и этоксисульфонил; ароил, такой, как бензоил, толуоил и нафтоил; аралканоил, такой, как фенилалканоил (например, фенилацетил, фенилпропаноил, фенилбутаноил, фенилизобутаноил, фенилпентаноил и фенилгексаноил) и нафтилалканоил (например, нафтилацетил, нафтилпропаноил и нафтилбутаноил); аралкеноил, такой, как фенилалкеноил (например, фенилпропеноил, фенилбутеноил, фенилметакрилоил, фенилпентеноил и фенилгексеноил), и нафтилалкеноил (например, нафтилпропеноил, нафтилбутеноил и нафтилпентеноил); аралкоксикарбонил, такой, как фенилалкоксикарбонил (например, бензилоксикарбонил); арилоксикарбонил, такой, как феноксикарбонил и нафтилоксикарбонил; арилоксиалканоил, такой, как феноксиацетил и феноксипропионил; арилкарбамоил, такой, как фенилкарбамоил; арилтиокарбамоил, такой, как фенилтиокарбамоил; арилглиоксилоил, такой, как фенилглиоксилоил и нафтилглиоксилоил; арилсульфонил, такой, как фенилсульфонил и нафтилсульфонил; гетероциклокарбонил; гетероциклоалканоил, такой, как тиенилацетил, тиенилпропаноил, тиенилбутаноил, тиенилпентаноил, тиенилгексаноил, тиазолилацетил, тиадиазолилацетил и тетразолилацетил; гетероциклоалкеноил, такой, как гетероциклопропеноил, гетероциклобутеноил, гетероциклопентеноил и гетероциклогексеноил; и гетероциклоглиоксилоил, такой, как тиазолилглиоксилоил и тиенилглиоксилоил.
Термин “ацилокси” относится к ацилу, определенному здесь выше, в том случае, когда он связан через кислород.
В данном описании “необязательно замещенный” использован для обозначения того, что группа может быть, а может не быть далее замещена или конденсирована для образования конденсированной полициклической группы одной или более группами, выбранными из алкила, алкенила, алкинила, арила, галогена, галогеналкила, галогеналкенила, галогеналкинила, галогенарила, гидрокси, алкокси, алкенилокси, арилокси, бензилокси, галогеналкокси, галогеналкенилокси, галогенарилокси, нитро, нитроалкила, нитроалкенила, нитроалкинила, нитроарила, нитрогетероциклила, амино, алкиламино, диалкиламино, алкениламино, алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, ацила, алкенилацила, алкинилацила, арилацила, ациламино, диациламино, ацилокси, алкилсульфонилокси, арилсульфенилокси, гетероциклила, гетероциклокси, гетероцикламина, галогенгетероциклила, алкилсульфенила, арилсульфенила, карбоалкокси, карбоарилокси, меркапто, алкилтио, бензилтио, ацилтио, циано, нитро, сульфат- и фосфатгрупп. Термин “необязательно защищенная” использован для обозначения того, что группа, такая, как гидроксигруппа, может быть, а может не быть защищена защитной группой. Подходящие защитные группы известны и их примеры описаны в Protective Groups in Organic Synthesis, T.W. Greene (1981), John Wiley & Son.
Использованный здесь “гетероатом” относится к любому атому, отличному от атома углерода, который может являться членом циклического органического соединения. Примеры подходящих гетероатомов включают в себя азот, кислород, серу, фосфор, бор, кремний, мышьяк, селен и теллур, особенно, азот, кислород и серу.
Предпочтительными вариантами воплощения являются соединения формул (I) и (II), где U, определенный в Z, выбирают из CH2, NH, кислорода и серы. Более предпочтительно, U является NH или кислородом. Наиболее предпочтительно, U является кислородом. Для другого предпочтительного значения Z, n+о=0, 1, 2, 3 или 4. Подходящие примеры Z включают -О-СН2-, -CH2-N-, -О-СН2-О-, -(СН2)3-, -CH2-NH-CH2- или -CH2-O-CH2-. В следующем предпочтительном варианте воплощения и n, и о оба равны нулю.
В следующем предпочтительном варианте V является водородом, йодом или бромом.
Другими вариантами воплощения являются соединения формул (I) и (II), когда W и Х вместе с атомами азота и углерода, с которыми они связаны, образуют насыщенную или ненасыщенную гетероциклическую группу, причем эта группа предпочтительно представляет собой необязательно замещенный хинолинил, необязательно замещенный изохинолинил, необязательно замещенный дигидрохинолинил, необязательно замещенный дигидроизохинолинил, необязательно замещенный пиридил или их дигидро или тетрагидро-аналоги, или необязательно замещенный фенантридин. Предпочтительно, W и Х вместе с атомами азота и углерода, с которыми они связаны, образуют необязательно замещенную изохинолинильную или необязательно замещенную дигидроизохинолинильную группу общей формулы (i):
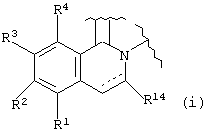
где R1-R4 и R14 такие, как определено выше для У, а 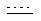 представляет собой необязательную двойную связь.
представляет собой необязательную двойную связь.
Предпочтительно, R1-R4 формулы (i) является водородом; гидрокси; необязательно замещенным алкилом; необязательно замещенным алкилокси; ацилокси; карбокси; сложным карбоксиэфиром, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым сложным эфиром; необязательно замещенным амино; карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила; или сульфатом. Наиболее предпочтительно они являются водородом, гидрокси, метокси, этокси, изо-пропокси, метилом, этилом, пропилом, ацетокси или сульфатом. Предпочтительно, R14 является водородом или гидрокси.
Следующим вариантом воплощения являются соединения формул (I) и (II), когда RA1RA2C-CRA3RA4 образует арильную группу или ароматическую гетероциклическую группу, она может быть необязательно замещенным бензольным или нафталиновыми кольцом или необязательно замещенной ароматической гетероциклической группой, такой, как пиридин, фуран, пиррол или тиофен, и их аналогами, конденсированными с бензолом, например, хинолином, индолом, бензофураном и бензотиофеном.
Присоединение бициклической гетероциклической группы может осуществляться через бензольное или гетероциклическое кольцо. Предпочтительно, RA1RA2C-CRA3RA4 образует необязательно замещенную бензольную группу. Предпочтительно, заместителями являются водород; гидрокси; необязательно замещенный алкил; необязательно замешенный алкилокси; ацилокси; карбокси; сложный карбоксиэфир, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым сложным эфиром; необязательно замещенный амино; карбоксамидо, в котором его атом необязательно замещен одной или двумя алкильными группами, независимо выбранными из метильной, этильной, пропильной или бутильной; или сульфатом. Наиболее предпочтительно, чтобы они являлись водородом, гидрокси, метокси, этокси, изо-пропокси, метилом, этилом, пропилом, ацетокси или сульфатом.
В следующем варианте воплощения RA1-A4 предпочтительно независимо выбирают из водорода, необязательно замещенного алкила, необязательно защищенного гидрокси, необязательно замещенного алкокси, необязательно замещенного фенила или ацилокси. В одном из предпочтительных вариантов воплощения, по меньшей мере, один из RA1 или RA3 может быть водородом. В другом варианте воплощения как RA1, так и RA3 являются водородом. Еще в следующем варианте воплощения три или четыре из RA1-A4 являются водородом.
В следующем варианте воплощения, когда RA2 и RA3 совместно образуют связь так, чтобы образовать группу RA1C=CRA4, каждый из RA1 и RA4 может быть независимо выбран из водорода; гидрокси; необязательно замещенного алкила; необязательно замещенного алкилокси; ацилокси; карбокси; сложного карбоксиэфира, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым сложным эфиром; необязательно замещенного амино или карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила. В особенно предпочтительных вариантах один или оба RA1 и RA4 являются водородом.
Когда RA2 и RA3 вместе с углеродами, с которыми они связаны, образуют карбоциклическую или гетероциклическую группу, как определено выше, предпочтительно, они образуют 3-8-членную циклическую группу, предпочтительно, 5-6-членную циклическую группу. Предпочтительно, они образуют циклопентановую, циклегексановую, циклопентеновую, циклогексеновую, циклопентадиеновую, циклогексадиеновую, тетрагидрофурановую, дигидрофурановую, пирролидиновую, пирролиновую, пирановую, дигидропирановую, тетрагидропирановую или пиперидиновую группу. Предпочтительно, RA1 и RA4 являются водородом.
В еще одном следующем варианте воплощения У предпочтительно является необязательно замещенной фенильной группой формулы (ii):
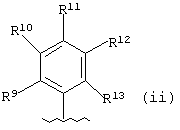
где R9-R13 такие, как определено для R1-R4, a R14 определен выше.
Более предпочтительно, R9-R13 являются водородом; гидроксилом; необязательно замещенным алкилом; необязательно замещенным алкилокси; ацилокси; карбокси; сложным карбоксиэфиром, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым сложным эфиром; необязательно замещенным амино; карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила; или сульфатом. Наиболее предпочтительно, R9-R13 выбирают из водорода, гидрокси, метокси, этокси, изо-пропокси, метила, этила, н-пропила, изо-пропила, ацетокси или сульфата.
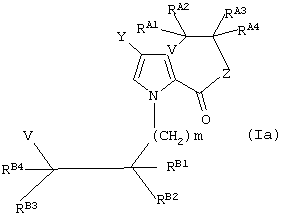
Следующий предпочтительный вариант воплощения являются соединения формулы (I), представляющие собой соединение формулы (Iа), где Х является водородом, a W является группой формулы (iii):
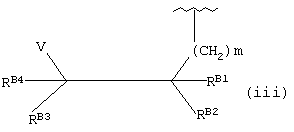
где V является водородом или галогеном; RВ1-В4 соответственно, как определено для RA1-A4 выше; а
m равно 1, 2, 3 или 4.
Таким образом, в предпочтительном варианте воплощения, настоящее изобретение относится к способу получения соединения формулы (IIа):
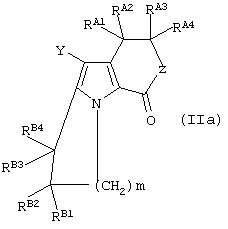
включающему стадию проведения двух внутримолекулярных циклизации соединения формулы (Iа):
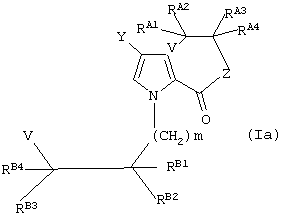
где:
RA1-A4, V, Y, Z имеют значения определенные выше;
RB1-B4 каждый независимо выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидрокси, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкенокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамидо, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано; или
RB2 и RB3 необязательно могут вместе образовывать связь, a RA1 и RA4 такие, как определено выше, или вместе с атомами углерода, с которыми они связаны, образуют необязательно замещенную карбоциклическую или гетероциклическую группу; или
RB2 и RB3 вместе с атомами углерода, с которыми они связаны, образуют необязательно замещенную насыщенную или ненасыщенную карбоциклическую или гетероциклическую группу; или
RB1RB2C-CRB3RB4 образуют необязательно замещенную арильную группу или ароматическую гетероциклическую группу; а
m равно 1, 2, 3 или 4.
Следующий предпочтительный вариант воплощения изобретения предоставляет промежуточное соединение формулы (Iа):
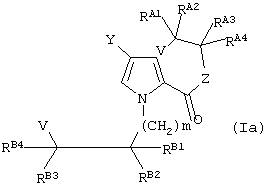
где:
RA1-A4, RB1-B4, V, Y, Z и m имеют значения, определенные выше, и, необязательно, одна или более (CH2) групп из групп (CH2)m, определенных в формуле (iii), может быть необязательно замещена группой R14, определенной выше.
В предпочтительном варианте m равно 1 или 2.
Более предпочтительно, когда m равно 2.
Следующими вариантами воплощения являются соединения формул (Iа) и (IIа), когда RB1RB2C-CRB3RB4 образует арильную группу или ароматическую гетероциклическую группу, она может быть необязательно замещенным бензольным или нафталиновым кольцом, или необязательно замещенной ароматической гетероциклической группой, такой, как пиридин, фуран, пиррол или тиофен, и их конденсированными с бензолом аналогами, например, хинолином, индолом, бензофураном и бензотиофеном. Присоединение бициклической гетероциклической группы может осуществляться через бензольное или гетероциклическое кольцо. Предпочтительно, RB1RB2C-CRB3RB4 образует необязательно замещенную бензольную группу. Когда RB1RB2C-CRB3RB4 образует замещенную бензольную группу (содержащую заместитель V), циклизация может привести к группе формулы (i), как здесь описано выше. Предпочтительно, заместителями являются водород, гидрокси, необязательно замещенный алкил, необязательно замещенный алкилокси, ацилокси, карбокси, сложный карбоксиэфир, в котором сложный эфир является предпочтительно метиловым, этиловым, пропиловым или бутиловый сложным эфиром; необязательно замещенный амино, карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила; или сульфат. Наиболее предпочтительными заместителями являются водород, гидрокси, метокси, этокси, изо-пропокси, метил, этил, пропил, ацетокси или сульфат.
В другом варианте воплощения RB1-B4 предпочтительно независимо выбирают из водорода, необязательно замещенного алкила, необязательно защищенного гидрокси, необязательно замешенного алкокси, необязательно замещенного фенила или ацилокси. В одном из предпочтительных вариантов воплощения, по меньшей мере, один из RB1 или RB3 может быть водородом. В другом варианте воплощения и RB1 и RB3 оба являются водородом. В еще одном варианте воплощения три или четыре из RB1-B4 являются водородом.
В следующем варианте воплощения, когда RB2 и RB3 вместе образуют связь так, чтобы образовать группу RB1C=СRB4, каждый из RB1 и RB4 может быть независимо выбран из водорода; гидрокси; необязательно замещенного алкила; необязательно замешенного алкилокси; ацилокси; карбокси; сложного карбоксиэфира, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым сложным эфиром; необязательно замещенного амино или карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила. В особенно предпочтительных вариантах один или оба RA1 и RA4 являются водородом.
Когда RB2 и RB3 вместе с углеродами, с которыми они связаны, образуют карбоциклическую или гетероциклическую группу, определенную выше, они предпочтительно образуют 3-8-членную циклическую группу, предпочтительно, 5-6-членную циклическую группу. Предпочтительно, они образуют циклопентановую, циклогексановую, циклопентеновую, циклогексеновую, циклопентадиеновую, циклегексадиеновую, тетрагидрофурановую, дигидрофурановую, пирролидиновую, пирролиновую, лирановую, дигидропирановую, тетрагидропирановую или пиперидиновую группу. Предпочтительно, RB1 и RB4 являются водородом.
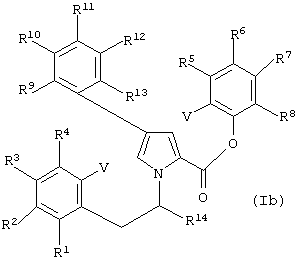
Особенно предпочтительные соединения формулы (I) имеют структуру приведенной ниже формулы (Ib):
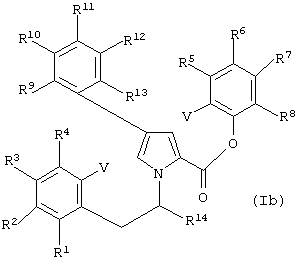
где R1-R14 независимо выбирают из водорода, необязательно замещенного алкила, необязательно замещенного алкенила, необязательно замещенного алкинила, необязательно защищенного гидрокси, необязательно замещенного амино, необязательно замещенного алкокси, необязательно замещенного алкенокси, необязательно замещенного алкинокси, необязательно замещенного арила, необязательно замещенного гетероциклила, карбокси, сложного карбоксиэфира, карбоксамидо, ацила, ацилокси, меркапто, необязательно замещенного алкилтио, галогена, нитро, сульфата, фосфата и циано. Предпочтительные R1-R14 выбирают из водорода; гидрокси; необязательно замещенного алкила; необязательно замещенного алкилокси; ацилокси; карбокси; сложного карбоксиэфира, в котором сложный эфир предпочтительно является метиловым, этиловым, пропиловым или бутиловым; необязательно замещенного амино, такого, как моно- или диалкиламино; карбоксамидо, в котором его атом азота необязательно замещен одной или двумя алкильными группами, независимо выбранными из метила, этила, пропила или бутила; или сульфата. Более предпочтительно R1-R13 выбирают из водорода; гидрокси; необязательно замещенного алкила, такого, как метил, этил или пропил; необязательно замещенного алкилокси, такого, как метокси, этокси, н-пропокси, изо-пропокси; ацилокси, такого, как ацетокси; или сульфата, a R14 предпочтительно является водородом или гидрокси. V является определенным выше, предпочтительно водородом, йодом или бромом.
Таким образом, в предпочтительном варианте изобретение предоставляет способ получения конденсированного полициклического пирролсодержащего соединения формулы (IIb):
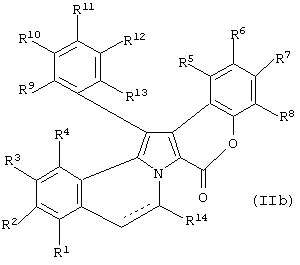
включающий стадию проведения двух внутримолекулярных циклизаций соединения формулы (Ib).
Внутримолекулярные циклизации соединений формулы (I), предпочтительно, формулы (Iа) или (Ib), с образованием полициклических конденсированных соединений формулы (II), предпочтительно формулы (IIа) или (IIb), можно осуществить любым подходящим образом, известным специалистам в данной области техники. Подходящие методы описаны ниже, однако любой другой метод, с помощью которого можно осуществить желаемую циклизацию, также составляет часть настоящего изобретения. Понятно, что группы V, W, X, Y, Z, RA1-A4, RB1-B4 и R1-14 являются такими, чтобы не препятствовать процессу циклизации.
В том случае, когда V представляет собой атом водорода, для осуществления циклизации можно использовать способ окислительной внутримолекулярной циклизации, такой, как описанно у Black et al., Tetrahedron Lett., 1989, 30, 5807, и Kita et al., Chem. Соmmunn., 1996, 1481.
Альтернативно, если V является атомом галогена, внутримолекулярная циклизация может протекать через генерацию подходящего радикала способом, аналогичным способу, описанному Antonio et al., Can. J. Chem., 1994, 72, 15 и Moody et al, Tetrahedron Lett., 1995, 36, 9501.
Еще один способ внутримолекулярной циклизации соединения формулы (I) в случае, когда V является галогеном, включает циклизацию с участием Pd[0]. Внутримолекулярное Pd[0]-катализируемое олефинирование органического галогенида (внутримолекулярная реакция Хека) известна специалистам в данной области и может быть осуществлена при помощи любого сочетания реагентов, которое обеспечит палладий в нейтральном состоянии (Pd[0]).
Подходящие сочетания реагентов для проведения Pd[0])-катализируемой циклизации описаны, например, у Burwood et
al, Tetrahedron Lett., 1995, 36, 9053; Desarbe et al, Heterocycles, 1995, 41, 1987; Harayoma et al, Chem. Pharm. Bull., 1997, 45, 1723; и Grigg et al. Tetrahedron, 1995, 50, 359.
Таким образом, в одном из вариантов воплощения изобретения Pd[0]-катализируемую циклизацию соединения формулы (I) можно осуществить, генерируя Pd[0] in situ при сочетании Pd(II) реагента и “лиганда”, и далее обеспечивая базу для генерации Pd[0]-катализатора.
Подходящие примеры Pd(II)/Pd(0) реагента включают в себя, но не ограничиваются ими: Pd(OAc)2, PdCl2(СН3СN)2, PdCl2(PPh3)2, Pd(C6H5CN)2Cl2, Pd (дибензилиденацетон)3.
Подходящие примеры “лиганд” обеспечивающих реагентов включают в себя, но не ограничиваются ими: РРh3, Р(о-толил)3, 1,3-бис[дифенилфосфино]пропан и 1,3-бис[дифенил-фосфино]этан.
Подходящие основания для генерирования Pd[0] из Pd[II], который образуется при Pd[0]-катализируемой циклизации, включают в себя, но не ограничиваются ими: алкиламины, такие, как триэтиламин и диизопропилэтиламин; ацетаты, такие, как ацетат натрия и ацетат калия; карбонаты, такие, как карбонат калия, карбонат натрия, карбонат серебра; и гидроксиды, такие, как гидроксид натрия и калия.
При обработке соединения формулы (Iа) или (Ib) с целью проведения двойной циклизации для получения соединения формулы (IIа) или (IIb) циклизацию можно осуществить радикальным, окислительным или Pd-катализируемым способами, как описано выше, и каждую циклизацию можно провести тем же самым, похожим, или другим образом.
Так, в одном из вариантов воплощения две циклизации можно осуществить последовательно, в любом порядке, и, необязательно, можно использовать различные реагенты и условия, например, описанные выше. Необязательно, после проведения одной циклизации моноциклизованный продукт можно выделять перед тем, как его обрабатывают в подходящих условиях для проведения второй внутримолекулярной циклизации. В другом варианте “двойную циклизацию” можно осуществить “в одной колбе”, предпочтительно, при единственном подборе условий реакции.
В более предпочтительном варианте соединение формулы (Iа), предпочтительно, (Ib), подвергают “двойной циклизации” для получения соединения формулы (IIа), предпочтительно, (IIb), в условиях катализа Pd[0].
В еще более предпочтительной форме обе циклизации осуществляют “в одной колбе”, при единственном подборе условий реакции.
Соединения формулы (I), (Ia) и (Ib) можно получить, исходя из пиррольного ядра, по известным специалистам стандартным методикам, которые направлены на проведение замещения атомов углерода пиррольного ядра, например, путем электрофильного ароматического замещения или путем галогенирования пиррольного ядра и проведения замещения по реакциям кросс-сочетания Штиля, Сузуки или Негуши с использованием станнана, бороновой кислоты или соединений цинка, таких, как арилстаннаны, арилбороновая кислота и арилцинковые соединения. Замещение N-атома можно осуществить по стандартным методикам.
Один из пригодных подходов, хотя никоим образом не ограничивающий, рассматриваемый как иллюстрация подходящих методов замещения пиррольного ядра, приведен далее на схеме 1.
Будет понятно, что при использовании соответствующих реагентов на стадиях, используемых для введения замещения в положениях 1-, 2-, 4- пиррольного ядра, например, фенилсодержащих реагентов, используемых на стадиях (d), (е) и (f), в которых фенильный фрагмент далее замещают, как здесь описано выше, для получения промежуточных соединений, поддающихся процессу циклизации и образованию соответствующих циклических соединений, можно ввести ряд моделей замещения и заместителей.
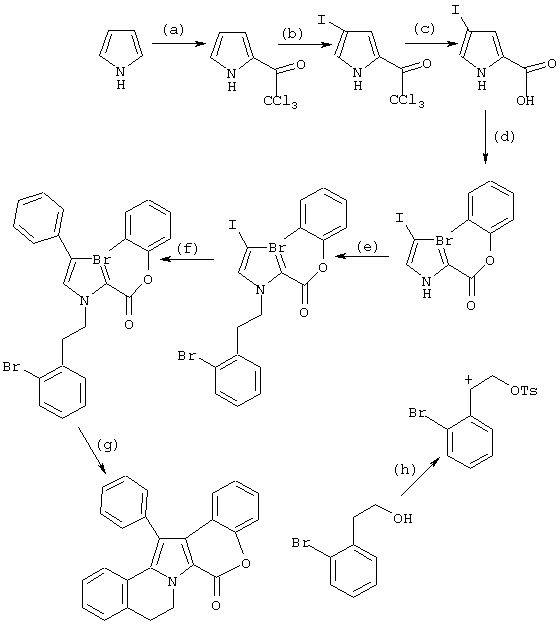
СХЕМА I
Схема 1: Реагенты и условия: (а) Сl3ССОСl (1 мол. экв.), Et2O, 35°С, 1 ч (80%); (b) I2 (1 мол. экв.), АqО2ССF3 (1 мол. экз.), СНСl3, 18°С, 1 ч (82%); (с) К2СО3 (2 М в H2O), ДМСО, 18°С, 32 ч (92%); (d) (i) (COCl)2 (1,1 мол. экв.), ДМФА (кат.), СН2Сl2, 18°С, 2 ч; (ii) о-бромфенол (1 мол. экв.), ДМАП (кат.), СН2Сl2, 18°С, 1 ч (92%); (е) К2СО3, (1,14 мол. экв.), Вu4МСl (0,1 мол. экв.), ДМФА, 80°С, 2 ч (90%); (f) PhZnCl (1,3 мол. экв.), PdCl2(PPh3)2 (0,05 мол. экв)/ ТГФ.ДМФА, 1 ч (95%); (g) Pd(OAC)2 (0,5 мол. экв.), PPh3, (1 экв.), NaOAc (4 экв.), ДМФА, 130°С, 6 ч (16%); (h) TsCl (2,4 мол. экв.), КОН (2,4 мол. экв.), Et2O, 0® 18°С, 2 ч (98%).
При наличии необязательной двойной связи, как в соединениях формулы (II), которые содержат часть формулы (I), таких как соединения формулы (IIb), ее можно ввести либо дегидрогенизацией продукта циклизации или, альтернативно, введением соответствующей двойной связи в его предшественник. Подходящие для этого методы будут известны специалистам (смотри, например, Advanced Organic Chemistry, Reactions, Mechanisms and Structure, Jerry March, 3-е издание, Wiley Interscience). Один из таких подходящих методов включает в себя обработку циклизуемого соединения формулы (IIb) ДДХ (2,3-дихлор-5,6-дициано-1,4-бензохинон). Например, диизопропиловый эфир ламелларина Т (соединение 37 в таблице 2) можно перевести в диизопропиловый эфир ламелларина W (соединение 11 в таблице 1) обработкой ДДХ в сухом хлороформе при 60-65°С (смотри пример 11 в WO 98/50365).
В WO 97/01336 (полное содержание которого взято для включения здесь в виде ссылки) соединения класса ламелларинов описаны, как обладающие ингибирующей и цитотоксической активностью по отношению к опухолям, устойчивым к большому числу лекарственных препаратов.
Соответственно, в следующем аспекте настоящего изобретения рассмотрен способ лечения, включающий введение эффективного для лечения количества соединения общей формулы (II), полученного по описанным здесь способам, в качестве активного ингредиента, животному, включая человека, нуждающемуся в этом.
Как использовано здесь, термин “эффективное количество” относится к такому количеству соединения, которое при введении в соответствии с желательным режимом дозировки обеспечивает желательную терапевтическую активность. Эта доза будет зависеть от возраста, веса и состояния субъекта, а определение подходящих дозировок находится в компетенции лечащего врача. Дозировка (назначение лекарственного препарата определенной дозы) может происходить с интервалом в минуты, часы, дни, недели, месяцы или годы, или постоянно в течение любого из этих периодов. Подходящие дозировки находятся в интервале от около 0,1 нг на кг массы тела до 1 г на кг массы тела на дозу. Предпочтительно, дозировка находится в интервале от около 1 мкг до 1 г на кг массы тела на дозу. Более предпочтительно, дозировка находится в интервале от около 1 мг до 1 г на кг массы тела. Удобно, чтобы дозировка находилась в интервале от около 1 мг до 500 мг на кг массы тела, например, между 1 мг и 250 мг, или 1 мг и 100 мг.
В предпочтительном варианте воплощения способ лечения относится к лечению опухолей, устойчивых к большому числу лекарственных препаратов.
В следующем варианте воплощения способ лечения предусматривает улучшение противоопухолевого хемотерапевтического эффекта лекарств, вызывающих устойчивость к большому числу лекарственных средств.
В следующем предпочтительном варианте воплощения способ лечения представляет собой способ индуцирования апоптоза. Более предпочтительно, способ лечения представляет собой способ индуцирозания апоптозз в клетке, устойчивой к бодьшому числу лекарств.
В следующем варианте воплощения способ лечения рассматривает модулирование иммунологических функций.
Активный ингредиент можно вводить в одной дозе или в разделенных дозах. Хотя активный ингредиент можно вводить сам по себе, предпочтительно чтобы он находился в композиции, предпочтительно, в фармацевтической композиции.
В следующем аспекте изобретения рассмотрены композиции, содержащие соединение общей формулы (II), полученное согласно настоящему изобретению, вместе с фармацевтически приемлемым носителем, эксципиентом или разбавителем.
Носитель должен быть фармацевтически “приемлемым” в смысле совместимости с прочими ингредиентами композиции и в отсутствии вреда для субъекта. Композиции включают в себя композиции для перорального, ректального, назального, местного (включая трансбуккальное и подъязычное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное и внутрикожное) введения. Композиции могут подходящим образом находиться в виде стандартной лекарственной формы и могут быть получены любым из известных в области фармации методов. Подобные методы включают в себя стадию объединения активного ингредиента с носителем, который составляет один или более дополнительных ингредиентов. Как правило, эти композиции готовят путем равномерного и тонкого объединения активного ингредиента с жидкими носителями или тонкоизмельченными твердыми носителями, или обоими, а затем, при необходимости, формования продукта.
Композиции настоящего изобретения, пригодные для перорального введения, могут находиться в виде отдельных единиц, таких, как желатиновые капсулы, саше или таблетки, каждая из которых содержит заранее определенное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; или в виде жидкой эмульсии масло в воде, или жидкой эмульсии вода в масле. Активный ингредиент может также находиться в виде болюса, электуария или пасты.
Таблетку можно изготовить путем прессования или формования, необязательно с одним или более дополнительными ингредиентами. Прессованные таблетки можно изготовить при прессовании в подходящем устройстве активного ингредиента в свободно-текучей форме, такой, как порошок или гранулы, необязательно в смеси со связующим веществом (например, инертным разбавителем, консервирующем разрыхлителем (гликолят крахмала натрия, сшитый поливинилпирролидон, сшитая натрий карбоксиметилцеллюлоза)), поверхностно-активным или диспергирующим агентом. Формованные таблетки можно изготовить путем формования в подходящем устройстве смеси порошкообразного соединения, увлажненного инертным жидким разбавителем. На таблетки можно необязательно нанести покрытие или зарубки и можно составить их таким образом, чтобы обеспечить быстрое или контролируемое высвобождение активного ингредиента с использованием, например, гидроксипропилметилцеллюлозы в различных пропорциях для обеспечения желательного профиля высвобождения. Таблетки можно необязательно покрыть кишечным покрытием для обеспечения высвобождения в частях кишок, а не в желудке.
Композиции, пригодные для местного введения через рот, включают в себя лепешки, содержащие активный ингредиент во вкусовой основе, обычно сахарозе и аравийской или трагакантовой камеди; пастилки, содержащие активный ингредиент в инертной основе, такой, как желатин и глицерин, или сахароза и аравийская камедь; и жидкости для полоскания рта, содержащие активный ингредиент в подходящей жидком носителе.
Композиции для ректального введения могут представлять собой суппозитории (свечи) с подходящей основой, включающей, например, масло какао.
Композиции, подходящие для вагинального введения, могут представлять собой пессарии, тампоны, крем, гель, пасту, пену или спрей, содержащие в дополнение к активному ингредиенту такие носители, которые, как известно из данной области техники, подходят для этого.
Композиции, пригодные для парентерального введения, включают водные и неводные изотонические стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактерициды и растворенные вещества, делающие эту композицию изотоничной с кровью ожидаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие агенты и загустители. Эти композиции могут представлять собой однодозовые или многодозовые запаянные контейнеры, например ампулы или сосуды, и могут храниться в высушенном методом вымораживания (лиофилизованном) состоянии, требуя лишь прибавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед использованием. Импровизированные растворы для инъекций суспензии можно получить из стерильных порошков, гранул и таблеток описанного выше типа.
Предпочтительными композициями со стандартной дозой являются композиции, содержащие дневную дозу или единицу, дневную субдозу, как здесь описано выше, или соответствующую ее фракцию активного ингредиента.
Следует понять, что в дополнение к активным ингредиентам, особо отмеченным выше, композиции данного изобретения могут включать другие обычные в данной области техники агенты, имеющие отношение к типу рассматриваемой композиции, например, композиции, подходящие для перорального введения, могут включать в себя такие дополнительные агенты, как связующие вещества, подсластители, загустители, ароматизаторы, разрыхляющие агенты, покрывающие агенты, консерванты, смазывающие вещества и/или задерживающие агенты. Подходящие подсластители включают в себя сахарозу, лактозу, глюкозу, аспартам или сахарин. Подходящие разрыхлители включают в себя кукурузный крахмал, метилцеллюлозу, поливинилпирролидон, ксантановую камедь, бентонит, альгиновую кислоту или агар-агар. Подходящие ароматизаторы включают в себя мятное масло, масло грушанки, вишневую, апельсиновую или малиновую отдушку. Подходящие покрывающие агенты включают в себя полимеры или сополимеры акриловой кислоты, и/или метакриловой кислоты, и/или их сложных эфиров, парафины, жирные спирты, цеин, шеллак или глютен. Подходящие консерванты включают в себя бензоат натрия, витамин Е, альфа-токоферол, аскорбиновую кислоту, метилпарабен, пропилпарабен или бисульфит натрия. Подходящие смазывающие вещества включают в себя стеарат магния, стеариновую кислоту, олеат натрия, хлорид натрия или тальк. Подходящие задерживающие агенты включают в себя глицерилмоностеарат или глицерилдистеарат.
Настоящее изобретение также представляет использование соединения общей формулы (II), полученного согласно настоящему изобретению, в производстве лекарственного препарата для лечения животного или человека, нуждающегося в этом.
В другом аспекте изобретения рассмотрен агент для лечения животного или человека, нуждающегося в этом, содержащий соединение общей формулы (II), полученное согласно настоящему изобретению.
В первом варианте воплощения агент предназначен для лечения опухолей, устойчивых к большому числу лекарств.
В следующем варианте воплощения агент предназначен для индуцирования аноптоза в клетке, устойчивой к большому числу лекарств.
В следующем варианте воплощения агент предназначен для усиления противоопухолевого хемотерапевтического эффекта лекарств, вызывающих устойчивость к большому числу лекарственных средств.
Следующим вариантом воплощения является агент для модулирования иммунологических функций.
Подходящие, но никоим образом не ограничивающие, примеры соединений, которые можно получить через промежуточные соединения данного изобретения, описаны ниже в таблицах 1 и 2:
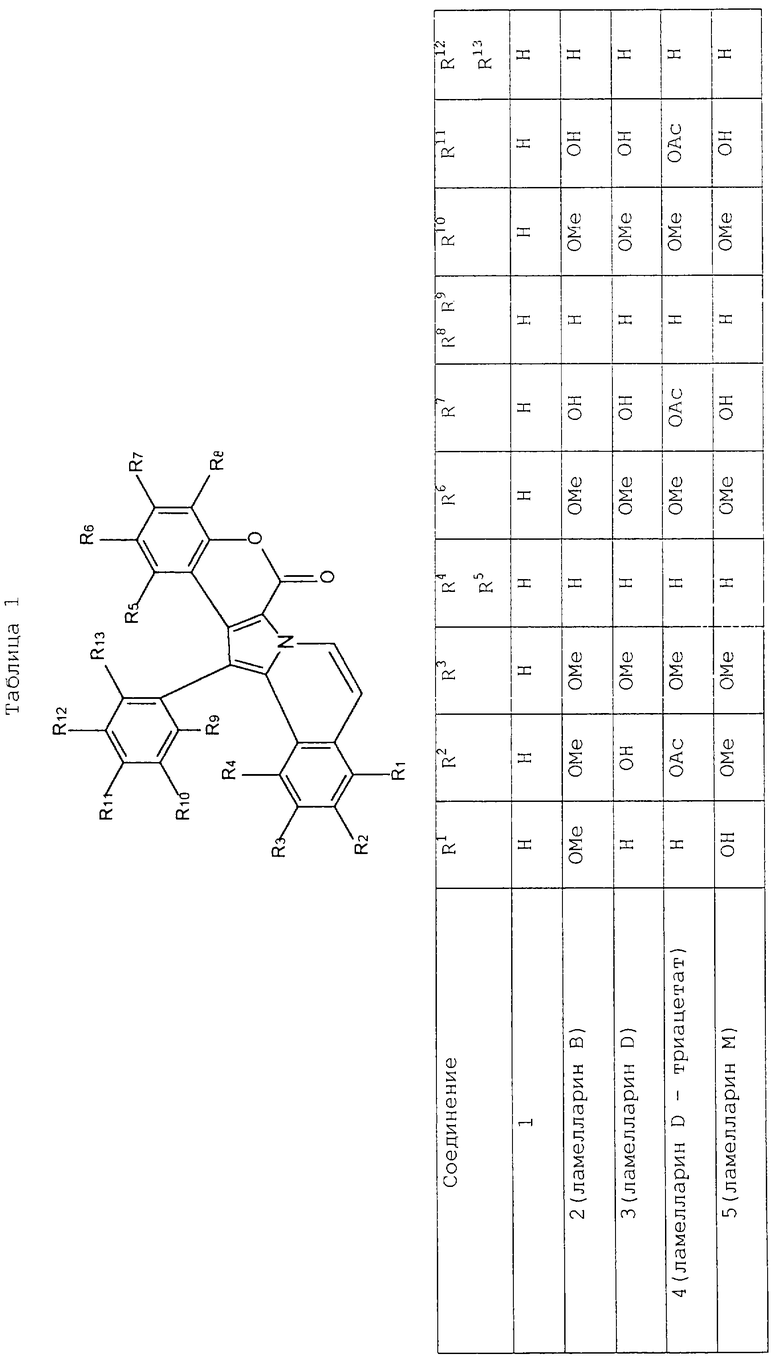
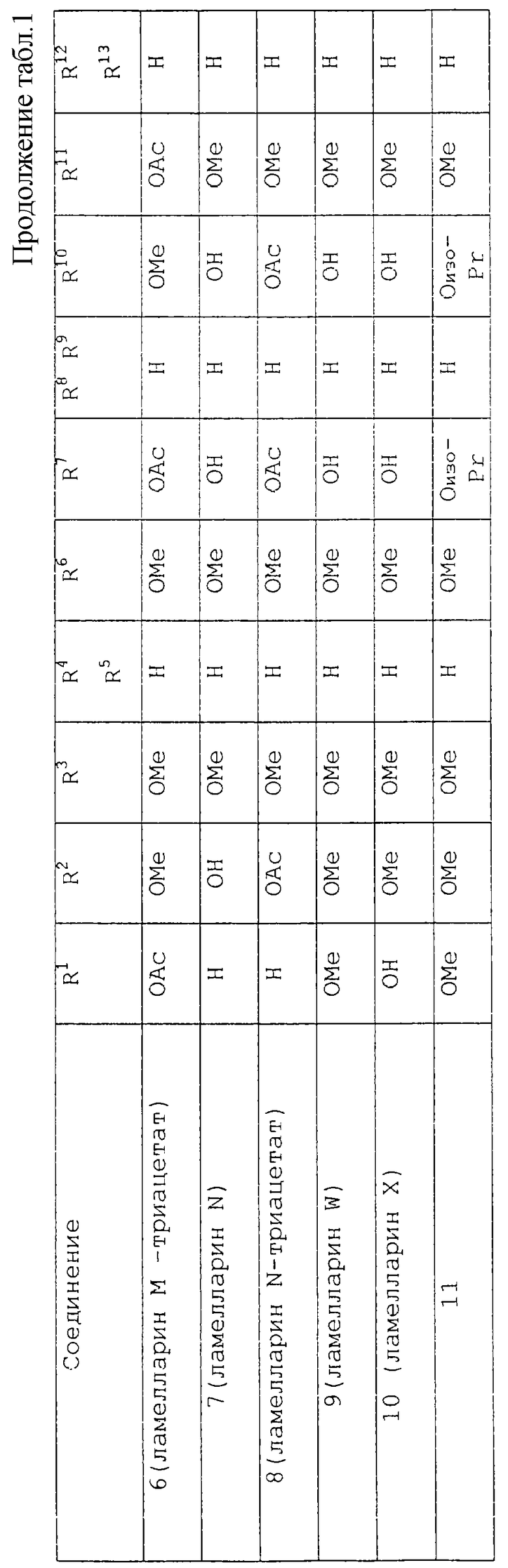
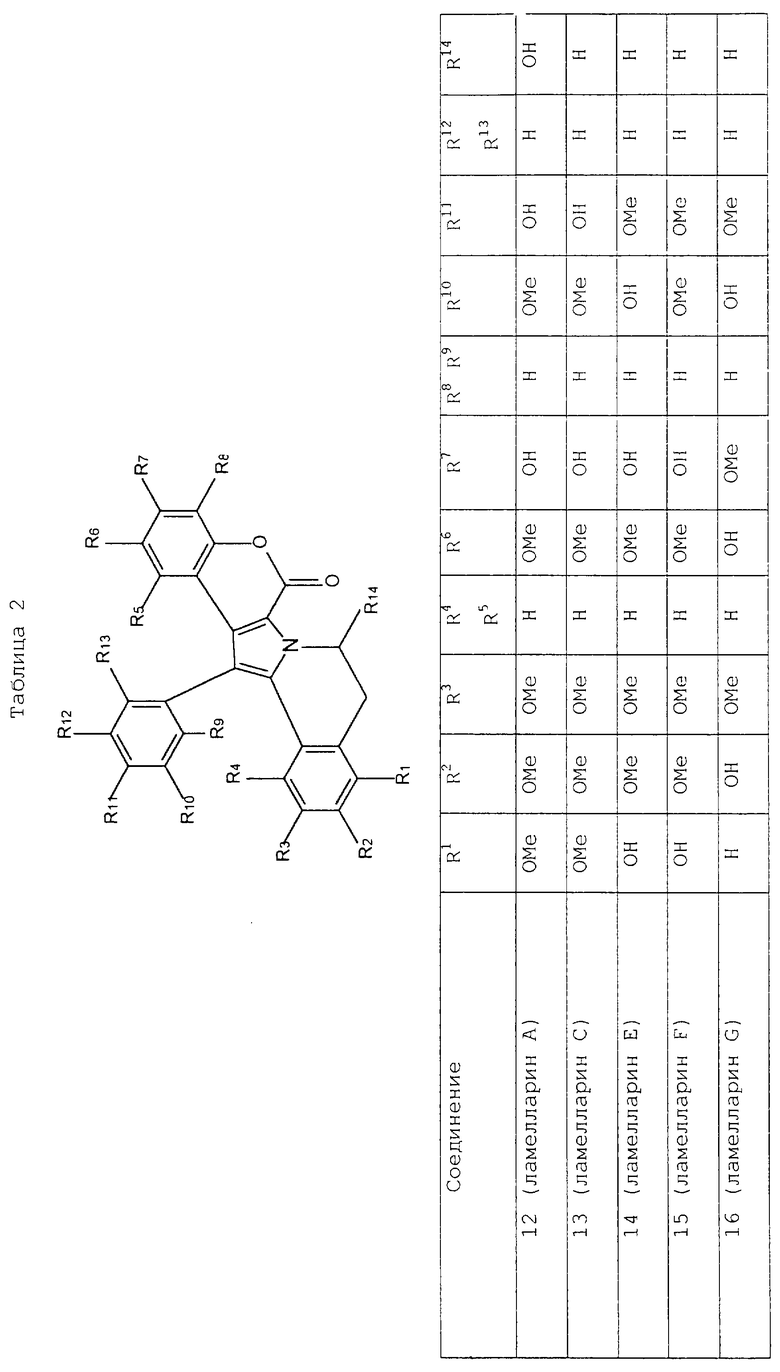
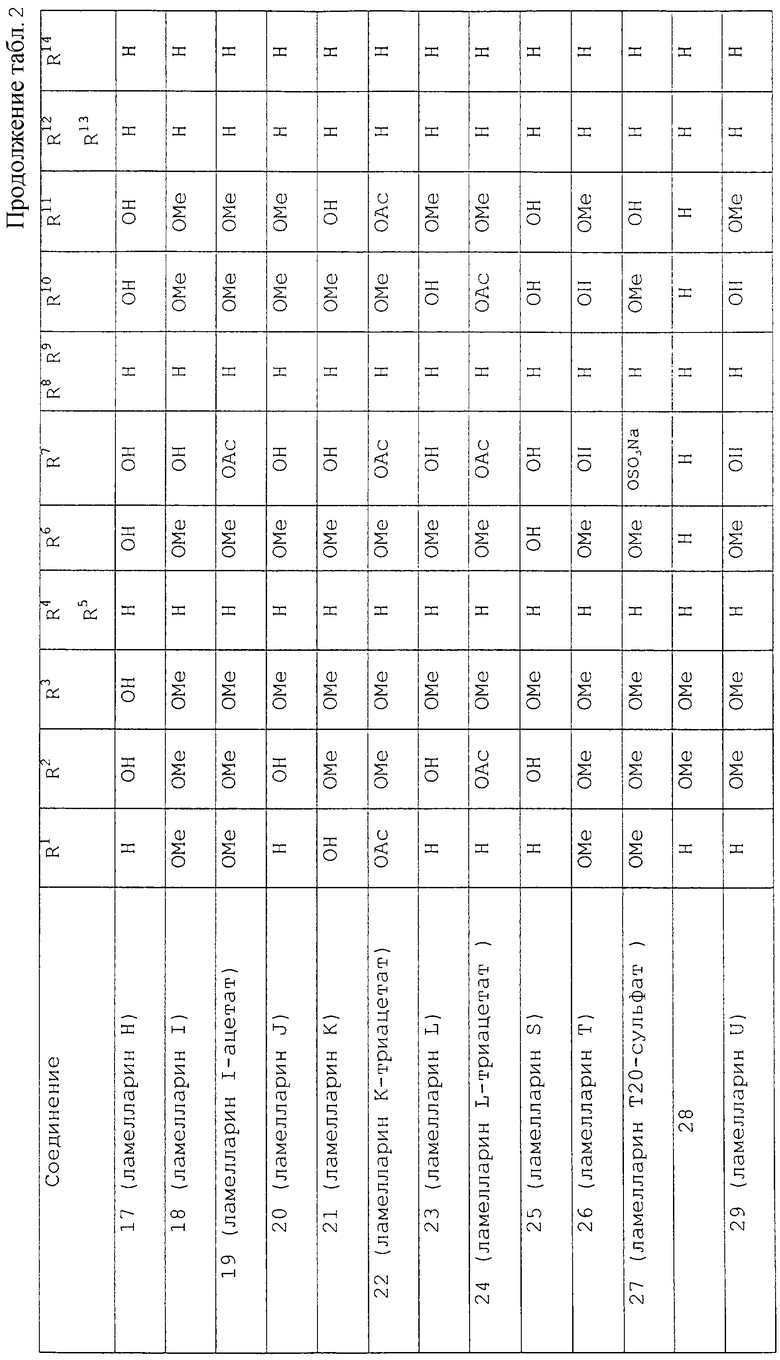
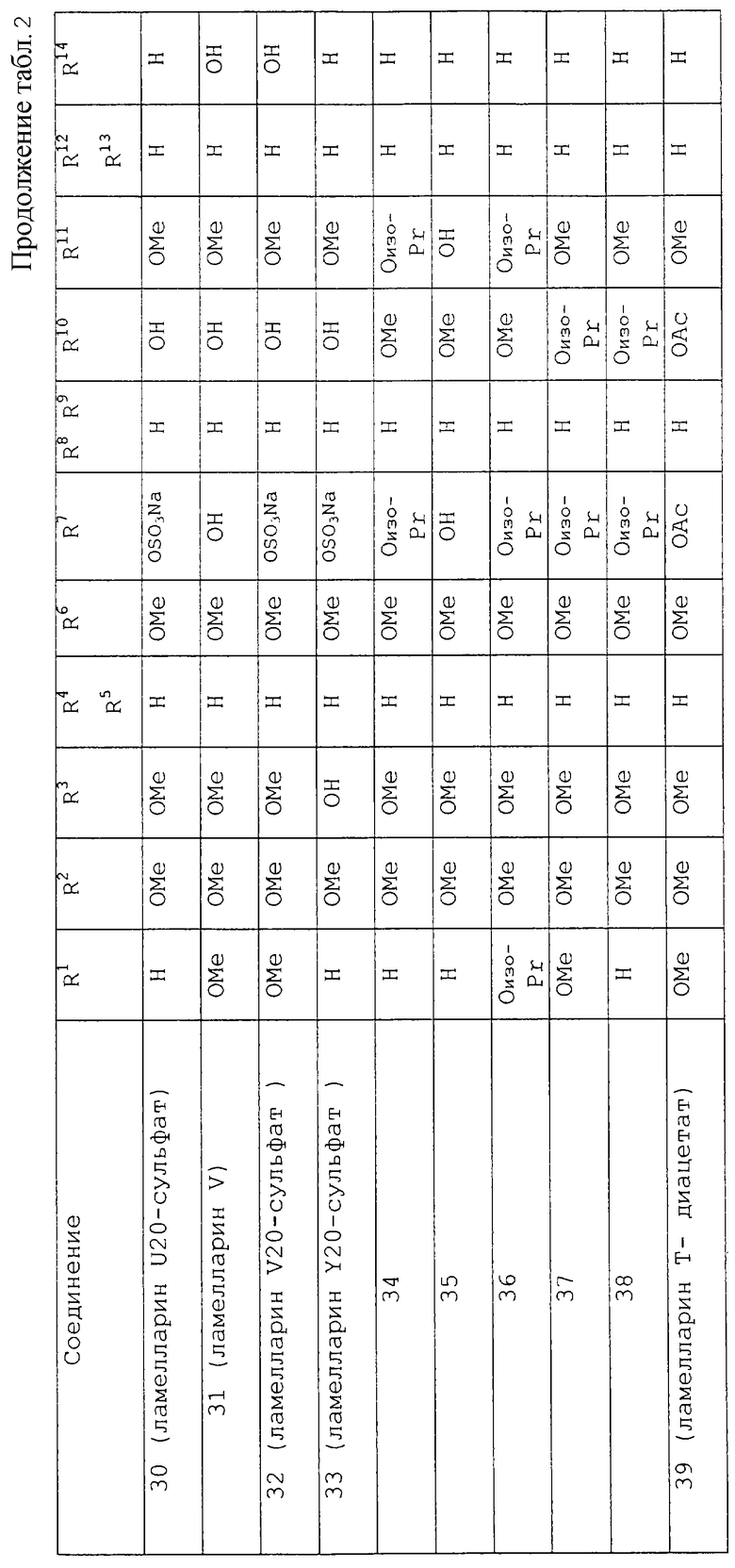
Теперь изобретение будет описано со ссылкой на следующие примеры. Однако необходимо понять, что они не заменяют общности предшествующего описания.
Примеры
Пример 1
2-(Трихлорацетил)пиррол
2-(Трихлорацетил)пиррол получают из пиррола (12,5 г, 186 ммоль) и трихлорацетилхлорида (36,5 г, 200 ммоль) по способу Bailey et al., Orq. Synth., 1971, 100. Таким образом, целевое соединение (31,3 г, 80%) получают в виде твердого вещества кремового цвета, т.пл. 73-74°С (точнее т.пл. 73-75°С). ЯМР 1H δ 9,30, шир. с. 1 Н; 7,39, м, 1 Н; 7,17, м, 1 Н; 6,40 дт, J 3,9 и 2,4 Гц, 1 Н (смотри также J. Оrg. Chem., 1972, 37, 3618; 1993, 58, 7245).
4-Йод-2-(Трихлорацетил)пиррол
Целевое соединение получают из 2-(Трихлорацетил) пиррола по способу Belanger, Tetrahedron Lett., 1979, 2505. Так, к перемешиваемой на магнитной мешалке смеси трифторацетата серебра (11,0 г, 49,8 ммоль) и 2-(трихлорацетил)пиррола (10,0 г, 47,1 ммоль) в сухом хлороформе (70 мл), выдерживаемой при 0°С (ледяная баня), прибавляют йод (12,0 г, 47,2 ммоль) порциями (приблизительно 1 г за порцию) в течение 0,17 ч. По завершении прибавления реакционной смеси дают нагреться до 18°С и перемешивают при этой температуре еще в течение 2 часов. Полученную суспензию фильтруют через воронку со стеклянным припоем (пористость №3), а фильтрат промывают Na2S2O5 (1×80 мл 5%-ный масс./об. водный раствор) и водой (2×80 мл.), сушат (MgSOq), фильтруют и концентрируют при пониженном давлении. Полученное при этом твердое вещество обрабатывают смесью гексан/эфир (50 мл смеси 4:1 об./об.) и полученную суспензию перемешивают при 18°С в течение 5 часов, затем твердое вещество отфильтровывают, получая целевое соединение (13,1 г, 82%) в виде твердого вещества кремового цвета, т.пл. 129-130°С (точнее т.пл. 128-130°С) ЯМР 1H δ 9,45, широкий с, 1 Н; 7,44, дд, J 2,6 и 1,3 Гц, 1 Н; 7,19, дд, J 2,6 и 1,3 Гц, 1 Н.
4-Йодпиррол-2карбоновая кислота
К раствору 4-йод-2-(трихлорацетил)пиррола (8,5 г, 2,5 ммоль) в ДМСО (30 мл) прибавляют К2СО3 (100 мл 2М водного раствора) и перемешивают полученную смесь при 18°С 3 часа, после чего разбавляют H2O (200 мл). Полученный при этом раствор промывают этилацетатом (2×100 мл), затем подкисляют до рН 3, прибавляя по каплям НСl (2 М водный раствор). Полученную суспензию экстрагируют этилацетатом (3×100 мл), а объединенные органические фракции сушат (MgSO4), фильтруют и концентрируют при пониженном давлении, получая целевое соединение (8) (5,51 г, 92%) в виде белого твердого вещества, т.пл. 200°С (Найдено: M+ - 236,9285. Для C5H4INO2 вычислено M+ - 236,9287). nmax (КВr) 3287, 3129, 3035, 1703, 1544, 1430, 1300, 1212, 1122 см-1. ЯМР 1H [300 МГц, 3:1 (СD3)2SO/СDСl3] δ 11,98 широкий с, 1 Н; 6,98, т, J 1,5 Гц, 1 Н; 6,76 уширенный с, 1 Н (резонанс вследствие ненаблюдаемой N-H). ЯМР 13С [75,5 МГц, 3:1 (СD3)2SO/СDСl3] δ 159,0 (С), 126,0 (СН), 123,3 (С), 118,8 (СН), 59,0 (С). Масс-спектр m/z 237 (100%) (М+); 219 (87) [(М-Н2О)+].
2-Бромфенил 4-йодпиррол-2-карбоксилат
К суспензии 4-йодпиррол-2-карбоновой кислоты (8) (500 мг, 2,11 ммоль) в сухом CH2Cl2 (15,0 мл), содержащей ДМФА (диметилформамид) (1 каплю), прибавляют оксалилхлорид (203 мл, 2,32 ммоль) при перемешивании на магнитной мешалке. После перемешивания полученного раствора при 18°С в течение 2 ч его добавляют к перемешиваемому на магнитной мешалке раствору о-бромфенола (363 мг, 2,11 ммоль), триэтиламина (660 мл, 4,73 ммоль) и 4-(N,N-диметиламино)пиридина (ДМАП, несколько кристаллов) в СН2Сl3 (10 мл). Спустя 1 ч реакционную смесь концентрируют на силикагеле (5 г) и повергают остаток флэш-хроматографии (силикагель, элюирование смесью гексан/эфир 3:1). При концентрировании соответствующих фракций (Rf 0,2) получают целевое соединение (761 мг, 92%) в виде белого кристаллического вещества, т.пл. 126-127°С (Найдено: С, 33,9; Н, 1,7; Вr, 20,4; I, 32,4; N, 4,0. Для С11Н7ВrINO2 вычислено С, 33,7; Н, 1,8; Вr, 20,4; I, 32,4; N, 3,6%). nmах 3383, 2969, 1709, 1580, 1541, 1472, 1444, 1377, 1312, 1218, 1169, 1133, 1043 см-1. ЯМР 1H δ 9,57 широкий С, 1 H; 7,65, дд, J 8,1 и 1,5 Гц, 1 Н; 7,37 тд, J 8,1 и 1,5 Гц, 1 H; 7,27, м, 2 Н; 7,18, тд, J 8,1 и 1,5 Гц, 1H; 7,08, м, 1 H. ЯМР 13С δ 158,0 (С), 148,3 (С), 134,0 (СН), 129,8 (СН), 129,1 (СН), 128,1 (СН), 124,4 (СН), 124,3 (СН), 123,6 (С), 116,9 (С), 62,9 (С). Масс-спектр m/z 393 (24%) 391 (22) (М+); 220 (100) [(M-C6H4BrO)+].
2-(2-Бромфенил)этил 4-метилбензолсульфонат (13)
Перемешиваемый на магнитной мешалке раствор 2-бромфенетилового спирта (5,00 г, 24,9 ммоль, ALDRICH) и 4-метилбензолсульфонилхлорида (11,20 г, 59,7 ммоль) в диэтиловом эфире (50 мл) охлаждают до 0°С (ледяная баня), затем обрабатывают растертым в порошок КОН (3,2 г, 2,4 молярного эквивалента). Полученной при этом реакционной смеси дают нагреться до 18°С, перемешивают при этой температуре в течение 2,0 ч, затем разбавляют водой (100 мл). Отделенную органическую фазу промывают водой (1×100 мл), затем сушат (МgSO4), фильтруют и концентрируют при пониженном давлении, получая белое твердое вещество. Поскольку это вещество содержит остаточный 4-метилбензолсульфонилхлорид, его растворяют в пиридине (75 мл) и полученный раствор перемешивают при 18°С в течение 0,16 ч, после чего разбавляют водой (500 мл) и экстрагируют диэтиловым эфиром (1×500 мл). Отделенную органическую фазу перед сушкой (MgSO4) промывают НС1 (1×250 мл 5М водного раствора), затем гидрокарбонатом натрия (1×250 мл 0,5М водного раствора), фильтруют и концентрируют при пониженном давлении, получая целевое соединение (8,66 г, 98%) в виде белой кристаллической массы, т.пл. 39-39,5°С (Найдено: С, 50,9; Н, 4,2; Вr, 22,6; S, 8,8. Для C15H15BrO3S вычислено С, 50,7; Н, 4,3; Вr, 22,5; S, 9,0%). nmах (КВr) 1356, 1177, 1021, 980, 962, 895, 812, 769, 752, 665, 557 см-1, ЯМР 1H δ 7,68, д, J 8,3 Гц, 2 Н; 7,45, д, J 7,7 Гц, 1 Н; 7,27, д, J 8,3 Гц, 2 Н; 7,17, м, 2 Н; 7,07, м, 1 Н; 4,25, т, J 7,0 Гц, 2 Н; 3,09, т, J 7,0 Гц, 2 Н; 2,43, с, 3 Н. ЯМР 13С δ 144,5 (С), 135,3 (С), 132,7 (СН), 132,8 (С), 131,3 (СН), 129,7 (СН), 128,5 (СН), 127,6 (СН), 127,4 (СН), 124,2 (С), 68,6 (СН2), 35,5 (СН2), 21,5 (СН3). Масс-спектр m/z 356 (0,7%) 354 (0,7) (M+); 184 (98) 182(100) [(М-H3CC6H4SO3H)+]; 171 (49) 169 (51); 155 (45); 103 (32); 91 (80) (С7H
2-Бромфенил 1-[2’-(2’’-бромфенил)этил]-4-йодпиррол-2-карбоксилат
К раствору соединения (11) (700 мг, 1,79 ммоль) в сухом ДМФА (30 мл) прибавляют соединение (13) (700 мг, 1,97 ммоль), тетраэтиламмонийхлорид (30 мг, 0,18 ммоль) и К2СО3 (278 мг, 2,0 ммоль) и перемешивают полученную суспензию при 80°С в течение 2 часов. Охлажденную реакционную смесь разбавляют этилацетатом (150 мл) и промывают водой (3×150 мл). Затем отделенную органическую фазу высушивают (MgSO4), фильтруют и концентрируют при пониженном давлении. Полученное при этом твердое вещество подвергают флэш-хроматографии (силикагель, элюирование смесью гексан/эфир 4:1) и при концентрировании соответствующих фракций (Rf 0,5, элюирование смесью гексан/эфир 3:1) получают целевое соединение (14) (920 мг,89%) в виде белого кристаллического твердого вещества, т.пл. 122-123°С (Найдено: С, 39,5; Н, 2,1; Вr, 27,6; I, 22,1; N, 2,3. Для C19H14Br2INO2 вычислено С, 39,7; Н, 2,5; Br, 27,8; I, 22,1; N, 2,4%). nmax (KBr) 2949, 1716, 1517, 1468, 1438, 1411, 1374, 1326, 1232, 1216, 1191, 1055, 1028 см-1. ЯМР 1H δ 7,65, дд, J 7,8 и 1,8 Гц, 1 Н; 7,55, дд, J 7,8 и 1,8 Гц, 1 Н; 7,37, м, 2 Н; 7,28-7,04, м, 5 Н; 6,70, д, J 2,1 Гц, 1 Н; 4,55, т, J 7,5 Гц, 2 Н; 3,20, т, J 7,5 Гц, 2 Н. ЯМР 13С δ 157,0 (С), 147,8 (С), 136,9 (С), 134,5 (СН), 133,3 (СН), 132,7 (СН), 131,2 (СН), 128,6 (СН), 128,4 (СН), 127,6 (СН), 127,3 (СН), 126,7 (СН), 124,4 (С), 124,0 (СН), 122,0 (С), 116,6 (С), 59,6 (С), 49,0 (CH2), 38,0 (CH2). Масс-спектр m/z 577 (1%) 575 (2) 573 (1) (М+); 496 (10) 494 (11) [(M-Br)+]; 404 (98) 402 (100) [(М-С6Н4ВrО)+].
2-Бромфенил 1-[2’-(2’’-бромфенил)этил]-4-фенилпиррол-2-карбоксилат (4)
К перемешиваемому на магнитной мешалке раствору соединения (14) (1,75 г, 3,04 ммоль) и Pd, (РРh3)2Cl2 (106 мг, 0,152 ммоль) в ДМФА (15 мл), прибавляют по каплям в течение 2 мин хлорид фенилцинка [полученный при прибавлении безводного хлорида цинка (540 мг, 3,96 ммоль) к раствору фениллития (2,0 мл 1,8 М раствора в смеси циклогексан/эфир, 3,6 ммоль) в ТГФ (4,0 мл)]. Перемешивание продолжают при 18°С в течение 1 ч, затем реакционную смесь переносят в разделительную воронку, разбавляют этилацетатом (100 мл) и промывают NH4Cl (100 мл насыщенного водного раствора), затем H2O (2×100 мл). Отделенную органическую фазу высушивают (МgSO4), фильтруют и концентрируют при пониженном давлении, получая светло-желтое масло, которое подвергают флэш-хроматографии (двуокись кремния, элюирование смесью 2:1 гексан/СН2Сl2). При концентрировании соответствующих фракций (Rf 0,5) получают целевое соединение (1,52 г, 95%) в виде микрокристаллического твердого вещества, т.пл. 90-92°С (найдено: С, 57,1; Н, 3,4; Вr, 30,7; N, 2,5. Для С25Н19Вr2NО2 вычислено С, 57,2; Н, 3,7; Вr, 30,4; N, 2,7%). nmах (КВr) 2958, 2930, 1718, 1603, 1580, 1562, 1472, 1397, 1215, 1196, 1066, 1024 см-1. ЯМР 1H δ 7,70, дд, J 8,0 и 1,5 Гц, 1 Н; 7,60-7,00, м, 14 Н; 4,63, т, J 6,9 Гц, 2 Н; 3,32, т, J 6,9 Гц, 2 Н. ЯМР 13С (75,5 МГц, CDCl3) δ 158,4 (С), 148,3 (С), 137,5 (С), 134,2 (С), 133,5 (СН), 132,9 (С), 131,5 (СН), 128,9 (СН), 128,6(3) (СН), 128,6(1) (СН), 127,8 (СН), 127,4 (СН), 127,3 (СН), 126,5 (СН), 125,4 (СН), 124,8 (С), 124,6 (С), 124,4 (СН), 120,9 (С), 117,5 (СН), 116,9 (С), 49,3 (СН2), 38,2 (СН2). Масс-спектр m/z 527 (3%) 525 (6) 523 (3) (М+); 446 (12) 444 (11) [(M-Br)+]; 354 (100) 352 (96) [(M-C6H4BrO)+].
14-Фенил-8,9-дигидро-6Н-[1]бензопирано[4’,3’:4,5] пирроло[2,1-а]изохинолин-6-он
К пeремешиваемому на магнитной мешалке раствору соединения (4) (148 мт, 0,292 ммоль), NaOAc (92,7 мг, 1,13 ммоль) и РРh3 (74,0 мг, 0,282 ммоль) в ДМФА (2 мл), содержащемуся в пробирке Шленка, прибавляют Pd(OAc)2 (32 мг, 0,143 ммоль). Из полученной смеси откачивают газ (1/0 мм рт.ст.) и вновь наполняют N2 (газообразным) три раза (для удаления растворенного кислорода), затем нагревают в атмосфере азота при 135°С в течение 6 ч. Охлажденную реакционную смесь разбавляют эфиром (25 мл) и перед сушкой (МgSO4) промывают рассолом (2×20 мл) и затем водой (20 мл), фильтруют и концентрируют на двуокиси кремния (2 г). Остаток подвергают флэш-хроматографии (двуокись кремния, элюирование смесью СН2Сl2-г/гексан 1:2, 1:1, затем 2:1) и при концентрировании соответствующих фракций (Rf 0,3, элюирование смесью 2:1 CH2Cl2/гeкcaн) при пониженном давлении получают целевое соединение (16 мг, 16%) в виде микрокристаллов кремового цвета, т.пл. 259-260°С (найдено: М+, 363,1257. Для C25H17NO2 вычислено М+, 363,1259). nmах (КВr) 2925, 2853, 1708, 1449, 1420, 1396, 1339, 1281, 1241, 1198, 1151, 1133, 1106, 1085, 1047 см-1. ЯМР 1H δ 7,58-7,55, м, 2 Н; 7,51-7,50, м, 3 Н; 7,40, дд, и 7,5 и 0,9 Гц, 1 Н; 7,32-7,18, м, 4 Н; 7,10, дд, J 7,8 и 1,2 Гц, 1 Н; 7,01-6,97, м, 3 Н; 4,88, т, J 6,9 Гц, 2 Н; 3,21, т, J 6,9 Гц, 2 Н. ЯМР 13С δ 155,3 (С), 151,2 (С), 135,6 (С), 135,3 (С), 133,8 (С), 130,7 (СН), 129,4 (СН), 128,3 (СН), 128,1 (СН), 127,5 (С), 127,4 (СН), 126,9 (СН), 125,7 (СН), 123,7 (СН), 123,3 (СН), 118,2 (С), 117,5 (С), 117,1 (СН), 42,3 (CH2), 29,3 (CH2) (три заслоненных или перекрывающихся пика). Масс-спектр m/z 363 (100%) (М+).
2’-Бромфенил 5,6-дигидро-1-фенилпирроло[2,1-а]изохи-нолин-3-карбоксилат (16) и бром{2’-(5’’,6’’-дигидро-1’’-фенилпирроло[2’’,1’’-а]изохинолин-3’’-карбокси)фенил}бис(трифенилфосфин)палладий (17)
К раствору соединения (4) (230 мг, 0,438 ммоль), NaOAc (80 мг, 0,975 ммоль) и РРh3 (460 мг, 1,75 ммоль) в ДМФА (20 мл) прибавляют Pd(OAc)2 (197 мг, 0,88 ммоль). Из полученного раствора откачивают газ (1,0 мм рт.ст.) и вновь наполняют N2 (газообразным) три раза для удаления растворенного кислорода, а затем нагревают в атмосфере азота при 110°С в течение 19 ч. Охлажденную реакционную смесь разбавляют этилацетатом (25 мл), затем промывают рассолом (2×20 мл) и водой (20 мл). После этого отделенную органическую фазу высушивают (МgSO4), фильтруют и концентрируют при пониженном давлении на двуокиси кремния (2 г). При очистке полученного вещества флэш-хроматографией (двуокись кремния, элюирование смесью 1:2, затем 1:1 CH2Cl2/гeкcaн, после чего 4:1 СН2Сl2/этилацетат) получают две фракции, А и В.
При концентрировании фракции A (Rf 0,6, элюирование смесью 2:1 CH2Cl2/гексан) получат соединение (16) (34 мг, 17%) в виде грязно-белой кристаллической массы, т. пл. 130-131°С (Найдено: М+, 443,0529. Для C25H2879BrNO2 вычислено М+, 443,0521). nmах (КВr) 2950, 1710, 1471, 1439, 1418, 1240, 1212, 1176, 1046 см-1. ЯМР 1Н δ 7,57, дд, J 8,1 и 1,5 Гц, 1 H; 7,45-7,05, м, 12 Н; 6,95, шир. т, J 8,1 Гц, 1 Н; 4,57, т, J 6,3 Гц, 2 Н; 3,05, т, J 6,3 Гц, 2 Н. ЯМР 13С δ 158,5 (С), 148,1 (С), 136,1 (С), 133,4 (С), 133,3 (СК), 132,9 (С), 129,1 (СН), 128,6 (С), 128,4 (СH), 128,1 (С), 127,9 (СН), 127,7 (СН), 127,1 (СН), 126,9 (СН), 126,7 (СН), 125,5 (СН), 124,2 (СН), 123,5 (С), 121,3 (СН), 119,4 (С), 116,7 (С), 42,4 (CH2), 29,5 (CH2). Масс-спектр m/z 445(10%) 443 (9) (М+); 272 (100) [(M-C6H4BrO)+].
При концентрировании фракции В (Rf 0,1, элюирование CH2Cl2) получают соединение (17) (40 мг, 8,5%) в виде грязно-белой кристаллической массы, т.пл. 159-162°С. nmах (КВr) 3052, 2923, 1705, 1481, 1435, 1416, 1238, 1172, 1095, 1058, 1024 см-1. ЯМР 1H δ 7,65-7,40, м, 18 Н; 7,30-7,05, м, 22 Н; 6,58, м, 1 Н; 6,52, т, J 6,6 Гц, 1 Н; 6,39, м, 1 Н; 6,07, кв, J 6,6 Гц, 1 H; 4,73, м, 2Н; 3,05, м, 2 Н. ЯМР 13С δ 159,2 (С), 151,8 (С), 138,3 (СН), 136,5 (С), 134,8 (СН), 133,2 (С), 131,8 (С), 131,5 (С), 131,0 (С), 129,9 (СН), 129,8 (СН), 129,5 (СН), 129,0 (СН), 128,7 (С), 127,8 (СН), 127,5 (СН), 127,2 (СН), 127,0 (СН), 125,7 (СН), 125,0 (СН), 123,2 (С), 123,0 (СН), 121,9 (СН), 121,1 (С), 120,5 (СН), 42,2 (CH2), 29,7 (СН2). Масс-спектр m/z 365 (6) [(М-Pd(PPh3)2Br+H)+]; 277 (26); 272 (32) {[М-С6Н4OРd(РРh3)2Вr]+}; 262 (100) (Ph3P+).
1-Фенилпирроло[2,1-a]изохинолин (18) и 1-[2’-(2’’-бромфенил)этил]-4-фенилпиррол (19)
Раствор дибромида (4) (13 мг, 25 ммоль), транс-ди(м-ацетато)-бис[о-(ди-о-толилфосфино)бензил]дипалладия (11) Chem. Eur. J., 1997, 3, 1357, (2,5 мг, 2,5 ммоль) и безводного ацетата натрия (6,2 мг, 75 ммоль) в дегазированном N,N-диметилацетамиде (0,25 мл) нагревают в атмосфере азота при 140°С в течение 72 часов, после этого охлажденную реакционную смесь разбавляют диэтиловым эфиром (5 мл) и промывают полученный раствор смесью рассол/вода (3×5 мл смеси 1:1 об/об). Затем органическую фазу высушивают (МgSO4), фильтруют и концентрируют при пониженном давлении, получив светло-желтое масло. После очистки этого вещества флэш-хроматографией (двуокись кремния, элюирование смесью 3:7, затем 7:3 СН2Сl2/гексан) получают, после концентрирования соответствующих фракций (Rf 0,7, элюирование смесью 3:7 CH2Cl2/гексан), смесь 1:3 соединений (18) и (19) (4 мг, общий выход 52%) в виде светло-желтого и неустойчивого масла. nmах (КВr) 1705, 41,2, 1555, 1500, 1471, 1441, 1359, 1202, 1071, 1027, 751, 694, 655 см-1. ЯМР 1H δ [соединение (18)] 7,60-6,95, сложный м, 9 Н; 6,92, т, J 2,0 Гц, 1 Н, Н-2; 6,63, т, J 1,6 Гц, 1 Н, Н-5; 6,43, уширенный т, J 2,3 Гц, 1 Н, Н-4; 4,14, т, J 7,7 Гц, 2 Н; [соединение (19)] 7,60-6,95, сложный м, 9 Н; 6,73, д, J 2,7 Гц, 1 Н, Н-3; 6,23, д, J 2,7 Гц, 1 Н, Н-2; 4,08, т, J 7,7 Гц, 2 Н; 3,10, т, J 7,7 Гц, 2 Н. Г.х./м.с. [соединение (18)] (Rf 4,52 мин) 245 (100) (М+.), 167 (21), 149 (28), 120 (6); [соединение (19)] (Rf 5,85 мин) 327 (12) 325 (12) (М+.), 246 (100) [(M-Br.)+].
На протяжении этого описания и последующей формулы изобретения, если в контексте не подразумевается другое, слово “включать” и варианты, такие, как “включает” и “включающий”, следует понимать как означающие включение заявленного целого или стадии, или группы целых или стадий, но не как исключающие любое другое целое или стадию, или группу целых или стадий.
Специалистам в данной области будет понятно, что описанное здесь изобретение допускает изменения и модификации, отличающиеся от тех, которые конкретно описаны. Необходимо понять, что данное изобретение включает в себя все подобные изменения и модификации. Кроме того, данное изобретение включает в себя все стадии, особенности, композиции и соединения, на которые ссылались или указывали в данном описании, по отдельности или вместе, и любую и все сочетания любых двух или более упомянутых стадий или особенностей.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКСЫ МЕТАЛЛОВ ДЛЯ ИСПОЛЬЗОВАНИЯ В РЕАКЦИЯХ ОБМЕНА ОЛЕФИНОВ И ПЕРЕНОСА АТОМОВ ИЛИ ГРУПП | 2005 |
|
RU2394039C2 |
| Новый ингибитор на основе производного хинолина | 2019 |
|
RU2802283C2 |
| ДЕАЗАПУРИНЫ И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2380368C2 |
| ПРОТИВОВИРУСНЫЕ СОЕДИНЕНИЯ | 2006 |
|
RU2441869C2 |
| АРИЛФОСФОРАМИДАТЫ НУКЛЕОЗИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВОВИРУСНЫХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА С | 2007 |
|
RU2464272C2 |
| СОЕДИНЕНИЯ ИНГИБИТОРЫ VLA-4 | 2000 |
|
RU2264386C2 |
| ПИРИДО [2,3-d] ПИРИМИДИНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ HCV, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2444522C2 |
| КОМБИНАЦИИ, ВКЛЮЧАЮЩИЕ АГОНИСТ РЕЦЕПТОРА S1P И ИНГИБИТОР КИНАЗЫ JAK3 | 2005 |
|
RU2415678C2 |
| 6,7,8,9-ЗАМЕЩЕННЫЕ 1-ФЕНИЛ-1,5-ДИГИДРОПИРИДО (3,2-b) ИНДОЛ-2-ОНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ АНТИИНФЕКЦИОННЫХ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2377243C2 |
| 5-(ГИДРОКСИМЕТИЛЕН- И АМИНОМЕТИЛЕН)ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2452737C2 |
Изобретение касается способов получения ламеллариновых соединений формулы II:
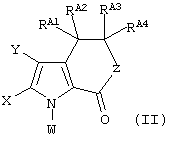
который включает стадию проведения внутримолекулярной циклизации соединения формулы (I):
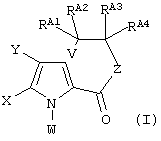
в которой:
RA1RA2C-CRA3RA4 образуют арильную группу, необязательно замещенную заместителем, или ароматическую 3-6-членную гетеромоноциклическую группу с одним атомом азота, необязательно замещенную заместителем;
Y выбирают из водорода; С1-20алкила, необязательно замещенного заместителем; С2-20алкенила, необязательно замещенного заместителем; C2-20алкинила, необязательно замещенного заместителем; гидрокси; амино, необязательно замещенного заместителем; С1-20алкокси, необязательно замещенного заместителем; С2-20алкенокси, необязательно замещенного заместителем; С2-20алкинокси, необязательно замещенного заместителем; арила, необязательно замещенного заместителем; насыщенной или ненасыщенной 3-6-членной гетеромоноциклической группы с одним атомом азота, необязательно замещенной заместителем; карбокси; сложного карбоксиэфира; карбоксамида; C1-20ацила; C1-20ацилокси; меркапто; С1-20алкилтио, необязательно замещенного заместителем; галогена; нитро; сульфата; фосфата и циано;
W и Х вместе с атомами азота и углерода, с которыми они связаны, образуют группу, выбранную из хинолинильной группы, необязательно замещенной заместителем; изохинолинильной группы, необязательно замещенной заместителем; дигидрохинолильной группы, необязательно замещенной заместителем; дигидроизохинолинильной группы, необязательно замещенной заместителем; пиридильной группы, необязательно замещенной заместителем, или из дигидро- или тетрагидропроизводных указанных структур, или фенантридина, необязательно замещенного заместителем;
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, C1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоС6-С24арилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата;
V является атомом галогена или атомом водорода; О; и промежуточных соединений формул Iа и Ib:
5 н. и 23 з.п. ф-лы, 2 табл.
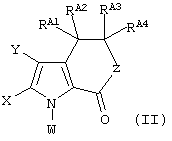
включающий стадию проведения внутримолекулярной циклизации соединения формулы (I):
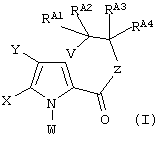
в которой RA1RA2C-CRA3RA4 образуют арильную группу, необязательно
замещенную заместителем, или ароматическую 3-6-членную гетеромоноциклическую группу с одним атомом азота, необязательно замещенную заместителем;
Y выбирают из водорода; С1-20алкила, необязательно замещенного заместителем; С2-20алкенила, необязательно замещенного заместителем; С2-20алкинила, необязательно замещенного заместителем; гидрокси; амино, необязательно замещенного заместителем; С1-20алкокси, необязательно замещенного заместителем; C2-20алкенокси, необязательно замещенного заместителем; С2-20алкинокси, необязательно замещенного заместителем; арила, необязательно замещенного заместителем; насыщенной или ненасыщенной 3-6-членной гетеромоноциклической группы с одним атомом азота, необязательно замещенной заместителем; карбокси; сложного карбоксиэфира; карбоксамида; С1-20ацила; С1-20ацилокси; меркапто; С1-20алкилтио, необязательно замещенного заместителем; галогена; нитро; сульфата; фосфата и циано; W и Х вместе с атомами азота и углерода, с которыми они связаны, образуют группу, выбранную из хинолинильной группы, необязательно замещенной заместителем; изохинолинильной группы, необязательно замещенной заместителем; дигидрохинолильной группы, необязательно замещенной заместителем; дигидроизохинолинильной группы, необязательно замещенной заместителем; пиридильной группы, необязательно замещенной заместителем, или из дигидро- или тетрагидропроизводных указанных структур, или фенантридина, необязательно замещенного заместителем;
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата;
V является атомом галогена или атомом водорода;
Z выбран из NH или О.
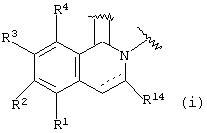
где R1 - R4 и R14 определены для Y в п.1, а 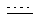 представляет собой необязательную двойную связь.
представляет собой необязательную двойную связь.
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата.
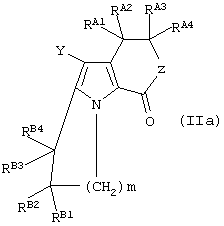
включающий стадию проведения двух внутримолекулярных циклизаций в соединении формулы (Iа):
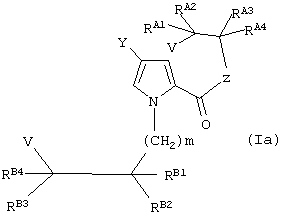
где
RA1 - RA4, V, Y, Z определены в п.1;
RB1RB2C-CRB3RB4 образуют арильную группу, необязательно замещенную заместителем, или ароматическую 3-6-членную гетеромоноциклическую группу с одним атомом азота, необязательно замещенную заместителем,
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоC1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата, и
m равно 2.
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила. С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата.
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата.
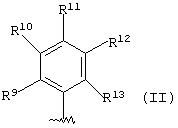
где R9 - R13 определены также, как R1 - R4 в п.2.
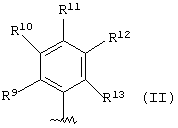
где R9 - R13 определены также, как R1 - R4 в п.4.
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоC1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата.
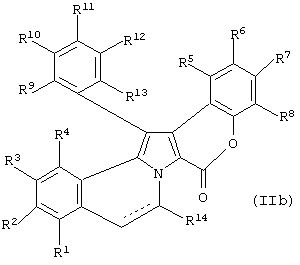
включающий стадию проведения двух внутримолекулярных циклизаций в соединении формулы (Ib):
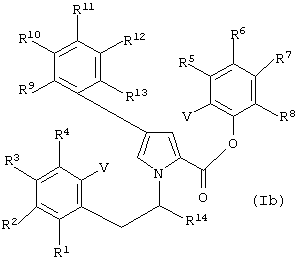
где V является галогеном или водородом, а R1 -R14 независимо выбирают из водорода; C1-20алкила, необязательно замещенного заместителем; С2-20алкенила, необязательно замещенного заместителем; С2-20алкинила, необязательно замещенного заместителем; гидрокси; амино, необязательно замещенного заместителем; С1-20алкокси, необязательно замещенного заместителем; С2-20алкенокси, необязательно замещенного заместителем; С2-20алкинокси, необязательно замещенного заместителем; арила, необязательно замещенного заместителем; насыщенной или ненасыщенной 3-6-членной гетеромоноциклической группы с одним атомом азота, необязательно замещенной заместителем; карбокси; сложного карбоксиэфира; карбоксамидо; C1-20ацила; С1-20ацилокси; меркапто, C1-20алкилтио, необязательно замещенного заместителем; галогена, нитро, сульфата, фосфата и циано,
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, C1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, C1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, C1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоC1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата, и
необязательную дегидрогенизацию продукта циклизации с образованием соединения формулы (Ib), в котором имеется необязательная двойная связь  .
.
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, С1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), С1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, С1-20алкилтио, бензилтио, С1-20ацилтио, циано, сульфата и фосфата.
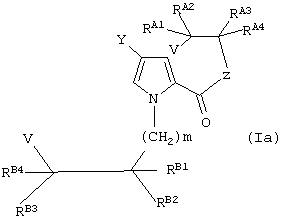
где RA1 - RA4, RB1 - RВ4, V, Y и m определены в п.4, a Z является О.
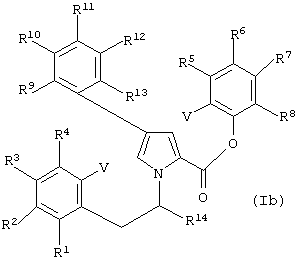
где
R1 - R14 независимо выбирают из водорода; С1-20алкила, необязательно замещенного заместителем; необязательно замещенного С2-20алкенила, необязательно замещенного заместителем; С2-20алкинила, необязательно замещенного заместителем; гидрокси; амино, необязательно замещенного заместителем; С1-20алкокси, необязательно замещенного заместителем; С2-20алкенокси, необязательно замещенного заместителем; С2-20алкинокси, необязательно замещенного заместителем; арила, необязательно замещенного заместителем; насыщенной или ненасыщенной 3-6-членной гетеромоноциклической группы с одним атомом азота, необязательно замещенной заместителем; карбокси; сложного карбоксиэфира; карбоксамидо; С1-20ацила, C1-20ацилокси, меркапто, С1-20алкилтио, необязательно замещенного заместителем; галогена, нитро, сульфата, фосфата и циано;
где указанный необязательно присутствующий заместитель выбран из С1-20алкила, С2-20алкенила, С2-20алкинила, арила, галогена, галогенС1-20алкила, галогенС2-20алкенила, галогенС1-20алкинила, галогенарила, гидрокси, С1-20алкокси, С2-20алкенилокси, арилокси, бензилокси, галогенС1-20алкокси, галогенС1-20алкенилокси, галогенарилокси, нитро, нитроС1-20алкила, нитроС2-20алкенила, нитроС2-20алкинила, нитроарила, нитро(3-6-членного гетеромоноциклила с одним атомом азота), амино, С1-20алкиламино, диС1-20алкиламино, С2-20алкениламино, С2-20алкиниламино, ариламино, диариламино, бензиламино, дибензиламино, С1-20ацила, С2-20алкенилацила, С2-20алкинилацила, арилацила, С1-20ациламино, диС1-20ациламино, С1-20ацилокси, C1-20алкилсульфонилокси, арилсульфенилокси, 3-6-членного гетеромоноциклила с одним атомом азота, (3-6-членный гетеромоноциклил с одним атомом азота)окси, (3-6-членный гетеромоноциклил с одним атомом азота)амино, галоген(3-6-членный гетеромоноциклила с одним атомом азота), C1-20алкилсульфенила, арилсульфенила, карбоС1-20алкилокси, карбоарилокси, меркапто, C1-20алкилтио, бензилтио, C1-20ацилтио, циано, сульфата и фосфата, и V является галогеном или водородом,
| Aust.J.Chem | |||
| Механическая топочная решетка с наклонными частью подвижными, частью неподвижными колосниковыми элементами | 1917 |
|
SU1988A1 |
| Устройство для радиоприема | 1924 |
|
SU1583A1 |
| J | |||
| Am | |||
| Chem | |||
| Soc | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| US 3407199, 22.10.1968 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5-НИТРОПИРРОЛА | 1967 |
|
SU225089A1 |
Авторы
Даты
2005-04-20—Публикация
1999-06-25—Подача