Изобретение относится к области получения производных 5-нитропиррола, которые могут найти применение как антибактериальные и антивирусные средства.
Предлагаемый способ получения соединения формулы
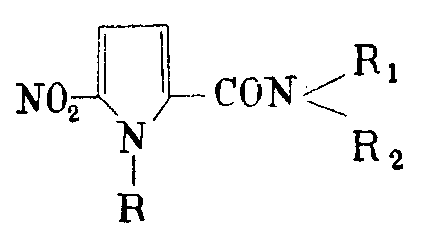
где R является алкильным остатком с 1-4 атомами углерода, который может быть замещенным, или аралкильным остатком, и R1 и R2, которые могут быть одинаковыми или различными, обозначают атом водорода, алкильный остаток с 1-4 атомами углерода, который может быть замещенным, или циклоалкильный остаток, или образуют вместе с атомом азота гидразиновый остаток или насыщенный одноядерный гетероцикл с 5- или 6-звеньями, в данном случае он может содержать второй гетероатом из группы кислорода, серы или азота, например пирролидинил-(1), причем, если R1=R2-Н, остаток в случае незамещенного алкильного радикала должен иметь по меньшей мере 2 атома углерода.
Предлагаемый способ состоит в том, что щелочное производное соответственно замещенного 5-нитропиррола подвергают взаимодействию со сложным эфиром R-X, где R имеет вышеуказанные значения, а X обозначает атом галоида или остаток сложного эфира серной кислоты при сульфокислоты в среде органического растворителя, например диметилформамиде, преимущественно при температуре кипения растворителя.
Пример 1. К суспензии из 16,9 г 2-морфолинокарбонил-5-нитропиррола в 500 см3 абсолютного метанола добавляют 54 см3 9,5%-ного раствора этилата натрия в этаноле при 20°С. После 2-час перемешивания вводят в эту же реакционную смесь 40 см3 диметилформамида и выпаривают этанол при пониженном давлении и температуре ниже 50°С. Получают красноватый раствор производного натрия 2-морфолинокарбонил-5-нитропиррола, к которому добавляют раствор из 15,4 г этилсульфата в 25 см3 диметилформамида. Доводят реакционную смесь в течение 15 мин до кипения и оставляют ее затем на ночь при комнатной температуре.
Получают коричневый раствор, который вливают в 600 см3 ледяной воды. Образуется светло-бежевый осадок, его отсасывают, трижды промывают 50 см3 5%-ного раствора карбоната натрия и затем трижды 50 см3 дистиллированной воды и очищают в 75 см3 кипящего метанола в присутствии животного угля. После фильтрования, добавления 100 см3 предварительно нагретой до 50°С дистиллированной воды к фильтрату, охлаждения, фильтрования и сушки получают 14 г 1-этил-2-морфолинокарбонил-5-нитропиррола с т. пл. 100°С.
Пример 2. Готовят производное натрия из 16,9 г 2-морфолинокарбонил-5-нитропиррола, как описано в примере 1, и добавляют к его смеси с диметилформамидом раствор и 17 г йодистого пропила в 40 см3 диметилформамида. В течение 30 мин доводят до кипения и после охлаждения выливают оранжево-красный раствор в 700 см3 ледяной воды. Образуется бесцветный осадок, его очищают, как описано в примере 1. После сушки получают 7,5 г 1-пропил-2-морфолинокарбонил-5-нитропиррола с т. пл. 61-62°С.
Пример 3. По методике примера 1 добавляют к раствору соли натрия из 16,9 г 2-морфолинокарбонил-5-нитролиррола в диметилформамиде раствор из 18,4 г n-йодистого бутила 25 см3 диметилформамида и нагревают в течение 15 мин до кипения. Получают коричневый раствор, который после охлаждения растворяют в 600 см3 воды. Образуется коричневое твердое вещество, его промывают как в примере 1 и перекристаллизовывают из смеси этанола и воды. Получают 14,7 г 1-n-бутил-2-морфолинокарбонил-5-нитропиррола в т. пл. 88-89°С.
Пример 4. Реакцию проводят как в примере 1, но добавляют к раствору соли натрия из 18 г 2-морфолинокарбонил-5-нитропиррола в диметилформамиде 21,6 г йодистого изобутила и нагревают в течение 30 мин до кипения. Получают сильно окрашенный раствор, который после охлаждения поглощают в 800 см3 ледяной воды. Образуется черноватое масло, его экстрагируют в 250 см3 и затем трижды 100 см3 хлористого метилена. Промывают органическую фазу разбавленным натронным щелоком (5%-ный) и затем водой, сушат и выпаривают. Получают 11 г смазки, которая медленно затвердевает (т. пл. 45°С). Ее поглощают в 75 см3 кипящего метанола в присутствии животного угля. После фильтрования добавляют 150 см3 воды. Выпадает 6,9 г окрашенных в бежевый цвет кристаллов с т. пл. 58°С, их очищают хроматографией на окиси алюминия в простом изопропиловом эфире и новой перекристаллизацией из водного метанола. Получают, наконец, 4,5 г 1-изобутил-2-морфолинокарбонил-5-нитропиррола в форме бледно-желтых кристаллов с т. пл. 66°С.
Пример 5. Опыт проводят как в примере 1, но добавляют к раствору соли натрия из 22,5 г 2-морфолинокарбонил-5-нитропиррола в 100 см3 диметилформамида и 25 г хлористого бензила и нагревают в течение 1 час до кипения. Получают суспензию, ее поглощают в 100 см3 ацетона и фильтруют. Фильтрат выпаривают при пониженном давлении. Полученный жирный остаток растирают 100 см3 простого изопропилового эфира. После фильтрования и сушки получают 31 г кристаллов с т. пл. 92°С.
После перекристаллизации из смеси 150 см3 изопропилового спирта и 50 см3 простого изопропилового эфира получают 21,2 г 1-бензил-2-морфолинокарбонил-5-нитропиррола с т. пл. 98°С.
Пример 6. Работают как описано в примере 1, но добавляют к раствору соли натрия из 22,5 г 2-морфолинокарбонил-5-нитропиррола в 150 см3 диметилформамида 24,1 г гликольмонохлоргидрина и нагревают в течение 2 час при 140°С. После охлаждения выпаривают диметилформамид при пониженном давлении и поглощают остаток в 100 см3 воды и 100 см3 хлороформа. Размешивают до растворения, декантируют и экстрагируют водный слой трижды 50 см3 хлороформа. Органические экстракты трижды промывают 50 см3 водного 10%-ного раствора карбоната натрия и трижды 50 см3 воды, сушат их над сульфатом натрия и выпаривают. Получают 15,3 г кристаллов с т. пл. 120°С.
После перекристаллизации из 50 см3 кипящего метанола получают 11,2 г 1-(2-оксиэтил)-2-морфолинокарбонил-5-нитропиррола с т. пл. 132°С.
Новая перекристаллизация из метанола позволяет получить продукт с т. пл. 134°С.
Пример 7. Аналогично примеру 1 добавляют к раствору соли натрия из 20 г 2-морфолинокарбонил-5-нитропиррола в 130 см3 диметилформамида, 16,4 г 1-ацетокси-2-хлорэтана и нагревают 90 мин при 140-145°С. После охлаждения выпаривают диметилформамид и поглощают остаток в хлороформе и воде. Экстрагируют и промывают как в примере 6. Полученный после выпаривания хлороформа продукт растирают с 20 см3 петролейного эфира и 5 см3 метанола. После перекристаллизации из 10 см3 кипящего метанола получают 4,16 г 1-(2-ацетоксиэтил)-2-морфолинокарбонил-5-нитропиррола с т. пл. 82-84°С.
Пример 8. По примеру 1 добавляют к раствору соли натрия из 2,25 г 2-морфолинокарбонил-5-нитропиррола в 15 см3 диметилформамида 3,06 г бензилоксиэтил-n-толуолсульфоната и нагревают в течение 30 мин при 140-145°С. После охлаждения выпаривают диметилформамид при пониженном давлении, поглощают в воде и хлороформе, экстрагируют и промывают как в примере 6. После сушки и выпаривания хлороформа получают черновато-коричневый остаток, который очищают в кипящем метаноле в присутствии животного угля. Получают 1 г 1-(2-бензилоксиэтил)-2-морфолинокарбонил-5-нитропиррола с т. пл. 75°С.
Пример 9. Аналогично примеру 1 добавляют к раствору соли натрия и 11,3 г 2-морфолинокарбонил-5-нитропиррола в 100 см3 диметилформамида, 11,3 г N,N-диэтилхлорацетамида и нагревают в течение 30 мин при 145°С. После охлаждения выпаривают диметилформамид при пониженном давлении и получают жирный остаток, который затвердевает в разбавленном натронном щелоке (13%-ный).
После фильтрования, промывки до нейтрального состояния и сушки получают 8,6 г 1-(N,N-диэтилкарбамоилметил)-2-морфолинокарбонил-5-нитропиррола с т. пл. 117°С.
После очистки растворением в 25 см3 кипящего бензола, фильтрования и осаждения при помощи 60 см3 петролейного эфира получают 7,4 г вещества с т. пл. 119-120°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ароилзамещенных фенилуксусных кислот | 1973 |
|
SU719490A3 |
| Способ получения производных -фенилжирной кислоты или их солей | 1971 |
|
SU528865A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2 | 1972 |
|
SU345684A1 |
| ЯДТЕНТНО- ТЕХНИЧЕСКАЯ БИБЛИОТЕКА | 1969 |
|
SU240564A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЗЕПИНА ИЛИ ИХ СОЛЕИ | 1971 |
|
SU422149A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА | 1973 |
|
SU363248A1 |
| Способ получения 6-аза-3н-1,4-бензодиазепинов | 1972 |
|
SU468423A3 |
| Способ получения простых и сложных эфиров N-бензил-пипередил-2-арилкарбинолов | 1958 |
|
SU133424A1 |
| Способ получения проивзодных бензимидазола или их солей | 1975 |
|
SU581866A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 0-АНИЛИНО- ФЕНИЛЭТИЛОВЫХ СПИРТОВ | 1973 |
|
SU381217A1 |
Способ получения производных 5-нитропиррола формулы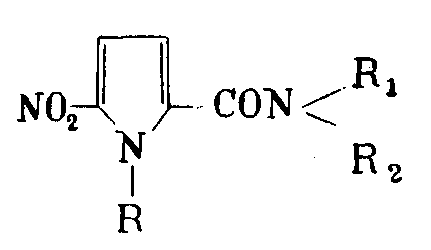
где R обозначает алкильный остаток с 1-4 атомами углерода, который в данном случае замещен, или аралкильный остаток и R1 и R2, которые могут быть одинаковыми или различными, обозначают атом водорода, алкильный остаток с 1-4 атомами углерода, который в данном случае замещен, или циклоалкильный остаток или с атомом азота, к которому они присоединены, образуют гидразиновый остаток или насыщенный одноядерный гетероцикл с 5- или 6-звеньями, который в данном случае содержит второй гетероатом из группы кислорода, серы и азота, как пирролидинил-(1), пиперидино, морфолино или замещенный в данном случае пиперазинил-(1), причем, если R1=R2-H, остаток в случае незамещенного алкильного радикала может иметь по меньшей мере 2 атома углерода, а также их солей, отличающийся тем, что щелочное производное соответственно замещенного 5-нитропиррола подвергают взаимодействию с соединением R-X, где R имеет вышеуказанное значение и X означает атом галоида или остаток сложного эфира серной кислоты или сульфокислоты в среде органического растворителя, например диметилформамида, при температуре кипения растворителя.
Авторы
Даты
1968-12-08—Публикация
1967-01-26—Подача