Изобретение относится к химии кремнийсодержащих органических соединений, а именно к новому способу получения замещенных 1,3,2-оксазасилолов общей формулы
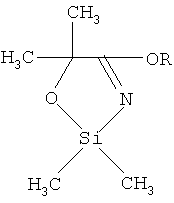
где R=С2Н5, i-C3H7, C4H9;
которые являются новыми по структуре кремнийсодержащими гетероциклическими соединениями и могут служить исходными в получении биологически активных соединений для нужд медицины и сельского хозяйства.
Известен метод взаимодействия С-фосфорилированных имидатов с диметилдихлорсиланом в среде инертных растворителей (диэтиловый эфир, бензол) при 18-25°С в присутствии триэтиламина. В результате были получены N-кремнийсодержащие С-фосфорилированные имидаты [В.Е.Шишкин, Е.В.Медников, Е.В.Исакова, Б.И.Но ЖОХ, 1997, Т.67, вып.7, с.1219-1220].
Автором в патентной и научной литературе веществ, подобных синтезированной структуре, не было найдено.
Задачей предлагаемого изобретения является разработка одностадийного метода синтеза 2,2-диметил-4-алкокси-5,5-диметил-1,3,2-оксазасилолов.
Техническим результатом является расширение арсенала химических соединений, получение новых замещенных 1,3,2-оксазасилолов с выходом не менее 75%.
Технический результат достигается разработкой нового способа получения 2,2-диметил-4-алкокси-5,5-диметил-1,3,2-оксазасилола формулы

где R=С2Н5, i-С3Н7, С4Н9,
заключающегося во взаимодействии гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата с диметилдихлорсиланом при температуре 20-25°С в среде обезвоженного бензола в течение 2-2.5 ч, с последующим охлаждением до 8-10°С и добавлением триэтиламина, при мольном соотношении реагентов гидрохлорид алкил(2-метил-2-гидрокси)пропанимидат:диметилдихлорсилан:триэтиламин (1.0-1.05:1.0:3.0-3.2) соответственно.
Химическая схема предложенного способа получения 2,2-диметил-4-алкокси-5,5-диметил-1,3,2-оксазасилолов:
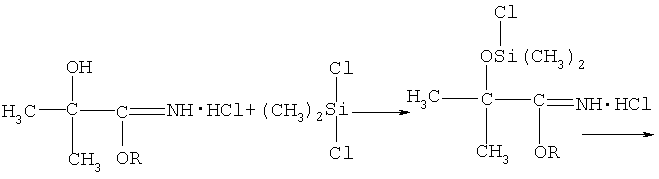
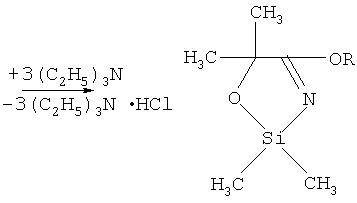
где R=C2H5, i-C3H7, C4H9.
При выборе растворителя для проведения реакции взаимодействия диметилдихлорсилана с гидрохлоридом алкил(2-метил-2-гидрокси)пропанимидатом были учтены следующие требования: создание гомогенной реакционной массы, поддержание необходимого температурного режима и инертность по отношению к реагирующим компонентам. Всем этим требованиям отвечает бензол, в нем хорошо растворимы все реагенты, есть возможность понижения температуры до 8-10°С, а также он абсолютно инертен по отношению к реагентам. Следует отметить, что образующийся в ходе реакции гидрохлорид триэтиламина не растворим в бензоле, что также обусловливает его применение в качестве растворителя.
Выбор в качестве реагента гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата обусловлен снижением образования продуктов линейного строения и способствует росту выхода целевого продукта не менее 75%.
Поддержание температуры на первой стадии взаимодействия гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата с диметилдихлорсиланом в интервале 20-25°С связано с тем обстоятельством, что при росте температуры выше 40-45°С возможен процесс термического распада гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата.
Понижение температуры до 8-10°С на стадии добавления триэтиламина необходимо с целью предотвращения образования продуктов осмоления.
Триэтиламин подается в небольшом избытке с целью полного связывания, образующегося в ходе реакции хлористого водорода.
Способ осуществляли следующим образом.
С целью синтеза замещенных 1,3,2-оксазасилолов к диметилдихлорсилану, растворенному в бензоле, прибавляли по каплям гидрохлорид алкил(2-метил-2-гидрокси)пропанимидата, растворенный в бензоле. Синтез осуществляли при температуре 20-25°С, по истечении 2-2.5 ч температуру понижали до 8-10°С и прибавляли по каплям триэтиламин. Соотношение реагентов гидрохлорид алкил(2-метил-2-гидрокси)пропанимидат:диметилдихлорсилан:триэтиламин (1.0-1.05:1.0:3-3.1). После чего температуру реакционной смеси повышали до комнатной температуры, отфильтровывали солянокислый триэтиламин, из фильтрата в вакууме водоструйного насоса отгоняли растворитель. Окончательную очистку осуществляли методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40. Контроль чистоты продуктов осуществляли методом тонкослойной хроматографии на пластинках Silufol. Выход 2,2-диметил-4-алкокси-5,5-диметил-1,3,2-оксазасилолов составлял не менее 75%. Идентификация синтезированных соединений проводилась по данным молекулярной рефракции, ИК-, масс-спектроскопии.
Для лучшего понимания сущности предложенного технического решения приводятся конкретные примеры синтезов.
Пример 1. 2,2-диметил-4-этокси-5,5-диметил-1,3,2-оксазасилол.
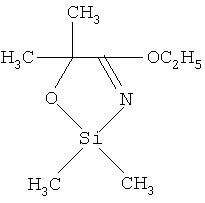
В реактор загружали 0.018 моля (2.3 г) диметилдихлорсилана, растворенного в 50 мл обезвоженного бензола. Затем прибавляли по каплям 0.018 моля (4.04 г) гидрохлорида этил(2-гидрокси-2-метил)пропанимидата, растворенного в 40 мл бензола. Температуру реакционной среды поддерживали в пределах 20-25°С. По истечении 2 ч температуру понижали до 8°С и прибавляли по каплям 0.055 моля (5.6 г) триэтиламина. Соотношение реагентов гидрохлорид этил(2-гидрокси-2-метил)пропанимидат:диметилдихлорсилан:триэтиламин (1.0:1.0:3.1). Выпавший гидрохлорид триэтиламина отфильтровывали, из фильтрата в вакууме водоструйного насоса отгоняли бензол. Очистку полученного продукта осуществляли методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир: метанол (1:3 об). Выход 75%. n20 D 1.4430, d20 4 1.0011, MRD 49.55, выч. 50.01, Rf 0.42. ИК-спектр, v, см-1: 825 [Si(СН3)2], 1040 (C-O-Si), 1675 (C=N), 1175 (С-О-С), 1345 [С(СН3)2]. Масс-спектр (70 эВ), m/z (I, %): 187(20.4) [M]+, 172 (11.6) [М-СН3]+, 142 (17.1) [M-C2H5O]+, 129 (10.5) [M-C3H7O]+.
Пример 2. 2,2-диметил-4-изопропокси-5,5-диметил-1,3,2-оксазасилол.
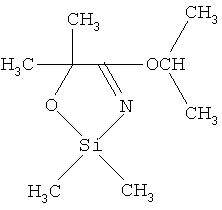
К 0.035 молям (4.5 г) диметилдихлорсилана, растворенного в 70 мл обезвоженного бензола, прибавляли по каплям 0.036 молей (8.5 г) гидрохлорида изопропил(2-метил-гидрокси)пропанимидата при температуре 20-25°С. Синтез осуществляли в течение 2.5 ч, после чего температуру понижали до 10°С и прибавляли по каплям 0.105 моля (10.6 г) триэтиламина. Соотношение реагентов гидрохлорид изопропил(2-гидрокси-2-метил)пропанимидат:диметилдихлорсилан:триэтиламин (1.05:1.0:3.0). Выпавший гидрохлорид триэтиламина отфильтровывали, из фильтрата в вакууме водоструйного насоса отгоняли бензол. Очистку полученного продукта осуществляли методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир: метанол (1:3 об). Выход 77%, n20 D 1.4479, d20 4 1.0289, MRD 53.14, выч. 53.05, Rf 0.39. ИК-спектр, v, см-1: 810 [Si(СН3)2], 1045 (C-O-Si), 1670 (C=N), 1160 (С-О-С), 1345 [С(СН3)2]. Масс-спектр (70 эВ), m/z (I, %): 201 (30.7) [М]+, 186 (12.6) [М-СН3], 158 (4.1) [М-С3H7]+ 145 (12.5) [М-С3Н7O]+.
Пример 3. 2,2-диметил-4-бутокси-5,5-диметил-1,3,2-оксазасилол.
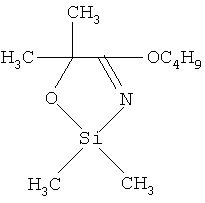
К 0.02 молям (2.6 г) диметилдихлорсилана, растворенного в 50 мл обезвоженного бензола, прибавляли по каплям 0.02 молей (3.03 г) гидрохлорида бутил(2-метил-гидрокси)пропанимидата при температуре 20-25°С. Синтез осуществляли в течение 2 ч, после чего температуру понижали до 8°С и прибавляли по каплям 0.065 моля (6.5 г) триэтиламина. Соотношение реагентов гидрохлорид бутил(2-гидрокси-2-метил)пропанимидат:диметилдихлорсилан:триэтиламин (1.0:1.0:3.2). Выпавший гидрохлорид триэтиламина отфильтровывали, из фильтрата в вакууме водоструйного насоса отгоняли бензол. Очистку полученного продукта осуществляли методом колоночной адсорбционной хроматографии на силикагеле марки μLC 5/40, элюент диэтиловый эфир: метанол (1:3 об). Выход 80%, n20 D 1.4554, d20 4 1.0291, MRD 59.02, выч. 59.77, Rf 0.35. ИК-спектр, v, см-1: 824 [Si(СН3)2], 1045 (C-O-Si), 1670 (C=N), 1125 (С-О-С), 1340 [С(СН3)2]. Масс-спектр (70 эВ), m/z (I, %): 215 (18.7) [М]+, 200 (34) [М-СН3]+, 186 (21.08) [М-С2Н5]+, 142 (27.4) [M-C4H9O]+.
Предложенный метод позволяет получать новые гетероциклические соединения, а именно 2,2-диметил-4-алкокси-5,5диметил-1,3,2-оксазасилол из гидрохлоридов гидроксиимидатов, путем взаимодействия последних с диметилдихлорсиланом с последующим добавлением триэтиламина. Преимуществом предложенного метода является возможность повышения выхода целевого продукта.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,2-ДИМЕТИЛ-4-АЛКОКСИ-5,5-ДИМЕТИЛ-1,3,2-ОКСАЗАСИЛОЛОВ | 2003 |
|
RU2254339C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ОКСО-2-АЛКОКСИ-5,5-ДИМЕТИЛ-1,3-2-ОКСАЗАФОСФОЛИДИН-4-ИОНОВ | 2004 |
|
RU2279436C1 |
| 5-ЗАМЕЩЕННЫЕ 1-АМИНО -8,9-ДИГИДРО -8,8-ДИМЕТИЛ-3,6Н- ПИРАЗОЛО [3,4-B] ПИРАНО[[4′,3′-d]] ПИРИДИНА ИЛИ ИХ ГИДРОХЛОРИДЫ, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 1988 |
|
SU1540240A1 |
| ЗАМЕЩЕННЫЕ N-АРИЛКАРБАМОИЛФОСФОНАТЫ В КАЧЕСТВЕ РЕГУЛЯТОРОВ РОСТА ХЛОПЧАТНИКА | 1993 |
|
RU2030420C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ОКСО -2- МЕТИЛ -4- ДИЭТИЛАМИНО -5,5- ДИМЕТИЛ -1,3,2- ОКСАЗАФОСФОЛ -3-ИНА | 1991 |
|
RU2026299C1 |
| 3-ОКСОТИАЗОЛИДИНО [3,2-A] ПИПЕРАЗИНЫ ИЛИ ИХ ГИДРОХЛОРИДЫ, ОБЛАДАЮЩИЕ ТРАНКВИЛИЗИРУЮЩИМ ДЕЙСТВИЕМ | 1991 |
|
SU1823452A1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-ГИДРОКСИ-4-ТИОМЕТИЛПИРАЗОЛЬНОГО СОЕДИНЕНИЯ | 2005 |
|
RU2386619C2 |
| ГЕПАТОПРОТЕКТОР | 1996 |
|
RU2156130C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ГЕТЕРОЦИКЛОМ ПРОИЗВОДНЫХ ПИРИДИНА | 2008 |
|
RU2474581C2 |
| 5-АЛКИЛ-3-(ПИРИД-3-ИЛ)ИЗОКСАЗОЛЫ И ИХ 4,5-ДИГИДРОПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2565754C2 |
Описывается способ получения замещенных 1,3,2-оксазасилолов общей формулы
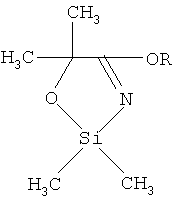
где R=C2H5, i-C3H7, C4H9, заключающийся во взаимодействии гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата с диметилдихлорсиланом при температуре 20-25°С в среде обезвоженного бензола в течение 2-2.5 ч, с последующим охлаждением до 8-10°С и добавлением триэтиламина, при мольном соотношении реагентов гидрохлорид алкил(2-метил-2-гидрокси)пропанимидат:диметилдихлорсилан:триэтиламин (1.0-1.05:1.0:3.0-3.2) соответственно. Техническим результатом является расширение арсенала химических соединений, получение новых замещенных 1,3,2-оксазасилолов с выходом не менее 75%.
Способ получения 5,5-диметил-4-алкокси-2,2-диметил-1,3,2-оксазасилолов формулы
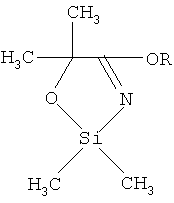
где R=C2H5, i-C3H7, C4H9,
заключающийся во взаимодействии гидрохлорида алкил(2-метил-2-гидрокси)пропанимидата с диметилдихлорсиланом при температуре 20-25°С в среде обезвоженного бензола в течение 2-2,5 ч, с последующим охлаждением до 8-10°С и добавлением триэтиламина, при мольном соотношении реагентов гидрохлорид алкил(2-метил-2-гидрокси)пропанимидат:диметилдихлорсилан:триэтиламин (1,0-1,05:1,0:3,0-3,2) соответственно.
| ШИШКИН В.Е | |||
| и др | |||
| ЖОХ, 1997, т.67, вып.7, с.1219-1220. |
Авторы
Даты
2005-06-20—Публикация
2003-12-22—Подача