Изобретение относится к медицине и фармацевтической технологии и касается лекарственного препарата для лечения нарушений ритма сердца.
Этмозин относится к антиаритмическим препаратам 1 класса (мембраностабилизирующего действия). Кроме того, он оказывает умеренный коронарорасширяющий, спазмолитический и м-холинолитический эффекты. Он нашел применение при экстрасистолиях, пароксизмальной тахикардии и пароксизмах мерцательной аритмии, возникающих при ИБС, а также аритмиях другой этиологии. При этом препарат подчас активен в тех случаях, при которых применение других антиаритмических средств (хинидин, новокаинамид, лидокаин и др.) не оказывает желаемого результата. Этмозин эффективен при аритмиях, вызываемых передозировкой сердечных гликозидов. Сравнительные исследования показывают, что этмозин является препаратом выбора при желудочковых аритмиях [Информация о лекарственных средствах для специалистов здравоохранения. Лекарственные средства, действующие на сердечно-сосудистую систему. Выпуск 2. Москва: Фармединфо, 1997. - 388 с.]. Важной характеристикой является то, что он не оказывает влияния на артериальное давление, сократительную функцию миокарда, почти не изменяет атрио-вентрикулярную и внутрижелудочковую проводимость (в тех случаях, когда функция проводимости не нарушена) и улучшает кровоснабжение сердечной мышцы [Шугушев Х.Х., Розенштраух Л.В. Влияние этмозина на функцию предсердно-желудочковой проводящей системы у больных с пароксизмальными наджелудочковыми тахикардиями // Кардиология, 1982. - №4. - С.56-62].
В настоящее время зарегистрированные лекарственные формы этмозина для перорального применения представлены только таблетками, покрытыми оболочкой, выпускаемыми «Олайнским химико-фармацевтическим заводом» (Латвия). Однако в традиционной лекарственной форме он создает определенные неудобства больным (частые приемы от 3 до 6 раз в день) и не исключает приступов аритмии при нарушении режима приема [Машковский М.Д. Лекарственные средства. Т. 1, изд. 13-е, новое, Харьков: Торсинг, 1998. - 560 с.].
Задачей изобретения является создание пролонгированных таблеток этмозина, позволяющих получить длительный терапевтический эффект при однократном приеме, избежать колебания концентраций лекарственных веществ в организме, снизить их токсичность и побочное действие, а также сделать лечение более экономичным за счет уменьшения суточной дозы лекарственного вещества и применения более простых технологических приемов создания лекарственной формы.
Поставленная задача достигается путем разработки состава и технологии пролонгированных средств на основе этмозина, содержащие в качестве модификатора высвобождения интерполимерный комплекс полиметакриловой или полиакриловой кислоты и полиэтиленгликоля, которые по эффективности превосходят прототип и лишены указанных недостатков. Согласно изобретению описывается антиаритмическое средство пролонгированного действия на основе этмозина, содержащее в качестве активного вещества этмозин, в качестве модификатора высвобождения интерполимерный комплекс (ИПК) полиметакриловой (ПМАК) или полиакриловой кислоты (ПАК) и полиэтиленгликоля и фармакологически приемлемое скользящее вещество при следующем соотношении компонентов, мас.%:
Используемые интерполимерные комплексы являются продуктами межмолекулярного взаимодействия линейной или редкосшитой полиакриловой или полиметакриловой кислоты с полиэтиленгликолем при соотношении 5:1-1:2.
Комплексы представляют собой структуры с регулярными последовательностями водородных связей, разделенных дефектами - полимерными звеньями, не вошедшими в реакцию комплексообразования. Дополнительный вклад в стабилизацию ИПК вносит гидрофобное взаимодействие между полимерными цепями. Эти комплексы нерастворимы в кислой среде и распадаются на водорастворимые компоненты в нейтральной среде. Использование ИПК не только позволяет обеспечить пролонгирующий эффект, но и позволяет избежать многокомпонентности состава, а также снизить количество вспомогательных веществ.
Введение в состав таблеток ИПК в качестве модификатора высвобождения обусловлено его способностью переходить от слабо набухающего продукта к неограниченно набухающему при рН более 5. Основное всасывание этмозина происходит в кишечнике в неионизированной (депротонированной) форме (рКа=6,4). В связи с этим полное высвобождение этмозина в желудке нецелесообразно. Технология покрытия таблеток кишечнорастворимой оболочкой достаточно сложна и требует высоких экономических затрат. Методом сканирующей электронной микроскопии показано, что особенностью разработанного препарата является самопроизвольное образование при контакте с кислой средой желудка на поверхности таблеток пленки ИПК. Толщина пленки определяет скорость диффузии этмозина из глубоко лежащих слоев таблетки и зависит от доли полимера, введенного в состав композиции.
Были исследованы различные слои таблеток методом ИК-спектроскопии после их пребывания в условиях моделирующих ЖКТ. Анализ полученных результатов позволил сделать вывод, что часть молекул этмозина находится в свободном состоянии и способна к быстрому высвобождению из лекарственной формы, а часть в виде комплекса с ПМАК и соответственно медленнее высвобождается. Таким образом, особенностью данной лекарственной формы является также способность компонентов матрицы взаимодействовать с лекарственным веществом, замедляя тем самым процесс высвобождения.
Испытание по тесту «Растворение» используется как контроль качества, отражающий постоянство свойств лекарственной формы, которое свидетельствует о надлежащих условиях производственного процесса. Кроме того, учитывая, что для части препаратов наблюдается корреляция скорости растворения и скорости всасывания, данный тест является критерием оценки пролонгирующего действия препаратов in vitro.
Тест «Растворение» проводили на приборе типа «Вращающаяся корзинка» фирмы «Sotax AT6» (Швейцария). В качестве среды растворения использовали буферные растворы с рН 1,16 и 6,8. Объем среды составлял 500 мл, скорость вращения корзинки 100 об/мин. Количество высвободившегося этмозина из таблеток в отобранных пробах определяли по интенсивности поглощения растворов в УФ области спектра на двулучевом регистрирующем приборе «UV-160» фирмы «Shiniadzu» (Япония).
Анализ таблеток прототипа показал их полное растворение уже через 30 минут от начала эксперимента, в то время как высвобождение этмозина из композиций, содержащих ИПК, наблюдается в течение длительного времени. Данные по высвобождению этмозина из модельных таблеток с разным соотношением лекарственное вещество: полимерный носитель показывают, что кинетика высвобождения зависит от доли ИПК, введенного в состав таблеток. Из кривых высвобождения этмозина из разных типов таблеток (см. чертеж) видно, что при увеличении количества полимера в составе лекарственной формы скорость высвобождения лекарственного вещества в кислом буфере падает и достигает наименьшего значения у состава, содержащего наибольшее количество ИПК (пример 4). Анализ данных по высвобождению этмозина в буфере с рН 6,8 показывает противоположную зависимость: чем больше содержание полимера в составе лекарственной формы, тем быстрее происходит высвобождение действующего вещества. Увеличение содержания ИПК в лекарственной композиции свыше 60% нецелесообразно, так как это не способствует существенному уменьшению количества высвободившегося этмозина в кислой среде. Напротив, это приводит к увеличению средней массы таблетки, что затрудняет ее прием больными и ухудшает технологические характеристики таблетируемой массы. Уменьшение содержания ИПК в композиции приводит к значительному выходу этмозина из таблетки в кислой среде и может способствовать его преждевременному окислению. Следующие примеры иллюстрируют изобретение.
Пример 1. Состав на 1 таблетку, г:
Модельные таблетки были приготовлены смешиванием компонентов и прямым прессованием полученной смеси. Кинетические данные высвобождения этмозина в процентах приведены в таблице 1.
Пример 2. Состав на 1 таблетку, г:
Модельные таблетки были приготовлены смешиванием компонентов, брикетированием, размалыванием брикетов и таблетированием полученного гранулята. Кинетические данные высвобождения этмозина в процентах приведены в таблице 1.
Пример 3. Состав на 1 таблетку, г:
Модельные таблетки были приготовлены по примеру 2. Кинетические данные высвобождения этмозина в процентах приведены в таблице 1.
Пример 4. Состав на 1 таблетку, г:
Модельные таблетки были приготовлены по примеру 1. Кинетические данные высвобождения этмозина в процентах приведены в таблице 1.
Пример 5 (прототип). Состав на одну таблетку, г:
Кинетические данные высвобождения этмозина в процентах приведены в таблице 1.
Пример 6. Состав на 1 таблетку, г:
Модельные таблетки были приготовлены по примеру 1 и покрыты оболочкой методом дражирования. В состав оболочки входили следующие компоненты, г:
Пример 7. Полученные по примеру 2 таблетки покрывали пленочной оболочкой с использованием в качестве раствора пленкообразователя 5% спиртового раствора ИПК полиметакриловой кислоты и полиэтиленгликоля с последующим удалением растворителя.
Для проведения фармакокинетического исследования заявляемого препарата в сравнении с прототипом был использован состав по примеру 3. Эксперимент проводили на кроликах с использованием 5 животных для каждого препарата. Отбор венозной крови производили через 0,5, 1, 1,5, 2, 4, 6 и 8 часов после введения внутрь таблеток прототипа и через 1, 2, 3, 4, 5, 6, 7, 8, 12 и 24 часа после введения внутрь заявляемых таблеток. Фармакокинетические параметры этмозина заявляемого препарата и прототипа при однократном введении кроликами представлены в таблице 2. Изучение фармакокинетических параметров показало, что среднее значение максимальной концентрации (Смах) этмозина после введения заявляемого препарата близко по значению к этому показателю таблеток прототипа. Однако время достижения максимальной концентрации (Тмах) для разработанного препарата почти в 5 раз дольше. Через 24 часа после введения заявляемых таблеток среднее значение концентрации этмозина в крови было близко к аналогичному показателю в крови животных, наблюдаемому через 8 часов после введения таблеток прототипа. Период полуэлиминации (Т1/2) для разработанных таблеток более чем в 2,5 раза дольше, как и среднее время удерживания препарата (MRT). Увеличение данных фармакокинетических параметров свидетельствует о более медленном высвобождении этмозина из разработанных таблеток по сравнению с прототипом, что и обуславливает эффект пролонгирования. Биодоступность (F) этмозина при введении разработанных таблеток, вычисленная по средним значениям площади под кинетической кривой и дозы, более чем в 1,5 раза выше, чем в случае введения прототипа, что можно объяснить лучшей защищенностью лекарственного вещества от воздействия агрессивной среды желудка.
Таким образом, проведенные исследования показали, что заявляемый препарат обладает пролонгированным действием и более высокой по сравнению с прототипом биодоступностью.
Степень высвобождения этмозина из разных типов таблеток в условиях, моделирующих ЖКТ
Фармакокинетические параметры этмозина при однократном пероральном введении кроликам таблеток прототипа и заявляемого препарата
Смах, мкг/мл
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОЛОНГИРОВАННЫЙ АНТИАРИТМИЧЕСКИЙ ПРЕПАРАТ ЭТАЦИЗИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2267322C1 |
| ПРОЛОНГИРОВАННЫЙ АНТИАНГИНАЛЬНЫЙ ПРЕПАРАТ ИЗОСОРБИДА ДИНИТРАТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2267318C1 |
| ПРОТИВОВОСПАЛИТЕЛЬНЫЙ СОСТАВ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ НА ОСНОВЕ ДИКЛОФЕНАКА НАТРИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2070034C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТАБЛЕТОК ХИНИДИНА СУЛЬФАТА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1992 |
|
RU2036641C1 |
| БРОНХОЛИТИЧЕСКОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2000 |
|
RU2203062C2 |
| Интерполимерный носитель для пероральных систем контролируемой доставки активных фармацевтических ингредиентов | 2018 |
|
RU2725879C2 |
| СПОСОБ ПОЛУЧЕНИЯ БРОНХОЛИТИЧЕСКОЙ ЛЕКАРСТВЕННОЙ КОМПОЗИЦИИ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ НА ОСНОВЕ ТЕОФИЛЛИНА | 1992 |
|
RU2036642C1 |
| ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ЛЕКАРСТВЕННАЯ ФОРМА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ (ВАРИАНТЫ) | 2009 |
|
RU2435584C2 |
| БРОНХОЛИТИЧЕСКОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2097036C1 |
| Интерполимерный материал для медицинского и ветеринарного применения и пролонгированные лекарственные и ветеринарные средства на его основе | 2017 |
|
RU2684608C1 |
Изобретение относится к области медицины и фармакологии и касается пролонгированного антиаритмического препарата, содержащего этмозин, интерполимерный комплекс полиметакриловой или полиакриловой кислоты и полиэтиленгликоля, и скользящее, а также способа получения указанного препарата путем смешения компонентов с последующим сухим гранулированием. Препарат обеспечивает длительное поддержание концентрации действующего вещества на терапевтически эффективном уровне. 3 н. и 4 з.п. ф-лы, 2 табл., 1 ил.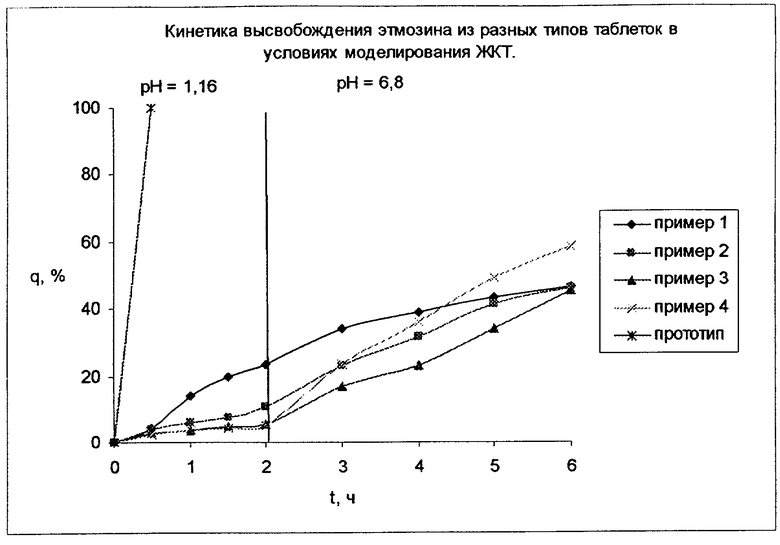
| Машковский М.Д | |||
| Лекарственные средства | |||
| Харьков: Торсинг | |||
| Изд | |||
| Насос | 1917 |
|
SU13A1 |
| ЗАМОК АНКЕРНОЙ КРЕПИ | 1990 |
|
RU2011841C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТАБЛЕТОК ХИНИДИНА СУЛЬФАТА ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1992 |
|
RU2036641C1 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ | 0 |
|
SU329891A1 |
Авторы
Даты
2006-01-10—Публикация
2004-05-25—Подача