ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
В данной заявке испрашивается приоритет на основании предварительной заявки Соединенных Штатов, регистрационный № 60/204646, поданной 17 мая 2000, содержание которой, таким образом, включено в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к новым производным пирролопиридинона, промежуточным продуктам, используемым в синтезе, и фармацевтическим композициям, содержащим соединения, и их использованию для лечения половой дисфункции. Соединения настоящего изобретения являются ингибиторами фосфодиэстеразы, пригодными для лечения половой дисфункции, более конкретно, мужской эректильной дисфункции.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Эректильную дисфункцию (ED) определяют как неспособность достичь или поддерживать эрекцию, достаточно твердую для удовлетворительных половых сношений. В настоящее время оценивается, что приблизительно 7-8% мужской популяции страдает некоторой степенью ED, что эквивалентно, по меньшей мере, 20 миллионам мужчин только в Соединенных Штатах. Поскольку вероятность ED повышается с возрастом, предсказывается, что распространенность этого состояния будет расти в будущем, так как средний возраст популяции растет.
Мужская эректильная дисфункция может быть следствием психогенных и/или органических факторов. Хотя ED является многофакторной, более вероятно, что некоторые подгруппы в пределах мужской популяции имеют симптомы нарушения. В частности, пациенты с диабетом, гипертензией, сердечным заболеванием и рассеянным склерозом имеют особенно высокое распространение ED. Кроме того, пациенты, которые принимают некоторые классы лекарственных средств, таких как гипотензивные средства, антидепрессанты, седативные средства и анксиолитики, имеют большую склонность к ED.
Лечения ED включают различные фармакологические агенты, вакуумные устройства и протезы полового члена. Среди фармакологических агентов на практике в настоящее время используют папаверин, фентоламин и алпростадил. Эти агенты эффективны только после прямой интракавернозной или интрауретральной инъекции и связаны с побочными действиями, такими как приапизм, фиброз, боль полового члена и гематома у места инъекции. Вакуумные устройства являются устройствами для неинвазивного альтернативного лечения ED. Эти устройства вызывают эрекцию созданием вакуума вокруг тела полового члена, что приводит к повышенному потоку крови в объемное кавернозное тело посредством пассивной артериальной дилатации. Хотя эта форма терапии часто является удачной при лечении ED органического происхождения, жалобы включают отсутствие спонтанности и времени, затрачиваемого при использовании устройства, и трудность и дискомфорт при эякуляции. С некоторым успехом использовали различные полутвердые или надуваемые протезы полового члена, особенно у мужчин с диабетом. Эти устройства обычно рассматривают, когда другие варианты лечения были неудачными и ассоциируются с повышенным риском инфекции и ишемии.
Недавно ингибитор фосфодиэстеразы V (PDEV) силденафил (виагра) был одобрен FDA в качестве перорально эффективной лекарственной терапии для лечения ED. Силденафил, 5-[2-этокси-5-(4-метилпиперазин-1-илсульфонил)фенил]-1-метил-3-н-пропил-6,7-дигидро-1Н-пиразоло[4,3-d]пиримидин-7-он, и ряд относящихся к нему аналогов и их использование в качестве агентов против стенокардии описаны в патентах США 5250534 и 5346901. Использование силденафила и относящихся к нему аналогов для лечения мужской эректильной дисфункции описано в публикации Международной патентной заявки РСТ WO 94/28902, опубликованной 22 декабря 1994. В клинических исследованиях лекарственное средство повышало половую функцию приблизительно у 70% мужчин, которые страдают ED психогенной или органической этиологии. Однако лекарственное средство проявило менее значительную эффективность у пациентов, которые подвергались радикальной простатэктомии, наблюдали повышенную эрекцию у 43% пациентов, которые принимали силденафил, по сравнению с 15% пациентов, принимавших плацебо. Кроме того, использование силденафила ассоциируется с несколькими нежелательными побочными эффектами, включающими головную боль, прилив крови к лицу и нарушенное цветовосприятие, которые являются результатом неселективных действий на различные ткани. Несмотря на эти недостатки, лекарственное средство рассматривается пациентами как предпочтительное по сравнению с другими способами лечения, которые заключаются во введении лекарственного средства непосредственно в половой член посредством инъекции, использовании наружного устройства или хирургической операции.
Daugan et al. в патенте США 5859009 и ЕР 0740668 В1 описали синтез ряда тетрациклических производных в качестве ингибиторов циклического гуанозин-3',5'-монофосфата особенно фосфодиэстеразы и их применение при лечении сердечно-сосудистых заболеваний. Daugan et al. в WO 97/03675 сообщали об использовании тетрациклических производных для лечения импотенции.
Garinaux, J.-F. et al. в Tetrahedron Letters 38(17), (1997), рр. 2997-3000 описали синтез трициклических производных хинолона окислением 1,2,3,4-тетрагидро-β-карболинов.
Pfenninger, E. в патенте Германии 2803541 и патенте США 4235907 описали замещенные 9Н-пирроло[3,4-b]хинолин-9-оны и их использование при лечении аллергической астмы.
Сексуально стимулированная эрекция полового члена является результатом сложного взаимодействия физиологических процессов, включающих процессы центральной нервной системы, периферической нервной системы и гладкой мышцы. В частности, выделение оксида азота из неадренергических, нехолинергических нервов и эндотелия активирует гуанилилциклазу и повышает уровни внутриклеточного цГМФ в объемном пещеристом теле. Повышение внутриклеточного цГМФ снижает уровни внутриклеточного кальция, что приводит к релаксации трабекулярной гладкой мышцы, которая, в свою очередь, приводит к увеличению в телесном объеме и сжатию подоболочечных венул, приводящих к эрекции полового члена.
PDE V найден в тромбоцитах и васкулярной гладкой мышце человека, что предполагает роль данного фермента в регуляции внутриклеточных концентраций цГМФ в сердечно-сосудистой ткани. На самом деле, показано, что ингибиторы PDEV вызывают эндотелиально-зависимое расширение сосудов потенцированием повышений уровней внутриклеточного цГМФ, индуцированного оксидом азота. Кроме того, ингибиторы PDEV селективно снижают легочное артериальное давление на животных моделях застойной сердечной недостаточности и легочной гипертензии. Поэтому, помимо их полезности при ED, ингибиторы PDEV могут, вероятно, быть терапевтически полезными при состояниях, подобных сердечной недостаточности, легочной гипертензии и стенокардии.
Предполагается, что агенты, которые повышают концентрацию цГМФ в ткани полового члена посредством либо повышенного высвобождения, либо пониженного разложения цГМФ, являются эффективными средствами для лечения ED. Внутриклеточные уровни цГМФ регулируют ферментами, принимающими участие в их образовании и деградации, а именно, гуанилатциклазами и циклонуклеотидфосфодиэстеразами (PDE). К настоящему времени описано, по меньшей мере, девять семейств PDE млекопитающих, пять из которых способны гидролизовать активный цГМФ в неактивный ГМФ в физиологических условиях (PDEs I, II, V, VI и IX). PDE V является преобладающей изоформой в объемном кавернозном теле. Следовательно, можно предположить, что ингибиторы PDEV повышают концентрацию цГМФ в объемном кавернозном теле и повышают продолжительность и частоту эрекции полового члена.
Кроме того, известно, что селективные ингибиторы PDE являются пригодными при лечении различных нарушений и состояний, включая мужскую эректильную дисфункцию (ED), женскую дисфункцию половой возбудимости, женскую половую дисфункцию, относящуюся к кровотоку и продуцированию оксида азота в тканях влагалища и клитора, преждевременные роды, дисменорею, сердечно-сосудистые нарушения, атеросклероз, артериальные окклюзивные нарушения, тромбоз, коронарный стеноз в состоянии покоя, стенокардию, инфаркт миокарда, сердечную недостаточность, ишемические нарушения сердца, гипертензию, легочную гипертензию, астму, перемежающуюся хромоту и диабетические осложнения.
В соответствии с этим, целью изобретения является идентификация соединений, которые повышают концентрацию цГМФ в ткани полового члена посредством ингибирования фосфодиэстераз, особенно PDEV. Другой целью изобретения является идентификация соединений, которые пригодны для лечения половой дисфункции, особенно, эректильной дисфункции и/или импотенции у животных мужского пола и половую дисфункцию у животных женского пола.
Еще одной целью изобретения является определение способов лечения половой дисфункции, особенно, эректильной дисфункции, с применением соединений настоящего изобретения.
Другой целью изобретения является определение соединений, которые пригодны для лечения состояний нарушений, опосредованных PDEV, таких как мужская эректильная дисфункция, женская сексуальная дисфункция, сердечно-сосудистые нарушения, атеросклероз, артериальные окклюзивные нарушения, тромбоз, коронарный стеноз в состоянии покоя, стенокардия, инфаркт миокарда, сердечная недостаточность, ишемические нарушения сердца, гипертензия, легочная гипертензия, астма, перемежающаяся хромота или диабетические осложнения.
Далее авторами описан ряд производных пирролопиридинона, обладающих способностью ингибировать фосфодиэстеразу типа V в ферментных анализах.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым производным пирролопиридинона, пригодным в качестве ингибиторов фосфодиэстеразы. Более конкретно, настоящее изобретение относится к соединениям общей формулы (I) или (II):
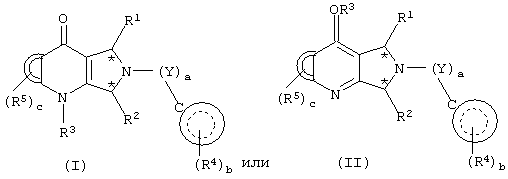
где R1 выбран из группы, состоящей из водорода, карбокси, -С(О)-C1-С6алкил, -С(О)-C1-С6алкокси, -С(О)-NH-С1-С6алкил-NH2, -С(О)-NH-С1-С6алкил-NHRA, -С(О)-NH-С1-С6алкил-N(RA)2, -С(О)-NH2, -C(O)-NHRA, -C(O)-N(RA)2, -С1-С6алкил-NH2, -С1-С6алкил-NHRA, -С1-С6алкил-N(RA)2, -NH-C1-C6алкил-N(RA)2;
где каждый RA независимо выбран из группы, состоящей из C1-С6алкила, арила, С1-С6аралкила и гетероарила, где арил, аралкил или гетероарил может быть необязательно замещен одним-тремя RB;
где каждый RB независимо выбран из группы, состоящей из галогена, нитро, циано, С1-С6алкила, C1-С6алкокси, C1-С6алкилкарбонила, карбоксиС1-С6алкила, C1-С6алкилсульфонила, трифторметила, амино, ди(C1-С6алкил)амино, ацетиламино, карбоксиС1-С6алкилкарбониламино, гидроксиС1-С6алкиламино, NHRA и N(RA)2;
R2 выбран из группы, состоящей из С5-С10алкила (необязательно замещенного одним-тремя заместителями, независимо выбранными из галогена, гидрокси, нитро, амино, NHRA или N(RA)2), арила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RC), циклоалкила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RA), гетероарила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RC) и гетероциклоалкила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RC);
где RC выбран из группы, состоящей из галогена, нитро, циано, C1-С6алкила, C1-С6алкокси, трифторметила, трифторметокси, NH2, NH(C1-С6алкил) и N(C1-Сб-алкил)2;
R3 выбран из группы, состоящей из водорода, С1-С6алкила, C1-С6алкилкарбонила, С2-С6алкенилкарбонила и С2-С6алкинилкарбонила;
b равно целому числу от 0 до 4;
R4 независимо выбран из группы, состоящей из галогена, гидрокси, карбокси, оксо, нитро, С1-С6алкила, C1-С6алкокси, C1-С6алкоксикарбонила, трифторметила, фенила (где фенильная группа может быть необязательно замещена одним-тремя заместителями, независимо выбранными из RD), фенилсульфонила, нафтила, C1-С6аралкила, -O-аралкила (где аралкильная группа может быть необязательно замещена одним-тремя заместителями, независимо выбранными из RD), гетероарила (где гетероарил может быть необязательно замещен одним-тремя заместителями, независимо выбранными из RD), гетероциклоалкила, NH2, NHRA, N(RA)2,
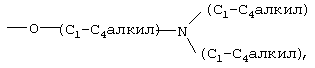
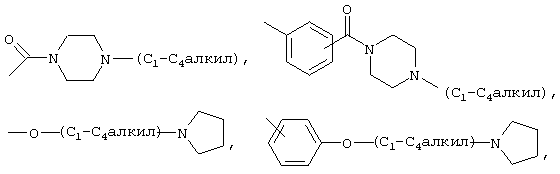
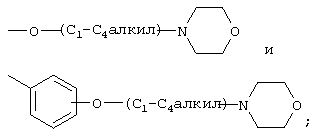
где каждый RD независимо выбран из галогена, гидрокси, карбокси, оксо, С1-С4алкила, С1-С4алкилтио, гидроксиС1-С4алкила, С1-С4алкокси, С1-С4алкилоксикарбонила, С1-С4алкилкарбонила, трифторметила, трифторметокси, NH2, NHRA, N(RA)2, C(O)N(RA)2, ацетиламино, нитро, циано, формила, C1-С6алкилсульфонила, карбоксиС1-С6алкила и аралкила;
с равно целому числу от 0 до 4;
R5 независимо выбран из группы, состоящей из галогена, нитро, гидрокси, C1-С6алкила, C1-С6алкокси, -NH2, -NHRA, -N(RA)2, -ORA, -С(О)NH2, -C(O)NHRA, -C(O)N(RA)2, -NHC(O)RA, -SO2NHRA, -SO2N(RA)2, где RA имеет указанные выше значения, фенила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RB), гетероарила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RB) и гетероциклоалкила (необязательно замещенного одним-тремя заместителями, независимо выбранными из RB);
а равно целому числу от 0 до 1;
Y выбран из группы, состоящей из следующих: -C1-С6алкил-, -С(О)-, -(C1-С6алкил)карбонил-, -(С2-С6алкенил)карбонил, -(С2-С6алкинил)карбонил-, -карбонил(C1-С6алкил)-, -карбонил-(С2-С6алкенил), -С(O)O-(C1-С6алкил)-, -C(S)-, -SO2-, -(С1-С6алкил)сульфонил-, -сульфонил(С1-С6алкил)-, -C(O)NH-, -С(O)NH-(С1-С6алкил)-, -С(О)(С3-С7циклоалкил)- и (С3-С7циклоалкил)-С(О)-;
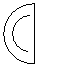 выбран из группы, состоящей из фенила, фурила, тиенила и пирролила;
выбран из группы, состоящей из фенила, фурила, тиенила и пирролила;
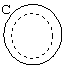 выбран из группы, состоящей из арила, гетероарила, циклоалкила и гетероциклоалкила;
выбран из группы, состоящей из арила, гетероарила, циклоалкила и гетероциклоалкила;
при условии, что, когда R1 представляет водород, R3 представляет водород, b равно 0, с равно 0, а равно 1, Y представляет -СН2-,  представляет фенил и
представляет фенил и  представляет фенил, тогда R2 не является триметоксифенилом (т.е. соединение не является 1,2,3,4-тетрагидро-2-(фенилметил)-3-(3,4,5-триметоксифенил)-9Н-пирроло[3,4-b]хинолин-9-оном);
представляет фенил, тогда R2 не является триметоксифенилом (т.е. соединение не является 1,2,3,4-тетрагидро-2-(фенилметил)-3-(3,4,5-триметоксифенил)-9Н-пирроло[3,4-b]хинолин-9-оном);
и их фармацевтически приемлемым солям.
Иллюстрацией изобретения является фармацевтическая композиция, включающая фармацевтически приемлемый носитель и любое из соединений, описанных выше. Иллюстрацией изобретения является фармацевтическая композиция, полученная смешиванием любого из соединений, описанных выше, и фармацевтически приемлемого носителя. Иллюстрацией изобретения является способ получения фармацевтической композиции, включающий смешивание любого из соединений, описанных выше, и фармацевтически приемлемого носителя.
Примером изобретения является способ лечения состояния, выбранного из группы, состоящей из мужской эректильной дисфункции (ED), импотенции, женской дисфункции половой возбудимости, женской половой дисфункции, относящейся к кровотоку и продуцированию оксида азота в тканях влагалища и клитора, преждевременных родов, дисменореи, сердечно-сосудистых нарушений, атеросклероза, артериальных окклюзивных нарушений, тромбоза, коронарного стеноза в состоянии покоя, стенокардии, инфаркта миокарда, сердечной недостаточности, ишемических нарушений сердца, гипертензии, легочной гипертензии, астмы, перемежающейся хромоты и диабетических осложнений у субъекта, нуждающегося в этом, включающий введение субъекту терапевтически эффективного количества любого из соединений или описанных выше фармацевтических композиций.
Примером осуществления изобретения является способ повышения концентрации цГМФ в ткани полового члена посредством ингибирования фосфодиэстераз, особенно PDEV, у субъекта мужского пола, нуждающегося в этом, включающий введение субъекту эффективного количества любого из соединений или фармацевтических композиций, описанных выше.
Следующим примером осуществления изобретения является способ продуцирования. эндотелиально-зависимого расширения сосудов потенцированием повышений уровней внутриклеточного цГМФ, индуцированного оксидом азота, у субъекта, нуждающегося в этом, включающий введение субъекту эффективного количества любого из соединений или фармацевтических композиций, описанных выше.
Примером осуществления изобретения является применение любого из соединений, описанных выше, для получения лекарственного средства для: (а) лечения половой дисфункции, особенно, мужской эректильной дисфункции, (b) лечения импотенции, (с) повышения концентрации цГМФ в ткани полового члена посредством ингибирования фосфодиэстеразы, особенно, PDE V и/или d) лечения состояния, выбранного из группы, состоящей из преждевременных родов, дисменореи, сердечно-сосудистых нарушений, атеросклероза, артериальных окклюзивных нарушений, тромоза, коронарного стеноза в состоянии покоя, стенокардии, инфаркта миокарда, сердечной недостаточности, ишемических нарушений сердца, гипертензии, легочной гипертензии, астмы, перемежающейся хромоты и диабетических осложнений у субъекта, нуждающегося в этом.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым производным пирролопиридинона, пригодным для лечения половой дисфункции, особенно, мужской эректильной дисфункции (ED). Хотя соединения настоящего изобретения пригодны, главным образом, для лечения мужской половой дисфункции или эректильной дисфункции, они могут быть также пригодны для лечения женской половой дисфункции, например, женской дисфункции половой возбудимости, женской половой дисфункции, относящейся к кровотоку и продуцированию оксида азота в ткани влагалища и клитора, и преждевременных родов и дисменореи.
Более конкретно, соединениями настоящего изобретения являются соединения формулы (I) или (II):

где все символы имеют значения, указанные выше, и их фармацевтически приемлемые соли.
R1, предпочтительно, представляет водород.
В примере осуществления настоящего изобретения R2 выбран из группы, состоящей из фенила (необязательно замещенного одним или двумя заместителями, выбранными из галогена, нитро, циано, C1-С3алкила, C1-С3алкокси, трифторметила, трифторметокси, NH2, NH(C1-С3алкил) или N(C1-С3-алкил)2), гетероарила и гетероциклоалкила. Предпочтительно, R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 3,4-диметоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 5-бензофурила, 5-инданила и 3-тиенила. Более предпочтительно, R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 3-тиенила, 5-инданила и 5-бензофурила. Еще более предпочтительно, R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 3-тиенила, 5-инданила и 5-бензофурила. Наиболее предпочтительно, R2 выбран из группы, состоящей из 3,4-метилендиоксифенила и 5-(2,3-дигидробензофурила).
Предпочтительно, R3 выбран из группы, состоящей из водорода и С1-С4алкила. Более предпочтительно, R3 выбран из группы, состоящей из водорода и метила. Наиболее предпочтительно, R3 представляет водород.
Предпочтительно, b равно целому числу от 0 до 4. Более предпочтительно, b равно целому числу 0 или 1.
В примере осуществления настоящего изобретения R4 выбран из группы, состоящей из галогена, гидрокси, карбокси, оксо, C1-С3алкила, C1-С3алкокси, C1-С3алкоксикарбонила, фенила (где фенил может быть необязательно замещен одним или двумя заместителями, выбранными из гидрокси, карбокси, С1-С4алкила, С1-С4алкилтио, гидроксиС1-С4алкила, С1-С4алкокси, С1-С4алкилоксикарбонила, C(O)N(RA)2, трифторметила, трифторметокси, амино, (С1-С4алкил)амино, ди(С1-С4алкил)амино, нитро, циано или формила), O-аралкила, гетероарила (где гетероарил может быть необязательно замещен одним или двумя заместителями, выбранными из гидрокси, карбокси, оксо, C1-С3алкила, C1-С3алкокси, C1-С3алкилоксикарбонила, С(O)N(RA)2, трифторметила, трифторметокси, амино, нитро, C1-С3алкилкарбонила или С1-С4аралкила), гетероциклоалкила,
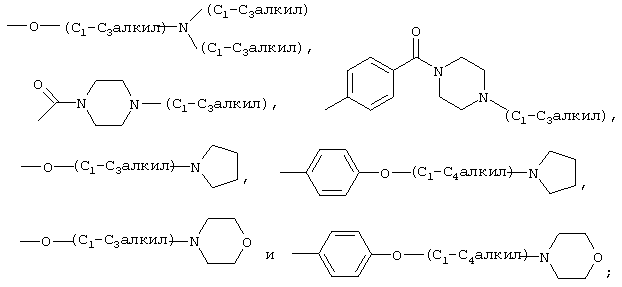
Предпочтительно, R4 выбран из группы, состоящей из брома, гидрокси, карбокси, оксо, метила, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-цианофенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-формилфенила, 4-метилтиофенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-окси-2-пиридинила, 3-тиенила, 2-фурила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 5-(1-метилимидазолила), 5-(1-бензилимидазолила), 3,4-метилендиоксифенила,
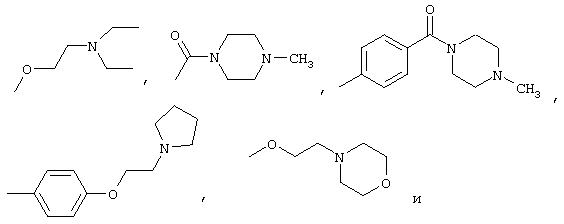
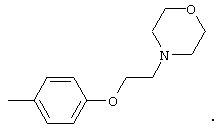
Более предпочтительно, R4 выбран из группы, состоящей из 5-брома, 2-гидрокси, 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-цианофенила, 4-формилфенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, 2-фурила, 3-тиенила, N-оксо-2-пиридинила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 3,4-метилендиоксифенила,
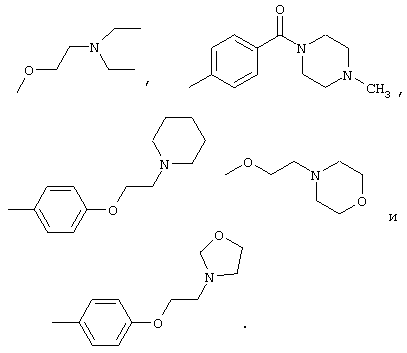
Еще более предпочтительно, R4 выбран из группы, состоящей из 5-брома, 2-гидрокси, 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-цианофенила, 4-формилфенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-оксо-2-пиридинила, 3-тиенила, 2-фурила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 3,4-метилендиоксифенила,
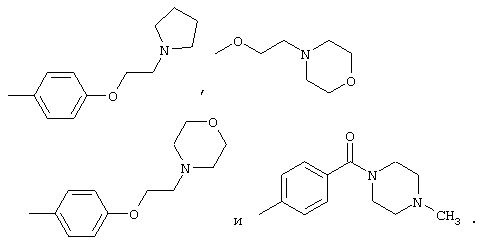
Еще более предпочтительно, R4 выбран из группы, состоящей из 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 3-трифторметилфенила, 3-нитрофенила, 4-нитрофенила, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-оксо-2-пиридинила, 3-тиенила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила),
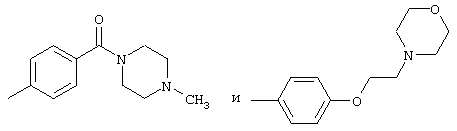
Наиболее предпочтительно, R4 выбран из группы, состоящей из гидрокси, 4-метилфенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 3-трифторметилфенила, 4-нитрофенила, 2-пиридинила, 3-пиридинила,
В предпочтительном примере осуществления с равно 0. В другом предпочтительном примере осуществления а равно целому числу от 0 до 1.
В примере осуществления настоящего изобретения Y выбран из группы, состоящей из -С1-С4алкил-, -C(S)-, -С(О)-, -С(О)О-(С1-С4алкил)-, -С(О)-(С1-С4алкил)-, С(О)-(С2-С4алкенил)-, -С(О)-(С3-С7циклоалкил)- и -С(О)NH-(C1-С3алкил)-. Предпочтительно, Y выбран из группы, состоящей из -СН2-, -С(S)-, -С(О)-, -С(O)O-СН2-, -С(O)-СН2СН2-, -С(O)-СН=СН-, C(O)NH-CH2-, -С(О)-циклопропил и -С(O)СН2-. Более предпочтительно, Y выбран из группы, состоящей из -С(О)-, -С(O)O-СН2-, -С(O)-СН2СН2-, -С(O)-СН=СН- и -С(О)-циклопропил. Еще более предпочтительно, Y выбран из группы, состоящей из -С(О)-, -С(O)O-СН2- и -С(О)-СН=СН-. Наиболее предпочтительно, Y выбран из группы, состоящей из -С(О)- и -С(O)O-СН2-.
Предпочтительно,  представляет фенил.
представляет фенил.
В одном предпочтительном примере осуществления  выбран из группы, состоящей из фенила, гетероарила и гетероциклоалкила. Предпочтительно,
выбран из группы, состоящей из фенила, гетероарила и гетероциклоалкила. Предпочтительно,  выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила, 1-имидазолила, 2-имидазолила, 2-тиазолила и 2-оксабицикло[2.2.1]гептанила. Более предпочтительно,
выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила, 1-имидазолила, 2-имидазолила, 2-тиазолила и 2-оксабицикло[2.2.1]гептанила. Более предпочтительно,  выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила и 2-тиазолила. Наиболее предпочтительно,
выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила и 2-тиазолила. Наиболее предпочтительно,  выбран из группы, состоящей из 2-фурила, 2-бензо(b)фурила, 4-пиридинила, 2-пиримидинила и 2-тиазолила.
выбран из группы, состоящей из 2-фурила, 2-бензо(b)фурила, 4-пиридинила, 2-пиримидинила и 2-тиазолила.
Термин «галоген» включает иод, бром, хлор и фтор.
Термин «алкил», независимо от того, используют ли его отдельно или как часть группы-заместителя, означает алканы с неразветвленной или разветвленной цепью, содержащие от одного до десяти атомов углерода или любое число атомов в этом диапазоне. Алкильные радикалы включают, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, 3-(2-метил)бутил, 2-пентил, 2-метилбутил, неопентил, н-гексил и 2-метилпентил. Аналогично этому, алкенильные и алкинильные группы включают алкены и алкины с неразветвленной или разветвленной цепью, содержащие от двух до десяти атомов углерода или любое число атомов в этом диапазоне.
Термин «алкокси» означает кислородный эфирный радикал описанной выше алкильной группы с неразветвленной или разветвленной цепью. Алкоксирадикалы включают, например, метокси, этокси, н-пропокси, н-бутокси, втор-бутокси, трет-бутокси и тому подобное.
Термин «арил» означает ароматическую группу, такую как фенил, нафтил и тому подобное.
Термин «аралкил» означает алкильную группу, замещенную арильной группой, например, бензил, фенилэтил и тому подобное. Аналогично этому, термин «аралкенил» означает алкенильную группу, замещенную арильной группой, например, фенилэтиленил и тому подобное.
Термин «гетероарил», используемый здесь, представляет систему пяти- или шестичленного моноциклического ароматического кольца, содержащую от одного до трех гетероатомов, независимо выбранных из N, О или S; и систему любого девяти- или десятичленного бициклического ароматического кольца, содержащую атомы углерода и от одного до четырех гетероатомов, независимо выбранных из N, О или S. Гетероарильная группа может быть присоединена у любого гетероатома или атома углерода, который приводит к образованию стабильной структуры. Примеры гетероарильных групп включают, но не ограничиваются перечисленным, пиридинил, пиримидинил, тиенил, фурил, имидазолил, изоксазолил, оксазолил, пиразолил, пиразинил, пирролил, тиазолил, тиадиазолил, триазолил, бензимидазолил, бензофуранил, бензотиенил, бензизоксазолил, бензоксазолил, индазолил, индолил, бензотиазолил, бензотиадиазолил, бензотриазолил, хинолинил, изохинолинил, пуринил. Предпочтительные гетероарильные группы включают пиримидинил, пиридинил, фурил, имидазолил, бензофуранил и тиазолил.
Термин «циклоалкил», используемый здесь, представляет структуру стабильного три-восьмичленного моноциклического кольца, состоящего из насыщенных атомов углерода. Подходящие примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
Термин «гетероциклоалкил» представляет структуру стабильного насыщенного или частично ненасыщенного три-восьмичленного моноциклического кольца, содержащую атомы углерода и от одного до четырех, предпочтительно, от одного до двух, гетероатомов, независимо выбранных из N, О или S; или систему любого стабильного насыщенного, частично ненасыщенного или частично ароматического девяти-десятичленного бициклического кольца, содержащую атомы углерода и от одного до четырех гетероатомов, независимо выбранных из N, О или S. Гетероциклоалкил может быть присоединен у любого атома углерода или гетероатома, который приводит к образованию стабильной структуры. Подходящие примеры гетероциклоалкильных групп включают пирролидинил, пиразолидинил, пиперидинил, пиперазинил, морфолинил, дитианил, тритианил, диоксоланил, диоксанил, тиоморфолинил, 3,4-метилендиоксифенил, 2,3-дигидробензофурил, 2,3-дигидробензо[1,4]диоксин-6-ил, 2,3-дигидрофуро[2,3-b]пиридинил, 1,2-(метилендиокси)циклогексан, инданил, 2-оксабицикло[2.2.1]гептанил и тому подобное. Предпочтительные гетероциклоалкильные группы включают пиперидинил, пирролидинил, морфолинил, инданил, 2-оксабицикло[2.2.1]гептанил, 3,4-метилендиоксифенил, 2,3-дигидробензофурил и 2,3-дигидробензо[1,4]диоксин-6-ил.
Используемое здесь обозначение «*» обозначает присутствие стереогенного центра.
Имеется в виду, что определение любого заместителя или индекса у определенного положения в молекуле является независимым от его определений в другом месте этой молекулы. Понятно, что средним специалистом в данной области могут быть выбраны заместители и их взаимное расположение в соединениях данного изобретения для получения соединений, которые являются химически стабильными и которые можно легко синтезировать способами, известными в данной области, а также теми способами, которые предложены здесь. Далее имеется в виду, что, когда b или с>1, соответствующие заместители R4 или R5 могут быть одинаковыми или различными.
Когда соединения по данному изобретению имеют, по меньшей мере, один хиральный центр, они могут в соответствии с этим существовать в виде энантиомеров. Когда соединения имеют два или более хиральных центров, они могут дополнительно существовать в виде диастереомеров. Должно быть понятно, что все такие изомеры и их смеси включены в объем настоящего изобретения. Кроме того, некоторые из кристаллических форм соединений могут существовать в виде полиморфов, и подразумевается, что они как таковые включены в настоящее изобретение. Кроме того, некоторые из соединений могут образовывать сольваты с водой (т.е. гидраты) или обычными органическими растворителями, и подразумевается, что такие сольваты также включены в объем данного изобретения.
В стандартной номенклатуре, используемой на всем протяжении данного описания, концевую часть указанной боковой цепи описывают первой с последующим указанием соседней функциональной группы в направлении места присоединения. Таким образом, например, заместитель
«фенилС1-С6алкиламинокарбонилС1-С6алкил» относится к группе формулы
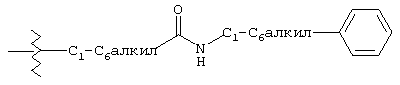
Используемый здесь термин «половая дисфункция» включает мужскую половую дисфункцию, мужскую эректильную дисфункцию, импотенцию, женскую половую дисфункцию, женскую дисфункцию половой возбудимости и женскую половую дисфункцию, относящуюся к кровотоку и продуцированию оксида азота в тканях влагалища и клитора.
Термин «субъект», используемый в данном описании, относится к животному, предпочтительно, млекопитающему, наиболее предпочтительно, человеку, который является объектом лечения, наблюдения или эксперимента.
Термин «терапевтически эффективное количество», используемый в данном описании, означает количество активного соединения или фармацевтического агента, который вызывает биологическую или медицинскую ответную реакцию в системе тканей у животного или человека, которая определяется исследователем, ветеринаром, врачом или другим клиницистом и которая включает ослабление симптомов заболевания или нарушения, подвергаемого лечению.
Имеется в виду, что используемый в данном описании термин «композиция» включает продукт, содержащий определенные ингредиенты в определенных количествах, а также любой продукт, который получают прямым или непрямым способом из комбинаций определенных ингредиентов в определенных количествах.
Для применения в медицине соли соединений данного изобретения относятся к нетоксичным «фармацевтически приемлемым солям». Однако другие соли являются пригодными для получения соединений по данному изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений включают кислотно-аддитивные соли, которые можно, например, получить смешиванием раствора соединения с раствором фармацевтически приемлемой кислоты, такой как хлористоводородная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, когда соединения изобретения имеют кислотную часть, подходящие фармацевтически приемлемые соли их могут включать соли щелочных металлов, например, соли натрия или калия; соли щелочноземельных металлов, например, соли кальция или магния; и соли, образованные с подходящими органическими лигандами, например, четвертичные аммониевые соли. Таким образом, типичные фармацевтически приемлемые соли включают следующие соли: ацетат, бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, эдетат кальция, камфорасульфонат, карбонат, хлорид, клавуланат, цитрат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат, фумарат, глуцептат, глюконат, глутамат, гликоллиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, иодид, изетионат, лактат, лактобионат, лаурат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напсилат, нитрат, аммониевую соль N-метилглюкамина, олеат, памоат (эмбонат), пальмитат, пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, сульфат, субацетат, сукцинат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат.
Настоящее изобретение включает в свой объем пролекарства соединений изобретения. В общем, такие пролекарства будут функциональными производными соединений и способны легко превращаться in vivo в требуемое соединение. Таким образом, в способах лечения настоящего изобретения термин «введение» будет включать лечение различных 'описанных нарушений соединением, определенно описанным, или соединением, которое не может быть определенно описано, но которое превращается в определенное соединение in vivo после введения пациенту. Общепринятые методики для выбора и получения подходящих пролекарственных производных описаны, например, в «Design of Prodrugs», ed. H.Bundgaard, Elsevier, 1985.
Аббревиатуры, используемые в описании, особенно в схемах и примерах, являются следующими:
Соединения формулы (I), где R3 представляет водород, можно получить в соответствии с двумя альтернативными способами из подходящим образом замещенного соединения формулы (III):
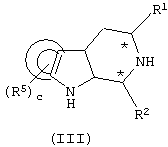
где R1, R2, R5 и с имеют указанные выше значения, которые выбирают и используют в качестве исходного реагента.
Соединение формулы (III) является известным соединением или соединением, полученным известными способами, например, в соответствии со способом, представленным на приведенной ниже схеме 1:
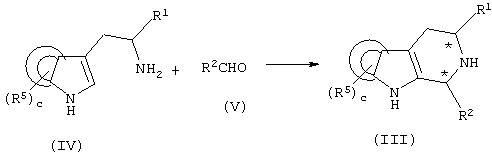
Схема 1
В соответствии с этим, соединение формулы (IV), известное соединение или соединение, полученное известными способами, подвергают взаимодействию с подходящим образом замещенным альдегидом формулы (V) в органическом растворителе, таком как DCM, ТГФ, толуол и тому подобное, в присутствии кислотного катализатора, такого как ТФУ, толуолсульфоновая кислота и тому подобное, получая соответствующее соединение формулы (III).
Обычно в первом из двух альтернативных способов соединения формулы (I) можно получить взаимодействием подходящим образом замещенного соединения формулы (III) с получением соответственно замещенного производного пирролопиридинона. Во втором способе из двух альтернативных способов соединения формулы (I) можно получить сначала взаимодействием подходящим образом замещенного соединения формулы (III) с образованием трициклической пирролопиридиноновой части с последующим введением дополнительных заместителей. Второй способ является особенно предпочтительным для получения соединений формулы (I), где Y представляет -C(S)-, -C(O)O-RA или -C(O)RA.
Более определенно, соединения формулы (I), где R3 представляет водород, можно получить из подходящим образом замещенного соединения формулы (III) в соответствии со способами, представленными на схеме 2.
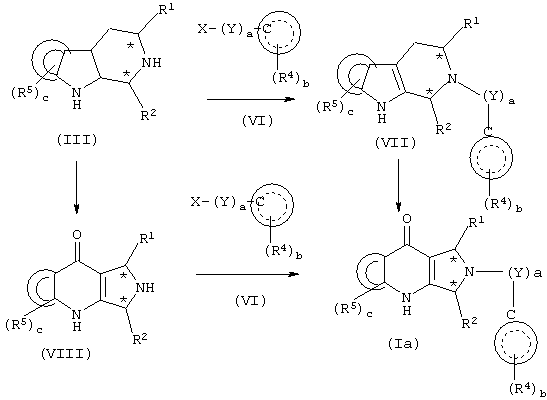
Схема 2
В первом способе подходящим образом замещенное соединение формулы (III) подвергают взаимодействию с подходящим образом замещенным соединением формулы (VI), где Х представляет галоген, гидрокси, тозилат, мезилат, п-нитрофеноксид или тому подобное, предпочтительно, Х представляет галоген, гидрокси или п-нитрофеноксид, в органическом растворителе, таком как ДМФ, ТГФ, DCM, толуол и тому подобное, получая соответствующее соединение формулы (VII). Для соединений формулы (I), где (Y)a представляет (Y)0 (т.е., где а равно 0, так что Y отсутствует), реакционную смесь, предпочтительно, нагревают до температуры, выше чем или равной приблизительно 100°С. Для соединений формулы (I), где (Y)a представляет (Y)0 (т.е., где а равно 0, так что Y отсутствует), и  представляет пиридинил, реакционную смесь, предпочтительно, катализируют при температуре в диапазоне приблизительно 30-120°С катализатором, таким как Pd(OAc)2, Pd2dba3, Pd(dppf)Cl2 и тому подобное, в органическом растворителе, таком как 1,4-диоксан, ТГФ, ДМФ, DCM, толуол и тому подобное, получая соответствующее соединение формулы (VII).
представляет пиридинил, реакционную смесь, предпочтительно, катализируют при температуре в диапазоне приблизительно 30-120°С катализатором, таким как Pd(OAc)2, Pd2dba3, Pd(dppf)Cl2 и тому подобное, в органическом растворителе, таком как 1,4-диоксан, ТГФ, ДМФ, DCM, толуол и тому подобное, получая соответствующее соединение формулы (VII).
Соединение формулы (VII) затем подвергают взаимодействию с окисляющим агентом, таким как NaIO4, KO2, синглетный кислород, газообразный кислород, озон и тому подобное, причем, предпочтительно, применяют газообразный кислород приблизительно при атмосферном давлении, получая соответствующее производное пирролопиридинона формулы (Ia). Когда окисляющим агентом является газообразный кислород, взаимодействие проводят в присутствии основания, такого как гидрид натрия, трет-бутоксид калия и тому подобное.
В альтернативном способе, указанном на схеме 2, подходящим образом замещенное соединение формулы (III) сначала подвергают взаимодействию с окисляющим агентом, таким как NaIO4, KO2, синглетный кислород, газообразный кислород, озон и тому подобное, причем, предпочтительно, применяют газообразный кислород приблизительно при атмосферном давлении, получая соответствующее соединение формулы (VIII). Когда окисляющим агентом является газообразный кислород, взаимодействие проводят в присутствии основания, такого как гидрид натрия, трет-бутоксид калия и тому подобное.
Соединение формулы (VIII) затем подвергают взаимодействию с подходящим образом замещенным соединением формулы (VI), где Х представляет галоген, гидрокси, тозилат, мезилат, п-нитрофеноксид или тому подобное, предпочтительно, Х представляет галоген, гидрокси или п-нитрофеноксид, в органическом растворителе, таком как ДМФ, ТГФ, DCM, толуол и тому подобное, необязательно в присутствии катализатора, такого как DMAP, получая соответствующий замещенный пирролопиридинон формулы (Ia). Для соединений формулы (I), где (Y)a представляет (Y)0 (т.е., где а равно 0, так что Y отсутствует), реакционную смесь, предпочтительно, нагревают до температуры, выше или равной приблизительно 50°С. Для соединений формулы (VIII), где (Y)a представляет (Y)0 (т.е., где а равно 0, так что Y отсутствует), и  представляет пиридинил, реакционную смесь, предпочтительно, катализируют при температуре в диапазоне приблизительно 30-120°С катализатором, таким как Pd(OAc)2, Pd2dba3, Pd(dppf)Cl2 и тому подобное, в органическом растворителе, таком как 1,4-диоксан, ТГФ, ДМФ, DCM, толуол и тому подобное, получая соответствующее соединение формулы (Ia).
представляет пиридинил, реакционную смесь, предпочтительно, катализируют при температуре в диапазоне приблизительно 30-120°С катализатором, таким как Pd(OAc)2, Pd2dba3, Pd(dppf)Cl2 и тому подобное, в органическом растворителе, таком как 1,4-диоксан, ТГФ, ДМФ, DCM, толуол и тому подобное, получая соответствующее соединение формулы (Ia).
Альтернативно, для соединений формулы (I), где (Y)a представляет СН2 и  представляет незамещенный или замещенный арил или незамещенный или замещенный гетероарил, соединение формулы (VIII) можно получить взаимодействием соединения формулы (Ia) с газообразным водородом, где газообразный водород применяют при давлении в диапазоне приблизительно от атмосферного давления до приблизительно 80 фунт/кв. дюйм (551,6 кПа) в присутствии катализатора, такого как Pd, Pt, палладий на угле и тому подобное, в органическом растворителе, таком как метанол, этанол, этилацетат и тому подобное. Соединение формулы (VIII) можно затем далее функционализировать, как описано выше.
представляет незамещенный или замещенный арил или незамещенный или замещенный гетероарил, соединение формулы (VIII) можно получить взаимодействием соединения формулы (Ia) с газообразным водородом, где газообразный водород применяют при давлении в диапазоне приблизительно от атмосферного давления до приблизительно 80 фунт/кв. дюйм (551,6 кПа) в присутствии катализатора, такого как Pd, Pt, палладий на угле и тому подобное, в органическом растворителе, таком как метанол, этанол, этилацетат и тому подобное. Соединение формулы (VIII) можно затем далее функционализировать, как описано выше.
Соединение формулы (I), где b равно 1 (т.е., где группа, представленная  , замещена одним заместителем R4), можно получить из подходящим образом замещенного соединения формулы (III) в соответствии с тремя альтернативными способами.
, замещена одним заместителем R4), можно получить из подходящим образом замещенного соединения формулы (III) в соответствии с тремя альтернативными способами.
В первом способе подходящим образом замещенное соединение формулы (III) сначала превращают в соответствующий пирролопиридинон способом, указанным на схеме 2, с последующим двухстадийным замещением у азота пиррола, как указано на схеме 3.
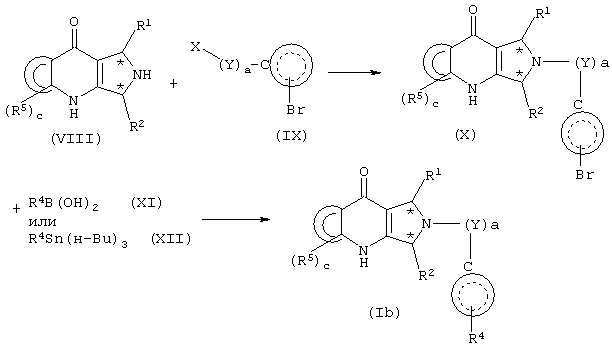
Схема 3
В частности, соединение формулы (VIII) подвергают взаимодействию с подходящим образом замещенным соединением формулы (IX), где Х представляет галоген, в присутствии основания, такого как TEA, DIPEA и тому подобное, в органическом растворителе, таком как ДМФ, DCM, ТГФ и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 20 до приблизительно 150°С, получая соответствующее соединение формулы (X).
Соединение формулы (X) подвергают взаимодействию с подходящим образом замещенной бороновой кислотой формулы (XI) или подходящим образом замещенным трибутилстаннаном формулы (XII), получая соответствующее соединение формулы (Ib). Когда выбранным реагентом является бороновая кислота формулы (XI), соединение формулы (X) подвергают взаимодействию в органическом растворителе, таком как ДМФ, ТГФ, диоксан и тому подобное, в присутствии катализатора, такого как Pd(Ph3Р)4, Pd(dppf)(OAc)2 и тому подобное, предпочтительно, при температуре в диапазоне приблизительно 80-150°С. Когда выбранным реагентом является трибутилстаннан формулы (XII), соединение формулы (X) подвергают взаимодействию в растворителе, таком как ДМФ, в присутствии катализатора, такого как Pd(dppf)(OAc)2.
Во втором способе соединение формулы (III) сначала замещают бромзамещенным  , затем превращают в соответствующий пирролопиридинон и затем далее замещают у
, затем превращают в соответствующий пирролопиридинон и затем далее замещают у  , как показано на схеме 4.
, как показано на схеме 4.
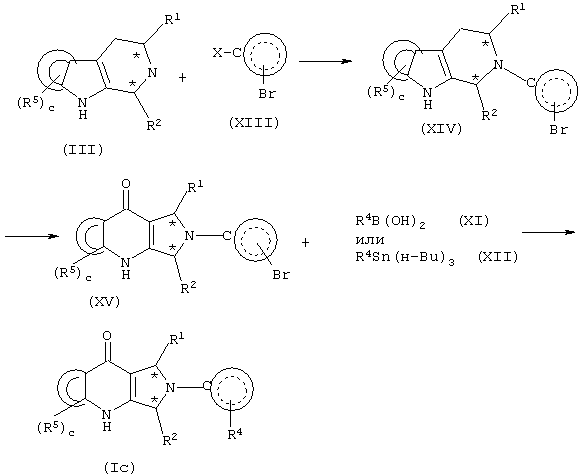
Схема 4
Более конкретно, подходящим образом замещенное соединение формулы (III) подвергают взаимодействию с подходящим образом замещенным соединением формулы (XIII), где Х представляет галоген, в присутствии основания, такого как TEA, DIPEA и тому подобное, в органическом растворителе, таком как ДМФ, толуол и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 100 до приблизительно 150°С, получая соответствующее соединение формулы (XIV).
Соединение формулы (XIV) подвергают взаимодействию с окисляющим агентом, таким как NaIO4, KO2, синглетный кислород, газообразный кислород, озон и тому подобное, причем предпочтительно, применяют газообразный кислород при атмосферном давлении, получая соответствующее соединение формулы (XV).
Соединение формулы (XV) подвергают взаимодействию с подходящим образом замещенной бороновой кислотой формулы (XI) или подходящим образом замещенным трибутилстаннаном формулы (XII), получая соответствующее соединение формулы (Ic). Когда выбранным реагентом является бороновая кислота формулы (XI), соединение формулы (XV) подвергают взаимодействию в органическом растворителе, таком как ДМФ, диоксан, вода и тому подобное, в присутствии катализатора, такого как Pd(Ph3Р)4, Pd(dppf)(OAc)2 и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 80 до приблизительно 160°С. Когда выбранным реагентом является трибутилстаннан формулы (XII), соединение формулы (XV) подвергают взаимодействию в растворителе, таком как ДМФ, TEA и тому подобное, в присутствии катализатора, такого как Pd(dppf)(OAc)2.
В третьем способе соединение формулы (III) сначала замешают бромзамещенным  , далее замещают у
, далее замещают у  заместителем R4 и затем превращают в соответствующий пирролопиридинон, как показано на схеме 5.
заместителем R4 и затем превращают в соответствующий пирролопиридинон, как показано на схеме 5.
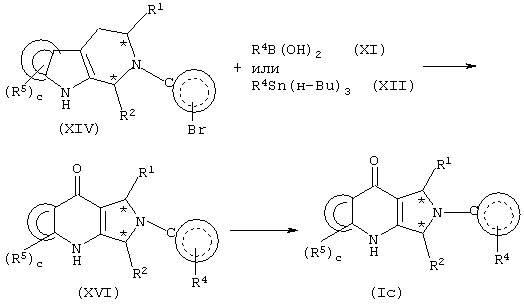
Схема 5
Более конкретно, соединение формулы (XIV) подвергают взаимодействию с подходящим образом замещенной бороновой кислотой формулы (XI) или подходящим образом замещенным трибутилстаннаном формулы (XII), получая соответствующее соединение формулы (XVI). Когда выбранным реагентом является бороновая кислота формулы (XI), соединение формулы (XIV) подвергают взаимодействию в органическом растворителе, таком как ДМФ, диоксан, вода и тому подобное, в присутствии катализатора, такого как Pd(Ph3Р)4, Pd(dppf)(OAc)2 и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 80 до приблизительно 120°С. Когда выбранным реагентом является трибутилстаннан формулы (XII), соединение формулы (XIV) подвергают взаимодействию в растворителе, таком как ДМФ, диоксан и тому подобное, в присутствии катализатора, такого как Pd(dppf)(OAc)2.
Соединение формулы (XVI) подвергают взаимодействию с окисляющим агентом, таким как NaIO4, KO2, синглетный кислород, газообразный кислород, озон и тому подобное, причем, предпочтительно, применяют газообразный кислород при атмосферном давлении, получая соответствующее соединение формулы (Ic).
Соединения формулы (I), где b равно целому числу, выбранному из 2, 3 и 4 (т.е., где  замещен 2, 3 или 4 группами R4), можно аналогично получить в соответствии со способами, указанными на схемах 3, 4 и 5, с подходящей заменой реагента, содержащего
замещен 2, 3 или 4 группами R4), можно аналогично получить в соответствии со способами, указанными на схемах 3, 4 и 5, с подходящей заменой реагента, содержащего  , соответствующим реагентом, у которого замещен 2, 3 или 4 атомами брома, группы брома затем подвергают взаимодействию для введения нужных групп R4.
, соответствующим реагентом, у которого замещен 2, 3 или 4 атомами брома, группы брома затем подвергают взаимодействию для введения нужных групп R4.
Соединения формулы (I), где (Y)a представляет С(О), можно получить в соответствии с двумя альтернативными способами. В первом способе пирролопиридиноновое соединение формулы (VIII) сначала замещают подходящей выбранной карбоновой кислотой или хлорангидридом кислоты с последующим дальнейшим замещением  заместителем R4, как показано на схеме 6.
заместителем R4, как показано на схеме 6.
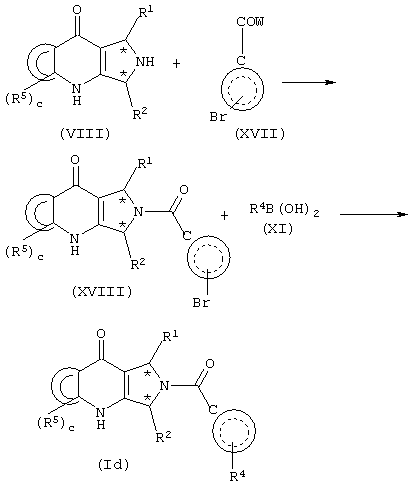
Схема 6
Более конкретно, подходящим образом замещенное пирролопиридиноновое соединение формулы (VIII) подвергают взаимодействию с подходящим образом замещенной карбоновой кислотой или хлорангидридом кислоты формулы (XVIII), где W представляет ОН или Cl, в органическом растворителе, таком как ДМФ, ТГФ, диоксан и тому подобное, и, когда W представляет ОН, в присутствии катализатора, такого как PyBrop, DCC и тому подобное, и, когда W представляет Cl, в присутствии основания, такого как TEA, DIPEA и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 0 до приблизительно 30°С, получая соответствующее соединение формулы (XVIII).
Соединение формулы (XVIII) подвергают взаимодействию с подходящим образом замещенной бороновой кислотой формулы (XI) в органическом растворителе, таком как ДМФ, диоксан, вода и тому подобное, в присутствии катализатора, такого как Pd(Ph3Р)4 и тому подобное, и, предпочтительно, при температуре в диапазоне приблизительно от 80 до приблизительно 120°С, получая соответствующее соединение формулы (Id).
По второму способу подходящим образом замещенное соединение формулы (III) сначала превращают в соответствующий пирролопиридинон с последующим замещением в две стадии с использованием подходящей выбранной карбоновой кислоты и затем бороновой кислоты или станнана, как указано на схеме 7.
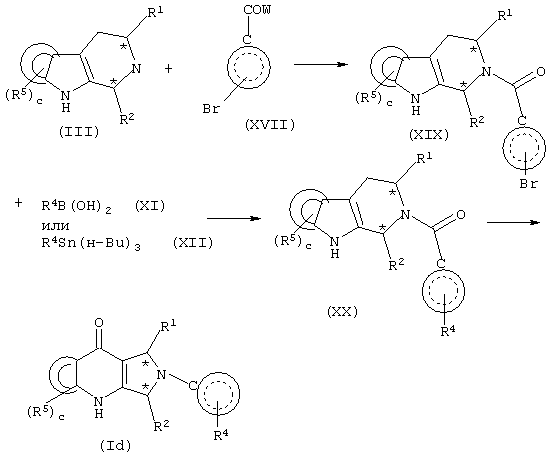
Схема 7
Более конкретно, подходящим образом замещенное соединение формулы (III) подвергают взаимодействию с подходящим образом замещенной карбоновой кислотой формулы (XVII), где W представляет галоген или гидрокси, в органическом растворителе, таком как TEA, DIPEA и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 80 до приблизительно 130°С, получая соответствующее соединение формулы (XIX).
Соединение формулы (XIX) подвергают взаимодействию с подходящим образом замещенной бороновой кислотой формулы (XI) или подходящим образом замещенным трибутилстаннаном формулы (XII), получая соответствующее соединение формулы (XX). Когда выбранным реагентом является бороновая кислота формулы (XI), соединение формулы (XIX) подвергают взаимодействию в органическом растворителе, таком как ДМФ, диоксан, вода и тому подобное, в присутствии катализатора, такого как Pd(Ph3Р)4, Pd(dppf)(OAc)2 и тому подобное, предпочтительно, при температуре в диапазоне приблизительно от 80 до приблизительно 120°С. Когда выбранным реагентом является трибутилстаннан формулы (XII), соединение формулы (XIX) подвергают взаимодействию в растворителе, таком как ДМФ, диоксан и тому подобное, в присутствии катализатора, такого как Pd(dppf)(OAc)2.
Соединение формулы (XX) подвергают взаимодействию с окисляющим агентом, таким как NaIO4, KO2, синглетный кислород, газообразный кислород, озон и тому подобное, предпочтительно, KO2, получая соответствующее соединение формулы (Id).
Соединения формулы (I), где R3 не является водородом, и соединения формулы II можно получить в соответствии со способом, указанным на схеме 8.
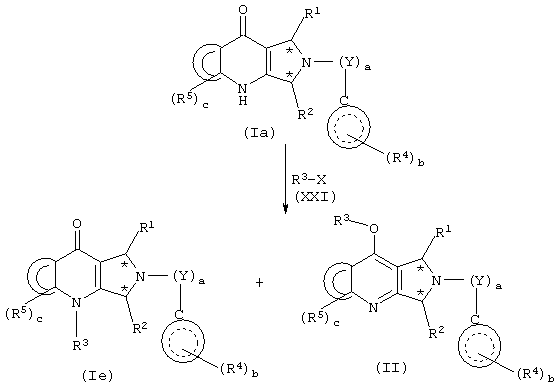
Схема 8
Более конкретно, соединение формулы (Ia) подвергают взаимодействию с подходящим образом замещенным соединением формулы (XXI), где Х представляет галоген, гидрокси, тозилат, мезилат и тому подобное, предпочтительно, Х представляет галоген, в органическом растворителе, таком как ТГФ, ДМФ, дихлорметан, толуол и тому подобное, предпочтительно, ТГФ или ДМФ, получая смесь соответственно замещенного соединения формулы (Ie) и соответствующего замещенного соединения формулы (II). Когда в соединении формулы (XXI) Х представляет галоген, реакцию, предпочтительно, проводят в присутствии органического или неорганического основания, такого как триэтиламин, диизопропилэтиламин, карбонат калия, гидрид натрия, гидроксид натрия и тому подобное.
Соединения формул (Ie) и (II), предпочтительно, разделяют известными способами, такими как перекристаллизация, колоночная хроматография, ВЭЖХ и тому подобное.
Соединения формулы (VII), где Ya представляет Y0 (т.е., где Y отсутствует) и  представляет 2-(4-замещенный)тиазолил, можно получить способом, указанным на схеме 9.
представляет 2-(4-замещенный)тиазолил, можно получить способом, указанным на схеме 9.
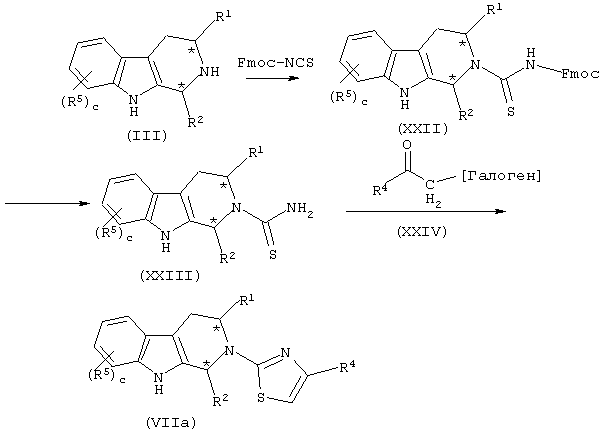
СХЕМА 9
В соответствии с этим, подходящим образом замещенное соединение формулы (III) подвергают взаимодействию с Fmoc-NCS в органическом растворителе, таком как DCM, ДМФ, ТГФ и тому подобное, предпочтительно, при комнатной температуре, получая соответствующее соединение формулы (XXII).
Соединение (XXII) подвергают взаимодействию с 20% пиперидином в спирте, таком как метанол, этанол и тому подобное, получая соответствующий амин формулы (XXIII).
Амин формулы (XXIII) подвергают взаимодействию с подходящим образом замещенным α-галогенметилкетоном формулы (XXIV) в присутствии органического растворитель или смеси растворителей, таких как ДМФ, этанол:диоксан и тому подобное, в присутствии основания, такого как TEA, DIPEA и тому подобное, предпочтительно, при температуре приблизительно 70°С, получая соответствующее соединение формулы (VIIa).
Определенные диастереомеры соединений формулы (I), более конкретно, соединения формулы (I), где R1 представляет водород и нужной является R-конфигурация у хирального центра связи R2 с пирролопиридиноном, можно получить способом, указанным на схеме 10.

Схема 10
В соответствии с этим, подходящим образом замещенное соединение формулы (XXV), известное соединение или соединение, полученное известными способами, где R1 представляет водород и Ar представляет арильную группу, предпочтительно, нафтил, более предпочтительно, 1-нафтил, подвергают взаимодействию с подходящим образом замещенным альдегидом, соединением формулы (XXVI), в органическом растворителе, таком как п-ксилол, о-ксилол, толуол, DCM и тому подобное, при температуре в диапазоне приблизительно 25-270°С в апротонных или протонных условиях, получая смесь соответствующих диастереомеров, соединений формул (XXVII) и XXVIII).
R-диастереомер, соединение формулы (XXVII) отделяют от соединения формулы (XXVIII) перекристаллизацией или хроматографией на силикагеле.
Соединение формулы (XXVII) (S-диастереомер) превращают в нужный R-диастереомер, соединение формулы (XXVIII), перемешивая соединение формулы (XXVII) в кислоте, такой как ТФУ, HCl, TsOH и тому подобное, в присутствии органического растворителя, такого как СН2Cl2, DCM, 1,4-диоксан и тому подобное, получая нужный R-диастереомер, соединение формулы (XXVIII).
Соединение формулы (XXVIII) подвергают взаимодействию с окисляющим агентом, таким как газообразный кислород, синглетный кислород, KO2, NaIO4, озон и тому подобное, предпочтительно, газообразный кислород, приблизительно при атмосферном давлении, получая соответствующее соединение формулы (XXIX). Когда окисляющим агентом является газообразный кислород, взаимодействие проводят в присутствии основания, такого как гидрид натрия, трет-бутоксид калия и тому подобное, в органическом растворителе, таком как ДМФ, ДМСО, NMP и тому подобное.
Соединение формулы (XXIX) подвергают взаимодействию с восстанавливающим агентом, таким как газообразный водород, в присутствии катализатора, такого как палладий на угле, в полярном растворителе, таком как метанол, этанол и тому подобное, получая соответствующее соединение формулы (VIIIa).
Соединение формулы (VIIIa) можно затем далее подвергнуть взаимодействию с получением соответствующего соединения формулы (I) способом, указанным выше на схеме 3.
У соединений формулы (I), где R1 не является водородом, может присутствовать второй хиральный центр у связи группы R1 с пирролопиридиноном. Если определенная ориентация группы R1 присутствует в исходном реагенте, соединении формулы (XXV) на приведенной выше схеме 10, ее ориентация будет влиять на превращение диастереомеров.
Когда способы получения соединений по изобретению дают смесь стереоизомеров, эти изомеры можно разделить общепринятыми способами, такими как препаративная хроматография. Соединения можно получить в рацемической форме, или индивидуальные энантиомеры можно получить энантиоселективным синтезом, разделением смесей энантиомеров или из энантиомерно обогащенных реагентов. Соединение можно, например, разделить на его энантиомерные компоненты стандартными способами, такими как образование диастереомерной пары образованием соли с оптически активной кислотой, такой как (-)-ди-п-толуоил-d-винная кислота и/или (+)-ди-п-толуоил-l-винная кислота, с последующей фракционной кристаллизацией и получением свободного основания. Соединения можно также разделить образованием диастереомерных эфиров, амидов или аминов с последующим хроматографическим разделением и удалением хирального вспомогательного соединения. Альтернативно, соединения можно разделить с использованием хиральной колонки ВЭЖХ.
Во время проведения любого из способов получения соединений настоящего изобретения может быть необходимо и/или желательно защитить чувствительные или реакционноспособные группы в любых молекулах, принимающих участие в способах получения. Этого можно достичь при помощи общепринятых защитных групп, таких как группы, описанные в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973, и T.W.Greene and P.G.M.Wuts, Protective Groups in Organic Synthesis, John Willey and Sons, 1991. Защитные группы можно удалить на удобной последующей стадии с использованием способов, известных в данной области.
Пригодность соединений для лечения половой дисфункции можно определить по методикам, описанным в приведенных ниже примерах 95, 96 и 97.
Настоящее изобретение, следовательно, относится к способу лечения половой дисфункции, более конкретно, мужской эректильной дисфункции у субъекта, нуждающегося в этом, который включает введение любого из соединений, как определено выше, в количестве, эффективном для лечения ED. Соединение можно вводить пациенту любым общепринятым путем введения, включая, но не ограничиваясь перечисленным, внутривенный, пероральный, подкожный, внутримышечный, внутрикожный и парентеральный. Количество соединения, которое эффективно для лечения ED, находится между 0,01 мг на кг и 20 мг на кг массы тела субъекта.
Настоящее изобретение относится также к фармацевтическим композициям, включающим одно или несколько соединений данного изобретения в сочетании с фармацевтически приемлемым носителем. Эти композиции, предпочтительно, находятся в виде единичных дозированных форм, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные парентеральные растворы или суспензии, дозированный аэрозоль или жидкие спреи, капли, ампулы, устройства для аутоинъекции или суппозитории, для перорального, парентерального, интраназального, сублингвального или ректального введения или для введения ингаляцией или инсуффляцией. Альтернативно, композиция может быть представлена в форме, подходящей для введения раз в неделю или один раз в месяц; например, нерастворимую соль активного соединения, такую как деканоатная соль, можно приспособить для получения препарата-депо для внутримышечной инъекции. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например, общепринятыми ингредиентами для таблетирования, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальцийфосфат или камеди, и другими фармацевтическими разбавителями, например, водой для образования твердой предварительно составленной композиции, содержащей гомогенную смесь соединения настоящего изобретения или его фармацевтически приемлемой соли. Когда указывают на такие предварительно составленные композиции, как гомогенные, это означает, что активный ингредиент диспергирован равномерно во всей композиции, так что композицию можно легко разделить на равно эффективные лекарственные формы, такие как таблетки, пилюли и капсулы. Такую твердую предварительно составленную композицию затем разделяют на единичные дозированные формы описанного выше типа, содержащие от 1 до приблизительно 1000 мг активного ингредиента настоящего изобретения. Таблетки или пилюли новой композиции можно покрыть оболочкой или приготовить иным путем для получения лекарственной формы, обеспечивающей преимущества пролонгированного действия. Например, таблетка или пилюля может включать внутренний дозированный компонент и внешний дозированный компонент, причем последний находится в форме оболочки на первом. Два компонента можно разделить энтеросолюбильным слоем, который служит для придания устойчивости к дезинтеграции в желудке и позволяет внутреннему компоненту проходить в неизменном виде в двенадцатиперстную кишку или задерживает его высвобождение. Для таких энтеросолюбильных слоев или покрытий можно использовать различные материалы, причем такие материалы включают ряд полимерных кислот с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы.
Жидкие формы, в которые можно включить новые композиции настоящего изобретения для введения перорально или инъекцией, включают водные растворы, сиропы, подходящим образом обработанные для придания запаха и вкуса, водные или масляные суспензии и обработанные для придания вкуса и запаха эмульсии с пищевыми маслами, такими как хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические наполнители. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические и натуральные камеди, такие как трагакант, аравийская камедь, альгинат, декстран, натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, поливинилпирролидон или желатин.
Способ лечения половой дисфункции, более конкретно, мужской эректильной дисфункции, описанный в настоящем изобретении, можно также осуществить с применением фармацевтической композиции, включающей любое из соединений, как определено выше, и фармацевтически приемлемый носитель. Фармацевтическая композиция может содержать между приблизительно 1 мг и 1000 мг, предпочтительно, приблизительно от 1 до 200 мг, соединения и может быть представлена в любой форме, подходящей для выбранного способа введения. Носители включают необходимые и инертные фармацевтические эксципиенты, содержащие, но не ограничивающиеся перечисленным, связующие, суспендирующие агенты, смазывающие вещества, корригенты, подслащивающие агенты, консерванты, красители и покрытия. Композиции, пригодные для перорального введения, включают твердые формы, такие как пилюли, таблетки, мелкие капсулы, капсулы (причем, каждая включает готовые формы с немедленным высвобождением, регулируемым во времени высвобождением и длительным высвобождением), гранулы и порошки, и жидкие формы, такие как растворы, сиропы, эликсиры, эмульсии и суспензии. Формы, пригодные для парентерального введения, включают стерильные растворы, эмульсии и суспензии.
Соединения настоящего изобретения можно вводить, преимущественно, в виде единственной суточной дозы или общую суточную дозу можно вводить в виде разделенных доз два, три или четыре раза в день. Кроме того, соединения настоящего изобретения можно вводить в интраназальной форме с местным использованием подходящих интраназальных наполнителей или посредством чрескожных пластырей на кожу, хорошо известных специалисту в данной области. При введении форме системы чрескожной доставки дозированное введение будет, конечно, непрерывным, а не прерывистым, на всем протяжении схемы приема лекарственного средства.
Например, для перорального введения в форме таблетки или капсулы активный лекарственный компонент можно смешать с пероральным, нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и тому подобное. Кроме того, когда желательно или необходимо, в смесь можно ввести подходящие связующие, смазывающие вещества, дезинтегрирующие агенты и красящие агенты. Подходящие связующие включают, но не ограничиваются ими, крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, подслащивающие вещества кукурузы, природные и синтетические камеди, такие как аравийская камедь, трагакант, или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и тому подобное. Дезинтеграторы включают, но не ограничиваются ими, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и тому подобное.
Жидкие формы могут включать подходящим образом обработанные для придания запаха и вкуса суспендирующие или диспергирующие агенты, такие как синтетические и природные камеди, например, трагакант, аравийская камедь, метилцеллюлоза и тому подобное. Для парентерального введения желательны стерильные суспензии и растворы. Когда желательно внутривенное введение, применяют изотоничные препараты, которые обычно содержат подходящие консерванты.
Соединение настоящего изобретения можно также ввести в форме липосомных систем доставки, таких как мелкие однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы можно образовать из различных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Соединения настоящего изобретения можно также доставить с использованием моноклональных антител в качестве индивидуальных носителей, с которыми сочетают молекулы соединения. Соединения настоящего изобретения можно также сочетать с растворимыми полимерами как носителями доставляемых лекарственных средств. Такие полимеры могут включать поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидфенол, полигидроксиэтиласпартамамидфенол или полиэтиленоксидполилизин, замещенный остатком пальмитоилом. Кроме того, соединения настоящего изобретения можно сочетать с классом биоразрушаемых полимеров, пригодных для достижения регулируемого высвобождения лекарственного средства, например, полиакриловой кислотой, поли-эпсилон-капролактоном, полигидроксимасляной кислотой, полиортоэфирами, полиацеталями, полигидропиранами, полицианоакрилатами и сшитыми или амфипатическими блок-сополимерами гидрогелей.
Соединения настоящего изобретения можно вводить в любых указанных выше композициях и в соответствии со схемами приема лекарственных средств, установленными в данной области всегда, когда требуется лечение половой дисфункции, более конкретно, мужской эректильной дисфункции.
Суточная доза продуктов может варьировать в широком диапазоне от 1 до 1000 мг на взрослого человека в день. Для перорального введения композиции, предпочтительно, представляют в форме таблеток, содержащих 1,0, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 250 и 500 миллиграмм активного ингредиента, для симптоматического регулирования дозы для подвергаемого лечению пациента. Эффективное количество лекарственного средства обычно поставляют при уровне дозы приблизительно от 0,01 мг/кг до приблизительно 20 мг/кг массы тела в день. Диапазон, предпочтительно, составляет приблизительно от 0,1 мг/кг до приблизительно 10 мг/кг массы тела в день и, особенно, приблизительно от 0,1 мг/кг до приблизительно 3 мг/кг массы тела в день.
Оптимальные дозы, которые нужно ввести, могут быть легко определены специалистом в данной области, они будут варьировать в зависимости от конкретного используемого соединения, способа введения, эффективности препарата и прогресса в состоянии заболевания. Кроме того, факторы, связанные с конкретным пациентом, подвергаемым лечению, в том числе возраст пациента, масса, диета и время введения, будут приводить к необходимости регулирования доз.
Следующие примеры приводятся, чтобы помочь понять изобретение, и не предназначаются и не должны ни коем образом истолковываться как ограничивающие изобретение, заявленное в формуле изобретения, представленной ниже. Если не оговорено особо, спектры 1Н-ЯМР регистрировали на спектрометре Bruker.
ПРИМЕР 1
1-(3,4-Метилендиоксифенил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболина (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) (7,37 г, 25 ммоль) в безводном ДМФ (25 мл) добавляют триэтиламин (3,52 мл, 25 ммоль) и бензилбромид (3,00 мл, 25 ммоль). Смесь перемешивают при температуре окружающей среды в течение ночи и добавляют по каплям к раствору гидроксида натрия (25 ммоль) в воде (200 мл). Образуется осадок, который отфильтровывают в вакууме, промывают водой (2×50 мл) и сушат в вакууме в течение ночи, получая продукт в виде свободно сыпучего светло-желтого порошка.
МС (m/z) 383 (МН+)
1H-ЯМР (CDCl3) δ 2,57-2,89 (серия м, 3Н), 3,18-3,23 (м, 1Н), 3,33 (д, J=13,7 Гц, 1Н), 3,63 (д, J=13,7 Гц, 1Н), 4,55 (с, 1Н), 5,94 (нд, J=2,2 Гц, 2Н), 6,77-7,52 (сериям, 13Н).
ПРИМЕР 1А
(R)-1-(3,4-Метилендиоксифенил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин
По методике, описанной в примере 1, (R)-1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 383 (МН+)
ПРИМЕР 2
1-(2,З-Дигидробензофуран-5-ил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин
Указанное в заголовке соединение получают способом, описанным в примере 1, используя 1-(2,3-дигидробензофуран-5-ил)-2,3,4,9-тетрагидро-1H-β-карболин в качестве исходного реагента.
МС (m/z) 381 (MH+)
1H-ЯМР (CDCl3) δ 2,59-2,90 (серия м, 3Н), 3,13-3,24 (м, 3Н), 3,33 (д, J=13,5 Гц, 1Н), 3,93 (д, J=13,5 Гц, 1Н), 4,56 (т, J=8,6 Гц, 2Н), 6,75 (д, J=8,1 Гц, 1Н), 7,05-7,35 (серия м, 10Н), 7,49-7,52 (м, 1Н).
ПРИМЕР 2А
(R)-1-(2,3-Дигидробензофуран-5-ил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин
По методике, описанной в примере 2, (R)-1-(2,3-дигидробензофуран-5-ил)-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 381 (МН+)
[α]=-56,9° (с=0,62, СН3ОН)
ПРИМЕР 3
1,2,3,4-Тетрагидро-2-бензил-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#54)
1-(3,4-Метилендиоксифенил)-2-бензил-2,3,4,9-тетрагидро-1H-β-карболин (0,79 г, 2,0 ммоль) (получен, как в примере 1) растворяют в безводном ДМФ (15 мл). Добавляют трет-бутоксид калия (0,56 г, 5,0 ммоль), затем через иглу шприца барботируют кислород. Смесь выдерживают при комнатной температуре в течение одного часа и затем выливают на смесь 1 н. HCl (5 мл), воды (35 мл) и этилацетата (35 мл). Пушистый желтый осадок отделяют, органический слой удаляют и водный раствор экстрагируют этилацетатом (15 мл). Экстрагированный слой перемешивают и оставляют на ночь. На следующий день выделяют дополнительное количество продукта (в виде осадка). Сушка объединенных твердых веществ дает продукт в виде желтого порошка.
МС (m/z) 397 (МН+)
1H-ЯМР (ДМСО-d6) δ 3,52 (дд, J=11,9, 3 Гц, 1Н), 3,63 (д, J=13,2 Гц, 1Н), 3,84 (д, J=13,2 Гц, 1Н), 3,93 (дд, J=11,9, 3 Гц, 1Н), 5,10 (с, 1Н), 6,05 (нд, J=3,4 Гц, 2Н), 6,98 (с, 3Н), 7,26-7,36 (м, 6Н), 7,54-7,59 (м, 2Н), 8,10 (д, J=8 Гц, 1Н), 11,42 (с, 1Н).
ПРИМЕР 3А
(R)-1,2,3,4-Тетрагидро-2-бензил-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#67)
По методике, описанной в примере 3, (R)-1-(3,4-метилендиоксифенил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 397 (МН+)
ПРИМЕР 4
1,2,3,4-Тетрагидро-2-бензил-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он (#60)
1-(2,З-Дигидробензофуран-5-ил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин (получен, как в примере 2) (3,10 г, 8,15 ммоль) растворяют в безводном ДМФ (20 мл). Добавляют трет-бутоксид калия (2,29 г, 20,38 ммоль), затем через иглу шприца барботируют кислород. Раствор перемешивают в течение 1,5 часов. К реакционной смеси добавляют раствор HCl в эфире (10 мл, 2М) и раствор по каплям вносят в интенсивно перемешиваемую воду. Полученную суспензию перемешивают в течение ночи. Коричневое твердое вещество отфильтровывают и промывают водой. Фильтрат нейтрализуют 1 н. NaOH, получая желтый осадок. Твердое вещество отфильтровывают, промывают водой, быстро сушат и частично растворяют в смеси ТГФ/метанол. Осажденное твердое вещество отфильтровывают и промывают эфиром, получая продукт в виде бледно-желтого твердого вещества.
МС (m/z) 395 (МН+)
1H-ЯМР (ДМСО-d6) δ 3,19 (т, J=8,7 Гц, 2Н), 3,53 (д, J=11,8 Гц, 1Н), 3,61 (д, J=12,2 Гц, 1Н), 3,82 (д, J=12,2 Гц, 1Н), 3,92 (д, J=11,8 Гц, 1Н), 4,55 (т, J=8,7 Гц, 2Н), 5,08 (с, 1Н), 6,81 (д, J=8,1 Гц, 1Н), 7,16-7,59 (серия м, 9Н), 8,10 (д, J=8,1 Гц, 1Н), 11,42 (с, 1Н).
ПРИМЕР 4А
(R)-1,2,3,4-Тетрагидро-2-бензил-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он (#77)
По методике, описанной в примере 4, (R)-1-(2,3-дигидробензофуран-5-ил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 395 (MH+)
[α]=-110,0° (с=0,43, СН3ОН); ВЭЖХ, колонка Chiralpak 0,46×25 см (внутр. диаметр), 0,1% DEA/MeOH, Tr=5,360 мин.
ПРИМЕР 5
Гидрохлоридная соль 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (#4)
Способ А: соль HCl
К суспензии 1,2,3,4-тетрагидро-2-бензил-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (получен, как в примере 3) (1,12 г, 2,82 ммоль) в метаноле (50 мл) и 10% Pd/C (500 мг) добавляют HCl в эфирном растворе (1,41 мл, 2 н.). Реакционную смесь перемешивают в атмосфере азота (45 фунт/кв. дюйм, 310,3 кПа) в аппарате Парра в течение 6 час. Полученный раствор фильтруют через целит и концентрируют в вакууме, получая продукт в виде зеленого твердого вещества.
МС (m/z) 307 (MH+)
1H-ЯМР (ДМСО-d6) δ 4,39-4,48 (м, 2Н), 6,09 (шир.с, 3Н), 6,97-7,05 (м, 3Н), 7,40 (т, J=7,1 Гц, 1Н), 7,60-7,71 (м, 2Н), 8,17 (д, J=8,0 Гц, 1Н), 9,68 (с, 1Н), 11,13 (с, 1Н).
Способ В: Свободное основание
1-(3,4-Метилендиоксифенилен)-2,3,4,9-тетрагидро-1Н-β-карболин, известное соединение (получено способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) (15,35 г, 52,5 ммоль), растворяют в безводном ДМФ (90 мл). Одной порцией вводят трет-бутоксид калия (10,02 г, 89,3 ммоль) и суспензию перемешивают до тех пор, пока не получат прозрачный раствор. Затем через раствор посредством иглы шприца в течение 50 мин пропускают газообразный кислород. Реакцию гасят добавлением ледяной уксусной кислоты (5,11 мл, 89,3 ммоль) и реакционную смесь выливают в диэтиловый эфир (1 л), что приводит к образованию осадка, который отфильтровывают. Продукт очищают флэш-хроматографией (0-50% EtOH/ТГФ), получая продукт в виде желтого порошка.
МС (m/z) 307 (МН+)
1H-ЯМР (CD3OD) δ 4,18 (д, J=13,7 Гц, 1Н), 4,36 (д, J=13,7 Гц, 1Н), 4,92 (шир.с, 2Н), 5,43 (с, 1Н), 5,92 (с, 1Н), 6,74 (с, 1Н), 6,81 (с, 1Н), 7,36-7,70 (сериям, 4Н), 8,31 (д, J=8,6 Гц, 1Н).
ПРИМЕР 5А
Гидрохлоридная соль (R)-1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (#48)
По методике, описанной в примере 5, способ А, (R)-1,2,3,4-тетрагидро-2-бензил-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 307 (МН+)
ПРИМЕР 6
Гидрохлоридная соль 1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-она
Способ А: соль HCl
Указанный в заголовке продукт получают по методике, описанной в примере 4, с заменой соответствующими реагентами.
МС (m/z) 305 (МН+)
1H-ЯМР (ДМСО-d6) δ 3,17-3,20 (м, 2Н), 4,38-4,60 (м, 4Н), 6,10 (с, 1H), 6,85 (д, J=8,2 Гц, 1H), 7,21 (д, J=8,1 Гц, 1Н), 7,30 (с, 1H), 7,40 (т, J=7,1 Гц, 1H), 7,61 (т, J=8,2 Гц, 1H), 7,68 (д, J=7,2 Гц, 1H), 8,17 (д, J=8,9 Гц, 1H), 9,71 (с, 1H), 11,17 (с, 1H).
Способ В: Свободное основание
1-(2,3-Дигидро-5-бензофуранил)-2,3,4,9-тетрагидро-1Н-β-карболин (1,06 г, 3,64 ммоль), известное соединение (получено способом, описанным в WO 97/43287, промежуточный продукт 10, страница 25), растворяют в безводном ДМФ (8 мл). Одной порцией вводят трет-бутоксид калия (829 мг, 7,38 ммоль) и суспензию перемешивают до тех пор, пока не получат прозрачный раствор. Затем через раствор посредством иглы шприца в течение 50 мин пропускают газообразный кислород. Реакцию гасят добавлением ледяной уксусной кислоты (0,42 мл, 7,34 ммоль) и выливают в диэтиловый эфир (50 мл), что приводит к образованию осадка, который отфильтровывают. Продукт очищают флэш-хроматографией (0-50% МеОН/ТГФ), получая продукт в виде желтого порошка.
МС (m/z) 305 (МН+)
1H-ЯМР (CD3OD) δ 3,17 (т, J=8,7 Гц, 2Н), 3,29-3,31 (м, 2Н), 4,18 (д, J=12,9 Гц, 1H), 4,38 (д, J=12,9 Гц, 1H), 4,53 (т, J=8,7 Гц, 2Н), 5,44 (с, 1H), 6,74 (д, J=8,2 Гц, 1H), 7,07 (д, J=8,2 Гц, 1H), 7,13 (с, 1H), 7,40 (т, J=7,9 Гц, 1H), 7,54 (д, J=8,3 Гц, 1H), 7,65 (т, J=7,9 Гц, 1H), 8,29 (д, J=8,1 Гц, 1H).
ПРИМЕР 6А
Гидрохлоридная соль (R)-1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-она
По методике, описанной в примере 6, способ А, (R)-1,2,3,4-тетрагидро-2-бензил-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он подвергают взаимодействию с получением указанного в заголовке соединения.
МС (m/z) 305 (МН+)
[α]=+39,0° (с=0,605, 1% ТФУ в СН3ОН)
ПРИМЕР 7
Эфир (4-пиридинил)метил-4-нитрофенилугольной кислоты
К раствору 4-пиридинилкарбинола (50 моль) и триэтиламина (50 ммоль) в безводном дихлорметане (100 мл) добавляют раствор 4-нитрофенилхлорформиата (50 ммоль). Реакционную смесь перемешивают в течение ночи при температуре окружающей среды, что приводит к образованию желтого осадка, который отфильтровывают, и смесь концентрируют. Полутвердый остаток обрабатывают ТГФ (50 мл) с образованием белого осадка. Осадок отфильтровывают, концентрируют и очищают флэш-хроматографией (20% ТГФ/CHCl3), получая продукт в виде оранжевого твердого вещества.
МС (m/z) 275 (МН+)
1H-ЯМР (CDCl3) δ 5,33 (с, 2Н), 7,36 (д, J=5,8 Гц, 2Н), 7,41 (д, J=9,4 Гц, 2Н), 8,30 (д, J=9,4 Гц, 2Н), 8,68 (д, J=5,8 Гц, 2Н).
ПРИМЕР 8
6-[2-(1-Морфолино)этокси]-2-бензофуранкарбоновая кислота
Раствор метилового эфира 6-метокси-2-бензофуранкарбоновой кислоты (868 мг, 4,52 ммоль) в безводном бензоле обрабатывают трифенилфосфином (1,18 г, 4,52 ммоль) и 1-(2-гидроксиэтил)морфолином (0,72 мл, 4,57 ммоль) в атмосфере аргона. К реакционной смеси при комнатной температуре добавляют по каплям DEAD (0,55 мл, 4,5 ммоль). Раствор перемешивают на протяжении ночи, концентрируют в вакууме и остаток очищают флэш-хроматографией (0-10% МеОН/CHCl3).
Очищенный продукт подвергают омылению в течение 3 час в смеси 1:1 метанола и водного 1 н. NaOH (80 мл) при температуре дефлегмации. Реакционную смесь нейтрализуют концентрированной HCl и концентрируют, получая остаток, который растирают с метанолом (20 мл). Полученную соль отфильтровывают и остаток концентрируют, получая второй остаток, который аналогично растирают с ТГФ. Третий остаток сушат в вакууме, получая продукт в виде желтого порошка.
МС (m/z) 292 (МН+)
1H-ЯМР (ДМСО-d6) δ 2,57 (шир.с, 4Н), 2,87 (т, J=5,3 Гц, 2Н), 3,64 (т, J=4,6 Гц, 4Н), 4,23 (т, J=5,5 Гц, 2Н), 6,97 (дд, J=8,7, 2 Гц, 1Н), 7,31 (с, 1Н), 7,53 (с, 1Н), 7,63 (д, J=8,7 Гц, 1Н).
ПРИМЕР 9
1-(3,4-Метилендиоксифенил)-2-(трет-бутоксикарбонил)-2,3,4,9-тетрагидро-1Н-β-карболин
К суспензии 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболина (27,7 г, 94,8 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) в безводном метаноле (300 мл) добавляют трет-бутилпирокарбонат (25,0 г, 114 ммоль). Вскоре после добавления пирокарбоната образуется прозрачный раствор. Раствор перемешивают при температуре окружающей среды в течение 1 часа, что приводит к образованию белого осадка. Твердое вещество отфильтровывают, промывают смесью 1:1 диэтиловый эфир:пентан и сушат в вакууме, получая продукт в виде белого твердого вещества.
МС (m/z) 415 (MNa+)
1H-ЯМР (CDCl3) δ 1,53 (с, 9Н), 2,75-3,17 (серия м, 3Н), 4,22 (шир., 1Н), 5,93 (с, 2Н), 6,31 (шир., 1Н), 6,64-6,72 (м, 2Н), 6,80 (с, 1Н), 7,12-7,33 (серия м, 3Н), 7,54 (д, J=7,7 Гц, 1Н), 7,93 (шир., 1Н).
ПРИМЕР 10
1-(3,4-Метилендиоксифенил)-2-(бензилоксикарбонил)-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1H-β-карболина (9,11 г, 31,1 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) в безводном дихлорметане (100 мл) добавляют триэтиламин (8,80 мл, 63,1 ммоль) и диметиламинопиридин (5 мг) с последующим добавлением по каплям бензилхлорформиата (4,60 мл, 30,6 ммоль) на протяжении 30 мин. Реакционную смесь перемешивают в течение 16 час, переносят в делительную воронку, промывают 2 н. HCl, насыщенным раствором соли, сушат над безводным сульфатом магния и концентрируют в вакууме. Флэш-хроматография дает продукт в виде белого твердого вещества.
MC (m/z) 425 (М-1)
1H-ЯМР (CDCl3) δ 2,78-2,95 (шир.м, 2Н), 3,15-3,25 (м, 1Н), 4,40 (шир., 1Н), 5,14 (д, J=12,3 Гц, 1Н), 5,22 (д, J=12,3 Гц, 1Н), 5,90 (с, 2Н), 6,35 (шир., 1Н), 6,80 (шир., 3Н), 7,09-7,35 (сериям, 8Н), 7,53 (д, J=7,6 Гц, 1Н), 7,70 (шир., 1Н).
ПРИМЕР 11
1-(3,4-Диметоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору триптамина (5,0 г, 0,0312 моль) и 3,4-диметоксибензальдегида (5,7 г, 0,0312 моль) в СН2Cl2 (220 мл) добавляют ТФУ (4,5 мл, 0,0548 моль). Темно-синий раствор перемешивают при комнатной температуре в течение 20 час. Реакционную смесь нейтрализуют NaHCO3 (4,9 г, 0,0584 моль) в Н2O (50 мл) и органический слой промывают насыщенным раствором соли (2×100 мл). Реакционную смесь сушат MgSO4 и растворитель выпаривают. Продукт выделяют колоночной хроматографией (силикагель; СН3ОН:EtOAc=1:9) в виде желтоватого масла, которое медленно отверждается при стоянии при комнатной температуре.
Т.пл.: 146-148°С; MC (m/z) 307 (М-1), 309 (МН+)
1H-ЯМР (CDCl3) δ 2,70˜2,92 (м, 2Н), 3,05 (м, 1Н), 3,31 (м, 1Н), 3,65 (с, 3Н), 3,81 (с, 3Н), 5,01 (с, 1Н), 6,72 (м, 2Н), 7,12 (м, 3Н), 7,52 (м, 1Н), 8,18 (с, 1Н).
ПРИМЕР 12
1-(3,4-Метилендиоксифенил)-2-[5-(4-метоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
1-(3,4-Метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (2,72 г, 9,6 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлор-5-(4-метоксифенил)пиримидин (1,04 г, 4,78 ммоль) перемешивают в ДМФ (20 мл, безводный) при 120°С в течение 16 час. Полученную смесь гасят насыщенным NH4Cl, экстрагируют этилацетатом и сушат MgSO4. Растворитель реакционной смеси выпаривают и остаток очищают колоночной хроматографией (силикагель, этилацетат:гексаны=1:2), получая продукт в виде белого твердого вещества.
Т.пл.: 200-202°С; МС (m/z): 477 (MH+)
1H-ЯМР (ДМСО-d6) δ 2,71 (м, 2Н), 3,25 (м, 1Н), 3,78 (с, 3Н), 4,93 (д, J=12 Гц, 1Н), 5,99 (д, J=5 Гц, 2Н), 6,76 (д, J=8 Гц, 1Н), 6,87 (д, J=8 Гц, 2Н), 7,02 (д, J=9 Гц, 2Н), 7,06 (д, J=7 Гц, 1Н), 7,11 (с, 1Н), 7,31 (д, J=8 Гц, 1Н), 7,46 (д, J=8 Гц, 1Н), 7,59 (д, J=9 Гц, 2Н), 8,74 (с, 2Н), 11,00 (с, 1Н).
ПРИМЕР 13
1-(3,4-Метилендиоксифенил)-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
По такой же методике, как указано в примере 12, 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (3,73 г, 12,8 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлор-5-(3,4-диметоксифенил)пиримидин (1,60 г, 6,4 ммоль) в ДМФ (50 мл, безводный) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
Т.пл.: 173-175°С; МС (m/z) 507 (МН+)
1H-ЯМР (CDCl3) δ 2,89 (д, J=15 Гц, 1Н), 3,02 (м, 1Н), 3,39 (м, 1Н), 3,92, 3,94 (2с, 6Н), 5,03 (д, J=12 Гц, 1Н), 5,92 (д, J=4 Гц, 2Н), 6,71 (д, J=7 Гц, 1Н), 6,87-7,32 (м, 6Н), 7,56 (д, J=7 Гц, 2Н), 7,80 (с, 1Н), 8,56 (с, 2Н).
ПРИМЕР 14
1-(3,4-Метилендиоксифенил)-2-[5-(4-метилфенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
По такой же методике, как указано в примере 12, 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (2,19 г, 7,5 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлор-5-(4-метилфенил)пиримидин (1,03 г, 5 ммоль) в толуоле (50 мл, безводный) и DBU (0,9 мл) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
МС (m/z) 459 (МН+)
1H-ЯМР (CDCl3) δ 2,43 (с, 3Н), 2,85 (д, J=14 Гц, 1Н), 3,01 (т, J=12 Гц, 1Н), 3,38 (т, J=12 Гц, 1Н), 5,04 (дд, J=14 Гц, 1Н), 5,88 (д, J=4 Гц, 2Н), 6,73 (д, J=7 Гц, 1Н), 6,89 (д, J=7 Гц, 1Н), 7,02 (с, 1Н), 7,25-7,50 (м, 7Н), 7,56 (д, J=7 Гц, 1Н), 7,79 (с, 1H), 8,54 (с, 2Н).
ПРИМЕР 15
1-(3,4-Метилендиоксифенил)-2-(пиридин-4-ил)метил-2,3,4,9-тетрагидро-1Н-β-карболин
Раствор 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболина (2,92 г, 10 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24), гидрохлорида 4-пиколилхлорида (1,64 г, 10 ммоль) и DBU (3,1 г, 20 ммоль) в ДМФ (50 мл) перемешивают при комнатной температуре в течение 16 час. К реакционной смеси добавляют воду (100 мл) и этилацетат (100 мл). Растворенное вещество, присутствующее в органической фазе, очищают колоночной хроматографией (силикагель, этилацетат), получая продукт в виде не совсем белого твердого вещества.
МС (m/z) 382 (М-1)
1H-ЯМР (CDCl3) δ 2,65 (м, 1Н), 2,75 (д, 1Н), 2,88 (м, 1Н), 3,15 (м, 1Н), 3,35 (д, J=15 Гц, 1Н), 3,92 (д, J=15 Гц, 1Н), 4,57 (с, 1Н), 5,94 (с, 1Н), 6,79 (д, J=8 Гц, 1Н), 6,89 (м, 2Н), 7,20-7,40 (м, 7Н), 7,51 (д, J=6 Гц, 1Н), 8,53 (д, J=7 Гц, 1Н).
ПРИМЕР 16
1-(3,4-Метилендиоксифенил)-2-(пиримидин-2-ил)-2,3,4,9-тетрагидро-1Н-β-карболин
1-(3,4-Метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (2,3 г, 8,0 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлорпиримидин (0,914 г, 8,0 ммоль) перемешивают в безводном ДМФ (15 мл) при 140°С в течение 24 час. Реакционную смесь разбавляют этилацетатом (100 мл) и промывают насыщенным водным раствором NH4Cl (100 мл). Водный слой экстрагируют этилацетатом (2×50 мл). Объединенные органические слои промывают насыщенным раствором соли (2×80 мл) и сушат MgSO4. Растворители выпаривают и продукт выделяют колоночной хроматографией (силикагель, EtOAc:гексан=1:9) в виде желтоватого твердого вещества.
Т.пл. 176-177°С;
МС (m/z): 371 (МН+), 369 (М-1); Анал. вычислено для C22H18N4O2, С 71,34, Н 4,90, N 15,13; найдено С 70,57, Н 4,92, N 15,38
1H-ЯМР (CDCl3) δ 2,71 (м, 1Н), 2,92 (м, 1Н), 3,29 (м, 1Н), 4,92 (дд, 1H, J=14,7 Гц), 5,91 (д, 2Н, J=6 Гц), 6,43 (т, 1Н, J=6 Гц), 6,63 (д, 1H, J=10 Гц), 6,81 (д, 1H, J=10 Гц), 6,95 (с, 1H), 7,08 (м, 3Н), 7,21 (д, 1H, J=8 Гц), 7,54 (д, 1H, J=10 Гц), 8,12 (с, 1H), 8,30 (д, 2Н, J=6 Гц).
ПРИМЕР 17
1-(3,4-Метилендиоксифенил)-2-[5-(4-хлорфенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
По такой же методике, как указано выше в примере 12, 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (295 мг, 1 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 1, страница 24) и 2-хлор-5-(4-хлорфенил)пиримидин (113 мг, 0,5 ммоль) в ДМФ (5 мл, безводный) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
МС (m/z) 479 (МН+)
1H-ЯМР (CDCl3) δ 2,87 (дд, J=4,14 Гц, 1Н), 3,01 (дт, J=5,12 Гц, 1Н), 3,38 (дт, J=4,14 Гц, 1Н), 5,04 (дд, J=5,14 Гц, 1Н), 5,91 (д, J=4 Гц, 2Н), 6,73 (д, J=7 Гц, 1Н), 6,89 (д, J=7 Гц, 1Н), 7,00 (с, 1Н), 7,20 (с, 1Н), 7,25 (м, 2Н), 7,30 (д, J=7 Гц, 1Н), 7,40 (м, 4Н), 7,56 (д, J=7 Гц, 1Н), 7,83 (с, 1Н), 8,54 (с, 2Н).
ПРИМЕР 18
[5-(3,4-Диметоксифенил)пиримидин-2-ил]-1-(3,4-диметоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин
По такой же методике, как указано в примере 16, 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлор-5-(3,5-диметоксифенил)пиримидин подвергают взаимодействию, получая продукт в виде белого твердого вещества.
Т.пл. 184-186°С;
МС (m/z) 523 (МН+), 521 (М-1)
1H-ЯМР (CDCl3) δ 2,81˜3,20 (м, 2Н), 3,40 (м, 1Н), 3,71 (с, 3Н), 3,79 (с, 3Н), 3,88 (с, 3Н), 3,91 (с, 3Н), 5,01 (дд, 1Н, J=14 Гц, 5 Гц), 6,68 (д, 1Н, J=8 Гц), 6,70˜7,19 (м, 7Н), 7,28 (т, 1H, J=8 Гц), 7,52 (т, 1Н, J=8 Гц), 8,20 (с, 1Н), 8,52 (с, 2Н).
ПРИМЕР 19
1,2,3,4-Тетрагидро-3-(3,4-диметоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#12)
1-(3,4-Диметоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (1,854 г, 6,04 ммоль) (получен, как в примере 11) и КО-трет-Bu (1,14 г, 10,15 ммоль) перемешивают в ДМФ (60 мл) при комнатной температуре в течение 10 мин. Через раствор в течение 1 часа барботируют кислород. Реакционную смесь нейтрализуют 1 н. раствором HCl (10,15 мл, 10,15 ммоль) и воду удаляют в вакууме в виде азеотропа с толуолом. К оставшемуся раствору в ДМФ добавляют силикагель (˜5 г), затем добавляют диэтиловый эфир (600 мл), что приводит к осаждению продукта на силикагеле. Диэтиловый эфир декантируют и силикагель промывают диэтиловым эфиром (2×100 мл). После декантации растворителя и выпаривания любых оставшихся следовых количеств растворителя остаток очищают колоночной хроматографией (силикагель; EtOH:EtOAc=1:9), получая продукт в виде ярко-желтого твердого вещества. Продукт перекристаллизовывают из метанола.
Т.пл. 223-225°С;
МС (m/z): 323 (МН+), 321 (М-1)
1H-ЯМР (CD3OD) δ 3,71 (с, 3Н), 3,88 (с, 3Н), 4,18 (д, 1Н, J=14 Гц), 4,38 (д, 1Н, J=14 Гц), 5,41 (с, 1Н), 6,83 (м, 3Н), 7,39 (т, 1Н, J=7 Гц), 7,58 (м, 2Н), 8,22 (д, 1Н, J=6 Гц), 11,85 (с, 1Н).
ПРИМЕР 20
1,2,3,4-Тетрагидро-2-[5-(4-метоксифенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#2)
Гидрид натрия (60% в минеральном масле, 36 мг, 0,9 ммоль) и 1-(3,4-метилендиоксифенил)-2-[5-(4-метоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин (186 мг, 0,39 ммоль) (получен, как в примере 12) в ДМФ (10 мл, безводный) перемешивают при комнатной температуре в течение 30 мин. Через раствор в течение 16 час барботируют сухой воздух. Добавляют этилацетат (100 мл) и насыщенный NaHCO3, органическую фазу промывают водой, насыщенным раствором соли и сушат MgSO4. Растворитель выпаривают и остаток растирают с этилацетатом, получая продукт в виде белого твердого вещества.
Т.пл.: 325-327°С.
МС (m/z) 491 (МН+); 489 (М-1)
1H-ЯМР (ДМСО-d6) δ 3,77 (с, 3Н), 4,86 (д, J=12 Гц, 1Н), 4,96 (дд, J=15 Гц, 1Н), 5,98 (с, 2Н), 6,29 (д, J=2,5 Гц, 1Н), 6,87 (д, J=8 Гц, 1Н), 6,95 (д, J=9 Гц, 2Н), 6,98 (с, 1Н), 7,02 (д, J=4 Гц, 3Н), 7,34 (т, J=7 Гц, 1Н), 7,57 (д, J=9 Гц, 2Н), 7,63 (дд, J=8 Гц, 3Н), 8,16 (д, J=8 Гц, 1Н), 8,69 (шир.с, 2Н), 11,85 (с, 1Н).
ПРИМЕР 21
1,2,3,4-Тетрагидро-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#1)
Гидрид натрия (60% в минеральном масле, 40 мг, 1,0 ммоль) и 1-(3,4-метилендиоксифенил)-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин (218 мг, 0,43 ммоль) (получен, как в примере 13) в ДМФ (10 мл, безводный) перемешивают при комнатной температуре в течение 30 мин. Через раствор в течение 16 час барботируют сухой воздух. Добавляют этилацетат (100 мл) и насыщенный NaHCO3, органическую фазу промывают водой, насыщенным раствором соли и сушат MgSO4. Растворитель выпаривают и остаток очищают хроматографией (силикагель, этилацетат), получая продукт в виде белого твердого вещества.
МС (m/z) 521 (МН+); 519 (М-1)
1H-ЯМР (ДМСО-d6) δ 3,77 (с, 3Н), 3,83 (с, 3Н), 4,86 (д, J=12 Гц, 1Н), 4,96 (дд, J=15 Гц, 1Н), 5,99 (с, 2Н), 6,31 (д, J=2,5 Гц, 1Н), 6,87 (д, J=8 Гц, 1Н), 6,95 (д, J=9 Гц, 2Н), 6,98 (с, 1Н), 7,02 (м, 1Н), 7,17 (д, J=7 Гц, 1Н), 7,22 (с, 1Н), 7,35 (т, J=7 Гц, 1Н), 7,62 (м, 2Н), 8,17 (д, J=8 Гц, 1Н), 8,74 (шир.с, 2Н), 11,85 (с, 1Н).
ПРИМЕР 21А
(S)-1,2,3,4-Тетрагидро-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#35)
По методике, описанной в примере 21, (S)-1-(3,4-метилендиоксифенил)-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию, получая указанное в заголовке соединение.
ПРИМЕР 21В
(R)-1,2,3,4-Тетрагидро-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#36)
По методике, описанной в примере 21, (R)-1-(3,4-метилендиоксифенил)-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин подвергают взаимодействию, получая указанное в заголовке соединение.
ПРИМЕР 22
1,2,3,4-Тетрагидро-2-[5-(4-метилфенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (# 7)
По такой же методике, как указано в примере 21, гидрид натрия (60% в минеральном масле, 43 мг, 1,09 ммоль) и 1-(3,4-метилендиоксифенил)-2-[5-(4-метилфенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин (278 мг, 0,60 ммоль) (получен, как в примере 12) в ДМФ (15 мл, безводный) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
МС (m/z) 475 (МН+)
1H-ЯМР (ДМСО-d6) δ 2,32 (с, 3Н), 4,86 (д, J=12 Гц, 1Н), 4,96 (дд, J=15 Гц, 1Н), 5,98 (с, 2Н), 6,30 (д, J=2,5 Гц, 1Н), 6,87 (д, J=8 Гц, 1Н), 6,95 (д, J=9 Гц, 2Н), 7,02 (д, J=4 Гц, 3Н), 7,24 (д, J=7 Гц, 2Н), 7,34 (т, J=7 Гц, 1Н), 7,40-7,65 (м, 3Н), 8,16 (д, J=8 Гц, 1Н), 8,69 (шир.с, 2Н), 11,85 (с, 1Н).
ПРИМЕР 23
1,2,3,4-Тетрагидро-[5-(3,4-диметоксифенил)пиримидин-2-ил]-3-(3,4-диметоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#15)
По такой же методике, как указано в примере 19, [5-(3,4-диметоксифенил)пиримидин-2-ил]-1-(3,4-диметоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (получен, как в примере 18) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
МС (m/z) 535 (МН+), 537 (МН-)
1H-ЯМР (CD3OD) δ 3,74 (с, 3Н), 3,79 (с, 3Н), 3,80 (с, 3Н), 3,85 (с, 3Н), 5,0 (м, 2Н), 6,31 (с, 1Н), 6,75˜7,15 (м, 5Н), 7,36 (т, 1Н, J=8 Гц), 7,32 (д, 1Н, J=8 Гц), 7,61 (м, 2Н), 8,29 (д, 1Н, J=8 Гц), 8,58 (с, 2Н).
ПРИМЕР 24
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(пиридин-4-ил)метил-9Н-пирроло[3,4-b]хинолин-9-он (#5)
По такой же методике, как указано в примере 21, гидрид натрия (60% в минеральном масле, 40 мг, 1,0 ммоль) и 1-(3,4-метилендиоксифенил)-2-(пиридин-4-ил)метил-2,3,4,9-тетрагидро-1H-β-карболин (192 мг, 0,50 ммоль) (получен, как в примере 15) в ДМФ (10 мл, безводный) подвергают взаимодействию, получая продукт в виде белого твердого вещества.
МС (m/z) 398 (МН+)
1H-ЯМР (ДМСО-d6) δ 3,58 (д, J=14 Гц, 1Н), 3,76 (д, J=15 Гц, 1Н), 3,88 (д, J=15 Гц, 1Н), 4,01 (д, J=14 Гц, 1Н), 5,17 (с, 1H), 6,03 (с, 1H), 6,97 (с, 3Н), 7,35 (м, 3Н), 7,60 (м, 2Н), 7,34 (т, J=7 Гц, 1H), 8,11 (д, J=8 Гц, 1H), 8,53 (д, J=6 Гц, 2Н), 11,45 (с, 1H).
ПРИМЕР 25
1,2,3,4-Тетрагидро-2-(трет-бутоксикарбонил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#3)
2-трет-Бутоксикарбонил-1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (4,09 г, 10,4 ммоль) (получен, как в примере 9) растворяют в безводном ДМФ (100 мл). Одной порцией вводят трет-бутоксид калия (2,55 г, 22,7 ммоль) и суспензию перемешивают до тех пор, пока не получат прозрачный раствор. Затем через раствор пропускают газообразный кислород через иглу шприца в течение 16 час. Реакционную смесь гасят добавлением ледяной уксусной кислоты (25 ммоль) и выливают в смесь диэтилового эфира и воды, что приводит к образованию осадка, который отфильтровывают. Продукт очищают флэш-хроматографией (0-10% МеОН/CHCl3), получая продукт в виде белого твердого вещества.
МС (m/z) 405 (М-1)
1H-ЯМР (CDCl3) δ 1,38-1,65 (серия с, 9Н), 4,79-4,88 (м, 2Н), 5,86-6,27 (серия м, 3Н), 6,71-7,50 (серия м, 7Н), 11,57 и 11,64 (с, 1H).
ПРИМЕР 26
1,2,3,4-Тетрагидро-2-(бензилоксикарбонил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#27)
2-Бензилоксикарбонил-1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболин (3,63 г, 8,51 ммоль) (получен, как в примере 10) растворяют в безводном ДМФ (25 мл). Одной порцией вводят трет-бутоксид калия (2,40 г, 21,4 ммоль) и суспензию перемешивают до тех пор, пока не получат прозрачный раствор. Затем через раствор пропускают газообразный кислород через иглу шприца в течение 16 час. Реакционную смесь гасят добавлением ледяной уксусной кислоты (1,23 мл, 21,0 ммоль) и выливают в воду (250 мл), что приводит к образованию осадка, который отфильтровывают. Продукт очищают флэш-хроматографией (2-10% МеОН/CHCl3), получая продукт в виде красного порошка.
МС (m/z) 439 (М-1)
1H-ЯМР (CDCl3) δ 4,63-5,18 (серия м, 4Н), 5,71-5,85 (серия м, 3Н), 6,54-6,72 (серия м, 3Н), 6,98-7,01 (м, 1Н), 7,25-7,57 (серия м, 7Н), 8,27-8,32 (м, 1Н), 10,04 и 10,33 (с, 1Н).
ПРИМЕР 27
Метиловый эфир (Е)-4-[3-оксо-3-[1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (#20)
А. Раствор (Е)-4-карбометоксикоричной кислоты (5,09 г, 24,7 ммоль) растворяют в безводном ТГФ (25 мл) и обрабатывают в атмосфере аргона оксалилхлоридом (3,00 мл, 34,4 ммоль) и каплей безводного ДМФ. После нагревания при 50°С в течение 2 часов реакционную смесь концентрируют в вакууме, получая хлорангидрид (Е)-карбоксиметилкоричной кислоты в виде рыжевато-коричневого твердого вещества.
В. Продукт части А (78 мг, 0,35 ммоль) добавляют к раствору 1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-она (93,5 мг, 0,31 ммоль) (получен, как в примере 6), ТГФ (3 мл), триэтиламина (0,20 мл, 1,43 ммоль) и DMAP (5 мг). Смесь перемешивают в течение 16 час при комнатной температуре, разбавляют 1 н. HCl (10 мл) и образовавшийся белый осадок отфильтровывают. Твердое вещество промывают водой (3×), диэтиловым эфиром (3×) и сушат в вакууме, получая продукт в виде слабо-розового твердого вещества.
МС (m/z): 493 (МН+)
1H-ЯМР (ДМСО-d6) δ 3,10-3 (м, 2Н), 3,87 (с, 3Н), 4,43-4,52 (м, 2Н), 4,70-5,14 (серия м, 2Н), 6,23 и 6,61 (с, 1Н), 6,72-6,79 (м, 1Н), 7,07-8,19 (серия м, 12Н), 10,69 и 10,77 (с, 1Н).
ПРИМЕР 28
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)2-[5-(3-трифторметилфенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#13)
К раствору 5-(3-трифторметилфенил)-2-фуранкарбоновой кислоты (80,44 мг, 0,314 ммоль) в смеси 1:1 DCM:ТГФ (5 мл, безводная) добавляют оксалилхлорид (43,85 мг, 0,345 ммоль), затем две капли ДМФ. Смесь перемешивают при комнатной температуре в течение 1 часа. Добавляют суспензию 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (96,2 мг, 0,314 ммоль) (получен, как в примере 5), триэтиламин (0,13 мл) и DMAP (следы) в смеси 1:1 DCM/ТГФ (5 мл). Полученную смесь перемешивают при комнатной температуре в течение 16 час. Добавляют этилацетат (50 мл) и раствор промывают водным NaHCO3, насыщенным раствором соли, 1 н. HCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель выпаривают и остаток растирают с этилацетатом, получая продукт в виде белого твердого вещества.
Т.пл.: 219-221°С
МС (m/z): 545 (МН+), 567 (М+23), 543 (МН-)
1H-ЯМР (ДМСО-d6) δ 5,09 (д, J=14 Гц, 1H), 5,46 (д, J=14 Гц, 1H), 5,99 (с, 2Н), 6,39 (с, 1Н), 6,91 (д, J=8 Гц, 1Н), 6,97 (д, J=8 Гц, 1H), 7,02 (с, 1H), 7,33 (д, J=8 Гц, 1H), 7,38 (д, J=4 Гц, 1H), 7,43 (д, J=4 Гц, 1H), 7,60 (м, J=8 Гц, 2Н), 7,77 (д, J=5 Гц, 2Н), 8,16 (д, J=4 Гц, 3Н), 11,55 (с, 1H).
ПРИМЕР 29
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)2-(6-гидрокси-2-бензофуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#9)
К раствору 6-гидрокси-2-бензофурановой кислоты (0,054 г, 0,3 ммоль) в тетрагидрофуране (5 мл) при 0°С добавляют по каплям оксалилхлорид (0,046 г, 0,36 ммоль), затем ДМФ (2 капли). Раствор нагревают до 25°С и перемешивают в течение 30 мин, затем концентрируют в вакууме. Остаток растворяют в тетрагидрофуране (5 мл) и добавляют к раствору 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (0,092 г, 0,3 ммоль) (получен, как в примере 5) в ТГФ (5 мл), триэтиламине (0,045 г, 0,45 ммоль) и 4-диметиламинопиридине (0,01 г, катал.). Раствор перемешивают в течение 20 час при 25°С и затем концентрируют в вакууме. Полученный неочищенный остаток очищают колоночной хроматографией на силикагеле с элюированием 3% метанолом в дихлорметане, получая продукт в виде прозрачного масла.
1H-ЯМР (CD3OD) δ 5,25 (д, J=15 Гц, 1Н), 5,48 (д, J=15 Гц, 1Н), 5,91 (с, 2Н), 6,45 (шир.с, 1Н), 6,84 (м, 3Н), 6,93 (м, 2Н), 7,00 (с, 1Н), 7,25-7,89 (нечеткие м, 5Н), 8,32 (д, 1Н).
ПРИМЕР 30
Метиловый эфир (Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (#6)
По методике, указанной в примере 20, 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (398 мг, 1,30 ммоль) (получен, как в примере 5) подвергают взаимодействию с хлорангидридом (Е)-карбоксиметилкоричной кислоты (301 мг, 1,34 ммоль) в присутствии триэтиламина (0,54 мл, 3,87 ммоль) в смеси 1:1 дихлорметан:ТГФ (40 мл), получая продукт в виде рыжевато-коричневого твердого вещества.
МС (m/z) 493 (М-1)
1H-ЯМР (CD3OD) δ 3,86 (с, 3Н), 4,69-5,29 (серия м, 2Н), 5,93-6,02 (м, 2Н), 6,27 и 6,62 (с, 1Н), 6,89-8,21 (серия м, 13Н), 9,50 и 11,96 (шир.с, 1Н).
ПРИМЕР 31
1,2,3,4-Тетрагидро-2-(имидазол-1-ил)тиокарбонил-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#18)
К суспензии 1,1'-тиокарбонилдиимидазола (0,192 г, 1,08 ммоль) в ДМФ (5 мл, безводный) при 0°С добавляют 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (0,30 г, 0,98 ммоль) (получен, как в примере 5). Смесь нагревают до комнатной температуры и перемешивают в течение 20 час. Раствор разбавляют водой и экстрагируют в этилацетат. Органические слои объединяют и промывают водным NaHCO3 и насыщенным раствором соли, сушат MgSO4 и концентрируют в вакууме, получая продукт в виде светлого рыжевато-коричневого твердого вещества.
Т.пл.: 211-215°С (разл.)
МС (m/z) 415 (М-1)
1H-ЯМР (CD3OD) δ 4,71˜5,16 (м, 1Н), 5,46 (д, J=15 Гц, 1Н), 6,36-7,17 (нечеткие м, 5Н), 7,42 (м, 2Н), 7,52 (м, 1Н), 7,58 (м, 2Н), 8,28 (м, 1Н).
ПРИМЕР 32
(Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойная кислота (#8)
Метиловый эфир (Е)-4-[3-оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (149 мг, 0,30 ммоль) (получен, как в примере 30) суспендируют в смеси 1:1 1 н. водный гидроксид натрия:метанол (10 мл) и кипятят с обратным холодильником в течение 8 час. Реакционную смесь обрабатывают водной HCl до рН 1, что приводит к образованию белого осадка. Осадок отфильтровывают и промывают водой (30 мл) и диэтиловым эфиром (160 мл), получая продукт в виде белого твердого вещества.
MC (m/z) 481 (МН+)
1H-ЯМР (ДМСО-d6) δ 4,71-5,13 (серия д, 2Н), 5,95-5,98 (м, 2Н), 6,23 и 6,61 (с, 1Н), 6,84-7,78 (серия м, 10Н), 7,89-7,92 (м, 3Н), 8,13-8,17 (м, 1Н), 11,94 (шир.с, 1Н).
ПРИМЕР 33
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-нитрофенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#16)
1,2,3,4-Тетрагидро-3-(З,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (70,3 мг, 0,229 ммоль) (получен, как в примере 5), 5-(4-нитрофенил)-2-фуранкарбоновую кислоту (58,9 мг, 0,25 ммоль) и PyBrOP (0,118 г, 0,25 ммоль) перемешивают в ДМФ (3 мл) и DIPEA (0,088 мл, 0,50 ммоль) в течение 16 час. Реакционную смесь выливают в этилацетат (80 мл) и полученный органический слой промывают 1 н. водной HCl (3×50 мл), насыщенным водным раствором Na2CO3 (1×50 мл) и насыщенным раствором соли (1×50 мл). Органический слой сушат MgSO4 и растворитель выпаривают в вакууме. Колоночная хроматография остатка (силикагель, 5% СН3ОН/СН3Cl) дает продукт в виде желтого порошка.
MC (m/z): 522 (МН+), 520 (М-1)
1H-ЯМР (ДМСО-d6) δ 5,05 (д, 1Н, J=14 Гц), 5,45 (д, 1Н, J=14 Гц), 6,0 (с, 2Н), 6,42 (с, 1Н), 6,95 (м, 3Н), 7,32˜7,41 (м, 2Н), 7,55˜7,65 (м, 3Н), 8,12 (м, 3Н), 8,39 (м, 2Н), 11,91 (с, 1Н).
ПРИМЕР 34
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-аминофенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#26)
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[(5-(4-нитрофенил))фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (25 мг, 0,0479 ммоль) (получен, как в примере 33) перемешивают с 10% Pd на угле (5,1 мг, 0,00479 ммоль) при 1 атм Н2 и комнатной температуре в течение 14 час. Растворитель выпаривают и продукт выделяют препаративной ТСХ в виде желтого порошка.
МС (m/z): 492 (МН+); 490 (М-1)
1H-ЯМР (CD3OD) δ 5,25 (д, 1Н, J=14 Гц), 5,45 (д, 1Н, J=14 Гц), 5,91 (с, 2Н), 6,45 (с, 1Н), 6,70˜8,60 (м, 13Н).
ПРИМЕР 35
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[2-гидроксиникотиноил]-9Н-пирроло[3,4-b]хинолин-9-он (#25)
По методике, указанной в примере 33, с соответствующей заменой реагентов получают продукт в виде бледно-желтого твердого вещества.
МС (m/z): 428 (МН+); 426 (М-1)
1H-ЯМР (CD3OD) δ 4,65 (д, J=14 Гц), 5,10 (д, 1Н, J=14 Гц), 5,85 (с, 2Н), 5,92 (с, 1Н), 6,50˜7,10 (м, 3Н), 7,30˜7,70 (м, 5Н), 8,25 (м, 2Н).
ПРИМЕР 36
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-метоксифенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#21)
По методике, указанной в примере 33, с соответствующей заменой реагентов получают продукт в виде бледно-желтого твердого вещества.
МС (m/z) 507 (МН+); 505 (М-1)
1H-ЯМР (CDCl3) δ 3,85 (с, 3Н), 5,10 (д, 1Н, J=14 Гц), 5,38 (д, 1Н, J=14 Гц), 6,02 (с, 2Н), 6,41 (с, 1Н), 6,80˜8,35 (м, 13Н), 11,80 (с, 1Н).
ПРИМЕР 37
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-гидроксифенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#22)
По методике, указанной в примере 33, с соответствующей заменой реагентов получают продукт в виде бледно-желтого твердого вещества.
МС (m/z) 493 (МН+); 491 (М-1)
1H-ЯМР (ДМСО-d6) δ 5,05 (д, 1Н, J=14 Гц), 5,15 (д, 1Н, J=14 Гц), 5,75 (с, 2Н), 6,31 (с, 1Н), 6,80˜8,35 (м, 13Н), 11,60 (с, 1Н).
ПРИМЕР 38
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-метоксикарбонилфенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#24)
По методике, указанной в примере 33, с соответствующей заменой реагентов получают продукт в виде бледно-желтого твердого вещества.
1H-ЯМР (ДМСО-d6) δ 4,10 (с, 3Н), 5,10 (д, 1Н, J=14 Гц), 5,50 (д, 1Н, J=14 Гц), 6,02 (с, 2Н), 6,45 (с, 1Н), 6,80˜8,35 (м, 13Н).
ПРИМЕР 39
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(4-формилфенил)фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#23)
По методике, указанной в примере 33, с соответствующей заменой реагентов получают продукт в виде бледно-желтого твердого вещества.
МС (m/z) 503 (М-1)
1H-ЯМР (ДМСО-d6) δ 5,10 (д, 1Н, J=14 Гц), 5,55 (д, 1Н, J=14 Гц), 6,02 (с, 2Н), 6,45 (с, 1Н), 6,80˜8,35 (м, 13Н).
ПРИМЕР 40
Метиловый эфир (Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-4-метил-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (#63) и метиловый эфир (Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9-метокси-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (#64)
Раствор метилового эфира (Е)-4-[3-оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты (349 мг, 0,62 ммоль) (получен, как в примере 30) и иодметана (0,060 мл, 0,96 ммоль) в безводном ацетоне (10 мл) обрабатывают безводным карбонатом калия (241 мг, 1,74 ммоль) и кипятят с обратным холодильником в течение 3 час в атмосфере аргона. Реакционную смесь концентрируют в вакууме и остаток очищают флэш-хроматографией (0-10% метанола в дихлорметане), получая смесь N- и O-метилированных продуктов.
Смесь N- и O-метилированных продуктов разделяют колоночной хроматографией (0-10% MeOH/DCM), получая N-метилированный продукт, метиловый эфир (Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-4-метил-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты, в виде рыжевато-коричневого твердого вещества.
МС (m/z): 509 (М-1)
1H-ЯМР (CDCl3) δ 3,55 (с, 3Н), 3,93 (с, 3Н), 5,10 (м, 2Н), 5,94 (нд, J=3,7 Гц, 2Н), 6,53 (с, 1Н), 6,78 (д, J=7,9 Гц, 1Н), 6,86-6,96 (м, 3Н), 7,44-7,76 (серия м, 6Н), 8,05 (д, J=8,2 Гц, 2Н), 8,55 (д, J=7,4 Гц) и O-метилированный продукт, метиловый эфир (Е)-4-[3-Оксо-3-[1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9-метокси-9Н-пирроло[3,4-b]хинолин-9-он-2-ил]-1-пропенил]бензойной кислоты, в виде розового твердого вещества.
МС (m/z): 509 (М-1)
1H-ЯМР (CDCl3) δ 3,93 (с, 3Н), 4,38 (с, 3Н), 5,45 (д, J=17,1 Гц, 1Н), 5,64 (д, J=17,1 Гц, 1Н), 5,91 (с, 2Н), 6,26 (с, 1Н), 6,75-7,09 (серия д, 4Н), 7,39-8,23 (серия м, 9Н).
ПРИМЕР 41
1,2,3,4-Тетрагидро-2-(пиримидин-2-ил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#11)
К раствору 1-(3,4-метилендиоксифенил)-2-(пиримидин-2-ил)-2, 3, 4, 9-тетрагидро-1Н-β-карболина (0,153 г, 0,415 ммоль) (получен, как в примере 16) в безводном ДМФ (4,1 мл) добавляют КО-трет-Bu (0,079 г, 0,70 ммоль, 1,7 экв.). Спустя 5 мин через раствор в течение 1 часа барботируют газообразный кислород. К реакционной смеси добавляют диэтиловый эфир (45 мл) и супернатант декантируют. К остатку добавляют насыщенный раствор соли (2 мл) и рН доводят приблизительно до 7 добавлением нескольких капель 1 н. HCl. Воду удаляют в вакууме в виде азеотропа с толуолом. Полученный темно-красный остаток растворяют в минимальном количестве ТГФ и очищают колоночной хроматографией (силикагель; EtOH:CH2Cl2=l:9), получая продукт в виде белого твердого вещества.
МС (m/z): 383 (М-1); 385 (МН+)
1H-ЯМР (ДМСО-d6) δ 4,84 (дд, 2Н, J=14 Гц, 10 Гц), 5,98 (с, 2Н), 6,25 (с, 1Н), 6,69 (т, 1Н, J=5 Гц), 6,85 (д, 1Н, J=8 Гц), 6,92 (д, 1Н, J=8 Гц), 7,00 (с, 1Н), 7,33 (т, 1Н, J=7 Гц), 7,60 (м, 2Н), 8,15 (д, 1Н, J=8 Гц), 8,41 (шир.с, 2Н), 11,9 (с, 1Н).
ПРИМЕР 42
1,2,3,4-Тетрагидро-2-(пиримидин-2-ил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#11)
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (100 мг, 0,3265 ммоль) (получен, как в примере 5) и 2-хлорпиримидин (38 мг, 0,3265 ммоль) перемешивают в ДМФ (2,5 мл) при 100°С в течение 16 час. Растворитель удаляют в вакууме и остаток очищают колоночной хроматографией (силикагель, 5% СН3ОН/СН3Cl), получая желтое масло. Растирание масла с МеОН дает продукт в виде светло-желтого твердого вещества.
МС (m/z) 383 (М-1); 385 (МН+)
1H-ЯМР (ДМСО-d6) δ 4,84 (дд, 2Н, J=14 Гц, 10 Гц), 5,98 (с, 2Н), 6,25 (с, 1Н), 6,69 (т, 1Н, J=5 Гц), 6,85 (д, 1Н, J=8 Гц), 6,92 (д, 1Н, J=8 Гц), 7,00 (с, 1Н), 7,33 (т, 1Н, J=7 Гц), 7,60 (м, 2Н), 8,15 (д, 1Н, J=8 Гц), 8,41 (шир.с, 2Н), 11,9 (с, 1Н).
ПРИМЕР 43
Гидрохлоридная соль 1,2,3,4-тетрагидро-2-[(4-пиридинил)метилоксикарбонил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (#37)
Смесь гидрохлоридной соли 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (101 мг, 0,33 ммоль) (получен, как в примере 5), эфира (4-пиридинил)метил-4-нитрофенилугольной кислоты (106 мг, 0,38 ммоль) (получен, как в примере 7) и триэтиламина (2 экв.) кипятят с обратным холодильником в течение 1 часа. Реакционную смесь концентрируют в вакууме и очищают флэш-хроматографией (0-10% МеОН/CHCl3). Соответствующую соль получают осаждением из раствора свободного основания в метаноле раствором HCl-эфир.
МС (m/z) 442 (МН+)
1H-ЯМР (CD3OD) δ 5,02-5,62 (серия м, 4Н), 5,93-6,00 (м, 2Н), 6,23 и 6,44 (с, 1Н), 6,82-7,04 (м, 3Н), 7,71-7,90 (м, 4Н), 8,12 (д, J=6,2 Гц, 1Н), 8,44 (с, 1Н), 8,78 (с, 1Н), 8,84 (с, 1Н).
ПРИМЕР 44
1,2,3,4-Тетрагидро-2-[(4-пиридинил)метилоксикарбонил]-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он (#53)
По методике, указанной в примере 36, гидрохлоридную соль 1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-она (получена, как в примере 6) и эфира (4-пиридинил)метил-4-нитрофенилугольной кислоты (получен, как в примере 7) подвергают взаимодействию, получая продукт в виде светло-розового твердого вещества.
МС (m/z) 440 (МН+)
1H-ЯМР (ДМСО-d6) δ 2,82-2,94 (м, 2Н), 4,35-5,26 (серия м, 6Н), 5,91 (с, 1Н) 6,45-7,58 (серия м, 9Н), 8,30-8,46 (м, 2Н), 12,26 (шир., 1Н).
ПРИМЕР 45
Гидрохлоридная соль 1,2,3,4-тетрагидро-2-[[5-[2-(4-морфолинил)этокси]-2-бензофурил]карбонил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (#49)
Гидрохлоридную соль 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (222 мг, 0,65 ммоль) (получена, как в примере 5) и 6-[2-(1-морфолино)этокси]-2-бензофуранкарбоновую кислоту (209 мг, 0,72 ммоль) (получена, как в примере 8) суспендируют в безводном ТГФ (10 мл). К этой смеси добавляют PyBrOP (358 мг, 0,77 ммоль) и триэтиламин (0,40 мл, 2,87 ммоль). Смесь перемешивают на протяжении ночи в атмосфере аргона и концентрируют в вакууме. Очистка остатка флэш-хроматографией (0-10% МеОН/CHCl3) дает свободное основание. Соответствующую соль получают осаждением из раствора свободного основания в метаноле раствором HCl-эфир.
MC (m/z) 580 (MH+)
1H-ЯМР (ДМСО-d6) δ 3,17-3,24 (м, 2Н), 3,52-3,61 (м, 4Н), 3,80 (т, J=11,7 Гц, 2Н), 3,98 (д, J=12,1 Гц, 2Н), 4,53 (шир.с, 1Н), 5,10 (д, J=13,3 Гц, 1Н), 5,40 (д, J=13,3 Гц, 1Н), 6,00 (с, 2Н), 6,42 (с, 1Н), 6,90-7,08 (серия м, 4Н), 7,32-7,66 (серия м, 4Н), 7,73 (д, J=8,5 Гц, 1Н), 8,16 (д, J=8,0 Гц, 1Н), 10,81 (с, 1Н), 12,06 (с, 1Н).
ПРИМЕР 46
1-(2,3-Дигидробензофуранил)-2-[5-(4-метоксифенил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
1-(2,3-Дигидробензо-5-фуранил)-2,3,4,9-тетрагидро-1Н-β-карболин (получен способом, описанным в WO 97/43287, промежуточный продукт 10, страница 25) (3,35 г, 11,54 ммоль), 5-(4-метоксифенил)-2-хлорпиримидин (2,55 г, 11,54 ммоль) и N,N-диизопропилэтиламин (3,5 мл) перемешивают в ДМФ (10 мл, безводный) при 120°С в течение 16 час. Полученную смесь гасят 10% NaCl и экстрагируют этилацетатом. Органический слой промывают 10% NaCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель реакционной смеси выпаривают, полученный остаток растирают с СН2Cl2 и фильтруют. Фильтрат очищают колоночной хроматографией (силикагель, этилацетат:гексаны=4:6), получая продукт в виде белого твердого вещества.
Т.пл.: 242-243°С
MC (m/z) 475 (МН+), 483 (М-1)
1H-ЯМР (ДМСО-d6) δ 2,50 (с, 1Н), 2,83 (м, 2Н), 3,12 (т, J=8,7 Гц, 2Н), 3,24 (м, 1Н), 3,78 (с, 3Н), 4,49 (т, J=8,7 Гц, 2Н), 4,90 (д, J=12 Гц, 1Н), 6,72 (д, J=8,2 Гц, 1Н), 7,03 (м, 4Н), 7,06 (д, J=7 Гц, 1Н), 7,17 (д, J=9,3 Гц, 2Н), 7,30 (д, J=8 Гц, 1Н), 7,46 (д, J=7,6 Гц, 1Н), 7,59 (д, J=8,6 Гц, 2Н), 8,73 (с, 2Н), 11,00 (с, 1Н).
ПРИМЕР 47
1,2,3,4-Тетрагидро-2-[5-(4-метоксифенил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-он (#39)
Гидрид натрия (60% в минеральном масле, 87 мг, 2,18 ммоль) и 1-(2,3-дигидро-5-бензфуранил)-2,3,4,9-тетрагидро-2-[5-(4-метоксифенил)-2-пиримидинил]-1H-β-карболин (450 мг, 0,95 ммоль) (получен, как в примере 4,6) в ДМФ (30 мл, безводный) перемешивают при комнатной температуре в течение 30 мин. Затем через раствор в течение 16 час барботируют сухой воздух. К раствору затем добавляют этилацетат (200 мл). Полученную смесь промывают 10% раствором NaCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель выпаривают и остаток растирают с этилацетатом, получая продукт в виде белого твердого вещества.
Т.пл.: 301-302°С
МС (m/z) 489 (МН+); 487 (М-1)
1H-ЯМР (ДМСО-d6) δ 3,11 (т, J=8,7 Гц, 2Н), 3,77 (с, 3Н), 4,47 (т, J=8,7 Гц, 2Н), 4,89 (м, 2Н), 6,29 (с, 1Н), 6,72 (д, J=8,1 Гц, 1Н), 6,95 (д, J=8,7 Гц, 2Н), 7,29 (м, 3Н), 7,57 (д, J=8,6 Гц, 2Н), 7,64 (д, J=8,2 Гц, 2Н), 8,16 (д, J=8,0 Гц, 1Н), 8,67 (с, 2Н), 11,87 (с, 1Н).
ПРИМЕР 47А
(R)-1,2,3,4-Тетрагидро-2-[5-(4-метоксифенил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-он (#66)
(R)-1,2,3,4-Тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-он (0,23 г, 0,678 ммоль) (получен, как в примере 6А) и 5-(4-метоксифенил)-2-хлорпиримидин (0,167 г, 0,758 ммоль) перемешивают с диизопропилэтиламином (0,33 мл) и KF (44,8 мг, 0,758 ммоль) в ДМФ (5 мл) при 60°С в течение 36 час. Реакционную смесь разбавляют СН2Cl2 (75 мл) и EtOAc (75 мл). Промывают 1 н. водной HCl (3×100 мл). Затем смесь промывают насыщенным раствором соли (2×100 мл). После сушки над MgSO4 ее концентрируют до образования желтого масла. Неочищенный продукт очищают на колонке с силикагелем, получая продукт в виде белого твердого вещества.
МС (m/z) 499 (МН+), 497 (М-1)
1H-ЯМР (CDCl3) δ 3,02 (т, 2Н, J=11,7 Гц), 3,82 (с, 3Н), 4,44 (т, 2Н, J=11,7 Гц), 4,95 (д, 1Н, J=15,6 Гц), 5,08 (д, 1Н, J=15,6 Гц), 6,24 (с, 1Н), 6,62 (д, 1Н, J=7,8 Гц), 6,92 (д, 2Н, J=7,8 Гц), 7,14˜7,61 (м, 7Н), 8,45 (м, 3Н), 9,65 (с, 1Н).
Rf=0,47 (10% СН3ОН/CHCl3). Элементный анализ для С30Н24N4О3, вычислено: %С 73,76, %Н 4,95, %N 11,47, %O 9,82; найдено: %С 73,73, %Н 4,87, %N 11,40, %O 9,65.
ПРИМЕР 48
(R)-1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-[5-(3-трифторметилфенил)фуро-2-ил]-9Н-пирроло[3,4-b]хинолин-9-он (#50)
К раствору 5-(3-трифторметилфенил)-2-фуранкарбоновой кислоты (504,4 мг, 1,97 ммоль) в смеси 1:1 DCM:ТГФ (10 мл, безводная) добавляют оксалилхлорид (275 мг, 2,17 ммоль), затем две капли ДМФ. Реакционную смесь перемешивают при комнатной температуре в течение 2 час. К реакционной смеси добавляют триэтиламин (1,1 мл), DMAP (следы) и суспензию энантиомерно чистого 1,2,3,4-тетрагидро-3-(3,4-метилендиксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (603 мг, 1,97 ммоль) (получен, как в примере 5А) в смеси 1:1 DCM:ТГФ (10 мл). Полученную смесь перемешивают при комнатной температуре в течение 16 час. Добавляют этилацетат (100 мл) и раствор промывают водным NaHCO3, насыщенным раствором соли, 1 н. HCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель реакционной смеси выпаривают и остаток растирают с этилацетатом, получая продукт в виде белого твердого вещества.
Т.пл.: 219-221°С
МС (m/z) 545 (МН+), 543 (М-1)
1H-ЯМР (ДМСО-d6) δ 5,09 (д, J=13 Гц, 1Н), 5,47 (д, J=13 Гц, 1Н), 6,00 (с, 2Н), 6,39 (с, 1Н), 6,91 (д, J=8 Гц, 1Н), 6,97 (д, J=8 Гц, 1Н), 7,02 (с, 1Н), 7,33 (д, J=7 Гц, 1Н), 7,38 (д, J=4 Гц, 1Н), 7,43 (д, J=4 Гц, 1Н), 7,60 (м, J=8 Гц, 2Н), 7,77 (д, J=5 Гц, 2Н), 8,16 (д, J=5 Гц, 3Н), 11,90 (с, 1Н).
ПРИМЕР 49
1-(2,3-Дигидробензофуранил)-2-[5-(2-пиридинил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
1-(2,3-Дигидробензфуранил)-2,3,4,9-тетрагидро-1Н-β-карболин (получен способом, описанным в WO 97/43287, промежуточный продукт 10, страница 25) (1,35 г, 4,66 ммоль), 2-хлор-5-(2-пиридинил)пиримидин (893 мг, 4,66 ммоль) и N,N-диизопропилэтиламин (1,4 мл) перемешивают в ДМФ (10 мл, безводный) при 120°С в течение 16 час. Полученную смесь гасят 10% NaCl и экстрагируют этилацетатом. Экстрагированный органический слой промывают 10% NaCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель реакционной смеси выпаривают и остаток очищают колоночной хроматографией (силикагель, этилацетат:гексаны=4:6), получая продукт в виде белого твердого вещества.
Т.пл.: 170-171°С
МС (m/z) 446 (МН+), 444 (М-1)
1H-ЯМР (ДМСО-d6) δ 2,85 (д, J=5 Гц, 2Н), 3,12 (т, J=8,7 Гц, 2Н), 3,27 (д, J=12,4 Гц, 1Н), 4,96 (д, J=12,6 Гц, 1Н), 6,72 (д, J=8,2 Гц, 1Н), 6,99 (т, J=7,4 Гц, 1Н), 7,07 (т, J=7,1 Гц, 2Н), 7,21 (с, 2Н), 7,31 (д, J=8,2 Гц, 2Н), 7,47 (д, J=7,6 Гц, 1Н), 7,85 (д, J=7,8 Гц, 1Н), 7,93 (д, J=8 Гц, 1Н), 8,62 (д, J=4,5 Гц, 1Н), 9,13 (с, 2Н), 11,01 (с, 1Н).
ПРИМЕР 50
1,2,3,4-Тетрагидро-2-[5-(2-пиридинил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-он (#61)
Гидрид натрия (60% в минеральном масле, 182 мг, 4,55 ммоль) и 1-(2,3-дигидро-5-бензофуранил)-2,3,4,9-тетрагидро-2-[5-(2-пиридинил)-2-пиримидинил]-1H-β-карболин (16176-23) (882 мг, 1,99 ммоль) (получен, как в примере 49) в ДМФ (30 мл, безводный) перемешивают при комнатной температуре в течение 30 мин. Через раствор в течение 16 час барботируют сухой воздух. Добавляют этилацетат (200 мл) и полученную смесь промывают 10% раствором NaCl, насыщенным раствором соли и затем сушат MgSO4. Растворитель реакционной смеси выпаривают и остаток растирают с этилацетатом, получая продукт в виде белого твердого вещества.
Т.пл. 201-203°С
МС (m/z) 460 (МН+); 458 (М-1)
lH-ЯМР (ДМСО-d6) δ 3,11 (т, J=8,5 Гц, 2Н), 4,46 (т, J=8,5 Гц, 2Н), 4,91 (м, 2Н), 6,34 (с, 1Н), 6,73 (д, J=8,1 Гц, 1Н), 7,31 (м, 4Н), 7,59 (т, J=8,6 Гц, 2Н), 7,84 (д, J=7,1 Гц, 1Н), 7,91 (д, J=7,7 Гц, 1Н), 8,16 (д, J=7,9 Гц, 1Н), 8,60 (д, J=4,5 Гц, 1Н), 8,98 (с, 1Н), 9,12 (с, 2Н), 11,90 (с, 1Н).
ПРИМЕР 50А
(R)-1,2,3,4-Тетрагидро-2-[5-(2-пиридинил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-он (#65)
А. 1-Метил-5-(2-пиридинил)-2(1H)пиримидон
Смесь 2-(2-пиридинил)малонового диальдегида (5 г, 0,0335 моль), метилмочевины (4,72 г, 0,0637 моль) и толуолсульфоновой кислоты (450 мг) кипятят с обратным холодильником в толуоле (100 мл) в аппарате, снабженном водоотделителем Дина-Старка, в течение 4 час. Смесь охлаждают и осадок отфильтровывают. Твердое вещество растирают с водой и перекристаллизовывают из этанола, получая продукт.
МС (m/z) (MH+) 188
1H-ЯМР (ДМСО-d6) δ 7,48 (м, 1H), 7,98 (м, 1H), 8,18 (д, J=8,0 Гц, 1H), 8,75 (c, 1Н), 9,41 (с, 2Н).
В. 2-Хлор-5-(2-пиридинил)пиримидин
Смесь 1-метил-5-(2-пиридинил)-2(1H)пиримидона (8,994 г, 0,048 моль), пентахлорида фосфора (2,156 г, 0,0104 моль) и оксихлорида фосфора (24 мл) кипятят с обратным холодильником при 120°С в течение 8 час. POCL3 отгоняют при пониженном давлении. Остаток охлаждают до комнатной температуры и добавляют смесь лед-вода. Смесь экстрагируют EtOAc, органический слой промывают 15% раствором NaCl, насыщенным раствором соли и сушат над MgSO4. Растворитель отгоняют при пониженном давлении, получая твердое вещество. рН водного слоя доводят до 6-7 с использованием насыщенного Na2СО3, затем экстрагируют EtOAc. Органический слой промывают 15% NaCl, насыщенным раствором соли, сушат над MgSO4. Растворитель отгоняют при пониженном давлении, получая твердое вещество. После растирания с МеОН получают дополнительный продукт.
МС (m/z) (MH+) 192
1H-ЯМР (ДМСО-d6) δ 3,56 (с, 3Н), 7,33 (м, 1H), 7,89 (д, J=8,8 Гц, 2Н), 8,61 (д, J=4,7 Гц, 1H), 8,95 (с, 1H), 9,31 (с, 1H).
С. (R)-1,2,3,4-Тетрагидро-2-[5-(2-пиридинил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-он
Смесь гидрохлоридной соли (R)-1,2,3,4-тетрагидро-3-(2,3-дигидробензофуран-5-ил)-9Н-пирроло[3,4-b]хинолин-9-она (1,273 г, 0,00373 моль) (получен в примере 6А), 2-хлор-5-(2-пиридинил)пиримидина (0,714 г, 0,00373 моль), KF (0,216 г, 0,00373 моль) и диизопропилэтиламина (2,27 мл) в ДМФ (45 мл) нагревают при 55°С в течение 4 час. Добавляют EtOAc и смесь промывают 0,5 н. лимонной кислотой, затем 15% NaCl, насыщенным раствором соли и сушат над MgSO4. Растворитель отгоняют при пониженном давлении, получая твердое вещество. Твердое вещество растворяют в 10% метаноле в дихлорметане и очищают колоночной хроматографией (от EtOAc до 10% СН3ОН в EtOAc), получая указанное в заголовке соединение.
Т.пл. 231-233°С
МС (m/z) (MH+) 460
1H-ЯМР (ДМСО-d6) δ 3,11 (д, J=8,7 Гц, 2Н), 4,46 (д, J=8,7 Гц, 2Н), 4,92 (м, 2Н), 6,34 (д, J=1,6 Гц, 1Н), 6,73 (д, J=8,1 Гц, 1Н), 7,28 (м, 4Н), 7,59 (м, 2Н), 7,82 (м, 1Н), 7,91 (д, J=8,0, 1Н), 8,16 (д, J=8,0, 1Н), 8,60 (J=4,5 Гц, 1Н), 8,98 (с, 1Н), 9,12 (с, 1Н), 11,92 (с, 1Н).
Указанное в заголовке соединение растворяют в метаноле, добавляют один эквивалент 0,02 М метансульфоновой кислоты (в метаноле). Растворитель отгоняют при пониженном давлении, получая соль метансульфоновой кислоты.
[α]=-236,2° (с=1,0333 г/дл, СН3ОН).
ПРИМЕР 51
2-Хлор-5-бромпиримидин
2-Хлор-5-бромпиримидин получают из 2-гидроксипиримидина (куплен у Frontier Scientific Inc.) по методике, описанной в патенте США №5693611, получение 6, колонка 17.
ПРИМЕР 52
1-(3,4-Метилендиоксифенил)-2-(5-бромпиримидин-2-ил)-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1H-β-карболина (4,38 г, 15,0 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и 2-хлор-5-бромпиримидина (2,90 г, 15,0 ммоль) (получен, как в примере 51) в безводном дегазированном ДМФ (30 мл) добавляют N,N-диизопропилэтиламин (4,2 мл, 30 ммоль). Смесь нагревают при 120-130°С на протяжении ночи. Смесь затем охлаждают и разбавляют этилацетатом. Раствор промывают 0,5 н. лимонной кислотой, водой и насыщенным раствором соли, затем сушат над Na2SO4 и концентрируют в вакууме. Очистка колоночной флэш-хроматографией (силикагель, гексан:этилацетат=6:1, об./об., затем гексан:этилацетат=4:1, об./об.) дает продукт в виде белого твердого вещества.
МС (m/z) 451 и 499 (МН+), 447 и 449 (М-1)
1H-ЯМР (CDCl3) δ 2,82-3,02 (м, 2Н), 3,30-3,40 (м, 1Н), 4,92 (дд, J=18,1 Гц, 1Н), 5,92 (д, J=3,2 Гц, 2Н), 6,72 (д, J=8,0 Гц, 1Н), 6,85 (д, J=8,0 Гц, 1Н), 6,95 (с, 1Н), 7,02 (с, 1Н), 7,13-7,21 (м, 2Н), 7,30 (д, J=7,7 Гц, 1Н), 7,55 (д, J=7,5 Гц, 1Н), 7,73 (с, 1Н), 8,34 (с, 2Н).
ПРИМЕР 53
1,2,3,4-Тетрагидро-2-(5-бромпиримидин-2-ил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#55)
Способ А:
Раствор 1-(3,4-метилендиоксифенил)-2-(5-бромпиримидин-2-ил)-2,3,4,9-тетрагидро-1Н-β-карболина (1,0 г, 2,2 ммоль) (получен, как в примере 52) в безводном ДМФ (40 мл) охлаждают на ледяной бане. Добавляют NaH (60% в минеральном масле, 0,18 г, 4,4 ммоль) и смесь перемешивают при 0°С в течение 45 мин. Через раствор барботируют высушенный воздух и смеси дают нагреться до комнатной температуры на протяжении ночи. Реакционную смесь гасят водой и экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли и водой, затем сушат над Na2SO4, концентрируют и очищают на флэш-колонке (силикагель, гексан:этилацетат=1:1, об./об., затем только этилацетатом), получая продукт в виде белого твердого вещества.
МС (m/z) 465 и 463 (MH+), 463 и 461 (М-1)
1H-ЯМР (ДМСО-d6) δ 4,80 (д, J=8,2 Гц, 1Н), 4,89 (дд, J=6,8 Гц, 1Н), 5,98 (с, 2Н), 6,20 (с, 1Н), 6,85-6,93 (м, 2Н), 6,98 (с, 1Н), 7,34 (т, J=7,3 Гц, 2Н), 7,57-7,64 (м, 3Н), 8,15 (д, J=8,0 Гц, 2Н).
Способ В:
К раствору 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (31 мг, 0,1 ммоль) (получен, как в примере 5, свободное основание) и 2-хлор-5-бромпиримидина (19 мг, 0,1 ммоль) (получен, как в примере 51) в безводном дегазированном ДМФ (2 мл) добавляют N,N-диизопропилэтиламин (28 мкл, 0,2 ммоль). Смесь выдерживают при 120-130°С на протяжении ночи. Раствор охлаждают, разбавляют этилацетатом и промывают 0,5 н. лимонной кислотой, водой и насыщенным раствором соли, затем сушат над Na2SO4 и концентрируют в вакууме. Очистка на флэш-колонке (силикагель, гексан:этилацетат=1:1, об./об., затем только этилацетат) дает продукт в виде белого твердого вещества.
МС (m/z) 465 и 463 (МН+), 463 и 461 (М-1)
1H-ЯМР (ДМСО-d6) δ 4,80 (д, J=8,2 Гц, 1Н), 4,89 (дд, J=6,8 Гц, 1Н), 5,98 (с, 2Н), 6,20 (с, 1Н), 6,85-6,93 (м, 2Н), 6,98 (с, 1Н), 7,34 (т, J=7,3 Гц, 2Н), 7,57-7,64 (м, 3Н), 8,15 (д, J=8,0 Гц, 2Н).
ПРИМЕР 54
1,2,3,4-Тетрагидро-2-[5-(3-пиридинил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#56)
Способ А:
Перемешиваемую смесь ацетата палладия(II) (0,8 мг, 3,6 мкмоль) и 1,1'-бис(дифенилфосфино)ферроцена (dppf) (2,4 мг, 4,3 мкмоль) в безводном ДМФ (1,0 мл) нагревают до 50°С в течение 15 мин и охлаждают. К раствору добавляют 1,2,3,4-тетрагидро-2-(5-бромпиримидин-2-ил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (20 мг, 43 мкмоль) (получен, как в примере 53), пиридин-3-бороновую кислоту (6,0 мг, 43 мкмоль) и триэтиламин (8 мкл, 60 мкмоль) и смесь нагревают до 90°С в течение 16 час. Раствор разбавляют этилацетатом и фильтруют через фильтровальную бумагу. Органическую фазу промывают насыщенным раствором соли и водой и затем сушат над Na2SO4. Небольшое количество силикагеля добавляют в раствор и раствор сушат в вакууме. Очистка на флэш-колонке (силикагель, 10% гидроксид аммония в смеси вода:ацетонитрил=1:10, об./об.) дает продукт в виде белого твердого вещества.
МС (m/z) 460 (М-1)
1H-ЯМР (ДМСО-d6) δ 4,88 (д, J=4,1 Гц, 1Н), 4,99 (д, J=4,1 Гц, 1Н), 5,99 (с, 2Н), 6,31 (с, 1Н), 6,88 (д, J=7,9 Гц, 1Н), 6,96 (д, J=8,1 Гц, 1Н), 7,04 (с, 1Н), 7,34 (т, J=6,9 Гц, 1Н), 7,43-7,50 (м, 1Н), 7,56-7,70 (м, 2Н), 8,08 (д, J=8,0 Гц, 1Н), 8,16 (д, J=7,9 Гц, 1Н), 8,53 (д, J=4,1 Гц, 1Н), 8,72-8,82 (шир., 1Н), 8,89 (с, 2Н), 11,87 (с, 1Н).
Способ В:
Раствор 1-(3,4-метилендиоксифенил)-2-[5-(3-пиридинил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболина (100 мг, 0,22 ммоль) (получен, как в примере 55) в безводном ДМФ (4,0 мл) охлаждают на ледяной бане. Добавляют NaH (60% в минеральном масле, 31 мг, 0,78 ммоль) и смесь перемешивают при 0°С в течение 45 мин. Через раствор барботируют высушенный воздух и смеси дают нагреться до комнатной температуры на протяжении ночи. Реакционную смесь гасят водой и экстрагируют этилацетатом. Органическую фазу промывают насыщенным раствором соли и водой, затем сушат над Na2SO4, концентрируют и очищают на флэш-колонке (силикагель, 10% гидроксид аммония в смеси вода:ацетонитрил=1:10, об./об.), получая продукт в виде белого твердого вещества.
МС (m/z) 460 (М-1)
1H-ЯМР (ДМСО-d6) δ 4,88 (д, J=4,1 Гц, 1Н), 4,99 (д, J=4,1 Гц, 1Н), 5,99 (с, 2Н), 6,31 (с, 1Н), 6,88 (д, J=7,9 Гц, 1Н), 6,96 (д, J=8,1 Гц, 1Н), 7,04 (с, 1Н), 7,34 (т, J=6, 9 Гц, 1Н), 7,43-7,50 (м, 1Н), 7,56-7,70 (м, 2Н), 8,08 (д, J=8,0 Гц, 1Н), 8,16 (д, J=7,9 Гц, 1Н), 8,53 (д, J=4,1 Гц, 1Н), 8,72-8,82 (шир., 1Н), 8,89 (с, 2Н), 11,87 (с, 1Н).
ПРИМЕР 55
1-(3,4-Метилендиоксифенил)-2-[5-(3-пиридинил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
Перемешиваемую смесь ацетата палладия (II) (27 мг, 0,12 ммоль) и 1,1'-бис(дифенилфосфино)ферроцена (dppf) (83 мг, 0,15 ммоль) в безводном ДМФ (20 мл) нагревают до 50°С в течение 15 мин и затем охлаждают. К раствору добавляют 1-(3,4-метилендиоксифенил)-2-(5-бромпиримидин-2-ил)-2,3,4,9-тетрагидро-1Н-β-карболин (674 мг, 1,5 ммоль) (получен, как в примере 52), пиридин-3-бороновую кислоту (203 мг, 1,7 ммоль) и триэтиламин (0,3 мл, 2,1 ммоль) и смесь нагревают до 90°С в течение 16 час. Раствор разбавляют этилацетатом и фильтруют через фильтровальную бумагу. Органическую фазу промывают насыщенным раствором соли и водой, сушат над Na2SO4. В раствор добавляют небольшое количество силикагеля и раствор сушат в вакууме. Очистка на флэш-колонке (силикагель, гексан:этилацетат=1:1, об./об., затем гексан:этилацетат=1:2, об./об.), дает продукт в виде белого твердого вещества.
МС (m/z) 448 (МН+) и 446 (М-1)
1H-ЯМР (CDCl3) δ 2,85-3,10 (м, 2Н), 3,33-3,48 (м, 1Н), 5,06 (дд, J=8,5 Гц, 1Н), 5,94 (д, J=4,7, 2H), 6,73 (д, J=8,0, 1H), 6,90 (д, J=8,0, 1H), 7,02 (с, 1H), 7,13-7,23 (м, 2H), 7,32-7,42 (м, 2H), 7,56 (д, J=7,4 Гц, 1H), 7,79-7,84 (м, 2H), 8,58 (с, 1H), 8,60 (с, 2H) 8,77 (с, 1H).
ПРИМЕР 56
1,2,3,4-Тетрагидро-2-[5-(4-пиридинил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-он (#57)
Перемешиваемую смесь 1,2,3,4-тетрагидро-2-(5-бромпиримидин-2-ил)-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (46 мг, 0,1 ммоль) (получен, как в примере 53), (PPh3)4Pd (3,5 мг, 3,0 мкмоль) и 4-три-н-бутилстаннилпиридина (37 мг, 0,1 ммоль) в безводном ДМФ (2,0 мл) нагревают при 140°С в течение 12 час. Добавляют катализатор (3,5 мг) и смесь кипятят с обратным холодильником в течение 4 час и затем охлаждают. Раствор разбавляют этилацетатом и фильтруют через фильтровальную бумагу. Органическую фазу промывают насыщенным раствором соли и водой, затем сушат над Na2SO4. В раствор добавляют небольшое количество силикагеля и раствор сушат в вакууме. Очистка на флэш-колонке (силикагель, только ацетонитрил, затем 10% гидроксид аммония в смеси вода:ацетонитрил=1:10, об./об.), дает продукт в виде белого твердого вещества.
МС (m/z) 460 (М-1)
1H-ЯМР (ДМСО-d6) δ 4,93 (д, J=4,2 Гц, 1Н), 5,00 (д, J=4,2 Гц, 1Н), 6,01 (с, 2Н), 6,33 (с, 1Н), 6,90 (д, J=8,0 Гц, 1Н), 6,98 (д, J=8,0 Гц, 1Н), 7,05 (с, 1Н), 7,34 (шир., 1Н), 7,62 (шир., 2Н), 7,77 (д, 2Н), 8,19 (д, J=7,9 Гц, 1Н), 8,61 (шир., 2Н), 8,78 (шир., 1Н), 9,00 (шир., 1Н).
ПРИМЕР 57
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(2-бром)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (#30)
2-Бром-2-фуранкарбоновую кислоту (1,44 г, 7,54 ммоль) в ТГФ (20 мл) перемешивают с оксалилхлоридом (1,06 мл, 7,54 ммоль) при комнатной температуре. К смеси добавляют 2 капли ДМФ, что приводит к энергичной реакции с выделением газа. После прекращения выделения газа через шприц вводят дополнительное количество оксалилхлорида (0,1 мл, 0,71 ммоль) и смесь перемешивают при комнатной температуре в течение 10 мин и затем перемешивают при 90°С в течение 10 мин. Растворитель и избыточный оксалилхлорид удаляют в вакууме, что приводит к образованию бледно-желтого кристаллического твердого вещества. К твердому веществу добавляют ТГФ (20 мл) и раствор 3-(2,3-дигидро-5-бензофуран)-1,2,3,4-тетрагидро-9Н-пирроло[3,4-b]хинолин-9-она (2,1 г) (получен, как в примере 6) в ТГФ (20 мл). К реакционной смеси добавляют Et3N (4,55 мл, 32,6 ммоль) и каталитическое количество DMAP (40 мг). Добавляют несколько капель ДМФ, что приводит к образованию прозрачной реакционной смеси. Реакционную смесь перемешивают при комнатной температуре в течение 4 час. Растворитель реакционной смеси выпаривают, получая твердый остаток. Остаток снова растворяют в CHCl3 (200 мл), промывают водой (3×200 мл) и органический слой сушат над MgSO4. Органический растворитель выпаривают, получая продукт в виде не совсем белого твердого вещества.
МС (m/z) 480 (МН+), 478 (М-1)
1H-ЯМР (CDCl3) δ 5,03 (д, 1Н, J=15,5 Гц), 5,23 (д, 1Н, J=15,5 Гц), 5,85 (д, 2Н, J=8,0 Гц), 6,40 (м, 2Н), 6,56 (м, 1Н), 6,81 (м, 2Н), 7,00 (д, 1Н, J=4,3 Гц), 7,32 (т, 1Н, J=8,6 Гц), 7,53 (т, 1Н, J=8,6 Гц), 7,65 (д, 1Н, J=8,6 Гц), 8,38 (д, 1Н, J=8,6 Гц), 12,8 (с, 1Н).
ПРИМЕР 58
4-(4-Метил)пиперазинилкарбонилбензолбороновая кислота
4-Карбоксибензолбороновую кислоту (0,332 г, 2 ммоль), 1-метилпиперазин (0,22 мл, 2 ммоль) и PyBrOP (0,9334 г, 2 ммоль) перемешивают с DIPEA (0,696 мл, 4 ммоль) в ДМФ (7 мл) при комнатной температуре в течение 16 час. Препаративная ТСХ (10% МеОН/CHCl3) дает продукт в виде белого твердого вещества.
МС (m/z) 251 (МН+), 249 (М-1)
1H-ЯМР (CD3OD) δ 2,36 (с, 3Н), 2,43 (с, 2Н), 2,57 (с, 2Н), 3,51 (с, 2Н), 3,82 (с, 2Н), 7,34 (с, 2Н), 7,76 (с, 2Н).
ПРИМЕР 59
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(1-(4-метил)пиперазинилкарбонил)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (#44)
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(2-бром)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (59,6 мг, 0,12 ммоль) (получен, как в примере 57) перемешивают с Pd(PPh3)4 (7,37 мг, 0,0062 ммоль) в диоксане (5,5 мл) с барботированием N2 в течение 10 мин. Затем добавляют раствор 4 -(4-метил)пиперазинилкарбонилбензолбороновой кислоты (37,0 мг, 0,15 ммоль) и К2СО3 (51,5 мг, 0,37 ммоль) в Н2O (1,1 мл). Реакционную смесь перемешивают при 100°С в течение 1 часа. Растворитель выпаривают, остаток очищают препаративной ТСХ (10% МеОН/CHCl3) и затем растирают со смесью эфир/МеОН (15 мл/1 мл), получая продукт в виде бледно-желтого порошка.
МС (m/z): 603 (МН+), 601 (М-1)
1H-ЯМР (CD3OD) δ 2,32 (с, 3Н), 2,53˜2,62 (м, 4Н), 3,53 (шир.с, 2Н), 3,83 (шир.с, 2Н), 5,17 (д, 1Н, J=15,5 Гц), 5,41 (д, 1Н, J=15,5 Гц), 5,83 (с, 2Н), 6,22 (с, 1Н), 6,70 (м, 1Н), 6,82 (м, 2Н), 7,03 (м, 1Н), 7,25˜7,34 (м, 2Н), 7,46˜7,56 (м, 4Н), 7,93 (д, 2Н, J=8,6 Гц), 8,31 (д, 2Н, J=8,6 Гц).
ПРИМЕР 59А
(R)-1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(1-(4-метил)пиперазинилкарбонил)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (#69)
А. Метиловый эфир 5-(4-(4-метил)пиперазинилкарбонилфенил)фуранкарбоновой кислоты
Смесь 4-(4-метил)пиперазинилкарбонилбензолбороновой кислоты (получена, как в примере 58) (1,31 г, 5,28 ммоль), метилового эфира бромфуранкарбоновой кислоты (1,08 г, 5,28 ммоль) (получен из 5-бромфуранкарбоновой кислоты в HCl/MeOH в течение 5 час при комнатной температуре) в смеси диоксана (45 мл) и H2O (9 мл) дегазируют барботированием N2 в течение 10 мин. К смеси добавляют Pd(PPh3)4 (0,627 г, 0,528 ммоль) и К2СО3 (2,185 г, 15,84 ммоль). Раствор перемешивают при 100°С в течение 3 час. Растворитель выпаривают и остаток растворяют в СН2Cl2 (100 мл). Раствор промывают насыщенным раствором соли (3×100 мл), сушат над MgSO4, концентрируют в вакууме и неочищенный продукт очищают на колонке с силикагелем (5% СН3ОН/CHCl3), получая продукт в виде желтого твердого вещества.
МС (m/z) 315 (МН+), 313 (М-1)
1H-ЯМР (CDCl3) δ 2,32˜2,48 (м, 7Н), 3,48 (с, 2Н), 3,80 (с, 2Н), 3,92 (с, 3Н), 6,81 (д, 1Н, J=2,0 Гц), 7,24 (д, 1Н, J=2,0 Гц), 7,49 (д, 2Н, J=7,9 Гц), 7,83 (д, 2Н, J=7,9 Гц).
Rf=0,51 (10% СН3ОН/CHCl3).
В. 5-(4-(4-Метил)пиперазинилкарбонилфенил)фуранкарбоновая кислота
К продукту указанной выше стадии А (метиловый эфир 5-(4-(4-метил)пиперазинилкарбонилфенил)фуранкарбоновой кислоты) (1,08 г, 3,29 ммоль), растворенному в ТГФ (98,7 мл), добавляют LiOH (16,45 мл, 0,2 н. в Н2О). Раствор перемешивают при комнатной температуре в течение 3,5 час и нейтрализуют HCl (3,29 мл, 1,0 М в эфире). После концентрирования неочищенное вещество используют без дополнительной очистки.
МС (m/z) 329 (МН+), 327 (М-1)
1H-ЯМР (CD3OD) δ 2,35 (с, 3Н), 2,36˜2,58 (шир.с, 4Н,), 3,48 (с, 2Н), 3,85 (с, 2Н), 6,90 (д, J=2,0 Гц), 7,02 (д, 1Н, J=2,0 Гц), 7,46 (д, 2Н, J=7,9 Гц), 7,95 (д, 2Н, J=7,9 Гц).
С. (R)-1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(1-(4-метил)пиперазинилкарбонил)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (#69)
Смесь гидрохлоридной соли R-1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она (1,12 г, 3,29 ммоль) (получен, как в примере 5А) и продукта стадии В (1,034 г, 3,29 ммоль) перемешивают с PyBrOP (1,535 г, 3,29 ммоль) и диизопропилэтиламином (1,716 мл, 9,87 ммоль) в ДМФ (30 мл) при комнатной температуре в течение 12 час. Реакционную смесь разбавляют CH2Cl2 (75 мл) и EtOAc (75 мл). Очищают на колонке с силикагелем (от неразбавленного CH2Cl2 до 2,5% CH3OH/CH2Cl2), получая продукт в виде не совсем белого твердого вещества.
МС (m/z): 603 (МН+), 601 (М-1)
1H-ЯМР (CD3OD) δ 2,32 (с, 3Н), 2,43˜2,55 (м, 4Н), 3,53 (шир.с, 2Н), 3,83 (шир.с, 2Н), 5,25 (д, 1Н, J=15,5 Гц), 5,51 (д, 1Н, J=15,5 Гц), 5,87 (с, 2Н), 6,29 (с, 1Н), 6,70 (м, 1Н), 6,82 (м, 2Н), 7,08 (м, 1Н), 7,20˜7,39 (м, 2Н), 7,46˜7,58 (м, 4Н), 8,01 (д, 2Н, J=8,6 Гц), 8,31 (д, 2Н, J=8,6 Гц).
ВЭЖХ Chiralpak внутр. диаметр 4,6×250 мм, 1% DEA/MeOH, Tr=4,846 мин)
ПРИМЕР 60
Натриевая соль 1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(2-(4-гидрокси)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-она (Na соль #22)
По методике, описанной в примере 59, с соответствующей заменой реагентов получают продукт в виде не совсем белого твердого вещества.
МС (m/z) 493 (МН+), 491 (М-1)
1H-ЯМР (CDCl3) δ 5,21 (д, 1Н, J=15,6 Гц), 5,57 (д, 1Н, J=15,6 Гц), 6,12 (с, 2Н), 6,51 (с, 2Н) 6,68 (д, 1Н, J=4,1 Гц), 6,98˜7,14 (м, 4Н), 7,38 (с, 1Н), 7,48 (т, 1Н, J=8,6 Гц), 7,62˜7,79 (м, 4Н), 8,08 (с, 1Н), 8,28 (д, 1Н, J=8,6 Гц).
ПРИМЕР 61
(4-(2-(1-Пирролидинил)этокси)фенил)бороновая кислота
(Получена по методике, описанной Hoye, T.R. and Chen. M. in J. Org. Chem. 1996, 61, 7940)
К раствору 1-[2-(4-бромфенокси-)этил]пирролидина (2,70 г, 10 ммоль) в ТГФ (40 мл) добавляют н-бутиллитий (6,9 мл 1,6 М в гексанах, 11 ммоль) при -78°С. Реакционную смесь перемешивают при -78°С в течение 15 мин и затем при 0°С в течение 15 мин. Затем к реакционной смеси при 0°С добавляют триметилборат (2,5 мл, 22 ммоль). Смесь постепенно нагревают до комнатной температуры на протяжении ночи. Метилборат в реакционной смеси гидролизуют взаимодействием с насыщенным водным раствором NH4Cl (100 мл) при комнатной температуре в течение 30 мин. Отделяют верхний органический слой. Водный слой экстрагируют CHCl3 (2×100 мл). Органические слои объединяют, промывают насыщенным раствором соли (2×100 мл) и сушат MgSO4. Растворитель выпаривают, получая густое масло, которое очищают колоночной хроматографией (10% МеОН/CHCl3 и 1% Et3N), получая продукт в виде белого твердого вещества.
МС (m/z) 236 (МН+), 234 (М-1)
1H-ЯМР (CD3OD) δ 1,81 (м, 4Н), 2,67 (м, 4Н), 2,89 (т, 2Н, J=6,0 Гц), 4,08 (т, 2Н, J=6,0 Гц), 6,74 (д, 2Н, J=8,6 Гц), 7,62 (д, 2Н, J=8,6 Гц).
ПРИМЕР 62
1,2,3,4-Тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(2-(1-пирролидинил)этокси)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-он (#45)
По методике, описанной в примере 59, с соответствующей заменой реагентов получают продукт в виде не совсем белого твердого вещества.
МС (m/z): 590 (МН+), 588 (М-1)
1H-ЯМР (CDCl3) δ 2,18 (с, 4Н), 2,55 (с, 4Н), 2,75 (м, 2Н), 2,90 (м, 2Н), 4,67 (д, 1Н, J=15,6 Гц), 4,82 (д, 1Н, J=15,6 Гц), 5,18 (с, 2Н), 5,81 (м, 1Н), 6,08 (м, 1Н), 6,21 (с, 2Н), 6,35 (с, 1Н), 6,60 (с, 1Н), 6,82 (м, 3Н), 6,92 (м, 1Н), 7,04 (м, 1Н), 7,21 (с, 2Н), 7,62 (д, 1Н, J=8,6 Гц).
ПРИМЕР 63
3-(2,3-Дигидро-5-бензофуранил)-1,2,3,4-тетрагидро-2-(бензил)-9Н-пирроло[3,4-b]хинолин-9-он (#60)
1-(2,3-Дигидро-5-бензофуранил)-2-бензил-2,3,4,9-тетрагидро-1H-β-карболин (получен, как в примере 2) (5,25 г, 13,81 ммоль), диоксид калия (3,92 г, 55,24 ммоль) и 18-краун-6 (3,65 г, 13,81 ммоль) смешивают с ДМФ (100 мл) в колбе на 200 мл. Реакционную смесь выдерживают при комнатной температуре на протяжении ночи. Реакционную смесь медленно добавляют в отдельную колбу на 500 мл, содержащую смесь EtOAc (172 мл), Н2О (172 мл) и 1 н. водную HCl (50 мл). Наблюдают, что смесь образует пузырьки газа малого размера. Реакционную смесь перемешивают при 0°С в течение 30 мин, что приводит к образованию осадка на границе раздела двух жидких слоев. Осадок отфильтровывают, промывают Н2О (20 мл) и затем сушат в вакуумном сушильном шкафу, получая продукт в виде не совсем белого твердого вещества.
МС (m/z): 395 (МН+), 393 (М-1)
1H-ЯМР (CDCl2) δ 3,12 (т, 2Н, J=8,7 Гц), 3,50˜3,65 (м, 2Н), 3,99 (д, 1Н, J=13,0 Гц), 4,22 (д, 1Н, J=13,0 Гц), 4,55 (т, 2Н, J=8,7 Гц), 4,91 (с, 1Н), 6,74 (д, 1Н, J=8,7 Гц), 7,11˜7,32 (м, 9Н), 7,48 (т, 1Н, J=8,7 Гц), 8,30 (т, 1Н, J=8,7 Гц).
ПРИМЕР 64
3-(3,4-Метилендиоксифенил)-1,2,3,4-тетрагидро-2-[5-(3-трифторметил)фенил-2-фуроил]-9Н-пирроло[3,4-b]хинолин-9-он (#13)
По методике, описанной в примере 63, с соответствующей заменой реагентов 1-(3,4-метилендиоксифенил)-2-бензил-2,3,4,9-тетрагидро-1Н-β-карболин (0,381 г, 0,719 ммоль) подвергают взаимодействию с получением продукта в виде не совсем белого твердого вещества. Следует отметить, что для полного образования осадка две жидкие реакционные смеси выдерживают при комнатной температуре в течение 48 час, а не в течение ночи.
МС (m/z): 545 (МН+), 567 (М+23), 543 (М-1)
1H-ЯМР (ДМСО-d6) δ 5,09 (д, J=14 Гц, 1Н), 5,46 (д, J=14 Гц, 1Н), 5,99 (с, 2Н), 6,39 (с, 1Н), 6,91 (д, J=8 Гц, 1Н), 6,97 (д, J=9 Гц, 1Н), 7,02 (с, 1Н), 7,33 (д, J=8 Гц, 1Н), 7,38 (д, J=4 Гц, 1Н), 7,43 (д, J=4 Гц, 1Н), 7,60 (м, J=8 Гц, 2Н), 7,77 (д, J=5 Гц, 2Н), 8,16 (д, J=4 Гц, 3Н), 11,55 (с, 1Н).
ПРИМЕР 65
1-(3,4-Метилендиоксифенил)-2-[4-(4-метоксифенил)тиазол-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
А. 1-(3,4-Метилендиоксифенил)-2-[3-(флуоренилметилоксикарбонил)тиокарбамоил]-2,3,4,9-тетрагидро-1H-β-карболин
Смесь 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболина (2,66 г, 9,08 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и Fmoc-изотиоцианат (2,82 г, 10,14 ммоль) растворяют в безводном дихлорметане (50 мл). Смесь перемешивают в течение 16 часов при температуре окружающей среды и затем концентрируют в вакууме. Очистка флэш-хроматографией (0-10% метанол в дихлорметане) дает защищенную тиомочевину в виде светло-желтого твердого вещества.
МС (m/z) 574 (МН+)
1H-ЯМР (CDCl3) δ 2,86 (дд, J=12,9, 5,1 Гц, 1Н), 3,09 (дт, J=17,1, 6,9 Гц, 1Н), 3,56 (дт, J=12,9, 5,1 Гц, 1Н), 4,19 (т, J=6,9 Гц, 1Н), 4,43-4,53 (м, 2Н), 5,91 (с, 2Н), 6,70 (д, J=8 Гц, 1Н), 6,90 (шир.д, J=7,6 Гц, 1Н), 6,97 (шир.с, 1Н), 7,11-7,78 (серия м, 17Н).
В. 1-(3,4-Метилендиоксифенил)-2-(тиокарбамоил)-2,3,4,9-тетрагидро-1Н-β-карболин
Раствор защищенной тиомочевины из части А (4,78 г, 8,33 ммоль) в 20% (об./об) пиперидине в метаноле кипятят с обратным холодильником в течение 5 час. Смесь концентрируют в вакууме с получением желтого твердого остатка, который очищают флэш-хроматографией (SiO2, 0-10% метанол в дихлорметане), получая желтое твердое вещество.
МС (m/z): 352 (МН+)
1H-ЯМР (CDCl3) δ 2,69-2,87 (серия м, 2Н), 3,10-3,19 (м, 1Н), 4,24 (шир.с, 1Н), 6,00 (д, J=3,3 Гц, 2Н), 6,72 (д, J=8,0 Гц, 1Н), 6,87 (д, J=8,0 Гц, 1Н), 7,00-7,11 (серия м, 3Н), 7,30 (д, J=8,0 Гц, 1Н), 7,46 (д, J=7,7 Гц, 1Н), 7,74 (шир.с, 3Н), 11,06 (с, 1Н).
С. 1-(3,4-Метилендиоксифенил)-2-[4-(4-метоксифенил)тиазол-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору тиомочевины из части В (223 мг, 0,63 ммоль) в смеси 1:1 диоксан:этанол (5 мл) добавляют 4-метоксифенил-2'-бромацетофенон (175 мг, 0,76 ммоль) и триэтиламин (0,40 мл). Смесь нагревают до 70°С в течение 3 час, охлаждают до комнатной температуры и концентрируют на роторном испарителе. Остаток очищают флэш-хроматографией (SiO2, 0-10% метанол в дихлорметане), получая бесцветное твердое вещество.
МС (m/z) 482 (МН+)
1H-ЯМР (CDCl3) δ 2,86-2-3,07 (серия м, 2Н), 3,61-3,71 (м, 1Н), 3,78 (с, 3Н), 3,91-4,02 (м, 1Н), 5,99 (д, J=3,3 Гц, 2Н), 6,58 (с, 1Н), 6,80-7,11 (серия м, 8Н), 7,31 (д, J=7,8 Гц, 1Н), 7,48 (д, J=7,6 Гц, 1Н), 7,82 (д, J=8,7 Гц, 2Н), 10,93 (с, 1Н).
ПРИМЕР 66
1-(3,4-Метилендиоксифенил)-2-[4-фенилтиазол-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
А. 1-(3,4-Метилендиоксифенил)-2-[3-(флуоренилметилоксикарбонил)тиокарбамоил]-2,3,4,9-тетрагидро-1H-β-карболин
Смесь 1-(3,4-метилендиоксифенил)-2,3,4,9-тетрагидро-1Н-β-карболина (2,66 г, 9,08 ммоль) (получен способом, описанным в WO 97/43287, промежуточный продукт 7, страница 24) и Fmoc-изотиоцианата (2,82 г, 10,14 ммоль) растворяют в безводном дихлорметане (50 мл). Смесь перемешивают в течение 16 час при температуре окружающей среды и затем концентрируют в вакууме. Очистка флэш-хроматографией (0-10% метанола в дихлорметане) дает защищенную тиомочевину в виде светло-желтого твердого вещества.
МС (m/z): 574 (МН+)
1H-ЯМР (CDCl3) δ 2,86 (дд, J=12,9, 5,1 Гц, 1Н), 3,09 (дт, J=17,1, 6,9 Гц, 1Н), 3,56 (дт, J=12,9, 5,1 Гц, 1Н), 4,19 (т, J=6,9 Гц, 1Н), 4,43-4,53 (м, 2Н), 5,91 (с, 2Н), 6,70 (д, J=8 Гц, 1Н), 6,90 (шир.д, J=7,6 Гц, 1Н), 6,97 (шир.с, 1Н), 7,11-7,78 (серия м, 17Н).
В. 1-(3,4-Метилендиоксифенил)-2-(тиокарбамоил)-2,3,4,9-тетрагидро-1Н-β-карболин
Раствор защищенной тиомочевины из части А (4,78 г, 8,33 ммоль) в 20% (об./об.) пиперидина в метаноле кипятят с обратным холодильником в течение 5 час. Смесь концентрируют в вакууме, получая неочищенный остаток, который очищают флэш-хроматографией (SiO2, 0-10% метанол в дихлорметане) с получением желтого твердого вещества.
МС (m/z): 352 (МН+)
1H-ЯМР (CDCl3) δ 2,69-2,87 (серия м, 2Н), 3,10-3,19 (м, 1Н), 4,24 (шир.с, 1Н), 6,00 (д, J=3,3 Гц, 2Н), 6,72 (д, J=8,0 Гц, 1Н), 6,87 (д, J=8,0 Гц, 1Н), 7,00-7,11 (серия м, 3Н), 7,30 (д, J=8,0 Гц, 1Н), 7,46 (д, J=7,7 Гц, 1Н), 7,74 (шир.с, 3Н), 11,06 (с, 1Н).
С. 1-(3,4-Метилендиоксифенил)-2-[4-фенилтиазол-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
К раствору тиомочевины части В (227 мг, 0,65 ммоль) добавляют β-бромацетофенон (159 мг, 0,80 ммоль) и триэтиламин (0,40 мл). Данную смесь нагревают до 70°С в течение 3 час, охлаждают до комнатной температуры и концентрируют в роторном испарителе. Остаток очищают флэш-хроматографией (SiO2, 0-10% метанол в дихлорметане), получая светло-желтое твердое вещество.
МС (m/z): 452 (МН+)
1H-ЯМР (CDCl3) δ 2,87-2-3,06 (серия м, 2Н), 3,63-3,73 (м, 1Н), 3,93-3,99 (м, 1Н), 5,99 (д, J=3,3 Гц, 2Н), 6,59 (с, 1Н), 6,81-7,11 (серия м, 5Н), 7,25-7,69 (серия м, 6Н), 7,89 (д, J=7,4 Гц, 2Н), 10,95 (с, 1Н).
ПРИМЕР 67
3-(2,3-Дигидробензофуран-5-ил)-1,2,3,4-тетрагидро-3R-9Н-пирроло[3,4-b]хинолинон
А: [2-(1H-Индол-3-ил)этил]-(1-нафталин-1-илэтил)амин получают способом, описанным Kawate, Т.; Yamanaka, М.; Nakagawa, M. in Heterocycles, 1999, 50, 1033.
В: R- и S-Диастереомеры 1-(2,3-дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1Н-β-карболина
[2-(1H-Индол-3-ил)этил]-(1-нафталин-1-илэтил)амин (1,0 г, 3,18 ммоль) и 2,3-дигидробензофуран-5-карбальдегид (2,356 г, 15,92 ммоль) перемешивают в п-ксилоле (20 мл) при 165°С в течение 7 час. К реакционной смеси добавляют силикагель (10 г) и гексан (200 мл). Реакционную смесь фильтруют и бесцветный фильтрат отбрасывают. Силикагель промывают этилацетатом (100 мл). Растворитель после промывки этилацетатом выпаривают, концентрированное неочищенное вещество растворяют в небольшом количестве CH2Cl2 и вводят в колонку с силикагелем. Колонку элюируют 5% этилацетатом в гексане, получая два диастереомера.
1-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1S-1Н-β-карболин (побочный диастереомер A) (Rf=0,59 в 30% EtOAc/гексан) получают в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 1,58, 1,62 (д, 3Н, J=6,5 Гц), 2,61 (м, 1Н), 2,91 (м, 1Н), 3,05˜3,20 (м, 4Н), 4,51 (т, 2Н, J=8,8 Гц), 4,72 (м, 1Н), 4,81 (с, 1Н), 6,68 (м, 1Н), 6,92 (м, 4Н), 7,05-7,65 (м, 5Н), 7,70˜7,95 (м, 4Н).
МС (m/z) MH+ (445), МН- (443).
1-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1R-1Н-β-карболин (целевой диастереомер В) (Rf=0,51 в 30% EtOAc/гексан) получают в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 1,58 (д, 3Н, J=6,5 Гц), 2,65 (м, 1Н), 2,91 (м, 2Н), 3,05 (т, 2Н, J=8,8 Гц), 3,15 (м, 1Н), 4,51 (т, 2Н, J=8,8 Гц), 4,65 (м, 1Н), 5,10 (с, 1Н), 6,68 (м, 1Н), 6,85 (с, 2Н), 7,11 (м, 2Н), 7,20˜7,50 (м, 5Н), 7,68 (м, 2Н), 7,81 (м, 1Н), 8,21 (м, 1Н).
МС (m/z) MH+ (445), МН- (443).
С. Превращение 3-диастереомера в R-диастереомер
1-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1S-1Н-β-карболин (побочный диастереомер А) (190 г, 0,428 ммоль) перемешивают в 1000 мл СН2Cl2 с ТФУ (52 мл, 701 моль) при комнатной температуре на протяжении ночи. Реакцию гасят NaOH (35 г, 0,875 моль) в воде (100 мл). Реакционную смесь хорошо перемешивают и затем выдерживают в течение 0,5 часа, в течение этого времени образуется осадок. Осадок отфильтровывают, твердое вещество промывают водой и сушат в высоком вакууме, получая продукт в виде твердого вещества.
1H-ЯМР идентичен с 1H-ЯМР 1-(2,3-дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1R-1Н-β-карболина (целевой диастереомер).
D: 3-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-1,2,3,4-тетрагидро-3R-9Н-пирроло[3,4-b]хинолинон
1-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-2,3,4,9-тетрагидро-1R-1Н-β-карболин (0,6469 г, 1,46 ммоль) и трет-бутоксид калия (0,279 г, 2,48 ммоль) перемешивают в ДМФ (14 мл) при комнатной температуре. На протяжении ночи в реакционную смесь барботируют газообразный O2. Реакцию гасят HCl (2,48 мл, 1 н. водная). Добавляют этилацетат (50 мл) и Н2O (50 мл). Органический слой отделяют. Водный слой экстрагируют этилацетатом (50 мл) и СН2Cl2 (50 мл). Органические слои промывают насыщенным раствором соли (3 х 50 мл) и сушат над MgSO4. Образовавшийся продукт концентрируют и очищают с помощью силикагеля (2% метанол/СН2Cl2), получая продукт в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 1,65 (д, 3Н, J=6,5 Гц), 3,05 (т, 2Н, J=8,8 Гц), 4,01 (м, 2Н), 4,51 (т, 2Н, J=8,8 Гц), 4,68 (м, 1Н), 5,31 (с, 1Н), 6,62 (с, 1Н), 6,88˜7,89 (м, 12Н), 8,25 (д, 1Н).
МС (m/z) MH+ (459), МН- (457).
Е: 3-(2,3-Дигидробензофуран-5-ил)-1,2,3,4-тетрагидро-3R-9Н-пирроло[3,4-b]хинолинон
3-(2,3-Дигидробензофуран-5-ил)-2-(1R-1-нафталин-1-илэтил)-1,2,3,4-тетрагидро-3R-9Н-пирроло[3,4-b]хинолинон (24 мг, 0,0524 ммоль) растворяют в 5 мл этанола. К реакционной смеси добавляют 10% Pd/C (50 мг) и HCl (1,0 М в диэтиловом эфире (0,05 мл, 0,05 мл)). Реакционную смесь перемешивают при 35 фунт/кв. дюйм (241,3 кПа) газообразного Н2 в течение 3 час при комнатной температуре. Катализатор отфильтровывают на пробке из целита. Реакционную смесь концентрируют, получая неочищенный продукт. Очистка препаративной ТСХ (5% MeOH/CH2Cl2) дает указанный в заголовке продукт в виде желтоватого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 13,23 (д, 2Н, J=8,8 Гц), 4,59 (т, 2Н, J=8,8 Гц), 4,78 (м, 2Н), 5,32 (с, 1Н), 6,88 (м, 1Н), 7,31 (м, 2Н), 7,72 (м, 3Н), 8,32 (м, 1Н).
МС (m/z) МН+ (305), МН- (303).
ПРИМЕР 68
3-Бензо[1,3]диоксол-5-ил-2-(5-бромфуран-2-карбонил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он
К раствору 5-бром-2-фуранкарбоновой кислоты (2,1 г, 6,856 ммоль) в ТГФ (20 мл) добавляют оксалилхлорид (0,66 мл, 7,541 ммоль). К реакционной смеси затем добавляют 2 капли ДМФ с наблюдаемым энергичным выделением пузырьков СО. Затем добавляют оксалилхлорид ((COCl)2) (0,1 мл). Реакционную смесь перемешивают при комнатной температуре в течение 10 мин и при 90°С в течение 10 мин. Растворитель и избыточный (COCl)2 удаляют в вакууме, получая 5-бромфуран-2-карбонилхлорид в виде светло-желтого кристаллического твердого вещества.
Твердый 5-бромфуран-2-карбонилхлорид растворят в ТГФ (20 мл). Затем добавляют раствор 3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидро-9Н-пирроло[3,4-b]хинолинона (2,1 г, 6,856 ммоль) в ТГФ (20 мл). Затем последовательно добавляют триэтиламин (4,55 мл, 32,64 ммоль) и DMAP (40 мг, 0,327 ммоль). К реакционной смеси добавляют несколько капель ДМФ для сохранения прозрачности раствора. Реакционную смесь перемешивают при комнатной температуре в течение 4 час и затем концентрируют в вакууме. Остаток растворяют в CHCl3 (200 мл) и промывают H2O (3×200 мл). Органический слой сушат над MgSO4, получая указанный в заголовке продукт в виде не совсем белого твердого вещества. Дальнейшая очистка не является обязательной.
1H-ЯМР 300 МГц (CD3OD) δ 4,87 (д, 1Н, J=11,5 Гц), 5,19 (д, 1Н, J=11,5 Гц), 5,78 (м, 2Н), 6,24˜7,60 (м, 8Н), 8,39 (д, 1Н, J=8,3 Гц).
МС (m/z): 479, 481 (МН+), 479, 477 (МН-)
ПРИМЕРЫ 69-79
Общая процедура
3-Бензо[1,3]диоксол-5-ил-2-(5-бромфуран-2-карбонил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (0,100 г, 0,2086 ммоль) перемешивают со смесью подходящим образом замещенной бороновой кислоты (0,2296 ммоль, 1,1 экв.), Pd(PPh3)4 (12,4 мг, 0,1043 ммоль), К2СО3 (86,4 мг, 0,6258 ммоль) в 1,4-диоксане (8 мл) и H2O (2 мл), дегазированной при помощи N2, и затем перемешивают при 100°С в течение 1,5 часов. Реакционную смесь загружают на пластину препаративной ТСХ с силикагелем и элюируют 5% CH3OH/CH2Cl2, получая выделенный продукт в виде твердого вещества.
Соединение #110 (проводят взаимодействие с фенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,19 (д, 1Н, J=11,5 Гц), 5,42 (д, 1Н, J=11,5 Гц), 5,93 (с, 2Н), 6,38 (с, 1Н), 6,74˜8,31 (м, 14Н).
МС (m/z): 477 (МН+), 475 (МН-)
Соединение #111 (проводят взаимодействие с 4-метилтиофенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,21 (д, 1Н, J=11,5 Гц), 5,44 (д, 1Н, J=11,5 Гц), 5,91 (с, 2Н), 6,40 (с, 1Н), 6,77 (д, 1Н, J=9,0 Гц), 6,98 (с, 2Н), 7,21˜7,81 (м, 11Н), 8,31 (д, 1Н, J=9,0 Гц).
МС (m/z): 523 (МН+), 521 (МН-).
Соединение #112 (проводят взаимодействие с 3-тиенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,22 (д, 1H, J=11,5 Гц), 5,43 (д, 1H, J=11,5 Гц), 5,88 (с, 2Н), 6,38 (с, 1Н), 6,72˜8,38 (м, 12Н).
МС (m/z): 483 (МН+), 481 (МН-)
Соединение #116 (проводят взаимодействие с 4-метилфенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 2,25 (с, 3Н), 5,21 (д, 1H, J=11,5 Гц), 5,42 (д, 1H, J=11,5 Гц), 5,80 (с, 2Н), 6,38 (с, 1H), 6,74˜8,31 (м, 13Н).
МС (m/z): 491 (МН+), 489 (МН-).
Соединение #113 (проводят взаимодействие с 2-нитрофенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,25 (д, 1H, J=11,5 Гц), 5,42 (д, 1H, J=11,5 Гц), 5,88 (с, 2Н), 6,39 (с, 1H), 6,68˜8,66 (м, 13Н).
МС (m/z): 522 (МН+), 520 (МН-).
Соединение #117 (проводят взаимодействие с 2-тиенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,19˜5,42 (м, 2Н), 5,93 (с, 2Н), 6,40 (с, 1H), 6,74˜8,35 (м, 11Н).
МС (m/z): 467 (МН+), 465 (МН-).
Соединение #118 (проводят взаимодействие с 3,4-метилендиоксифенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,19˜5,42 (м, 2Н), 5,93 (м, 4Н), 6,38 (с, 1Н), 6,74˜8,31 (м, 12Н).
MC (m/z): 521 (МН+), 519 (МН-).
Соединение #119 (проводят взаимодействие с 4-цианофенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,21˜5,42 (м, 2Н), 5,70 (м, 2Н), 6,18 (с, 1Н), 6,60˜8,51 (м, 13Н).
MC (m/z): 502 (МН+), 500 (МН-).
Соединение #120 (проводят взаимодействие с 4-гидроксиметилфенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 4,79 (с, 2Н), 5,25 (д, 1Н, J=11,5 Гц), 5,52 (д, 1Н, J=11,5 Гц), 5,89 (с, 2Н), 6,48 (с, 1Н), 6,70˜8,31 (м, 13Н).
MC (m/z): 507 (МН+), 505 (МН-).
Соединение #121 (проводят взаимодействие с 3-гидроксиметилфенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 4,79 (с, 2Н), 5,21 (д, 1Н, J=11,5 Гц), 5,48 (д, 1Н, J=11,5 Гц), 5,89 (с, 2Н), 6,31 (с, 1Н), 6,62˜8,31 (м, 13Н).
MC (m/z): 507 (МН+), 505 (МН-).
Соединение #122 (проводят взаимодействие с 4-диметиламинофенилбороновой кислотой)
1H-ЯМР 300 МГц (CD3OD) δ 5,21˜5,50 (д, 1Н, J=11,5 Гц), 5,90 (с, 2Н), 6,40 (д, 1Н), 6,64˜8,31 (м, 13Н).
MC (m/z): 520 (МН+), 518 (МН-).
ПРИМЕР 80
3-(2,3-Дигидробензофуран-5-ил)-2-пиримидин-2-ил-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#123)
Соль 3-(2,3-Дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он·HCl (0,15 г, 0,440 ммоль) перемешивают с хлорпиримидином (60,5 мг, 0,528 ммоль), KF (31 мг, 0,528 ммоль) и DIEA (0,19 мл, 1,1 ммоль) при 60°С в течение 16 час. Реакционную смесь разбавляют Н3О (20 мл). Твердое вещество отфильтровывают и сушат на воронке с отсасыванием в вакууме. После препаративной ТСХ на силикагеле указанный в заголовке продукт выделяют в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 3,10 (т, 2Н, J=8,8 Гц), 4,52 (т, 2Н, J=8,8 Гц), 4,92 (м, 2Н), 6,15˜8,45 (м, 10Н), 9,81 (шир.с, 1Н).
МС (m/z) 383 (МН+), 381 (МН-).
ПРИМЕР 81
3-Бензофуран-5-ил-2-(5-пиридин-2-илпиримидин-2-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#126)
А: Бензофуран-5-карбальдегид получают способом, описанным Hiroya, К.; Hashimura, К.; Ogasawara, К. in Heterocycles, 1994, vol.38, № 11, 2463-72.
В: 1-Бензофуран-5-ил-2,3,4,9-тетрагидро-1Н-β-карболин получают способом, указанным в примере 12.
1H-ЯМР 300 МГц (CDCl3) δ 2,68˜2,95 (м, 2Н), 3,10 (м, 1Н), 3,28 (м, 1Н), 5,25 (с, 1Н), 6,65 (с, 1Н), 7,15 (м, 3Н), 7,38 (м, 2Н), 7,51 (м, 1Н), 7,58 (с, 1Н), 8,22 (с, 1Н).
MC (m/z) MH+ (289), МН- (287).
С: 1-Бензофуран-5-ил-2-(5-пиридин-2-илпиримидин-2-ил)-2,3,4,9-тетрагидро-1Н-β-карболин получают способом, указанным в примере 12.
1H-ЯМР 300 МГц (CDCl3) δ 3,00 (м, 2Н), 3,40 (м, 1Н), 5,11 (м, 1Н), 6,65 (с, 1Н), 7,15˜8,00 (м, 12Н), 8,61 (м, 1Н), 8,91 (м, 1Н), 8,22 (с, 2Н).
MC (m/z) MH+ (444), МН- (442).
D: 1-(5-Бензофурил)-2,3,4,9-тетрагидро-2-[5-(2-пиридинил)-2-пиримидинил]-1H-β-карболин (30 мг, 0,06764 ммоль) и КО-трет-Bu (12,9 мг, 0,115 ммоль) перемешивают в ДМФ (1 мл) в атмосфере газообразного O2 в течение 10 часов при комнатной температуре. Препаративная ТСХ (5% метанол в СН2Cl2) дает указанный в заголовке продукт в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CD3OD) δ 5,15 (м, 2Н), 6,55 (с, 1Н), 6,82˜8,98 (м, 15Н).
MC (m/z) 383 (МН+), 456 (МН-).
ПРИМЕР 82
3-(2,3-Дигидробензофуран-5-ил)-2-[5-(1-оксипиридин-2-ил)пиримидин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#125)
3-(2,3-Дигидро-5-бензофуранил)-1,2,3,4-тетрагидро-2-[5-(2-пиридинил)-2-пиримидинил]-(3R)-9Н-пирроло[3,4-b]хинолин-9-он (4,5 мг, 0,010 ммоль) и mCPBA (1,73 мг, 0,010 ммоль) перемешивают в ТГФ (2 мл). Для получения прозрачного раствора добавляют несколько капель ДМФ. Реакционную смесь перемешивают при комнатной температуре в течение 80 часов и затем при 60°С в течение 8 часов. Препаративная ТСХ (10% МеОН в СН2Cl2) дает указанный в заголовке продукт в виде не совсем белого твердого вещества с некоторым количеством выделенного исходного соединения.
1H-ЯМР 300 МГц (CD3OD) δ 3,12 (т, 2Н, J=8,8 Гц), 4,45 (т, 2Н, J=8,8 Гц), 6,35 (с, 1Н), 6,55 (д, 1Н), 7,21˜8,99 (м, 11Н).
МС (m/z) 458 (МН+), 456 (МН-).
ПРИМЕРЫ 83-86
1-(2,3-Дигидробензофуран-5-ил)-2-[5-(2,3-диметил-3Н-имидазол-4-ил)пиримидин-2-ил]-2,3,4,9-тетрагидро-1Н-β-карболин
2-(5-Бром-2-пиримидинил)-1-(2,3-дигидро-5-бензофуранил)-2,3,4,9-тетрагидро-1Н-β-карболин (0,45 г, 1,00 ммоль), 1,2-диметил-1Н-имидазол (0,18 г, 1,87 ммоль), Pd(OAc)2 (12 мг, 0,05 ммоль), PPh3 (26 мг, 0,1 ммоль) и К2СО3 (0,28 г, 2 ммоль) перемешивают в 3,5 мл ДМФ при 140°С в течение 14 часов. Смесь выливают в водный 10% раствор NaOH (50 мл). Полученный раствор экстрагируют СН2Cl2 (3×50 мл) и сушат над Na2SO4. Очистка препаративной ТСХ дает указанный в заголовке продукт в виде желтого порошка.
1H-ЯМР 300 МГц (CDCl3) δ 2,21 (с, 3Н), 2,35 (с, 3Н), 2,90 (м, 2Н), 3,10 (т, 2Н, J=8,8 Гц), 3,35 (м, 1Н), 4,52 (т, 2Н, J=8,8 Гц), 4,91 (м, 1Н), 6,68˜7,61 (м, 10Н).
МС (m/z) 463 (МН+), 461 (МН-).
Следующие соединения получали аналогично методике, описанной выше, с соответствующим выбором и заменой соответствующим образом замещенных реагентов.
2-[5-(3-Бензил-2-метил-3Н-имидазол-4-ил)пиримидин-2-ил]-1-(2,3-дигидробензофуран-5-ил)-2,3,4,9-тетрагидро-1Н-β-карболин
МС (m/z) 539 (МН+), 537 (МН-).
3-(2,3-Дигидробензофуран-5-ил)-2-[5-(2,3-диметил-3Н-имидазол-4-ил)пиримидин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#128)
1H-ЯМР 300 МГц (CD3OD) δ 3,08 (т, 2Н, J=9,5 Гц), 3,28 (с, 3Н), 3,50 (с, 3Н), 4,42 (т, 2Н, J=9,5 Гц), 5,02 (шир.с, 2Н), 6,24 (с, 1Н), 6,63 (м, 1Н), 6,84 (с, 1Н), 7,19 (м, 2Н), 7,31 (м, 1Н), 7,53 (с, 2Н), 8,35 (м, 3Н).
МС (m/z) 477 (МН+), 475 (МН-).
2-[5-(3-Бензил-2-метил-3Н-имидазол-4-ил)пиримидин-2-ил]-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#127)
1H-ЯМР 300 МГц (CD3OD) δ 1,90 (с, 3Н), 2,21 (с, 2Н), 3,12 (т, 2Н, J=8,8 Гц), 4,48 (т, 2Н, J=8,8 Гц), 5,12 (м, 2Н), 6,15 (с, 1Н), 6,61˜8,85 (м, 15Н).
МС (m/z) МН+ (553), МН- (551).
ПРИМЕР 87
3-[2,3-Дигидробензофуран-5-ил)-2-пиридин-2-ил-1,2,3,4-тетрагидропирроло[З,4-b]хинолин-9-он (#129)
3-(2,3-Дигидро-5-бензофуранил)-1,2,3,4-тетрагидро-9Н-пирроло[3,4-b]хинолин-9-он·HCl (0,30 г, 0,88 ммоль) и 2-бромпиридин (2 мл), Pd2dba3 (0,23 г, 0,25 ммоль), BINAP (0,47 г, 0,75 ммоль) и NaO-трет-Bu (0,66 г, 6,87 ммоль) перемешивают в 1,4-диоксане (4 мл) при 90°С в течение 1 часа. Полученную смесь концентрируют и затем фильтруют на пробке целита с CH2Cl2. Очистка препаративной ТСХ (5% СН3ОН/СН2Cl2) дает указанный в заголовке продукт в виде желтого твердого вещества.
1Н-ЯМР 300 МГц (CD3OD) δ 2,92 (т, 2Н, J=9,5 Гц), 4,40 (т, 2Н, J=9,5 Гц), 4,54 (д, 1Н, J=22 Гц), 4,85 (д, 1Н, J=22 Гц), 6,55 (м, 2Н), 7,10 (м, 3Н), 7,35 (м, 4Н), 8,02 (м, 1Н), 8,30 (д, 1Н, J=9,3 Гц).
МС (m/z) 382 (MH+), 380 (МН-).
ПРИМЕР 88
3-Бензо[1,3]диоксол-5-ил-2-(4-имидазол-1-илфенил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#133)
3-(1,3-Бензодиоксол-5-ил)-1,2,3,4-тетрагидро-9Н-пирроло[3,4-b]хинолин-9-он (30,6 мг, 0,1 ммоль), 1-(4-бромфенил)-1H-имидазол (22,3 мг, 0,1 ммоль), Pd2dba3 (4,6 мг, 0,005 ммоль), бифенил-2-ил-ди-трет-бутилфосфан (3,0 мг, 0,01 ммоль) и NaO-трет-Bu (14 мг, 0,14 ммоль) перемешивают в 1,4-диоксане (0,6 мл) при 89°С в течение 17 часов. Очистка препаративной ТСХ (5% CH3OH/CH2Cl2) дает указанный в заголовке продукт в виде желтого порошка.
1H-ЯМР 300 МГц (CD3OD) δ 4,70 (д, 1Н), 5,02 (д, 1Н), 5,48 (с, 2Н), 5,88 (с, 2Н), 6,75-8,32 (м, 14Н).
МС (m/z) MH+ (449), МН- (447).
ПРИМЕР 89
2-[2,3']Бипиридинил-6'-ил-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#134)
А. 2-(5-Бромпиридин-2-ил)-1-(2,3-дигидробензофуран-5-ил)-2,3,4,9-тетрагидро-1Н-β-карболин
1-(2,3-Дигидро-5-бензофуранил)-2,3,4,9-тетрагидро-1Н-β-карболин (11,6 г, 40 ммоль), 2,5-дибромпиридин (10,42 г, 44 ммоль), Pd2dba3 (1,465 г, 1,6 ммоль, dppp (1,32 г, 3,2 ммоль) и NaO-трет-Bu (5,38 г, 56 ммоль) перемешивают в 60 мл ДМФ при 80°С в течение 3 дней. Реакционную смесь фильтруют через пробку целита с CH2Cl2. Реакционную смесь затем концентрируют, неочищенную смесь затем загружают в колонку Foxy (110 г силикагеля) и элюируют смесью этилацетат/гексан (3:7). Продукт кристаллизуется в пробирках. Продукт концентрируют и затем перекристаллизовывают из ТГФ, получая продукт в виде желтых кристаллов.
1H-ЯМР 400 МГц (ТГФ-d8) δ 0,91 (м, 1Н), 1,15 (м, 1Н), 1,25 (т, 2Н, J=9,5 Гц), 1,60 (м, 1Н), 2,31 (м, 1Н), 2,60 (т, 2Н, J=9,5 Гц), 4,75 (д, 1Н, J=7,6 Гц), 5,02 (д, 1Н, J=7,6 Гц), 5,10˜5,28 (м, 4Н), 5,380 (м, 2Н), 5,58 (м, 1Н), 5,72 (м, 1Н), 6,28 (с, 1Н), 8,12 (с, 1Н).
MC (m/z) 446, 448 (МН+), 444, 446 (МН-).
В: 2-[2,3']Бипиридинил-6'-ил-1-(2,3-дигидробензофуран-5-ил)-2,3,4,9-тетрагидро-1Н-β-карболин
Продукт указанной выше стадии А (0,4 г, 0,896 ммоль), 2-трибутилстаннанилпиридин (0,8 г, 2,17 ммоль) и Pd(PPh3)4 (0,12 г, 0,104 ммоль) перемешивают в 1,4-диоксане (5 мл) при 88°С в течение 24 час. Реакционную смесь фильтруют через пробку целита с СН2Cl2 и затем концентрируют до небольшого объема. Препаративная ТСХ (смесь 3:7 этилацетат/гексан; затем 5% CH3OH/CH2Cl2) дает продукт в виде желтого твердого вещества.
1H-ЯМР (CDCl3) δ 2,82 (м, 1Н), 3,10 (м, 3Н), 3,58 (м, 1Н), 4,31 (м, 1Н), 4,53 (т, 2Н, J=9,5 Гц), 6,71 (д, 1Н, J=7,6 Гц), 6,85 (д, 1Н, J=7,6 Гц).
MC (m/z) 445 (МН+), 443 (МН-).
С: 2-[2,3']Бипиридинил-6'-ил-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#134)
По методике, описанной в примере 19, с соответствующим выбором и заменой реагентов получают указанный в заголовке продукт в виде твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 3,16 (т, 2Н, J=9,5 Гц), 4,43 (т, 2Н, J=9,5 Гц), 4,98˜5,20 (м, 2Н), 6,12 (с, 1Н), 6,60˜8,70 (15Н).
MC (m/z) 459 (МН+), 457 (MH-).
ПРИМЕР 90
3-(2,3-Дигидробензофуран-5-ил)-2-[5-(3-метил-3Н-имидазол-4-ил)пиридин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#137)
А. 2-Хлор-5-(3-метил-3Н-имидазол-4-ил)пиридин
2-Хлор-4-иодпиридин (0,239 г, 1 ммоль), 1-метил-1Н-имидазол (0,41 г, 5 ммоль), Pd(OAc)2 (22,5 мг, 0,1 ммоль), PPh3 (53 мг, 0,2 ммоль) и Cs2СО3 (0,326 г, 1 ммоль) перемешивают в ДМФ (3 мл) при 120°С в течение 6 часов. Очистка препаративной ТСХ дает продукт в виде масла, содержащий 1-метил-1Н-имидазол. Продукт используют на следующей стадии без дополнительной очистки.
1H-ЯМР (CDCl3) δ 3,68 (с, 3Н), 7,19 (с, 1Н), 7,27 (с, 1Н), 7,56 (с, 1Н), 7,68 (дд, 1Н), 8,45 (д, 1Н).
МС (m/z) MH+ (194).
В: 3-(2,3-Дигидробензофуран-5-ил)-2-[5-(3-метил-3Н-имидазол-4-ил)пиридин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#137)
3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (0,127 г, 0,372 ммоль), 2-хлор-5-(3-метил-3Н-имидазол-4-ил)пиридин (0,06 г, 0,31 ммоль), Pd(OAc)2 (3,5 мг, 0,0155 ммоль), бифенил-2-илдициклогексилфосфан (5,43 мг, 0,0155 ммоль) и NaO-трет-Bu (0,104 г, 1,085 ммоль) перемешивают в 1,4-диоксане (0,6 мл) при 90°С. Очистка препаративной ТСХ (5% МеОН в СН2Cl2) дает продукт в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CDCl3) δ 3,12 (т, 2Н), 3,60 (с, 3Н), 3,50 (т, 2Н), 5,12 (м, 2Н), 6,08 (с, 1Н), 6,70 (м, 2Н), 7,20˜8,55 (м, 10Н).
МС (m/z) MH+ (462), МН- (460).
ПРИМЕР 91
2-[5-(3-Бензил-3Н-имидазол-4-ил)пиридин-2-ил]-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#138)
А: 5-(3-Бензил-3Н-имидазол-4-ил)-2-хлорпиридин
По методике, описанной в примере 90, стадия А, с соответствующим выбором и заменой реагентов получают продукт в виде твердого вещества.
1Н-ЯМР (CDCl3) δ 5,15 (с, 2Н), 6,86˜8,30 (м, 10Н).
МС (m/z) MH+ (270).
В: По методике, описанной в примере 90, стадия В, с соответствующим выбором и заменой реагентов получают продукт в виде твердого вещества.
1H-ЯМР 300 МГц (CD3OD) δ 3,12 (т, 2Н), 3,60 (м, 2Н), 4,55 (т, 2Н), 5,10 (м, 2Н), 6,05 (с, 1Н), 6,45˜8,54 (м, 12Н).
МС (m/z) МН+ (538), МН- (536).
ПРИМЕР 92
3-(2,3-Дигидробензофуран-5-ил)-2-пиридин-2-ил-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он (#136)
3-(2,3-Дигидро-5-бензофуранил)-1,2,3,4-тетрагидро-(3R)-9Н-пирроло[3,4-b]хинолин-9-он·HCl (0,0341 г, 0,1 ммоль), 2-иодпиридин (0,0341 г, 0,2 ммоль), Pd2dba3 (22,9 мг, 0,025 ммоль), BINAP (46,7 мг, 0,075 ммоль) и NaO-трет-Bu (58 мг, 0,6 ммоль) перемешивают в 1,4-диоксане (0,8 мл) при 50°С в течение 3 часов. Очистка препаративной ТСХ (5% метанол/СН2Cl2) дает продукт в виде желтого твердого вещества.
1H-ЯМР 300 МГц (CD3OD) δ 2,92 (т, 2Н, J=9,5 Гц), 4,40 (т, 2Н, J=9,5 Гц), 4,54 (д, 1Н, J=22 Гц), 4,85 (д, 1Н, J=22 Гц), 6,55 (м, 2Н), 7,10 (м, 3Н), 7,35 (м, 4Н), 8,02 (м, 1Н), 8,30 (д, 1Н, J=9,3 Гц).
МС (m/z) МН+ (382), MH- (380).
ВЭЖХ с отделением примеси: хиральная фаза, OD, метанол, 25°С, tr=5,201 мин.
ПРИМЕР 93
3-(2,3-Дигидробензофуран-5-ил)-2-[5-(3Н-имидазол-4-ил)пиридин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он
Перемешиваемый раствор 2-[5-(3-бензил-3Н-имидазол-4-ил)пиридин-2-ил]-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-она (0,005 ммоль, 1 эквивалент), полученного, как в примере 91, и п-толуолсульфонилгидразид (0,25 ммоль, 50 эквивалентов) в СН3ОН (3 мл) приблизительно при 80°С добавляют к раствору ацетата натрия (0,5 ммоль, 100 эквив.) в Н2О (2 мл) на протяжении приблизительно 2 час. Смесь перемешивают еще в течение приблизительно 3 час приблизительно при 80°С, затем охлаждают приблизительно до 25°С и растворитель выпаривают. Остаток растворяют в СН2Cl2 (20 мл), промывают насыщенным водным NaCl (10 мл), сушат (Na2SO4) и концентрируют, получая указанный в заголовке продукт.
ПРИМЕР 94
3-(2,3-Дигидробензофуран-5-ил)-2-[5-(2-метил-3Н-имидазол-4-ил)пиримидин-2-ил]-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он
По методике, описанной в примере 93, 2-[5-(3-бензил-2-метил-3Н-имидазол-4-ил)пиримидин-2-ил]-3-(2,3-дигидробензофуран-5-ил)-1,2,3,4-тетрагидропирроло[3,4-b]хинолин-9-он, полученный как в примере 86, подвергают взаимодействию, получая указанное в заголовке соединение.
ПРИМЕР 95
ИСПЫТАНИЕ IN VITRO
Анализ циклонуклеотидфосфодиэстеразы (PDE)
Выделение PDEV
PDEV выделяли из тканей кроликов и человека по протоколу, описанному Boolell et al. [Boolell, M., Allen, M.J., Ballard., S.A., Gelo-Aktee, S., Muirhead, G.J., Naylor, A.M., Osterloh, I.Н., and Gingell, С) в International Journal of Impotence Research 1996 8, 47-52, с небольшими модификациями.
Кратко, ткани кролика или человека гомогенизируют в охлажденном льдом буферном растворе, содержащем 20 мМ HEPES (рН 7,2), 0,25 M сахарозу, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид (PMSF). Гомогенаты центрифугируют при 100000 g в течение 60 минут при 4°С. Супернатант фильтруют через фильтр 0,2 мкМ и загружают в анионообменную колонку Pharmacia Mono Q (объем гранул 1 мл), которая была уравновешена 20 мМ HEPES, 1 мМ ЭДТА и 0,5 мМ PMSF. После вымывания несвязанных белков фермент элюируют с линейным градиентом 100-600 мМ NaCl в том же самом буфере (всего от 35 до 50 мл, в зависимости от ткани. Ферменты из скелетной мышцы, объемного кавернозного тела, сетчатки, сердца и тромбоцитов элюируют 35, 40, 45, 50 и 50 мл соответственно). Опыты на колонке выполняют при объемном расходе 1 мл/мин и собирают 1 мл фракции. Фракции, обладающие различной активностью PDE, объединяли по отдельности и использовали в последующих исследованиях.
Измерение ингибирования PDEV
Анализ PDE проводили, как описано Thompson and Appleman в Biochemistry, 1971 10, 311-316 с небольшими модификациями, как указано ниже.
Анализы были приспособлены для 96-луночного формата. Ферменты анализировали в 5 мМ MgCl2, 15 мМ Трис HCl (рН 7,4), 0,5 мг/мл альбумина бычьей сыворотки, 1 мкМ цГМФ или цАМФ, 0,1 мкКи [3Н]-цГМФ или [3Н]-цАМФ и 2-10 мкл элюата из колонки. Общий объем для анализа был 100 мкм. Реакционную смесь инкубировали при 30°С в течение 30 минут. Реакцию останавливали кипячением в течение 1 минуты и затем охлаждали на льду. Образовавшиеся [3Н]-5'-мононуклеотиды далее превращали в незаряженные [3Н]-нуклеозиды добавлением 25 мкл (1 мг/мл) яда змеи (Ophiophagus Hannah) и инкубированием при 30°С в течение 10 минут. Реакцию останавливали добавлением 1 мл суспензии смолы Bio-Rad AG1-X2 (1:3). Все заряженные нуклеотиды были связаны смолой и только незаряженные [3Н]-нуклеозиды оставались в супернатанте после центрифугирования. Аликвоту 200 мкл отбирали и считали сцинтилляцией. Активность PDE выражали как пкмоль гидролизованного циклического нуклеотида/мин/мл препарата фермента.
Исследования ингибиторов проводили в буфере для анализа с конечной концентрацией ДМСО 10%. В этих условиях гидролиз продукта повышается с увеличением времени и концентрации фермента линейным образом.
ПРИМЕР 96
Определение in vitro Ki ингибиторов фосфодиэстеразы:
Анализы были приспособлены для 96-луночного формата. Фосфодиэстеразу анализировали в 5 мМ MgCl2, 15 мМ Трис HCl (рН 7,4), 0,5 мг/мл альбумина бычьей сыворотки, 30 нМ 3H-цГМФ и при различных концентрациях испытуемого соединения. Количество используемого для реакции фермента было таким, чтобы менее чем 15% первоначального субстрата превращалось во время анализа. Для всех измерений испытуемое соединение растворяли и разводили в 100% ДМСО (2% ДМСО в анализе). Общий объем для анализа составлял 100 мкл. Реакционную смесь инкубировали при 30°С в течение 90 минут. Реакцию останавливали кипячением в течение 1 минуты и затем немедленно охлаждали переносом на ледяную баню. В каждую лунку затем добавляли 25 мкл (1 мг/мл) змеиного яда [Ophiophagus Hannah) и реакционную смесь инкубировали при 30°С в течение 10 минут. Реакцию останавливали добавлением 1 мл суспензии смолы Bio-Rad AG1-X2 (1:3). Отбирали аликвоту 200 мкл и считали с использованием сцинтилляционного счетчика.
Ингибирование в % максимального превращения субстрата (ферментом в отсутствие ингибитора) вычисляли для каждой концентрации испытуемого соединения. С использованием нелинейного регрессионного анализа GraphRadPrism (сигмоидальная функция доза-ответ) строили кривые % ингибирования в зависимости от log концентрации испытуемого соединения для определения IC50. В условиях, когда концентрация субстрата «Кm фермента (Km=концентрации субстрата, при которой достигается половина максимальной скорости фермента), Ki является эквивалентным величине IC50.
По методикам, описанным выше, получены соединения, перечисленные в таблицах 1-6. PDEV-ингибирующие активности для данных соединений представлены либо как IC50 (мкМ), как процентное ингибирование при данной концентрации испытуемого соединения, либо как величина Ki в приведенных ниже таблицах. Если не оговорено особо, PDEV-ингибирующие активности измеряли с использованием ткани человека. Сокращение «стерео» относится к стереогенной конфигурации, сокращение «Rac» обозначает рацемическую смесь.
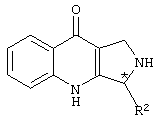
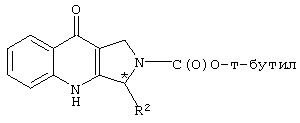
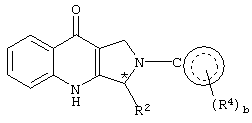
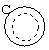
(нМ)
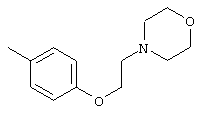
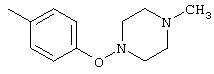
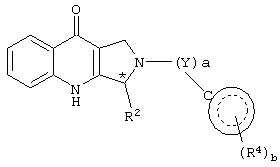

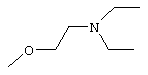
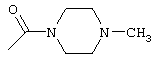


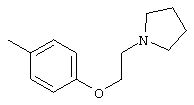
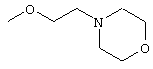

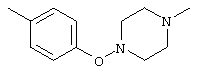
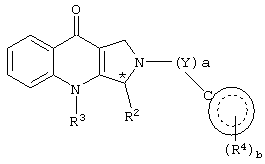
(в виде рацемата)
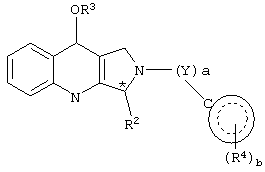
(в виде рацемата)
ПРИМЕР 97
ИСПЫТАНИЕ IN VIVO
По методике, описанной Carter et al. (Carter, A.J., Ballard, S.A., and Naylor, A.M.) в The Journal of Urology 1998, 160, 242-246, соединения, перечисленные в таблице 7, испытывали для определения эффективности In vivo с результатами, приведенными в таблице ниже.
ПРИМЕР 98
В качестве частного примера пероральной композиции 100 мг соединения примера 21 объединяют с достаточно мелко измельченной лактозой с получением общего количества от 580 до 590 мг для заполнения твердой гелевой капсулы размера О.
Хотя приведенное выше описание объясняет принципы настоящего изобретения вместе с примерами, представленными с целью иллюстрации, должно быть понятно, что на практике изобретение включает все обычные варианты, адаптации и/или модификации, которые входят в объем следующих пунктов формулы изобретения и их эквивалентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕТА-КАРБОЛИНА, ОБЛАДАЮЩИЕ ДЕЙСТВИЕМ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ИНГИБИРОВАНИЯ ДЕЙСТВИЯ ФОСФОДИЭСТЕРАЗЫ (ВАРИАНТЫ) И СПОСОБ УВЕЛИЧЕНИЯ КОНЦЕНТРАЦИИ ЦГМФ | 2001 |
|
RU2271358C2 |
| ЗАМЕЩЕННЫЕ ПИРИМИДИНТИОАЛКИЛЬНЫЕ ИЛИ АЛКИЛЭФИРНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИНГИБИРОВАНИЯ ОБРАТНОЙ ТРАНСКРИПТАЗЫ ВИРУСОВ | 1996 |
|
RU2167155C2 |
| N-ГИДРОКСИ-БЕНЗАМИДЫ ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2577861C2 |
| ТИЕНОПИРИМИДИНДИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2002 |
|
RU2294937C9 |
| ИНГИБИТОРЫ КИНАЗЫ | 2013 |
|
RU2637944C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИЗОТИАЗОЛ-ПИРИДОН АЦЕТИДИНИЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2041226C1 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ АКТИВНОСТИ КАТЕПСИНА S | 2001 |
|
RU2278863C2 |
| НОВЫЕ ФОСФАТНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2617682C2 |
| ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ N-ОКСИДЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2113437C1 |
| ИНДАЗОЛИЛИЗОКСАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ТАКИХ КАК ЗЛОКАЧЕСТВЕННОЕ НОВООБРАЗОВАНИЕ | 2020 |
|
RU2836662C2 |
Изобретение относится к органической химии и может найти применение в медицине. Описывается соединение общей формулы I или II
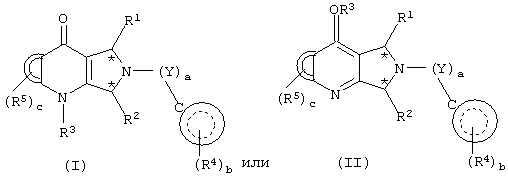
где R1 представляет водород; R2 выбран из группы, состоящей из арила, и гетероарила; R3 выбран из группы, состоящей из галогена, нитро, циано, C1-С6алкила, C1-С6алкокси, трифторметила, трифторметокси, NH2, NH(С1-С6алкил) и N(С1-С6алкил)2; b равно целому числу от 0 до 4; R4 независимо выбран из группы, состоящей из галогена, гидрокси, карбокси, оксо, C1-С6алкила, C1-С6алкокси, C1-С6алкоксикарбонила, фенила, (где фенильная группа может быть необязательно замещена одним-тремя заместителями, независимо выбранными из RD), фенилсульфонила, гетероарила (где гетероарил может быть необязательно замещен одним-тремя заместителями, независимо выбранными из RD), гетероциклоалкила, NH2, NHRA, N(RA)2,
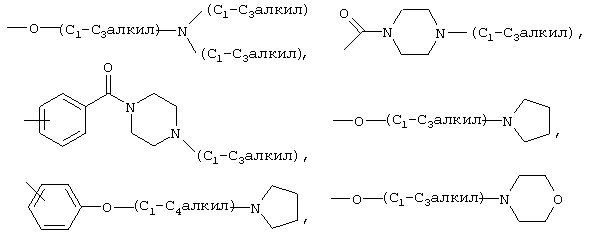
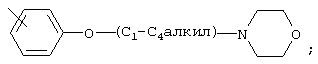
где каждый RD независимо выбран из галогена, гидрокси, карбокси, оксо, C1-C4алкила, C1-C4алкилтио, гидроксиC1-C4алкила, C1-C4алкокси, C1-C4алкоксикарбонила, C1-C4алкилкарбонила, трифторметила, трифторметокси, NH2, NHRA N(RA)2, C(O)N(RA)2, SO2N(RA)2, ацетиламино, нитро, циано, формила, C1-С6алкилсульфонила, карбоксиC1-С6алкила и аралкила; с равно 0; а равно целому числу от 0 до 1; Y выбран из группы, состоящей из остатка -C1-C4алкил-, -С(O)-,-(С2-С6алкенил)карбонил-, -карбонил(С1-С6алкил)-, -C(S)-, -С(O)NH-(С1-С6алкил)-, -С(O) (С3-С7циклоалкил)- и (С3-С7циклоалкил)-С(O)-;
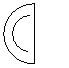 представляет фенил;
представляет фенил;
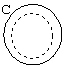 выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
при условии, что когда R1 представляет водород, R3 представляет водород, b равно 0, с равно 0, а равно 1, Y представляет -СН2-,
 представляет фенил и
представляет фенил и
 представляет фенил, тогда R2 не является триметоксифенилом; и его фармацевтически приемлемые соли. Также описываются фармацевтическая композиция, предназначенная для ингибирования фосфодиэстеразы, включающая фармацевтически приемлемый носитель и соединение по п.1, способ получения фармацевтической композиции, способы лечения половой дисфункции с использованием соединения по п.1 или фармацевтической композиции, способ повышения концентрации цГМФ в ткани полового члена и способ лечения состояния, при котором ингабирование фосфодиэстеразы оказывает благотворное действие. Технический результат - получены новые соединения, обладающие полезньми биологическими свойствами. 8 н. и 9 з.п. ф-лы, 7 табл.
представляет фенил, тогда R2 не является триметоксифенилом; и его фармацевтически приемлемые соли. Также описываются фармацевтическая композиция, предназначенная для ингибирования фосфодиэстеразы, включающая фармацевтически приемлемый носитель и соединение по п.1, способ получения фармацевтической композиции, способы лечения половой дисфункции с использованием соединения по п.1 или фармацевтической композиции, способ повышения концентрации цГМФ в ткани полового члена и способ лечения состояния, при котором ингабирование фосфодиэстеразы оказывает благотворное действие. Технический результат - получены новые соединения, обладающие полезньми биологическими свойствами. 8 н. и 9 з.п. ф-лы, 7 табл.
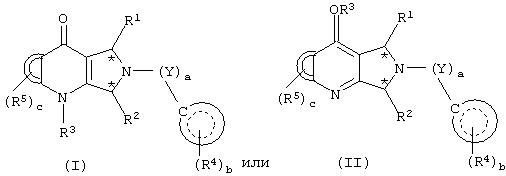
где
R1 представляет водород;
R2 выбран из группы, состоящей из арила и гетероарила;
R3 выбран из группы, состоящей из галогена, нитро, циано, C1-С6алкила, C1-С6алкокси, трифторметила, трифторметокси, NH2, NH(С1-С6алкил) и N(С1-С6алкил)2;
b равно целому числу от 0 до 4;
R4 независимо выбран из группы, состоящей из галогена, гидрокси, карбокси, оксо, C1-С6алкила, C1-С6алкокси, C1-С6-алкоксикарбонила, фенила (где фенильная группа может быть необязательно замещена одним-тремя заместителями, независимо выбранными из RD), фенилсульфонила, гетероарила (где гетероарил может быть необязательно замещен одним-тремя заместителями, независимо выбранными из RD), гетероциклоалкила, NH2, NHRA, N(RA)2,
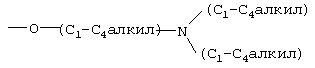
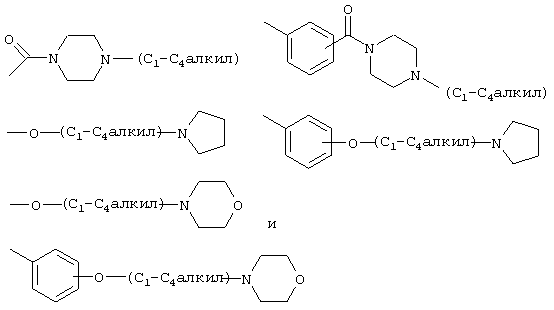
где каждый RD независимо выбран из галогена, гидрокси, карбокси, оксо, С1-С4алкила, С1-С4алкилтио, гидроксиС1-С4алкила, С1-С4алкокси, С1-С4алкоксикарбонила, С1-С4алкилкарбонила, трифторметила, трифторметокси, NH2, NHRA, N(RA)2, C(O)N(RA)2, SO2N(RA)2, ацетиламино, нитро, циано, формила, C1-С6алкилсульфонила, карбоксиС1-С6алкила и аралкила;
с равно 0;
а равно целому числу от 0 до 1;
Y выбран из группы, состоящей из остатка -С1-С4алкил-, -С(О)-, -(С2-С6алкенил) карбонил-, -карбонил (C1-С6алкил)-, -C(S)-, -C(O)NH-(C1-С6алкил)-, -С(O)(С3-С7циклоалкил)- и (С3-С7циклоалкил)-С(О)-;
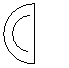 представляет фенил;
представляет фенил;
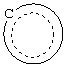 выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
при условии, что, когда R1 представляет водород, R3 представляет водород, b равно 0, с равно 0, а равно 1, Y представляет -СН2-,  представляет фенил и
представляет фенил и  представляет фенил, тогда R2 не является триметоксифенилом;
представляет фенил, тогда R2 не является триметоксифенилом;
и его фармацевтически приемлемые соли.
R1 представляет водород;
R2 выбран из группы, состоящей из фенила или гетероарила;
R3 представляет С1-С4алкил;
b равно целому числу от 0 до 4;
R4 выбран из группы, состоящей из галогена, гидрокси, карбокси, оксо, C1-С3алкила, C1-С3алкокси, C1-С3алкоксикарбонила, фенила (где фенил может быть необязательно замещен одним или двумя заместителями, выбранными из гидрокси, карбокси, С1-С4алкила, С1-С4алкилтио, гидроксиС1-С4алкила, С1-С4алкокси, С1-С4алкилоксикарбонила, C(O)N(RA)2, трифторметила, трифторметокси, амино, (С1-С4алкил)амино, ди(С1-С4алкил) амино, нитро, циано или формила), гетероарила (где гетероарил может быть необязательно замещен одним или двумя заместителями, выбранными из гидрокси, карбокси, оксо, C1-С3алкила, C1-С3алкокси, C1-С3алкилоксикарбонила, С(O)N(RA)2, трифторметила, трифторметокси, амино, нитро, C1-С3алкилкарбонила или C1-С4аралкила), гетероциклоалкила,
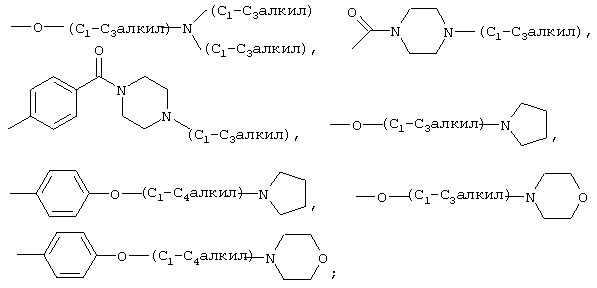
с равно 0;
а равно целому числу от 0 до 1;
Y выбран из группы, состоящей из остатков -С1-С4алкил-, -С(S)-, -С(О)-, -С(O)-(С1-С4алкил)-, -С(О)-(C2-С4алкенил)-, -С(О)-(С3-С7циклоалкил)- и -С(O)NH-(C1-С3-алкил)-;
 представляет фенил;
представляет фенил;
 выбран из группы, состоящей из фенила, гетероарила и гетероциклоалкила;
выбран из группы, состоящей из фенила, гетероарила и гетероциклоалкила;
и его фармацевтически приемлемые соли.
R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 3,4-диметоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 5-бензофурила, 5-инданила и 3-тиенила;
R3 представляет метил;
R4 выбран из группы, состоящей из брома, гидрокси, карбокси, оксо, метила, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-цианофенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-формилфенила, 4-метилтиофенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-оксо-2-пиридинила, 3-тиенила, 2-фурила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 5-(1-метилимидазолила, 5-(1-бензилимидазолила), 3,4-метилендиоксифенила,
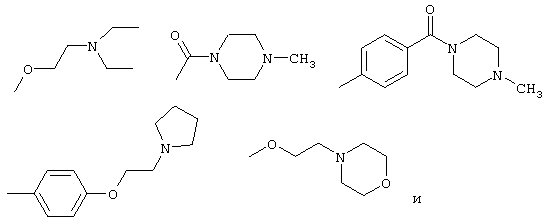
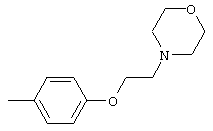
Y выбран из группы, состоящей из -СН2-, -C(S)-, -С(O)-, -С(O)-СН2СН2-, -С(O)-СН=СН-, C(O)NH-CH2-, -С(O)-циклопропила и -С(O)СН2-;
 выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила, 1-имидазолила, 2-имидазолила, 2-тиазолила и 2-оксабицикло[2.2.1]гептанила;
выбран из группы, состоящей из фенила, 2-фурила, 2-бензо(b)фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила, 1-имидазолила, 2-имидазолила, 2-тиазолила и 2-оксабицикло[2.2.1]гептанила;
и его фармацевтически приемлемые соли.
R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 3-тиенила, 5-инданила и 5-бензофурила;
b равно целому числу от 0 до 1;
R4 выбран из группы, состоящей из 5-брома, 2-гидрокси, 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-цианофенила, 4-формилфенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, 2-фурила, 3-тиенила, N-оксо-2-пиридинила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 3,4-метилендиоксифенила,

Y выбран из группы, состоящей из -С(О)-, -С(О)-CH2CH2-, и -С(О)-циклопропила;
 выбран из группы, состоящей из фенила, 2-фурила, 2-бензо[b]фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила и 2-тиазолила;
выбран из группы, состоящей из фенила, 2-фурила, 2-бензо[b]фурила, 2-пиримидинила, 2-пиридинила, 3-пиридинила, 4-пиридинила и 2-тиазолила;
и его фармацевтически приемлемые соли.
R2 выбран из группы, состоящей из 3,4-метилендиоксифенила, 5-(2,3-дигидробензофурила), 3,4-дигидробензо[1,4]диоксин-6-ила, 3-тиенила, 5-инданила и 5-бензофурила;
R4 выбран из группы, состоящей из 5-брома, 2-гидрокси, 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-гидроксиметилфенила, 4-карбоксифенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 4-метоксикарбонилфенила, 3-трифторметилфенила, 4-аминофенила, 4-диметиламинофенила, 3-нитрофенила, 4-нитрофенила, 4-цианофенила, 4-формилфенила, бензилокси, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-оксо-2-пиридинила, 3-тиенила, 2-фурила, 1-имидазолила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила), 3,4-метилендиоксифенила,

Y представляет -С(О)-;
и его фармацевтически приемлемые соли.
R4 выбран из группы, состоящей из 6-гидрокси, 4-карбокси, фенила, 4-гидроксифенила, 3-гидроксиметилфенила, 4-метилфенила, 4-метилтиофенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 3-трифторметилфенила, 3-нитрофенила, 4-нитрофенила, 2-пиридинила, 3-пиридинила, 4-пиридинила, N-оксо-2-пиридинила, 3-тиенила, 5-(1-бензил-2-метилимидазолила), 5-(1,2-диметилимидазолила),
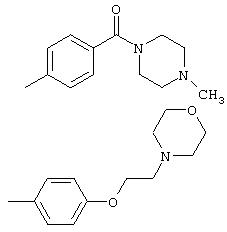
и его фармацевтически приемлемые соли.
R2 выбран из группы, состоящей из 3,4-метилендиоксифенила и 5-(2,3-дигидробензофурила);
R4 выбран из группы, состоящей из гидрокси, 4-метилфенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонила, 3-трифторметилфенила, 4-нитрофенила 2-пиридинила, 3-пиридинила, 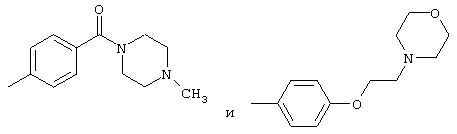
Y представляет -С(О)-;
 выбран из группы, состоящей из 2-фурила, 2-бензо(b)фурила, 4-пиридинила, 2-пиримидинила и 2-тиазолила;
выбран из группы, состоящей из 2-фурила, 2-бензо(b)фурила, 4-пиридинила, 2-пиримидинила и 2-тиазолила;
и его фармацевтически приемлемые соли.
1,2,3,4-тетрагидро-2-[(4-пиридинил)метилоксикарбонил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она;
1,2,3,4-тетрагидро-2-[5-(2-пиридинил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
1,2,3,4-тетрагидро-2-[5-(4-метоксифенил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(1-(4-метил)пиперазинилкарбонил)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-она;
1,2,3,4-тетрагидро-2-[2,3'-бипиридин]-6'-ил-3-(2,3-дигидро-5-бензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
1,2,3,4-тетрагидро-2-(2-пиридинил)-3-(2,3-дигидро-5-бензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
и их фармацевтически приемлемых солей.
R-1,2,3,4-тетрагидро-2-[5-(3,4-диметоксифенил)пиримидин-2-ил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b] хинолин-9-она;
R-1,2,3,4-тетрагидро-2-[(4-пиридинил)метилоксикарбонил]-3-(3,4-метилендиоксифенил)-9Н-пирроло[3,4-b]хинолин-9-она;
R-1,2,3,4-тетрагидро-2-[5-(2-пиридинил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
R-1,2,3,4-тетрагидро-2-[5-(4-метоксифенил)пиримидин-2-ил]-3-(3,4-дигидробензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
R-1,2,3,4-тетрагидро-3-(3,4-метилендиоксифенил)-2-(5-(4-(1-(4-метил)пиперазинилкарбонил)фенил)фуроил)-9Н-пирроло[3,4-b]хинолин-9-она;
R-1,2,3,4-тетрагидро-2-(2-пиридинил)-3-(2,3-дигидро-5-бензофуранил)-9Н-пирроло[3,4-b]хинолин-9-она;
и их фармацевтически приемлемых солей.

где
R1 представляет водород;
R2 выбран из группы, состоящей из арила и гетероарила;
R3 выбран из группы, состоящей из водорода, C1-С6алкила, C1-С6алкилкарбонила, С2-С6алкенилкарбонила и С2-С6алкинилкарбонила;
b равно целому числу от 0 до 4;
R4 независимо выбран из группы, состоящей из галогена, гидрокси, карбокси, фенила, фенилсульфонила, гетероарила, NH2, NHRA, N(RA)2,
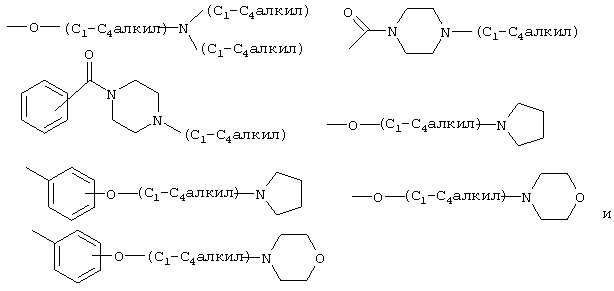
где каждый RD независимо выбран из галогена, гидрокси, карбокси, С1-С4алкила, С1-С4алкокси, С1-С4алкилоксикарбонила, С1-С4алкилкарбонила, трифторметила, трифторметокси, NH2, NHRA, N(RA)2, C(O)N(RA)2, SO2N(RA)2, ацетиламино, нитро, циано, формила, C1-С6алкилсульфонила и карбоксиС1-С6алкила;
с равно 0;
а равно целому числу от 0 до 1;
Y выбран из группы, состоящей из остатка -C1-С6алкил-, -С(О)-, -(С2-С6алкенил) карбонил-, -карбонил(C1-С6алкил)-, -C(S)-, -C(O)NH-(C1-С6алкил)-, -С(О)(С3-С7циклоалкил)- и -(С3-С7циклоалкил)-С(О)-;
 представляет фенил;
представляет фенил;
 выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
выбран из группы, состоящей из фенила, гетероарила и циклоалкила;
при условии, что, когда R1 представляет водород, R3 представляет водород, b равно 0, с равно 0, а равно 1, Y представляет -СН2-,  представляет фенил и
представляет фенил и  представляет фенил, тогда R2 не может быть триметоксифенилом;
представляет фенил, тогда R2 не может быть триметоксифенилом;
и его фармацевтически приемлемые соли.
| US 6043252 B1, 28.03.2000 | |||
| ПРОИЗВОДНЫЕ ПИРРОЛХИНОЛИНОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2129554C1 |
| ПРОИЗВОДНОЕ 1,3-ДИГИДРО-2H-ИМИДАЗО/4,5-B/ХИНОЛИН-2-ОНА В КАЧЕСТВЕ ИНГИБИТОРА ФОСФОДИЭСТЕРАЗЫ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ ДЛЯ НЕГО, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1992 |
|
RU2127273C1 |
Авторы
Даты
2006-01-10—Публикация
2001-05-03—Подача