Пиримидин-тиоалкильные и алкилэфирные производные формулы IA могут использоваться при лечении пациентов, которые являются ВИЧ-инфицированными, независимо от того, проявляют ли они симптомы СПИД в данное время. Пиримидин-тиоалкильные и алкилэфирные производные формулы IB могут использоваться при получении пиримидин-тиоалкильных и алкилэфирных производных соединений формулы IA.
2. Описание уровня техники
Пиримидин-тиоалкильные пиридиновые производные по патенту США 5025016 (и EP 124630) соответствуют общей формуле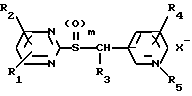
в которой R1 - R4 независимо друг от друга представляют водород, низший алкил, галоген, амино- или гидроксигруппы, R5 представляет свободную электронную пару или низшую алкильную группу, атом галогена, m имеет значение 0 или 1, при этом пиримидин-тиоалкильная группа присоединена по 2-, 3- или 4- положению пиридинового кольца, и их терапевтически совместимым кислотно-аддитивным солям. Соединения, как утверждается, проявляют неожиданно повышенную бронхосекрето-литическую и муколитическую активность, а также, как обнаружено, проявляют противовоспалительную активность.
В J. Med. Chem. 1987, 30, 547-551 описаны различные 2-[(пиридинилметил)тио] пиримидиновые производные и их влияние на бронхосекретолитические свойства на фенольной эритроцитной скриннинговой модели на мышах в сравнении с известным лекарственным средством амброксолом.
В EP 477778 (Derwent 92-106190/14) описаны различные производные бензола, пиридина и пиримидина в качестве ингибиторов ACAT ферментов для лечения атеросклероза и заболевания сосудов мозга.
В J. Org. Chem, 1954, 19, 1793-1801 описаны пиримидиновые производные, включая 2-бензилмеркапто-4-амино-6-пиримидинол, 2-бензилмеркапто-4-амино-6-хлорпиримидин, 2-бензилмеркапто-4-амино-6-диэтиламинопиримидин, а также аналоги 6-диметиламинопурина.
В патенте Великобритании 744867 (CA 51:2063i) описаны различные 2-R'-S-6-RR'N-замещенные 4-аминопиримидины.
Как установлено, от одного до полутора миллионов людей в Соединенных Штатах инфицированы ретровирусом человека, вирусом иммунодефицита человека типа I (ВИЧ-1), который является этиологическим агентом приобретенного синдрома иммунодефицита, СПИДа, смотри Science, 661-662 (1986). Из тех, кто инфицирован, как оценивается, у двухсот пятидесяти тысяч людей, разовьется СПИД в ближайшие пять лет, смотри Science, 1352-1357 (1985). 20 марта 1987 года Администрация по продуктам питания и лекарственным средствам США (FDA) одобрила использование соединения AZT (зидовудин) для лечения больных СПИДом пациентов с только что выявленной начальной стадией плазмоклеточной бронхопневмонии, больных СПИДом пациентов с состояниями иными, чем плазмоклеточная бронхопневмония, или пациентов, инфицированных вирусом, с абсолютным отсчетом CD4 менее чем 200/мм3 в периферической крови. AZT является известным ингибитором обратной транскриптазы вирусов, фермента, необходимого для репликации вируса иммунодефицита человека.
В патенте США 4724232 описан способ лечения людей, имеющих приобретенный синдром иммунодефицита, при котором используется 3'-азидо-3'-деокситимидин (азидотимидин, AZT).
Из литературы известно, что некоторые антибиотики и полианионные красители ингибируют обратную транскриптазу ретровирусов.
Во многих публикациях сообщается о способности различных сульфатированных соединений ингибировать репликации вирусов, включая ВИЧ.
В Nature 343470 (1990) и Science 250, 1411 (1990) описаны сильные ингибиторы обратной транскриптазы типа бензодиазепина. Соединения по настоящему изобретению не являются соединениями бензодиазепинового типа.
В J. Org. Chem. 1962, 27, 181-185 описаны различные 2-бензилтиопиримидиновые производные, включая 4-хлор-5-метил-2-[(фенилметил)тио]пиримидин, 4-хлор-5-метил-2-[[(2,4-дихлорфенил)метил] тио]пиримидин, 4-хлор-5-метил-2-[[(2-хлорфенил)метил] тио]пиримидин и 4-хлор-5-метил-2-[[(4-хлорфенил)метил] тио] пиримидин, и их активность в качестве противоопухолевых соединений при скрининге в отношении опухолевых систем SA-180, CA 755 и L-1210.
В J. Med. Chem. 1977, 20, 88-92 описаны 2-алкокси и 2-алкилтио-4-аминопиримидины, включая 2-[(фенилметил)тио]-4-пиримидинамин, 2-[[(4-хлорфенил)метил] тио] -4-пиримидинамин, 2-[(3-пиридинилметил)тио]-4-пиримидинамин и 2-(фенилметокси)-4-пиримидинамин, и их активность в качестве ингибиторов деоксицитидинкиназы.
В Collect. Czech. Chem. Comm. 1975, 40, 1078-1088 (CA 83:114326e) описаны 5-(3-йодпропаргилокси)пиримидины в качестве эффективных фунгистатиков.
В Synthesis 1981, 397-400 описаны пероксипиримидины.
В J. Org. Chem. 1961, 26, 1884 описан синтез азиридинилпиримидинов в качестве аналогов метиоприма.
В J. Med. Chem. 1991, 34, 315-319 описаны производные тиоурацила, которые имеют дигидроксиборильную группу в C-5-положении. Эти соединения могут использоваться при B-нейтронной терапии злокачественной меланомы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Предложены пиримидин-тиоалкильные и алкилэфирные соединения формулы I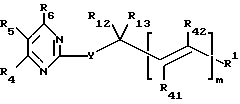
и их терапевтически/фармацевтически совместимые кислотно-аддитивные соли.
Соединения, соответствующие формуле I, могут существовать в различных таутомерных формах и включены в объем формулы I, а также формул IA и IB.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Предложены пиримидин-тиоалкильные и алкилэфирные соединения формулы I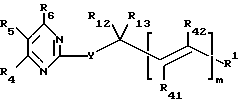
где m равно 0 или 1;
R1 выбран из группы, состоящей из -C≡CH, -CO2R53, -CONR54R55,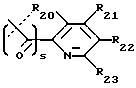
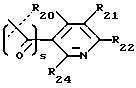
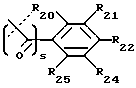
где s равно 0 или 1 (предпочтительно 0) и R20, R21, R22, R23, R24 и R25 являются одинаковыми или различными и выбраны из -H, C1-C6 алкила, C1-C6 алкенила, C1-C6 алкокси, C1-C6 алкилтио, C3-C8 циклоалкила, -CF3, -NO2, галогена, -OH, -CN, фенила, фенилтио, стирила, -CO2(R31), -CON(R31)(R32), -CO(R31), -(CH2)n-N(R31)(R32), -C(OH)(R31)(R33), -(CH2)nN(R31)(CO(R33)), (CH2)nN(R31)(SO2(R33)), или, где R20 и R21, или R21 и R22, или R22 и R23, взятые вместе, образуют пяти- или шестичленное насыщенное или ненасыщенное кольцо, содержащее 0 или 1 атом кислорода, азота или серы, где ненасыщенное кольцо может быть необязательно 1, 2 или 3 замещено C1-C6 алкилом, C1-C6 алкокси, -OH, -CH2OH, -(CH2)n-N(R31)(R32), -C3-C8 циклоалкилом, -CF3, -галогеном, -CO2(R31), -CON(R31)(R32), -CO(R31), -(CH2)nN(R31)(CO(R33)), -(CH2)nN(R31)(SO2(R33)), -CN, -CH2CF3 или -CH(CF3)2, или фенилом, и насыщенное кольцо может быть необязательно 1, 2 или 3 замещено -C1-C6 алкилом, -C1-C6 алкокси, -OH, -CH2OH, или -(CH2)n-N(R31)(R32), или одним оксо (=O);
где n равно 0-3 и R31, R32, и R33 являются одинаковыми или различными и выбраны из
-H,
C1-C6алкила,
фенила, необязательно замещенного 1, 2, или 3-галогеном, C1-C6 алкилом, C1-C6 алкокси, -CF3, -OH или -CN,
или где R31 и R32, взятые вместе с азотом, к которому они присоединены, образуют кольцо, выбранное из -пирролидинила, -пиперидинила, -4-морфолинила, -4-тиоморфолинила, -4-пиперазинила, -4-(1-С1-C6 алкил)пиперазинила,
или представителя группы, состоящей из:
1-циклогексенила, 2-пиримидинила, 4-пиримидинила, 5-пиримидинила, 2-имидазолила, 4-имидазолила, 2-бензотиазолила, 2-бензоксазолила, 2-бензимидазолила, 2-оксазолила, 4-оксазолила, 2-тиазолила, 3-изоксазолила, 5-изоксазолила, 5-метил-3-изоксазолила, 5-фенил-3-изоксазолила, 4-тиазолила, 3-метил-2-пиразинила, 5-метил-2-пиразинила, 6-метил-2-пиразинила, 5-хлор-2-тиенила, 3-фурила, бензофуран-2-ила, бензотиен-2-ила, 2H-1-бензопиран-3-ила, 2,3-дигидробензопиран-5-ила, 1-метилимидазол-2-ила, хиноксалин-2-ила, пиперон-5-ила, 4,7-дихлорбензоксазол-2-ила, 4,6-диметилпиримидин-2-ила, 4-метилпиримидин-2-ила, 2,4-диметилпиримидин-6-ила, 2-метилпиримидин-4-ила, 4-метилпиримидин-6-ила, 6-хлорпиперон-5-ила, 5-хлоримидазо[1,2-a]пиридин-2-ила, 1-H-инден-3-ила, 1-H-2-метилинден-2-ила, 3,4-дигидронафт-1-ила, S-4-изопропенилциклогексен-1-ила или 4-дигидронафт-2-ила,
где R53 выбран из группы, состоящей из -H, C1-C6 алкила, C3-C6 циклоалкила, фенила (необязательно замещенного 1, 2, или 3 атомами галогена, C1-C6 алкилами, C1-C6 алкокси, -CF3, -OH, -CN), или пяти- или шестичленного ненасыщенного кольца, содержащего 0 или 1 атом кислорода, азота или серы, где ненасыщенное кольцо может быть необязательно замещено -H, C1-C6 алкилом, C1-C6 алкокси, -OH, -CH2OH, или -(CH2)n-N(R31)(R32);
где R54 и R55 являются одинаковыми или различными, выбранными из -H, C1-C6 алкила, аллила, или фенила (необязательно замещенного 1, 2, или 3 атомами галогена, C1-C6 алкилами, C1-C6 алкокси или -CF3), или, взятые вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из -пирролидинила, -пиперидинила, -4-морфолинила, -4-тиоморфолинила, -4-пиперазинила, -4-(1-С1-C6алкил)пиперазинила;
R41 и R42 являются одинаковыми или различными, выбранными из группы, состоящей из -H и C1-C4 алкила;
R12 выбран из группы, состоящей из -H, C1-C6 алкила, C3-C6 циклоалкила, -CN, -С(O)NH2, -С(O)N(C1-C6алкил)(C1-C6алкила), -CO2H, -CO2(C1-C6алкила), -CH2OH, -CH2NH2 или -CF3;
R13 выбран из группы, состоящей из -H, C1-C6 алкила или -CF3;
Y выбран из -S-, -S(O)-, -S(O)2, или -O-;
R4 выбран из группы, состоящей из -H, -OH, галогена или -NR15R16, где R15 является -H, и R16 является -H, C1-C6 алкилом, -NH2, или R15 и R16, взятые вместе с -N, образуют 1-пирролидино, 4-морфолино или 1-пиперидино;
R5 выбран из группы, состоящей из -H, -C2H4OH, -C2H4-O-ТБДМС, галогена, -C3-C8 циклоалкила, C1-C3 алкокси, -CH2CH2Cl или C1-C4 алкила, при условии, что R5 не является изобутилом;
или R4 и R5, взятые вместе, образуют пяти- или шестичленное насыщенное или ненасыщенное кольцо, которое вместе с пиримидиновым кольцом образует группу, включающую 7H-пирроло[2,3-d]пиримидин, 5,6-дигидро-7H-пирроло[2,3-d] пиримидин, фуро[2,3-d] пиримидин, 5,6-дигидрофуро[2,3-d] пиримидин, тиено[2,3-d]пиримидин, 5,6-дигидротиено[2,3-d]пиримидин, 1H-пиразоло[3,4-d]пиримидин, 1H-пурин, пиримидо[4,5-d]пиримидин, птеридин, пиридо[2,3-d]пиримидин или хиназолин, где ненасыщенное кольцо может быть необязательно 1, 2 или 3 замещено C1-C6 алкилом, C1-C6 алкокси, -OH, -CH2OH, -(CH2)n-N(R31)(R32), C3-C8 циклоалкилом, -CF3, галогеном, -CO2(R31), -CON(R31)(R32), -CO(R31), -(CH2)nN(R31)(CO(R33)), -(CH2)nN(R31)(SO2(R33)), и насыщенное кольцо может быть необязательно 1, 2 или 3 замещено -C1-C6 алкилом, -C1-C6 алкокси, -OH, -CH2OH, или -(CH2)n-N(R31)(R32), или одним оксо (=O); и
R6 выбран из группы, состоящей из -H, -OH, галогена (предпочтительно, -Cl), -CN, -CF3, -CO2(R61), -C(O)R61 или -C(O)N(R61)(R62), где R61 и R62 являются одинаковыми или различными, и выбран из
-H,
C1-C6 алкила,
фенила, необязательно 1, 2, или 3 замещенного галогеном, C1-C6 алкилами, C1-C6 алкокси, -CF3, -OH, -CN,
или, где R61 и R62 взятые вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из пирролидинила, пиперидинила, 4-морфолинила, 4-тиоморфолинила, 4-пиперазинила или 4-(C1-C6алкил)пиперазинила;
при общем условии, что R4 и R6 не являются оба -H; и со следующим условием, что и R12, и R13 не являются оба -H, за исключением случая, когда R6 выбран из -CN, -CF3, -CO2(R61), -C(O)R61 или -C(O)N(R61)(R62) или R1 выбран из -CO2R53 или -C(O)N(R54)(R55);
их фармацевтически приемлемые соли, гидраты, N-оксиды и сольваты; иные чем
4-амино-6-хлор-2-(1-(4-(4-морфолинилкарбинил)-2- пиридинил)этил)тиопиримидин или
4-амино-6-хлор-2-(1-(4-метил-2-пиридил)пентил)тиопиримидин.
Воплощением настоящего изобретения являются соединения формулы IA, где R12 и R13 не являются оба -H.
Воплощением настоящего изобретения являются пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA, а именно соединения формулы I, где
R4 выбран из группы, состоящей из -H или -NR15R16, где R15 является -H и R16 является -H, C1-C6 алкилом, -NH2, или R15 и R16, взятые вместе с -N, образуют 1-пирролидино, 4-морфолино или 1-пиперидино; и
R6 выбран из группы, состоящей из -H, галогена (предпочтительно, -Cl), -CN, -CF3, -CO2(R61), -C(O)R61 или -C(O)N(R61)(R62).
Соединения формулы IB, а именно соединения формулы I,
где:
i) R4 и/или R6 являются -OH; или
ii) R4 и R6 оба являются галогеном, могут использоваться в качестве промежуточных продуктов для получения пиримидин-тиоалкильных и алкилэфирных анти-СПИД соединений формулы IA.
Воплощением настоящего изобретения являются соединения формулы I (а также формул IA и IB), где Y является -O-.
Предпочтительным воплощением настоящего изобретения являются соединения формулы I (а также формул IA и IB), где S является O, и Y выбран из группы, состоящей из -S-, -S(O)-или -S(O)2; более предпочтительно Y является -S-.
Предпочтительным воплощением настоящего изобретения являются соединения формулы I (а также формул IA и IB), где S является O, и Y выбран из группы, состоящей из -S-, -S(O)- или -S(O)2 (более предпочтительно Y является -S-); и при условии, что R12 и R13 оба не являются -H.
Предпочтительным воплощением настоящего изобретения являются новые соединения формулы I (а также формул IA и IB), где S является O, и Y выбран из группы, состоящей из -S-, -S(O)- или -S(O)2 (более предпочтительно Y, является -S-); и при условии, что R12 и R13 оба не являются -H, и при следующем условии, что, когда R4 является галогеном или амино и R6 является галогеном, R1 не является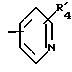
в котором R'4 представляет водород, низший алкил, галоген, амино или гидроксигруппы.
R4 предпочтительно является -NH2.
m предпочтительно равно 0.
R6 предпочтительно является -Cl, -CF3 или -CN.
R41 и R42 являются предпочтительно -H.
R12 является предпочтительно -CH3.
R13 является предпочтительно -H.
R1 предпочтительно выбран из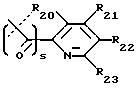
более предпочтительно из представителя группы, включающей: 3-изохинолинил, 1-изохинолинил, 2-хинолинил, 3-хинолинил, 3-(5,6,7,8-тетрагидро)изохинолинил, 1-(5,6,7,8-тетрагидро)изохинолинил, 2-(5,6,7,8-тетрагидро)хинолинил, 3-(5,6,7,8-тетрагидро)хинолинил, 3-(5,6-дигидро)-2H-2-пиридинил, 1-(5,6-дигидро)-2H-2-пиридинил, 2-(5,6-дигидро)-1H-1-пиридинил, 3-(5,6-дигидро)-1H-1-пиридинил, 5-фуро[2,3-c]пиридинил, 6-фуро[3,2-c]пиридинил, 4-фуро[3,2-c]пиридинил, 7-фуро[2,3-c]пиридинил, 6-фуро[2,3-b]пиридинил, 5-фуро[3,2-b] пиридинил, 5-(2,3-дигидро)-фуро[2,3-c]пиридинил, 6-(2,3-дигидро)-фуро[3,2-c] пиридинил, 4-(2,3-дигидро)-фуро[3,2-c]пиридинил, 7-(2,3-дигидро)-фуро[2,3-c] пиридинил, 6-(2,3-дигидро)-фуро[2,3-b]пиридинил, 5-(2,3-дигидро)-фуро[3,2-b] пиридинил, 6-(1,3-дигидро)-фуро[3,4-c] пиридинил, 4-(1,3-дигидро)-фуро[3,4-c] пиридинил, 2-(5,7-дигидро)-фуро[3,4-b]пиридинил, 6-(3,4-дигидро)-2H-пирано[2,3-c] пиридинил, 6-(3,4-дигидро)-1H-пирано[3,4-c] пиридинил, 7-(3,4-дигидро)-1H-пирано[4,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[3,2-c] пиридинил, 5-(3,4-дигидро)-2H-пирано[3,2-c]пиридинил, 5-(3,4-дигидро)-1H-пирано[4,3-c]пиридинил, 8-(3,4-дигидро)-1H-пирано[3,4-c]пиридинил, 8-(3,4-дигидро)-2H-пирано[2,3-c] пиридинил, 7-(3,4-дигидро)-2H-пирано[2,3-b]пиридинил, 2-(5,6-дигидро)-1H-пирано[3,4-b]пиридинил, 2-(5,6-дигидро)-2H-пирано[4,3-b] пиридинил, 6-(3,4-дигидро)-2H-пирано[3,2-b]пиридинил, 5-1H-пирроло[2,3-c] пиридинил, 6-1H-пирроло[3,2-c] пиридинил, 4-1H-пирроло[3,2-c]пиридинил, 7-1H-пирроло[2,3-c]пиридинил, 6-1H-пирроло[2,3-b]пиридинил, 5-1H-пирроло[3,2-b] пиридинил, 5-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинил, 6-(2,3-дигидро)-1H-пирроло[3,2-c] пиридинил, 4-(2,3-дигидро)-1H-пирроло[3,2-c]пиридинил, 7-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинил, 6-(2,3-дигидро)-1H-пирроло[2,3-b]пиридинил, 5-(2,3-дигидро)-1H-пирроло[3,2-b]пиридинил, 6-(1,3-дигидро)-1H-пирроло[3,4-c] пиридинил, 4-(1,3-дигидро)-1H-пирроло[3,4-c] -пиридинил, 2-(5,7-дигидро)-1H-пирроло[3,4-b]пиридинил, 6-1,7-нафтиридинил, 6-2,7-нафтиридинил, 7-2,6-нафтиридинил, 7-1,6-нафтиридинил, 5-1,6-нафтиридинил, 5-2,6-нафтиридинил, 8-2,7-нафтиридинил, 8-1,7-нафтиридинил, 7-1,8-нафтиридинил, 2-1,7-нафтиридинил, 2-1,6-нафтиридинил, 6-1,5-нафтиридинил, 6-(1,2,3,4-тетрагидро)-1,7-нафтиридинил, 6-(1,2,3,4-тетрагидро)-2,7-нафтиридинил, 7-(1,2,3,4-тетрагидро)-2,6-нафтиридинил, 7-(1,2,3,4-тетрагидро)-1,6-нафтиридинил, 5-(1,2,3,4-тетрагидро)-1,6-нафтиридинил, 5-(1,2,3,4-тетрагидро)-2,6-нафтиридинил, 8-(1,2,3,4-тетрагидро)-2,7-нафгиридинил, 8-(1,2,3,4-тетрагидро)-1,7-нафтиридинил, 7-(1,2,3,4-тетрагидро)-1,8-нафтиридинил, 2-(5,6,7,8-тетрагидро)-1,7-нафтиридинил, 2-(5,6,7,8-тетрагидро)-1,6-нафтиридинил, 6-(1,2,3,4-тетрагидро)-1,5-нафтиридинил, 1-нафтил, 2-нафтил, 5-(1,2,3,4-тетрагидро)нафтил, 6-(1,2,3,4-тетрагидро)нафтил, 4-(2,3-дигидро)-1H-инденил, 5-(2,3-дигидро)-1H-инденил, 5-бензофуранил, 4-бензофуранил, 6-бензофуранил, 7-бензофуранил, 5-(2,3-дигидро)бензофуранил, 4-(2,3-дигидро)бензофуранил, 6-(2,3-дигидро)бензофуранил, 7-(2,3-дигидро)бензофуранил, 4-(1,3-дигидро)изобензофуран, 5-(1,3-дигидро)изобензофуран, 4-1H-индолил, 5-1H-индолил, 6-1H-индолил, 7-1H-индолил, 4-(2,3-дигидро)-1H-индолил, 5-(2,3-дигидро)-1H-индолил, 6-(2,3-дигидро)-1H-индолил, 7-(2,3-дигидро)-1H-индолил, 4-(1,3-дигидро)-1H-изоиндолил, 5-(1,3-дигидро)-1H-изоиндолил, 5-(3,4-дигидро)-1H-2-бензопиранил, 6-(3,4-дигидро)-1H-2-бензопиранил, 7-(3,4-дигидро)-1H-2-бензопиранил, 8-(3,4-дигидро)-1H-2-бензопиранил, 5-(3,4-дигидро)-2H-1-бензопиранил, 6-(3,4-дигидро)-2H-1-бензопиранил, 7-(3,4-дигидро)-2H-1-бензопиранил, 8-(3,4-дигидро)-2H-1-бензопиранил, 5-(1,2,3,4-тетрагидро)-изохинолинил, 6-(1,2,3,4-тетрагидро)-изохинолинил, 7-(1,2,3,4-тетрагидро)-изохинолинил, 8-(1,2,3,4-тетрагидро)-изохинолинил, 5-(1,2,3,4-теграгидро)-хинолинил, 6-(1,2,3,4-тетрагидро)-хинолинил, 7-(1,2,3,4-тeтpaгидро)-хинолинил, 8-(1,2,3,4-тетрагидро)-хинолинил, 5-тиено[2,3-c] пиридинил, 6-тиено[3,2-c]пиридинил, 4-тиено[3,2-c]пиридинил, 7-тиено[2,3-c] пиридинил, 6-тиено[2,3-b]пиридинил, 5-тиено[3,2-b]пиридинил, 5-(2,3-дигидро)-тиено[2,3-c] пиридинил, 6-(2,3-дигидро)-тиено[3,2-c]пиридинил, 4-(2,3-дигидро)-тиено[3,2-c]пиридинил, 7-(2,3-дигидро)-тиено[2,3-c]пиридинил, 6-(2,3-дигидро)-тиено-[2,3-b] пиридинил, 5-(2,3-дигидро)-тиено[3,2-b] пиридинил, 6-(1,3-дигидро)-тиено[3,4-c] пиридинил, 4-(1,3-дигидро)-тиено[3,4-c]пиридинил, 2-(5,7-дигидро)-тиено[3,4-b]пиридинил, 6-(3,4-дигидро)-2H-тиопирано[2,3-c] пиридинил, 6-(3,4-дигидро)-1H-тиопирано[3,4-c] пиридинил, 7-(3,4-дигидро)-1H-тиопирано[4,3-c]пиридинил, 7-(3,4-дигидро)-2H-тиопирано[3,2-c] пиридинил, 5-(3,4-дигидро)-2H-тиопирано[3,2-c]пиридинил, 5-(3,4-дигидро)-1H-тиопирано[4,3-c] пиридинил, 8-(3,4-дигидро)-1H-тиопирано[3,4-c]пиридинил, 8-(3,4-дигидро)-2H-тиопирано[2,3-c]пиридинил, 7-(3,4-дигидро)-2H-тиопирано[2,3-b] пиридинил, 2-(5,6-дигидро)-1H-тиопирано[3,4-b] пиридинил, 2-(5,6-дигидро)-2H-тиопирано[4,3-b]пиридинил, 6-(3,4-дигидро)-2H-тиопирано[3,2-b] пиридинил, 5-бензо[b] тиофенил, 4-бензо[b]тиофенил, 6-бензо[b] тиофенил, 7-бензо[b]тиофенил, 5-(2,3-дигидро)-бензо[b]тиофенил, 4-(2,3-дигидро)-бензо[b]тиофенил, 6-(2,3-дигидро)-бензо[b]тиофенил, 7-(2,3-дигидро)-бензо[b] тиофенил, 4-(1,3-дигидро)-бензо[c] тиофенил, 5-(1,3-дигидро)-бензо[c] тиофенил, 5-(3,4-дигидро)-1H-2-бензотиопиранил, 6-(3,4-дигидро)-1H-2-бензотиопиранил, 7-(3,4-дигидро)-1H-2-бензотиопиранил, 8-(3,4-дигидро)-1H-2-бензотиопиранил, 5-(3,4-дигидро)-2H-1-бензотиопиранил, 6-(3,4-дигидро)-2H-1-бензотиопиранил, 7-(3,4-дигидро)-2H-1-бензотиопиранил, или 8-(3,4-дигидро)-2H-1-бензотиопиранил; где такой член является необязательно замещенным, как описано выше;
наиболее предпочтительно из представителя группы, включающей:
3-изохинолинил, 1-изохинолинил, 2-хинолинил, 3-хинолинил, 3-(5,6,7,8-тетрагидро)изохинолинил, 1-(5,6,7,8-тетрагидро)изохинолинил, 2-(5,6,7,8-тетрагидро)хинолинил, 3-(5,6,7,8-тетрагидро)хинолинил, 3-(5,6-дигидро)-2H-2-пириндинил, 1-(5,6-дигидро)-2H-2-пириндинил, 2-(5,6-дигидро)-1H-1-пириндинил, 3-(5,6-дигидро)-1H-1-пириндинил, 5-фуро[2,3-c] пиридинил, 6-фуро[3,2-c] пиридинил, 4-фуро[3,2-c] пиридинил, 7-фуро[2,3-c]пиридинил, 6-фуро[2,3-b]пиридинил, 5-фуро[3,2-b]пиридинил, 5-(2,3-дигидро)-фуро[2,3-c]пиридинил, 6-(2,3-дигидро)-фуро[3,2-c]пиридинил, 4-(2,3-дигидро)-фуро[3,2-c]пиридинил, 7-(2,3-дигидро)-фуро[2,3-c] пиридинил, 6-(2,3-дигидро)-фуро[2,3-b] пиридинил, 5-(2,3-дигидро)-фуро[3,2-b]пиридинил, 6-(1,3-дигидро)-фуро[3,4-c] пиридинил, 4-(1,3-дигидро)-фуро[3,4-c]пиридинил, 2-(5,7-дигидро)-фуро[3,4-b] пиридинил, 6-(3,4-дигидро)-2H-пирано[2,3-c]пиридинил, 6-(3,4-дигидро)-1H-пирано[3,4-c] пиридинил, 7-(3,4-дигидро)-1H-пирано[4,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[3,2-c]пиридинил, 5-(3,4-дигидро)-2H-пирано[3,2-c]пиридинил, 5-(3,4-дигидро)-1H-пирано[4,3-c] пиридинил, 8-(3,4-дигидро)-1H-пирано[3,4-c]пиридинил, 8-(3,4-дигидро)-2H-пирано[2,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[2,3-b] пиридинил, 2-(5,6-дигидро)-1H-пирано[3,4-b]пиридинил, 2-(5,6-дигидро)-2H-пирано[4,3-b] пиридинил или 6-(3,4-дигидро)-2H-пирано[3,2-b] -пиридинил; где такой член является необязательно замещенным, как описано выше.
Представители группы R1 включают:
фенил, необязательно замещенный одним, 2 или 3 C1-C4 алкилом, С1-C3 алкокси, галогеном, C1-C3 алкилтио, трифторметилом, C2-C6 диалкиламино или нитро; 2- или 3-пиридинил, необязательно замещенный C1-C6 алкилом, C1-C6 алкенилом, C1-C6 алкокси, C1-C6 алкилтио, -C3-C8 циклоалкилом, -CF3, -NO2, -галогеном, -OH, -CN, фенилом, фенилтио, -стирилом, -CO2(R31), -CON(R31)(R32), -CO(R31), -(CH2)n-N(R31)(R32), -C(OH)(R31)(R33), -(CH2)nN(R31)(CO(R33)), -(CH2)nN(R31)(SO2(R33)); нафтил, необязательно замещенный одним или 2 C1-C4 алкилом, C1-C3 алкокси, галогеном, трифторметилом, C2-C6 диалкиламино, C1-C3 алкилтио или нитро; -C≡CH; а также 3-изохинолинил, 1-изохинолинил, 2-хинолинил, 3-хинолинил, 3-(5,6,7,8-тетрагидро)-изохинолинил, 1-(5,6,7,8-тетрагидро)-изохинолинил, 2-(5,6,7,8-тетрагидро)-хинолинил, 3-(5,6,7,8-тетрагидро)-хинолинил, 3-(5,6-дигидро)-2H-2-пириндинил, 1-(5,6-дигидро)-2H-2-пириндинил, 2-(5,6-дигидро)-1H-1-пириндинил, 3-(5,6-дигидро)-1H-1-пириндинил, 5-фуро[2,3-c]пиридинил, 6-фуро[3,2-c]пиридинил, 4-фуро[3,2-c]пиридинил, 7-фуро[2,3-c]пиридинил, 6-фуро[2,3-b]пиридинил, 5-фуро[3,2-b] пиридинил, 5-(2,3-дигидро)-фуро[2,3-c]пиридинил, 6-(2,3-дигидро)-фуро[3,2-c] пиридинил, 4-(2,3-дигидро)-фуро[3,2-c]пиридинил, 7-(2,3-дигидро)-фуро[2,3-c] пиридинил, 6-(2,3-дигилро)-фуро[2,3-b]пиридинил, 5-(2,3-дигидро)-фуро[3,2-b] пиридинил, 6-(1,3-дигидро)-фуро[3,4-c] пиридинил, 4-(1,3-дигидро)-фуро[3,4-c] пиридинил, 2-(5,7-дигидро)-фуро[3,4-b]пиридинил, 6-(3,4-дигидро)-2H-пирано[2,3-c] пиридинил, 6-(3,4-дигидро)-1H-пирано[3,4-c] пиридинил, 7-(3,4-дигидро)-1H-пирано[4,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[3,2-c] пиридинил, 5-(3,4-дигидро)-2H-пирано[3,2-c]пиридинил, 5-(3,4-дигидро)-1H-пирано[4,3-c] пиридинил, 8-(3,4-дигидро)-1H-пирано[3,4-c]пиридинил, 8-(3,4-дигидро)-2H-пирано[2,3-c] пиридинил, 7-(3,4-дигидро)-2H-пирано[2,3-b]пиридинил, 2-(5,6-дигидро)-1H-пирано[3,4-b]пиридинил, 2-(5,6-дигидро)-2H-пирано[4,3-b] пиридинил, 6-(3,4-дигидро)-2H-пирано[3,2-b]пиридинил, 5-1H-пирроло[2,3-c] пиридинил, 6-1H-пирроло[3,2-c] пиридинил, 4-1H-пирроло[3,2-c]пиридинил, 7-1H-пирроло[2,3-c]пиридинил, 6-1H-пирроло[2,3-b]пиридинил, 5-1H-пирроло[3,2-b] пиридинил, 5-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинил, 6-(2,3-дигидро)-1H-пирроло[3,2-c] пиридинил, 4-(2,3-дигидро)-1H-пирроло[3,2-c]пиридинил, 7-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинил, 6-(2,3-дигидро)-1H-пирроло[2,3-b]пиридинил, 5-(2,3-дигидро)-1H-пирроло[3,2-b]пиридинил, 6-(1,3-дигидро)-1H-пирроло[3,4-c] пиридинил, 4-(1,3-дигидро)-1H-пирроло[3,4-c] пиридинил, 2-(5,7-дигидро)-1H-пирроло[3,4-b]пиридинил, 6-1,7-нафтиридинил, 6-2,7-нафтиридинил, 7-2,6-нафтиридинил, 7-1,6-нафтиридинил, 5-1,6-нафтиридинил, 5-2,6-нафтиридинил, 8-2,7-нафтиридинил, 8-1,7-нафтиридинил, 7-1,8-нафтиридинил, 2-1,7-нафтиридинил, 2-1,6-нафтиридинил, 6-1,5-нафтиридинил, 6-(1,2,3,4-тетрагидро)-1,7-нафтиридинил, 6-(1,2,3,4-тетрагидро)-2,7-нафтиридинил, 7-(1,2,3,4-тетрагидро)-2,6-нафтиридинил, 7-(1,2,3,4-тетрагидро)-1,6-нафтиридинил, 5-(1,2,3,4-тетрагидро)-1,6-нафтиридинил, 5-(1,2,3,4-тетрагидро)-2,6-нафтиридинил, 8-(1,2,3,4-тетрагидро)-2,7-нафтиридинил, 8-(1,2,3,4-тетрагидро)-1,7-нафтиридинил, 7-(1,2,3,4-тетрагидро)-1,8-нафтиридинил, 2-(5,6,7,8-тетрагидро)-1,7-нафтиридинил, 2-(5,6,7,8-тетрагидро)-1,6-нафтиридинил, 6-(1,2,3,4-тетрагидро)-1,5-нафтиридинил, 1-нафтил, 2-нафтил, 5-(1,2,3,4-тетрагидро)нафтил, 6-(1,2,3,4-тетрагидро)нафтил, 4-(2,3-дигидро)-1H-инденил, 5-(2,3-дигидро)-1H-инденил, 5-бензофуранил, 4-бензофуранил, 6-бензофуранил, 7-бензофуранил, 5-(2,3-дигидро)-бензофуранил, 4-(2,3-дигидро)-бензофуранил, 6-(2,3-дигидро)-бензофуранил, 7-(2,3-дигидро)-бензофуранил, 4-(1,3-дигидро)-изобензофуран, 5-(1,3-дигидро)-изобензофуран, 4-1H-индолил, 5-1H-индолил, 6-1H-индолил, 7-1H-индолил, 4-(2,3-дигидро)-1H-индолил, 5-(2,3-дигидро)-1H-индолил, 6-(2,3-дигидро)-1H-индолил, 7-(2,3-дигидро)-1H-индолил, 4-(1,3-дигидро)-1H-изоиндолил, 5-(1,3-дигидро)-1H-изоиндолил, 5-(3,4-дигидро)-1H-2-бензопиранил, 6-(3,4-дигидро)-1H-2-бензопиранил, 7-(3,4-дигидро)-1H-2-бензопиранил, 8-(3,4-дигидро)-1H-2-бензопиранил, 5-(3,4-дигидро)-2H-1-бензопиранил, 6-(3,4-дигидро)-2H-1-бензопиранил, 7-(3,4-дигидро)-2H-1-бензопиранил, 8-(3,4-дигидро)-2H-1-бензопиранил, 5-(1,2,3,4-тетрагидро)-изохинолинил, 6-(1,2,3,4-тетрагидро)-изохинолинил, 7-(1,2,3,4-тетрагидро)-изохинолинил, 8-(1,2,3,4-тетрагидро)-изохинолинил, 5-(1,2,3,4-тетрагидро)-хинолинил, 6-(1,2,3,4-тетрагидро)-хинолинил, 7-(1,2,3,4-тетрагидро)-хинолинил, 8-(1,2,3,4-тетрагидро)-хинолинил, 5-тиено[2,3-c] пиридинил, 6-тиено[3,2-c]пиридинил, 4-тиено[3,2-c]пиридинил, 7-тиено[2,3-c] пиридинил, 6-тиено[2,3-b]пиридинил, 5-тиено[3,2-b]пиридинил, 5-(2,3-дигидро)-тиено[2,3-c] пиридинил, 6-(2,3-дигидро)-тиено[3,2-c]пиридинил, 4-(2,3-дигидро)-тиено[3,2-c]пиридинил, 7-(2,3-дигидро)-тиено[2,3-c]пиридинил, 6-(2,3-дигидро)-тиено[2,3-b]пиридинил, 5-(2,3-дигидро)-тиено[3,2-b] пиридинил, 6-(1,3-дигидро)-тиено[3,4-c] пиридинил, 4-(1,3-дигидро)-тиено[3,4-c] пиридинил, 2-(5,7-дигидро)-тиено[3,4-b] пиридинил, 6-(3,4-дигидро)-2H-тиопирано[2,3-c] пиридинил, 6-(3,4-дигидро)-1H-тиопирано[3,4-c]пиридинил, 7-(3,4-дигидро)-1H-тиопирано[4,3-c] пиридинил, 7-(3,4-дигидро)-2H-тиопирано[3,2-c] пиридинил, 5-(3,4-дигидро)-2H-тиопирано[3,2-c] пиридинил, 5-(3,4-дигидро)-1H-тиопирано[4,3-c] пиридинил, 8-(3,4-дигидро)-1H-тиорирано[3,4-c]пиридинил, 8-(3,4-дигидро)-2H-тиопирано[2,3-c]пиридинил, 7-(3,4-дигидро)-2H-тиопирано[2,3-b] пиридинил, 2-(5,6-дигидро)-1H-тиопирано[3,4-b] пиридинил, 2-(5,6-дигидро)-2H-тиопирано[4,3-b]пиридинил, 6-(3,4-дигидро)-2H-тиопирано[3,2-b] пиридинил, 5-бензо[b]тиофенил, 4-бензо-[b]тиофенил, 6-бензо[b] тиофенил, 7-бензо[b]тиофенил, 5-(2,3-дигидро)-бензо[b]тиофенил, 4-(2,3-дигидро)-бензо[b] тиофенил, 6-(2,3-дигидро)-бензо[b]тиофенил, 7-(2,3-дигидро)-бензо[b] -тиофенил, 4-(1,3-дигидро)-бензо[c] тиофенил, 5-(1,3-дигидро)-бензо[c] -тиофенил, 5-(3,4-дигидро)-1H-2-бензотиопиранил, 6-(3,4-дигидро)-1H-2-бензотиопиранил, 7-(3,4-дигидро)-1H-2-бензотиопиранил, 8-(3,4-дигидро)-1H-2-бензотиопиранил, 5-(3,4-дигидро)-2H-1-бензотиопиранил, 6-(3,4-дигидро)-2H-1-бензотиопиранил, 7-(3,4-дигидро)-2H-1-бензотиопиранил, 8-(3,4-дигидро)-2H-1-бензотиопиранил;
или представителя группы, включающей: 4-хинолинил, 5-хинолинил, 6-хинолинил, 7-хинолинил, 8-хинолинил, 1-циклогексенил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 2-имидазолил, 4-имидазолил, 2-бензотиазолил, 2-бензоксазолил, 2-бензимидазолил, 2-оксазолил, 4-оксазолил, 2-тиазолил, 3-изоксазолил, 5-изоксазолил, 5-метил-3-изоксазолил, 5-фенил-3-изоксазолил, 4-тиазолил, 3-метил-2-пиразинил, 5-метил-2-пиразинил, 6-метил-2-пиразинил, 5-хлор-2-тиенил, 3-фурил, бензофуран-2-ил, бензотиен-2-ил, 2H-1-бензопиран-3-ил, 2,3-дигидробензопиран-5-ил, 2,3-дигидробензофуран-2-ил, 1-метил-имидазол-2-ил, хиноксалин-2-ил, изохинолин-3-ил, пиперон-5-ил, 4,7-дихлорбензоксазол-2-ил, 4,6-диметилпиримидин-2-ил, 4-метилпиримидин-2-ил, 2,4-диметилпиримидин-6-ил, 2-метилпиримидин-4-ил, 4-метилпиримидин-6-ил, 6-хлорпиперон-5-ил, 5-хлоримидазо[1,2-a] пиридин-2-ил, 1-H-инден-3-ил, 1-H-2-метилинден-2-ил, 3,4-дигидронафт-1-ил, S-4-изопропенилциклогексен-1-ил и 4-дигидронафт-2-ил.
Новые альфа-замещенные пиримидин-тиоалкильные соединения формулы I включают соединения, где R1 не является 2- или 3-пиридинилом, необязательно замещенным C1-C4 алкилом, атомом галогена, NH2 или -OH, когда m равно O, Y является S, R13 является -H, R12 является -H или C1-C4 алкилом, R4 является -H, -OH, галогеном или NH2, R5 является -H, галогеном или C1-C4 алкилом, и R6 выбран из группы, состоящей из -H, галогена или -OH.
Предпочтительные новые альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA включают соединения, где Y является S и m равно 0.
Следующие предпочтительные новые альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA включают соединения, где Y является S, m равно 0, R12 является CH3, и R13 является -H.
Следующие предпочтительные новые альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA включают соединения, где Y является S, m равно 0, R12 является CH3, R13 является -H, R4 является NH2, R5 является -H, и R6 является -Cl, CF3 или CN.
Более предпочтительные новые альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA включают соединения, где Y является S, m равно 0, s равно 0, R12 является CH3, R13 является -H, R4 является NH2, R5 является -H, R6 является -Cl, CF3 или CN, и R1 выбран из группы, состоящей из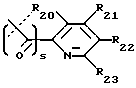
Наиболее предпочтительные новые альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA включают соединения, где Y является S, m равно 0, s равно 0, R12 является CH3, R13 является -H, R4 является NH2, R5 является -H, R6 является -Cl, CF3 или CN, и R1 выбран из группы, состоящей из 3-изохинолинила, 1-изохинолинила, 2-хинолинила, 3-хинолинила, 3-(5,6,7,8-тетрагидро)-изохинолинила, 1-(5,6,7,8-тетрагидро)-изохинолинила, 2-(5,6,7,8-тетрагидро)-хинолинила, 3-(5,6,7,8-тетрагидро)-хинолинила, 3-(5,6-дигидро)-2H-2-пириндинила, 1-(5,6-дигидро)-2H-2-пириндинила, 2-(5,6-дигидро)-1H-1-пириндинила, 3-(5,6-дигидро)-1H-1-пириндинила, 5-фуро[2,3-c] пиридинила, 6-фуро[3,2-c]пиридинила, 4-фуро[3,2-c]пиридинила, 7-фуро[2,3-c] пиридинила, 6-фуро[2,3-b]пиридинила, 5-фуро[3,2-b]пиридинила, 5-(2,3-дигидро)-фуро[2,3-c] пиридинила, 6-(2,3-дигидро)-фуро[3,2-c] пиридинила, 4-(2,3-дигидро)-фуро[3,2-c]пиридинила, 7-(2,3-дигидро)-фуро[2,3-c]пиридинила, 6-(2,3-дигидро)-фуро[2,3-b]пиридинила, 5-(2,3-дигидро)-фуро[3,2-b] пиридинила, 6-(1,3-дигидро)-фуро[3,4-c] -пиридинила, 4-(1,3-дигидро)-фуро[3,4-c] пиридинила, 2-(5,7-дигидро)-фуро[3,4-b]пиридинила, 6-(3,4-дигидро)-2H-пирано-[2,3-c]пиридинила, 6-(3,4-дигидро)-1H-пирано[3,4-c]пиридинила, 7-(3,4-дигидро)-1H-пирано[4,3-c]пиридинила, 7-(3,4-дигидро)-2H-пирано[3,2-c] пиридинила, 5-(3,4-дигидро)-2H-пирано[3,2-c] пиридинила, 5-(3,4-дигидро)-1H-пирано[4,3-c] -пиридинила, 8-(3,4-дигидро)-1H-пирано[3,4-c] пиридинила, 8-(3,4-дигидро)-2H-пирано[2,3-c]пиридинила, 7-(3,4-дигидро)-2H-пирано[2,3-b] пиридинила, 2-(5,6-дигидро)-1H-пирано[3,4-b]-пиридинила, 2-(5,6-дигидро)-2H-пирано[4,3-b] пиридинила, 6-(3,4-дигидро)-2H-пирано[3,2-b]пиридинила, 5-1H-пирроло[2,3-c] пиридинила, 6-1H-пирроло[3,2-c]пиридинила, 4-1H-пирроло-[3,2-c]пиридинила, 7-1H-пирроло[2,3-c]пиридинила, 6-1H-пирроло[2,3-b]пиридинила, 5-1H-пирроло[3,2-b]пиридинила, 5-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинила, 6-(2,3-дигидро)-1H-пирроло[3,2-c] пиридинила, 4-(2,3-дигидро)-1H-пирроло[3,2-c] пиридинила, 7-(2,3-дигидро)-1H-пирроло[2,3-c]пиридинила, 6-(2,3-дигидро)-1H-пирроло[2,3-b]пиридинила, 5-(2,3-дигидро)-1H-пирроло[3,2-b] пиридинила, 6-(1,3-дигидро)-1H-пирроло[3,4-c]пиридинила, 4-(1,3-дигидро)-1H-пирроло[3,4-c] пиридинила, 2-(5,7-дигидро)-1H-пирроло[3,4-b]пиридинила, 6-1,7-нафтиридинила, 6-2,7-нафтиридинила, 7-2,6-нафтиридинила, 7-1,6-нафтиридинила, 5-1,6-нафтиридинила, 5-2,6-нафтиридинила, 8-2,7-нафтиридинила, 8-1,7-нафтиридинила, 7-1,8-нафтиридинила, 2-1,7-нафтиридинила, 2-1,6-нафтиридинила, 6-1,5-нафтиридинила, 6-(1,2,3,4-тетрагидро)-1,7-нафтиридинила, 6-(1,2,3,4-тетрагидро)-2,7-нафтиридинила, 7-(1,2,3,4-тетрагидро)-2,6-нафтиридинила, 7-(1,2,3,4-тетрагидро)-1,6-нафтиридинила, 5-(1,2,3,4-тетрагидро)-1,6-нафтиридинила, 5-(1,2,3,4-тетрагидро)-2,6-нафтиридинила, 8-(1,2,3,4-тетрагидро)-2,7-нафтиридинила, 8-(1,2,3,4-тетрагидро)-1,7-нафтиридинила, 7-(1,2,3,4-тетрагидро)-1,8-нафтиридинила, 2-(5,6,7,8-тетрагидро)-1,7-нафтиридинила, 2-(5,6,7,8-тетрагидро)-1,6-нафтиридинила, 6-(1,2,3,4-тетрагидро)-1,5-нафтиридинила, 1-нафтила, 2-нафтила, 5-(1,2,3,4-тетрагидро)нафтила, 6-(1,2,3,4-тетрагидро)нафтила, 4-(2,3-дигидро)-1H-инденила, 5-(2,3-дигидро)-1H-инденила, 5-бензофуранила, 4-бензофуранила, 6-бензофуранила, 7-бензофуранила, 5-(2,3-дигидро)-бензофуранила, 4-(2,3-дигидро)-бензофуранила, 6-(2,3-дигидро)-бензофуранила, 7-(2,3-дигидро)-бензофуранила, 4-(1,3-дигидро)-изобензофурана, 5-(1,3-дигидро)-изобензофурана, 4-1H-индолила, 5-1H-индолила, 6-1H-индолила, 7-1H-индолила, 4-(2,3-дигидро)-1H-индолила, 5-(2,3-дигидро)-1H-индолила, 6-(2,3-дигидро)-1H-индолила, 7-(2,3-дигидро)-1H-индолила, 4-(1,3-дигидро)-1H-изоиндолила, 5-(1,3-дигидро)-1H-изоиндолила, 5-(3,4-дигидро)-1H-2-бензопиранила, 6-(3,4-дигидро)-1H-2-бензопиранила, 7-(3,4-дигидро)-1H-2-бензопиранила, 8-(3,4-дигидро)-1H-2-бензопиранила, 5-(3,4-дигидро)-2H-1-бензопиранила, 6-(3,4-дигидро)-2H-1-бензопиранила, 7-(3,4-дигидро)-2H-1-бензопиранила, 8-(3,4-дигидро)-2H-1-бензопиранила, 5-(1,2,3,4-тетрагидро)-изохинолинила, 6-(1,2,3,4-тетрагидро)-изохинолинила, 7-(1,2,3,4-тетрагидро)-изохинолинила, 8-(1,2,3,4-тетрагидро)-изохинолинила, 5-(1,2,3,4-тетрагидро)-хинолинила, 6-(1,2,3,4-тетрагидро)-хинолинила, 7-(1,2,3,4-тетрагидро)-хинолинила, 8-(1,2,3,4-тетрагидро)-хинолинила, 5-тиено[2,3-c] пиридинила, 6-тиено[3,2-c]пиридинила, 4-тиено[3,2-c] пиридинила, 7-тиено[2,3-c]-пиридинила, 6-тиено[2,3-b]пиридинила, 5-тиено[3,2-b] -пиридинила, 5-(2,3-дигидро)-тиено[2,3-c]пиридинила, 6-(2,3-дигидро)-тиено[3,2-c] пиридинила, 4-(2,3-дигидро)-тиено[3,2-c]пиридинила, 7-(2,3-дигидро)-тиено[2,3-c] пиридинила, 6-(2,3-дигидро)-тиено[2,3-b] пиридинила, 5-(2,3-дигидро)-тиено[3,2-b] пиридинила, 6-(1,3-дигидро)-тиено[3,4-c] пиридинила, 4-(1,3-дигидро)-тиено[3,4-c]пиридинила, 2-(5,7-дигидро)-тиено[3,4-b] пиридинила, 6-(3,4-дигидро)-2H-тиопирано[2,3-c]пиридинила, 6-(3,4-дигидро)-1H-тиопирано[3,4-c] пиридинила, 7-(3,4-дигидро)-1H-тиопирано[4,3-c] пиридинила, 7-(3,4-дигидро)-2H-тиопирано[3,2-c] пиридинила, 5-(3,4-дигидро)-2H-тиопирано[3,2-c] пиридинила, 5-(3,4-дигидро)-1H-тиопирано[4,3-c] пиридинила, 8-(3,4-дигидро)-1H-тиопирано[3,4-c] пиридинила, 8-(3,4-дигидро)-2H-тиопирано[2,3-c] пиридинила, 7-(3,4-дигидро)-2H-тиопирано[2,3-b] пиридинила, 2-(5,6-дигидро)-1H-тиопирано[3,4-b] пиридинила, 2-(5,6-дигидро)-2H-тиопирано[4,3-b] пиридинила, 6-(3,4-дигидро)-2H-тиопирано[3,2-b] пиридинила, 5-бензо[b] тиофенила, 4-бензо[b]тиофенила, 6-бензо[b] тиофенила, 7-бензо[b]тиофенила, 5-(2,3-дигидро)-бензо[b]тиофенила, 4-(2,3-дигидро)-бензо[b]тиофенила, 6-(2,3-дигидро)-бензо[b]тиофенила, 7-(2,3-дигидро)-бензо[b] тиофенила, 4-(1,3-дигидро)-бензо[c]тиофенила, 5-(1,3-дигидро)-бензо[c] тиофенила, 5-(3,4-дигидро)-1H-2-бензотиопиранила, 6-(3,4-дигидро)-1H-2-бензотиопиранила, 7-(3,4-дигидро)-1H-2-бензотиопиранила, 8-(3,4-дигидро)-1H-2-бензотиопиранила, 5-(3,4-дигидро)-2H-1-бензотиопиранила, 6-(3,4-дигидро)-2H-1-бензотиопиранила, 7-(3,4-дигидро)-2H-1-бензотиопиранила, 8-(3,4-дигидро)-2H-1-бензотиопиранила;
наиболее предпочтительно представителя группы, включающей:
3-изохинолинил, 1-изохинолинил, 2-хинолинил, 3-хинолинил, 3-(5,6,7,8-тетрагидро)-изохинолинил, 1-(5,6,7,8-тетрагидро)-изохинолинил, 2-(5,6,7,8-тетрагидро)-хинолинил, 3-(5,6,7,8-тетрагидро)-хинолинил, 3-(5,6-дигидро)-2H-2-пириндинил, 1-(5,6-дигидро)-2H-2-пириндинил, 2-(5,6-дигидро)-1H-1-пириндинил, 3-(5,6-дигидро)-1H-1-пириндинил, 5-фуро[2,3-c] пиридинил, 6-фуро[3,2-c] пиридинил, 4-фуро[3,2-c] пиридинил, 7-фуро[2,3-c]пиридинил, 6-фуро[2,3-b] пиридинил, 5-фуро[3,2-b]пиридинил, 5-(2,3-дигидро)фуро[2,3-c]пиридинил, 6-(2,3-дигидро)фуро[3,2-c]пиридинил, 4-(2,3-дигидро)фуро[3,2-c]пиридинил, 7-(2,3-дигидро)фуро[2,3-c]пиридинил, 6-(2,3-дигидро)фуро[2,3-b]пиридинил, 5-(2,3-дигидро)фуро[3,2-b]пиридинил, 6-(1,3-дигидро)фуро[3,4-c]пиридинил, 4-(1,3-дигидро)фуро[3,4-c]пиридинил, 2-(5,7-дигидро)фуро[3,4-b]пиридинил, 6-(3,4-дигидро)-2H-пирано[2,3-c] пиридинил, 6-(3,4-дигидро)-1H-пирано[3,4-c]пиридинил, 7-(3,4-дигидро)-1H-пирано[4,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[3,2-c] пиридинил, 5-(3,4-дигидро)-2H-пирано[3,2-c]пиридинил, 5-(3,4-дигидро)-1H-пирано[4,3-c] пиридинил, 8-(3,4-дигидро)-1H-пирано[3,4-c] пиридинил, 8-(3,4-дигидро)-2H-пирано[2,3-c]пиридинил, 7-(3,4-дигидро)-2H-пирано[2,3-b] пиридинил, 2-(5,6-дигидро)-1H-пирано[3,4-b]пиридинил, 2-(5,6-дигидро)-2H-пирано[4,3-b]пиридинил, 6-(3,4-дигидро)-2H-пирано[3,2-b]пиридинил.
Пиримидин-тиоалкильные соединения формулы I обычно и наиболее часто получают путем взаимодействия 2-меркаптопиримидина с соответствующим алкилирующим агентом, например мезилатом или галогенидом. Смотри, например, Схему A в конце описания.
Когда R12 и R13 являются различными, соединения формулы I (а также IA и IB) выделяют в виде рацемической смеси, и она содержит R и S изомеры, которые могут быть выделены из рацемической смеси с помощью ВЭЖХ с использованием колонки с хиральной фазой, такой как Chiralcel OD-H, элюированием соответствующей смесью растворителей, такой как изопропанол/гексан. R и S изомеры соединения формулы I (когда R12 и R13 являются различными) могут быть получены из соответствующего хирального галогенида (или мезилата) II (смотри Схему B в конце описания). Соответствующий хиральный галогенид (или мезилат) II получают из хирального спирта IV. Соответствующий хиральный спирт IV может быть получен из соответствующего кетона V с использованием хирального восстанавливающего агента, такого как (+) или (-)-диизопинокамфеилхлорборан, или другие хиральные восстанавливающие агенты, известные из литературы. Соответствующий хиральный спирт IV также получают путем разделения рацемического спирта VII путем ферментативного гидролиза соответствующего ацетата VI соответствующим ферментом, таким как PS-30 аминолипаза или L1754, тип VII, из candidae cylindracea, или другие ферменты, известные из литературы. Соответствующий хиральный спирт IV также получают путем разделения рацемического спирта VII ферментативной этерификацией (такой как ацетилирование или бутилирование) рацемического спирта VII (с получением хирального соединения VIII), используя соответствующий фермент, такой как липаза из поджелудочной железы свиньи, тип II, или другие ферменты, известные из литературы.
Альфа-замещенные пиримидин-тиоалкильные и алкилэфирные соединения формулы I включают соединения примеров 193-291. Предпочтительными являются анти-СПИД соединения по примерам 230, 231, 233, 234, 237, 238, 239, 240, 241, 242, 243, 246, 247, 248, 249, 250, 251, 252, 256, 269, 270, 271, 272, 273, 277, 194, 199, 203, 207, 282, 283, 284, 285, 286, 287, 289, 290, 297, 299, и предпочтительно 237, 238, 239, 246, 289, 290, 297, 299, и более предпочтительно 290, 297, 299, и их соли (например, 302, 306 и 301).
Пиримидин-тиоалкильные и алкилэфирные соединения формулы 1 образуют кислотно-аддитивные соли, такие как мезилат, гидрохлорид, гидробромид, гидройодид, сульфат, фосфат, ацетат, пропионат, лактат, малеат, малат, сукцинат, тартрат и
тому подобное. Некоторые из возможных взаимозаменяемых заместителей являются кислотными и в таком качестве образуют основно-аддитивные соли, когда взаимодействуют с достаточно сильными основаниями. Фармацевтически приемлемые соли включают соли как неорганических, так и органических оснований. Предпочтительные фармацевтически приемлемые соли включают соли следующих оснований, например, гидроксида аммония, трометамина (ТНАМ), 2-амино-2-(гидроксиметил)-1,3-пропандиола. Соответствующие катионы включают, например, натрий, калий, кальций и магний.
Пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA могут использоваться в качестве ингибиторов обратной транскриптазы вирусов, фермента, необходимого для репликации вируса иммунодефицита человека, и поэтому могут использоваться при лечении таких заболеваний, как СПИД.
Термин ретровирус человека (РВЧ) обозначает вирус иммунодефицита человека типа I или его штаммы, очевидные для специалиста в данной области, которые принадлежат к этим же семействам вирусов и которые вызывают физиологические эффекты у людей, подобно различным ретровирусам человека.
Пациенты, подлежащие лечению, включают тех индивидуумов, которые (1) инфицированы одним или несколькими штаммами ретровируса человека, что определяется по присутствию либо измеряемого количества антител к вирусу, либо антигенов в сыворотке крови, и (2) имеют либо определенную по симптомам СПИД-инфекцию, такую как (а) диссеминированный гистоплазмоз, (b) изопсориаз, (c) бронхиальный и легочный кандидоз, включая плазмоклеточную пневмонию, (d) лимфому, отличную от лимфомы Ходжкина, или (e) саркому Капоши, и имеющие возраст менее 60 лет; или имеющие абсолютный отсчет CD4 лимфоцитов в периферической крови менее чем 200/мм3.
Соединения формулы IA могут вводиться перорально. Подходящие стандартные лекарственные формы включают таблетки, капсулы, суспензии, растворы и эликсиры. Эффективное количество составляет от около 0,1 до около 500 мг/кг/день. Типичная стандартная доза для человека весом 70 кг должна составлять от около 10 мг до около 2000 мг, предпочтительно от около 100 мг до около 1000 мг, вводимых от одного до шести раз в день.
Точная доза и частота введения в такой степени, как это хорошо известно специалистам в данной области, зависят от конкретного используемого соединения формулы IA, конкретного состояния, которое необходимо излечить, тяжести состояния, которое необходимо излечить, возраста, веса, общего физического состояния конкретного пациента, другого медикаментозного лечения индивидуума, может производиться и может определяться более точно путем определения уровня в крови или концентрации соединений формулы IA в крови пациента и/или реакции пациента в отношении конкретного состояния, которое подлежит лечению.
Пациенты, которые имеют положительную реакцию на ВИЧ, но не имеют симптомов, обычно могут лечиться более низкими пероральными дозами (от около 0,2 до около 100 мг/кг/день). Пациенты с ARC (комплекс, связанный со СПИД) и со СПИДом должны обычно лечиться с помощью более высоких пероральных доз (от около 1 до около 500 мг/кг/день).
Пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения формулы IA по настоящему изобретению могут быть использованы в сочетании (или последовательно) с другими антивирусными агентами, такими как AZT, ddI, ddC, с ненуклеозидными анти-СПИД агентами, такими как те, которые описаны в N 08/400095, кассета 4788.1, CP, подано 7 марта 1995 года, Международной патентной публикации N WO 91/09849, опубликованной 11 июля 1991 года, и Международной патентной публикации N WO 93/01181, опубликованной 21 января 1993 года, а также с ингибиторами протеазы.
Полезность пиримидин-тиоалкильных и алкилэфирных анти-СПИД соединений формулы IA по настоящему изобретению может быть определена по их способности к ингибированию обратной транскриптазы вирусов, фермента, необходимого для репликации вируса иммунодефицита человека. Этот фермент обладает характеристиками, которые отличают его от других известных клеточных полимераз, и он является уникальным ферментом, который не обнаруживают в неинфицированных клетках. Обратную транскриптазу вирусов (дикого типа) обнаруживают в экстрактах из бактериальных клонов, полученных в соответствии со способом, описанным в AIDS Virus Reverse Transcriptase defined by high level expression in Escherichia coli, EMBO J. 6:3133-3137 (1987). Обратную транскриптазу вирусов P236L получают в соответствии с PNAS 90: 4713-4717 (1993). Ингибирование этого фермента определяют клеточным свободным анализом, по которому измеряют уровень радиоактивных предшественников, включенных в ДНК. Экстракты, приготовленные в соответствии со способом Science, 1125-1129 (1981), инкубируют в смеси ингибитора, 20 мМ дитиотреитола, 60 мМ хлорида натрия, 0,05% NP-40, 10 мМ хлорида магния, 50 мМ Трис-буфера с pH 8,3, 10 мкМ [35S]-меченного деоксинуклеозид-5'-трифосфата, 10 мкг/мл матрицы РНК (поли rC или поли rG) и 5 мкг/мл праймера ДНК (олиго dG или олиго dT) в течение 30 минут при 37oC. Включение радиоактивно-меченного предшественника определяют с помощью отбора аликвот реакционной смеси, вызывающих пятна на бумаге DE81, промываниями бумаги для удаления несвязанного предшественника, сушки и определяющего счета. Результаты (IC50 означает концентрацию, лекарство в мкМ, необходимую для ингибирования активности обратной транскриптазы (P236L и дикого типа) до степени в 50%) различных анализов объединяют и представляют как % ингибирования и/или IC50 (рассчитано) в таблице I (P236L) и таблице II (дикий тип).
ОБОЗНАЧЕНИЯ И ОПРЕДЕЛЕНИЯ
Определения и пояснения ниже относятся к терминам, которые используются во всем документе, включая как описание, так и формулу изобретения.
1. ОПРЕДЕЛЕНИЯ ДЛЯ ФОРМУЛ И ОБОЗНАЧЕНИЯ ДЛЯ ПЕРЕМЕННЫХ
Химические формулы, представляющие различные соединения и молекулярные фрагменты в описании и в формуле изобретения, могут содержать взаимозаменяемые заместители, помимо четко определенных структурных признаков. Эти взаимозаменяемые заместители указаны буквой или буквой с последующим нижним индексом, например "Z1" или "Ri", где "i" является целым числом. Эти взаимозаменяемые заместители являются либо одновалентными, либо двухвалентными, то есть они представляют собой группу, связанную с соединением данной формулы с помощью одной или двух химических связей. Например, группа Z1 может представлять двухвалентную переменную, если она присоединена к соединению формулы CH3-C(= Z1)H. Группы Ri и Rj могут представлять одновалентные взаимозаменяемые заместители, если они присоединены к соединению формулы CH3-CH2-C(Ri)(Rj)H. Когда химические формулы записаны в линию, как формулы выше, взаимозаменяемые заместители, содержащиеся в скобках, присоединяются к атому непосредственно слева от взаимозаменяемого заместителя, окруженного скобками. Когда два или более последовательных взаимозаменяемых заместителя заключены в скобки, каждый из последовательных взаимозаменяемых заместителей присоединен к непосредственно предшествующему атому слева, который не заключен в скобки. Таким образом, в формуле выше как Ri, так и Rj присоединены к предшествующему атому углерода.
Химические формулы или их части, записанные в линию, представляют атомы в линейной цепи. Символ "-" обычно представляет связь между двумя атомами в цепи. Так, CH3-O-CH2-CH(Ri)-CH3 представляет 2-замещенное 1-метоксипропановое соединение. Подобным же образом, символ "=" представляет двойную связь, например CH2= C(Ri)-O-CH3, а символ ″≡″ представляет тройную связь, например HC≡C-CH(Ri)-CH2-CH3. Карбонильные группы изображены одним из двух способов: -CO- или -C(=O)-, причем первое является предпочтительным из-за простоты.
Химические формулы циклических (кольцевых) соединений или молекулярных фрагментов могут быть представлены в линию. Так, соединение 4-хлор-2-метилпиридин может быть представлено в линию как N*=C(CH3)-CH=CCl-CH=C*H при условии, что атомы, обозначенные звездочкой (*), связаны друг с другом с образованием кольца. Подобным же образом циклический молекулярный фрагмент 4-(этил)-1-пиперазинил может быть представлен как -N*-(CH2)2-N(C2H5)-CH2-C*H2.
Жесткая циклическая (кольцевая) структура для любого из рассматриваемых соединений определяет ориентацию по отношению к плоскости кольца для заместителей, присоединенных к каждому атому углерода жесткого циклического соединения. Для насыщенных соединений, которые имеют два заместителя, присоединенных к атому углерода, который является частью циклической системы, -C(X1)(X2)-, два заместителя могут быть либо в аксиальном, либо в экваториальном положении по отношению к кольцу и могут изменять свое положение как аксиальное/экваториальное. Однако положение двух заместителей по отношению к кольцу и друг к другу остается фиксированным. В то время как один из заместителей время от времени может скорее лежать в плоскости кольца (экваториально), чем выше или ниже этой плоскости (аксиально), один из заместителей всегда находится над другим. В химических структурных формулах, изображающих такие соединения, заместитель (X1), который "ниже" другого заместителя (X2), будет обозначаться как находящийся в альфа (α) конфигурации и обозначаться с помощью штриховой, штрихпунктирной или пунктирной линии присоединения к атому углерода, то есть с помощью символа "---" или "...". Соответствующий заместитель, расположенный "выше" (X2) другого (X1), определяется как находящийся в бета (β) конфигурации и обозначается с помощью непрерывной линии присоединения к атому углерода.
Когда взаимозаменяемый заместитель является двухвалентным, валентности могут быть взяты вместе или по отдельности, или обоими способами при определении переменной. Например, взаимозаменяемый заместитель Ri, присоединенный к атому углерода как -C(=Ri)-, может быть двухвалентным и определяться как оксо или кето (таким образом, образуя карбонильную группу (-CO-)), или как два по отдельности присоединенных одновалентных взаимозаменяемых заместителя α-Ri-j и β-Ri-k. Когда двухвалентный взаимозаменяемый заместитель Ri определяется как состоящий из двух одновалентных взаимозаменяемых заместителей, используемое обозначение для определения двухвалентного взаимозаменяемого заместителя представляет собой форму "α -Ri-j: β-Ri-k" или какой-либо ее вариант. В таком случае как α-Ri-j, так и β-Ri-k присоединены к атому углерода с образованием -C(α -Ri-j) (β-Ri-k)-. Например, когда двухвалентный взаимозаменяемый заместитель R6, -C(= R6)- определяется как состоящий из двух одновалентных взаимозаменяемых заместителей, два одновалентных взаимозаменяемых заместителя являются α-R6-1: β-R6-2, ... ... α-R6-9: β-R6-10 и тому подобное, давая -C(α -R6-1)(β -R6-2)-, ... ... -C(α -R6-9)(β -R6-10)- и тому подобное. Подобно этому, для двухвалентного взаимозаменяемого заместителя R11, -C(= R11)-, два одновалентных взаимозаменяемых заместителя являются α-R11-1: β-R11-2. Для кольцевого заместителя, для которого отдельные ориентации α и β не существуют (например, из-за присутствия углеродной двойной связи в кольце), и для заместителя, присоединенного к атому углерода, который не является частью кольца, продолжает использоваться указанное выше обозначение, но обозначения α и β не используются.
Именно потому что двухвалентный взаимозаменяемый заместитель может определяться как два отдельных одновалентных взаимозаменяемых заместителя, два отдельных одновалентных взаимозаменяемых заместителя могут быть определены как взятые вместе с образованием двухвалентного взаимозаменяемого заместителя. Например, в формуле -C1(Ri)H-C2(Rj)H- (C1 и C2 определяют произвольным образом первый и второй атом углерода соответственно) Ri и Rj могут быть определены как взятые вместе с образованием (1) второй связи между C1 и C2 или (2) двухвалентной группы, такой как окса (-O-) и тем самым формула описывает эпоксид. Когда Ri и Rj, взятые вместе, образуют более сложный фрагмент, такой как группа -X-Y-, тогда ориентация фрагмента является такой, что C1 в формуле выше присоединен к X и C2 присоединен к Y. Таким образом, в принятых обозначениях обозначение ". . . Ri и Rj, взятые вместе с образованием -CH2-CH2-O-CO-. . . ", обозначает лактон, в котором карбонил связан с C2. Однако, когда обозначается ". ..Ri и Rj, взятые вместе с образованием -CO-O-CH2-CH2-...", обозначение относится к лактону, в котором карбонил соединен с C1.
Содержание атомов углерода во взаимозаменяемых заместителях обозначается одним из двух способов. По первому способу используется приставка для полного имени переменной, такая как "C1-C4", где как "1", так и "4" являются целыми числами, представляющими минимальное и максимальное число атомов углерода во взаимозаменяемом заместителе. Приставка отделяется от переменной пробелом. Например, "C1-C4 алкил" представляет алкил с от 1 до 4 атомов углерода (включая его изомерные формы, если не имеется указания на обратное). Там, где дается единственная такая приставка, полное содержание атомов углерода в переменной является определенным. Так, C2-C4 алкоксикарбонил описывает группу CH3-(CH2)n-O-CO-, где n равно нулю, единице или двум. С помощью второго способа содержание атомов углерода только в каждой части определения обозначается по отдельности путем применения обозначения "Ci-Cj" в скобках и расположения его непосредственно (без пробела) перед той частью определения, которая определяется. С помощью этого необязательного обозначения (C1-C3)алкоксикарбонил имеет то же самое значение, как и C2-C4 алкоксикарбонил, поскольку "C1-C3" относится только к содержанию атомов углерода в алкоксигруппе. Подобно этому, хотя как C2-C6 алкоксиалкил, так и (C1-C3)алкокси(C1-C3)алкил, определяют алкоксиалкильные группы, содержащие от 2 до 6 атомов углерода, два определения отличаются, поскольку первое определение позволяет либо алкокси, либо алкильной части самим по себе содержать 4 или 5 атомов углерода, в то время как второе определение ограничивает любую из этих групп до 3 атомов углерода.
Когда формула изобретения содержит достаточно сложный (циклический) заместитель, в конце фразы указывается/обозначается, что конкретный заместитель будет обозначением (в скобках), которое будет соответствовать тому же самому названию/обозначению в схемах, которое будет также представлять химическую структурную формулу этого конкретного заместителя.
II. ОПРЕДЕЛЕНИЯ
Все температуры обозначены в градусах Цельсия.
ТСХ означает тонкослойную хроматографию.
Хроматография означает хроматографию при давлении окружающей среды на силикагеле.
ТГФ означает тетрагидрофуран.
ТБДМС означает трет-бутилдиметилсилил.
Солевой раствор означает водный насыщенный раствор хлорида натрия.
ЯМР означает спектроскопию ядерного магнитного (протонного) резонанса, химические сдвиги приведены в м.д. (δ) относительно тетраметилсилана.
ИК означает инфракрасную спектроскопию.
-φ означает фенил (C6H5).
МС означает масс-спектрометрию, выраженную как m/e или единицы масса/заряд. [M+H]+ означает исходный положительный ион плюс атом водорода. ЭИ означает электронный импульс. ХИ означает химическую ионизацию. FAB означает бомбардировку быстрыми атомами.
Эфир означает диэтиловый эфир.
Галоген означает атом галогена (-Cl, -Br, -F или -I).
Фармацевтически приемлемый относится к таким свойствам и/или веществам, которые являются приемлемыми для пациента с фармакологической/токсикологической точки зрения и для промышленного химика-фармацевта с физической/химической точки зрения по отношению к композиции, препарату, стабильности, приемлемости для пациента и биологической доступности.
Пиридинил означает пиридильный радикал согласно номенклатуре IUPAC. Например, 2-пиридил (пиридиновое кольцо, замещенное в 2-положении).
Когда используются пары растворителей, используемые отношения растворителей даны как объем/объем (о/о).
ВИЧ означает ВИЧ-1 (дикий тип и/или его устойчивые к лекарственным средствам мутанты, например M41L, K65N, K67L, K70R, L74V, V75T, A98F, L100I, K103E, K103N, K103Q, V106A, V108I, E138K, V179D, V179E, Y181C, Y188H, Y188H, G190A, T215Y, T215F, K219Q, K219E, P236L и K238T).
Лечение означает ингибирование ВИЧ вируса и будет различаться в зависимости от инфицированного индивидуума. Для индивидуумов, которые имеют положительную ВИЧ реакцию (инфицированы), но не имеют симптомов, пиримидин-тиоалкильные соединения формулы I будут замедлять или предотвращать появление симптомов. Для индивидуумов, которые имеют положительную ВИЧ реакцию, у которых симптомы проявлены и которые страдают от СПИДа или ARC, пиримидин-тиоалкильные производные формулы IA будут замедлять или предотвращать наступление "последней стадии СПИДа". Для индивидуумов, которые имеют "последнюю стадию СПИДа", пиримидин-тиоалкильные и алкилэфирные производные формулы IA будут продлевать время жизни этих индивидуумов.
Пиримидин-тиоалкильные и алкилэфирные соединения формулы I (а также формул IA и/или IB) включают альфа-замещенные пиримидин-тиоалкильные и алкилэфирные соединения. Все указания на "пиримидин-тиоалкильные и алкилэфирные соединения" и "пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения" включают "альфа-замещенные пиримидин-тиоалкильные и алкилэфирные соединения" и "альфа-замещенные пиримидин-тиоалкильные и алкилэфирные анти-СПИД соединения", если специально не указано иного.
ПРИМЕРЫ
Без дальнейших уточнений предполагается, что специалист в данной области может, используя предшествующее описание, осуществить настоящее изобретение в его наиболее полном объеме. Последующие подробные примеры описывают то, как получить различные соединения и/или осуществить различные способы по настоящему изобретению, и предусмотрены как исключительно иллюстративные, и не являются ограничениями предшествующего описания каким-либо образом. Специалист в данной области легко обнаружит соответствующие изменения в способах как в отношении реагентов, так и в отношении условий и способов проведения реакций.
ПРИМЕР 1. Получение 4-амино-6-гидрокси-2-(2,6- дифторфенилметилтио)пиримидина (Соед. N 1)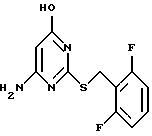
Моногидрат 4-амино-6-гидрокси-2-меркаптопиримидина (1,61 г, 10,0 ммоль) суспендируют в 50% этаноле (10 мл), затем обрабатывают твердым гидроксидом натрия (440 мг, 11,0 ммоль) и перемешивают до тех пор, пока твердый продукт не растворится. Добавляют 2,6-дифторбензилбромид (2,17 г, 10,5 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 1,5 часов. После охлаждения до 22oC твердый продукт собирают, промывают водой, затем сушат на воздухе. Указанное в заголовке соединение перекристаллизовывают из этанола, т.пл. 245-246oC.
Следуя общему способу примера 1 и производя несущественные изменения, но используя соответствующий галогенид, синтезируют соединения, представленные в табл. 1.
ПРИМЕР 34. Получение 4-амино-6-хлор-2- 2,6-дифторфенил-метилтио)пиримидина (Соед. N 34)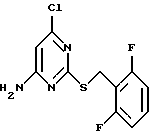
4-амино-6-гидрокси-2-(2,6-дифторфенилметилтио)пиримидин (1,33 г, 4,94 ммоль; Соед. N 1) и 2-пиколин (0,5 мл) нагревают с обратным холодильником с дефлегмацией POCl3 (6 мл) в течение ночи. После удаления избыточного растворителя в вакууме остаток обрабатывают на льду, а затем нагревают с обратным холодильником в течение 30 минут. Водный слой декантируют, затем остаток обрабатывают избытком NH4OH и нагревают с обратным холодильником в течение 30 минут. После охлаждения твердый продукт собирают и промывают водой, затем перекристаллизовывают из толуола, т.пл. 154oC.
Следуя общему способу примера 34 и производя несущественные изменения, но используя соответствующий гидроксипиримидин, синтезируют соединения, представленные в табл. 2.
ПРИМЕР 67. Получение 4-амино-6-хлор-2-(3-бромфенилметилсульфинил)пиримидина (Соед. N 67)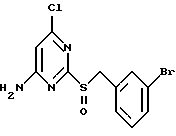
4-Амино-6-хлор-2-(3-бромфенилметилтио)-пиримидин (165 мг, 0,5 ммоль; Соед. N 43) в метиленхлориде (10 мл) обрабатывают 50% mCPBA (172 мг, 0,50 ммоль) и перемешивают в течение 17 часов. Твердый продукт собирают путем фильтрования, промывают эфиром и сушат, т.пл. 216-217oC.
Следуя способу примера 67 и производя несущественные изменения, но используя в качестве исходного продукта 4-амино-6-хлор-2-(2-нафтилметилтио)-пиримидин (Соед. N 59), получают соединение 4-амино-6-хлор-2-(2-нафтилметилсульфинил)-пиримидин (Соед. N 68) (т.пл. 222-223oC).
ПРИМЕР 69. Получение 4-амино-6-хлор-2-(3-бромфенилметилсульфонил)-пиримидина (Соед. N 69)
4-Амино-6-хлор-2-(3-бромфенилметилтио)-пиримидин (660 мг, 2,0 ммоль; Соед. N 43) в уксусной кислоте (5 мл) обрабатывают 30% H2O2 (1 мл) и перемешивают при комнатной температуре в течение 72 часов. Сырой продукт разбавляют этилацетатом, промывают водой, насыщенным NaHCO3 и насыщенным солевым раствором, сушат MgSO4 затем концентрируют в вакууме. Продукт очищают путем хроматографии, используя 1:1 этилацетат/гексан, т.пл. 191-192oC.
ПРИМЕР 70. Получение 4-амино-5-бром-6-хлор-2-(2-нафтилметилтио)-пиримидина (Соед. N 70)
4-Амино-6-хлор-2-(2-нафтилметилтио)-пиримидин (302 мг, 1,0 ммоль; Соед. N 59) и NaHCO3 (100 мг, 1,2 ммоль) растворяют в 50% метаноле (3 мл) и обрабатывают по каплям раствором брома в метаноле (0,92 М, 1,2 мл, 1,1 ммоль). Реакционную смесь обесцвечивают насыщенным NaHSO3 и экстрагируют этилацетатом. Органические фракции промывают водой, сушат MgSO4, затем концентрируют в вакууме. Продукт очищают путем хроматографии, используя 15:85 этилацетат/гексан, т.пл. 158oC.
Следуя общему способу примера 67 и производя несущественные изменения, из 4-амино-6-хлор-2-(2-пиридилметилтио)-пиримидина (Соед. N 55) получают 4-амино-5-бром-6-хлор-2-(2-пиридилметилтио)-пиримидин (Соед. N 71; т.пл. 119-120oC).
ПРИМЕР 72. Получение 4,6-дигидрокси-2-(фенилметилтио)-пиримидина
Тиобарбитуровую кислоту (5,22 г, 36,2 ммоль) в этаноле (52 мл) обрабатывают 3,25 М NaOH (11,1 мл, 36,2 ммоль), и смесь нагревают с обратным холодильником в течение 30 минут. После быстрого охлаждения к реакционной смеси добавляют бензилбромид (4,3 мл, 36,2 ммоль) и раствор нагревают с обратным холодильником в течение одного часа. Реакционную смесь охлаждают и концентрируют в вакууме и полученный твердый продукт фильтруют и промывают холодной H2O, затем холодным этанолом, т.пл. >320oC.
Следуя общему способу примера 72 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий дигидроксипиримидинтион, синтезируют соединения, представленные в табл. 3.
ПРИМЕР 78. Получение 4,6-дихлор-2-(бензилтио)-пиримидина (Соед. N 78)
2-(Бензилтио)-4,6-дигидроксипиримидин (5,95 г, 25,4 ммоль; Соед. N 72) обрабатывают POCl3 (26 мл) и нагревают с обратным холодильником в течение 2 часов. Реакционную смесь охлаждают и избыток POCl3 удаляют путем перегонки в вакууме. Горячий остаток выливают на лед и водный слой нейтрализуют с твердым NaOH до pH 7-8. Водный раствор экстрагируют этилацетатом три раза и объединенные органические слои промывают разбавленным NaOH и насыщенным солевым раствором, затем сушат MgSO4. Раствор фильтруют и концентрируют в вакууме, затем очищают путем перегонки, т.к. (0,2 мм рт.ст.) 155-160oC с получением указанного в заголовке соединения.
ЯМР: (CDCl3) 7,43 (м, 2H), 7,29 (м, 3H), 7,02 (с, 1H), 4,37 (с, 2H).
Следуя общему способу примера 78 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий дигидроксипиримидин, синтезируют соединения, представленные в табл. 4.
ПРИМЕР 84. Получение 4-пиперидо-6-хлор-2-(бензилтио)-пиримидина, Соед. N 84
4,6-Дихлор-2-(бензилтио)-пиримидин (261 мг, 0,96 ммоль; Соед. 78) растворяют в метиленхлориде (3 мл), обрабатывают триэтиламином (0,17 мл, 1,20 ммоль) и пиперидином (0,10 мл, 1,06 ммоль) и перемешивают при комнатной температуре в течение 60 часов. Реакционную смесь гасят насыщенным NH4Cl, промывают насыщенным NaHCO3, сушат MgSO4 и концентрируют в вакууме. Образец очищают путем хроматографии, используя 1:3 этилацетат/гексан, т.пл. 85-86oC.
Следуя общему способу примера 84 и производя несущественные изменения, но используя в качестве исходного продукта соответствующим образом замещенный амин, синтезируют соединения, представленные в табл. 5.
ПРИМЕР 89. Получение 4-амино-5-метокси-6-хлор-2-(2-нафтил-метилтио)-пиримидина (Соед.N 89)
4,6-Дихлор-5-метокси-2-(2-нафтилметилтио)-пиримидин (1,40 г, 4,0 ммоль; Соед. N 79) растворяют в ацетонитриле (10 мл), обрабатывают концентрированным гидроксидом аммония (2 мл), затем нагревают до 120oC в герметично закрытой трубке в течение 2,5 часов. После охлаждения продукт фильтруют, промывают водой и сушат, т.пл. 115-117oC.
Следуя общему способу примера 89 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий дихлорпиримидин, синтезируют соединения, представленные в табл. 6.
ПРИМЕР 94. Получение 4-амино-2-(2-пиридилметилтио)-пиримидина (Соед. N 94)
4-Амино-2-меркаптопиримидин (0,40 г, 3,15 ммоль) суспендируют в этаноле (2 мл), и добавляют 3,25 М NaOH (2,0 мл, 6,5 ммоль). Раствор нагревают с обратным холодильником в течение 10 минут и после охлаждения до 22oC добавляют 2-пиколилхлорид•HCl (0,49 г, 2,98 ммоль). Раствор нагревают с обратным холодильником в течение дополнительных 15 минут. Раствор охлаждают и концентрируют в вакууме. Остаток растворяют в 1 н HCl и разбавляют этилацетатом. Смесь нейтрализуют NaOH до pH 8 и водный слой отделяют и промывают дважды этилацетатом. Объединенные органические слои промывают насыщенных NaHCO3, насыщенным NaCl, сушат с MgSO4 и концентрируют в вакууме, т.пл. 133-134oC.
Следуя общему способу примера 94 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий тиол, синтезируют соединения, представленные в табл. 7.
ПРИМЕР 103. Получение 4-амино-6-хлор-2-(1-нафтилметилокси)-пиримидина;
1-Нафталинметанол (227 мг, 1,44 ммоль) добавляют к суспензии 50% гидрида натрия (69 мг, 1,44 ммоль) в сухом ТГФ (4 мл) при 0oC. После перемешивания в течение 30 минут добавляют 4-амино-2,6-дихлорпиримидин (157 мг, 0,96 ммоль) и перемешивают при 22oC в течение 72 часов. Раствор гасят насыщенным NH4Cl и концентрируют в вакууме. Остаток растворяют в метиленхлориде и промывают 3 раза насыщенным NaHCO3, сушат с MgSO4, фильтруют и концентрируют в вакууме. Образец очищают путем хроматографии, используя 1:2 этилацетат/гексан и перекристаллизовывают из смеси гептан/толулол, т.пл. 160-161oC.
Следуя общему способу примера 103 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий спирт, синтезируют соединения, представленные в табл. 8.
ПРИМЕР 108. Получение 4-амино-6-хлор-2-(3-гидроксифенилметилтио)-пиримидина.
4-Амино-6-хлор-2-(3-метоксифенилметилтио)-пиримидин (36 мг, 0,128 ммоль; Соед. N 39) растворяют в метиленхлориде (0,25 мл), охлаждают до 0oC и обрабатывают раствором BBr3 (0,32 мл, 0,32 ммоль, 1 моль в метиленхлориде). Реакционную смесь перемешивают при 0oC в течение 20 минут, затем нагревают с обратным холодильником в течение 2 часов. После охлаждения реакцию гасят водой и нагревают с обратным холодильником в течение дополнительных 30 минут. При охлаждении твердый продукт собирают и очищают путем перекристаллизации из смеси этанол/вода, т.пл. 147,5-148,5oC.
ПРИМЕР 109. Получение 4-амино-6-хлор-2-(3-изопропоксифенилметилтио)-пиримидина (Соед. N 108)
4-Амино-6-хлор-2-(3-гидроксифенилметилтио)-пиримидин (135 мг, 0,50 ммоль; Соед. 108) добавляют к раствору КОН (280 мг, 5 ммоль) в ДМСО (2,5 мл) при комнатной температуре. Добавляют 2-бромпропан (615 мг, 5 ммоль) и реакционную смесь перемешивают в течение ночи, затем выливают в воду. Водный раствор экстрагируют этилацетатом, сушат с MgSO4, фильтруют и концентрируют в вакууме. Образец очищают путем хроматографии, используя 1:3 этилацетат/гексан, т.пл. 71oC.
ПРИМЕР 110. Получение 4-амино-6-хлор-2-тиопиримидина (Соед. N 110)
4-Амино-6-хлор-2-(4-метоксифенилметилтио)-пиpимидин (11,0 г, 39,15 ммоль; Соед. N 93) и трифторуксусную кислоту (84 мл) нагревают с обратным холодильником в течение 20 часов, затем избыток растворителя удаляют в вакууме. Образец растирают в порошок с хлороформом, затем перемешивают с эфиром и фильтруют. Твердый продукт промывают эфиром, затем сушат на воздухе, т.пл. >320oC.
ПРИМЕР 110A. Получение мезилатной соли 4-амино-6-хлор- 2-тиопиримидина;
Соед. N 110A. Мезилат 4-амино-6-хлор-2-меркаптопиримидина
Суспензию 4-амино-6-хлор-2-(4-метоксифенилметилтио)-пиримидина (10,0 г, 33,22 ммоль) в 160 мл метиленхлорида при комнатной температуре обрабатывают метансульфоновой кислотой (31,89 г, 332,2 ммоль, 10 эквив.) за один прием. После того как ТСХ анализ покажет отсутствие исходного продукта (около 50 мин), сначала добавляют по каплям 1280 мл диэтилового эфира. Когда объем белого твердого продукта становится достаточно большим, очень быстро добавляют оставшийся Et2O. Суспензию перемешивают в течение ночи и продукт собирают путем фильтрования и промывают диэтиловым эфиром с получением 8,62 г указанного в заголовке соединения (Температура плавления 166-167oC). Анализ: Рассчитано для C5H8ClN3O3S2•4,94% H2O; C, 23,22; H, 3,16; N, 16,25. Найдено: C, 23,48; H, 3,25; N, 15,70.
ПРИМЕР 111. Получение 4-амино-6-хлор-2-[2-(4-хлор)пиридилметилтио]-пиримидина (Соед. N 111)
4-Амино-6-хлор-2-тиопиримидин (Соед. N 110; 614 мг, 2,38 ммоль) в этаноле (1,5 мл) обрабатывают 3,25 М NaOH (1,47 мл, 4,8 ммоль) и смесь нагревают до 50oC. Добавляют 4-хлор-2-хлорметилпиридин и раствор перемешивают, подогревая, в течение 1 часа. Реакционную смесь охлаждают и концентрируют в вакууме и полученный твердый продукт фильтруют и промывают водой, затем холодным этанолом, т.пл. 195oC.
Следуя общему способу примера 111 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий хлорметиларен, синтезируют соединения, представленные в табл. 9.
ПРИМЕР 163. Получение 4-амино-6-хлор-2-[2-(4-карбоксамидо)пиридилметилтио]-пиримидина (Соед. N 163)
4-Амино-6-хлор-2-[2-(4-карбометокси)пиридилметилтио] -пиримидин (100 мг, 0,32 ммоль) и свежеперегнанный формамид (48 мг, 1,06 ммоль) растворяют в ТГФ (0,5 мл) и раствор нагревают с обратным холодильником. Добавляют метоксид натрия (25%, 24 мкл, 0,107 ммоль) и смесь нагревают с обратным холодильником в течение 1 часа. Реакционную смесь охлаждают и фильтруют через целит, затем концентрируют в вакууме. Полученный твердый продукт растирают в порошок с ацетоном. т.пл. 191-192oC.
ПРИМЕР 164. Получение 4-амино-6-хлор-2-[2-(4-гидроксиметил)пиридилметилтио]-пиримидина (Соед. N 164)
Литийалюминийгидрид (12 мг, 0,32 ммоль) суспендируют в ТГФ (1 мл) и охлаждают до 0oC. Суспензию затем обрабатывают раствором 4-амино-6-хлор-2-[2-(4-карбометокси)пиридилметилтио] -пиримидина (100 мг, 0,32 ммоль) в ТГФ (0,5 мл). Раствору дают нагреться до комнатной температуры и перемешивают в течение 1 часа. Реакцию гасят водой (1 капля), 1н NaOH (1 капля) и водой (3 капли) и разбавляют этилацетатом. Реакционную смесь сушат с MgSO4 и концентрируют в вакууме. Полученный твердый продукт растирают в порошок с этилацетатом, т.пл. 117-118oC.
Следуя общему способу примера 70 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий 4-амино-6-хлор-2-[2-(4-замещенный)пиридилметилтио]пиримидин, синтезируют соединения, представленные в табл. 10.
Следуя общему способу примера 111 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий хлорметиларен, синтезируют соединения, представленные в табл. 11.
Следуя общему способу примера 72 и производя несущественные изменения, но используя в качестве исходного продукта соответствующий дигидроксипиримидинтион, синтезируют следующее соединение:
Пр. /Соед. N 190 4,6-дигидрокси-5-фтор-2-[2-(4-хлор)пиридилметилтио]пиримидин
ЯМР: (ДМСО) 8,48 (д, J = 5,5, 1H), 7,71 (с, 1H), 7,44 (с, 1H), 4,44 (с, 2H)
Следуя общему способу примера 78 и производя несущественные изменения, но используя в качестве исходного
продукта соответствующий дигидроксипиримидин, синтезируют следующее соединение:
Пр. /Соед. N 191 4,6-дихлор-5-фтор-2-[2-(4-хлор)пиридилметилтио]пиримидин
ЯМР: (CDCl3) 8,54 (д, J=5,5, 1H), 7,77 (с, 1H), 7,39 (д, J=5,4, 1H), 4,59 (с, 2H)
ПРИМЕР 193. Метиловый эфир (E)-4-[(4-амино-6-хлор-2-пиримидинил)тио]-2-бутеновой кислоты (Соед. N 193)
4-Амино-6-хлор-2-меркаптопиримидин мезилат (0,30 г, 1,16 ммоль) растворяют в 3,25 н гидроксиде натрия (2 мл) и этаноле (1 мл) при температуре окружающей среды с последующим добавлением метил-4-бромкротоната (0,16 мл, 1,40 ммоль). Реакционную смесь перемешивают в течение от 2 до 15 часов, гасят избытком воды, экстрагируют метиленхлоридом (2 х 25 мл). Экстракты объединяют, промывают соляным раствором (25 мл), сушат над сульфатом натрия, концентрируют в вакууме и перекристаллизовывают из смеси гексан/этилацетат с получением Соед. N 193, т.пл. 146-149oC.
ПРИМЕР 194. (E)-N,N-Диэтил-4-[(4-амино-6-хлор-2-пиримидинил)тио]-2-бутенамид (Соед. N 194)
4-Хлоркротонилхлорид (1,36 г, 9,80 ммоль) в эфире (20 мл) объединяют с диэтиламином в эфире (5 мл) при -15oC в колбе, высушенной на огне. Реакционную смесь нагревают до температуры окружающей среды, перемешивают в течение от 1 до 2 часов, гасят водой (30 мл), экстрагируют этилацетатом (2 х 30 мл), промывают солевым раствором (30 мл), сушат над сульфатом натрия и концентрируют в вакууме с получением сырого 4-хлор-N,N-диэтилкротонамида.
Следуя общему способу примера 193 и производя несущественные изменения, но замещая сырой 4-хлор-N,N-диэтилкротонамид (1,72 г, 9,80 ммоль) цис/транс-1,3-дихлор-2-бутеном, получают указанное в заголовке соединение, т.пл. 143-145oC.
ПРИМЕР 195. (E)-4-метил-1-[4-[(4-амино-6-хлор-2-пиримидинил)тио] -1- оксо-2-бутенил]пиперазин (Соед. N 195)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин 1-метилпиперазином (2,15 г, 21,50 ммоль), получают указанное в заголовке соединение, т.пл. 155-156oC.
ПРИМЕР 196. (E)-N-этил-4-[(4-амино-6-хлор-2-пиримидинил)тио] -2- бутенамид (Соед. N 196)
Следуя общему способу ПРИМЕРА 194 и производя несущественные изменения, но замещая диэтиламин этиламином (0,73 г, 16,17 ммоль), получают указанное в заголовке соединение, т.пл. 160-161oC.
ПРИМЕР 197. (E)-1-[4-((4-амино-6-хлор-2-пиримидинил)тио]-1- оксо-2-бутенил]пиперидин (Соед. N 197)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин пиперидином (1,38 г, 16,17 ммоль), получают указанное в заголовке соединение, т.пл. 159-163oC.
ПРИМЕР 198. (E)-4-[4-[(4-амино-6-хлор-2-пиримидинил)тио]-1- оксо-2-бутенил]морфолин (Соед. N 198)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин морфолином (1,41 г, 16,17 ммоль), получают указанное в заголовке соединение, т.пл. 154-157oC.
ПРИМЕР 199. (E)-1-[4-[(4-амино-6-хлор-2-пиримидинил)тио]-1- оксо-2-бутенил]пирролидин (Соед. N 199)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин пирролидином (1,15 г, 16,17 ммоль), получают указанное в заголовке соединение, т.пл. 178-180oC.
ПРИМЕР 200. (E)-N-метил-N-фенил-4-[(4-амино-6-хлор-2- пиримидинил)тио] -2-бутенамид (Соед. N 200)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин N-метиланилином (2,31 г, 21,56 ммоль), получают указанное в заголовке соединение, т.пл. 152-154oC.
ПРИМЕР 201. (E)-N-аллил-N-метил-4-[(4-амино-6-хлор-2- пиримидинил)тио] -2-бутенамид (Соед. N 201)
Следуя общему способу примера 194 и производя несущественные изменения, но замещая диэтиламин N-метилаллиламином (1,15 г, 16,17 ммоль), получают указанное в заголовке соединение, т.пл. 140-142oC.
ПРИМЕР 202. (E)-N,N-Дипропил-4-[(4-амино-6-хлор-2- пиримидинил)тио]-2-бутенамид (Соед. N 202)
4-Хлоркротонилхлорид (1,02 г, 7,35 ммоль) в эфире (10 мл) объединяют с дипропиламином (1,64 г, 16,17 ммоль) в эфире (5 мл) при -15oC в колбе, высушенной на огне. Реакционную смесь нагревают до температуры окружающей среды, перемешивают в течение от 1 до 2 часов, гасят водой (30 мл), экстрагируют этилацетатом (2 х 30 мл), промывают солевым раствором (30 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя смесью гексан/этилацетат (60/40). Соответствующие фракции объединяют (Rf = 0,53, ТСХ, гексан/этилацетат, 25/75) и концентрируют в вакууме с получением 4-хлор-N,N-дипропил-кротонамида. 4-Амино-6-хлор-2-меркаптопиримидинмезилат (0,30 г, 1,16 ммоль) растворяют в ДМФ (5 мл) и гидриде натрия (0,06 г, 2,55 ммоль) при температуре окружающей среды с последующим добавлением 4-хлор-N,N-дипропилкротонамида (0,23 г, 1,13 ммоль). Реакционную смесь перемешивают в течение от 2 до 15 часов, гасят избытком воды, экстрагируют этилацетатом (3 х 20 мл). Экстракты объединяют, промывают солевым раствором (20 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя гексан/этилацетатом (60/40). Соответствующие фракции объединяют (Rf = 0,40, ТСХ, гексан/этилацетат, 25/75) и концентрируют в вакууме с получением указанного в заголовке соединения, т.пл. 139-142oC.
ПРИМЕР 203. (E)-N-этил-N-метил-4-[(4-амино-6-хлор-2- пиримилинил)тио]-2-бутенамид (Соед. N 203)
Следуя общему способу примера 202 и производя несущественные изменения, но замещая дипропиламин N-этилметиламином (0,87 г, 14,70 ммоль), получают указанное в заголовке соединение, т.пл. 170-172oC.
ПРИМЕР 204. (E)-N,N-Диметил-4-[(4-амино-6-хлор-2- пиримидинил)тио]-2-бутенамид (Соед. N 204)
Следуя общему способу примера 202 и производя несущественные изменения, но замещая дипропиламин диметиламином (0,50 г, 11,03 ммоль), получают указанное в заголовке соединение, т.пл. 173-176oC.
ПРИМЕР 205. (E)-N,N-Диэтил-4-оксо-2-пентенамид
В колбе, высушенной на огне, содержащей (E)-4-оксо-2-пентеноилхлорид (1,16 г, 8,76 ммоль), в эфире, охлажденном до -15oC, добавляют диэтиламин (1,41 г, 19,28 ммоль) в эфире (5 мл) и перемешивают в течение 2 часов при подогреве до температуры окружающей среды. Растворители удаляют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя гексан/этилацетатом (75/25). Соответствующие фракции объединяют (Rf = 0,31, ТСХ, гексан/этилацетат, 25/75) и концентрируют в вакууме с получением указанного в заголовке соединения, ЯМР (CDCl3) 7,15, 7,04, 3,45, 3,40, 2,33, 1,20, 1,15.
ПРИМЕР 206. (E)-N,N-Диэтил-4-гидрокси-2-пентенамид
К (E)-N, N-диэтил-4-оксо-2-пентенамиду (0,73 г, 4,31 ммоль) в метаноле (10 мл), охлажденному до 0oC, добавляют боргидрид натрия (0,18 г, 4,75 ммоль), перемешивают в атмосфере азота в течение 30 минут, гасят избытком воды и экстрагируют этилацетатом (3 х 50 мл). Органические экстракты объединяют, промывают солевым раствором (50 мл), сушат над сульфатом натрия, концентрируют в вакууме с получением указанного в заголовке соединения, ЯМР (CDCl3) 6,89, 6,42, 4,49, 3,41, 2,51, 1,33, 1,17.
ПРИМЕР 207. (E)-N, N-Диэтил-4-[(4-амино-6-хлор-2- пиримидинил)тио]-2-пентенамид (Соед. N 207)
К (E)-N, N-Диэтил-4-гидрокси-2-пентенамиду (0,67 г, 3,93 ммоль) в метиленхлориде, охлажденном до -15oC, в колбе, высушенной на огне, добавляют дихлортрифенилфосфоран (1,40 г, 4,33 ммоль). Реакционную смесь нагревают до температуры окружающей среды, гасят путем добавления льда (10 мл), экстрагируют метиленхлоридом (3:20 мл), промывают солевым раствором (30 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя гексан/этилацетатом (75/25). Соответствующие фракции объединяют (Rf = 0,48, ТСХ, гексан/этилацетат, 25/75) и концентрируют в вакууме с получением (E)-4-хлор-N,N-диэтил-2-пентенамида. 4-Амино-6-хлор-2-меркаптопиримидинмезилат (0,56 г, 2,19 ммоль) растворяют в ДМФ (4 мл) и гидриде натрия (0,12 г, 4,82 ммоль) при температуре окружающей среды с последующим добавлением (E)-4-хлор-N,N-диэтил-2-пентенамида (0,41 г, 2,19 ммоль). Реакционную смесь перемешивают в течение 15 часов, гасят избытком воды, экстрагируют этилацетатом (3 х 25 мл). Экстракты объединяют, промывают солевым раствором (25 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя градиентом гексан/этилацетата (80/20-60/40). Соответствующие фракции объединяют (Rf = 0,27, ТСХ, гексан/этилацетат, 25/75) концентрируют в вакууме с получением указанного в заголовке соединения, т.пл. 152-153oC.
ПРИМЕР 208. Метиловый эфир (E)-4-[(4-амино-6-хлор-2-пиримидинил)тио]-3-метил-2-бутеновой кислоты (Соед. N 208)
К метиловому эфиру (E)-4-гидрокси-3-метил-2-бутеновой кислоты (0,75 г, 5,76 ммоль) в метиленхлориде, охлажденном до -15oC, в колбе, высушенной на огне, добавляют дибромтрифенилфосфоран (2,68 г, 6,34 ммоль). Реакционную смесь перемешивают при -15 - 0oC в течение двух часов, гасят путем добавления льда (10 мл), экстрагируют метиленхлоридом (2 х 10 мл), промывают солевым раствором (10 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя гексан/этилацетатом (95/5). Соответствующие фракции объединяют и концентрируют в вакууме с получением метилового эфира (E)-4-хлор-3-метил-2-бутеновой кислоты. 4-Амино-6-хлор-2-меркаптопиримидинмезилат (0,30 г, 1,16 ммоль) растворяют в ДМФ (4 мл) и гидриде натрия (0,06 г, 2,56 ммоль) при температуре окружающей среды с последующим добавлением метилового эфира (E)-4-бром-3-метил-2-бутеновой кислоты (0,22 г, 1,16 ммоль). Реакционную смесь перемешивают в течение 15 часов, гасят избытком воды, экстрагируют этилацетатом (3 х 20 мл). Экстракты объединяют, промывают солевым раствором (20 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя гексан/этилацетатом (80/20). Соответствующие фракции объединяют (Rf = 0,43, ТСХ, гексан/этилацетат, 50/50) и концентрируют в вакууме с получением указанного в заголовке соединения, т. пл. 134-136oC.
ПРИМЕР 209. Метиловый эфир (E)-4-[(4-амино-6-хлор-2-пиримидинил)тио]-3-метил-2-пентеновой кислоты (Соед. N 209)
К метиловому эфиру (E)-4-гидрокси-3-метил-2-пентеновой кислоты (1,00 г, 6,94 ммоль) в метиленхлориде, охлажденном до -15oC, в колбе, высушенной на огне, добавляют дихлортрифенилфосфоран (2,47 г, 7,63 ммоль). Реакционную смесь нагревают до температуры окружающей среды, гасят путем добавления льда (10 мл), экстрагируют метиленхлоридом (2 х 10 мл), промывают солевым раствором (10 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 75 мл), элюируя гексан/этилацетатом (95/5). Соответствующие фракции объединяют (Rf = 0,55, ТСХ, гексан/этилацетат, 75/25) и концентрируют в вакууме с получением метилового эфира (E)-4-хлор-3-метил-2-пентеновой кислоты. 4-Амино-6-хлор-2-меркаптопиримидинмезилат (0,30 г, 1,16 ммоль) растворяют в ДМФ (4 мл) и гидриде натрия (0,06 г, 2,56 ммоль) при температуре окружающей среды с последующим добавлением метилового эфира (E)-4-хлор-3-метил-2-пентеновой кислоты (0,19 г, 1,16 ммоль). Реакционную смесь перемешивают в течение 15 часов, гасят избытком воды, экстрагируют этилацетатом (3 х 15 мл). Экстракты объединяют, промывают солевым раствором (15 мл), сушат над сульфатом натрия, концентрируют в вакууме и хроматографируют на силикагеле (230-400 меш, 100 мл), элюируя смесью гексан/этилацетат (85/15). Соответствующие фракции объединяют (Rf = 0,18, ТСХ, гексан/этилацетат, 50/50) и концентрируют в вакууме с получением указанного в заголовке соединения, т.пл. 124-126oC.
ПРИМЕР 210. 4-Амино-6-хлор-2-(1-(4-(1,1-диметил)этил-2- пиридил)этил)тиопиримидин (Соед. N 210)
Часть A: 4-Трет-Бутил-пиридин-N-оксид
4-Трет-бутил-пиридин (14,8 мл, 100 ммоль) растворяют в 35 мл ледяной уксусной кислоты в атмосфере азота в 200 мл одногорлой круглодонной колбе. Раствор нагревают до 95-100oC, обрабатывают 30% перекисью водорода (28 мл, 274 ммоль) и перемешивают 6 часов. Реакционную смесь обрабатывают по частям параформальдегидом до тех пор, пока не будет получена отрицательная реакция на крахмальной йодидной бумаге. Летучие продукты удаляют в вакууме, и остаток азеотропно отгоняют с 2 х 100 мл толуола. Остаток распределяют между 1 х 100 мл дихлорметана и 2 х 75 мл насыщенного бикарбоната натрия. Водный слой подвергают обратной промывке 3 х 50 мл дихлорметана. Объединенные органические слои сушат над сульфатом магния и концентрируют в вакууме с получением 14,5 г (96%) 4-трет-бутил-пиридин-N-оксида в виде бледно-желтого твердого продукта.
1H-ЯМР (CDCl3, ТМС): δ 1,32 (с, 9), 7,27 (м, 2), 8,15 (м, 2) м.д.
13C-ЯМР (CDCl3): δ 30,3; 34,4; 122,9; 138,3; 150,7 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,42, 10% метанол/дихлорметан.
Температура плавления 93-95oC.
Инфракрасный спектр (νmax, минеральное масло): 3098, 2924, 1685, 1488, 1466, 1250, 1183, 825 см-1.
Масс-спектр: Рассчитано для C9H13NO: 151,0997. Найдено: 151,0993.
Анализ: Рассчитано для C9H13NO: C, 71,49; H, 8,67; N,9,26. Найдено: C, 71,10; H, 9,17; N,9,20.
Часть B:
4-Трет-бутилпиридин-N-оксид (11,0 г, 72,9 ммоль) растворяют в 200 мл дихлорметана в атмосфере азота в 500-мл одногорлой круглодонной колбе. Раствор обрабатывают тетрафторборатом триметилоксония (10,8 г, 72,9 ммоль), перемешивают 1 час при комнатной температуре, и летучие продукты удаляют в вакууме. Твердый остаток растворяют в 200 мл метанола в 500-мл одногорлой круглодонной колбе. Раствор нагревают с обратным холодильником, обрабатывают персульфатом аммония (3,3 г, 14,5 ммоль) в 15 мл воды, и реакционную смесь интенсивно нагревают с обратным холодильником в течение 30 мин. Реакционную смесь обрабатывают второй частью персульфата аммония (1,65 г, 7,2 ммоль) в 7 мл воды и нагревают с обратным холодильником в течение дополнительного 1 часа. Реакционную смесь охлаждают и объем метанола удаляют в вакууме. Остаток разбавляют 300 мл конц. гидроксида аммония, и смесь экстрагируют 4 х 100 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 400 г силикагеля (230-400 меш), элюируя 40% смесью ацетон/гексан, собирая 50-мл-вые фракции. Фракции 26-52 объединяют и концентрируют с получением 8,79 г (73%) 4-трет-бутил-2-гидроксиметилпиридина в виде желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,31 (с, 9), 3,99 (ушир.с, 1), 4,75 (с, 2), 7,18 (м, 1), 7,27 (м, 1), 8,43 (м, 1) м.д.
13C-ЯМР (CDCl3): δ 30,5; 34,7; 64,5; 117,6; 119,5; 148,3; 159,2; 161,0 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,31, 40% ацетон/гексан.
Инфракрасный спектр (νmax, минеральное масло): 3233, 2966, 1606, 1552, 1479, 1405, 1066 см-1.
Масс-спектр: Рассчитано для C10H15NO: 165,1154, Найдено: 165,1147.
Часть C:
4-Трет-бутил-2-гидроксиметилпиридин (4,13 г, 25 ммоль) растворяют в 75 мл диоксана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают диоксидом селена (1,53 г, 13,75 ммоль) и реакционную смесь нагревают до 80-85oC в течение 1 час. Смесь охлаждают, разбавляют дихлорметаном и фильтруют через целит. Отфильтрованную лепешку тщательно промывают дихлорметаном, и фильтрат концентрируют до янтарного масла. Сырое масло пропускают через 50 г слоя силикагеля (230-400 меш), элюируя 20% смесью ацетон/гексан, собирая 100-мл-вые фракции. Фракции 1-3 объединяют и концентрируют с получением 3,91 г (96%) 4-трет-бутил-2-пиридинкарбоксальдегида в виде светло-янтарного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,36 (с, 9), 7,53 (м, 1), 7,99 (м, 1), 8,70 (м, 1), 10,10 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 30,3; 35,0; 118,7; 124,9; 150,1; 152,7; 161,5; 193,8 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,62, 40% ацетон/гексан.
Инфракрасный спектр (νmax, жидкость): 2968, 1712, 1597, 1481, 1367, 1210, 822 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [324] (71).
Часть D:
Бромид метилмагния (9,7 мл, 29 ммоль) добавляют к 20 мл сухого тетрагидрофурана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи при 0oC. Раствор обрабатывают 4-трет-бутил-2-пиридинкарбоксальдегидом (3,8 г, 23,3 ммоль) в 2 х 5 мл диэтилового эфира, а затем 10 мл диэтилового эфира. Реакционную смесь нагревают до комнатной температуры, а затем до температуры, при которой происходит орошение, в течение 1 час. Смесь охлаждают до 0oC, гасят 1 х 20 мл 10% соляной кислоты и устанавливают pH 9 2н гидроксидом натрия. Слои отделяют, водный слой экстрагируют дихлорметаном 4 х 25 мл, и объединенные органические слои сушат над карбонатом калия. Сухие органические слои концентрируют в вакууме с получением 3,9 г (93%) 4-трет-бутил-2-(1-гидроксиэтил)-пиридина в виде желтовато-коричневого твердого продукта. Аналитический продукт получают путем перекристаллизации из гексана.
1H-ЯМР (CDCl3, ТМС): δ 1,31 (с, 9), 1,50 (д, J=6,5 Гц, 3), 4,10 (ушир.с, 1), 4,87 (кв, J=6,5, 13 Гц, 1), 7,18 (м, 1), 7,26 (м, 1), 8,41 (м, 1) м.д.
13C-ЯМР (CDCl3): δ 24,3; 30,4; 34,7; 69,1; 116,4; 119,4; 147,8; 160,9; 162,9 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,37, 40% ацетон/гексан.
Температура плавления 85-86oC.
Инфракрасный спектр (νmax, минеральное масло): 3158, 2925, 1608, 1551, 1409, 1341, 1093, 1069 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [179] (10), [164] (100).
Анализ: Рассчитано для C11H17NO: C, 73,70; H, 9,56; N, 7,82. Найдено: C, 73,79; H, 9,91; N, 7,74,
Часть E:
4-трет-Бутил-2-(1-гидроксиэтил) пиридин (3,6 г, 20,1 ммоль) растворяют в 60 мл дихлорметана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (2,2 мл, 30 ммоль) в 10 мл дихлорметана, и реакционную смесь перемешивают 1 час при 0oC, затем 2 часа при комнатной температуре. Реакционную смесь гасят 1 х 75 мл насыщенного бикарбоната натрия, слои разделяют, и водный слой экстрагируют дихлорметаном 3 х 25 мл. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 3,9 г (98%) 4-трет-бутил-2-(1-хлорэтил)пиридина в виде желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,33 (с, 9), 1,89 (д, J=6,5 Гц, 3), 5,14 (кв, J= 6,5, 13 Гц, 1), 7,21 (м, 1), 7,44 (м, 1), 8,47 (м, 1) м.д.
13C-ЯМР (CDCl3): δ 24,7; 30,2; 34,6; 59,0; 117,8; 119,9; 148,7; 160,2; 161,0 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,61, 40% ацетон/гексан.
Масс-спектр: Рассчитано для C11H16ClN-CH3: 182,0747, Найдено: 182,0736,
Часть F:
Мезилатную соль 4-амино-6-хлор-2-тиопиримидина (1,29 г, 5 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают 60% гидридом натрия (400 мг, 10 ммоль) (экзотерм. ), и смесь перемешивают 1 час 1-(1-хлорэтил)-5,6,7,8-тетрагидроизохинолин (978 мг, 5 ммоль) в 2 х 2 мл сухого диметилформамида, добавляют к реакционной смеси, и смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь выливают в 100 мл 50% насыщенного хлорида натрия и экстрагируют этилацетатом 4 х 25 мл. Объединенные органические слои подвергают обратной промывке 50% насыщенным хлоридом натрия 4 х 50 мл. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 120 г силикагеля (230-400 меш), элюируя 25% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 16-27 объединяют и концентрируют с получением белой пены. Кристаллизация из диэтилового эфира дает 888 мг (55%) 1-амино-4-хлор-2-(1-(4-(1,1-диметил)этил-2-пиридил)этил)тиопиримидина в виде белого твердого продукта.
1H-ЯМР (CDCl3, ТМС): δ 1,30 (с, 9), 1,76 (д, J=6,5 Гц, 3), 5,10 (кв, J= 6,5, 13 Гц, 1), 5,53 (ушир.с, 1), 6,10 (с, 1), 7,14 (м, 1), 7,45 (м, 1), 8,46 (м, 1) м.д.
13C-ЯМР (CDCl3): δ 21,0; 30,4; 34,7; 45,5; 99,1; 119,2; 119,5; 148,9; 159,2; 160,7; 161,4; 163,3; 171,4 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,49, 40% ацетон/гексан.
Температура плавления 153-154oC, раз.
Ультрафиолетовый спектр (λmax, этанол), нм (ε): 230 (22,700); 255 (12,200); 268 (8,790); 286 (7,000).
Инфракрасный спектр ( νmax, минеральное масло): 3177, 3140, 2925, 1642, 1565, 1527, 1368, 1280, 825 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [322] (8), [289] (100).
Анализ: Рассчитано для C15H19ClN4S: C 55,80; H, 5,93; N, 17,35. Найдено: C, 55,74; H, 5,90; N, 17,16.
ПРИМЕР 211. 4-Амино-6-хлор-2-(1-(2-пиридил)этил)тиопиримидин (Соед. N 211)
Часть A:
К суспензии 4,6-дигидрокси-2-(2-пиридилметил)тиопиримидина (7,0 г, 0,0298 моль) в 105 мл диметилформамида при комнатной температуре добавляют имидазол (5,06 г, 0,0744 моль, 2,5 эквив.), затем трет-бутилдиметилсилилхлорид (9,48 г, 0,0626 моль, 2,10 эквив.). Реакционную смесь перемешивают в течение 2,5 часов, выливают в 350 мл воды и экстрагируют дважды эфиром. Объединенные органические экстракты сушат с безводным Na2SO4 и концентрируют при пониженном давлении. Сырой продукт растворяют в смеси этилацетат/метиленхлорид/метанол, обрабатывают 37 г силикагеля и концентрируют до сыпучего порошка. Его вводят с набивкой в верхнюю часть колонки с набивкой из силикагеля (350 г) и элюируют смесью этилацетат/гексан (1/10) с получением 7,81 г (56%) 4,6-ди-(трет-бутилдиметилсилилокси)-2-(2-пиридилметил) тиопиримидина.
ТСХ (силикагель GF): Rf = 0,38 этилацетат/гексан (1/9).
1H-ЯМР (CDCl3, ТМС): δ\ 8,55 (д, 1H, J=5,01 Гц), 7,64 (дт, 1H, J=1,8, 7,72 Гц), 7,47 (д, 1H, J=7,86 Гц), 7,20 (т, 1H, J=16,72 Гц), 5,70 (с, 1H), 4,52 (с, 2H), 0,930 (с, 18H), 0,265 (с, 12H) м.д.
Часть B:
Раствор н-бутиллития (11,02 мл, 17,63 ммоль, 1,2 эквив., 1,6 М в гексане) в 60 мл тетрагидрофурана охлаждают до -78oC, обрабатывают по каплям диизопропиламином (1,93 г, 19,10 ммоль, 1,3 эквив.) в течение двухминутного периода. После перемешивания в течение следующих 10 минут добавляют по каплям раствор 4,6-ди-(трет-бутилдиметилсилилокси)-2-(2-пиридилметил)тиопиримидина (6,80 г, 14,69 ммоль) в 16 мл тетрагидрофурана в течение 10 минутного периода. Реакционную смесь медленно перемешивают в течение 30 минут и обрабатывают по каплям метилйодидом (2,29 г, 16,16 ммоль, 1,1 эквив. ) в 6 мл тетрагидрофурана в течение 3 мин периода. Перемешивание облегчают путем добавления дополнительных 30 мл тетрагидрофурана. Через час после добавления метилйодида охлаждающую баню удаляют, и смеси дают нагреться до комнатной температуры. Содержимое затем выливают в воду со льдом и экстрагируют один раз этилацетатом. Органический слой промывают насыщенным солевым раствором, сушат с безводным Na2SO4 и концентрируют при пониженном давлении. Раствор сырого продукта в метиленхлориде обрабатывают силикагелем (36 г), концентрируют до сыпучего порошка и вводят в верхнюю часть колонки с набивкой из 350 г силикагеля, и элюируют смесью этилацетат/гексан (5/95) с получением 2,23 г (32%) 4, 6-ди-(трет-бутилдиметилсилилокси)-2-(1-(2- пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,50 этилацетат/гексан (1/9).
1H-ЯМР (CDCl3, ТМС): δ 8,49 (д, 1H, J=4,80 Гц), 7,54 (дт, 1H, J=1,81, 7,68 Гц), 7,31 (д, 1H, J=7,84 Гц), 7,06 (т, 1H, J=4,93 Гц), 5,59 (с, 1H), J= 5,01 (кв, 1H, J= 7,04 Гц), 1,71 (д, 3H, J=7,02 Гц), 0,90-0,82 (м, 18H), 0,28-0,17 (м, 12H) м.д.
Масс-спектр: M/Z (относительная интенсивность %): 477 (5), 462 (6), 444 (79), 420 (100), 315 (34), 257 (16).
Часть C:
Раствор 4, 6-ди-(трет-бутилдиметилсилилокси)-2-(1-(2-пиридил)этил)тиопиримидина (1,23 г, 2,58 ммоль) в 8 мл тетрагидрофурана обрабатывают 2н HCl (5,2 мл, 10,31 ммоль, 4,0 эквив.) при комнатной температуре. Через 30 минут реакционную смесь непосредственно концентрируют при пониженном давлении, разбавляют толуолом и снова повторно концентрируют. Полученный белый твердый продукт растирают в порошок с метиленхлоридом, собирают и сушат с получением 0,819 г сырого 4,6-дигидрокси-2-(1-(2-пиридил)этил)тиопиримидингидрохлорида.
ТСХ (силикагель GF): Rf = 0,32 хлороформ/метанол (4/1).
1H-ЯМР (d6-ДМСО, ТМС): δ 8,55 (ушир.с, 1H), 7,80 (м, 1H), 7,53 (д, 1H, J= 7,72 Гц), 7,31 (м, 1H), 5,15 (кв, 1H, J=7,04 Гц), 4,35 (с, 1H), 3,72-3,26 (ушир.с, 1H), 1,66 (д, 3Н, J=6,95 Гц) м.д.
Часть D:
Сырой диолгидрохлорид (0,735 г, 2,58 ммоль) обрабатывают 2-пиколином (0,446 г, 4,80 ммоль, 1,86 эквив.), затем оксихлоридом фосфора (4,39 г, 28,7 ммоль, 11,1 эквив. ). Содержимое перемешивают при 90oC на масляной бане в течение 2,25 часов и при температуре окружающей среды в течение следующих 1,75 часа. Реакционную смесь гасят размельченным льдом, затем насыщенным раствором NaHCO3 до тех. пор, пока она не станет щелочной, затем экстрагируют дважды этилацетатом. Объединенные органические экстракты сушат с Na2SO4 и концентрируют при пониженном давлении. Хроматографию выполняют, используя 125 г силикагеля, с набивкой и элюированием смесью этилацетат/гексан (1/6), с получением 0,569 мг (73%) 4,6-дихлор-2-(1-(2-пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf=0,50 этилацетат/гексан (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,56 (д, 1H, J=3,11 Гц), 7,61 (т, 1H, J=7,60 Гц), 7,41 (д, 1H, J=7,86 Гц), 7,14 (м, 1H), 6,96 (с, 1 H), 5,08 (кв, 1H, J=7,12 Гц), 1,76 (д, 3H, J=7,07 Гц) м.д.
Масс-спектр: M/Z (относительная интенсивность %): HRMS
Рассчитано: 284,9894. Найдено 284,9905.
Часть E:
Колбу загружают 4,6-дихлор-2-(1-(2-пиридил)этил)тиопиримидином (0,560 г, 1,96 ммоль), ацетонитрилом (6,5 мл) и 13 мл 29% NH4OH. Содержимое перемешивают при 35oC в течение 15 часов, выливают в 50 мл воды, экстрагируют один раз этилацетатом. Органический слой промывают насыщенным солевым раствором (1 х 30 мл), сушат с безводным Na2SO4 и концентрируют в вакууме. Хроматографию выполняют на 100 г силикагеля с набивкой и элюированием смесью этилацетат/гексан (2/3), с получением 0,491 г (94%) 4-амино-6-хлор-2-(1-(2-пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,23 этилацетат/гексан (1/1).
Температура плавления 125-126oC.
1H-ЯМР (CDCl3, ТМС): δ 8,56 (м, 1H), 7,64 (т, 1H, J=7,71 Гц), 7,46 (д, 1H, J=7,82 Гц), 7,17 (м, 1H), 6,09 (с, 1H), 5,48 (ушир.с, 2H), 5,12 (кв, 1H, J=7,16), 1,74 (д, 3H, J=7,16 Гц) м.д.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,000), 255 (12,500), 269sh (8580), 287 (6920).
Инфракрасный спектр ( νmax, минеральное масло): см-1. 1572, 1531, 2925, 1275, 2954, 1594, 1117, 1293, 3089, 2855, 1665, 1359, 1372, 803, 3133, 1467, 2868, 1436, 1477, 1255, 988, 3269, 3011, 1454, 1443,
Масс-спектр: M/Z (относительная интенсивность %): 266 (6), 233 (100), 171 (6), 138 (26), 126 (12), 106 (98), 78 (61).
Анализ: Рассчитано для C11H11ClN4S: C 49,62; H, 4,13; N, 21,05, Найдено: C, 49,46; H, 4,18; N, 20,45.
ПРИМЕР 212. 4-Амино-6-хлор-2-(1-(2-пиридил)-1-метилэтил)тиопиримидин (Соед. N 212)
Следуя способу получения 4-амино-6-хлор-2-(1-(2-пиридил)этил)тиопиримидина, но применяя соответствующее алкилирование 4,6-ди-(трет-бутилдиметилсилилокси)-2-(1-(2-пиридил)этил)тиопиримидина метилйодидом, получают это соединение. Температура плавления 183-184,5oC.
ПРИМЕР 213. 4-Амино-6-хлор-2-(1-(2-(4-метил)пиридил)-1- метилэтил)тиопиридин (Соед. N 213)
Следуя способу получения 4-амино-6-хлор-2-(1-(2-пиридил)-1-метилэтил)тиопиримидина и начиная с 4,6-дигидрокси-2-(2-(4-метил)пиридилметил)тиопиримидина, получают это соединение. Температура плавления 149-151oC.
ПРИМЕР 214. 4-Амино-6-хлор-2-(1-(4-циано-2-пиридил)этил)тиопиримидин (Соед. N 214)
Часть A:
Раствор 4-цианопиридина (5,20 г, 50,0 ммоль) в 90 мл метанола обрабатывают смесью H2SO4 (6,42 г, 65,5 ммоль, 1,31 эквив.) и воды (45 мл) за один раз с последующим добавлением (NH4)2S2O8 (22,8 г, 100 ммоль, 2,0 эквив.). Содержимое нагревают с обратным холодильником, при этом осуществляют энергичную перегонку с обратным холодильником в течение нескольких минут. После перегонки с обратным холодильником в течение 24 часов реакционную смесь частично концентрируют до удаления большей части метанола, обрабатывают смесью лед-вода и подщелачивают гидроксидом аммония (20 мл, 29% водн.). Остаток экстрагируют четыре раза хлороформом, объединенные экстракты сушат с безводным Na2SO4 м концентрируют при пониженном давлении. Хроматографию выполняют, используя 300 г силикагеля с набивкой и элюированием смесью ацетон/метиленхлорид (1/6), с получением 2,65 г (39,5%) 4-циано-2-гидроксиметилпиридина.
ТСХ (силикагель GF): Rf = 0,30 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,78 (д, 1H, J=5,07 Гц), 7,66 (с, 1H), 7,49 (д, 1H, J= 5,12 Гц), 4,88 (д, 2H, J=4,96 Гц), 3,64 (т, 1H, J=5,21 Гц). Ультрафиолетовый спектр ( λmax, этанол): 216 sh (7,710), 220 sh (6,590), 280 (3,510), 287 sh (3,020).
Анализ: Рассчитано для C7H6N2O: C, 62,69; H, 4,48; N, 20,89. Найдено: C, 62,66; H, 4,46; N, 21,00.
Масс-спектр: M/Z (относительная интенсивность %): 134 (73), 133 (100), 105 (79), 104 (39), 77(38), 50 (30).
Часть B:
Колбу загружают 4-циано-2-гидроксиметилпиридином (2,60 г, 19,40 ммоль) и диоксидом селена (1,19 г, 10,75 ммоль, 0,554 молярн. эквив.) в 40 мл п-диоксана, и смесь нагревают на масляной бане при 80-85oC в течение 3,5 часов. Содержимое разбавляют 150 мл метиленхлорида, обрабатывают целитом и после перемешивания при температуре окружающей среды в течение примерно 15 мин фильтруют через пад из целита. Фильтрат концентрируют в вакууме, получая 2,77 г желтого твердого продукта, который хроматографируют на 125 г силикагеля с набивкой и элюированием смесью ацетон/метиленхлорид/гексан (0,5/1,5:8), с получением 2,32 г (90%) 4-циано-2-пиридинкарбоксальдегида в виде белого твердого продукта.
ТСХ (силикагель GF): Rf = 0,17 ацетон/метиленхлорил/гексан (0,5/1,5/8).
1H-ЯМР (CDCl3, ТМС): δ 9,93 (с, 1H), 8,82 (д, 1H, J=4,28 Гц), 8,00 (с, 1H), 7,60 (дд, 1H, J=4,84, 1,48 Гц).
Температура плавления 95-97oC.
Ультрафиолетовый спектр ( λmax, этанол): 219 sh (7,130), 276 (3,460), 283 sh (2,990).
Анализ: Рассчитано для C7H4N2O: C, 63,64; H, 3,03; N, 21,21. Найдено: C, 63,42; H, 2,95; N, 21,26.
Масс-спектр: M/Z (относительная интенсивность %): (FAB) [M + H]+ 133 (100), 104 (22), 77 (67).
Часть C:
В колбу, загруженную 70 мл эфира и 40 мл тетрагидрофурана, охлажденного на ледяной бане при 0-5oC, добавляют метилмагнийбромид (8,71 мл, 26,14 ммоль, 1,50 эквив.) за один раз. К этому по каплям добавляют раствор 4-циано-2-пиридинкарбоксальдегида (2,30 г, 17,42 ммоль), растворенного в 60 мл эфира и 5 мл тетрагидрофурана, в течение 20 мин периода. Полученную желтовато-коричневую суспензию нагревают с обратным холодильником в течение 1,5 часов, охлаждают и выливают в ледяную воду, содержащую 55 мл 3 н HCl, и перемешивают при температуре окружающей среды в течение 5 минут. Содержимое подщелачивают 23 мл 29% гидроксида аммония и экстрагируют 5 раз хлороформом. Объединенные органические экстракты сушат над Na2SO4 и концентрируют при пониженном давлении. Хроматографируют на 160 г силикагеля с набивкой и элюированием смесью ацетон/метиленхлорид (1/6), получая 1,60 г (62%) 4-циано-2-(2-гидрокси)этилпиридина.
ТСХ (силикагель GF): Rf = 0,27 ацетон/метиленхлорид (1/6).
1H-ЯМР (CDCl3, ТМС): δ 8,46 (д, 1H, J=4,33 Гц), 7,41 (с, 1H), 7,20 (дд, 1H, J= 4,87, 0,82 Гц), 4,72 (кв, 1H, J=6,08 Гц), 3,75 (с, 1H), 1,28 (д, 3H, J=6,55 Гц).
Ультрафиолетовый спектр ( λmax, этанол): 216 sh (7,760), 220 sh (6,530), 278 (3,560), 287 sh (2,960).
Анализ: Рассчитано для C8H8N2O: C, 64,86; H, 5,41; N, 18,92. Найдено: C, 64,77; H, 5,51; N, 18,90.
Масс-спектр: M/Z (относительная интенсивность %): (FAB) [M+H]+ 149 (100), 131(30), 105 (8).
Часть D:
К раствору 4-циано-2-(2-гидрокси)этилпиридина (1,44 г, 9,73 ммоль) в 55 мл метиленхлорида при комнатной температуре добавляют метансульфонилхлорид (1,16 г, 10,22 ммоль, 1,05 эквив.), затем триэтиламин (1,08 г, 10,70 ммоль, 1,1 эквив. ). После перемешивания в течение 1 час содержимое концентрируют непосредственно при пониженном давлении и полученный твердый продукт, 4-циано-2-(2-метансульфонил)этилпиридин, используют непосредственно в последующей реакции связывания.
ТСХ (силикагель GF): Rf = 0,69, ацетон/метиленхлорид (1/6).
Часть E:
К перемешиваемой суспензии NaH (0,817 г, 20,43 ммоль, 2,1 эквив., 60% масляная дисперсия) в 35 мл диметилформамида при комнатной температуре за один раз добавляют мезилатную соль 4-амино-6-хлор-2-тиопиримидина (2,50 г, 9,73 ммоль) в виде твердого продукта. Через 50 мин за один раз добавляют суспензию 4-циано-2-(2-метансульфонил)этилпиридина (2,20 г, 9,73 ммоль, 1,0 эквив. ) в 15 мл диметилформамида с промывкой 2 х 5 мл того же растворителя. Через 24 часа реакционную смесь быстро выливают в 200 мл воды со льдом плюс 50 мл насыщенного солевого раствора, экстрагируют дважды этилацетатом и объединенные органические экстракты сушат с безводным Na2SO4. Фильтрат концентрируют в вакууме, хроматографируют на 200 г силикагеля с набивкой и элюированием смесью ацетон/метилен (1/9), с получением 2,32 г в виде золотистого масла, загрязненного диметилформамидом. Повторная хроматография с использованием 150 г силикагеля с набивкой и элюированием этилацетат/гексан (2/3) дает 1,75 г (62%) Соед. N 214 в виде бесцветного масла. Кристаллизацию выполняют, используя смесь растворителей этилацетат/эфир/гексан.
ТСХ (силикагель GF): Rf = 0,50 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, TMC): δ 8,61 (д, 1H, J=5,04 Гц), 7,63 (с, 1H), 7,23 (д, 1H, J=5,03 Гц), 6,00 (с, 1H), 4,97 (м, 3H), 1,61 (д, 3H, J=7,30 Гц).
Температура плавления 119-120oC.
Ультрафиолетовый спектр ( λmax, этанол): 214 sh, (19,100), 222 (23,600), 228 sh (22,300), 249 sh (11,700), 286 (9,860).
Инфракрасный спектр ( νmax, минеральное масло): 1572, 1646, 2927, 1531, 2954, 1366, 1278, 2855, 1546, 1119, 2869, 1469, 3188, 3314, 834, 1457, 825, 1596, 3144, 3216, 1444, 855, 2979, 988, 3378 см-1.
Анализ: Рассчитано для C12H10ClN5S: C, 49,48; H, 3,44; N, 24,05. Найдено: C, 49,31; H, 3,69; N, 23,89.
Масс-спектр: M/Z (относительная интенсивность %): 291 (3), 293 (1), 258 (100), 196 (5), 162 (17), 131 (33), 103 (18) 67 (22).
ПРИМЕР 215. Гидрохлорид 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)этил)тиопиримидина (Соед. N 215)
Раствор 4-пиколин-N-оксида (3,0 г, 27,52 ммоль) в 90 мл метиленхлорида при комнатной температуре взаимодействует с триметилоксонийтетрафторборатом (4,07 г, 27,52 ммоль, 1,0 эквив.) в течение 1,5 часов. Реакционную смесь концентрируют непосредственно при пониженном давлении, белый твердый продукт растворяют в 60 мл метанола при нагреве с обратным холодильником и обрабатывают персульфатом аммония (1,25 г, 5,50 ммоль, 0,20 эквив.) в 5,5 мл воды с еще одним добавлением персульфата аммония (0,625 г, 0,10 эквив.) в 2,5 мл воды через 30 мин. После нагрева с обратным холодильником в течение дополнительных 40 минут содержимое концентрируют при пониженном давлении, обрабатывают 75 мл насыщенного солевого раствора плюс 75 мл воды и, наконец, 50 мл 3н HCl. После перемешивания при комнатной температуре в течение 1 часа смесь подщелачивают с помощью 20 мл 29% гидроксида аммония, экстрагируют 4 раза хлороформом, объединенные органические экстракты сушат с безводным Na2SO4 и концентрируют в вакууме. Хроматография с использованием 250 г силикагеля с набивкой и элюированием смесью ацетон/хлороформ/метанол (1/2/2%) дает 2,65 г (78%) 2-гидроксиметил-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,32 ацетон/хлороформ/метанол (1/2/2%).
1H-ЯМР (CDCl3, TMC): δ 8,38 (д, 1H, J=5,05 Гц), 7,18 (с, 1H), 7,03 (д, 1H, J=4,86 Гц), 5,02 (с, 1H), 4,75 (с, 2H), 2,37 (с, 3Н).
УФ ( λmax, этанол): 254 sh (2,240), 259 (2,690), 266 (2,180).
Анализ: Рассчитано для C7H9NO: C, 68,29; H, 7,32; N, 11,38. Найдено: C, 67,35; H, 7,37; N, 11,22.
Масс-спектр: M/Z (относительная интенсивность %): 123 (48), 122 (100), 94 (43), 93 (30), 92 (27), 39 (17).
Способом, подобным тому, что описан для получения 4-циано-2-пиридинкарбоксальдегида, 2-гидроксиметил-4-метилпиридин (2,60 г, 21,14 ммоль) дает 2,0 г (78%) 4-метил-2-пиридинкарбоксальдегида.
ТСХ (силикагель GF): Rf = 0,23 ацетон/метилен/гексан (0,5/1,5/8,0).
1H-ЯМР (CDCl3, ТМС): δ 10,09 (с, 1H), 8,67 (д, 1H, J=4,93 Гц), 7,81 (с, 1H), 7,38 (д, 1H, J=3,78 Гц), 2,48 (с, 3H).
Способом, подобным тому, что описан для получения 4-циано-2-(2-гидрокси)этилпиридина, 4-метил-2-пиридинкарбоксальдегид (2,0 г, 16,53 ммоль) и метилмагнийбромид (8,30 мл, 24,8 ммоль, 3 М в эфире) дают 1,95 г (86%) 2-(1-гидрокси)этил-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,30 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, TMC): δ 8,27 (д, 1H, J=5,03 Гц), 6,99 (с, 1H), 6,90 (д, 1H, J= 4,83 Гц), 4,74 (кв, 1H, J=6,52 Гц), 4,28 (ушир.с, 1H), 2,26 (с, 3H), 1,38 (д, 3H, J=6,58 Гц).
Температура плавления 76-78oC.
УФ ( λmax, этанол): 253 sh (2,320), 259 (2,810), 265 (2,270).
Анализ: Рассчитано для C8H11NO: C, 70,07; H, 8,03; N, 10,22. Найдено: C, 70,04; H, 8,14; N, 10,08.
Масс-спектр: M/Z (относительная интенсивность %): 137 (7), 136 (14), 122 (100), 120 (46), 93 (38).
2-(2-гидрокси)этил-4-метилпиридин (0,796 г, 5,81 ммоль), метансульфонилхлорид (0,695 г, 6,10 ммоль, 1,05 эквив.) и триэтиламин (0,649 г, 6,39 ммоль, 1,1 эквив.) при концентрировании при пониженном давлении дают 2-(2-метансульфонил)этил-4-метилпиридин, который используют непосредственно в последующем алкилировании.
ТСХ (силикагель GF): Rf = 0,70 ацетон-метиленхлорид (1:2).
Способом, подобным тому, что описан для получения Соед. N 214, мезилатная соль 4-амино-6-хлор-2-тиопиримидина (1,49 г, 5,81 ммоль) взаимодействует с 2-(2-метансульфонил)этил-4-метилпиридином (1,25 г, 5,81 ммоль, 1,0 эквив.) и NaH (0,488 г, 12,20 ммоль, 2,1 эквив., 60% масляная дисперсия) с получением 0,869 г (53%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)этил)тиопиримидина в виде бесцветного масла. Получение соли HCl проводят путем добавления ацетилхлорида (0,28,1 г, 2,93 ммоль, 1,0 эквив.) по каплям к 5 мл метанола, охлажденного на ледяной бане. После перемешивания в течение 25 мин при температуре окружающей среды раствор разбавляют 100 мл эфира и добавляют по каплям к 4-амино-6-хлор-2-(1-(4-метил-2-пиридил) этил) тиопиримидину (0,820 г, 2,93 ммоль, 1,0 эквив.) в 100 мл эфира в течение 20-минутного периода. После перемешивания суспензии в течение 4 часов добавляют 100 мл гексана, перемешивание продолжают в течение еще 2 часов, белый твердый продукт собирают и сушат в вакуумной печи с получением 0,845 г (91%) Соед. N 215. Оставшийся эфир удаляют путем растворения/повторного осаждения из смеси растворителей метиленхлорид-гексан с последующей сушкой при 90oC в вакуумной печи в течение ночи.
Свободное основание: ТСХ (силикагель GF): Rf = 0,26 ацетон-метиленхлорид (1:4).
Соль HCl: 1H-ЯМР (CDCl3, ТМС): δ 8,49 (д, 1H, J=5,96 Гц), 7,75 (с, 1H), 7,50 (д, 1H, J=5,57 Гц), 6,12 (с, 1H), 5,23 (кв, 1H, J=7,42 Гц), 2,56 (с, 3H), 1,69 (д, 3H, J=7,46 Гц).
Температура плавления 149-151oC.
Ультрафиолетовый спектр ( λmax, этанол): 229 (22,000), 254 (12,200), 267 sh (8,570), 287 (6,820).
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1567, 2954, 2854, 1638, 1528, 2869, 1374, 828, 1466, 3163, 3296, 1283, 1254, 3203, 1116, 3093, 3057, 2692, 985, 2538, 657, 1070, 1330, 960 см-1.
Анализ: Рассчитано для C12H14Cl2N4S: C, 45,43; H, 4,42; N, 17,67, Найдено: C, 45,79; H, 4,87; N, 17,28.
Масс-спектр: M/Z (относительная интенсивность %): 280 (8), 247 (100), 211 (2), 185 (5), 152 (33), 120 (93), 92 (36).
ПРИМЕР 216. 4-Амино-6-хлор-2-(1-(4-этил-2-пиридил)этил)тиопиримидин (Соед. N 216)
Раствор 4-этилпиридина (10,7 г, 0,10 моль) в 35 мл уксусной кислоты, нагретый до 95-100oC, обрабатывают по каплям 30% перекисью водорода (28 мл) в течение 18-минутного периода. Через 4 часа избыток перекиси водорода разлагают путем добавления по частям параформальдегида (10,0 г) при
температуре, поддерживаемой ранее, до тех пор, пока не будет получена отрицательная реакция при тесте с использованием йодида крахмала. Реакционную смесь охлаждают и концентрируют при пониженном давлении. Остаток хроматографируют на 325 г силикагеля с набивкой и элюированием сначала смесью ацетон/хлороформ/метанол (3/6,7/0,3), а затем с увеличивающимся градиентом метанола с получением 10,55 г (83%) 4-этилпиридин-1-оксида.
ТСХ (силикагель GF): Rf = 0,20 ацетон/хлороформ/метанол (3/6,5/0,5)
1H-ЯМР (CDCl3, ТМС): δ 7,94 (д, 2H, J=7,00 Гц), 6,93 (д, 2H, J=6,99 Гц), 2,44 (кв, 2H, J=7,61 Гц), 1,06 (т, 3H, J=7,53 Гц).
По способу, подобному тому, что описан для получения 4-гидроксиметил-4-метилпиридина, 4-этилпиридин-1-оксид (3,5 г, 27,56 ммоль) дает 1,64 г (43%) 4-этил-2-гидроксиметилпиридина.
ТСХ (силикагель GF): Rf = 0,09 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,50 (д, 1H, J=5,11 Гц), 7,32 (с, 1H), 7,15 (д, 1H, J= 4,88 Гц), 5,30 (ушир.с, 1H), 4,87 (с, 2H), 2,77 (кв, 2H, J=7,60 Гц), 1,37 (т, 3H, J=7,63 Гц).
Ультрафиолетовый спектр ( λmax, этанол): 254 sh (2,260), 259 (2,710), 264 (2220).
Инфракрасный спектр ( νmax, минеральное масло): 1610, 2969, 3221, 1055, 2935, 1067, 1561, 2877, 839, 1459, 1417, 3059, 2841, 1005, 3020, 1116, 994, 1364, 1481, 746, 2735, 890, 1327, 1264, 902 см-1.
Масс-спектр: M/Z (относительная интенсивность %): (FAB) 138 (100), 120 (28), 106 (4).
По способу, подобному тому, что описан для получения 4-метил-2-пиридинкарбоксальдегида, 4-этил-2-гидроксиметилпиридин (1,60 г, 11,68 ммоль) дает 1,33 г (84%) 4-этил-2-пиридинкарбоксальдегида.
ТСХ (силикагель GF): Rf = 0,23 ацетон/метиленхлорид/гексан (0,5/1,5/8).
1H-ЯМР (CDCl3, ТМС): δ 8,74 (д, 1H, J=4,95 Гц), 7,89 (с, 1H), 7,44 (д, 1H, J=5,08 Гц), 2,82 (кв, 2H, J=7,58 Гц), 1,37 (т, 3H, J=7,65 Гц).
По способу, подобному тому, что описан для синтеза 4-циано-2-(2-гидрокси)этилпиридина, 4-этил-2-пиридинкарбоксальдегид (1,33 г, 9,85 ммоль) и метилмагнийбромид (4,93 мл, 14,78 ммоль, 3 М в эфире) дает 1,29 г (86%) 4-этил-2-(2-гидрокси)этилпиридина в виде бесцветного масла.
ТСХ (силикагель GF): Rf = 0,37 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,19 (д, 1H, J=5,08 Гц), 6,91 (с, 1H), 6,83 (д, 1H, J= 5,11 Гц), 4,65 (кв, 1H, J=6,51 Гц), 4,24 (ушир.с, 1H), 2,45 (кв, 2H, J=7,64 Гц), 1,29 (д, 3H, J=6,57 Гц), 1,06 (т, 3H, J=7,66).
Мезилирование 4-этил-2-(2-гидрокси)этилпиридина (1,29 г, 8,54 ммоль) метансульфонилхлоридом (1,02 г, 8,97 ммоль, 1,05 эквив.) и триэтиламином (0,949 г, 9,39 ммоль, 1,1 эквив.) дает при концентрировании при пониженном давлении 4-этил-2-(2-метансульфонил)этилпиридин, который используют в последующей реакции алкилирования.
ТСХ (силикагель GF): Rf = 0,73 ацетон/метиленхлорид (1/2).
По способу, подобному тому, что описан для получения Соед. N 214, мезилатная соль 4-амино-6-хлор-2-тиопиримидина (2,19 г, 8,54 ммоль), NaH (0,717 г, 17,93 ммоль, 2,1 эквив. 60% масляная дисперсия) и 4-этил-2-(2-метансульфонил)этилпиридин (1,95 г, 8,54 ммоль, 1,0 эквив.) дают 1,27 г (51%) Соед. N 216.
ТСХ (силикагель GF): Rf = 0,22 этилацетат/гексан (1/1).
1H-ЯМР (CDCl3, ТМС): δ\] 8,29 (д, 1H, J=5,06 Гц), 7,15 (с, 1H), 6,84 (д, 1H, J= 5,06 Гц), 5,95 (с, 1H), 5,04 (ушир.с, 2H), 4,94 (кв, 1H, J=7,11 Гц), 2,48 (кв, 2H, J=7,60 Гц), 1,61 (д, 3H, J=7,13 Гц), 1,09 (с, 3H, J=7,59 Гц).
Температура плавления 113-115oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,500), 254 (12,400), 267 sh (8,620), 286 (6,940).
Инфракрасный спектр ( νmax, минеральное масло): 1574, 2926, 1281, 1663, 2954, 1529, 1359, 2855, 1363, 1114, 1560, 3147, 2870, 1608, 1467, 818, 3293, 1257, 988, 823, 836, 1484, 3051, 1209, 1059 см-1.
Анализ: Рассчитано для C13H15ClN4S: C, 53,06; H, 5,10; N, 19,05. Найдено: C, 52,61; H, 5,17; N, 18,84.
Масс-спектр: M/Z (относительная интенсивность %): 294 (6), 261 (87), 166 (40), 134 (100), 119 (67).
ПРИМЕР 217. 4-Амино-6-хлор-2-(1-(4-метил-2-пиридил)-1-цианометил)тиопиримидин (Соед. N 217)
К 4-метил-2-пиридинкарбоксальдегиду (2,10 г, 17,35 ммоль), охлажденному при -10oC, добавляют 2н HCl до тех пор, пока pH не достигнет 3,5. Затем насыщенный водный раствор KCN, охлажденный при -10oC, добавляют по каплям до тех пор, пока не будет достигнут pH 7. Осадок собирают через 10 минут, промывают три раза водой и сушат с получением 1,88 г (73%) 2-( α-циано-4-метил)пиридилкарбинола.
ТСХ (силикагель GF): Rf = 0,17 этилацетат/гексан (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,47 (д, 1H, J=5,09 Гц), 7,38 (с, 1H), 7,22 (д, 1H, J=5,09 Гц), 6,31-5,65 (ушир.с, 1H), 5,58 (с, 1H), 2,45 (с, 3H).
Температура плавления 99-102oC.
Ультрафиолетовый спектр ( λmax, этанол): 243 (3,230), 256 (2,620), 264 (2,260), 275 sh (939), 374 (369).
Инфракрасный спектр ( νmax, минеральное масло) 2924, 1056, 1613, 2854, 2954, 2867, 1013, 839, 3055, 2727, 3026, 1466, 963, 783, 1378, 1284, 1481, 1324, 1302, 604, 1169, 2626, 824, 669, 1411 см-1.
Масс-спектр: M/Z (относительная интенсивность %): 148 (15), 119 (5), 93 (100), 65 (52), 51 (14), 38 (58).
Мезилирование 2-( α -циано-4-метил)пиридилкарбинола (1,00 г, 6,76 ммоль) метансульфонилхлоридом (0,892 г, 7,83 ммоль, 1,16 эквив.) и триэтиламином (0,819 г, 8,11 ммоль, 1,2 эквив. ) дает 2-(1-циано-1-метансульфонилокси)метил-4-метилпиридин в виде темно-красного твердого продукта при концентрировании реакционной смеси при пониженном давлении.
ТСХ (силикагель GF): Rf = 0,76 ацетон/метиленхлорид (1/6).
По способу, подобному тому, что описан для синтеза соединения N 214, мезилатная соль 4-амино-6-хлор-2-тиопиримидина (Соед. N 110A; 1,74 г, 6,76 ммоль), NaH (0,568 г, 14,20 ммоль, 2,1 эквив., 60% масляная дисперсия) и 2-(1-циано-1-метансульфонилоксиметил)-4-метилпиридин (1,53 г, 6,76 ммоль, 1,0 эквив. ) дают 0,927 г (47%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)-1-цианометил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,33 ацетон/метиленхлорид (1/9).
1H-ЯМР (CDCl3, ТМС): δ 8,33 (д, 1H, J=5,00 Гц), 7,28 (с, 1H), 6,97 (д, 1H, J=5,03 Гц), 6,08 (с, 1H), 5,80 (с, 1H), 5,15 (ушир.с, 2H), 2,24 (с, 3H).
Температура плавления 145-146,5oC.
Ультрафиолетовый спектр ( λmax, этанол): 225 (27,700), 246 sh (12,000), 266 sh (6,640), 285 (6,860), 312 sh (1,730).
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1573, 1637, 1531, 2954, 2965, 2855, 1288, 1373, 1607, 1272, 1464, 2869, 832, 3445, 1128, 3322, 3192, 986, 3216, 841, 3161, 850, 605, 3062 см-1.
Анализ: Рассчитано для C12H10ClN5S: C, 49,48; H, 3,44; N, 24,05. Найдено: C, 49,25; H, 3,41; N, 23,87.
Масс-спектр: M/Z (относительная интенсивность %): 291 (32), 260 (33), 258 (100), 233 (8), 163 (15), 136 (16).
ПРИМЕР 218. 4-Амино-6-хлор-2-(1-(4-метил-2-пиридил)пропил)тиопиримидин (Соед. N 218)
4-Метил-2-пиридинкарбоксальдегид (1,21 г, 10,0 ммоль) и этилмагнийбромид (15,0 мл, 15,0 ммоль, 1,5 эквив. 1 М в ТГФ) дают 0,776 г (51%) 2-(1-гидроксипропил)-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,28 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,48 (д, 1H, J=5,06 Гц), 7,20 (с, 1H), 7,11 (д, 1H, J= 5,05 Гц), 4,75 (т, 1H, J=7,12 Гц), 4,55 (ушир.с, 1H), 2,48 (с, 3H), 2,07-1,91 (м, 1H), 1,91-1,74 (м, 1H), 1,06 (т, 3H, J=5,09 Гц).
Ультрафиолетовый спектр ( λmax, этанол): 254 sh (2,320), 259 (2,800), 265 (2,280).
Инфракрасный спектр ( νmax, минеральное масло): 1610, 2965, 2934, 825, 3374, 3258, 984, 2876, 1454, 1462, 1127, 1052, 1564, 1095, 3056, 1428, 1407, 1003, 3019, 1379, 1477, 1328, 1348, 659, 680 см-1.
Масс-спектр: M/Z (относительная интенсивность %): FAB 152 (88), 134 (24), 123(14), 109 (41), 95 (39), 81 (48), 69 (83), 55 (100), 43 (81).
Обработка 2-(1-гидроксипропил)-4-метилпиридина (0,775 г, 5,13 ммоль) метансульфонилхлоридом (0,659 г, 5,78 ммоль, 1,13 эквив.) и триэтиламином (0,570 г, 5,64 ммоль, 1,1 эквив.) при концентрировании в вакууме дает 2-(1-метансульфонилокси)пропил-4-метилпиридин, который используют непосредственно в последующей реакции алкилирования.
ТСХ (силикагель GF): Rf = 0,62 ацетон/метиленхлорид (1/4).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,32 г, 5,13 ммоль) 2-(1-метансульфонилокси)пропил-4-метилпиридином (1,17 г, 5,13 ммоль, 1,0 эквив.) и NaH (0,431 г, 10,77 ммоль, 2,1 эквив., 60% масляная дисперсия) дает 0,726 г (48%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)пропил)тиопиримидина. Обработка Соед. N 218 (0,294 г, 1,0 ммоль) метансульфоновой кислотой (0,096 г, 1,0 ммоль, 1,0 эквив.) в эфире дает аналитически чистую мезилатную соль Соед. N 218 (0,372 г, 95%).
ТСХ (силикагель GF): Rf = 0,20 этилацетат/гексан (1/2). Соль HCl:
1H-ЯМР (CDCl3, ТМС): δ 8,66 (д, 1H, J=6,07 Гц), 7,87 (с, 1H), 7,63 (д, 1H, J=6,04 Гц), 6,22 (с, 1H), 5,25 (т, 1H, J=8,17 Гц), 2,73 (с, 3H), 2,30-2,01 (м, 2H), 1,19 (т, 3H, J=7,35 Гц).
Температура плавления 116-120oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,500), 254 (12,500), 267 sh (8,760), 287 (6,940).
Инфракрасный спектр ( νmax, минеральное масло): 2924, 1567, 2955, 2855, 1528, 1633, 2870, 1374, 1461, 828, 3164, 3295, 1279, 1249, 3203, 1116, 3091, 3058, 2692, 2633, 986, 3453, 603, 1084, 1207 см-1.
Анализ: (свободное основание)
Рассчитано для C13H15ClN4S: C, 53,06; H, 5,10; N, 19,05. Найдено: C, 52,68; H, 5,29; N, 18,59.
Масс-спектр: M/Z (относительная интенсивность %): 294 (14), 279 (13), 261 (100), 233 (24), 166 (14), 134 (90).
Мезилатная соль Соед. N 218:
Температура плавления 172-175oC.
Анализ: Рассчитано для C14H19ClN4O3S2: C, 43,08; H, 4,87; N, 14,36. Найдено: C, 42,97; H, 5,04; N, 14,03.
ПРИМЕР 219. 4-Амино-6-хлор-2-(1-(4-ацетил-2-пиридил)этил)тиопиримидин (Соед. N 219)
4-Циано-2-пиридинкарбоксальдегид (1,0 г, 7,57 ммоль) и метилмагнийброиид (6,31 мл, 18,92 ммоль, 2,5 эквив., 3,0 М в эфире) дают 0,729 г (58%) 4-ацетил-2-(1-гидрокси)этилпиридина.
ТСХ (силикагель GF): Rf = 0,27 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,68 (д, 1H, J=5,1 Гц), 7,76 (с, 1H), 7,61 (дд, 1H, J=1,49, 5,05 Гц), 4,97 (кв, 1H, J=6,42 Гц), 4,20 (ушир.с, 1H), 2,62 (с, 3H), 1,52 (д, 3H, J=6,52 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 165 (7), 164 (9), 150 (100), 122 (24).
4-Ацетил-2-(1-гидрокси)этилпиридин (0,729 г, 4,42 ммоль), метансульфонилхлорид (0,554 г, 4,86 ммоль, 1,1 эквив.) и триэтиламин (0,536 г, 5,30 ммоль, 1,2 эквив.) дают при концентрировании при пониженном давлении 4-ацетил-2-(1-метансульфонилокси)этилпиридин.
ТСХ (силикагель GF): Rf = 0,59 ацетон/метиленхлорид (1/4).
Мезилатная соль 4-амино-6-хлор-2-тиопиримидина (1,13 г, 4,42 ммоль), NaH (0,371 г, 9,28 ммоль, 2,1 эквив., 60% масляная дисперсия) и 4-ацетил-2-(1-метансульфонилокси)этилпиридин (1,07 г, 4,42 ммоль, 1,0 эквив.) дают 0,774 г (57%) 4-амино-6-хлор-2-(1-(4-ацетил-2-пиридил)этил)тиопиримидина (Соед. N 219).
ТСХ (силикагель GF): Rf = 0,17 ацетон/метиленхлорид (1/9).
1H-ЯМР (CDCl3, ТМС): δ 8,75 (д, 1H, J=3,79 Гц), 7,96 (с, 1H), 7,58 (дд, 1H, J=1,24, 3,79 Гц), 6,11 (с, 1H), 5,17 (кв, 1H, J=5,40 Гц), 5,08 (ушир.с, 2H), 2,63 (с, 3H), 1,79 (д, 3H, J=5,41).
Температура плавления 149-150oC.
Ультрафиолетовый спектр ( λmax, этанол): 227 (27,400), 249 sh (11,400), 288 (9,370).
Инфракрасный спектр ( νmax, минеральное масло): 1568, 2925, 2954, 1692, 1555, 1526, 1653, 1275, 2855, 3208, 1369, 1115, 3372, 3329, 1284, 3224, 601, 815, 1460, 982, 1105, 1259, 621, 849, 1445 см-1.
Анализ: Рассчитано для C13H13ClN4OS: C, 50,65; H, 4,22; N, 18,18, Найдено: C, 50,40; H, 4,28; N, 18,16.
Масс-спектр: M/Z (относительная интенсивность %): 308 (4), 275 (100), 148 (33), 105 (13).
ПРИМЕР 220. 4-Амино-6-хлор-2-(1-(4-метил-2-пиридил)-1- карбометоксиметил)тиопиримидин (Соед. N 220)
Колбу загружают 2-(1-циано-1-гидрокси)метил-4-метилпиридином (0,863 г, 5,83 ммоль) в 3,5 мл метанола, обрабатывают 1,8 мл концентрированной H2SO4, затем 0,30 мл воды, и смесь нагревают с обратным холодильником в течение 1,25 часа. Содержимое охлаждают, выливают в 50 мл насыщенного NaHCO3, экстрагируют дважды этилацетатом, объединенные органические экстракты сушат над безводным Na2SO4 и фильтрат концентрируют при пониженном давлении. Хроматографическую очистку выполняют, используя 75 г силикагеля, набивку и элюирование смесью ацетон/метиленхлорид (1/6) с получением 0,739 г (70%) 2-(1-карбометокси-1-гидрокси)метил-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,35 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,41 (с, 1H), 7,30 (с, 1H), 7,09 (д, 1H, J=3,75 Гц), 5,25 (с, 1H), 3,76 (с, 3H), 2,37 (с, 3H).
Масс-спектр: M/Z (относительная интенсивность %): 181 (0,4), 150 (0,3), 122 (100), 92 (32).
2-(1-Карбометокси-1-гидрокси)метил-4-метилпиридин (0,735 г, 4,06 ммоль), метансульфонилхлорид (0,509 г, 4,47 ммоль, 1,1 эквив.) и триэтиламин (0,492 г, 4,87 ммоль, 1,2 эквив. ) дают 2-(1-карбометокси-1-метансульфонилокси)метил-4-метилпиридин при непосредственной концентрации в вакууме.
ТСХ (силикагель GF): Rf = 0,70 ацетон/метиленхлорид (1/9).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,04 г, 4,06 ммоль) NaH (0,341 г, 8,53 ммоль, 2,1 эквив., 60% масляная дисперсия) и 2-(1-карбометокси-1-метансульфонилокси)метил-4-метилпиридином (1,05 г, 4,06 ммоль, 1,0 эквив.) дает 0,765 г (58%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)-1-карбометоксиметил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,26 ацетон-метиленхлорид (1:6).
1H-ЯМР (CDCl3, ТМС): δ 8,44 (д, 1H, J=4,99 Гц), 7,36 (с, 1H), 7,06 (д, 1H, J=5,06 Гц), 6,15 (с, 1H), 5,77 (с, 1H), 5,40 (ушир.с, 2H), 3,79 (с, 3H), 2,37 (с, 3H).
Температура плавления 137,5-139oC.
Ультрафиолетовый спектр ( λmax, этанол): 228 (25,77), 250 sh (12,300), 267 sh (7,650), 286 (6,880).
Инфракрасный спектр ( νmax, минеральное масло): 1573, 2925, 1645, 1736, 1532, 2955, 2964, 1188, 1167, 2855, 1282, 1292, 1603, 1368, 1124, 828, 1158, 835, 1430, 2869, 3461, 1467, 3188, 3315, 3163 см-1.
Анализ: Рассчитано для C13H13ClN4O2S: C, 48,15; H, 4,01; N, 17,28. Найдено: C, 47,99; H, 4,10; N, 17,11.
Масс-спектр: M/Z (относительная интенсивность %): 324 (11), 293 (42), 291 (100), 265 (37), 229 (9), 196 (7), 171 (20), 136 (39).
ПРИМЕР 221. 4-Амино-6-хлор-2-(1-(4-(1-метилэтенил)-2- пиридил)этил)тиопиримидин (Соед. N 221)
Суспензию метилтрифенилфосфонийбромида (14,90 г, 0,0417 моль, 2,2 эквив. ) в 170 мл ТГФ, охлажденную до 0-5oC, обрабатывают по каплям н-бутиллитием (26,1 мл, 0,0417 моль, 2,2 эквив., 1,6 М в гексане) в течение периода 20 минут. После перемешивания в течение дополнительных 35 мин 4-ацетил-2-(2-гидрокси)этилпиридин (3,13 г, 0,0190 моль, 1,0 эквив.), растворенный в 25 мл ТГФ, добавляют по каплям к реакционной смеси в течение 20 мин периода. Через 3,5 часа содержимое выливают в 500 мл воды со льдом, экстрагируют 4 раза этилацетатом и объединенные органические экстракты сушат с безводным Na2SO4. Концентрированный фильтрат хроматографируют на 500 г силикагеля с набивкой и элюированием смесью этилацетат-гексан (1:1) с получением 2,55 г (82%) 4-(1-метилэтенил)-2-(1-гидрокси)этилпиридина.
ТСХ (силикагель GF): Rf = 0,23 этилацетат/гексан (1/1).
1H-ЯМР (CDCl3, ТМС): δ 8,47 (д, 1H, J=5,30 Гц), 7,33 (с, 1H), 7,24 (дд, 1H, J=1,75, 5,21 Гц), 5,58 (с, 1H), 5,28 (с, 1H), 4,90 (кв, 1H, J=6,53 Гц), 4,40 (ушир.с, 1H), 2,15 (с, 3H), 1,52 (д, 3H, J=6,57 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 163 (11), 162 (13), 148 (100), 146 (40), 120 (23).
4-(1-Метилэтенил)-2-(1-гидрокси)этилпиридин (0,775 г, 4,75 ммоль), метансульфонилхлорид (0,670 г, 5,88 ммоль, 1,24 эквив.) и триэтиламин (0,576 г, 5,70 ммоль, 1,2 эквив.) дают 4-(1-метилэтенил)-2-(1-метансульфонилокси)этилпиридин при концентрировании при пониженном давлении.
ТСХ (силикагель GF): Rf = 0,31 этилацетат/гексан (1/1).
4-(1-Метилэтенил)-2-(1-метансульфонилокси)этилпиридин (1,14 г, 4,75 ммоль), NaH (0,399 г, 9,98 ммоль, 2,1 эквив., 60% масляная дисперсия) и мезилатная соль 4-амино-6-хлор- 2-тиопиримидина (1,22 г, 4,75 ммоль, 1,0 эквив. ) дают 0,801 г (55%) 4-амино-6-хлор-2-(1-(4-(1-метилэтенил)-2-пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,22 этилацетат/гексан (1/1).
1H-ЯМР (CDCl3, ТМС): δ 8,51 (д, 1H, J=5,28 Гц), 7,53 (с, 1H), 7,19 (дд, 1H, J= 1,80, 5,20 Гц), 6,10 (с, 1H), 5,58 (с, 1H), 5,30-5,09 (м, 4H), 2,14 (с, 3H), 1,77 (д, 3H, J=7,19 Гц).
Температура плавления 133-135oC.
Ультрафиолетовый спектр ( λmax, этанол): 231 (28,200), 250 sh (19,900), 285 (9,270).
Инфракрасный спектр ( νmax, минеральное масло): 1569, 1529, 2925, 1642, 1281, 2953, 1359, 1119, 1600, 1367, 2855, 1467, 3184, 828, 3314, 3364, 1378, 902, 1052, 986, 3217, 2982, 1263, 603, 911 см-1.
Анализ: Рассчитано для C14H15ClN4S: C, 54,90; H, 4,90; N, 18,30. Найдено: C, 54,61; H, 5,11; N, 17,99.
Масс-спектр: M/Z (относительная интенсивность %): 306 (7), 291 (1), 273 (100), 211 (4), 178 (22), 146 (53).
ПРИМЕР 223. 4-Амино-6-хлор-2-(1-(4-(1-метилэтил)-2-пиридил)этил)тиопиримидин (Соед. N 223)
Колбу, снабженную отдельными входным и выходным клапанами, загружают 4-(1-метилэтил)-2-(1-гидрокси)этенилпиридином (1,00 г, 6,13 ммоль) в 50 мл 95% этанола, 10% палладия на угле (100 мг) и приводят в соприкосновение с атмосферой водорода с помощью надувной камеры при комнатной температуре. Через 1 час реакционную смесь фильтруют через пад из целита, используя метиленхлорид для промывки пада. Фильтрат концентрируют в вакууме и хроматографируют на 100 г силикагеля с набивкой и элюированием смесью этилацетат/гексан (1/1) с получением 91% выхода 4-(1-метилэтил)-2-(1-гидрокси)этилпиридина.
ТСХ (силикагель GF): Rf = 0,25 ацетон/гексан (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,19 (д, 1H, J=5,15 Гц), 6,92 (с, 1H), 6,84 (дд, 1H, J=1,51, 5,17 Гц), 4,65 (кв, 1H, J=6,51 Гц), 4,22 (ушир.с, 1H), 2,69 (м, 1H), 1,29 (д, 3H, J=6,45 Гц), 1,04 (д, 6Н, J=6,91 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 165 (9), 164 (14), 150 (100), 148 (45), 135 (20), 122 (21), 106 (15).
Мезилирование 4-(1-метилэтил)-2-(1-гидрокси)этилпиридина (1,07 г, 6,48 ммоль) метансульфонилхлоридом (0,887 г, 7,78 ммоль, 1,2 эквив.) и триэтиламином (0,851 г, 8,42 ммоль, 1,3 эквив.) дает 4-(1-метилэтил)-2-(1-метансульфонилокси)этилпиридин.
ТСХ (силикагель GF): Rf = 0,34 этилацетат/гексан (1/1).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,66 г, 6,48 ммоль) NaH (0,544 г, 13,61 ммоль, 2,1 эквив., 60% масляная дисперсия) и 4-(1-метилэтил)-2-(1-метансульфонилокси)этилпиридином (1,57 г, 6,48 ммоль, 1,0 эквив. ) дает 1,02 г (51%) 4-амино-6-хлор-2-(1-(4-(1-метилэтил)-2-пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,23 ацетон/метиленхлорид (1/6).
Анализ: Рассчитано для C14H17ClN4S: C, 54,54; H, 5,52; N, 18,18. Найдено: C, 54,06; H, 5,62; N, 17,77.
Мезилатная соль:
1H-ЯМР (CDCl3, ТМС): δ 8,83 (д, 1H, J=6,14 Гц), 7,90 (с, 1H), 7,63 (д, 1H, J= 6,16 Гц), 6,29 (с, 1H), 5,33 (кв, 1H, J=7,55 Гц), 3,19 (м, 1H), 2,98 (с, 3H), 1,83 (д, 3H, J=7,50 Гц), 1,41 (дд, 6Н, J=1,37, 6,91 Гц).
Температура плавления 155-159oC.
Ультрафиолетовый спектр ( λmax, этанол): 229 (21,300), 253 (11,600), 267 sh (8,250), 286 (6,530).
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1571, 2955, 2855, 1633, 1162, 2870, 1217, 1041, 1528, 1376, 1465, 1117, 828, 3192, 3323, 3219, 1282, 3089, 3060, 1479, 3370, 986, 774, 2719 см-1.
Масс-спектр: M/Z (относительная интенсивность %): 308 (8), 293 (2), 275 (100), 180 (34), 148 (67), 132 (55).
ПРИМЕР 224. 4-Амино-6-хлор-2-(1-(4-метил-2-пиридил)пентил)тиопиримидин (Соед. N 224)
Раствор н-бутиллития (6,71 мл, 10,74 ммоль, 1,3 эквив., 1,6 М в гексане) в 60 мл эфира при 0-5oC обрабатывают по каплям 4-метил-2-пиридинкарбоксальдегидом (1,0 г, 8,26 ммоль, 1,0 эквив.) в 40 мл эфира в течение периода в 10 мин. Через 30 минут содержимое выливают в 45 мл 3 н HCl, содержащей 60 мл размельченного льда. Холодную смесь нагревают до комнатной температуры, перемешивают в течение 20 минут, подщелачивают 15 мл 29% водного раствора гидроксида аммония и экстрагируют один раз этилацетатом. Органический слой сушат над безводным Na2SO4 и концентрируют при пониженном давлении. Хроматография на 150 г силикагеля с набивкой и элюированием смесью этилацетат/гексан (1/2) дает 0,364 г (24%) 2-(1-гидрокси)пентил-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,18 этилацетат/гексан (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,24 (д, 1H, J=5,05 Гц), 6,92 (с, 1H), 6,87 (д, 1H, J=4,93 Гц), 4,55 (м, 1H), 4,01 (ушир.с, 1H), 2,23 (с, 3H), 1,75-1,45 (м, 2H), 1,34-1,12 (м, 4H), 0,76 (т, 3H, J=7,19 Гц).
Раствор 2-(1-гидрокси)пентил-4-метилпиридина (0,364 г, 2,03 ммоль) в 10 мл метиленхлорида обрабатывают тионилхлоридом (0,525 г, 4,41 ммоль, 2,17 эквив. ) и триэтиламином (0,226 г, 2,23 ммоль, 1,1 эквив.). Через 1 час реакционную смесь выливают в 100 мл насыщенного NaHCO3, экстрагируют дважды метиленхлоридом, и объединенные органические экстракты сушат с безводным Na2SO4. Фильтрат концентрируют в вакууме с получением 2-(1-хлор)пентил-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,78 ацетон/метиленхлорид (1/6).
1H-ЯМР (CDCl3, ТМС): δ 8,25 (д, 1H, J=5,06 Гц), 7,10 (с, 1H), 6,86 (д, 1H, J= 5,15 Гц), 4,75 (т, 1H, J=7,11 Гц), 2,21 (с, 3H), 2,02-1,91 (м, 2H), 1,43-1,09 (м, 4H), 0,73 (т, 3H, J=6,73 Гц).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (0,514 г, 2,0 ммоль) NaH (0,176 г, 4,4 ммоль, 2,2 эквив., 60% масляная дисперсия) и 2-(1-хлор)пентил-4-метилпиридином (0,394 г, 2,0 ммоль, 1,0 эквив.) дает 0,400 г (62%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)пентил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,25 ацетон/метиленхлорид (1/6).
1H-ЯМР (CDCl3, ТМС): δ 8,35 (д, 1H, J=5,00 Гц), 7,20 (с, 1H), 6,90 (д, 1H, J=4,54 Гц), 6,02 (с, 1H), 5,12 (ушир.с, 2H), 4,88 (т, 1H, J=7,20), 2,27 (с, 3H), 2,13-1,92 (м, 2H), 1,39-1,12 (м, 4H), 0,81 (т, 3H, J=6,90 Гц).
Температура плавления 139,5-141oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,600), 254 (12,600), 267 sh (8,830), 287 (7,040).
Инфракрасный спектр ( νmax, минеральное масло): 1573, 2928, 2961, 1281, 1659, 1534, 1123, 3143, 2854, 1605, 1466, 990, 1367, 1271, 1362, 1264, 3314, 2872, 829, 1296, 1453, 1381, 824, 1097, 3231 см-1.
Анализ: KF H2O 0,20%.
Анализ: Рассчитано для C15H19ClN4S - 0,20% H2O: C, 55,80; H, 5,93; N, 17,37. Найдено: C, 55,25; H, 5,83; N, 17,62.
Масс-спектр: M/Z (относительная интенсивность %): 322 (11), 289 (38), 279 (25), 266 (24), 233 (54), 162 (100).
ПРИМЕР 225. 4-Амино-5-бром-6-хлор-2-(1-(4-метилэтил)-2- пиридил)этил)тиопиримидин (Соед. N 225)
Мезилатную соль 4-амино-6-хлор-2-(1-(4-(1-метилэтил)-2- пиридил)этил)тиопиримидина (0,404 г, 1,0 ммоль) растворяют в 10 мл метанола, охлажденного до 0-5oC, и обрабатывают по каплям бромом (0,160 г, 1,0 ммоль, 1,0 эквив. ) в течение 1 мин периода. Через 10 минут реакционную смесь выливают в смесь 50 мл насыщенного NaHCO3 плюс 75 мл воды и экстрагируют один раз этилацетатом. Органический экстракт сушат над Na2SO4 и концентрируют в вакууме. Хроматография на 75 г силикагеля с набивкой и элюированием смесью ацетон-метиленхлорид (1: 8) дают 0,308 г (80%) 4-амино-5-бром-6-хлор-2-(1-(4-метил-2-пиридил)пентил)тиопиримидина (Соед. N 225). Кристаллизацию осуществляют из смеси растворителей метиленхлорид/гексан.
ТСХ (силикагель GF): Rf = 0,33 ацетон/метиленхлорид (1/6).
1H-ЯМР (CDCl3, ТМС): δ 8,35 (д, 1H, J=5,04 Гц), 7,19 (с, 1H), 6,90 (дд, 1H, J=1,70, 5,15 Гц), 5,54 (ушир.с, 2H), 4,91 (кв, 1H, J=7,12 Гц), 2,85-2,69 (м, 1H), 1,65 (д, 3H, J=7,17 Гц), 1,14 (д, 6H, J=6,91 Гц).
Температура плавления 124-125oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (19,600), 261 (15,100), 297 (8,440).
Инфракрасный спектр ( νmax, минеральное масло): 1535, 2927, 1518, 2958, 1634, 1332, 2855, 1462, 3474, 2870, 1267, 838, 3132, 993, 1600, 3287, 758, 3178, 1245, 1248, 3062, 1480, 1443, 1364.
Анализ: Рассчитано для C14H16BrClN4S: C, 43,41; H, 4,13; N, 14,47. Найдено: C, 43,43; H, 4,31; N, 14,15.
Масс-спектр: M/Z (относительная интенсивность %): 388 (15), 387 (3), 386 (11), 206 (3), 180 (47), 148 (78), 132 (47).
ПРИМЕР 226. 4-Амино-6-хлор-2-(1-(4-метил-2-пиридил)-1- циклопропилметил)тиопиримидинмезилат (Соед. N 226)
Реакция Гриньяра 4-метил-2-пиридинкарбоксальдегида (1,21 г, 10,0 ммоль) и циклопропилмагнийбромида (24 мл, 15,0 ммоль, 1,5 эквив., 1,6 мл/ммоль) дает 1,42 г (87%) 2-(1-гидрокси-1-циклопропилметил)-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,21 ацетон/метиленхлорид (1/6).
1H-ЯМР (CDCl3, ТМС): δ 8,47 (д, 1H, J=5,08 Гц), 7,30 (с, 1H), 7,12 (д, 1H, J= 5,14 Гц), 4,70 (ушир.с, 1H), 4,16 (д, 1H, J=7,92 Гц), 2,47 (с, 3H), 1,26-1,12 (м, 1H), 0,74-0,57 (м, 4H).
Масс-спектр: M/Z (относительная интенсивность %): 163 (34), 162 (51), 146 (51), 135 (70), 122 (100), 107 (57), 92 (98).
К раствору 2-(1-хлор-1-циклопропилметил)-4-метилпиридина (1,42 г, 8,71 ммоль) в 40 мл хлороформа при комнатной температуре добавляют тионилхлорид (1,35 г, 11,32 ммоль, 1,3 эквив.). Через 1,5 часа содержимое выливают в 150 мл насыщенного NaHCO3, экстрагируют дважды метиленхлоридом, и объединенные органические экстракты сушат с безводным Na2SO4. Фильтрат концентрируют при пониженном давлении и хроматографируют на 160 г силикагеля, используя набивку и элюирование смесью этилацетат/гексан (1/6) с получением 0,894 г (56%) 2-(1-хлор-1-циклопропилметил)-4-метилпиридина.
ТСХ (силикагель GF): Rf = 0,19 этилацетат/гексан (1/6).
1H-ЯМР (CDCl3, TMC): δ 8,21 (д, 1H, J=5,03 Гц), 7,08 (с, 1H), 6,83 (д, 1H, J= 4,13 Гц), 4,10 (д, 1H, J=9,48 Гц), 2,16 (с, 3H), 1,52-1,39 (м, 1H), 0,68-0,55 (м, 1H), 0,51-0,25 (м, 3H).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,27 г, 4,94 ммоль) NaH (0,435 г, 10,87 ммоль, 2,2 эквив., 60% масляная дисперсия) и 2-(1-хлор-1-циклопропилметил)-4-метилпиридином (0,894 г, 4,94 ммоль, 1,0 эквив. ) дает 0,762 г (50%) 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)-1-циклопропилметил)тиопиримидина. Обработка одним эквивалентом метансульфоновой кислоты в эфире дает аналитически чистое указанное в заголовке соединение в виде белого кристаллического твердого вещества.
ТСХ (силикагель GF): (Свободное основание) Rf = 0,31 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,51 (д, 1H, J=6,08 Гц), 7,75 (с, 1H), 7,31 (д, 1H, J= 5,89 Гц), 5,90 (с, 1H), 4,22 (д, 1H, J=10,75 Гц), 2,72 (с, 3H), 2,45 (с, 3H), 1,08-0,91 (м, 1H), 0,76-0,60 (м, 2H), 0,60-0,42 (м, 2H).
Температура плавления 192-193oC.
Ультрафиолетовый спектр ( λmax, этанол): 229 (22,500), 254 (12,400), 268 sh (8,460), 287 (6,840).
Инфракрасный спектр ( νmax, минеральное масло): 2924, 1576, 1217, 1228, 1527, 1035, 2954, 1377, 2854, 827, 1242, 2869, 1653, 1638, 3187, 1160, 1169, 1116, 1256, 3348, 3323, 1182, 1461, 1466, 773 см-1.
Анализ: Рассчитано для C15H19ClN4O3S2: C, 44,78; H, 4,73; N, 13,93. Найдено: C, 44,58; H, 4,85; N, 13,86.
Масс-спектр: M/Z (относительная интенсивность %): 306 (7), 273 (13), 178 (17), 164 (19), 146 (100), 131 (40).
ПРИМЕР 227. 4-Амино-6-хлор-2-(1-(4-(4-морфолинил)метил-2- пиридил)этил)тиопиримидин (Соед. N 227)
Суспензию гидрохлорида 4-пиколилхлорида (10,0 г, 60,98 ммоль) в 100 мл метиленхлорида при комнатной температуре обрабатывают морфолином (26,52 г, 304,9 ммоль, 5,0 эквив.) за один раз. После перемешивания в течение 50 часов реакционную смесь выливают в 250 мл воды, экстрагируют шесть раз этилацетатом, три раза смесью этилацетат/метанол (9/1), и объединенные органические экстракты сушат над Na2SO4. Концентрированный фильтрат хроматографируют на 350 г силикагеля с набивкой и элюированием смесью ацетон/метиленхлорид (1/2) с получением 9,17 г (84%) 4-(4-морфолинил)метилпиридина в виде желтой жидкости.
ТСХ (силикагель GF): Rf = 0,28 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,59 (д, 2H, J=6,04 Гц), 7,33 (д, 2H, J=6,01 Гц), 3,77 (т, 4Н, J=4,55 Гц), 3,55 (с, 2H), 2,50 (т, 4H, J=4,66 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 178 (77), 147 (38), 134 (16), 119 (80), 100 (100).
По способу, подобному способу, описанному для получения 4-циано-2-гидроксиметилпиридина, 4-(4-морфолинил)метилпиридин (9,15 г, 51,40 ммоль), персульфат аммония (23,44 г, 102,81 ммоль, 2,0 эквив.), метанол (92 мл), вода (46 мл) и концентрированная H2SO4 (11,59 г, 118,2 ммоль, 2,3 эквив.) дают 2,29 г (21%) 2-гидроксиметил-4-(4-морфолинил)метилпиридина.
ТСХ (силикагель GF): Rf = 0,25 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 8,45 (д, 1H, J=5,05 Гц), 7,27 (с, 1H), 7,18 (д, 1H, J= 4,90 Гц), 4,73 (с, 2H), 4,12 (ушир.с, 1H), 3,70 (т, 4H, J=4,76 Гц), 3,48 (с, 2H), 2,43 (т, 4Н, J=4,63 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 208 (55), 177 (28), 149 (52), 123 (100), 100 (99), 86 (51).
По способу, подобному тому, что описан для получения 4-циано-2-пиридин-карбоксальдегида, 2-гидроксиметил-4-(4-морфолинил)метилпиридин (2,29 г, 11,01 ммоль) дает 1,03 г (45%) 4-(4-морфолинил)метил-2-пиридинкарбоксальдегида.
ТСХ (силикагель GF): Rf = 0,42 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 9,89 (с, 1H), 8,54 (д, 1H, J=4,87 Гц), 7,76 (с, 1H), 7,36 (д, 1H, J=4,86 Гц), 3,53 (т, 4Н, J=4,54 Гц), 3,39 (с, 2H), 2,27 (т, 4H, J=4,65 Гц).
Реакция Гриньяра между 4-(4-морфолинил)метил-2-пиридинкарбоксальдегидом (1,03 г, 5,00 ммоль) и метилмагнийбромидом (2,50 мл, 7,50 ммоль, 1,5 эквив., 3,0 М в эфире) дает 1,05 г (94%) 2-(1-гидроксиэтил)-4-(4-морфолинил)метилпиридина.
ТСХ (силикагель GF): Rf = 0,37 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 8,52 (д, 1H, J=5,04 Гц), 7,34 (с, 1H), 7,27 (д, 1H, J=5,04 Гц), 4,95 (кв, 1H, J=6,54 Гц), 3,79 (т, 4H, J=4,50 Гц), 3,58 (с, 2H), 2,52 (кв, 4H, J=4,62 Гц), 1,57 (д, 3H, J=6,50 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 222 (100), 207 (11), 191 (30), 177 (13), 163 (10), 149 (76), 147 (64), 137 (74), 121 (53), 100 (92).
Обработка 2-(1-гидроксиэтил)-4-(4-морфолинил)метилпиридина (1,05 г, 4,73 ммоль) тионилхлоридом (0,732 г, 6,15 ммоль, 1,3 эквив.) дает 1,08 г (96%) 2-(1-хлорэтил)-4-(4-морфолинил)метилпиридина.
ТСХ (силикагель GF): Rf = 0,39 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 8,46 (д, 1H, J=4,90 Гц), 7,42 (с, 1H), 7,19 (д, 1H, J=5,08 Гц), 5,09 (кв, 1H, J=6,86 Гц), 3,69 (т, 4H, J=4,54 Гц), 3,47 (с, 2H), 2,42 (т, 4H, J=4,64 Гц), 1,84 (д, 3H, J=6,88 Гц).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,16 г, 4,50 ммоль) NaH (0,396 г, 9,90 ммоль, 2,2 эквив., 60% масляная дисперсия) и 2-(1-хлорэтил)-4-(4-морфолинил)метилпиридином (1,08 г, 4,50 ммоль, 1,0 эквив. ) дает 0,900 г (68%) 4-амино-6-хлор-2-(1-(4-(4-морфолинил)метил-2-пиридил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,33 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,31 (д, 1H, J=4,90 Гц), 7,26 (с, 1H), 6,97 (д, 1H, J=4,96 Гц), 5,92 (с, 1H), 5,01 (ушир.с, 2H), 4,92 (кв, 1H, J=7,13), 3,53 (т, 4H, J=4,49 Гц), 3,30 (с, 2H), 2,25 (т, 4H, J=4,60 Гц), 1,58 (д, 3H, J= 7,20 Гц).
Температура плавления 146-147,5oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,400), 250 (12,200), 270 sh (8,290), 287 (7,010).
Инфракрасный спектр ( νmax, минеральное масло): 2924, 1566, 1559, 1533, 1109, 2957, 1374, 2855, 2865, 1639, 825, 865, 1464, 1454, 1255, 1604, 1291, 1117, 1272, 3400, 858, 1045, 604, 3301, 3155 см-1.
Анализ: Рассчитано для C16H20ClN5OS: C, 52,60; H, 5,48; N, 19,18. Найдено: C, 52,74; H, 5,68; N, 19,00.
Масс-спектр: M/Z (относительная интенсивность %): 365 (0,1), 332 (9), 280 (100), 247 (9), (20).
ПРИМЕР 228. 4-Амино-6-хлор-2-(1-(4-диметиламинометил-2- пиридил)этил)тиопиримидин (Соед. N 228)
По способу, подобному способу, описанному для синтеза 4-(4-морфолинил)метилпиридина, гидрохлорид 4-пиколилхлорид (6,00 г, 0,0366 моль) и диэтиламин (10,68 г, 0,146 моль, 4,0 эквив.) дают 5,28 г (88%) 4-(N,N-диэтиламинометил)пиридина.
ТСХ (силикагель GF): Rf = 0,32 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,44 (д, 2H, J=4,48 Гц), 7,20 (д, 2H, J=5,89 Гц), 3,48 (с, 2H), 2,45 (кв, 4Н, J=7,14 Гц), 0,960 (т, 6Н, J=7,13 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 164 (12), 149 (100), 92 (87).
Обработка 4-(N,N-диэтиламинометил)пиридина (2,0 г, 12,20 ммоль) персульфатом аммония (5,56 г, 24,4 г, 2,0 эквив.), метанолом (22 мл), водой (11 мл) и концентрированной H2SO4 (2,76 г, 28,18 ммоль, 2,31 эквив.), как описано для Соед. N 214, дает 0,697 г (29%) 4-(N,N-диэтиламинометил)-2-гидроксиметилпиридина.
ТСХ (силикагель GF): Rf = 0,28 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 8,34 (д, 1H, J=5,05 Гц), 7,15 (с, 1H), 7,10 (д, 1H, J=5,13 Гц), 4,63 (с, 2H), 3,45 (с, 2H), 2,41 (кв, 4H, J=7,12 Гц), 0,924 (т, 6H, J=7,16 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 194 (10), 179 (100), 122 (15), 86 (30).
Окисление 4-(N,N-диэтиламинометил-2-гидроксиметилпиридина (0,695 г, 3,58 ммоль), SeO2 (0,220 г, 1,98 ммоль, 0,554 эквив.), как описано для Соед. N 214, дает 0,395 г (57%) 4-(N,N-диэтиламинометил)-2-пиридинкарбоксальдегида.
ТСХ (силикагель GF): Rf = 0,27 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 10,02 (с, 1H), 8,64 (д, 1H, J=4,88 Гц), 7,89 (с, 1H), 7,51 (д, 1H, J=5,04 Гц), 3,58 (с, 2H), 2,47 (кв, 4H, J=7,18 Гц), 0,976 (т, 6H, J=7,16 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 192 (9), 177 (100), 149 (9), 134 (8), 120 (31), 86 (32).
Реакция Гриньяра 4-(N, N-диэтиламинометил)-2-пиридинкарбоксальдегида (0,840 г, 4,37 ммоль) с метилмагнийбромидом (2,19 мл, 6,56 ммоль, 1,5 эквив. , 3,0 М в эфире) дает 0,668 г (73%) 4-(N,N-диэтиламинометил)-2-(1-гидрокси)этилпиридин.
ТСХ (силикагель GF): Rf = 0,36 ацетон/метиленхлорид (2/1).
1H-ЯМР (CDCl3, ТМС): δ 8,43 (д, 1H, J=5,04), 7,30 (с, 1H), 7,20 (д, 1H, J= 5,03 Гц), 4,88 (кв, 1H, J=6,56 Гц), 4,52 (ушир.с, 1H), 3,57 (с, 2H), 2,52 (кв, 4H, J=7,11 Гц), 1,50 (д, 3H, J=6,54 Гц), 1,04 (т, 6H, J=7,08 Гц).
Масс-спектр: M/Z (относительная интенсивность %): 208 (23), 193 (100), 177 (0,8), 149 (3), 136 (9), 121 (53), 86 (50).
Обработка 4-(N,N-диэтиламинометил)-2-(1-гидрокси)этилпиридина (0,668 г, 3,21 ммоль) тионилхлоридом (0,497 г, 4,17 ммоль, 1,3 эквив.) дает 0,687 г (95%) 2-(1-хлор)этил-4-(N,N-диэтиламинометил)пиридина.
ТСХ (силикагель GF): Rf = 0,42 ацетон/метиленхлорид (1/4).
1H-ЯМР (CDCl3, ТМС): δ 8,45 (д, 1H, J=4,97 Гц), 7,44 (с, 1H), 7,21 (д, 1H, J=5,01 Гц), 5,11 (кв, 1H, J=6,81), 3,55 (с, 2H), 2,50 (кв, 4H, 7,15 Гц), 1,85 (д, 3H, J=6,84 Гц), 1,02 (т, 6H, J=7,12 Гц).
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (0,781 г, 3,04 ммоль) NaH (0,268 г, 6,69 ммоль, 2,20 эквив., 60% масляная дисперсия) и 2-(1-хлор)этил-4-(N, N-диэтиламинометил)пиридином (0,687 г, 3,04 ммоль, 1,0 эквив.) дает 4-амино-6-хлор-2-(1-(4-диметиламинометил-2-пиридил)этил)тиопиримидин.
ТСХ (силикагель GF): Rf = 0,26 ацетон/метиленхлорид (1/2).
1H-ЯМР (CDCl3, ТМС): δ 8,26 (д, 1H, J=5,04 Гц), 7,26 (с, 1H), 6,94 (д, 1H, 5,08 Гц), 5,88 (с, 1H), 5,17 (ушир.с, 2H), 4,88 (кв, 1H, J=7,15 Гц), 3,34 (с, 2H), 2,30 (кв, 4H, J=7,12 Гц), 1,55 (д, 3H, J=7,19 Гц), 0,816 (т, 6H, J=7,15 Гц).
Температура плавления 92-94oC.
Ультрафиолетовый спектр ( λmax, этанол): 230 (22,900), 253 (12,600), 286 (7,190).
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1570, 2955, 1561, 1278, 1529, 2855, 1117, 2871, 1366, 1658, 1462, 3144, 1604, 1453, 3297, 989, 1259, 1378, 825, 3228, 3058, 2826, 1099, 3013 см-1.
Анализ: Рассчитано для C16H22ClN5S: C, 54,70; H, 6,27; N, 19,94. Найдено: C, 54,52; H, 6,35; N, 19,76.
Масс-спектр: M/Z (относительная интенсивность %): 351 (0,2), 336 (47), 318 (5), 280 (100), 246 (12), 190 (33), 175 (24), 119 (82), 86 (76).
ПРИМЕР 229. 4-Амино-6-хлор-2-(1-(2-нафталинил)этил)тиопиримидин (Соед. N 229)
Алкилирование мезилатной соли 4-амино-6-хлор-2-тиопиримидина (1,49 г, 5,81 ммоль) NaH (0,490 г, 12,20 ммоль, 2,1 эквив., 60% масляная дисперсия) и мезилатом, полученным из коммерчески доступного α -метил-2-нафталинметанола (1,45 г, 5,81 ммоль, 1,0 эквив.), дает 0,363 г (20%) 4-амино-6-хлор-2-(1-(2-нафталинил)этил)тиопиримидина.
ТСХ (силикагель GF): Rf = 0,27 этилацетат/гексан (1/3).
1H-ЯМР (CDCl3, ТМС): δ м.д. 7,82 (с, 1H), 7,71 (м, 3H), 7,48 (дд, 1H, J= 1,81, 8,53 Гц), 7,36 (м, 2H), 6,00 (с, 1H), 5,09 (кв, 1H, J=7,14 Гц), 5,04 (ушир.с, 2H), 1,74 (д, 3H, J=7,10 Гц).
Температура плавления 55-58oC.
Ультрафиолетовый спектр ( λmax, этанол): 225 (81,200), 256 (18,300), 277 (11,500), 286 (11,400).
Инфракрасный спектр ( νmax, минеральное масло): 1564, 1531, 2925, 2954, 1367, 1359, 1285, 2856, 1631, 1612, 820, 2867, 1118, 1457, 3311, 1241, 748, 3180, 3390, 3209, 1508, 3462, 3054, 3016, 857 см-1.
Анализ: Рассчитано для C16H14ClN3S: C, 60,95; H, 4,44; N, 13,33. Найдено: C, 60,66; H, 4,49; N, 13,06.
Масс-спектр: M/Z (относительная интенсивность %): 315 (13), 282 (20), 171 (2), 155 (100), 128 (10), 115 (6).
ПРИМЕР 230. 4-Амино-6-хлор-2-(1-(3-изохинолил)этил)тиопиримидин (Соед. N 230)
Изохинолин-3-карбонитрил (1,76 г, 11,4 ммоль) растворяют в 10 мл тетрагидрофурана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, разбавляют 5 мл диэтилового эфира и обрабатывают метилмагнийбромидом в эфире (5,7 мл, 17,1 ммоль). Реакционную смесь нагревают с обратным холодильником в течение одного часа, охлаждают до 0oC и гасят 15 мл 6 М соляной кислоты. Реакционную смесь нагревают до 50oC в течение одного часа, охлаждают и выливают в 75 мл 2н гидроксида натрия. Смесь экстрагируют 3 х 50 мл этилацетата и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до сырого оранжевого твердого продукта. Сырой продукт хроматографируют на 60 г силикагеля (230-400 меш), элюируя 20% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 7-11 объединяют и концентрируют с получением 1,7 г (87%) 3-ацетилизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 2,83 (с, 3), 7,70-7,78 (м, 2), 7,97-8,06 (м, 2), 8,47 (с, 1), 9,28 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 26,6; 120,2; 127,6; 128,6; 129,4; 130,1; 131,0; 135,5; 124,7; 151,9; 200,3 м.д.
ТСХ (силикагель-60, F-254): Rf = 0,37, 20% ацетон/гексан.
Температура плавления 90-91oC.
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1689, 1418, 1386, 1220, 944, 764 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [171] (88).
Анализ: Рассчитано для C11H9N1O1: C, 77,17; H, 5,30; N, 8,18. Найдено: C, 76,98; H, 5,41; N, 8,29.
3-Ацетил-изохинолин (1,53 г, 8,9 ммоль) растворяют в 42 мл метанола в 100-мл одногорлой круглодонной колбе при 0oC. Раствор обрабатывают по частям боргидридом натрия (388 мг, 10,3 ммоль) и реакционную смесь перемешивают 30 мин при 0oC. Летучие продукты удаляют в вакууме и остаток распределяют между 1 х 100 мл 1 н гидроксида натрия и 3 х 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до бледно-желтого твердого продукта. Сырой продукт хроматографируют на 60 г силикагеля
(230-400 меш), элюируя 40% смесью ацетон/гексан, собирая 9-мл-вые фракции. Фракции 26-45 объединяют и концентрируют с получением 1,23 г (80%) 3-(1-гидроксиэтил)изохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,61 (д, J=6,5 Гц, 3), 3,91 (ушир.с, 1), 5,07 (кв, J= 6,5, 12,9 Гц, 1), 7,54-7,60 (м, 1), 7,65-7,71 (м, 2), 7,80 (д, J=8 Гц, 1), 7,95 (д, J=8 Гц, 1), 9,20 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 24,2; 69,6; 115,6; 126,6; 127,0; 127,6; 127,9; 130,6; 136,5; 151,6; 156,9 м.д.
ТСХ (силикагель-60, F-254): Rf=0,46, 50% ацетон/гексан.
Температура плавления 104-106oC.
Инфракрасный спектр ( νmax, минеральное масло): 3215, 2925, 1631, 1363, 1130, 1098, 959, 761 см-1.
Масс-спектр: Рассчитано для C11H11N1O1 + H: 174,0919.
Найдено: 174,0923.
3-(1-Гидроксиэтил)-изохинолин (1,32 г, 7,6 ммоль) растворяют в 20 мл дихлорметана в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают по каплям тионилхлоридом (835 мкл, 11,4 ммоль) и перемешивают 3 час при 0oC, затем 1 час при комнатной температуре. Смесь повторно охлаждают до 0oC, гасят 50 мл насыщенного бикарбоната натрия и слои разделяют. Водный слой экстрагируют 3 x 25 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до бледно-янтарного масла. Сырой продукт хроматографируют на 60 г силикагеля (230-400 меш), элюируя 20% смесью ацетон/гексан, собирая 9-мл-вые фракции. Фракции 17-26 объединяют и концентрируют с получением 1,39 г (95%) 3-(1-хлорэтил)-изохинолина в виде желтого масла.
1H-ЯМР (CDCl3, ТМС) : δ 1,99 (д, J=6,8 Гц, 3), 5,33 (кв, J=6,8, 13 Гц, 1), 7,58-7,63 (м, 1), 7,67-7,72 (м, 1), 7,78 (c,l), 7,82 (д, J=8 Гц, 1), 7,97 (д, J=8 Гц, 1), 9,24 (с, 1)
13C-ЯМР (CDCl3): δ 24,9; 59,1; 117,2; 126,7; 127,4; 127,5; 127,9; 130,6; 136,1; 152,3; 154,0 м.д.
ТСХ (силикагель-60, F-254): Rf=0,40, 20% ацетон/гексан.
Инфракрасный спектр ( νmax, жидкость): 2979, 1629, 1584, 1493, 1045, 947, 887, 752 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [191] (9), [156] (100).
Анализ: Рассчитано для C11H10ClN, C 68,94; H, 5,26; N, 7,31. Найдено: c, 68,69; H, 5,39; N, 7,21.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,79 г, 6,94 ммоль) растворяют в 12 мл сухого диметил-формамида в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают 60% гидридом натрия (605 мг, 15,1 ммоль) (экзотерм.) и смесь перемешивают один час. 3-(1-Хлорэтил-изохинолин (1,33 г, 6,94 ммоль) в 2 x 3 мл сухого диметилформамида добавляют к реакционной смеси и смесь перемешивают 6 часов при комнатной температуре. Реакционную смесь выливают в 300 мл воды и экстрагируют этилацетатом 3 x 100 мл. Объединенные органические слои подвергают обратной промывке 4 x 50 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 75 г силикагеля (230-400 меш), элюируя с 40% смесью ацетон/гексан, собирая 9-мл-вые фракции. Фракции 26-39 объединяют и концентрируют с получением 1,26 г (57%) 4-амино-6-хлор-2-(1-(3- изохинолил) этил) тиопиримидина в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,78 (д, J=7 Гц, 3), 5,19 (кв, J=7,14, Гц, 1), 6,18 (с, 1), 7,38 (ушир.с, 1), 7,63-7,69 (м, 1), 7,75-7,80 (м, 1), 7,94 (д, J=8 Гц, 1), 7,95 (с, 1), 8,10 (д, J=8 Гц, 1), 9,31 (с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,2; 45,0; 98,5; 117,6; 126,40; 127,1; 127,2; 127,4; 130,7; 135,5; 152,2; 154,2; 157,3; 164,1; 170,2 м.л.
ТСХ (силикагель-60, F-254): Rf=0,50, 50% ацетон/гексан.
Температура плавления 179-180oC.
Ультрафиолетовый спектр (λmax, этанол), нм (ε) : 220 (73,300); 237 (31,500); 252 (16,500); 282 (9640); 325 (3,100); 312 (3,000).
Инфракрасный спектр (νmax, минеральное масло): 3306, 2925, 1642, 1572, 1533, 1465, 1366, 1288, 1121 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [316] (18), [283] (680).
Анализ: Рассчитано для C15H13ClN4S: C, 56,87; H, 4,14; N, 17,68. Найдено: C, 56,93; H, 4,33; N, 17,25.
ПРИМЕР 231. 4-Амино-5-бром-6-хлор-2-(1-(3-изохинолил) этил)-тиопиримидин (Соед.N 231)
4-Амино-6-хлор-2-(1-(3-изохинолил) этил) тиопиримидин (475 мг, 1,5 ммоль) суспендируют в 15 мл метанола в атмосфере азота в 50-мл одногорлой круглодонной колбе при 0oC. Суспензию обрабатывают медленно по каплям бромом (85 мкл, 1,65 ммоль), и реакционную смесь перемешивают 20 мин при 0oC. Летучие продукты удаляют в вакууме и остаток распределяют между 1 х 50 мл дихлорметана и 1 х 50 мл насыщенного карбоната натрия, затем 1 х 50 мл насыщенного тиосульфата натрия. Органический слой сушат над карбонатом калия и концентрируют в вакууме до белой пены. Кристаллизация из диэтилового эфира/гексана 1: 9 дает 513 мг (86%) 4-амино-5-бром-6-хлор-2-(1-(3-изохинолил) этил) тиопиримидина в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,87 (д, J=7 Гц, 3), 5,23 (кв, J=7,14 Гц, 1), 7,39 (ушир. с, 1), 7,71-7,77 (м, 1), 7,83-7,89 (м, 1), 8,03 (д, J=8 Гц, 1), 8,06 (с, 1), 8,18 (д, J=8 Гц, 1), 8,21 (ушир.с, 1), 9,40 (с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,2; 45,7; 95,4; 117,9; 126,6; 127,4; 127,4; 127,6; 130,9; 135,7; 152,5; 154,1; 157,0; 161,5; 168,0 м.д.
ТСХ (силикагель-60, F-254): Rf=0,42, 40% ацетон/гексан.
Температура плавления 173-174oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 207 (35,100); 220 (71,100); 261 (18,600); 298 (10,400); 325 (3,300).
Инфракрасный спектр ( νmax, минеральное масло): 3472, 3291, 2925, 1640, 1538, 1464, 1334, 1273, 757 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [394] (8).
Анализ: Рассчитано для C15H12BrClN4S: C, 45,53; H, 3,06; N, 14,16. Найдено: C, 45,65; H, 3,38; N, 13,87.
ПРИМЕР 232. 4-Амино-6-хлор-2-(1-(1-изохинолил) этил) тиопиримидин (Соед. N 232)
Метилмагнийбромид в эфире (8,1 мл, 24,3 ммоль) растворяют в 16 мл тетрагидрофурана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, разбавляют 8 мл диэтилового эфира и обрабатывают 1-изохинолинкарбонитрилом (3,0 г, 19,5 ммоль). Реакционную смесь нагревают с обратным холодильником в течение одного часа, охлаждают до 0oC и гасят 20 мл 6 М соляной кислоты. Реакционную смесь нагревают до 50oC в течение двух часов, охлаждают и выливают в 75 мл 2н гидроксида натрия. Смесь экстрагируют 3 х 80 мл этилацетата, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до сырого янтарного масла. Сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 10% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 16-26 объединяют и концентрируют с получением 2,1 г (62%) 1-ацетилизохинолина.
1H-ЯМР (CDCl3,ТМС): δ 2,87 (с, 3), 7,64-7,73 (м, 2), 7,80 (д, J=5,5 Гц, 1), 7,83-7,88 (м, 1), 8,58 (д, J=5,5 Гц, 1), 8,94-8,98 (м, 1) м.д.
13C-ЯМР (CDCl3): δ 28,6; 124,6; 125,7; 126,9; 127,0; 129,1; 130,3; 137,0; 141,0; 152,8; 202,7 м.д.
ТСХ (силикагель-60, F-254): Rf=0,45, 20% ацетон/гексан.
Инфракрасный спектр ( νmax, жидкость): 3054, 1694, 1582, 1358, 1239, 1133, 940, 833, 750 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [171] (63).
Анализ: Рассчитано для C11H9NO: C, 77,17; H, 5,30; N, 8,18.
Найдено: C, 77,09; H, 5,33; N, 8,10.
1-Ацетилизохинолин (2,0 г, 11,7 ммоль) растворяют в 50 мл метанола в 100-мл одногорлой круглодонной колбе при 0oC. Раствор обрабатывают частями боргидрида натрия (495 мг, 13,1 ммоль), и реакционную смесь перемешивают в течение 1 часа при 0oC. Летучие продукты удаляют в вакууме, и остаток распределяют между 1 x 50 мл 1н гидроксида натрия и 4 x 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до мутного масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя с 15% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 23-37 объединяют и концентрируют с получением 1,99 г (98%) 1-(1-гидроксиэтил)-иэохинолина.
1H-ЯМР (CDCl3,ТМС): δ 1,62 (д, J=6,5 Гц, 3), 5,29 (ушир.с, 1), 5,59 (кв, J=6,5 Гц, 13 Гц, 1), 7,58-7,73 (м, 3), 7,85 (д, J=8 Гц, 1), 8,04 (д, J=8 Гц, 1), 8,44 (д, J=5,7 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 25,4; 66,0; 120,5; 124,2; 124,6; 127,3; 127,5; 130,2; 136,5; 140,4; 162,2 м.д.
Температура плавления 60-62oC.
Инфракрасный спектр ( νmax, минеральное масло): 3179, 2925, 1592, 1444, 1367, 1077, 751 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [173] (24), [158] (100).
Анализ: Рассчитано для C11H11NO: С, 76,28; H, 6,40; N, 8,09. Найдено: C, 76,15; H, 6,38; N, 8,00.
1-(1-Гидроксиэтил)изохинолин (1,9 г, 11 ммоль) растворяют в 30 мл дихлорметана в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают по каплям тионилхлоридом (1,2 мл, 16,4 ммоль) и перемешивают 2 час при 0oC, затем 1 час при комнатной температуре. Смесь повторно охлаждают до 0oC, гасят 50 мл насыщенного бикарбоната натрия, и слои разделяют. Водный слой экстрагируют 3 x 25 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до коричневого масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 15% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 17-26 объединяют и концентрируют с получением 1,99 г (94%) 1-(1-хлорэтил)-изохинолина.
1H-ЯМР (CDCl3,ТМС): δ 2,10 (д, J=6,7 Гц, 3), 5,93 (кв, J=6,7, 13 Гц, 1), 7,61-7,72 (м, 3), 7,84 (м, 1), 8,30 (м, 1), 8,52 (д, J=5,5 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 22,8; 54,3; 121,4; 124,5; 125,8; 127,6; 130,1; 136,7; 141,6; 158,1 м.д.
ТСХ (силикагель-60, F-254): Rf=0,63, 50% ацетон/гексан.
Инфракрасный спектр ( νmax, жидкость): 3054, 1624, 1584, 1563, 1376, 1224, 828, 747, 620 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [191] (2), [156] (100).
Анализ: Рассчитано для C11H10ClH: C, 68,94; H, 5,26; N, 7,31. Найдено: С, 68,65; H, 5,32; N, 7,21.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,29 г, 5 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают 60% гидридом натрия (400 мг, 10 ммоль) (экзотерм. ) и смесь перемешивают 45 мин. 1-(1-Хлорэтил)-изохинолин (958 мг, 5 ммоль) в 2 x 2 мл сухого диметилформамида добавляют к реакционной смеси, и смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь выливают в 200 мл воды и экстрагируют этилацетатом 4 x 50 мл. Объединенные органические слои подвергают обратной промывке 4 x 50 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 25% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 27-39 объединяют и концентрируют с получением бледно-желтой пены. Кристаллизация из диэтилового эфира дает 847 мг (54%) 4-амино-6-хлор-2-(1-(1-изохинолил) этил) тиопиримидина (Соед. N 232) в виде не совсем белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,79 (д, J=7 Гц, 1), 5,97 (кв, J=7, 14 Гц, 1), 6,19 (с, 1), 7,39 (ушир.с, 2), 7,64-7,76 (м, 3), 7,94 (д, J=8 Гц, 1), 8,28 (д, J= 8 Гц, 1), 8,44 (д, J=5,5 Гц, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,6; 40,7; 98,8; 120,2; 124,3; 124,8; 127,5; 127,8; 130,3; 135,9; 141,5; 157,5; 159,9; 164,3; 170,1 м.д.
Температура плавления 179-180oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 203 (25,400); (27,100); 219 (70,300); 236 (23,800); 250 (13,600); 277 (10,400); 286 (11,100); 295 (8,430); 311 (4,950); 323 (5,240).
Инфракрасный спектр ( νmax, минеральное масло): 3295, 3193, 2925, 1655, 1571, 1531, 1368, 1276, 1117, 825 см-1.
Масс-спектр, [M/Z] (относительная интенсивность) [316] (14).
Анализ: Рассчитано для C15H13ClN4S: C, 56,87; H, 4,14; N, 17,68. Найдено: С, 56,74; H, 4,22; N, 17,59.
ПРИМЕР 233. 4-Амино-6-хлор-2-(1-(3-(5,6,7,8- тетрагидроизохинолил))этил)тиопиримидин (Соед. N 233)
3-Mетил-5,6,7,8-тетpaгидpoизoиoxинoлин-N-oкcид (4,3 г, 26,3 ммоль) растворяют в 10 мл уксусного ангидрида и добавляют медленно по каплям к 40 мл уксусного ангидрида в атмосфере азота в 100-мл одногорлой круглодонной колбе при 140oC. По окончании добавления (20 мин) черную реакционную смесь перемешивают в течение 1 час при 140oC и летучие продукты удаляют при пониженном давлении.
Остаток хроматографируют на 150 г силикагеля (230-400 меш), элюируя 40% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 24-37 объединяют и концентрируют с получением 2,33 г мутного масла. Масло растворяют в 60 мл метанола в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают карбонатом калия (3,14 г, 22,7 ммоль), перемешивают 1,5 часа и летучие продукты удаляют в вакууме. Остаток извлекают 50 мл дихлорметана, нерастворимые продукты удаляют путем фильтрования и фильтрат концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на силикагеле (230-400 меш), элюируя 5,5% метанол/дихлорметаном, собирая 9-мл-вые фракции. Фракции 35-66 объединяют и концентрируют с получением 1,37 г (32%) 3-гидроксиметил-5, 6, 7, 8-тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,80 (м, 4), 2,73 (м, 4), 3,48 (ушир.с, 1), 4,67 (с, 2), 6,95 (5, 1), 8,22 (с, 1) м.д.
ТСХ (силикагель-60, F-254): Rf=0,16, 33% ацетон/хлороформ + 0,6% гидроксид аммония.
13C-ЯМР (CDCl3): δ 22,4; 22,6; 26,0; 28,8; 64,0; 120,6; 131,8; 147,1; 149,0; 155,6 м.д.
Инфракрасный спектр ( νmax, минеральное масло): 3228, 2925, 1608, 1437, 1069 см-1.
Масс-спектр: Рассчитано для C10H13NO+H: 164,1075. Найдено: 164,1074.
Анализ: Рассчитано для C10H13NO: С, 73,59; H, 8,03; N, 8,58. Найдено: C, 73,53; H, 8,14; N, 8,52.
3-Гидроксиметил-5,6,7,8-тетрагидроизохинолин (1,73 г, 10,6 ммоль) растворяют в 30 мл диоксана в атмосфере азота в 100-мл одногорлой крутитодонной колбе. Раствор обрабатывают диоксидом селена (647 мг, 5,8 ммоль) и реакционную смесь нагревают до 80-85oC в течение 1,5 час. Смесь охлаждают до комнатной температуры, разбавляют 30 мл дихлорметана и фильтруют через целит. Отфильтрованную лепешку тщательно промывают свежим дихлорметаном и фильтрат концентрируют в вакууме до темно-янтарного масла. Сырой продукт хроматографируют через 25 г слоя силикагеля (230-400 меш), элюируя 20% смесью ацетон/гексан, собирая 50-мл-вые фракции. Фракции 1-3 объединяют и концентрируют с получением 1,20 г (70%) 5, 6, 7, 8-тетрагидроизохинолин-3-карбальдегида.
1H-ЯМР (CDCl3, ТМС): δ 1,86 (м, 4), 2,83 (м, 4), 7,67 (с,1), 8,46 (с, 1), 10,02 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 22,1; 22,2; 26,7; 28,8; 122,2; 138,6; 147,3; 150,3; 150,9; 193,6 м.д.
ТСХ (силикагель-60, F-254): Rf=0,46, 40% ацетон/гексан.
Температура плавления 35-36oC.
Инфракрасный спектр ( νmax, минеральное масло): 2925, 1709, 1592, 1434, 1217, 1128, 931, 748 см-1.
Анализ: Рассчитано для C10H11NO: С, 74,51; H, 6,88; N, 8,69. Найдено: C, 74,60; H, 7,03; N, 8,66.
5,6,7,8-Тетрагидроизохинолин-3-карбальдегид (1,2 г, 7,44 ммоль) растворяют в 15 мл тетрагидрофурана в атмосфере азота при 0oC в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор обрабатывают метилмагнийбромидом в диэтиловом эфире (3,7 мл, 11,2 ммоль), затем 10 мл диэтилового эфира. Реакционную смесь нагревают до комнатной температуры и затем с обратным холодильником в течение 1 часа. Смесь охлаждают, гасят 20 мл 10% соляной кислоты и устанавливают pH 9 с помощью 2н гидроксида натрия. Слои разделяют, водный слой промывают 4 х 25 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 1,30 г (99%) 3-(1-гидроксиэтил) -5,6,7,8-тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,47 (д, J= 6,5 Гц, 3), 1,81 (м, 4), 2,72 (м, 4), 4,15 (ушир.с, 1), 4,81 (кв, J=6,5, 13 Гц, 1), 6,95 (с, 1), 8,22 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 22,4; 22,6; 24,3; 26,0; 28,9; 68,5; 119,7; 131,7; 147,2; 159,6 м.л.
ТСХ (силикагель-60, F-254):Rf=0,12, 10% ацетон/хлороформ.
Температура плавления 44-45oC.
Инфракрасный спектр ( νmax, минеральное масло): 3341, 3098, 2925, 1604, 1434, 1142, 1108, 1077 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [177] (2), [162] (100).
Анализ: Рассчитано для C11H15NO: C, 74,54; H, 8,53; N, 7,90. Найдено: C, 74,41; H, 8,83;. N, 7,84.
3-(1-Гидpoкcиэтил)-5,6,7,8-тетpaгидpoизoxинoлин (360 мг, 2,0 ммоль) растворяют в 4 мл дихлорметана в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают по каплям тионилхлоридом (218 мкл, 3,0 ммоль) в 3 мл дихлорметана и перемешивают 2 часа при 0oC, затем 1,5 часа при комнатной температуре. Смесь повторно охлаждают до 0oC, гасят насыщенным бикарбонатом натрия 20 мл и слои разделяют. Водный слой экстрагируют 4 x 10 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 20% ацетон/гексана, собирая 5-мл-вые фракции. Фракции 11-16 объединяют и концентрируют с получением 339 мг (87%) 3-(1-хлорэтил)-5,6,7,8-тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,81 (м, 4), 1,86 (д, J=7 Гц, 3), 2,75 (м, 4), 5,08 (кв, J=7, 14 Гц,1), 7,14 (c, 1), 8,26 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 22,3; 22,5; 24,9; 26,1; 28,8; 59,1; 121,2; 132,6; 147,2; 149,7; 157,4 м.д.
ТСХ (силикагель-60, F-254): Rf=0,42, 20% ацетон/гексан.
Инфракрасный спектр ( νmax, жидкость): 2932, 1599, 1436, 1398, 1238, 1050, 601 см-1.
Масс-спектр: Рассчитано для C11H14ClN+H: 196,0893.
Найдено: 196,0896.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (482 мг, 1,9 ммоль) растворяют в 4 мл сухого диметилформамида в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор обрабатывают 60% гидридом натрия (150 мг, 3,74 ммоль) (экзотерм. ) и смесь перемешивают 40 минут. 3-(1-Хлорэтил)- 5,6,7,8-тетрагидроизохинолин (325 мг, 1,7 ммоль) в 2 x 1 мл сухого диметилформамида добавляют к реакционной смеси и смесь перемешивают 3 часа при комнатной температуре. Реакционную смесь выливают в 100 мл воды и экстрагируют 4 x 25 мл этилацетата. Объединенные органические слои подвергают обратной промывке 4 x 50 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 40% смесью ацетон/гексан, собирая 5-мл-вые фракции. Фракции 15-21 объединяют и концентрируют с получением 335 мг не совсем белой пены. Кристаллизация из диэтилового эфира дает 261 мг (48%) 4-амино-6-хлор-2-(1-(3-(5,6,7,8-тетрагидроизохинолил)) этил)тиопиримидина в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,51 (д, J=6,5 Гц, 3), 1,59 (м, 4), 2,54 (м, 4), 4,80 (кв, J-6,5, 13 Гц, 1), 6,05 (с, 1), 7,04 (с, 1), 7,21 (ушир.с, 2), 8,08 (с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,4; 21,8; 22,1; 25,3; 28,0; 44,7; 98,6; 121,9; 131,3; 146,2; 149,6; 157,4; 164,3; 170,4 м.д.
ТСХ (силикагель-60, F-254): Rf=0,55, 50% ацетон/гексан.
Температура плавления 155-156oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 229 (25,100); 253 (12,600); 275 (8,050); 286 (7,260).
Инфракрасный спектр ( νmax, минеральное масло): 3303, 3156, 2925, 1641, 1571, 1535, 1462, 1368, 1283, 1124 см-1.
Анализ: Рассчитано для C15H17ClN4S: С, 56,15; H, 5,34; N, 17,46. Найдено: C, 55,94; H, 5,49; N, 17,35.
ПРИМЕР 234. 4-Амино-6-трифторметил-2-(1-(3-(5,6,7,8- тетрагидроизохинолил))этил)тиопиримидин (Соед. N 234)
Указанное в заголовке соединение получают по способу примера 233, за исключением того, что алкилирование 3-(1-хлорэтил)- 5,6,7,8-тетрагидроизохинолина проводят с мезилатной солью 4-амино-6-трифторметил-2-меркаптопиримидина. Температура плавления 60-161oC.
ПРИМЕР 235. 4-Амино-6-хлор-2-(1-(1-(5,6,7,8-тетрагидроизохинолил))этил) тиопиримидин, (Соед. N 235)
5,6,7,8-Тетрагидроизохинолин (13,3 г, 100 ммоль) растворяют в 35 мл ледяной уксусной кислоты в 200-мл одногорлой круглодонной колбе. Раствор нагревают до 95-100oC и обрабатывают по каплям 30% перекисью водорода (28 мл). Реакционную смесь перемешивают при 95-100oC в течение 6 часов, обрабатывают частями параформальдегида до тех пор, пока не получат отрицательную реакцию на крахмальной йодидной бумаге, и летучие продукты удаляют в вакууме. Остаток азеотропно перегоняют с 2 x 100 мл толуола, и сырой продукт хроматографируют на 500 г силикагеля (230-400 меш), элюируя 4 л 6% метанол/дихлорметана, затем 1 л 10% метанол/дихлорметана, собирая 50-мл-вые фракции. Фракции 39-82 объединяют и концентрируют с получением 12,8 г (86%) 5,6,7,8-тетрагидроизохинолин-N-оксида.
1H-ЯМР (CDCl3, ТМС): δ 1,77-1,97 (м, 4), 2,70 (м, 4), 6,98 (м, 1), 7,98 (м, 2) м.д.
13C-ЯМР (CDCl3): δ 21,4; 21,8; 27,6; 28,3; 125,7; 135,7; 135,9; 137,4; 138,2 м.д.
ТСХ (силикагель-60, F-254): Rf=0,39, 10% метанол/дихлорметан.
Температура плавления 94-98oC.
Инфракрасный спектр ( νmax, минеральное масло): 2926, 1485, 1450, 1260, 1141, 740 см-1.
Масс-спектр: Рассчитано для C9H11NO+H: 150,0919,
Найдено: 150,0918.
5,6,7,8-Тетрагидроизохинолин-N-оксид (12,7 г, 85 ммоль) растворяют в 250 мл дихлорметана в атмосфере азота в 500-мл одногорлой круглодонной колбе. Раствор обрабатывают триметилоксоний/тетрафторборатом (12,6 г, 85 ммоль), и реакционную смесь перемешивают 1 час при комнатной температуре. Летучие продукты удаляют в вакууме с получением мутного маслянистого остатка. Остаток растворяют в 225 мл метанола, и раствор нагревают с обратным холодильником. Персульфат аммония (8 г, 34 ммоль) в 34 мл воды быстро добавляют по каплям к смеси, нагретой с обратным холодильником. Реакционную смесь перемешивают 30 минут и обрабатывают второй порцией персульфата аммония (8 г, 34 ммоль) в 34 мл воды. Реакционную смесь перемешивают еще час при нагреве с обратным холодильником, охлаждают и основную массу метанола удаляют в вакууме. Остаток выливают в 100 мл льда, содержащего 100 мл 10% соляной кислоты. Смесь промывают 2 x 50 мл этилацетата, устанавливают pH 9 с помощью 45% гидроксида калия, и смесь экстрагируют 4 x 50 мл дихлорметана. Галогенорганические слои сушат над карбонатом калия и концентрируют в вакууме до коричневого твердого вещества. Сырой продукт хроматографируют на 350 г силикагеля (230-400 меш), элюируя 3 л 20% ацетон/хлороформа + 0,6% конц. гидроксида аммония, затем 1 л 32% ацетон/хлороформа + 0,6% конц. гидроксида аммония, собирая 50-мл-вые фракции. Фракции 19-27 объединяют и концентрируют с получением 4,3 г (31%) 1-гидроксиметил-5,6,7,8-тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,83 (м, 4), 2,50 (м, 2), 2,76 (м, 2), 4,60 (с, 1), 4,95 (ушир.с, 1), 6,94 (д, J=5 Гц, 1), 8,24 (д, J=5 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 21,8; 22,1; 23,0; 28,9; 60,9; 122,9; 128,7; 143,8; 146,3; 155,6 м.д.
ТСХ (силикагель-60, F-254): Rf=0,50, 33% ацетон/хлороформ + 0,6% гидроксид аммония.
Температура плавления 81-82oC.
Инфракрасный спектр ( νmax, минеральное масло): 3325, 2925, 1595, 1459, 1426, 1397, 1074, 839 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [163] (93).
Анализ: Рассчитано для C10H13NO: C, 73,59; H, 8,03; N, 8,58. Найдено: C, 73,77; H, 7,89; N, 8,69.
1-Гидроксиметил-5,6,7,8-тетрагидроизохинолин (4,14 г, 25,4 ммоль) растворяют в 75 мл диоксана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают диоксидом селена (1,56 г, 14,0 ммоль) и реакционную смесь
нагревают до 80-85oC в течение 2,5 часов. Смесь охлаждают до комнатной температуры, разбавляют 125 мл дихлорметана и фильтруют через целит. Отфильтрованную лепешку тщательно промывают свежим дихлорметаном, и фильтрат концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 200 г силикагеля (230-400 меш), элюируя 1:5:4 ацетон/хлороформ/гексаном, собирая 50-мл-вые фракции. Фракции 11-18 объединяют и концентрируют с получением 3,69 г (90%) 5,6,7,8-тетрагидроизохинолин-1-карбальдегида.
1H-ЯМР (CDCl3,ТМС): δ 1,81 (м, 4), 2,84 (м, 2), 3,19 (м, 2), 7,18 (д, J= 4,7 Гц, 1), 8,49 (д, J=4,7 Гц, 1), 10,18 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 21,5; 22,3; 25,3; 29,5; 127,6; 135,9; 146,4; 148,4; 149,6; 195,8 м.д.
ТСХ (силикагель-60, F-254): Rf=0,62, 50% ацетон/гексан.
Инфракрасный спектр ( νmax, минеральное масло): 2928, 1710, 1581, 1464, 846 см-1.
Масс-спектр: Рассчитано для C10H11NO+H: 162,0919.
Найдено: 162,0921.
Метилмагнийбромид в диэтиловом эфире (9,3 мл, 28 ммоль) растворяют в 10 мл тетрагидрофурана при 0oC в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор обрабатывают 5,6,7,8-тетрагидроизохинолин- 1-карбальдегидом (3,61 г, 22,4 ммоль). Затем 10 мл диэтилового эфира. Реакционную смесь нагревают до комнатной температуры, а затем - с обратным холодильником в течение 1 часа. Смесь охлаждают, гасят 20 мл 10% соляной кислоты и устанавливают pH 9 с помощью 2н гидроксида натрия. Слои разделяют, водный слой промывают 4 x 50 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 3,47 г (87%) 1-(1-гидроксиэтил)-5,6,7,8-тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,38 (д, J=6,5 Гц, 3), 1,73-1,97 (м, 4), 2,52-2,80 (м, 4), 4,92 (кв, J=6,5, 13 Гц, 1), 6,92 (ушир.с, 1), 6,91 (д, J=5 Гц, 1), 8,21 (д, J=5 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 22,0; 22,6; 23,7; 24,5; 29,3; 65,4; 123,3; 128,5; 144,4; 147,0; 160,6 м.д.
ТСХ (силикагель-60, F-254): Rf=0,54, 50% ацетон/гексан.
Температура плавления 60-61oC.
Инфракрасный спектр ( νmax, минеральное масло): 3053, 2923, 1590, 1457, 1401, 1118, 838 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [177] (26), [162] (100).
Анализ: Рассчитано для C11H15NO: C, 74,54; H, 8,53; N, 7,90. Найдено: C, 74,45; H, 8,42; N, 7,83.
1-(1-Гидроксиэтил)-5,6,7,8-тетрагидроизохинолин (1,77 г, 10 ммоль) растворяют в 30 мл дихлорметана в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают по каплям тионилхлоридом (1,1 мл, 15 ммоль) в 5 мл дихлорметана и перемешивают 2 часа при 0oC, затем 1 час при комнатной температуре. Смесь повторно охлаждают до 0oC, гасят 50 мл насыщенного бикарбоната натрия и слои разделяют. Водный слой экстрагируют дихлорметаном 3 x 25 мл, и объединенные органические экстракты сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 10% смесью ацетон/гексан, собирая 9-мл-вые фракции. Фракции 10-24 объединяют и концентрируют с получением 1,96 г (100%) 1-(1-хлорэтил)-5,6,7,8- тетрагидроизохинолина.
1H-ЯМР (CDCl3, ТМС): δ 1,68-1,94 (м, 7), 2,68-3,01 (м, 4), 5,32 (кв, J= 6,5, 13 Гц, 1), 6,93 (д, J=5 Гц, 1), 8,31 (д, J=5 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 21,8; 22,6; 22,8; 24,6; 29,4; 54,3; 124,1; 130,4; 145,7; 147,2; 157,1 м.д.
ТСХ (силикагель-60, F-254): Rf=0,65, 20% ацетон/гексан.
Инфракрасный спектр ( νmax, жидкость): 2932, 1586, 1435, 1042, 844, 654 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [160] (100).
Анализ: Рассчитано для C11H14ClN: C, 67,52; H, 7,21; N, 7,16. Найдено: C, 67,12; H, 7,16; N, 6,99.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,29 г, 5 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают 60% гидридом натрия (400 мг, 10 ммоль) (экзотерм. ) и смесь перемешивают 1 час. 1-(1-Хлорэтил)-5,6,7,8- тетрагидроизохинолин (978 мг, 5 ммоль) в 2 х 2 мл сухого диметилформамида добавляют к реакционной смеси и смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь выливают в 300 мл воды и экстрагируют 4 x 50 мл этилацетата. Объединенные органические слои подвергают обратной промывке 4 x 50 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтой пены. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 30% смесью ацетон/гексан, собирая 22-мл-вые фракции. Фракции 18-24 объединяют и концентрируют с получением белой пены. Кристаллизация из диэтилового эфира дает 945 мг (59%) 4-амино-6-хлор-2-(1-(1-(5,6,7,8-тетрагидроизохинолил))этил)- тиопиримидина в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,67-1,85 (м, 7), 2,73-2,97 (м, 4), 5,24 (кв, J=6,5, 13 Гц, 1), 6,22 (с, 1), 7,01 (д, J=5 Гц, 1), 7,36 (ушир.с, 1), 8,24 (д, J=5 Гц, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,4; 21,5; 21,6; 22,5; 24,5; 41,2; 98,9; 123,3; 129,6; 145,5; 146,6; 157,6; 158,6; 164,5; 171,0 м.д.
ТСХ (силикагель-60, F-254): Rf=0,46, 50% ацетон/гексан.
Температура плавления 186-187oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 229(23,600), 257(11,900); 265(10,800); 273(9,690); 285(7,840).
Инфракрасный спектр ( νmax, минеральное масло): 3280, 3138, 2931, 1661, 1573, 1532, 1366, 1275, 1113, 829 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [320] (18), [283] (26), [160] (100).
Анализ: Рассчитано для C15H17ClN4S: C, 56,15; H, 5,34; N, 17,46. Найдено: C, 56,30; H, 5,65; N, 17,09.
ПРИМЕР 236. 4-Амино-5-бром-6-хлор-2-(1-(1-(5,6,7, 8- тетрагидроизохинолил))этил)тиопиримидин (Соед. N 236)
1-[(4-Амино-6-хлорпиримидин-2-ил)] тио-1-(1- (5,6,7,8-тетрагидроизохинолил)этан (400 мг, 1,25 ммоль) суспендируют в 6 мл метанола в 25-мл одногорлой круглодонной колбе в атмосфере азота при 0oC. Суспензию медленно обрабатывают по каплям бромом (74 мкл, 1,44 ммоль) и реакционную смесь перемешивают 20 минут при 0oC. Летучие продукты удаляют в вакууме и остаток распределяют между 4 x 25 мл дихлорметана и 1 х 25 мл насыщенного карбоната натрия. Органический слой сушат над карбонатом калия и концентрируют в вакууме до бледно-желтой пены. Сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 30% смесью ацетон/гексан, собирая 5-мл-вые фракции. Фракции 17-24 объединяют и концентрируют с получением 379 мг бледной пены. Кристаллизация из гексана дает 325 мг (65%) 4-амино-5-бром-6- хлор-2-(1-(1-(5,6,7,8-тетрагидроизохинолил))этил)тиопиримидина в виде не совсем белого твердого продукта.
1H ЯМР (d6ДМСО): δ 1,72-1,91 (м, 7), 2,69-2,77 (м, 3), 3,04-3,14 (м, 1), 5,55 (кв, J=6,5, 13 Гц, 1), 5,96 (ушир.с, 2), 6,87 (д, J=5 Гц, 1), 8,27 (д, J=5 Гц, 1) м.д.
13C-ЯМР (d6ДМСО): δ 20,8; 21,8; 22,8; 24,8; 29,5; 42,0; 96,4; 123,0; 129,9; 145,6; 146,7; 158,0; 158,8; 160,8; 169,5 м.д.
ТСХ (силикагель-60, F-254): Rf=0,53, 50% ацетон/гексан.
Температура плавления 175-176 oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 230(20,700); 265(15,600); 297(9,290).
Инфракрасный спектр ( νmax, минеральное масло): 3482, 3283, 2922, 1632, 1537, 1520, 1459, 1339, 1274, 845 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [398] (13).
Анализ: Рассчитано для C15H16ClBrN4S: C, 45,07; H, 4,03; N, 14,02. Найдено: C, 45,03; H, 4,10; N, 19,94.
ПРИМЕР 237. 4-Амино-6-хлор-2-(1-(7-хлорфуро[2,3c]пиридин-5-ил) этил)тиопиримидин (Соед. N 237)
2-Хлор-3-пиридинол (60 г, 0,46 моль) растворяют в 700 мл воды, содержащей карбонат калия (220 г, 1,6 моль) в 2-л одногорлой круглодонной колбе. Раствор обрабатывают йодом (141 г, 0,56 моль) и реакционную смесь перемешивают 4 часа при комнатной температуре. Избыток йода гасят насыщенным тиосульфатом натрия и устанавливают pH смеси 2 с помощью 12н соляной кислоты. Смесь экстрагируют 3 x 250 мл этилацетата. Объединенные органические слои сушат над сульфатом магния и концентрируют в вакууме до желтого твердого продукта. Сырой твердый продукт перекристаллизовывают из 150 мл этилацетата и 700 мл гептана с получением 69 г (58%) 2-хлор-3-гидрокси-6-йодпиридина. Маточную жидкость концентрируют до желтого твердого продукта, который перекристаллизовывают из 60 мл этилацетата и 370 мл гептана с получением 15,5 г (13%).
1H ЯМР (d6ДМСО): δ 6,90 (д, J=8 Гц, 1); 7,43 (д, J=8 Гц, 1), 10,87 (ушир.с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 100,7; 126,5; 134,5; 137,6; 150,2 м.д.
Температура плавления 142-143oC.
Инфракрасный спектр ( νmax, минеральное масло): 3056, 2925, 1554, 1457, 1398, 1289, 1226, 1086 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [255] (80)
Анализ: Рассчитано для C5H3ClINO: C, 23,51; H, 1,18; N, 5,48. Найдено: C, 23,44; H, 1,22; N, 5,39
Высушенную в пламени 500-мл трехгорлую круглодонную колбу загружают в атмосфере азота 100 мл тетрагидрофурана и бутиллитием (82 мл, 132 ммоль). Раствор охлаждают до -78oC, обрабатывают по каплям 2-хлор-3-гидрокси-6-йодпиридином (15,3 г, 60 ммоль) в 100 мл сухого тетрагидрофурана и перемешивают 1 час при -78oC. Смесь обрабатывают по каплям ацетальдегидом
(7,4 мл, 132 ммоль) и перемешивают 1 час при -78oC, а затем дают температуре медленно подняться до -40oC. Реакционную смесь гасят 100 мл воды и слои разделяют. pH водного слоя устанавливают 3,5 10% соляной кислотой и смесь экстрагируют 4 x 50 мл этилацетата. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до сырого белого твердого продукта. Сырой продукт абсорбируют на 25 г силикагеля (280-400 меш), и этот слой хроматографируют на 500 г силикагеля (230-400 меш), элюируя 50% этилацетат/гексаном, собирая 50-мл-вые фракции. Фракции 58-92 объединяют и концентрируют с получением 4,75 г (46%) 2-хлор-3-гидрокси-6-(1 - гидроксиэтил) пиридина.
1H-ЯМР (d6ДМСО): δ 1,10 (д, J=6,5 Гц, 3), 4,40 (м, 1), 5,10 (д, J=4,5 Гц, 1), 7,12 (с, 2), 10,27 (с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 24,0; 68,4; 119,6; 124,6; 136,2; 147,9; 156,0 м.д.
ТСХ (силикагель-60, F-254): Rf=0,26, 50% этилацетат/гексан.
Температура плавления 89-92oC, раз.
Инфракрасный спектр ( νmax, минеральное масло): 3334, 2925, 2569, 1558, 1090, 840, 761 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [173] (12).
2-Хлор-3-гидрокси-6-(1-гидроксиэтил)пиридин (4,5 г, 28,6 ммоль) суспендируют 70 мл воды в 200-мл одногорлой круглодонной колбе. Суспензию обрабатывают последовательно карбонатом калия (6,5 г, 47,2 ммоль) и йодом (12,0 г, 47,2 ммоль), и реакционную смесь перемешивают 4 часа при комнатной температуре. Избыток йода гасят насыщенным тиосульфатом натрия и устанавливают pH реакционной смеси 3 с помощью 10% соляной кислоты. Твердый продукт собирают, промывают водой и извлекают этилацетатом. Органический слой сушат над сульфатом магния и концентрируют в вакууме до желтого твердого продукта. Твердый продукт промывают хлорформом и сушат с получением 4,4 г (62%) 2-хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)-пиридина.
1H-ЯМР (d6ДМСО): δ 1,10 (д, J-6,5 Гц, 3), 4,38 (кв, J=6,5, 13 Гц, 1), 5,22 (ушир.с, 1), 7,59 (с, 1), 10,2 (ушир. с, 1) м. д.
13C-ЯМР (d6ДМСО): δ 24,0; 68,1; 100,1; 129,6; 136,3; 148,1; 157,7 м.д.
ТСХ (силикагель-60, F-254): Rf=0,24, 50% этилацетат/гексан.
Температура плавления 114-116oC, раз.
Инфракрасный спектр ( νmax, минеральное масло): 3078, 2926, 1669, 1537, 1458, 1377, 1256, 1075, 874 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [299] (16).
Анализ: Рассчитано для C7H7ClINO2: C 28,07; H, 2,36; N, 4,68. Найдено: C, 27,96; H, 2,28; N, 4,55.
2-Хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)-пиридин (6,2 г, 20,7 ммоль) растворяют в 60 мл хлорформа в атмосфере азота в 250-мл одногорлой круглодонной колбе. Раствор разбавляют 60 мл триэтиламина и обрабатывают триметилсилил-ацетиленом (3,2 мл, 22,8 ммоль), затем бис(трифенилфосфин) палладийдихлоридом (435 мг, 0,62 ммоль) и йодидом меди (59 мг, 0,31 ммоль). Реакционную смесь перемешивают 4 часа при комнатной температуре, летучие продукты удаляют в вакууме и остаток разбавляют 50 мл воды. pH смеси устанавливают 2,5 с помощью 5% соляной кислоты, и смесь экстрагируют 4 x 50 мл этилацетата. Объединенные органические слои сушат над сульфатом магния и концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 21-44 объединяют и концентрируют с получением 3,82 г (67%) 2-хлор-3-гидрокси-6-(1- гидроксиэтил)-4-триметилсилилэтинилпиридина.
1H-ЯМР (CDCl3, ТМС): δ 0,20 (с, 9), 1,39 (д, J=6,5 Гц, 3), 2,77 (ушир.с, 1), 4,71 (кв, J=6,5, 13 Гц, 1), 6,07 (ушир.с, 1), 7,16 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 2; 23,8; 68,8; 96,2; 107,0; 119,6; 121,3; 137,1; 147,6; 154,8 м.д.
ТСХ (силикагель-60, F-254): Rf=0,49, 50% этилацетат/гексан.
Температура плавления 97-98oC.
Инфракрасный спектр ( νmax, минеральное масло): 3155, 2924, 2162, 1598, 1461, 1323, 1253, 1198, 1081, 959 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [269] (14).
Анализ: Рассчитано для C12H16ClNO2Si: C, 53,32; H, 5,99; N, 5,18 и найдено 0,18% воды.
Найдено: C, 52,85; H, 5,99; N, 5,02,
2-Хлор-3-гидрокси-6-(1-гидроксиэтил)-4-триметилсилил- этинилпиридин (3,82 г, 14,2 ммоль) растворяют в 125 мл тетрагидрофурана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают трифторацетатом ртути (8,2 г, 19,1 ммоль) и перемешивают 20 минут при 0oC. Реакционную смесь перемешивают 1 час при комнатной температуре, разбавляют 75 мл насыщенного хлорида натрия и смесь энергично перемешивают в течение 1 часа. Устанавливают pH смеси 8 с помощью 2н гидроксида натрия и слои разделяют. Водный слой экстрагируют 10% 4 x 50 мл метанол/дихлорметана, объединенные органические слои сушат над сульфатом магния и концентрируют в вакууме с получением желтой пены. Кристаллизация из эфира дает 5,69 г сырого промежуточного меркуриохлорида. Сырой твердый продукт растворяют в 77 мл этанола в атмосфере азота в 200-мл одногорлой круглодонной колбе при 50oC. Раствор обрабатывают триэтилсиланом (4,9 мл, 30,6 ммоль) и реакционную смесь перемешивают 30 мин при комнатной температуре. Реакционную смесь фильтруют через целит и отфильтрованную лепешку тщательно промывают метанол/дихлорметаном 1: 1. Фильтрат концентрируют в вакууме до желтого масла, которое распределяют между 1 x 75 мл насыщенного бикарбоната натрия и 4 x 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 125 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 18-33 объединяют и концентрируют с получением 1,93 г (50%) 7-хлор-5-(1-гидроксиэтил)-2-триметилсилилфуро [2, 3с] пиридина.
1H-ЯМР (CDCl3, ТМС): δ 0,40 (с, 9), 1,53 (д, J=6,5 Гц, 3), 3,45 (ушир.с, 1), 4,97 (кв, J=6,5, 13 Гц, 1), 6,98 (с, 1),7,46 (с,1)м.д.
13С-ЯМР (CDCl3): δ 1,6; 24,5; 69,5; 110,8; 115,8; 132,6; 137,3; 149,8; 156,6; 170,1 м.д.
ТСХ (силикагель-60, F-254): Rf=0,29, 50% этилацетат/гексан.
Инфракрасный спектр ( νmax, минеральное масло): 3319, 2924, 1607, 1566, 1255, 1296, 1143, 1078, 901 см-1.
Масс-спектр, (M/Z] (относительная интенсивность): [269] (3)
Получение 7-хлор-5-(1-гидроксиэтил)-фуро[2, 3c] пиридина.
Способ A:
Раствор 2-хлор-3-гидрокси-6-(1-гидроксиэтил)-4-триметил- силилэтинилпиридина (2,16 г, 8 ммоль) в 32 мл смеси 1:1 триэтиламин/этанол обрабатывают йодидом меди (76 мг, 0,4 ммоль) и реакционную смесь перемешивают в течение 2 часов при 75oC. Смесь разбавляют 32 мл метанола и обрабатывают 16 мл 2н гидроксида натрия. Смесь перемешивают в течение 25 мин при 75oC, охлаждают и летучие продукты удаляют в вакууме. Остаток растворяют в 50 мл метанола, обрабатывают DARCO и нагревают с обратным холодильником в течение 20 минут. Смесь фильтруют через целит и лепешку тщательно промывают метанолом. Фильтрат концентрируют в вакууме и сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном с получением 1,33 г (82%) 7-хлор-5-(1-гидроксиэтил)-фуро[2, 3c] пиридина.
Способ B:
7-хлор-5-(1-гидроксиэтил)-2-триметилсилилфуро[2,3с]-пиридин (809 мг, 3,0 ммоль) растворяют в 18 мл абсолютного этанола в 100-мл одногорлой круглодонной колбе. Раствор обрабатывают 2н гидроксидом натрия (6 мл, 12 ммоль) и реакционную смесь перемешивают 45 мин при комнатной температуре. Объем этанола удаляют при пониженном давлении и остаток распределяют между 50% насыщенным 1 x 25 мл хлорида натрия и 4 x 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 542 мг (92%) 7-хлор-5-(1-гидроксиэтил)-фуро-[2, 3с] пиридина.
1H-ЯМР (CDCl3, TMC): δ 1,54 (д, J=6,5 Гц, 3), 3,55 (ушир.с, 1), 4,97 (кв, J=6,5, 13 Гц, 1), 6,84 (д, J=2 Гц, 1), 7,53 (с, 1), 7,81 (д, J=2 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 24,4; 69,5; 107,2; 111,3; 132,8; 136,8; 146,8; 14,2; 157,3 м.д.
ТСХ (силикагель-60, F-254): Rf=0,35, 50% этилацетат/гексан.
Температура плавления: 71-73oC.
Инфракрасный спектр ( νmax, минеральное масло): 3205, 2925, 1611, 1572, 1445, 1342, 1122, 1034, 985 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [197] (3).
Анализ: Рассчитано для C9H8ClNO2: C, 54,70; H, 4,08; N, 7,09. Найдено: C, 54,46; H, 4,01; N, 7,04.
7-Хлор-5-(1-гидроксиэтил)фуро[2,3с] пиридин (510 мг, 2,58 ммоль) растворяют в 5 мл дихлорметана в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (281 мкл, 3,87 ммоль) в 2 мл дихлорметана и реакционную смесь перемешивают 30 мин при 0oC, затем 1 час при комнатной температуре. Реакционную смесь гасят 1 x 10 мл насыщенного бикарбоната натрия, слои разделяют и водный слой экстрагируют 3 x 10 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 525 мг (94%) 7-хлор-5-(1-хлорэтил)фуро[2, 3с]пиридина.
1H-ЯМР (CDCl3, ТМС): δ 1,91 (д, J=6,5 Гц, 3), 5,24 (кв, J=6,5, 13 Гц, 1), 6,88 (д, J=2 Гц, 1), 7,70 (с, 1), 7,82 (д, J=2 Гц, 1) м.д.
13C-ЯМР (CDCl3): δ 25,4; 58,4; 107,3; 113,2; 133,1; 136,7; 147,2; 149,3; 154,1 м.д.
ТСХ (силикагель-60, F-254): Rf=0,65, 50% этилацетат/гексан.
Инфракрасный спектр ( νmax, жидкость): 2981, 1610, 1571, 1451, 1316, 1137, 1031, 866 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [215] (6).
Анализ: Рассчитано для C9H7Cl2NO: C, 50,03; H, 3,27; N, 6,48. Найдено: C, 50,27; H, 3,23; N, 6,34.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (565 мг, 2,2 ммоль) растворяют в 4 мл сухого диметилформамида в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают 60% гидридом натрия (175 мг, 4,38 ммоль) и смесь перемешивают 1 час при комнатной температуре. 7-Хлор-5-(1-хлорэтил)-фуро[2, 3с]пиридин (474 мг, 2,2 ммоль) в 2 x 1 мл сухого диметилформамида добавляют к реакционной смеси и смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь разбавляют 1 x 50 мл диэтилового эфира и органический слой промывают 4 x 25 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла.
Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 12-24 объединяют и концентрируют с получением 484 мг бледной пены. Кристаллизация из диэтилового эфира дает 457 мг (61%) 4-амино-6-хлор-2-(1-(7-хлорфуро[2,3с]пиридин-5-ил)этил)тиопиримидина (Соед. N 237) в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,49 (д, J=6,5Гц, 3), 4,89 (кв, J=6,5, 13 Гц, 1), 5,97 (с, 1), 6,92 (д, J=2 Гц, 1), 7,16 (ушир.с, 2), 7,65 (с, 1), 8,12 (д, J= 2 Гц, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,5; 44,5; 99,0; 107,8; 115,0; 131,9; 137,0; 146,2; 151,2; 154,6; 157,6; 164,5; 170,2 м.д.
ТСХ (силикагель-60, F-254): Rf=0,34, 50% этилацетат/гексан
Температура плавления: 156oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 212(36,800); 230(27,000); 249(18,000); 285(12,000).
Инфракрасный спектр ( νmax, минеральное масло): 3471, 3152, 2926, 1649, 1537, 1441, 1365, 1286, 1117, 864 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [340] (41).
Анализ: Рассчитано для C13H10Cl2N4OS: C, 45,76; H, 2,95; N, 16,42. Найдено: C, 45,71; H, 2,75; N, 16,45.
ПРИМЕР 238. 4-Амино-6-хлор-2-(1-(фуро[2,3-с]пиридин-5-ил)- этил)тиопиримидин (Соед. N 238)
7-Хлор-5-(1-гидроксиэтил)фуро[2,3с]пиридин (1,1 г, 4,1 ммоль) растворяют в 10 мл этанола в 50-мл одногорлой круглодонной колбе в атмосфере азота. Раствор обрабатывают 20% гидроксидом палладия на угле (820 мг), затем циклогексеном (4,05 мл, 40,8 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 3,5 часов. Реакционную смесь фильтруют через целит и отфильтрованную лепешку промывают 16 мл этанола. Фильтрат разбавляют 2н гидроксидом натрия (8 мл, 16 ммоль) и реакционную смесь перемешивают 1 час при комнатной температуре. Этанол удаляют при пониженном давлении и остаток распределяют между 1 x 50 мл 50% насыщенного хлорида натрия и 4 x 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до бесцветного масла. Сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 70% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 11-24 объединяют и концентрируют с получением 504 мг (76%) 5-(1-гидроксиэтил)фуро[2,3с]-пиридина.
1H-ЯМР (CDCl3, ТМС): δ 1,55 (д, J=6,5 Гц, 3), 4,19 (ушир.с, 1), 5,01 (кв, J= 6,5, 13 Гц, 1), 6,78 (д, J=2 Гц, 1), 7,56 (с, 1), 7,76 (д, J=2 Гц, 1), 8,76 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 24,7; 69,6; 106,1; 111,8; 132,0; 135,0; 148,8; 151,4; 156,5 м.д.
ТСХ (силикагель-60, F-254): Rf=0,18, 50% этилацетат/гексан.
Инфракрасный спектр ( νmax, жидкость): 3355, 2973, 1614, 1465, 1280, 1130, 1096, 1034, 880 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [163] (2).
5-(1-Гидроксиэтил)-фуро[2,3с]пирилин (450 мг, 2,76 ммоль) растворяют в 6 мл дихлорметана в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (300 мкл, 4,14 ммоль) в 2 мл дихлорметана, и реакционную смесь перемешивают 20 мин при 0oC, затем 1 час при комнатной температуре. Реакционную смесь гасят 1 x 10 мл насыщенного бикарбоната натрия, слои разделяют и водный слой экстрагируют 3 x 10 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 478 мг (96%) 5-(1-хлорэтил)-фуро[2, 3с] пиридина.
1H-ЯМР (CDCl3, ТМС): δ 1,94 (д, J=6,5 Гц, 3), 5,30 (кв, J=6,5, 13 Гц, 1), 6,81 (д, J=2 Гц, 1), 7,73 (с, 1), 7,78 (д, J=2 Гц, 1), 8,84 (с, 1) м.д.
13C-ЯМР (CDCl3): δ 25,4; 59,3; 106,3; 113,6; 133,0; 134,9; 148,8; 151,5; 153,8 м.д.
ТСХ (силикагель-60, F-254): Rf=0,55, 50% этилацетат/гексан.
Инфракрасный спектр ( νmax, жидкость): 2980, 1610, 1462, 1303, 1127, 1033, 760 см-1.
Масс-спектр, [M/Z) (относительная интенсивность): [181] (4).
Анализ: Рассчитано для C9H8ClNO: C, 59,32; H, 4,46; N, 7,69 и найдено 0,34% воды. Найдено: C, 59,05; H, 4,39; N, 7,58.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (602 мг, 2,3 ммоль) растворяют в 4 мл сухого диметилформамида в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают 60% гидридом натрия (186 мг, 4,66 ммоль) и смесь перемешивают 1 час при комнатной температуре. 5-(1-Хлорэтил)- фуро[2,3с]пиридин (424 мг, 2,3 ммоль) в 2 x 1 мл сухого диметилформамида добавляют к реакционной смеси и смесь перемешивают в течение ночи при комнатной температуре. Реакционную смесь разбавляют 1 x 50 мл диэтилового эфира и органический слой промывают 4 x 25 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 50% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 14-24 объединяют и концентрируют с получением 509 мг бледной пены. Кристаллизация из диэтилового эфира дает 432 мг (60%) 4-амино-6-хлор-2-(1-(фуро[2,3c] -пиридин-5-ил)этил) тиопиримидина (Соед. N 238) в виде белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 1,66 (д, J=6,5 Гц, 3), 5,08 (кв, J=6,5, 13 Гц, 1), 6,11 (с, 1), 6,96 (д, J=2 Гц, 1), 7,29 (ушир.с, 2), 7,74 (с, 1), 8,16 (д, J= 2 Гц, 1), 8,84 (с, 1) м.д.
13C-ЯМР (d6ДМСО): δ 21,9; 44,9; 98,6; 106,3; 114,2; 132,9; 134,3; 149,8; 150,7; 153,7; 157,4; 164,2; 170,4 м.д.
ТСХ (силикагель-60, F-254): Rf=0,20, 50% этилацетат/гексан.
Температура плавления 187-188oC.
Ультрафиолетовый спектр ( λmax, этанол), нм (ε) : 231(26,000); 248(18,900); 281(10,200); 287(10,300); 296(6,340).
Инфракрасный спектр ( νmax, минеральное масло): 3453, 2925, 1640, 1567, 1532, 1467, 1370, 1284, 821 см-1.
Масс-спектр, [M/Z] (относительная интенсивность): [306] (8).
Анализ: Рассчитано для C13H11ClN4OS: C, 50,90; H, 3,61; N, 18,26. Найдено: C, 50,82; H, 3,66; N, 18,28.
ПРИМЕР 239. 4-Амино-6-трифторметил-2-(1-(фуро[2,3с]пиридин-5- ил)этил)тиопиримидин (Соед. N 239).
Указанное в заголовке соединение получают по способу, описанному для 4-амино-6-хлор-2-(1-(фуро[2,3с] пиридин-7-ил)этил)тиопиримидина за исключением того, что алкилирование 7-(1-хлорэтил)-фуро[2,3с]пиридина проводят с 4-амино-6- трифторметил-2-меркаптопиримидином (Пример 238). Температура плавления 180-181,5oC.
ПРИМЕР 242. 4-Амино-6-хлор-2-(1-(2-метилфуро[2, 3с]пиридин-5-ил)этил) тиопиримидин (Соед. N 242)
2-Хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)пиридин (3, 60 г, 12 ммоль) и пропаргилтриметилсилан (2,5 мл, 16,8 ммоль) объединяют с оксидом меди (930 мг, 6,5 ммоль) в 20 мл пиридина в пробирке высокого давления с завинчивающейся крышкой. Реакционную смесь нагревают до 110oC в течение 9 часов, охлаждают до комнатной температуры, и летучие продукты удаляют в вакууме. Остаток разбавляют 50 мл этилацетата, фильтруют через целит и фильтрат концентрируют в вакууме. Сырой продукт хроматографируют на 125 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 1,21 г (48%) 7-хлор-5-(1-гидроксиэтил)-2-метилфуро[2, 3с]пиридина (Температура плавления 77-79 oC).
Раствор 7-хлор-5-(1-гидроксиэтил)-2-метилфуро[2,3с] пиридина (269 мг, 1,27 ммоль) в 4 мл этанола обрабатывают последовательно 269 мг 20% палладия на угле и циклогексадиеном (1,2 мл, 12,7 ммоль). Реакционную смесь нагревают до 85oC в течение 45 минут, фильтруют через целит, и лепешку тщательно промывают метанолом. Фильтрат концентрируют в вакууме до масла, которое распределяют между 25 мл насыщенного бикарбоната натрия и 4 х 15 мл этилацетата. Органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 198 мг (88%) 5-(1-гидроксиэтил)-2- метилфуро[2, 3с]пиридина.
Раствор 5-(1-гидроксиэтил)-2-метилфуро[2, 3с]пиридина (207 мг, 1,17 ммоль) в 5 мл метиленхлорида при 0oC обрабатывают тионилхлоридом (0,127 мл, 1,75 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 1,5 часа. Смесь гасят 10 мл насыщенного бикарбоната натрия. Водный слой экстрагируют 3 х 10 мл метиленхлорида и объединенные органические слои сушат над карбонатом калия. Органические слои концентрируют в вакууме с получением 215 мг (94%) 5-(1-хлорэтил)-2-метилфуро[2, 3с]пиридина.
Раствор мезилатной соли 4-амино-6-хлор-2-меркаптопиримидина (283 мг, 1,1 ммоль) в 2 мл N,N-диметилформамида при 0oC обрабатывают 97 мг (60% в масле, 2,4 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 час. Раствор 5-(1-хлорэтил)-2-метилфуро[2, 3с] пиридина (211 мг, 1,1 ммоль) в 2 x 1 мл N,N-диметилформамида добавляют к смеси и реакционную смесь перемешивают в течение 3 дней. Реакционную смесь разбавляют 25 мл этилацетата, промывают 3 x 25 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме и сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя 60% этилацетат/гексаном с получением 220 г продукта, который кристаллизуют из эфира с получением 180 мг (52%) Соед. N 242 (температура плавления 161-163oC).
Следуя общему способу примера 242 и включая несущественные изменения, но используя промежуточные продукты из этого получения и/или соответствующий предшественник пиримидина, синтезируют следующие соединения:
ПРИМЕР 240/Соед. N 240 4-Амино-6-хлор-2-(1-(7-хлор-2- метилфуро[2, 3с] пиридин-5-ил)этил)тиопиримидин, температура плавления 174-175oC.
7-Хлор-5-(1-гидроксиэтил)-2-метилфуро[2, 3с] пиридин (634 мг, 3,0 ммоль) растворяют в 5 мл дихлорметана в атмосфере азота в 10-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (327 мкл, 4,5 ммоль), и реакционную смесь перемешивают в течение 30 минут при 0oC, затем 1 час при комнатной температуре. Реакционную смесь добавляют к 25 мл насыщенного бикарбоната натрия, разбавляют 15 мл дихлорметана и смесь энергично перемешивают. Водный слой промывают 3 х 10 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 640 мг (93%) 7-хлор-5-(1-хлорэтил)-2- метилфуро[2, 3с] пиридина в виде желтого твердого продукта (температура плавления: 48-50oC).
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (442 мг, 1,7 ммоль) суспендируют в 4 мл сухого диметилформамида в атмосфере азота в 10-мл одногорлой круглодонной колбе. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (137 мг, 3,44 ммоль) и смесь перемешивают в течение 1 часапри комнатной температуре. 7-Хлор-5-(1-хлорэтил)-2-метилфуро- [2, 3с] пиридин (395 мг, 1,7 ммоль) в 1 x 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 60 часов. Реакционную смесь разбавляют 50 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 17-30 объединяют и концентрируют с получением 410 мг не совсем белого твердого продукта, который промывают 20 мл 1:1 гексан/диэтиловым эфиром с получением 385 мг (64%) 4-амино-6-хлор-2-(1-(7-хлор-2-метилфуро[2, 3с]пиридин-5- ил)этилтио)пиримидина Соед. N 240 (температура плавления: 174-175 oC).
ПРИМЕР 241/Соед. N 241. 4-Амино-6-трифторметил-2-(1- (7-хлор-2-метилфуро[2, 3с]пиридин-5-ил)этил)тиопиримидин, температура плавления 160-161oC.
Мезилатную соль 4-амино-2-меркапто-6-трифторметилпиримидина (740 мг, 2,5 ммоль) суспендируют в 8 мл сухого диметилформамида в атмосфере азота в 25-мл одногорлой круглодонной колбе. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (220 мг, 5,5 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 7-Хлор-5-(1-хлорэтил)-2-метилфуро[2, 3с]пиридин (585 мг, 2,5 ммоль) в 2 х 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают 18 часов. Реакционную смесь разбавляют 60 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 19-39 объединяют и концентрируют с получением 410 мг не совсем белого твердого продукта, который промывают 20 мл 1:1 гексан/диэтиловым эфиром с получением 385 мг (63%) 4-амино-2-(1-(7-хлор-2-метилфуро[2, 3с] пиридин-5-ил) этилтио)-6-трифторметилпиримидина (Соед. 241) в виде белого твердого продукта (температура плавления 160-161oC).
ПРИМЕР 243/Соед. N 243 4-Амино-6-трифторметил-2-(1-(2- метилфуро[2, 3с] пиридин-5-ил)этил)тиопиримидин, температура плавления 180-181oC.
Мезилатную соль 4-амино-2-меркапто-6-трифторметилпиримидина (616 мг, 2,1 ммоль) суспендируют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл одногорлой круглодонной колбе. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (176 мг, 4,4 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1-Хлорэтил)-2-метилфуро[2, 3с]пиридин (413 мг, 2,1 ммоль) в 2 x 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают 18 часов. Реакционную смесь разбавляют 50 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 24-48 объединяют и концентрируют с получением 562 мг не совсем белого твердого продукта, который промывают диэтиловым эфиром с получением 478 мг (67%) 4-амино-2-(1-(2-метилфуро[2, 3с]пиридин-5-ил)-этилтио)-6- трифторметилпиримидина (Соед. 243) (температура плавления 180-181oС).
ПРИМЕР 244 4-Амино-6-хлор-2-(1-(6-хлор-5-метокси-4-винил- 2-пиридил) этил) тиопиримидин (Соед. N 244)
Раствор 2-хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)пиридина (3,6 г, 12 ммоль) в 36 мл N,N-диметилформамида обрабатывают бис(трифенилфосфин)палладийдихлоридом (632 мг, 0,9 ммоль) и тетравинилоловом (2,7 мл, 15 ммоль), и нагревают при 50oC в течение 24 часов и при комнатной температуре в течение 40 часов. Смесь выливают в 300 мл этилацетата, фильтруют через пад целита и фильтрат промывают 4 x 50 мл насыщенного хлорида натрия. Органические слои концентрируют в вакууме и сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 1,68 г (70%) 2-хлор-3-гидрокси-4-винил-6-(1-гидроксиэтил)пиридина.
Раствор 2-хлор-3-гидрокси-4-винил-6-(1-гидроксиэтил)пиридина (1,46 г, 7,31 ммоль) в 12 мл N,N-диметилформамида обрабатывают гидридом натрия (292 мг, 60% в масле, 7,31 ммоль) и перемешивают при комнатной температуре в течение 1 часа. Смесь обрабатывают метилйодидом (0,5 мл, 8,04 ммоль) и перемешивают в течение 2 часов. Реакционную смесь разбавляют 125 мл этилацетата и промывают 4 x 50 мл насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 25% смесью этилацетат/гексан с получением 1,09 г (78%) 2-хлор-3-метокси-4-винил-6-(1- гидроксиэтил)пиридина.
Раствор 2-хлор-3-метокси-4-винил-6-(1-гидроксиэтил)пиридина (446 мг, 2,09 ммоль) в 10 мл метиленхлорида при 0oC обрабатывают тионилхлоридом (0,227 мл, 3,13 ммоль) и перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь гасят 15 мл насыщенного бикарбоната натрия. Водный слой экстрагируют 3 x 10 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 447 мг (92%) 2-хлор-3-метокси-4-винил-6-(1-хлорэтил)пиридина.
Раствор мезилатной соли 4-амино-6-хлор-2-меркаптопиримидина (433 мг, 1,68 ммоль) в 4 мл N,N- диметилформамида при 0oC обрабатывают 141 мг (60% в масле, 3,53 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 часа. Раствор 2-хлор-3-метокси-4-винил-6-(1-хлорэтил)-пиридина (390 мг, 1,68 ммоль) в 2 x 1 мл N,N-диметилформамида добавляют к смеси и реакционную смесь перемешивают в течение 20 часов. Реакционную смесь разбавляют 50 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме, и сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 122 мг (20%) Соед. N 244 (температура плавления 157-158oC).
ПРИМЕР 245. 4-Амино-6-хлор-2-(1-(4-этил-5-метокси-2- пиридил)этил)тиопиримидин (Соед. N 245)
Раствор 2-хлор-3-метокси-4-винил-6-(1-гидроксиэтил) - пиридина (485 мг, 2,27 ммоль) в 10 мл этанола обрабатывают 485 мг 20% палладия на угле и 1,4-циклогексадиеном (2,0 мл, 21 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 4 часов. Катализатор удаляют путем фильтрования через целит и фильтрующий пад тщательно промывают метанолом. Фильтрат концентрируют в вакууме и остаток распределяют между 25 мл насыщенного бикарбоната натрия и 4 х 25 мл этилацетата. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя 100 мл 50% этилацетат/гексаном, затем 80% этилацетат/гексаном с получением 256 мг (63%) 3-метокси-4-этил-6-(1-гидроксиэтил) пиридина.
Раствор 3-метокси-4-этил-6-(1-гидроксиэтил)-пиридина (236 мг, 1,3 ммоль) в 5 мл метиленхлорида при 0oC обрабатывают тионилхлоридом (0,141 мл, 1,95 ммоль) и перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь гасят 12 мл насыщенного бикарбоната натрия. Водным слой экстрагируют 3 x 10 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 249 мг (96%) 3-метокси-4-этил-6-(1-хлорэтил)пиридина.
Раствор мезилатной соли 4-амино-6-хлор- 2-меркаптопиримидина (290 мг, 1,1 ммоль) в 2 мл N,N-диметилформамида при 0oC обрабатывают 92 мг (60% в масле, 2,3 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 час. Раствор 3-метокси-4-этил-6-(1-хлорэтил)пиридина (225 мг, 1,1 ммоль) в 2 x 1 мл N,N-диметилформамида добавляют по каплям к смеси и реакционную смесь перемешивают в течение 18 часов. Реакционную смесь разбавляют 50 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме и сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя 50% этилацетат/гексаном с получением 256 мг масла, кристаллизация которого из эфира дает 188 мг (53%) Соед. N 245 (температура плавления 136-137oC).
ПРИМЕР 246 4-Амино-6-хлор-2-(1-(3-метилфуро[2, 3с] пиридин-5-ил) этил)тиопиримидин (Соед. N 246)
Раствор 2-хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)пиридина (3,6 г, 12 ммоль) в 24 мл N, N-диметилформамида при 0oC обрабатывают 480 мг (60% в масле, 12 ммоль) гидрида натрия и перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь обрабатывают 1,14 г (13,2 ммоль) аллилбромида и перемешивают в течение 2 часов. Смесь выливают в 125 мл этилацетата и промывают 4 x 50 мл насыщенного хлорида натрия, 2 x 25 мл 50% насыщенного карбоната натрия, и сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме, разбавляют 20 мл гексана и быстро охлаждают до -15oC. Твердый продукт фильтруют с получением 3,61 г (89%) 2-хлор-3-(1-пропен-3-ил)-4-йод-6-(1-гидроксиэтил)пиридина.
Способ A: Раствор 2-хлор-3-(1-пропен-3-ил)-4-йод-6- (1-гидроксиэтил)-пиридин (3,50 г, 10,3 ммоль) в 30 мл N,N-диметилформамида обрабатывают последовательно формиатом натрия (872 мг, 12,8 ммоль), карбонатом натрия (3,28 г, 30,9 ммоль), тетрабутиламмонийхлоридом (3,91 г, 14,1 ммоль) и ацетатом палладия (130 мг, 0,6 ммоль). Реакционную смесь нагревают до 50oC в течение 2 часов, охлаждают до комнатной температуры и разбавляют 150 мл этилацетата. Органические слои промывают 4 x 50 мл 50% насыщенного хлорида натрия, сушат над карбонатом калия, и концентрируют в вакууме. Сырой продукт растворяют в 50 мл метанола, обрабатывают DARCO и нагревают с обратным холодильником в течение 20 минут. Смесь фильтруют через целит и концентрируют в вакууме. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 631 мг (29%) 7-хлор-5-(1-гидроксиэтил)-3-метилфуро[2, 3с] пиридина (температура плавления 67-68oC).
Раствор 7-хлор-5- (1-гидроксиэтил)-3-метилфуро[2,3с]- пиридина (550 мг, 2,6 ммоль) в 12 мл этанола обрабатывают 20% гидроксидом палладия на угле (550 мг) и циклогексадиеном (2,6 мл, 28 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 2 часов. Смесь охлаждают, фильтруют через целит, и фильтрующий пад тщательно промывают метанолом. Фильтрат концентрируют в вакууме и остаток распределяют между 25 мл насыщенного бикарбоната натрия и 4 х 20 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 422 мг (92%) 5-(1- гидроксиэтил)-3-метилфуро[2, 3с]пиридина. (Температура плавления 56-58oC).
Способ B:
Часть 1: 3-(1-пропен-3-ил)-2-хлор-6-(1-гидроксиэтил)-4-йодпиридин (40 г, 117,8 ммоль) объединяют с N,N'-азобис-(изобутирил) нитрилом (1,94 г, 11,8 ммоль) в 260 мл бензола в атмосфере азота в 500-мл одногорлой круглодонной колбе, осушенной в пламени. Раствор нагревают с обратным холодильником и быстро обрабатывают по каплям гидридом трибутилолова (34,2 мл, 127,2 ммоль) в 60 мл сухого бензола. Реакционную смесь перемешивают в течение 1 часа при нагреве с обратным холодильником, охлаждают и бензол удаляют в вакууме. Остаток хроматографируют на 750 г силикагеля (230-400 меш), элюируя 2 л 10% этилацетат/гексана, 2 л 20% этилацетат/гексана, затем 3 л 35% этилацетат/гексана и после прохождения 2 л мертвого объема элюента собирают 50-мл-вые фракции. Фракции 54-102 объединяют и концентрируют с получением 22,2 г (88%) 7-хлор-2,3-дигидро-5-(1-гидроксиэтил)-3- метилфуро [2, 3с] пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,37 (д, J=7 Гц, 3), 1,48 (д, J=6,5 Гц, 3), 2,91 (ушир. с, 1), 3,65 (ушир.с, 1), 4,24 (т, J=8,8 Гц, 1), 4,83 (м, 2), 7,12 (м, 1) м.д.
Часть 1 (предпочтительно альтернативная):
Раствор 2-хлор-3-(1-пропен-3-ил)-4-йод-6-(1-гидроксиэтил) пиридина (1,06 г, 3,14 ммоль) в ТГФ (5 мл) обрабатывают 50% фосфорноватистой кислоты (2,13 г, 15,73 ммоль), триэтиламином (1,75 г, 17,33 ммоль) и 2,2'-азобис(2-метилпропинонитрилом) (AIBN; 192 мг, 1,23 ммоль). Раствор перемешивают при нагреве с обратным холодильником в течение 2 часов. Раствору дают охладиться и концентрируют в вакууме. Добавляют насыщенный NaHCO3 и смесь экстрагируют 3 х EtOAc. Органические слои сушат над MgSO4 и концентрируют в вакууме. Сырое светло-желтое масло хроматографируют (SiO2, гексан/этилацетат, 2:1) с получением 650 мг (97%) 7-хлор-2,3-дигидро-5-(1-гидроксиэтил)-3-метилфуро[2, 3с] пиридина, т.пл. 67-68oC.
Часть 2: 7-Хлор-2,3-дигидро-5-(1-гидроксиэтил)-3-метилфуро [2, 3с] пиридин (26 г, 122 ммоль) растворяют в 200 мл метанола в 500-мл одногорлой круглодонной колбе, обрабатывают 5,5 г DARCO и нагревают с обратным холодильником в течение 20 минут. Смесь фильтруют через целит и отфильтрованную лепешку промывают метанолом. Фильтрат концентрируют в вакууме с получением 25 г бледного масла. Масло растворяют в 160 мл абсолютного этанола, обрабатывают 5,5 г 20% гидроксида палладия на угле и разбавляют 60 мл (120 ммоль) 2н водного гидроксида натрия. Смесь гидрогенируют при 22 фунт/кв. дюйм (1364 г/кв. см) в течение 20 часов. Катализатор удаляют путем фильтрования, и отфильтрованную лепешку промывают свежим абсолютным этанолом. Фильтрат концентрируют в вакууме до пастообразного остатка и распределяют между 1 x 200 мл 50% насыщенного бикарбоната натрия и 4 x 100 мл дихлорметана. Органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 20,1 г (93%) 2,3-дигидро-5-(1-гидроксиэтил)-3-метилфуро[2, 3с]пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,36 (м, 3), 1,48 (м, 3), 3,56 (м, 1), 4,05 (ушир.с, 1), 4,13 (м, 1), 4,86 (т, J=9 Гц, 1), 4,87 (кв, J=6,4, 12,9 Гц, 1), 7,15 (с, 1), 8,03 (с, 1) м.д.
2,3-Дигидро-5-(1-гидроксиэтил)-3-метилфуро [2, 3с] пиридин (20,1 г, 112 ммоль) растворяют в 112 мл пиридина в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают уксусным ангидридом (31,2 мл, 336 ммоль) и перемешивают в течение ночи при комнатной температуре. Пиридин удаляют в вакууме и остаток извлекают в 200 мл этилацетата. Раствор энергично перемешивают в течение одного часа с 200 мл насыщенного бикарбоната натрия, содержащим 35 г твердого бикарбоната натрия. Слои разделяют и органический слой экстрагируют 4 x 100 мл 50% насыщенного хлорида натрия. Органические слои сушат над безводным сульфатом магния и концентрируют в вакууме с получением 24,8 г (колич.) 5-(1-ацетоксиэтил)-2,3-дигидро-3-метилфуро[2, 3с]пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,36 (м, 3), 1,58 (м, 3), 2,11 (м, 3), 3,57 (м, 1), 4,14 (т, J=8,4 Гц, 1), 4,75 (т, J=8,4 Гц, 1), 5,89 (кв, J=6,5, 13 Гц, 1), 7,18 (м, 1), 8,12 (с, 1) м.д.
5-(1-Ацетоксиэтил)-2,8-дигидро-3-метилфуро[2, 3с] пиридин (24,3 г, 110 ммоль) объединяют с 2,3,5,6-тетрахлорбензохиноном (29,6 г, 120,4 ммоль) в 500 мл диоксана в атмосфере азота в 1000-мл одногорлой круглодонной колбе. Реакционную смесь осторожно нагревают с обратным холодильником в течение 24 часов, охлаждают до комнатной температуры, фильтруют и отфильтрованную лепешку тщательно промывают этилацетатом. Фильтрат концентрируют в вакууме до красновато-коричневой суспензии, которую разбавляют 100 мл диоксана, фильтруют и отфильтрованную лепешку промывают диэтиловым эфиром. Фильтрат концентрируют до коричневого масла, разбавляют 500 мл метанола, затем 185 мл (370 ммоль) 2н гидроксида натрия, и реакционную смесь перемешивают 1 час при комнатной температуре. Метанол удаляют в вакууме, водный остаток разбавляют 300 мл воды и смесь экстрагируют 4 x 100 мл дихлорметана. Объединенные органические слои подвергают обратной промывке 1н гидроксидом натрия 2x100 мл, сушат над карбонатом калия и концентрируют в вакууме до зеленоватого масла. Масло растворяют в 200 мл метанола и нагревают с обратным холодильником с DARCO в течение 20 мин Смесь фильтруют через целит, отфильтрованную лепешку тщательно промывают метанолом, и фильтрат концентрируют в вакууме с получением 18,4 г (94%) 5-(1-гидроксиэтил)-3-метилфуро[2, 3с]пиридина (температура плавления 56-58oC).
Раствор 5-(1-гидроксиэтил)-3-метилфуро[2, 3с]пиридин (436 мг, 2,46 ммоль) в 10 мл метиленхлорида при 0oC обрабатывают тионилхлоридом (0,268 мл, 3,69 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 1,5 часа. Смесь гасят 15 мл насыщенного бикарбоната натрия. Водный слой экстрагируют 3 x 10 мл метиленхлорида и объединенные органические слои сушат над карбонатом калия. Органические слои концентрируют в вакууме с получением 467 мг (97%) 5-(1-хлорэтил)-3-метилфуро [2, 3с]пиридина.
Раствор мезилатной соли 4-амино-6-хлор-2-меркаптопиримидина (589 мг, 2,28 ммоль) в 6 мл N,N-диметилформамида при 0oC обрабатывают 192 мг (60% в масле, 4,8 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 часа. Раствор 5-(1-хлорэтил)-3-метилфуро [2, 3с] пиридина (447 мг, 2,28 ммоль) в 2 x 2 мл N,N-диметилформамида добавляют к смеси и реакционную смесь перемешивают в течение 18 часов. Реакционную смесь разбавляют 70 мл этилацетата, промывают 4 x 50 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме, и сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 40% этилацетат/гексаном с получением 460 мг продукта, который промывают эфиром с получением 369 мг (50%) Соед. N 246 (температура плавления 184-185oC).
ПРИМЕР 247. 4-Амино-6-хлор-2-(1-(2,3-дигидрофуро[2, 3с] - пиридин-5-ил)этил)тиопиримидин (Соед. N 247)
5-(1-Гидроксиэтил)фуро[2, 3с] пиридин (489 мг, 3,0 ммоль) растворяют в небольшом сосуде PARR со встряхиванием, который предварительно обрабатывают 0,239 мл (3,6 ммоль) ацетилхлорида. Раствор обрабатывают 210 мг 20% катализатора гидроксида палладия на угле и реакционную смесь встряхивают при 20 фунт/кв. дюйм (1406 г/кв.см) (до 14 фунт/кв. дюйм (984 г/кв.см)) водорода в течение 2 часов. Катализатор удаляют путем фильтрования через целит, и фильтрующий пад слой тщательно промывают метанолом. Фильтрат концентрируют и распределяют между 20 мл насыщенного бикарбоната натрия и 4 х 10 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют. Сырой продукт хроматографируют на 20 г силикагеля (230-400 меш), элюируя смесью хлороформ/этилацетат/ацетон 4:2:1 с получением 495 мг (99%) 5-(1-гидроксиэтил)-(2,3-дигидро)фуро[2,3с] пиридина.
Раствор 5-(1-гидроксиэтил)-(2,3-дигидро)фуро[2, 3с]пиридина (495 мг, 3,0 ммоль) в 10 мл метиленхлорида при 0oC обрабатывают тионилхлоридом и перемешивают при комнатной температуре в течение 2 часов. Реакционную смесь гасят 10 мл насыщенного бикарбоната натрия и распределяют между 10 мл насыщенного бикарбоната натрия и 4 x 10 мл метиленхлорида. Объединенные органические слои концентрируют в вакууме с получением 495 мг (89%) 5-(1-хлорэтил)-(2,3-дигилро)фуро- [2, 3с]пиридина.
Раствор мезилатной соли 4-амино-6-хлор-2-меркаптопиримидина (783 мг, 3,0 ммоль) в 8 мл N,N-диметилформамида при 0oC обрабатывают 243 мг (60% в масле, 6,1 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 часа. Раствор 5-(1-хлорэтил)-(2,3-дигидро)фуро[2, 3с]пиридина (495 мг, 2,7 ммоль) в 2 x 2 мл N,N-диметилформамида добавляют по каплям к смеси и реакционную смесь перемешивают в течение ночи. Смесь разбавляют 60 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме и сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном с получением 600 мг (66%) Соед. N 247. Температура плавления 155-156oC.
ПРИМЕР 248. 4-Амино-6-хлор-2-(1-(3,3-диметил-2,3- дигидрофуро[2, 3с]пиридин-5-ил)этил)тиопиримидин (Соед. N 248).
Раствор 2-хлор-3-гидрокси-4-йод-6-(1-гидроксиэтил)-пиридина (4,49 г, 15 ммоль) в 25 мл N,N-диметилформамида при 0oC обрабатывают 600 мг (60% в масле, 15 ммоль) гидрида натрия и перемешивают при комнатной температуре в течение 1 часа. Реакционную смесь обрабатывают 1,7 мл (16,5 ммоль) 2-метил-3-бромпропена и перемешивают в течение 2 часов. Смесь разбавляют 150 мл этилацетата и промывают 4 x 50 мл 50% насыщенного хлорида натрия/бикарбоната натрия 1:1, и сушат над карбонатом калия. Сырой продукт хроматографируют на 150 г
силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 3,94 г (74%) 2-хлор-3-(2-метил-1-пропен-3-ил)-4-йод-6- (1-гидроксиэтил)-пиридина.
Раствор 2-хлор-3-(2-метил-1-пропен-3-ил)-4-йод-6- (1-гидроксиэтил)-пиридина (3,8 г, 10,9 ммоль) в 18 мл N,N-диметилформамида обрабатывают последовательно формиатом натрия (742 мг, 10,9 ммоль), триэтиламином (4,6 мл, 32,7 ммоль), тетрабутиламмонийхлоридом (3,03 г, 10,9 ммоль) и ацетатом палладия (122 мг, 0,54 ммоль). Реакционную смесь нагревают до 60oC в течение 3 часов и перемешивают при комнатной температуре в течение ночи. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 х 50 мл 50% насыщенного хлорида натрия, сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт растворяют в метаноле, обрабатывают DARCO и нагревают с обратным холодильником в течение 20 мин. Смесь фильтруют через целит и концентрируют в вакууме. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном с получением 1,41 г (55%) 7-хлор-5-(1-гидроксиэтил)-2,3-дигидро-3,3-диметилфуро [2, 3с] пиридина.
Раствор 7-хлор-5-(1-гидроксиэтил)-2,3-дигидро-3,3-диметилфуро [2, 3с] пиридина (425 мг, 1,87 ммоль) в 20 мл этанола обрабатывают 20% гидроксидом палладия на угле (200 мг) и встряхивают в атмосфере водорода (20-14 фунт/кв. дюйм (1406-984 г/кв. см)) в течение 3 часов. Смесь фильтруют через целит. Фильтрат концентрируют в вакууме и остаток распределяют между 20 мл насыщенного бикарбоната натрия и 4 x 20 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 305 мг (85%) 5-(1-гидроксиэтил)-2,3-дигидро-3,3-диметилфуро[2, 3с]-пиридина.
Раствор 5-(1-гидроксиэтил)-2,3-дигидро-3,3-диметилфуро- [2, 3с]-пиридина (805 мг, 4,17 ммоль) в 15 мл метиленхлорида при 0oC обрабатывают тионилхлоридом (0,439 мл, 6,25 ммоль), и реакционную смесь перемешивают при комнатной температуре в течение 2 часов. Смесь гасят 25 мл насыщенного бикарбоната натрия. Водный слой экстрагируют 3 x 20 мл метиленхлорида, и объединенные органические слои сушат над карбонатом калия/сульфатом магния. Органические слои концентрируют в вакууме с получением 880 мг (99%) 5-(1-хлорэтил)-2,3-дигидро-3,3-диметилфуро[2, 3с]-пиридина.
Раствор мезилатной соли 4-амино-6-хлор-2- меркаптопиримидина (1,04 г, 4,04 ммоль) в 12 мл N,N-диметилформамида при 0oC обрабатывают 339 мг (60% в масле, 8,5 ммоль) гидрида натрия и нагревают до комнатной температуры в течение 1 часа. Раствор 5-(1-хлорэтил)-2,3-дигидро-3,3-диметилфуро [2, 3с] -пиридина (856 мг, 4,04 ммоль) в 2 x 3 мл N,N-диметилформамида добавляют к смеси, и реакционную смесь перемешивают в течение 24 часов. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 x 50 мл 50% насыщенного хлорида натрия и сушат над карбонатом калия. Органические слои концентрируют в вакууме и сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 40% этилацетат/гексаном с получением 1 г продукта, который кристаллизуют из эфира с получением 878 мг (65%) Соед. N 248 (Температура плавления 169-170oC).
ПРИМЕР 250/Соед. N 250. 4-Амино-6-хлор-2-(1-(7-хлор-3,3- диметил-2, 3-дигидрофуро[2, 3с] пиридин-5-ил)этил)тиопиримидин, температура плавления 203-205oC.
7-Хлор-2,3-дигидро-3,3-диметил-5-(1-гидроксиэтил)фуро-[2, 3с] пиридин (1,12 г, 4,9 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (520 мкл, 7,4 ммоль), и реакционную смесь перемешивают в течение 20 мин при 0oC, затем 1 час при комнатной температуре. Реакционную смесь добавляют к 20 мл насыщенного бикарбоната натрия, водный слой промывают 3 x 10 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 1,14 г (94%) 7-хлор-5-(1-хлорэтил)-2,3-дигидро-3,3-диметилфуро[2, 3с] пиридина в виде бледно-желтого масла. 1H-ЯМР (CDCl3, ТМС): δ 1,39 (с, 3), 1,40 (с, 3), 1,85 (д, J=6,6 Гц, 3), 4,40 (с, 2), 5,10 (кв, J=6,6, 13,2 Гц, 1), 7,23 (с, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (541 мг, 2,1 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (176 мг, 4,4 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 7-Хлор-5-(1-хлорэтил)-2,3-дигидро-3,3-диметилфуро[2, 3с] пиридин (492 мг, 2,0 ммоль) в 2 x 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают в течение 24 часов. Реакционную смесь разбавляют 70 мл этилацетата, промывают 4 x 25 мл 50% насыщенного хлорида натрия, затем 1 x 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до светло-янтарного масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 22-33 объединяют и концентрируют с получением не совсем белого твердого продукта. Промывка твердого продукта диэтиловым эфиром дает 318 мг (43%) 4-амино-6-хлор-2-(1-(7-хлор-2,3-дигидро-3,3-диметилфуро [2, 3с]пиридин-5-ил)этилтио)-пиримидина в виде белого твердого продукта (температура плавления 203-205oC).
ПРИМЕР 249/Соед. N 249 4-Амино-6-хлор-2-(1-(3-этилфуро[2,3с]- пиридин-5-ил)этил)тиопиримидин, температура плавления 125-126oC.
2-Хлор-3-гидрокси-6-(1-гидроксиэтил)-4-йодпиридин (4,49 г, 15 ммоль) растворяют в 25 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (600 мг, 15 ммоль) и смесь перемешивают 1 час при комнатной температуре. Смесь обрабатывают кротилхлоридом (1,6 мл, 16,5 ммоль) и одним кристалликом литиййодида и реакционную смесь перемешивают 20 часов при комнатной температуре. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 x 50 мл 50% насыщенного хлорида натрия/бикарбоната натрия 1:1 и сушат над безводным сульфатом магния/карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла, которое кристаллизуют из гексана с получением 4,72 г (89%) 3-(2-бутенилокси)-2-хлор-6-(1-гидроксиэтил)-4-йодпиридина в виде белого твердого продукта (температура плавления 61-62,5oC).
2-Хлор-3-(2-бутенилокси)-6-(1-гидроксиэтил)-4-йодпиридин (2,12 г, 6 ммоль) объединяют с тетрабутиламмонийхлоридом (2,28 г, 8,2 ммоль), формиатом натрия (507 мг, 7,5 ммоль), карбонатом натрия (1,91 г, 18 ммоль) и ацетатом палладия (78 мг, 0,35 ммоль) в 18 мл диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Реакционную смесь нагревают до 80oC в течение 2 часов, разбавляют 100 мл этилацетата и смесь экстрагируют 4 х 50 мл 50% насыщенного хлорида натрия/бикарбоната натрия 1: 1. Органические слои сушат над карбонатом калия и концентрируют в вакууме до коричневого масла. Сырое масло извлекают 50 мл метанола, нагревают с обратным холодильником с Darco в течение 20 минут и фильтруют через целит. Фильтрат концентрируют в вакууме до сырого янтарного масла, которое хроматографируют на 50 г силикагеля (230-400 меш), элюируя 37,5% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 26-37 объединяют и концентрируют с получением 484 мг (36%) 7-хлор-5-(1-гидроксиэтил)-3-этил-фуро [2,3с] пиридина в виде бледного масла, которое кристаллизуют при выстаивании (температура плавления 43-45oC).
7-Хлор-5-(1-гидроксиэтил)-3-этилфуро[2, 3с] пиридин (600 мг, 2,7 ммоль) объединяют с 20% гидроксидом палладия на угле (600 мг) в 20 мл абсолютного этанола в атмосфере азота в 100-мл одногорлой круглодонной колбе. Смесь обрабатывают 1,4-циклогексадиеном (2,5 мл, 27 ммоль) и реакционную смесь нагревают с обратным холодильником (быстр. экзотерм.) в течение 2,5 часов. Смесь фильтруют через целит, и лепешку тщательно промывают свежим метанолом. Фильтрат концентрируют в вакууме, и остаток распределяют между 1 x 25 мл насыщенного бикарбоната натрия и 4 х 20 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 464 мг (91%) 5-(1-гидроксиэтил)-3-этилфуро[2, 3с]пиридина в виде не совсем белого твердого продукта.
1H-ЯМР (CDCl3, ТМС): δ 1,19 (т, J=7,5 Гц, 3), 1,51 (д, J=6,9 Гц, 3), 2,75 (м, 2), 4,45 (ушир.с, 1), 4,99 (кв, J= 6,9, 13,8 Гц, 1), 7,44 (с, 1), 7,51 (с, 1), 8,02 (с, 1) м.д.
5-(1-Гидроксиэтил)-3-этил-фуро(2, 3с] пиридин (434 мг, 2,3 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (247 мкл, 3,4 ммоль) и реакционную смесь перемешивают 20 минут при 0oC, затем 3 часа при комнатной температуре. Реакционную смесь добавляют к 25 мл насыщенного бикарбоната натрия, слои разделяют, водный слой промывают 3 x 10 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 467 мг (98%) 5-(1-хлорэтил)-3-этилфуро[2, 3с]пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3,ТМС): δ 1,34 (т, J=7,5 Гц, 3), 1,95 (д, J=7,0 Гц, 3), 2,72 (м, 2), 5,30 (кв, J=7,0, 14 Гц, 1), 7,53 (м, 1), 7,66 (м, 1), 8,77 (м, 1) м. д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (553 мг, 2,2 ммоль) растворяют в 6 мл сухого диметилформамида в атмосфере азота в 25-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (180 мг, 4,5 ммоль), и смесь перемешивают 1 час при комнатной температуре. 5-(1-Хлорэтил)-3-этилфуро[2, 3с]пиридин (450 мг, 2,2 ммоль) в 2x4 мл сухого диметилформамида, добавляют по каплям к реакционной смеси, и смесь перемешивают 24 часа. Реакционную смесь разбавляют 75 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 51-84 объединяют и концентрируют с получением белой пены. Кристаллизация из диэтилового эфира дает 382 мг (53%) 4-амино-6- хлор-2-(1-(3- этилфуро[2,3с] пиридин-5-ил)этиллтио)пиримидина в виде белого твердого продукта (температура плавления 125-126oC).
ПРИМЕР 251/Соед. N 251. 4-Амино-6-хлор-2-(1-(7-хлор-3- этилфуро-[2, 3с] пиридин-5-ил)этил)тиопиримидин, температура плавления 165-166oC.
7-Хлор-5-(1-гидроксиэтил)-3-этилфуро[2, 3с] пиридин (904 мг, 4,0 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (422 мкл, 6,0 ммоль), и реакционную смесь перемешивают 20 мин при 0oC, затем 1 час при комнатной температуре. Реакционную смесь добавляют к 20 мл насыщенного бикарбоната натрия, слои разделяют, водный слой промывают 3 х 10 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 965 мг (98%) 7-хлор-5-(1-хлорэтил)-3-этил-фуро[2, 3с]пиридина в виде желтого масла.
1H-ЯМР (CDCl3,TMC): δ 1,31 (т, J=7,5 Гц, 3), 1,90 (д, J=6,9 Гц, 3), 2,70 (м, 2), 5,23 (кв, J=6,9, 13,8 Гц, 1), 7,58 (м, 1), 7,69 (с, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,03 г, 4,0 ммоль) растворяют в 12 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (336 мг, 8,4 ммоль) и смесь перемешивают 1 час при комнатной температуре. 7-Хлор-5- (1-хлорэтил)-3-этилфуро[2, 3с]пиридин (924 мг, 3,8 ммоль) в 2 х 3 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают 60 часов. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 х 50 мл 50% насыщенного хлорида натрия, затем 1 х 50 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 21-33 объединяют и концентрируют с получением белого твердого продукта. Твердый продукт промывают диэтиловым эфиром с получением 782 мг (56%) 4- амино-6-хлор-2-(1-(7-хлор-3-этилфуро[2, 3с] пиридин-5-ил)- этилтио)-пиримидина (температура плавления 165-166oC).
ПРИМЕР 252/Соед.N 252. 4-Амино-6-хлор-2-(1-(3-(1-метилэтил) фуро[2, 3с] -пиридин-5-ил)этил)тиопиримидин. Температура плавления 115-117oC.
2-Хлор-3-гидрокси-6-(1-гидроксиэтил)-4-йодпиридин (2, 99 г, 10 ммоль) растворяют в 15 мл сухого диметилформамида в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (400 мг, 10 ммоль), и смесь перемешивают 1 час при комнатной температуре. Смесь обрабатывают 1-хлор-3-метил-2-бутеном (1,2 мл, 11 ммоль) и йодидом натрия (150 мг, 1 ммоль) и реакционную смесь перемешивают 18 часов при комнатной температуре. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 х 50 мл 50% насыщенного хлорида натрия/бикарбоната натрия 1: 1 и сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла, которое кристаллизуют из 25 мл гексана с получением 3,2 г (87%) 2-хлор-3-(3-метил-2-бутенилокси)-6-(1-гидроксиэтил)-4-йодпиридина в виде не совсем белого твердого продукта, температура плавления 80-81oC.
2-Хлор-3-(3-метил-2-бутенилокси)-6-(1-гидроксиэтил) -4-йодпиридин (3,12 г, 8,5 ммоль) объединяют с тетрабутиламмонийхлоридом (2,36 г, 8,5 ммоль), формиатом натрия (577 мг, 8,5 ммоль), триэтиламином (3,6 мл, 25 ммоль) и ацетатом палладия (95 мг, 0,42 ммоль) в 18 мл диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Реакционную смесь нагревают до 60oC в течение 2 часову, разбавляют 125 мл этилацетата и смесь экстрагируют 4 х 50 мл 50% насыщенного хлорида натрия. Органические слои сушат над карбонатом калия и концентрируют в вакууме до коричневого масла. Сырое масло извлекают 50 мл метанола, нагревают с обратным холодильником с Darco в течение 20 минут и фильтруют через целит. Фильтрат концентрируют в вакууме до сырого янтарного масла, которое хроматографируют на 100 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 14-21 объединяют и концентрируют с получением 698 мг (34%) 7-хлор-5-(1-гидроксиэтил)-3-изопропилфуро[2, 3с] пиридина в виде желтого масла, которое кристаллизуют при выстаивании (температура плавления 45-46,5oC).
7-Хлор-5-(1-гидроксиэтил)-3-изопропилфуро[2, 3с] пиридин (678 мг, 2,8 ммоль) объединяют с 20% гидроксидом палладия на угле (678 мг) в 20 мл абсолютного этанола в атмосфере азота в 50-мл одногорлой круглодонной колбе. Смесь обрабатывают 1,4-циклогексадиеном (2,7 мл, 28 ммоль) и реакционную смесь нагревают с обратным холодильником (быстр. экзотерм.) в течение 2 часов. Смесь фильтруют через целит, и лепешку тщательно промывают со свежим метанолом. Фильтрат концентрируют в вакууме, и остаток распределяют между 1 х 20 мл насыщенного бикарбоната натрия и 4 х 15 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 554 мг (96%) 5-(1-гидроксиэтил)-3-изопропилфуро[2, 3с] пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,33 (д, 6), 1,56 (д, J=6,5 Гц, 1), 3,09 (м, 1), 4,16 (ушир.с, 1), 5,02 (кв, J=6,5, 13 Гц, 1), 7,50 (м, 1), 7,54 (с, 1), 8,72 (с, 1) м.д.
5-(1-Гидроксиэтил)-3-изопропилфуро[2, 3с] пиридин (544 мг, 2,6 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (279 мкл, 4,0 ммоль) и реакционную смесь перемешивают 20 минут при 0oC, затем 1 час при комнатной температуре. Реакционную смесь добавляют к 15 мл насыщенного бикарбоната натрия, слои разделяют, водный слой промывают 3 х 10 мл дихлорметана и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 554 мг (93%) 5-(1-хлорэтил)-3-изопропилфуро[2, 3с] пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, TMC): δ 1,37 (д, 6), 1,96 (д, J=6,5 Гц, 3), 3,10 (м, 1), 5,23 (кв, J=6,5, 13 Гц, 1), 7,51 (м, 1), 7,70 (м, 1), 8,78 (м, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (785 мг, 3,0 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колб, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (267 мг, 6,7 ммоль) и смесь перемешивают 1 час при комнатной температуре. 5-(1-Хлорэтил)-3-изопропил-фуро[2, 3с]пиридин (524 мг, 2,3 ммоль) в 2 х 3 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают 24 часа. Реакционную смесь разбавляют 100 мл этилацетата, промывают 3 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 45 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции после 120 мл выведенного мертвого объема. Фракции 16-39 объединяют и концентрируют с получением 631 мг бледной пены. Кристаллизация из диэтилового эфира/гексана (капли) дает 564 мг (69%) 4-амино-6-хлор-2-(1-(3-изопропилфуро[2, 3с]пиридин-5- ил)этилтио)пиримидина в виде белого твердого продукта (температура плавления 115-117oC).
ПРИМЕР 253. Получение 4-амино-6-хлор-2-(1-(4- циклопентил)-2-пиридил)этил)тиоиримидина (Соед. N 253)
Часть A: 1-(2-(4-циклопентил)пиридил)этанол (100 мг, 0,52 ммоль) растворяют в CH2Cl2 (2 мл) при 0oC, затем обрабатывают триэтиламином (0,1 мл, 0,72 ммоль) и MsCl (60 мкл, 0,65 ммоль). После перемешивания при 20oC в течение 30 минут добавляют насыщенный NaHCO3 (1 мл), и водный слой экстрагируют три раза CH2Cl2, органические слои объединяют, промывают насыщенным NaHCO3 и насыщенным NaCl, сушат над MgSO4 и концентрируют в вакууме: 120 мг (0,44 ммоль, 85%) т.пл. 141-143oC.
Часть B: Мезилатную соль 4-амино-6-хлор-2-тиопиримидина (Соед. N 110A; 100 мг, 0,39 ммоль) в EtOH (0,5 мл) при 40oC обрабатывают 3,25М NaOH (0,25 мл, 0,8 ммоль) и перемешивают в течение 15 минут. Добавляют мезилат из Части A (120 мг, 0,44 ммоль) и перемешивают в течение 1 часа. После охлаждения до 20oC добавляют воду, и реакционную смесь фильтруют. Твердый продукт промывают водой и этанолом, затем сушат: 46 мг (0,14 ммоль, 35%) Соед. N 253, т. пл. 144-146oC.
Следуя общему способу примера 253 и проводя несущественные изменения, но используя в качестве исходного продукта соответствующий спирт, синтезируют следующие соединения:
ПРИМЕР 255. 4-амино-6-хлор-2-(1-(4-циклопропил)-2-пиридил) этил)тиопиримидин, т.пл. 148-149oC.
ПРИМЕР 256. 4-амино-6-хлор-2-(1-(4-(1-метилпропил)-2- пиридил)этил)тиопиримидин, т.пл. 108-110oC.
ПРИМЕР 257. 4-амино-6-хлор-2-(1-(4-циклогексил)-2- пмридил)этил)тиопиримидин, т.пл. 62-64oC.
ПРИМЕР 258. 4-амино-6-хлор-2-(1-(4-(1-пиррил))-2- пиридил)этил)тиопиримидин, т.пл. 189oC.
ПРИМЕР 259. 4-амино-6-хлор-2-(1-(4-диметиламино)-2- пиридил)этил)тиопиримидин
ЯМР: δ (CDCl3) 8,20-8,21 (д, J=5,90, 1H), 6,71 (м, 1H), 6,37-6,39 (м, 1H), 6,10 (с, 1H), 5,00-5,02 (м, 3H), 3,01 (с, 6H), 1,76-1,77 (д, J=7,13, 3H).
ПРИМЕР 260. 4-амино-6-хлор-2-(1-(5-(1-метилэтил)-3-пиридил) этил)тиопиримидин, т.пл. 123-124oC.
ПРИМЕР 261. 4-амино-6-хлор-2-(1-(4-(1-этилпропил)-2-пиридил) этил)тиопиримидин, т.пл. 146-147oC.
ПРИМЕР 262. 4-амино-6-хлор-2-(1-(4-метил-6-(1-пиррил))-2- пиридил)этил)тиопиримидин, т.пл. 155-157oC.
ПРИМЕР 263. 4-амино-6-хлор-2-(1-(4-(2-пропилокси)) -2-пиридил)этил)тиопиримидин
ЯМР: δ (CDCl3) 8,34-8,36 (д, J=5,76, 1H), 6,97 (м, 1H), 6,63-6,65 (м, 1H), 6,11 (с, 1H), 5,10 (с, 2H), 5,03-5,08 (кв, J=7,13, 1H), 4,61-4,67 (м, 1H), 1,74-1,76 (д, J=7,18, 3H), 1,34-1,36 (м, 6H).
ПРИМЕР 264. Получение 4-гидрокси-6-трифторметил-2-пиримидинтиола (Соед. N 264)
К раствору 25% NaOMe/MeOH (23 мл, 0,10 моль) и этанола (27 мл) добавляют тиомочевину (5,33 г, 0,70 моль) и этил-4,4,4-трифторацетоацетат (7,3 мл, 50 ммоль), затем реакционную смесь нагревают с обратным холодильником в течение 16 часов. Смесь охлаждают до 22oC, концентрируют в вакууме, и остаток растворяют в воде (50 мл), подкисляют HCl (7 мл) и фильтруют. Твердый продукт собирают, промывают водой и сушат: 6,58 г (32,5 ммоль, 65%).
ПРИМЕР 265. Получение 6-трифторметил-2-(4-метокси-фенил- метил)тио-4-пиримидинола (Соед. 265)
4-гидрокси-6-трифторметил-2-пиримидинтиол (Соед. N 264; 4,90 г, 25,0 ммоль) в этаноле (8 мл) обрабатывают 3,25н NaOH (8 мл, 26,0 ммоль), затем 4-метоксибензилхлоридом (3,5 мл, 25,7 ммоль). После нагревания с обратным холодильником в течение 1 час реакционную смесь разбавляют водой и фильтруют. Твердый продукт перекристаллизовывают из этанола: 4,63 г (14,6 ммоль, 58%), т.пл. 169-170oC.
ПРИМЕР 266. Получение 4-хлор-6-трифторметил-2-(4-метокси- фенилметил)тиопиримидина
6-Трифторметил-2-(4-метоксифенилметил)тио-4-пиримидинол (Соед. 265; 7,9 г, 25 ммоль), POCl3 (19 мл) и 2-пиколин (2,5 мл) объединяют и нагревают с обратным холодильником в течение 18 часов. Реакционную смесь выливают на лед, экстрагируют трижды с этилацетатом, сушат с MgSO4 и концентрируют в вакууме.
ПРИМЕР 267. Получение 4-амино-6-трифторметил-2-(4- метоксифенилметил)тиопиримидина
Сырое масло примера 266 (Соед. N 266) растворяют в ацетонитриле (75 мл) и гидроксиде аммония (150 мл), затем перемешивают в течение 18 часов при 22oC. Реакционную смесь экстрагируют трижды этилацетатом, сушат с MgS04 и концентрируют в вакууме: 7,20 г (22,8 ммоль, 91%).
ЯМР: δ (CDCl3) 7,35 (д, J=8,5, 1H), 6,83 (д, J=8,5, 1H), 6,41 (с, 1H), 5,2 (с, 2H), 4,33 (с, 2H), 3,79 (с, 3H).
ПРИМЕР 268. Получение мезилатной соли 4-амино-6-трифторметил- 2-пиримидинтиола (Соед. N 268).
4-амино-6-трифторметил-2-(4-метоксифенилметил) тиопиримидин (Соед. N 267; 7,20 г, 22,8 ммоль) растворяют в метиленхлориде (100 мл) и обрабатывают метансульфоновой кислотой (14,3 мл, 220 ммоль), и перемешивают в течение 21 часа. Твердый продукт фильтруют, промывают водой и сушат в вакууме. Температура плавления 222-223oC.
ПРИМЕР 269. Получение 4-амино-6-трифторметил-2-(1-(4-(1-диметилэтил)-2-пиридил)этил)тиопиримидина (Соед. N 269).
Мезилатную соль 4-амино-6-трифторметил-2-пиримидинтиола (Соед. N 268; 400 мг, 2,05 ммоль) в EtOH (0,63 мл) при 40oC обрабатывают 3,25М NaOH (0,63 мл, 2,05 ммоль) и перемешивают в течение 15 минут. Добавляют 1-(4-(1,1-диметилэтил)-2- пиридил)этилхлорид (550 мг, 2,30 ммоль) и перемешивают в течение 1 часа. После охлаждения до 20oC добавляют воду и реакционную смесь фильтруют. Твердый продукт промывают водой и этанолом, затем сушат: 315 мг (0,88 ммоль, 43%), т.пл. 162-163oC.
Следуя общему способу примера 269 и проводя несущественные изменения, но используя в качестве исходного продукта соответствующий галогенид, синтезируют следующие соединения:
ПРИМЕР 270/СОЕД. N 270. 4-амино-6- трифторметил-2-(2- нафтилметил)тиопиримидин, т.пл. 144-145oC.
ПРИМЕР 271/СОЕД. N 271. 4-амино-6-трифторметил-2-((4-(1- метилэтил)-2-пиридил)метил)тиопиримидин, т.пл. 150oC.
ПРИМЕР 272/СОЕД. N 272. 4-амино-6-трифторметил-2-(1-(4-(1- метилэтил)-2-пиридил)этил)тиопиримидин, т.пл. 145oC.
ПРИМЕР 273/СОЕД. N 273. 4-амино-6-трифторметил-2-((4-(1,1- диметилэтил)-2-пиридил) метил)тиопиримидин, т.пл. 164oC.
ПРИМЕР 274. Получение 4-(диэтоксиметил)-6-гидрокси-2- (2-нафтилметил)тиопиримидина (Соед. N 274)
Этил(4,4-диэтокси)ацетоацетат (12,4 г, 56,8 ммоль) и тиомочевину (4,57 г, 60 ммоль) в этаноле (45 мл) обрабатывают 25% NaOMe/MeOH (13 мл, 56,8 ммоль), затем нагревают с обратным холодильником в течение 4 часов. Реакционную смесь разбавляют с водой (50 мл), затем обрабатывают 2-бромметилнафтиленом (12,00 г, 54,3 моль). Через 1 час реакционную смесь разбавляют водой и фильтруют: 11,17 г (30,1 ммоль, 55%).
ЯМР: δ (ДМСО) 7,94 (с, 1H), 7,85 (м, 3H), 7,58 (дд, Jd1=8,4, Jd2=1,6, 1H), 7,47 (м, 3H), 6,15 (с, 1H), 5,21 (с, 1H), 4,56 (с, 2H), 3,58 (м, 4H), 1,14 (м, 6H).
ПРИМЕР 275. Получение 6-гидрокси-2-(2-нафтилметил)тио-4- пиримидинкарбоксальдегидоксима (Соед. N 275).
4-(Диэтоксиметил)-6-гидрокси-2-(2-нафтилметил) тиопиримидин (Соед. N 274; 1,00 г, 2,7 ммоль) суспендируют в 50% HOAc (20 мл) и нагревают с обратным холодильником в течение 2 часов, затем концентрируют в вакууме. Остаток суспендируют в горячем этаноле (25 мл), обрабатывают NaOAc (1,5 г), затем раствором гидроксиламингидрохлорида (1,0 г) в воде (25 мл). Раствор нагревают с обратным холодильником в течение 30 мин, затем охлаждают до 0oC и фильтруют: 720 мг (2,31 ммоль, 86%).
ЯМР: δ (ДМСО) 12,0 (с, 1H), 8,03 (с, 1H), 7,9 (с, 1H), 7,85 (м, 3H), 7,58 (д, J=8,4, 1H), 7,48 (м, 3H), 6,3 (с, 1H), 4,56 (с, 2H).
ПРИМЕР 276. Получение 6-хлор-2-(2-нафтилметил)тио-4- пиримидинкарбонитрила (Соед.276)
6-гидрокси-2- (2-нафтилметил)тио-4-пиримидинкарбоксальдегидоксим (720 мг, 2,31 ммоль), POCl3 (3 мл) и 2-пиколин (0,5 мл) нагревают с обратным холодильником в течение 2 часов. Реакционную смесь выливают на лед/воду, экстрагируют трижды этилацетатом, сушат с MgSO4 и концентрируют в вакууме. Продукт очищают с помощью хроматографии (SiO2, этилацетат/гексан, 5/95): 524 мг (1,67 ммоль, 73%), т.пл. 120-121oC.
ПРИМЕР 277. Получение 6-амино-2-(2-нафтилметил)тио-4- пиримидинкарбонитрила (Соед. 277)
6-Хлор-2-(2-нафтилметил)тио-4-пиримидинкарбонитрил, Соед. 276; (60 мг, 3,07 ммоль) перемешивают в ТГФ/NH4OH (1:1, 15 мл) при 22oC в течение 6 часов. Реакционную смесь разбавляют этилацетатом, промывают насыщенным солевым раствором, сушат с MgSO4, затем концентрируют в вакууме: 871 мг (2,97 ммоль, 97%), т.пл. 154-155oC.
ПРИМЕР 278. 4-aминo-6-гидpoкcи-2-тиo-5-пиpимидинилэтaнoл (Соед. 278).
Металлический натрий (3,91 г, 0,17 моль) добавляют к абсолютному этанолу (535 мл) и после окончательного растворения металла добавляют вместе тиомочевину (7,74 г, 0,102 моль) и α-циано-γ-бутиролактон (11,325 г, 0,102 моль) (Fissekis, Myles и Brown, G.B., J. Org. Chem., 29, 2670 (1964)). Реакционную смесь нагревают с обратным холодильником в течение 18 часов. После охлаждения и концентрации в вакууме остаток растворяют в холодной воде (75 мл), и водный слой промывают 2х диэтиловым эфиром. Водный слой нейтрализуют ледяной уксусной кислотой, и полученный осадок собирают путем фильтрования: 13,08 г (70 ммоль, 68%), т.пл. 293-295oC (раз.).
ПРИМЕР 279. Получение 2-(4-амино-6-гидрокси-2-[2- нафтилметил]тио-5-пиримидинил)-этанола (Соед. N 279)
4-Амино-6-гидрокси-2-тио-5-пиримидинилэтанол (Соед. 278; 2,33 г, 12,8 ммоль) суспендируют в этаноле (3,9 мл) и обрабатывают 3,25 М NaOH (3,92 мл, 12,8 ммоль). Добавляют 2-бромметилнафталин (2,88 г, 13,0 ммоль) и перемешивают в течение 18 часов при 22oC. Раствор охлаждают до 0oC и фильтруют: 3,87 г (11,9 ммоль, 93%), т.пл. 192-193oC.
ПРИМЕР 280. Получение 2-(4-амино-6-гидрокси-2- (2-нафтилметил)тио-5-пиримидинил)-1-(диметил-трет-бутилсилилокси)этана (Соед. N 280)
2-(4-Амино-6-гидрокси-2- [2-нафтилметил]тио-5-пиримидинил)-этанол (Соед. N 279; 106 мг, 0,32 ммоль) растворяют в пиридине (0,64 мл) и раствор охлаждают до 0oC, затем обрабатывают трет-бутилдиметилсилилхлоридом (0,058 г, 0,39 ммоль). Раствор перемешивают при 0oC в течение 2 часов, и два новых пятна появляются в смеси. Реакционную смесь выливают в метиленхлорид и промывают 3х 1 М HCl, 10% HCl, 3х H2O, 2х 6% NaHCO3, сушат с MgSO4, затем концентрируют в вакууме. Сырой продукт затем очищают с помощью хроматографии (SiO2 1:1 гексан/этилацетат): 60 мг (0,18 ммоль, 57%), т.пл. 156-158oC.
ПРИМЕР 281 Получение 4-хлор-2-(нафтилметил)тио-5,6-дигидро- 7H-пирроло[2, 3-d]пиримидина (Соед. N 281).
2-(4-Амино-6-гидрокси-2-(2-нафтилметил)тио-5-пиримидинил)-1- (диметил-трет-бутилсилилокси) этан (Соед. N 280; 104 мг, 0,23 ммоль) обрабатывают 2-пиколином (28 мкл, 0,28 ммоль) и оксихлоридом фосфора (0,22 мл, 2,3 ммоль). Раствор нагревают с обратным холодильником в течение 2 часов, перемешивают в течение ночи при 22oC, затем снова нагревают с обратным холодильником в течение дополнительного часа. Раствор охлаждают и добавляют лед. Полученный твердый продукт фильтруют, промывают холодным 50% этанолом и сушат в вакууме. Извлеченные твердые продукты, 81 мг, очищают путем хроматографии (SiO2 4:1 гексан/этилацетат): 64 мг (0,19 ммоль, 85%), т.пл. 107-110oC.
ПРИМЕР 282. Получение 4-амино-6-хлор-2-(1-(3-хлорфуро[2, 3с]- пиридин-5-ил) этил) тиопиримидина.
Раствор 5-(1-гидроксиэтил)фуро[2, 3с] пиридина (2,64 г, 16,2 ммоль) в 50 мл метиленхлорида при 0oC обрабатывают триэтиламином (2,7 мл, 19,4 ммоль), затем ацетилхлоридом (1,38 мл, 19,4 ммоль) и реакционную смесь перемешивают при комнатной температуре в течение 3 часов. Смесь промывают 2 х 50 мл насыщенного бикарбоната натрия, органические слои сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 15% этилацетат/гексаном с получением 2,4 г (72%) 5-(1- ацетилоксиэтил)фуро[2, 3с]пиридина.
Раствор 5-(1-ацетилоксиэтил)фуро[2, 3с]пиридина (616 мг, 3,0 ммоль) в 30 мл метиленхлорида при 0oC насыщают хлором (газ) и дают медленно нагреться до комнатной температуры. Реакционную смесь перемешивают в течение 2 часов, наслаивают 30 мл насыщенного бикарбоната натрия и осторожно перемешивают в течение 1,5 часа. Смесь далее разбавляют 20 мл насыщенного бикарбоната натрия и энергично перемешивают в течение 20 минут. Водный слой экстрагируют 3 х 15 мл метиленхлорида, и объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт (856 мг) объединяют с 256 мг подобным образом полученного продукта и хроматографируют на 50 г силикагеля (230-400 меш), элюируя 15% смесью этилацетат/гексан с получением 757 мг (69%) 5-(1- ацетилоксиэтил)-2,3-дихлор-2,3-дигидрофуро[2,3с]пиридина.
Раствор 5-(1-ацетилоксиэтил)-2,3-дихлор-2,3-дигидрофуро- [2, 3с]пиридина (680 мг, 2,46 ммоль) в 18 мл этанола обрабатывают 2,04 г (14,8 ммоль) карбоната калия и энергично перемешивают в течение 2 часов. Летучие продукты удаляют в вакууме, и остаток распределяют между 25 мл 50% насыщенного хлорида натрия и 4 х 25 мл метиленхлорида. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме. Сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 50% этилацетат/гексаном с получением 395 мг (81%) 5-(1-гидроксиэтил)- 3-хлорфуро[2, 3с]пиридина.
Хлорирование 370 мг (1,9 ммоль) 5-(1-гидроксиэтил)-3-хлорфуро[2, 3с] пиридина тионилхлоридом, как описано для Соед. N 246, дает 378 мг (92%) 5-(1-хлорэтил)-3- хлорфуро-[2, 3с]пиридина.
Алкилирование 365 мг (1,70 ммоль) 5-(1-хлорэтил)-3-хлорфуро [2, 3с]пиридина, 657 мг (2,55 ммоль) мезилатной соли, 4-амино-6-хлор-2-меркаптопиримидина (Соед. N 110A), как описано для Соед. N 246, дает 286 мг (49%) 4-амино-6-хлор-2-(1-(3- хлорфуро[2, 3с] пиридин-5-ил)этил)тиопиримидина (температура плавления 184-186oC).
ПРИМЕР 283. Получение 4-амино-6-хлор-2-(1-(3,7-дихлорфуро[2, 3с] пиридин-5-ил)этил)тиопиримидина, температура плавления 190-191oC.
7-Хлор-5-(1-гидроксиэтил)-фуро[2, 3с] пиридин (1,98 г, 10 ммоль) растворяют в 4 мл пиридина в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают с уксусным ангидридом (2 мл, 22 ммоль) и реакционную смесь перемешивают в течение 3 часов при комнатной температуре. Объем части летучих продуктов удаляют в вакууме, и остаток распределяют между 1 х 50 мл насыщенного бикарбоната натрия и 4 х 25 мл дихлорметана. Органические слои сушат над безводным карбонатом калия, концентрируют в вакууме до бледного масла. Сырой продукт хроматографируют на 40 г силикагеля, элюируя 16% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 17-33 объединяют и концентрируют с получением 1,10 г (92%) 5-(1-ацетоксиэтил)-7-хлорфуро[2, 3с]пиридина в виде бесцветного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,63 (д, J=6,6 Гц, 3), 2,13 (с, 3), 5,97 (кв, J= 6,6, 13,2 Гц, 1), 6,85 (д, J=2, 1), 7,55 (с, 1), 7,81 (д, J=2, 1) м.д.
5-(1-Ацетоксиэтил)-7-хлорфуро[2, 3с]пиридин (1,05 г, 4,4 ммоль) растворяют в 30 мл дихлорметана в атмосфере азота в 100-мл одногорлой круглодонной колбе. Реакционную смесь охлаждают до 0oC, насыщают газообразным хлором, дают медленно нагреться до комнатной температуры и перемешивают в течение 2 часов при комнатной температуре. На раствор наслаивают 40 мл насыщенного бикарбоната натрия, осторожно перемешивают в течение 6 часов, затем перемешивают энергично в течение 15 мин. Смесь дополнительно разбавляют 10 мл насыщенного бикарбоната натрия. Водный слой экстрагируют 2 х 20 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 1,34 г (98%) 5-(1-ацетоксиэтил)-2,3-дигидро-2,3,7-трихлорфуро [2,3с] пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,59 (м, 3), 2,13 (м, 3), 5,44 (м, 1), 5,90 (м, 1), 6,53 (с, 1), 7,43 (м, 1) м.д.
5-(1-Ацетоксиэтил)-2,3-дигидро-2,3,7-трихлорфуро[2,3c] пиридин (1,34 г, 4,3 ммоль) растворяют в 18 мл абсолютного этанола в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор обрабатывают карбонатом калия (3,5 г, 25 ммоль) и реакционную смесь энергично перемешивают в течение ночи. Суспензию доводят до гомогенности с водой, разбавляют 5 мл 2н гидроксида натрия, и летучие продукты удаляют в вакууме. Остаток распределяют между 1 х 50 мл 50% насыщенного хлорида натрия и 4 х 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до желтой пасты. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 20% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 27-48 объединяют и концентрируют с получением 857 мг (84%) 5-(1-ацетоксиэтил)- 3,7-дихлор-2,3-дигидрофуро[2, 3с]пиридина (9) в виде белого твердого продукта (температура плавления 98-101oC).
3-Хлор-(1-гидроксиэтил)-фуро[2, 3с]пиридин (800 мг, 3,5 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (375 мкл, 5,2 ммоль), и реакционную смесь перемешивают в течение 20 минут при 0oC, затем 1 час при комнатной температуре. Реакционную смесь добавляют к 50 мл насыщенного бикарбоната натрия, водный слой промывают 3 х 10 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 847 мг желтого масла. Сырой продукт хроматографируют на 40 г силикагеля (230-400 меш), элюируя 10% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 6-16 объединяют и концентрируют с получением 807 мг (93%) 5-(1- хлорэтил)-3,7-дихлорфуро[2, 3с] пиридина в виде бесцветного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,93 (д, J=6,7 Гц, 3), 5,23 (кв, J=6,7 Гц, 13,4 Гц, 1), 7,72 (с, 1), 7,85 (с, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,12 г, 4,4 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (224 мг, 5,6 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1- Хлорэтил)-3,7-дихлорфуро[2, 3с]пиридин (780 мг, 3,1 ммоль) в 2х2 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 72 часов. Реакционную смесь разбавляют 100 мл этилацетата, промывают 4 х 50 мл 50% насыщенным 1:1 хлоридом натрия/бикарбонатом натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтой пасты. Сырой продукт хроматографируют на 60 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 14-21 объединяют и концентрируют с получением 800 мг белого твердого продукта. Промывка диэтиловым эфиром дает 696 мг (60%) 4-амино-6- хлор-2-(1-(3,7-дихлорфуро[2,3с]пиридин-5-ил)этилтио пиримидина в виде белого твердого продукта (температура плавления 190-191oC).
ПРИМЕР 284. Получение 4-амино-6-хлор-2-(1-(3-бромфуро-[2, 3с] пиридин-5-ил)этил)тиопиримидина, температура плавления 175-176,5oC.
5-(1-Ацетоксиэтил)-фуро[2, 3с] пиридин (1,32 г, 6,4 ммоль) растворяют в 30 мл хлорметана в атмосфере азота в 100-мл одногорлой круглодонной колбе. На раствор наслаивают 50 мл насыщенного бикарбоната натрия и обрабатывают бромом (1,99 мл, 38,6 ммоль) весь вместе. Реакционную смесь осторожно перемешивают в течение 5 часов при комнатной температуре, и водный слой промывают 2 х 20 мл дихлорметана. Объединенные органические слои концентрируют в вакууме до янтарного масла. Масло распределяют между 1 х 50 мл насыщенного бикарбоната натрия и 4 x 25 мл дихлорметана. Органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 2,15 г (93%) 5-(1-ацетоксиэтил)-2,3-дибром-2,3-дигидрофуро[2, 3с] -пиридина в виде бледно-желтого масла.
5-(1-Ацетоксиэтил)-2,3-дибром-2,3-дигидрофуро[2,3с] пиридин (2,15 г, 5,9 ммоль) растворяют в 20 мл абсолютного этанола в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают карбонатом калия (4,9 г, 35,6 ммоль), и реакционную смесь энергично перемешивают в течение 18 часов. Смесь фильтруют, фильтрат концентрируют до желтого масла и содержащую карбонат калия, отфильтрованную лепешку распределяют между 1 х 50 мл воды и 4 х 25 мл дихлорметана. Органические слои объединяют с отфильтрованным остатком, сушат над карбонатом калия и концентрируют в вакууме до желтой пасты. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 40% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 24-51 объединяют и концентрируют с получением 1,04 г (всего 67%) 3-бром-5-(1-гидроксиэтил)фуро[2, 3с] пиридина в виде бледного желтовато-коричневого твердого продукта (температура плавления 108-110oC).
3-Бром-(1-гидроксиэтил)-фуро[2, 3с]пиридин (1,01 г, 4,2 ммоль) растворяют в 15 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (454 мкл, 6,2 ммоль) и реакционную смесь перемешивают в течение 20 минут при 0oC, а затем 1,5 часа при комнатной температуре. Реакционную смесь добавляют к 25 мл насыщенного бикарбоната натрия, водный слой промывают 3 х 25 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 1,05 г (97%) 3-бром-5-(1-хлорэтил)-фуро[2, 3с]пиридина в виде желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,95 (д, J=6,8 Гц, 3), 5,31 (кв, J=6,8, 13,7 Гц, 1), 6,68 (м, 1), 7,80 (с, 1), 8,83 (м, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,48 г, 5,7 ммоль) растворяют в 15 мл сухого диметилформамида в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (505 мг, 12,6 ммоль), и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1-Хлорэтил)-3-бромфуро[2, 3с]пиридин (856 мг, 4,0 ммоль) в 2 х 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 68 часов. Реакционную смесь разбавляют 125 мл этилацетата, промывают 4 х 50 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 40% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 14-23 объединяют и концентрируют с получением 978 мг не совсем белого твердого продукта. Промывка диэтиловым эфиром дает 880 мг (58%) 4-амино-6-хлор-2-(1-(3-бромфуро[2, 3с]пиридин-5-ил)- этилтио)-пиримидина в виде белого твердого продукта (температура плавления 175-176,5oC).
ПРИМЕР 285. Получение 4-амино-6-хлор-2-(1-(3-бром-7- хлорфуро[2, 3с] пиридин-5-ил)этил)тиопиримидина, температура плавления 181-182oC.
5-(1-Ацетоксиэтил)-7-хлорфуро[2, 3с] пиридин (1,4 г, 5,8 ммоль) растворяют в 35 мл дихлорметана в атмосфере азота в 200-мл одногорлой круглодонной колбе. На раствор наслаивают 75 мл насыщенного бикарбоната натрия и обрабатывают бромом (4,7 мл, 90,6 ммоль) весь вместе. Реакционную смесь осторожно перемешивают в течение 24 часов при комнатной температуре, обрабатывают твердым бикарбонатом натрия (3 г, 36 ммоль) и энергично перемешивают в течение 6 часов. Водный слой промывают 3 х 30 мл дихлорметана. Объединенные органические слои концентрируют в вакууме до янтарного масла. Масло распределяют между 1 х 50 мл насыщенного бикарбоната натрия и 4 х 25 мл дихлорметана. Органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 1,66 г (71%) 5-(1-ацетоксиэтил)-7-хлор-2,3- дибром-2,3-дигидрофуро[2, 3с]пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,60 (м, 3), 2,15 (м, 3), 5,67 (м, 1), 5,90 (м, 1), 6,94 (с, 1), 7,43 (м, 1) м.д.
5-(1-Ацетоксиэтил)-7-хлор-2,3-дибром-2,3-дигидрофуро-[2,3с] пиридин (1,66 г, 4,2 ммоль) растворяют в 20 мл 95% этанола в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор обрабатывают карбонатом калия (4,9 г, 35,6 ммоль) и реакционную смесь энергично перемешивают в течение 18 часов. Смесь фильтруют, фильтрат концентрируют до желтого масла и отфильтрованную лепешку, содержащую карбонат калия, распределяют между 1 х 50 мл воды и 4 х 25 мл дихлорметана. Органические слои объединяют с остатком фильтрата, сушат над карбонатом калия и концентрируют в вакууме до желтой пасты. Сырой продукт адсорбируют на 2 г силикагеля (230-400 меш), который хроматографируют на 50 г силикагеля (230-400 меш), элюируя 20% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 27-60 объединяют и концентрируют с получением 806 мг (70% всего) 3-бpoм-7-xлop-5-(1-гидpoкcиэтил)фуpo[2, 3c] -пиридина в виде белого твердого продукта (температура плавления 125-126oC).
3-Бpoм-(1-гидpoкcиэтил)фуpo[2, 3с]пиридин (430 мг, 1,6 ммоль) растворяют в 5 мл дихлорметана в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (169 мкл, 2,3 ммоль) и реакционную смесь перемешивают в течение 20 минут при ОoC, затем 3 часа при комнатной температуре. Реакционную смесь добавляют к 20 мл насыщенного бикарбоната натрия, и органический слой сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до бледного масла. Сырой продукт хроматографируют на 25 г силикагеля (230-400 меш), элюируя 20% этилацетат/гексаном,
собирая 5-мл-вые фракции. Фракции 6-12 объединяют и концентрируют с получением 406 мг (88%) 3-бром-7-хлор-5-(1- хлорэтил)фуро[2, 3с]пиридина в виде бесцветного масла, которое кристаллизуют при выстаивании (температура плавления 62-64oC).
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (437 мг, 1,7 ммоль) растворяют в 6 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (142 мг, 3,6 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1-Хлорэтил)-3-бром-7-хлорфуро[2, 3с] пиридин (385 мг, 1,3 ммоль) в 2 х 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 48 часов. Реакционную смесь разбавляют 75 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтой пасты. Сырой продукт хроматографируют на 40 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 26-39 объединяют и концентрируют с получением 347 мг не совсем белого твердого продукта. Промывка диэтиловым эфиром дает 267 мг (49%) 4-амино-6-хлор-2-(1-(3-бром-7-хлор-фуро [2, 3с]-пиридин-5-ил)-этилтио) пиримидина в виде белого твердого продукта (температура плавления 181-182oC).
ПРИМЕР 286. Получение 4-амино-6-хлор-2-(1-(7-хлор-3- метилфуро[2, 3с] пиридин-5-ил)этил)тиопиримидина, температура плавления 198-199,5oC.
7-Хлор-5-(1-гидроксиэтил)-3-метилфуро[2, 3с]пиридин (2,3 г, 10,9 ммоль) растворяют в 100 мл дихлорметана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (1,2 мл, 16,3 ммоль), и реакционную смесь перемешивают 20 минут при 0oC, затем 3 часа при комнатной температуре. Реакционную смесь добавляют к 85 мл насыщенного бикарбоната натрия, слои разделяют, водный слой промывают 3 х 25 мл дихлорметана, и объединенные органические слои сушат над карбонатом калия. Высушенные органические слои концентрируют в вакууме с получением 2,36 г (94%) 7-хлор-5-(1- хлорэтил)-3-метилфуро-[2, 3с]пиридина в виде бледно-желтого масла, которое кристаллизуют при выстаивании (температура плавления 49-51oC).
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (1,29 г, 5,0 ммоль) суспендируют в 20 мл сухого диметилформамида в атмосфере азота в 100-мл одногорлой круглодонной колбе. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (430 мг, 10,8 ммоль) и смесь перемешивают 1 час при комнатной температуре. 7-Хлор-5-(1-хлорэтил)-3-метилфуро [2, 3с] пиридин (920 мг, 4,0 ммоль) в 2 х 4 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают 48 часов. Реакционную смесь разбавляют 125 мл этилацетата, промывают 4 x 50 мл 50% насыщенного натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 25-36 объединяют и концентрируют с получением 1,04 г белого твердого продукта, который промывают 10 мл 20% диэтилового эфира/гексана с получением 1,02 г 4-амино-6-хлор-2-(1-(7-хлор-3-метилфуро- [2, 3с]пиридин-5-ил)этилтио)-пиримидина в виде белого твердого продукта (температура плавления 198-199,5oC).
ПРИМЕР 287. Получение 4-амино-6-трифторметил-2-(1-(7-хлор- 3,3-диметил-2,3-дигидрофуро[2, 3с] пиридин-5-ил)этил) тиопиримидина, температура плавления 170-172oC.
Мезилатную соль 4-амино-2-меркапто-6-трифторметилпиримидина (742 мг, 2,5 ммоль) растворяют в 8 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (210 мг, 5,3 ммоль) и смесь перемешивают в течение 1 часа при комнатной температуре. 7-Хлор-5-(1-хлорэтил)-2,3-дигидро-3,3-диметилфуро [2, 3с]пиридин (569 мг, 2,3 ммоль) в 2 х 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 24 часов. Реакционную смесь разбавляют 75 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 13-30 объединяют и концентрируют с получением белой пены. Кристаллизация из гексана/диэтилового эфира дает 786 мг (84%) 4-амино-2-(1-(7- хлор-2,3-дигидро-3,3-диметилфуро[2, 3с] пиридин-5-ил)этилтио)- 6-трифторметилпиримидина в виде не совсем белого твердого продукта (температура плавления 170-172oC).
ПРИМЕР 288. По общему способу примера 277 и включая несущественные изменения, но используя соответствующий амин, получают следующий соединения:
Соед. N 288 6-метиламино-2-(2-нафтилметил)-тио-4-пиримидин карбонитрил, т.пл. 169-171oC.
Когда R12 и R13 являются различными, соединения формулы I (так же, как IA и IB) извлекаются как рацемическая смесь и включают R и S изомеры, которые могут быть выделены из рацемической смеси путем ВЭЖХ, используя колонку с хиральной фазой, такую как Chiralcel OD-H, элюирование соответствующей смесью растворителей, такой как изопропанол/гексан (смотри, например, процедуру A). R и S изомеры формулы I (когда R12 и R13 являются различными) могут быть получены из соответствующего хирального галогенида (или мезилата) II (смотри схему I). Соответствующий хиральный галогенид (или мезилат) II получают из хирального спирта IV. Соответствующий хиральный спирт IV может быть получен из соответствующего кетона V, используя хиральный восстанавливающий агент, такой как (+) или (-)-диизопинокамфеилхлорборан или другой хиральный восстанавливающий агент, известный специалисту в данной области. Соответствующий хиральный спирт IV также получают при разделении рацемического спирта IV путем ферментативного гидролиза соответствующего рацемического ацетата VI соответствующим ферментом, таким как аминолипаза PS-30 или L1754 тип VII из candidae cylindracea или других ферментов, известных специалистам в данной области. Соответствующий хиральный спирт IV также получают при разделении рацемического спирта IV путем ферментативной этерификации (такой как ацетилирование или бутилирование) рацемического спирта, используя соответствующий фермент, такой как липаза из поджелудочной железы свиньи, тип II, или другие ферменты, известные специалистам в данной области.
ПРИМЕРЫ 289 и 290. (R)-(+)-4-Амино-6-хлор-2-(1-(3-метилфуро- [2, 3с]пиридин-5-ил)этил)тиопиримидин (Соед. N 289) и (S)-(-)-4-Амино-6-хлор-2-(1-(3-метилфуро[2, 3с]пиридин-5-ил)этил) -тиопиримидин (Соед. N 290)
Способ A: Соед. N 246 разделяют на (+) и (-) энантиомеры, используя ВЭЖХ колонку с хиральной фазой, Chiralcel OD-H, элюируя 20% изопропанол/гексаном, со скоростью потока 0,5 мл/мин. Соед.N 289 [α]D= +278° (с 0,91, хлороформ); Соед. N 290 [α]D= -276° (с 0,91, хлороформ).
Способ B:
Часть 1:
Раствор рацемического 5-(1-гидроксиэтил)-3-метил-фурано [2, 3с]пиридина (15,3 г, 0,0864 моль) в 200 мл эфира при комнатной температуре обрабатывают 2,2,2-трифторэтилбутиратом (58,8 г, 0,3458 моль, 4,0 эквив.) и PPL (липаза из поджелудочной железы свиньи, тип II, Sigma Chemical Co., 22,3 г) и перемешивают в течение 7 дней в закупоренной колбе. Содержимое разбавляют 150 мл эфира плюс 10 г целита, фильтруют через пад из целита (50 г) и тщательно промывают пад эфиром. Фильтрат концентрируют при пониженном давлении и откачивают в течение ночи при высоком вакууме. Хроматография на 400 г силикагеля с набивкой и элюированием смесью ацетон-метиленхлорид (1:6), (1:5) и, в заключение, (1:4), дают 10,8 г (50,6%) (R)-(+)-5-(1- бутирилоксиэтил)-3-метил-фурано[2, 3с]-пиридина (вращение: [α]D= +76,5° (с=1,50, CHCl3)); 99,9% ст. чистоты);
1H-ЯМР (CDCl3, ТМС): δ 8,78 (с, 1H), 7,50 (с, 2 H), 6,04 (кв, 1H, 6,62 Гц), 2,35 (т, 2H, J=7,45 Гц), 2,23 (с, 3H), 1,72-1,57 (м, 2H), 1,64 (д, 3H, J= 4,65 Гц), 0,92 (т, 3H, J=7,42 Гц) м.д.) и 7,51 г (49,1%) (3)-(-)-5-(1-гидроксиэтил)-3-метилфурано[2, 3с] пиридина (вращение: [α]D= -38,6° (с = 0,725, CHCl3)); 99% ст. чистоты;
1H-ЯМР (CDCl3, ТМС): δ 8,69 (с, 1H), 7,51 (с, 1H),7,46 (с, 1H), 5,00 (кв, 1H, J=6,46 Гц), 2,23 (с, 3H), 1,55 (д, 3H, J=6,49 Гц) м.д.
Часть 2: (R)-(+)-5-(1-Бутирилоксиэтил)-3-метилфурано-[2, 3с] пиридин (1,75 г, 7,085 ммоль) в 100 мл метанола, охлажденного до 0-5oC, обрабатывают K2CO3 (1,955 г, 14,17 ммоль, 2,0 эквив.) в 25 мл воды. Охлаждающую баню удаляют через 30 мин и реакционную смесь оставляют перемешиваться при температуре окружающей среды в течение 4 часов. Добавление 120 мл размельченного льда сопровождается последующим подкислением с помощью 2н NaHSO4 (14,17 мл, 28,34 ммоль) до pH 5. Содержимое выливают в 125 мл насыщенного NaHCO3, экстрагируют три раза этилацетом, объединенные органические экстракты сушат с безводным Na2SO4 и концентрируют в вакууме. Хроматография, используя 50 г силикагеля с набивкой и элюированием смесью ацетон-метиленхлорид (1:6), дает 1,12 г (89%) (R)-(+)-5-(1-гидроксиэтил)-3- метилфурано[2, 3с]пиридина в виде белого твердого продукта (вращение: [α]D= +42,4° (с=0,870, CHCl3));
1H-ЯМР (CDCl3, ТМС): δ 8,66 (с, 1H), 7,47 (с, 1H), 7,40 (с, 1H), 4,95 (кв, 1H, J= 6,45 Гц), 3,77 (ушир.с, 1H), 2,19 (с, 3H), 1,50 (д, 3H, J=6,43 Гц) м.д.).
Раствор (R)-(+)-5-(1-гидроксиэтил)-3-метилфурано[2, 3с] -пиридина (0,100 г, 0,565 ммоль) в 2 мл сухого тетрагидрофурана обрабатывают трифенилфосфином (0,148 г, 0,565 ммоль, 1,0 эквив.), бензойной кислотой (0,069 г, 0,565 ммоль, 1,0 эквив.). Добавляют по каплям диэтилазодикарбоксилат (0,098 г, 0,656 ммоль, 1,0 эквив. ) в течение 30-секундного периода. После перемешивания в течение 2 часов при комнатной температуре добавляют еще по 20% каждого реагента. Еще через 30 минут содержимое концентрируют при пониженном давлении, растворяют в этилацетате, обрабатывают 600 мг силикагеля и повторно концентрируют в вакууме. Свободно пересыпающийся порошок вводят в колонку с силикагелем с набивкой и элюированием смесью этилацетат-гексан (1:9) с получением 136 мг (85%) (S)-(+)-5-(1-бензоилоксиэтил)-3-метилфурано[2, 3с]пиридина (вращение: [α]D= +56,8° (с = 1,05, CHCl3);
1H-ЯМР (CDCl3, ТМС): δ 8,79 (с, 1H), 8,13 (с, 1H), 8,11 (с, 1H), 7,63-7,38 (м, 5H), 6,30 (кв, 1H, J=6,59 Гц), 2,22 (с, 3H), 1,78 (д, 3H, J=6,58 Гц) м.д.
Раствор (S)-(+)-5-(1-бензоилоксиэтил)-3-метилфурано-[2, 3с] пиридина (0,134 г, 0,477 ммоль) в 9 мл метанола при 0-5oC обрабатывают K2CO3 (0,132 г, 0,954 ммоль, 2,0 эквив.) в 2,2 мл воды. Через 5 минут охлаждающую баню удаляют, и реакционную смесь перемешивают в течение 4 часов. Содержимое охлаждают на ледяной бане, обрабатывают 2н NaHSO4 (0,954 мл, 1,91 ммоль), выливают в 20 мл насыщенного NaHCO3, экстрагируют дважды этилацетатом, и объединенные органические экстракты сушат с безводным Na2SO4, фильтрат концентрируют в вакууме и хроматографируют на 10 г силикагеля с набивкой и элюированием смесью ацетон-метиленхлорид (1: 6) с получением 83 мг (99%) (S)-(-)-5-(1-гидроксиэтил)-3-метил-фурано[2,3с] - пиридина (вращение: [α]D= -40,6° (с = 0,675, CHCl3)).
Часть 3: Оксалилхлорид (1,01 мл, 11,5 ммоль) растворяют в 40 мл сухого дихлорметана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до -60oC, обрабатывают по каплям диметилсульфоксидом (1,63 мл, 23 ммоль) в 1 х 5 мл дихлорметана и перемешивают в течение 20 мин. Смесь обрабатывают 7-хлор-2,3-дигидро-5-(1-гидроксиэтил)-3-метил-фурано[2,3с] пиридином (2,14 г, 10 ммоль) в 1 х 5 мл дихлорметана, и реакционную смесь перемешивают в течение 20 минут при -60oC. Реакционную смесь обрабатывают по каплям триэтиламином (7,0 мл, 50 ммоль), перемешивают в течение 20 минут при -60oC, затем 1 час при комнатной температуре. Смесь разбавляют 125 мл этилацетата, промывают 2 х 50 мл 1:1 5% соляной кислотой/насыщенным хлоридом натрия, и органические слои сушат над безводным сульфатом магния. Органические слои концентрируют в вакууме до темно-желтого масла. Сырой продукт хроматографируют на 75 г силикагеля (280-400 меш), элюируя 12% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 41-72 объединяют и концентрируют с получением 1,80 г (85%) 5-ацетил-7-хлор-2,3-дигидро-3-метилфурано [2, 3с]пиридина в виде белого твердого продукта.
1H- ЯМР (CDCl3, ТМС): δ 1,38 (д, J=7 Гц, 3), 2,65 (с, 3), 3,70 (м, 10), 4,31 (дд, J=7,5, 9 Гц, 1), 4,91 (т, J=9,2 Гц, 1), 7,88 (с, 1) м.д.
5-Ацетил-7-хлор-2,3-дигидро-3-метилфурано[2, 3с]пиридин (1,8 г, 8,5 ммоль) растворяют в 15 мл сухого тетрагидрофурана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до -30oC, и полученную суспензию обрабатывают медленно по каплям (-)диизопинокамфеилборанхлоридом (5,9 г, 18,3 ммоль) в 1 х 16 мл сухого тетрагидрофурана. Реакционную смесь размещают на бане изо льда/ацетона (-18oC) и оставляют перемешиваться в течение ночи до тех пор, пока охлаждающая баня не нагреется до комнатной температуры и ацетон не испарится. Реакционную смесь повторно охлаждают до -18oC, обрабатывают по каплям раствором, содержащим 15 мл насыщенного бикарбоната натрия и 4,5 мл 30% перекиси водорода, и смесь перемешивают в течение 1 часа при комнатной температуре. Смесь разбавляют 120 мл этилацетата, слои разделяют, и органический слой промывают 2 х 50 мл насыщенного бикарбоната натрия, 1 х 50 мл воды и 1 х 50 мл насыщенного хлорида натрия. Органические слои сушат над безводным карбонатом калия/безводным сульфатом магния 1:1 и концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 125 г силикагеля (230-400 меш), элюируя 1 л 20% этилацетат/гексана, затем 1 л 33% этилацетат/гексана, собирая 22-мл-вые фракции. Фракции 47-77 объединяют и концентрируют с получением 1,73 г (95%) (3)-7-хлор- 2,3-дигидро-5-(1-гидроксиэтил)-3-метилфурано [2, 3с] пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,36 (м, 3), 1,47 (д, J=6,4 Гц, 3), 2,86 (ушир.с, 1), 3,65 (м, 1), 4,22 (т, J=8,0 Гц, 1), 4,82 (м, 2), 7,09 (м, 1) м.д.
7-Хлор-2, 3-дигидро-5- (I- (S)-гидроксиэтил)-3-метилфурано-[2, 3с]пиридин (1,61 г, 7,5 ммоль) растворяют в 25 мл абсолютного этанола, содержащего 20% гидроксида палладия на угле (400 мг), в 250-мл сосуде PARR со встряхиванием. Реакционную смесь гидрогенируют при 25 фунт/кв. дюйм (1785 г/кв. см) в течение 4 часов, фильтруют через целит, и отфильтрованную лепешку тщательно промывают абсолютным этанолом. Фильтрат концентрируют в вакууме до бледной пасты, которую распределяют между 1 х 50 мл насыщенного бикарбоната натрия и 4 х 20 мл дихлорметана. Объединенные органические слои сушат над безводным карбонатом калия и концентрируют в вакууме с получением 1,24 г (92%) (S)-2,3-дигидро-5-(1-гидроксиэтил)-3-метилфурано [2, 3с] пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,31 (м, 3), 1,44 (д, J=6,4 Гц, 3), 3,54 (м, 1), 4,09 (т, J=8,4 Гц, 1), 4,28 (ушир.с, 1), 4,70 (т, J=8,8 Гц, 1), 4,81 (кв, J= 6,3, 12,8 Гц, 1), 7,11 (с, 1), 7,97 (с, 1) м.д.
(S)-2,3-Дигидро-5-(1-гидроксиэтил)-3-метилфурано[2, 3c] -пиридин (1,2 г, 6,7 ммоль) растворяют в 7 мл пиридина в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор обрабатывают уксусным ангидридом (1,4 мл, 14,7 ммоль) и перемешивают в течение ночи при комнатной температуре. Летучие продукты удаляют в потоке азота, и остаток распределяют между 1 х 40 мл этилацетата и 1 х 40 мл насыщенного бикарбоната натрия. Органические слои сушат над безводным сульфатом магния и концентрируют в вакууме с получением 1,43 г (96%) (3)-5-(1-ацетоксиэтил)-2,3-дигидро-3-метилфурано [2, 3с] пиридина в виде бледного масла. 1H-ЯМР (CDCl3, ТМС): δ 1,35 (м, 3), 1,56 (м, 3), 2,08 (м, 3), 3,54 (м, 1), 4,12 (т, J=8,2 Гц, 1), 4,73 (т, J=9 Гц, 1), 5,88 (кв, J=6,6, 13,2 Гц, 1), 7,16 (м, 1), 8,10 (с, 1) м.д.
(S)-2,3-Дигилро-5-(1-ацетоксиэтил)-3-метилфурано [2,3c] -пиридин (1,4 г, 6,3 ммоль) объединяют с 2,3,4,5-тетрахлорбензохиноном (1,7 г, 6,8 ммоль) в 25 мл диоксана в атмосфере азота в 100-мл одногорлой круглодонной колбе. Реакционную смесь нагревают с обратным холодильником в течение 28 часов, охлаждают до комнатной температуры, и объем диоксана удаляют в вакууме. Гидрохинон удаляют путем фильтрования, и отфильтрованную лепешку промывают 1:1 этилацетат/диэтиловым эфиром, и фильтрат концентрируют до коричневого масла. Сырой продукт растворяют в 25 мл метанола в 100-мл одногорлой круглодонной колбе, и раствор обрабатывают 2н гидроксидом натрия (10 мл, 20 ммоль). Смесь перемешивают 1 час при комнатной температуре, метанол удаляют в вакууме, и остаток распределяют между 1 х 50 мл насыщенного бикарбоната натрия и 4 х 20 мл дихлорметана. Органические слои сушат над безводным карбонатом калия и концентрируют в вакууме до желтовато-коричневого твердого продукта. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 32% этилацетат/гексаном, затем 40% этилацетат/гексаном, собирая 125-мл-вые фракции. Фракции 6-12 объединяют и концентрируют с получением 1,01 г (90%) (S)-5-(1-гидроксиэтил)-3- метилфурано[2, 3с] -пиридина в виде белого твердого продукта. Аликвоту преобразуют в соответствующий ацетат, который имеет 92% ст. чистоты согласно ВЭЖХ с хиральной фазой.
1H-ЯМР (CDCl3, ТМС): δ 1,57 (д, J=6,5 Гц, 3), 2,26 (д, J=1,3 Гц, 3), 4,04 (ушир. с, 1), 5,05 (кв, J=6,5, 13 Гц, 1), 7,50 (с, 1), 5,58 (д, J=l,2 Гц, 1), 8,74 (д, J=0,6 Гц, 1) м.д.
Часть 4: Раствор (3)-(-)-5-(1-гидроксиэтил)-3-метилфурано [2, 3с]пиридина (0,0691 г, 0,390 ммоль; Способ B, Часть 1) в четыреххлористом углероде (0,601 г, 3,90 ммоль, 10 эквив.) при 0-5oC обрабатывают хлорформом (0,150 мл) и трифенилфосфином (0,205 г, 0,781 ммоль, 2,0 эквив.), и реакционную смесь перемешивают в течение 20 мин. Охлаждающую баню удаляют и реакционную смесь перемешивают при комнатной температуре в течение ночи. Содержимое выливают в 25 мл воды, экстрагируют два раза смесью этилацетат-гексан (1:1), объединенные органические экстракты сушат с безводным Na2S04 и концентрируют при пониженном давлении. Перетирание остатка четыре раза со смесью этилацетат-гексан (1:6), затем хроматографирование на 15 г силикагеля с набивкой и элюированием смесью ацетон-метиленхлорид-гексан (0,5:2:7,5) дает 57,4 мг (75%) (R)-(+)-5-(1-хлорэтил)-3-метилфурано[2, 3с]пиридина (оптическое вращение: [α]D= +68,4° (с = 1,53, CHCl3)).
Перемешиваемую с помощью магнитной мешалки суспензию гидрида натрия (1,25 г, 0,0522 моль, 2,10 эквив., 60% масляная дисперсия) в 80 мл диметилформамида при 16oC обрабатывают мезилатной солью 4-амино-6-хлор-2-меркаптопиримидина (6,71 г, 0,0261 моль, 1,05 эквив.), и реакционную смесь перемешивают в течение 15 мин. Охлаждающую баню удаляют и содержимое перемешивают при температуре окружающей среды в течение 1,5 часа. Добавляют за один раз (R)-(+)-5-(1-хлорэтил)-3-метилфурано[2, 3с]пиридина (4,86 г, 0,0249 моль, 1,0 эквив.) в 15 мл диметилформамида с прополаскиванием 10 мл и 2 мл того же растворителя. Реакционной смеси дают перемешиваться при комнатной температуре в течение 5 дней. Содержимое выливают в ледяную воду, экстрагируют два раза эфиром, объединенные органические экстракты сушат с безводным Na2SO4 и концентрируют при пониженном давлении. Хроматография на 350 г силикагеля с набивкой и элюированием смесью этилацетат-гексан (2:3), затем (1: 1), дает 6,55 г (82%) (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфурано [2, 3с] пиридин-5-ил)-этилтио)-пиримидина. Фильтрат, полученный после двух кристаллизаций из смеси метил-трет-бутиловый эфир - метиленхлорид - этилацетат концентрируют в вакууме с получением 4,83 г (61%) (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфурано[2, 3с] пиридин-5-ил)этилтио)-пиримидина (температура плавления 156-157oC; оптическое вращение [α]D= -270,3° (с = 0,620, CHCl3)).
Соед. N 291 R-(+)- 4-Амино-6-хлор-2-(1-(4-этил-2-пиридил) этил)-тиопиримидин
Соед. N 292 (-)-4-Амино-6-хлор-2-(1-(4-этил-2-пирилил)этил) -тиопиримидин
Процедура A: Соед. N 216 разделяют на (+) и (-) энантиомеры, используя ВЭЖХ колонку с хиральной фазой, Chiralcel OD-Н, элюируя 20% изопропанол/гексан + 0,05% уксусная кислота, со скоростью потока 0,5 мл/минута. [α]D= +276,4° (с 1,21, хлороформ); [α]D= -288,6° (с 1,28, хлороформ).
Процедура B: Раствор рацемического 2-(1-гидроксиэтил)- 4-этилпиридина (1,0 г, 6,62 ммоль) в 10 мл эфира при комнатной температуре обрабатывают 2,2,2-трифторэтилбутиратом (1,0 мл, 6,62 ммоль) и 1,0 г липазы из поджелудочной железы свиньи, тип II, и перемешивают в атмосфере азота в течение 3 дней. К смеси добавляют целит и через 15 мин реакционную смесь фильтруют через целит, промывают эфиром и концентрируют с получением 1,38 г продукта. Продукт хроматографируют на 70 г силикагеля, элюируя смесью ацетон/метиленхлорид (1: 9) с получением 0,456 г (+)-1-(4-этилпиридин-2-ил)этилбутирата, [α]D= +84,0° (c 1,325, хлороформ) (99% ст. чистоты).
Раствор (+)-1-(4-этилпиридин-2-ил)этилбутирата (0,059 г, 0,27 ммоль) в 6 мл метанола обрабатывают 0,0737 г (0,534 ммоль) карбоната калия в 2 мл воды при 0oC. Через 30 минут смесь перемешивают при комнатной температуре в течение 2 часов. К смеси добавляют 57 мг хлорида аммония в 4 мл воды вместе с количеством 2н гидросульфата калия, достаточным для доведения pH раствора до 7, смесь экстрагируют дважды этилацетатом после того как выльют ее в 20 мл насыщенного солевого раствора и 10 мл воды. Объединенные органические слои сушат над сульфатом натрия и концентрируют. Продукт хроматографируют на 10 г силикагеля, элюируя (1: 5) ацетон/метиленхлорид с получением 30,5 мг (76%) R-(+)-2-(1-гидроксиэтил)-4-этилпиридина, [a]D=+33,0o (с 1,525, хлороформ).
Преобразование R-(+)-2-(1-гидроксиэтил)-4-этилпиридин в Соед. N 291 ( [α]D= +273,7°) выполняют так, как описано для Соед. N 216.
ПРИМЕР 293. 4-Амино-6-хлор-2-(1-(7-хлор-3-трифторметил)- фуро[2, 3с]пиридин-5-ил)этилтио)пиримидин (Соед. N 293).
2-Хлор-3-гидрокси-6-(1-гидроксиэтил)пиридин (7,19 г, 41,4 ммоль) растворяют в 80 мл воды, содержащей карбонат калия (17,2 г, 124 ммоль) в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают йодом (31,5 г, 124 ммоль) и перемешивают в течение 6 часов при комнатной температуре. Смесь гасят насыщенным трифторсульфатом натрия, и устанавливают pH 2 с помощью 12н соляной кислоты. Осадок собирают, промывают водой и сушат. Желтый твердый продукт далее промывают диэтиловым эфиром с получением 4,68 г (38%) 6-ацетил-2-хлор-3-гидрокси-4-йодпиридина в виде бледного желтовато-коричневого твердого продукта (температура плавления 223-224oC).
6-Ацетил-2-хлор-3-гидрокси-4-йодпиридин (6,12 г, 20,6 ммоль) объединяют с триметилсилилацетиленом (3,5 мл, 24,7 ммоль), бис(трифенилфосфин)палладийдихлоридом (730 мг, 10 ммоль) и йодидом меди (99 мг, 0,52 ммоль) в 37 мл смеси 2:1 хлороформ/тетрагидрофуран в атмосфере азота в 100-мл одногорлой круглодонной колбе. Суспензию обрабатывают триэтиламином (6 мл, 43 ммоль) и реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Смесь л разбавляют 150 мл этилацетата и промывают 2 х 50 мл 5% соляной кислотой. Органические слои сушат над безводным сульфатом магния, обрабатывают 10 г силикагеля (230-400 меш) и концентрируют досуха. Слой хроматографируют на 200 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном + 0,1% уксусной кислотой, собирая 50-мл-вые фракции. Фракции 10-18 объединяют и концентрируют с получением 4,88 г (88%) 6-ацетил-2-хлор-3-гидрокси-4-(2-триметилсилилэтинил)пиридина в виде бледного желтовато-коричневого твердого продукта.
1H ЯМР (d6ДМСО): δ 0,26 (с, 9), 2,51 (с, 3), 7,78 (с, 1) м.д.
6-Ацетил-2-хлор-3-гидрокси-(2-триметилсилилэтинил)- пиридин (4,8 г, 18,2 ммоль) растворяют в 50 мл сухого тетрагидрофурана в атмосфере азота в 100-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают трифторацетатом ртути (8,54 г, 20,0 ммоль), и перемешивают в течение 2 часов при комнатной температуре. Реакционную смесь разбавляют 40 мл насыщенного хлорида натрия, и смесь перемешивают в течение 1 часа при комнатной температуре. Устанавливают pH 8 с помощью 2н гидроксида натрия и смесь разбавляют 150 мл этилацетата. Водный слой промывают 50 мл этилацетата. Объединенные органические слои сушат над безводным сульфатом магния и концентрируют в вакууме до желтого твердого продукта. Сырой продукт растворяют в ацетоне и адсорбируют на 20 г силикагеля (230-400 меш) путем концентрации досуха. Слой хроматографируют на 200 г силикагеля (230-400 меш), элюируя 2 л 30% этилацетат/гексана, затем 2 л 50% этилацетат/гексана, собирая 50-мл-вые фракции. Фракции 8-48 объединяют и концентрируют с получением желтого твердого продукта, который промывают 100 мл 25% диэтилового эфира/гексана с получением 8,47 г (93%) 5-ацетил-7- хлор-3-хлорртуть-2-триметилсилилфуро [2,3с] пиридина в виде не совсем белого твердого продукта.
1H-ЯМР (d6ДМСО): δ 0,42 (с, 9), 2,65 (с, 3), 8,80 (с, 1) м.д.
5-Ацетил-7-хлор-3-хлорртуть-2-триметилсилилфуро[2, 3с]- пиридин (7,0 г, 14 ммоль) суспендируют в 190 мл смеси 1:1 вода/ацетонитрил в атмосфере азота в 500-мл одногорлой круглодонной колбе. Суспензию обрабатывают по каплям 60 мл воды, содержащей йодид калия (5,1 г, 30,8 ммоль) и йод (3,91 г, 15,4 ммоль), и реакционную смесь перемешивают в течение 2 часов при комнатной температуре. Смесь разбавляют 95 мл воды и охлаждают до -15oC в течение 1 часа. Осадок собирают, промывают водой и сушат в вакууме с получением 5,38 г (98%) 5-ацетил-7-хлор-3-йод-2-триметилсилилфуро[2, 3с]пиридина в виде желтовато-коричневого твердого продукта (температура плавления 92-93oC).
5-Ацетил-7-хлор-3-йод-2-триметилсилилфуро[2, 3с] пиридин (1,51 г, 3,8 ммоль) растворяют в 15 мл метанола в атмосфере азота в 100-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC (суспензия), обрабатывают боргидридом натрия (135 мг, 3,6 ммоль) и перемешивают в течение 20 мин при 0oC, затем 30 мин при комнатной температуре. Смесь разбавляют 15 мл метанола, затем 15 мл насыщенного бикарбоната натрия, и суспензию перемешивают в течение 3 часов при комнатной температуре. Метанол удаляют в вакууме, оставшуюся суспензию разбавляют 15 мл воды, и осадок собирают. Отфильтрованную лепешку промывают водой и сушат с получением 1,16 г (92%) 7-хлор-5-(1-гидроксиэтил)-3-йод-фуро [2, 3с] пиридина в виде бледно-серого твердого продукта.
1H-ЯМР (CDCl3, ТМС): δ 1,58 (д, J=6,6 Гц, 3), 5,01 (кв, J=6,6, 13,2 Гц, 1), 7,38 (с, 1), 7,84 (с, 1) м.д.
7-Хлор-3-йод-5-(1-гидроксиэтил)-фуро[2, 3с] пиридин (4,2 г, 13 ммоль) растворяют в 20 мл пиридина в атмосфере азота в 2 00-мл, одногорлой круглодонной колбе. Раствор обрабатывают с уксусным ангидридом (7 мл, 62 ммоль) и реакционную смесь перемешивают 4 часа при комнатной температуре. Летучие продукты удаляют в вакууме (толуол, 100 мл, азеотроп.), и остаток распределяют между 1 х 100 мл насыщенного бикарбоната натрия и 3 х 40 мл этилацетата. Объединенные органические слои сушат над безводным карбонатом калия/сульфатом магния с получением 4,74 г (колич.) 5-(1-ацетоксиэтил)-7-хлор-3- йод-фуро[2, 3с]пиридина в виде не совсем белого твердого продукта (температура плавления 102-104oC).
5-(1-Ацетоксиэтил)-7-хлор-3-йодфуро[2, 3с] пиридин (4,37 г, 12 ммоль) объединяют с йодидом меди (3,41 г, 18 ммоль), высушенным распылением фторидом калия (834 мг, 14,4 ммоль) и триэтилсилилтрифторметаном (2,65 мл, 14,4 ммоль) в 35 мл диметилформамида в атмосфере азота в трубке с завинчивающейся крышкой. Реакционную смесь нагревают до 85oC в течение 5,5 часов, охлаждают и разбавляют 500 мл этилацетата. Смесь промывают 3 х 200 мл 50% насыщенного хлорида натрия, 1 х 100 мл 50% насыщенного динатрий EDTA и 1 х 100 мл насыщенного хлорида натрия. Органические слои сушат над безводным карбонатом калия и концентрируют в вакууме до темного масла. Сырой продукт хроматографируют на 300 г силикагеля (230-400 меш), элюируя 10% этилацетат/гексаном, собирая 50-мл-вые фракции. Фракции 17-23 объединяют и концентрируют с получением 1,7 г (46%) 5-(1-ацетоксиэтил)-7-хлор-3-трифторметилфуро[2, 3с]пиридина в виде не совсем белого твердого продукта (температура плавления 98-99oC).
5-(1-Ацетоксиэтил)-7-хлор-3-трифторметилфуро[2, 3с]-пиридин (1,21 г, 3,9 ммоль) растворяют в 40 мл дихлорметана в атмосфере азота в 250-мл трехгорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до -78oC, обрабатывают по каплям с диизобутилалюминий гидридом (9,8 мл, 9,8 ммоль), и реакционную смесь перемешивают в течение 1 часа при -78oC. Смесь осторожно гасят 60 мл 0,5 М натрий калий тартратом при -78oC и энергично перемешивают при комнатной температуре в течение 2 часов. Слои разделяют, и водный слой экстрагируют 3 x 20 мл дихлорметана. Объединенные органические слои сушат над безводным карбонатом калия и концентрируют в вакууме с получением 1,04 г белого твердого продукта. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя смесью 20% этилацетат/гексан, собирая 9-мл-вые фракции. Фракции 20-32 объединяют и концентрируют с получением 1,0 г (96%) 7-хлор-5-(1-гидроксиэтил)-3-трифторметилфуро [2, 3с]- пиридина в виде белого твердого продукта (температура плавления 90-91oC).
7-хлор-5-(1-гидроксиэтил)-3-трифторметилфуро[2,3с]- пиридин (282 мг, 1,1 ммоль) растворяют в 5 мл дихлорметана в атмосфере азота в 25-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (116 мкл, 1,6 ммоль), и реакционную смесь перемешивают в течение 20 мин при 0oC, затем 2 часа при комнатной температуре. Реакционную смесь добавляют к 10 мл насыщенного бикарбоната натрия, и водный слой промывают 3 х 10 мл дихлорметана. Объединенные органические слои сушат над безводным карбонатом калия и концентрируют в вакууме с получением 280 мг (93%) 7-хлор-5-(1-хлорэтил)-3- трифторметилфуро[2, 3с]пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,93 (д, J=6,6 Гц, 3), 5,23 (кв, J=6,5, 13 Гц, 1), 7,77 (с, 1), 8,17 (м, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (300 мг, 1,1 ммоль) растворяют в 4 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (102 мг, 2,6 ммоль), и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1-Хлорэтил)-7-хлор-3- трифторметилфуро [2,3с] пиридин (300 мг, 1,1 ммоль) в 2 х 1 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 24 часов. Реакционную смесь разбавляют 70 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтой пасты. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 20% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 21-36 объединяют и концентрируют с получением 299 мг не совсем белого твердого продукта. Промывка 10% диэтиловым эфиром/гексаном дает 284 мг (66%) 4-амино-6-хлор-2-(1-(7-хлор-3- трифторметил)фуро[2, 3с]пиридин-5-ил)этилтио)-пиримидина в виде белого твердого продукта (температура плавления 169-170oC).
ПРИМЕР 294. 4-Амино-6-хлор-2-(1-(3-трифторметил)-фуро-[2, 3с] пиридин-5-ил)этилтио)-пиримидин (Соед. N 294)
7-Хлор-5-(1-гидроксиэтил)-3-трифторметилфуро[2, 3с]-пиридин (647 мг, 2,4 ммоль) объединяют с 20% гидроксидом палладия на угле (647 мг) в 20 мл абсолютного этанола в 100-мл одногорлой круглодонной колбе. Суспензию обрабатывают 1,4-циклогексадиеном (2,3 мл, 24,4 ммоль) и нагревают с обратным холодильником в течение 4 часов. Смесь фильтруют через целит, и лепешку промывают этанолом. Фильтрат концентрируют в вакууме до оранжевой пасты. Сырой продукт распределяют между 1 х 25 мл насыщенного бикарбоната натрия и 4 х 20 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме до бледно- янтарного масла. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 8-11 объединяют и концентрируют с получением 188 мг (29%) извлеченного 7-хлор-5-(1-гидроксиэтил)- 3-трифторметилфуро[2, 3с] пиридина в виде белого твердого продукта. Фракции 17-28 объединяют и концентрируют с получением 339 мг (60%) 5-(1-гидроксиэтил-)-3-трифторметилфуро [2,3с] пиридина в виде белого твердого продукта (температура плавления 88-90oC).
5-(1-Гидроксиэтил)-3-трифторметилфуро[2, 3с]пиридин (324 мг, 1,4 ммоль) растворяют в 10 мл дихлорметана в атмосфере азота в 50-мл одногорлой круглодонной колбе. Раствор охлаждают до 0oC, обрабатывают тионилхлоридом (153 мкл, 2,1 ммоль), и реакционную смесь перемешивают в течение 20 мин при 0oC, затем 2 часа при комнатной температуре. Реакционную смесь добавляют к 20 мл насыщенного бикарбоната натрия, и водный слой промывают 3 х 10 мл дихлорметана. Объединенные органические слои сушат над безводным карбонатом калия и концентрируют в вакууме с получением 327 мг (94%) 5-(1-хлорэтил)-3-трифторметилфуро[2, 3с]пиридина в виде бледно-желтого масла.
1H-ЯМР (CDCl3, ТМС): δ 1,95 (д, J=6,5 Гц, 3), 5,30 (кв, J=6,5, 13 Гц, 1), 7,81 (с, 1), 8,13 (м, 1), 8,93 (м, 1) м.д.
Мезилатную соль 4-амино-6-хлор-2-меркаптопиримидина (346 мг, 1,3 ммоль) растворяют в 4 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Раствор охлаждают до 0oC, обрабатывают гидридом натрия (118 мг, 2,9 ммоль), и смесь перемешивают в течение 1 часа при комнатной температуре. 5-(1-Хлорэтил)-3- трифторметилфуро[2, 3с]пиридин (305 мг, 1,2 ммоль) в 2 х 1 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают в течение 72 часов. Реакционную смесь разбавляют 70 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 30 г силикагеля (230-400 меш), элюируя 30% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 22-42 объединяют и концентрируют с получением 325 мг желтой пены. Кристаллизация из 10% диэтилового эфира/гексана дает 253 мг (56%) 4-амино-6-хлор-2-(1-(3-трифторметил)-фуро[2, 3с] пиридин-5- ил)этилтио)-пиримидина в виде не совсем белого твердого продукта (температура плавления 91-93oC).
ПРИМЕР 295. 4-Амино-2-(1-(7-хлор-3-метилфуро[2,3с] - пиридин-5-ил)этилтио)-6-трифторметилпиримидин (Соед. N 295)
Мезилатную соль 4-амино-2-меркапто-6-трифторметилпиримидина (1,12 г, 3,85 ммоль) суспендируют в 12 мл сухого диметилформамида в атмосфере азота в 100 мл одногорлой круглодонной колбе, высушенной в печи. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (331 мг, 8,3 ммоль), и смесь перемешивают 1 час при комнатной температуре. 7- Хлор-5-(1-хлорэтил)-3-метилфуро[2, 3с] пиридин (805 мг, 3,5 ммоль) в 2 х 3 мл сухого диметилформамида добавляют по каплям к реакционной смеси, и смесь перемешивают 48 часов. Реакционную смесь разбавляют 120 мл этилацетата, промывают 4 х 50 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до бледно-желтого твердого продукта. Сырой продукт хроматографируют на 100 г силикагеля (230-400 меш), элюируя 25% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 21-45 объединяют и концентрируют с получением 1,09 г белого твердого продукта, который промывают 10 мл 20% диэтилового эфира/гексана с получением 997 мг 4-амино-2-(1-(7-хлор-3- метилфуро[2, 3с]пиридин-5-ил)этилтио)-6-трифторметилпиримидина в виде белого твердого продукта (температура плавления 172-173oC).
ПРИМЕР 296. 4-Амино-6-трифторметил-2-(1-(3-метилфуро[2, 3с] пиридин-5-ил)этилтио)-пиримидин (Соед. N 296).
Мезилатную соль 4-амино-6-трифторметил-2-меркаптопиримидина (561 мг, 1,93 ммоль) суспендируют в 6 мл сухого диметилформамида в атмосфере азота в 50-мл двугорлой круглодонной колбе, высушенной в печи. Суспензию охлаждают до 0oC, обрабатывают гидридом натрия (162 мг, 4,04 ммоль), и смесь перемешивают 1 час при комнатной температуре. 5-(1-Хлорэтил)-3-метилфуро [2,3с] пиридин (350 мг, 1,75 ммоль) в 2 х 2 мл сухого диметилформамида добавляют по каплям к реакционной смеси и смесь перемешивают 24 часа. Реакционную смесь разбавляют 75 мл этилацетата, промывают 4 х 25 мл 50% насыщенного хлорида натрия, затем 1 х 25 мл насыщенного хлорида натрия, и органические слои сушат над безводным карбонатом калия. Высушенные органические слои концентрируют в вакууме до желтого масла. Сырой продукт хроматографируют на 50 г силикагеля (230-400 меш), элюируя 35% этилацетат/гексаном, собирая 9-мл-вые фракции. Фракции 40-80 объединяют и концентрируют с получением 290 мг (79%) 4-амино-6-трифторметил-2-(1-(3-метилфуро[2, 3с] пиридин-5-ил)этилтио)-пиримидина в виде не совсем белого твердого продукта (температура плавления 198-200 oC).
ПРИМЕРЫ 297 и 298. (S)-(-)-4-Амино-6-трифторметил-2-(1-(3- метилфуро[2, 3с] пиридин-5-ил)этилтио)-пиримидин (Соед. N 297) и (R)-(+)-4-Амино-6-трифторметил-2-(1-(3-метилфуро[2, 3с]- пиридин-5-ил)этилтио)-пиримидин (Соед. N 298)
Способ A: Образец 4-амино-6-трифторметил-2-(1- (3-метилфуро [2, 3с]пиридин-5-ил)этилтио)-пиримидина (Соед. N 296; 1,20 г) выделяют, используя ВЭЖХ с хиральной фазой (Chiralcel OD-H; 46 х 25 см; 0,5 мл/мин; 20% изопропанол/гексан) с получением (475,5 мг) (S)-(-)-4-амино-6-трифторметил-2-(1-(3-метилфуро- [2, 3с]пиридин-5-ил)этилтио)-пиримидина (13,6 мин) и 478,2 мг (R)-(+)-4-амино-6-трифторметил-2-(1-(3-метилфуро[2,3c] -пиридин- 5-ил)этилтио)-пиримидина (21,1 мин). (S)-(-)-4-амино-6- трифторметил-2-(1-(3-метилфуро[2, 3с]пиридин-5-ил)этилтио)- пиримидин растворяют в смеси растворителей ацетон-метиленхлоридметанол, обрабатывают 2,3 г силикагеля и концентрируют при пониженном давлении. Сыпучий порошок вводят в колонку с набивкой 25 г силикагеля и элюированием смесью ацетон-метиленхлорид-метанол (15: 93: 2), получают 376 мг чистого продукта. (R)-(+)-4-амино-6-трифторметил-2-(1-(3-метилфуро- [2, 3с] пиридин-5-ил)этилтио)-пиримидин хроматографируют таким же образом с получением 352 мг чистого энантиомера. Соед. 297, температура плавления 179-181oC; оптическое вращение: [α]D= -132,5° (с=0,495, CHCl3); > 99% ст. чистоты. Соед. 298, температура плавления 179-181oC; оптическое вращение: [α]D= +129,8° (c=0,645, CHCl3); 98% ст. чистоты.
Способ B: Перемешиваемую магнитной мешалкой суспензию гидрида натрия (2,55 г, 63,5 ммоль, 60% масляная дисперсия) в 110 мл диметилформамида охлаждают до 0oC, обрабатывают мезилатной солью 4-амино-6-трифторметил-2-меркаптопиримидина (8,86 г, 30,4 ммоль) и реакционную смесь перемешивают в течение 1 часа при температуре окружающей среды. Добавляют (R)-(+)-5-(1-хлорэтил)-3-метилфурано[2, 3с] пиридин (5,4 г, 27,6 ммоль) в 2 х 10 мл диметилформамида и реакционную смесь оставляют перемешиваться при комнатной температуре в течение 3,5 дней. Содержимое выливают в 800 мл воды со льдом, экстрагируют 4 х 100 мл этилацетата. Объединенные органические экстракты промывают 4 х 100 мл 50% насыщенного NaCI, сушат над смесью 1:1 карбонат калия/безводный MgSO4 и концентрируют при пониженном давлении. Хроматография на 300 г силикагеля с набивкой и элюирование 38% смесью этилацетат/гексан дает 9,3 г (95%, 94 % ст. чистоты) (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфурано[2, 3с] пиридин-5-ил) этилтио)-пиримидина. Перекристаллизация твердого продукта из этилацетата дает 6,5 г (66%, 97 % ст. чистоты) (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфурано[2, 3с] пиридин-5-ил) этилтио)-пиримидина (температура плавления 180,5-181,5oC; оптическое вращение: [α]D= -131,6° (с = 0,525, CHCl3)).
ПРИМЕРЫ 299 и 300. (S)-(-)-4- Амино-6-хлор-2-(1-(фуро[2, 3с]- пиридин-5-ил)этилтио)пиримидин, (Соед. N 299) и (R)-(+)-4- амино-6-хлор-2-(1-(фуро[2, 3с]пиридин-5-ил)этилтио)-пиримидин, (Соед. N 300).
Способ A: 200 мг образца 4-амино-6-хлор-2-(1- (фуро[2, 3с]пиридин-5-ил)этилтио)-пиримидина (Соед. N 238; рацемат) выделяют, используя колонку Chiralcel OD-H, элюируя 20% изопропанол/гексаном со скоростью потока 0,5 мл/мин. Две порции продукта выделяют с временами удерживания 15,6 мин (Соед. 299, 74 мг) и 26,1 мин (Соед. 300, 97 мг).
Фракции из колонки хроматографируют независимо друг от друга на 10 г силикагеля (230-400 меш), элюируя 45% смесью этилацетат/гексан, собирая 5 мл-вые фракции. Кристаллизация из гексана/диэтилового эфира дает либо 55 мг (Соед. 299, температура плавления 144-145oC, вращение: [α]
Способ B: 7-Хлор-5-(1-гидроксиэтил)-фуро[2, 3с] пиридин (3,95 г, 20 ммоль) растворяют в 110 мл метанола, содержащего 20% гидроксида палладия на угле (1 г), в 200-мл одногорлой круглодонной колбе в атмосфере азота. Суспензию обрабатывают циклогексеном (19,8 мл, 200 ммоль), затем гидроксидом натрия (15 мл, 30 ммоль) и реакционную смесь нагревают с обратным холодильником в течение 3,5 часов. Смесь охлаждают, фильтруют через целит и отфильтрованную лепешку тщательно промывают свежим метанолом. Фильтрат концентрируют в вакууме до желтой пасты. Остаток распределяют между 1 х 50 мл воды и 4 х 25 мл дихлорметана, органические слои сушат над карбонатом калия и концентрируют в вакууме до бледного масла (3,16 г). Сырой продукт хроматографируют на 125 г силикагеля (230-400 меш), элюируя 60% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 32-72 объединяют и концентрируют с получением 2,52 г (77%) указанного в заголовке соединения 5-(1-гидрокси-этил)фуро[2,3с]пиридина в виде бледного масла.
1H-ЯМР (CDCl3, ТМС): δ 1,55 (д, J=6,5 Гц, 3), 4,19 (ушир.с, 1), 5,01 (кв, J= 6,5, 13 Гц, 1), 6,78 (д, J=2 Гц, 1), 7,56 (с, 1), 7,76 (д, J=2 Гц, 1), 8,76 (с, 1) м.д.
Часть 1: 5-(1-Гидроксиэтил)-фуро[2, 3с] пиридин (11,3 г, 69,4 ммоль) объединяют с липазой из поджелудочной железы свиньи, тип (II) (16,5 г), и 2,2,2-трифторэтилбутиратом (41,8 мл, 227 ммоль) в 226 мл диэтилового эфира в атмосфере азота в 500-мл одногорлой круглодонной колбе. Реакционную смесь перемешивают 9 дней при комнатной температуре, фильтруют до удаления фермента и отфильтрованную лепешку тщательно промывают диэтиловым эфиром. Фильтрат концентрируют в вакууме до бледного масла. Остаток азеотропно отгоняют с 3 х 200 мл толуола и откачивают при высоком вакууме при 40oC в течение 3 часов. Сырой продукт хроматографируют на 300 г силикагеля (230-400 меш), элюируя 60% этилацетат/гексаном, собирая 50-мл-вые фракции. Фракции 10-18 объединяют и концентрируют с получением 7,53 г (46,5%) (R)-(+)-5-(1-бутирилокси)-фуро[2,3с]пиридина
1H-ЯМР (CDCl3, ТМС): δ 0,94 (т, J=7,4 Гц, 3), 1,61-1,74 (м, 5), 2,36 (м, 2), 6,04 (кв, J=6,6 Гц, 13,2 Гц, 1), 6,79 (м, 1), 7,59 (с, 1), 7,75 (д, J= 2,1 Гц, 1), 8,85 (с, 1) м.д.;
вращение [α]
Часть 2: (R)-(+)-5-(1-бутирилокси)-фуро[2, 3с]пиридин (7,5 г, 32,2 ммоль) растворяют в 88 мл метанола в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают 2н гидроксидом натрия (35,4 мл, 70,8 ммоль), реакционную смесь перемешивают в течение 1 часа, и летучие продукты удаляют в вакууме. Остаток распределяют между 1 х 25 дихлорметана и 1 х 100 мл воды. Нерастворимый продукт удаляют путем фильтрования через целит. Слои разделяют и водный слой дополнительно экстрагируют 3 х 25 мл дихлорметана. Объединенные органические слои сушат над карбонатом калия и концентрируют в вакууме с получением 4,68 г (89%) указанного в заголовке соединения (R)-(+)-5-(1- гидроксиэтил)-фуро-[2, 3с]пиридина в виде белого твердого продукта (температура плавления 60-61oC; вращение (c=1): [α]
(R)-(+) -5- (1-Гидроксиэтил)-фуро[2, 3с] пиридин (6,87 г, 25,7 ммоль) объединяют с бензойной кислотой (3,86 г, 31,6 ммоль) и трифенилфосфином (8,29 г, 31,6 ммоль) в 125 мл сухого тетрагидрофурана в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают по каплям с диэтилазидодикарбоксилатом (умеренная скорость добавления, допускается некотороя экзотерма), и реакционную смесь перемешивают в течение 1,5 часа при комнатной температуре. Летучие продукты удаляют в вакууме и масляный остаток разбавляют последовательно равными объемами диэтилового эфира и гексана, и белый твердый продукт собирают путем фильтрования. Фильтрат концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 250 г силикагеля (230-400 меш), элюируя 20% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 48-95 объединяют и концентрируют с получением 6,87 г (90%) указанного в заголовке соединения (S)-(+)-5-(1-бензоилоксиэтил)-фуро-[2, 3с] пиридина в виде бледного масла (вращение: [α]
1H-ЯМР (CDCl3, TMC): δ 1,79 (д, J=6,7 Гц, 3), 6,32 (кв, J=6,7, 13,4 Гц, 1), 6,80 (м, 1), 7,41-7,48 (м, 2), 7,52-7,60 (м, 1), 7,71 (с, 1), 7,76 (д, J=2,1 Гц, 1), 8,12 (м, 2), 8,95 (с, 1) м.д.
Часть 3: (S)-(+)-5-(1-бензоилоксиэтил)-фуро[2, 3с]пиридин (6,87 г, 25,7 ммоль) растворяют в 88 мл метанола в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают 2н гидроксидом натрия (28,3 мл, 56,6 ммоль), реакционную смесь перемешивают в течение 2 часов при комнатной температуре, и летучие продукты удаляют в вакууме. Остаток распределяют между 1 х 50 мл воды и 4 х 25 мл дихлорметана. Органические слои сушат над безводным карбонатом калия и концентрируют в вакууме до янтарного масла. Сырой продукт хроматографируют на 150 г силикагеля (230-400 меш), элюируя 65% этилацетат/гексаном, собирая 22-мл-вые фракции. Фракции 25-70 объединяют и концентрируют с получением 3,96 г (94%) указанного в заголовке соединения (S)-(-)-5-(1-гидроксиэтил)-фуро[2, 3с] пиридина в виде белого твердого продукта (температура плавления 60-61oC; вращение: [α]
(S)-(-)-5-(1-Гидроксиэтил)-фуро[2,3с] пиридин (9,0 г, 55,2 ммоль) растворяют в 35 мл хлорформа в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор обрабатывают трифенилфосфином (28,9 г, 110,3 ммоль), затем четыреххлористым углеродом (106 мл, 1,10 моль), и реакционную смесь перемешивают в течение 24 часов при комнатной температуре. Раствор разбавляют 35 мл гексана, перемешивают в течение 30 минут, и белый осадок удаляют путем фильтрования. Отфильтрованную лепешку промывают 100 мл 20% диэтилового эфира/гексана, и фильтрат концентрируют до малого объема (холодная баня, не досуха). Остаток хроматографируют на 350 г силикагеля (230-400 меш), элюируя 15% этилацетат/гексаном, собирая 50-мл-вые фракции. Фракции 23-48 объединяют и концентрируют с получением 8,48 г (83%) указанного в заголовке соединения (R)-(+)-5-(1-хлорэтил)- фуро[2, 3с] пиридина в виде слаборастворимого не совсем белого твердого продукта (температура плавления 36-38oC; 97% ст. чистоты; вращение:( [α]
250-мл Трехгорлую круглодонную колбу, высушенную в печи, в атмосфере азота загружают 60% гидридом натрия (3,5 г, 87,5 ммоль). Гидрид промывают 3 х 7 мл гексана, суспендируют в 75 мл сухого диметилформамида, и смесь охлаждают до 0oC. Суспензию обрабатывают частями мезилатной солью 4-амино-6-хлор-2-меркаптопиримидина (10,9 г, 42,3 ммоль) и перемешивают в течение 1 часа при комнатной температуре. Реакционную смесь обрабатывают по каплям (R)-(+)-5-(1-хлорэтил)- фуро[2, 3с]пиридином (7,4 г, 40,6 ммоль) в 1 х 20 мл диметилформамида (промывка 5 мл) и смесь перемешивают 5 дней при комнатной температуре. Смесь выливают в 400 мл этилацетата, экстрагируют 4 х 100 мл 50% насыщенного хлорида натрия, и сушат над безводным карбонатом калия/сульфатом магния. Высушенные органические слои концентрируют в вакууме до янтарного масла. Сырой продукт разбавляют ацетон/дихлорметаном и хроматографируют на 450 г силикагеля (230-400 меш), элюируя 45% этилацетат/гексаном и пропуская 1000 мл мертвого объема элюента, собирают 50-мл фракции. Фракции 21-63 объединяют и концентрируют с получением 11,05 г (89%, 97,6% ст. чистоты) (S)-(-)-4-амино-6-хлор-2-(1-(фуро[2, 3с]-пиридин-5-ил) этилтио)-пиримидина в виде белого твердого продукта. Перекристаллизация из этилацетата дает 7,92 г (64%, 99% ст. чистоты) (S)-(-)4-амино-6- хлор-2-(1-(фуро-[2, 3с>] пиридин-5-ил)этилтио)-пиримидина (температура плавления 169-170,5oC; вращение: [α]
1H-ЯМР (d6ДМСО): δ 1,70 (д, J=7 Гц, 3), 5,11 (кв, J=6,9, 13,8, Гц, 1), 6,15 (с, 1), 7,00 (м, 1), 7,30 (ушир.с, 2), 7,78 (д, J=l Гц, 1), 8,20 (д, J= 2,1 Гц, 1), 8,88 (с, 1) м.д.
ПРИМЕР 301. Мезилатная соль (S)-(-)-4-амино-6-хлор-2-(1- (фуро-[2, 3с] пиридин-5-ил)этилтио)-пиримидина (Соед. N 301)
(S)-(-)-4-Амино-6-хлор-2-(1-(фуро[2, 3с] пиридин-5-ил)-этилтио)- пиримидин (Соед. 299; 2,0 г, 6,52 ммоль) растворяют в 62 мл этилацетата в атмосфере азота в 200-мл одногорлой круглодонной колбе. Раствор затравливают предварительно полученным продуктом, медленно обрабатывают по каплям метансульфоновой кислотой (423 мкл, 6,52 ммоль) в 62 мл диэтилового эфира и перемешивают в течение 2 часов при комнатной температуре. Твердый продукт собирают, промывают диэтиловым эфиром и сушат в вакууме при 50oC с получением 2,57 г (98%) указанного в заголовке соединения мезилатной соли (S)-(-)-4-амино-6-хлор-2-(1-(фуро[2, 3с]пиридин-5-ил)-этилтио)- пиримидина в виде мелкодисперсного белого продукта (температура плавления 201-202oC).
ПРИМЕР 302. Эзилатная соль (S)-(-)-4-Амино-6-хлор-2-(1- (3-метилфуро[2, 3с]пиридин-5-ил)этилтио)-пиримидина (Соед. N 302)
К раствору (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфуро- [2, 3с]пиридин-5-ил)этилтио)-пиримидина (Соед. N 290; 1,45 г, 4,53 ммоль) в 36 мл метиленхлорида плюс 9 мл метанола при комнатной температуре добавляют 154 мл диэтилового эфира. Добавляют по каплям раствор этансульфоновой кислоты (0,525 г, 95%, 4,53 ммоль, 1,0 эквив.) в 54 мл диэтилового эфира при комнатной температуре в течение 17 мин периода. После завершения добавления реакционную смесь затравливают кристаллической солью и перемешивают в течение ночи при комнатной температуре. Клейкий нерастворимый остаток, который образуется на начальной стадии, становится чисто белым кристаллическим твердым продуктом, который собирают путем фильтрования и сушат с получением 1,87 г (96%) эзилатной соли (S)-(-)-4-амино-6-хлор-2-(1-(3-метилфуро[2, 3с]пиридин-5-ил) - этилтио)-пиримидина (т.пл. 203-204oC).
ПРИМЕР 303. 4-амино-6-хлор-2-(((5-бензилокси-6-хлор) - 2-пиридил)этил)тиопиримидин
Стадия 1: К раствору 2-хлор-6-йод-3-пиридинола (500 мг, 1,96 ммоль) и K2CO3 (690 мг, 5,0 ммоль) в метаноле (5 мл) добавляют бензилбромид (510 мг, 3,0 ммоль). Реакционную смесь нагревают с обратным холодильником в течение 60 минут и дают ей охладиться до 22oC. Смесь затем концентрируют в вакууме. Оставшиеся твердые продукты суспендируют в этилацетате и фильтруют. Фильтрат сушат над MgSO4 и концентрируют в вакууме с получением 416 мг (61%) 2-хлор-3-бензилокси-6-йодпиридина.
Стадия 2: 2-Хлор-3-бензилокси-6-йодпиридин (416 мг, 1,2 ммоль) в ТГФ (4 мл) охлаждают до -78oC и обрабатывают н-бутиллитием (1,2 мл 1,6М в гексане, 1,92 ммоль). Через 60 минут добавляют ацетальдегид (237 мг, 5,4 ммоль) и реакционной смеси дают нагреться до 22oC в течение 2 часов. Реакционную смесь гасят водой (5 мл) и концентрируют в вакууме. Оставшийся раствор экстрагируют несколько раз этилацетатом, сушат над MgSO4 и концентрируют в вакууме с получением масла. Масло хроматографируют 1:1 гексан/этилацетатом с получением 220 мг (70%) 2-хлор-3-бензилокси-6-(1-гидроксиэтил)- пиридина.
По общему способу примера 253, и проводя несущественные изменения, но используя в качестве исходного продукта 2-хлор-3-бензилокси-6-(1-гидроксиэтил)-пиридин, получают указанное в заголовке соединение, 98 мг (65%), т.пл. 70-72oC.
ПРИМЕР 304. 4-амино-6-хлор-2-(фуро[2,3-b]пиридин-5-ил- метилтио)-пиримидин (Соед. 304)
5- (Хлорметил)-фуро[2,3-b]пиридин получают по способу, описанному в I.N. Houpis, W. B. Choi, P.J. Reider, A. Molina, H. Churcill, J. Lynch, R.P. Volante Tetrahedron Lett. 9355-9358 (1994).
Указанное в заголовке соединение (Соед. N 304; т.пл. 124-126oC) получают по способу, описанному для примера 253, часть B, за исключением того, что алкилтио получают с 5-(хлорметил)-фуро[2,3-b]пиридином.
ПРИМЕР 305. Этиловый эфир 6-амино-2-(2-нафтилметилтио)- пиримидин-4-карбоновой кислоты (Соед. N 305)
Стадия 1: Тиооротоновую кислоту (1,72 г, 10,0 ммоль) суспендируют в 50% EtOH (30 мл), обрабатывают гидроксидом натрия (880 мг, 22 ммоль), затем перемешивают в течение 5 минут при комнатной температуре. Добавляют 2-бромметилнафталин (2,21 г, 10 ммоль), и реакционную смесь нагревают с обратным холодильником в течение 2 часов. Нагретую реакционную смесь подкисляют 1н HCl (11 мл) и затем охлаждают, осадок собирают и сушат с получением 3,03 г (97%) 6-гидрокси-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты.
Стадия 2: Раствор 6-гидрокси-2-(2-нафтилметилтио)- пиримидин-4-карбоновой кислоты (2,50 г, 8,0 ммоль) и 1,1-карбонилдиимидазола (1,94 г, 12 ммоль) в ДМФ (30 мл) перемешивают в течение 30 мин, затем обрабатывают абсолютным этанолом (8,0 мл). Через 1,5 часа перемешивания реакционную смесь выливают в воду, перемешивают в течение 20 мин, затем фильтруют и сушат с получением 2,371 г (88%) этилового эфира 6-гидрокси-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты.
Стадия 3: Раствор этилового эфира 6-гидрокси-2-(2- нафтилметилтио)-пиримидин-4-карбоновой кислоты (2,32 г, 6,81 ммоль) и 2-пиколина (0,7 мл) в POCl3 (7 мл) перемешивают при комнатной температуре в течение 3 часов, затем выливают на лед. Твердый продукт собирают путем фильтрования, затем быстро нагревают с NH4OH в течение 15 минут. Твердый продукт собирают и перекристаллизовывают из метанола с получением 1,72 г (70%) этилового эфира 6-хлор-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты, т.пл. 95-96oC.
Стадия 4: Этиловый эфир 6-хлор-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты (1,107 г, 2,08 ммоль) растворяют в ДМФ (9,0 мл), затем обрабатывают азидом натрия (600 мг, 9,23 ммоль) и перемешивают в течение 24 часов. Желтый раствор концентрируют в вакууме, затем разбавляют с этилацетатом. Органические слои фильтруют через целит, промывают водой и насыщенным солевым раствором, затем сушат MgSO4 и концентрируют в вакууме с получением 1,20 г (100%+) этилового эфира 6-азо-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты.
Стадия 5: Раствор этилового эфира 6-азо-2-(2-нафтилметилтио)-пиримидин-4-карбоновой кислоты (1,20 г) в этилацетате (45 мл) и этаноле (20 мл) обрабатывают хлоридом олова (II) (3,80 г, 16,9 ммоль) и перемешивают при комнатной температуре в течение 15 минут. Реакционную смесь выливают на лед/NaHCO3, фильтруют через целит, и фильтрат экстрагируют 2х этилацетатом. Органические слои промывают насыщенным солевым раствором, сушат с MgSO4, и концентрируют в вакууме: 646 мг (62%) этилового эфира 6-амино-2-(2-нафтилметилтио)- пиримидин-4-карбоновой кислоты (Соед. N 305), т.пл. 188-189oC.
ПРИМЕР 306. Мезилатная соль (S)-(-)4-амино-2-(3-метилфурано- [2, 3с]пиридин-5-ил)этилтио-6-трифторметилпиримидина (Соед. N 306)
(S)-(-)-4-Амино-2-(3-метилфурано[2, 3с] пиридин-5-ил)- этилтио-6-трифторметилпиримидин (354 мг, 1,0 ммоль) растворяют в 25 мл диэтилового эфира в 50-мл одногорлой круглодонной колбе. Раствор обрабатывают медленно по каплям метансульфоновой кислотой (64 мкл, 1,0 ммоль) в 5 мл диэтилового эфира. Выпадающей хлопьями суспензии дают перемешиваться в течение 20 часов при комнатной температуре. Мелкодисперсный белый твердый продукт собирают, промывают диэтиловым эфиром и сушат в вакууме при 50oC с получением 422 мг (94%) мезилатной соли (S)-(-)4-амино-2-(3-метилфурано-[2, 3с]-пиридин-5-ил)-этилтио-6- тирфторметилпиримидина. (Температура плавления 161-163oC).
ПРИМЕР 307. 4-амино-6-хлор-2-(((5-изобутокси-6-хлор)-2-пиридил)- этил)тиопиримидин (Соед. N 307)
По общему способу примера 303 и производя несущественные изменения, но используя в качестве исходного продукта изобутирилхлорид, синтезируют указанное в заголовке соединение 4-амино-6-хлор-2-(((5-изопропокси-6-хлор)-2-пиридил)этил)тиопиримидин
1H-ЯМР (CDCl3): δ 7,37 (д, J=6,2 Гц, 1H), 7,10 (д, J=6,2 Гц, 1H), 6,12 (с, 1H), 5,06 (кв, 1H), 4,96 (с, 2H), 3,77 (д, J=4,8 Гц, 2 H), 2,15 (м, 1H), 1,73 (д, J=5,4 Гц, 3H), 1,06 (д, J=5,0 Гц, 6 H).
Следуя указанным выше способам и производя несущественные изменения, получают следующие соединения:
4-амино-6-хлор-2-(1-(3-трифторметилфуро[2,3-с]пиридин-5- ил)этил)тиопиримидин, т.пл. 91-93oC,
4-амино-6-хлор-2-(1-(7-хлор- 3-трифторметилфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин, т.пл. 169-170oC,
4-амино-6-хлор-2-(1-(3-фторфуро[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-((2,2,2-трифтор)этил) фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2- (1-(3-((1-трифторметил-2,2,2-трифтор)этил)фуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3- цианофуро[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-карбометоксифуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-аминокарбинилфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(N, N-диметиламинокарбинил)-фуро [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилсульфониламино)фуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилкарбоксиамино)фуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-фенилфуро[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(трет-бутил)фуро [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-циклопропилфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фторфуро[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((2,2,2-трифтор)этил)-фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((1-трифторметил-2,2,2-трифтор) этил)фуро[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-цианофуро[2,3-c]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-карбометоксифуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-аминокарбинилфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(N,N-диметиламинокарбинил)фуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилсульфониламино) фуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилкарбоксиамино)-фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фенилфуро[2,3-с]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(трет-бутил)фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1- (3-циклопропилфуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фторфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-((2,2,2-трифтор)этил)фуро [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1- (3-((1-трифторметил-2,2,2-трифтор)этил)фуро[2,3-c] пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-цианофуро[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-карбометоксифуро[2,3-c]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-аминокарбинилфуро[2,3-c]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(N, N-диметиламинокарбинил)-фуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилсульфониламино)фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилкарбоксиамино)фуро [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фенилфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-(трет-бутил)фуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-циклопропилфуро[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-фтортиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-((2,2,2-трифтор)этил) тиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-((1-трифторметил-2,2,2-трифтор)этил)тиено [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-цианотиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-карбометокситиено[2,3-c]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-аминокарбинилтиено[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(N, N-диметиламинокарбинил)-тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилсульфониламино)тиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилкарбоксиамино)тиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-фенилтиено[2,3-c]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(трет-бутил)тиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-циклопропилтиено[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фтортиено[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((2,2,2-трифтор)этил)-тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((1-трифторметил-2,2,2-трифтор) этил)тиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-цианотиено[2,3-c] пиpидин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-карбометокситиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-аминокарбинилтиено[2,3-с] пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(N, N-диметиламинокарбинил)тиено [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилсульфониламино)тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилкарбоксиамино)-тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фенилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(трет-бутил)тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-циклопропилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-фтортиено[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-((2,2,2-трифтор)этил)тиено [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-((1-трифторметил-2,2,2-трифтор)этил)тиено [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-цианотиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-карбометокситиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-аминокарбинилтиено[2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(N, N-диметиламинокарбинил)-тиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилсульфониламино) тиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилкарбоксиамино)тиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-фенилтиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(трет-бутил)тиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-циклопропилтиено[2,3-c]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-фтор-1H-пирроло[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-((2,2,2-трифтор)этил)-1H- пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-((1-трифторметил-2,2,2-трифтор) этил)-1H-пирроло[2,3-с]пиридин-5-ил)этил)-тиопиримидин,
4-амино-6-хлор-2-(1-(3-циано-1H-пирроло[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-карбометокси-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-аминокарбинил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(N,N-диметиламинокарбинил)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилсульфониламино)-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилкарбоксиамино)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-фенил-1H-пирроло[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(трет-бутил)-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-циклопропил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фтор-1H-пирроло[2,3-c]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((2,2, 2-трифтор)этил)-1H- пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((1-трифторметил-2,2,2- трифтор)этил)-1H-пирроло[2,3-с]пиридин-5-ил)этил)- тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-циано-1H-пирроло [2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-карбометокси-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-аминокарбинил-1H- пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(N, N-диметиламинокарбинил)-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилсульфониламино)-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилкарбоксиамино)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фенил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(трет-бутил)-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-циклопропил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фтор-1H-пирроло[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-((2,2,2-трифтор)этил)-1H- пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-((1-трифторметил-2,2,2-трифтор)- этил)-1H-пирроло[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-циано-1H-пирроло[2,3-c]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-карбометокси-1H-пирроло[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-аминокарбинил-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(N, N-диметиламинокарбинил)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилсульфониламино)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилкарбоксиамино)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фенил-1H-пирроло[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-(трет-бутил)-1H-пирроло[2,3-с] -пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-циклопропил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-фтор-1-метил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-((2,2,2-трифтор)этил)-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-((1-трифторметил-2,2,2-трифтор)- этил)-1-метил-1H-пирроло[2,3-c]пиридин-5-ил)этил)- тиопиримидин,
4-амино-6-хлор-2-(1-(3-циано-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-карбометокси-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-аминокарбинил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(N, N-диметиламинокарбинил)-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилсульфониламино)-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(метилкарбоксиамино)-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-фенил-1-метил-1H-пирроло[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(трет-бутил)-1-метил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-циклопропил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фтор-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((2,2,2-трифтор)этил)-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-((1-трифторметил-2,2,2- трифтор)этил)-1-метил-1H-пирроло[2,3-c]пиридин-5-ил)этил)- тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-циано-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-карбометокси-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-аминокарбинил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(N, N-диметиламинокарбинил)-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(метилсульфониламино)-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-б-трифторметил-2-(1-(3-(метилкарбоксиамино)-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-фенил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(трет-бутил)-1-метил-1H-пирроло [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-циклопропил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фтор-1-метил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-((2,2,2-трифтор)этил)-1-метил-1H-пирроло [2, 3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-((1-трифторметил-2,2,2-трифтор)- этил)-1-метил-1H-пирроло[2,3-c]пиридин-5-ил)этил)- тиопиримидин,
4-амино-6-циано-2-(1-(3-циано-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-карбометокси-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-аминокарбинил-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(N, N-диметиламинокарбонил)-1-метил- 1H-пирроло[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилсульфониламино)-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(метилкарбоксиамино)-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-фенил-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-(трет-бутил)-1-метил-1H-пирроло[2,3-с] пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-циклопропил-1-метил-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлорфуро[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-aминo-6-трифтopмeтил-2-(1-(3-метилфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(2,3-дигидрофуро[2,3-с] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,3-диметил-2,3-дигидрофуро [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-этилфуро[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-этилфуро[2,3-с]-пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(1-метилэтил)фуро[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(7-хлорфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(фуро[2,3-с]пиридин-5-ил)этил)-тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-2-метилфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(2-метилфуро[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-метилфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(2,3-дигидрофуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3,3-диметил-2,3-дигидрофуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-этилфуро[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3,3-диметил-2,3-дигидро- фуро[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-этилфуро[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(1-метилэтил)фуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(7-хлортиено[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(тиено[2,3-с]пиридин-5-ил)этил)- тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-2-метилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(2-метилтиено[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-метилтиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(2,3-дигидротиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3,3-диметил-2, 3-дигидротиено [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-этилтиено[2,3-с]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3,3-диметил-2,3-дигидро- тиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-этилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-(1-метилэтил)тиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-1H-пирроло[2,3-c]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(1H-пирроло[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-2-метил-1H-пирроло[2,3-c] -пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(2-метил-1H-пирроло[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-метил-1H-пирроло[2,3-c]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(2,3-дигидро-1H-пирроло[2,3-c]-пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3,3-диметил-2,3-дигидро-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-этил-1H-пирроло[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3,3-диметил-2,3-дигидро-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-этил-1H-пирроло[2,3-c] -пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(1-мeтилэтил)-1H-пирроло [2,3-c] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(1-метил-1H-пирроло[2,3-с]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-2-метил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(2-метил-1-метил-1H-пирроло [2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-метил-1-метил-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(2,3-дигидро-1-метил-1H- пирроло[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3,3-диметил-2,3-дигидро-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-этил-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3,3-диметил-2,3-дигидро-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-этил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-(1-метилэтил)-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлортиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(тиено[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-2-метилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(2-метилтиено[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-метилтиено[2,3-c]пиридин-5-ил) этил)тиопиримидин
4-амино-6-хлор-2-(1-(2,3-дигидротиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3,3-диметил-2,3-дигидротиено[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-этилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3,3-диметил-2,3- дигидротиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-этилтиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(1-метилэтил)тиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-1H-пирроло[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(1H-пирроло[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-2-метил-1H-пирроло[2,3-с] -пиридин- 5-ил)этил)тиопиримидин,
4-Амино-6-хлор-2-(1-(2-метил-1H-пирроло[2,3-c]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-метил-1H-пирроло[2,3-c]пиридин-этил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(2,3-дигидро-1H-пирроло[2,3-с] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3,3-диметил-2,3-дигидро-1H-пирроло [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-этил-1H-пирроло[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3,3-диметил-2,3-дигидро-1H-пирроло [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-этил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-(1-метилэтил)1H-пирроло [2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-1-метил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-2-метил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(2-метил-1-метил-1H-пирроло[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-метил-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(2,3-дигидро-1-метил-1H-пирроло [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3,3-диметил-2,3-дигилро-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-этил-1-метил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3, 3-диметил-2,3-дигидро-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-этил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-(1-метилэтил)-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлортиено[2,3-c]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(тиено[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-2-метилтиено[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(2-метилтиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-метилтиено[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(2,3-дигидротиено[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,3-диметил-2,3-дигидротиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-этилтиено[2,3-с]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3,3-диметил-2,3-дигидротиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-этилтиено[2,3-с] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(1-метилэтил)тиено[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-1H-пирроло [2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(-1-(1-1H-пирроло[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-2-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(2-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-метил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(2,3-дигидро-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,3-диметил-2,3-дигидро-1H-пирроло [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-этил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3,3-диметил-2,3-дигидро-1H-пирроло [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-этил-1H-пирроло [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-(1-метилэтил)-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-1-метил-1H-пирроло [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-2-метил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(2-метил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-метил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(2,3-дигидро-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,3-диметил-2,3- дигидро-1-метил-1H-пирроло[2,3-c]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-этил-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3,3-диметил-2,3-дигидро-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-этил-1-метил-1H-пирроло[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-aминo-6-трифторметил-2-(1-(3-(1-метилэтил)-1- метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-хлорфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3, 7-дихлорфуро[2,3-с] -4 пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бромфуро[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-7- хлорфуро[2,3-c] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-метилфуро[2,3-с] -пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-хлорфуро[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3,7-дихлорфуро[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-бромфуро[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-7-хлорфуро[2,3-c]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-метилфуро[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-хлортиено[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3,7-дихлортиено[2,3-c] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-бромтиено[2,3-с]пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-бром-7-хлортиено [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-метилтиено[2,3-с]пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-хлоротиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,7-дихлортиено[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бромтиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-7-хлортиено[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-метилтиено[2,3-с] -пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-хлортиено[2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3,7-дихлортиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-бромтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-7-хлортиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-метилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-хлор-1H-пирроло[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3,7-дихлор-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-бром-1H-пирроло[2,3-с]пиридин-5- ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-бром-7-хлор-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-метил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-хлор-1H-пирроло[2,3-с] -пиридин-5- ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,7-дихлор-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-1H-пирроло[2,3-c] -пиридин-5- ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-7-хлор-1H-пирроло-[2,3-c] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-хлор-1H-пирроло[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3,7-дихлор-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-1H-пирроло[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-7-хлор-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-хлор-1-метил-1H-пирроло[2,3-с] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3,7-дихлор-1-метил-1H-пирроло[2,3-с] пиридин-5-ил) этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-бром-1-метил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(3-бром-7-хлор-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-метил-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-хлор-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3,7-дихлор-1-метил-1H-пирроло [2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-бром-7-хлор-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-метил-1-метил-1H-пирроло [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-хлор-1-метил-1H-пирроло[2,3-с] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3,7-дихлор-1-метил-1H-пирроло [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-1-метил-1H пирроло[2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-бром-7-хлор-1-метил-1H-пирроло- [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-метил-1-метил-1H-пирроло- [2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-трифторметилфуро[2,3-c] -пиридин-5-ил)этил) тиопиримидин,
4-амино-6-циано-2-(1-(3-трифторметилфуро[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-трифторметилфуро [2,3-c]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-трифторметилфуро [2,3-с] -пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-трифторметилтиено[2,3-с]пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-трифторметилтиено[2,3-с] пиридин-5- ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-трифторметилтиено[2,3-с] пиридин-5-ил)этил) тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-трифторметилтиено[2,3-с] -пиридин- 5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-трифторметилтиено[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-трифторметилтиено[2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-трифторметил-1H-пирроло[2,3-с]-пиридин-5-ил)этил) тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-трифторметил-1H-пирроло- [2,3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-трифторметил-1H-пирроло[2,3-c] - пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-трифторметил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-трифторметил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-трифторметил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(3-трифторметил-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(3-трифторметил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(3-трифторметил-1-метил-1H-пирроло-[2,3-c] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-хлор-2-(1-(7-хлор-3-трифторметил-1-метил-1H-пирроло[2 3-с] пиридин-5-ил)этил)тиопиримидин,
4-амино-6-трифторметил-2-(1-(7-хлор-3-трифторметил-1-метил-1H- пирроло[2,3-с]пиридин-5-ил)этил)тиопиримидин,
4-амино-6-циано-2-(1-(7-хлор-3-трифторметил-1-метил-1H-пирроло[2,3-c] пиридин-5-ил)этил)тиопиримидин. Тр



















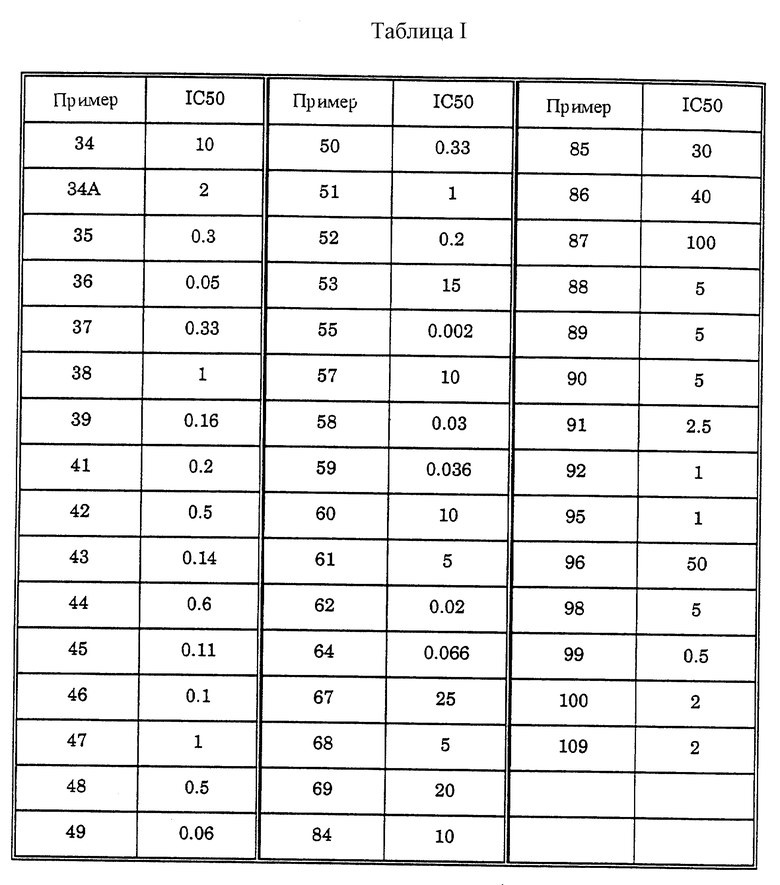
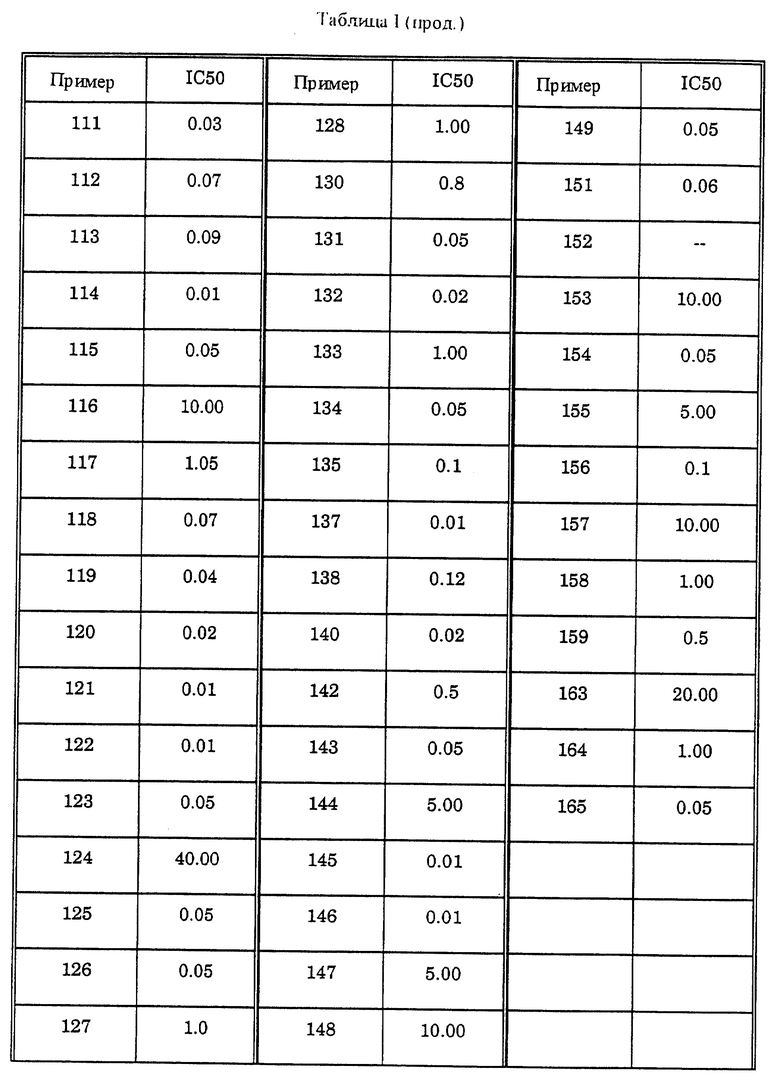
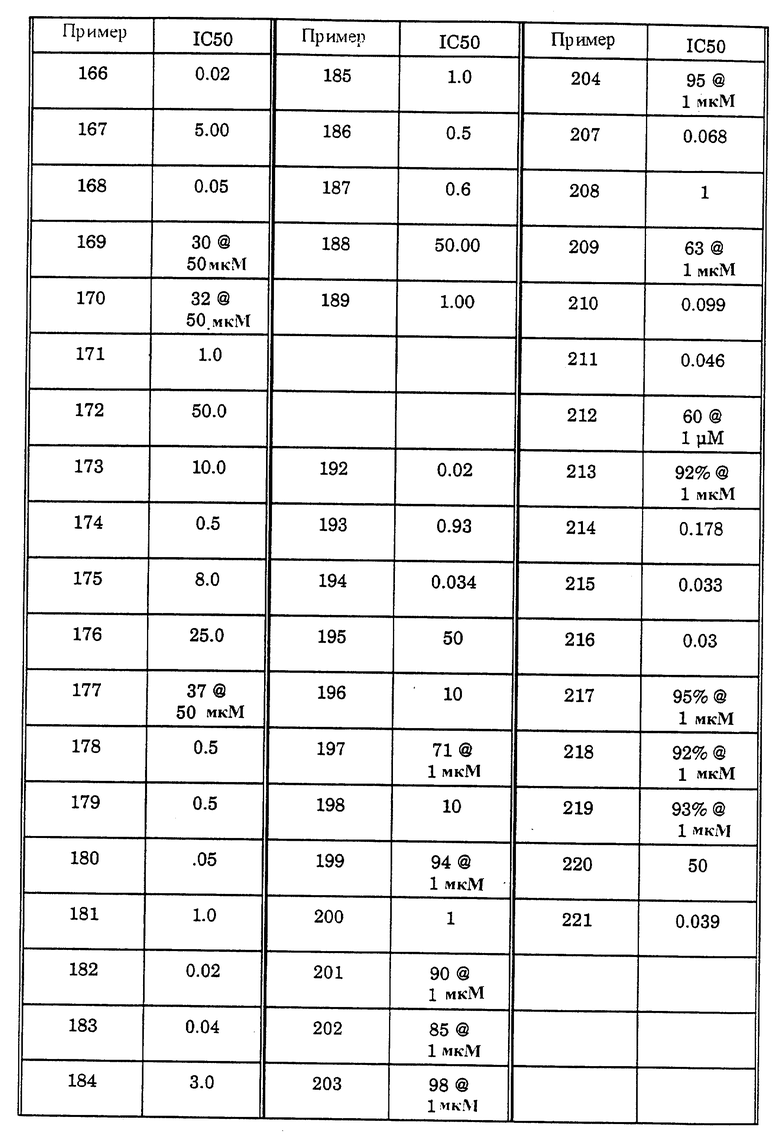

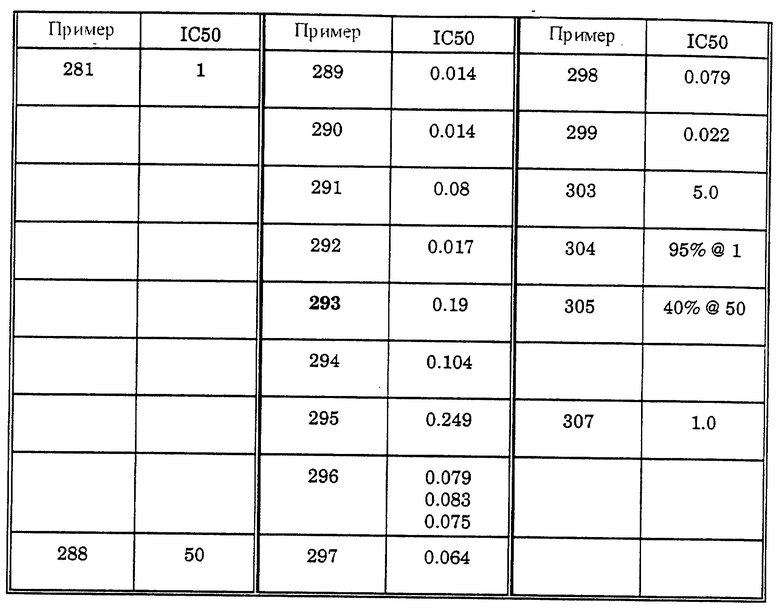
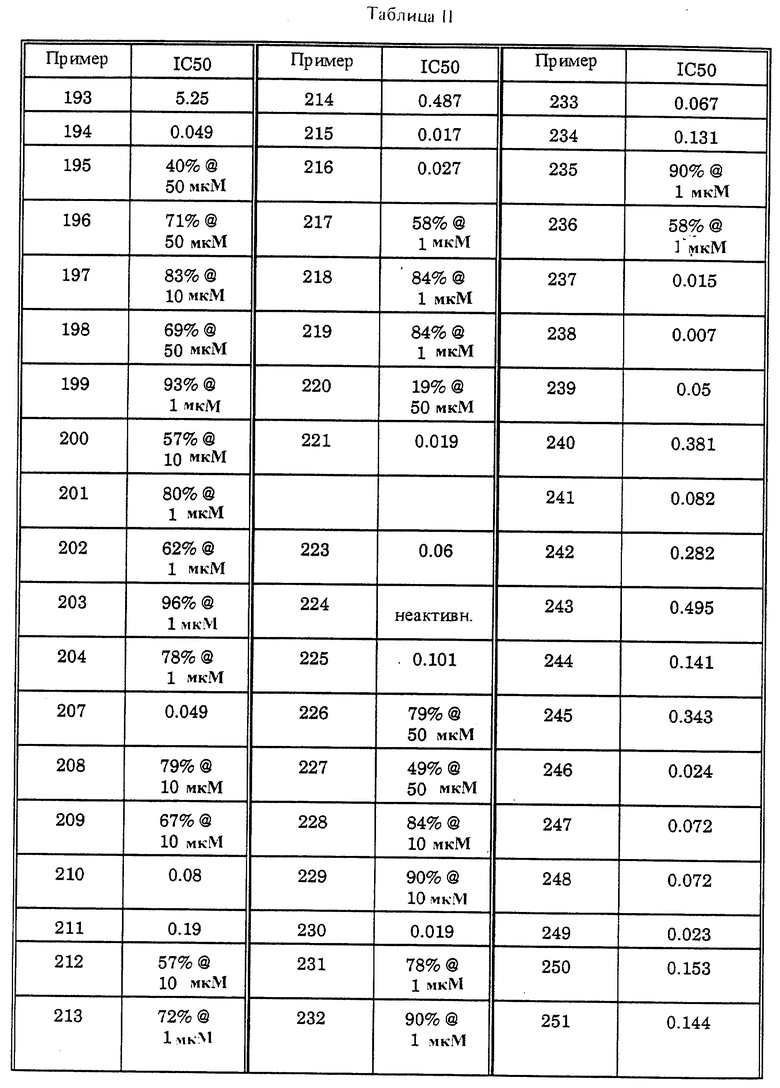
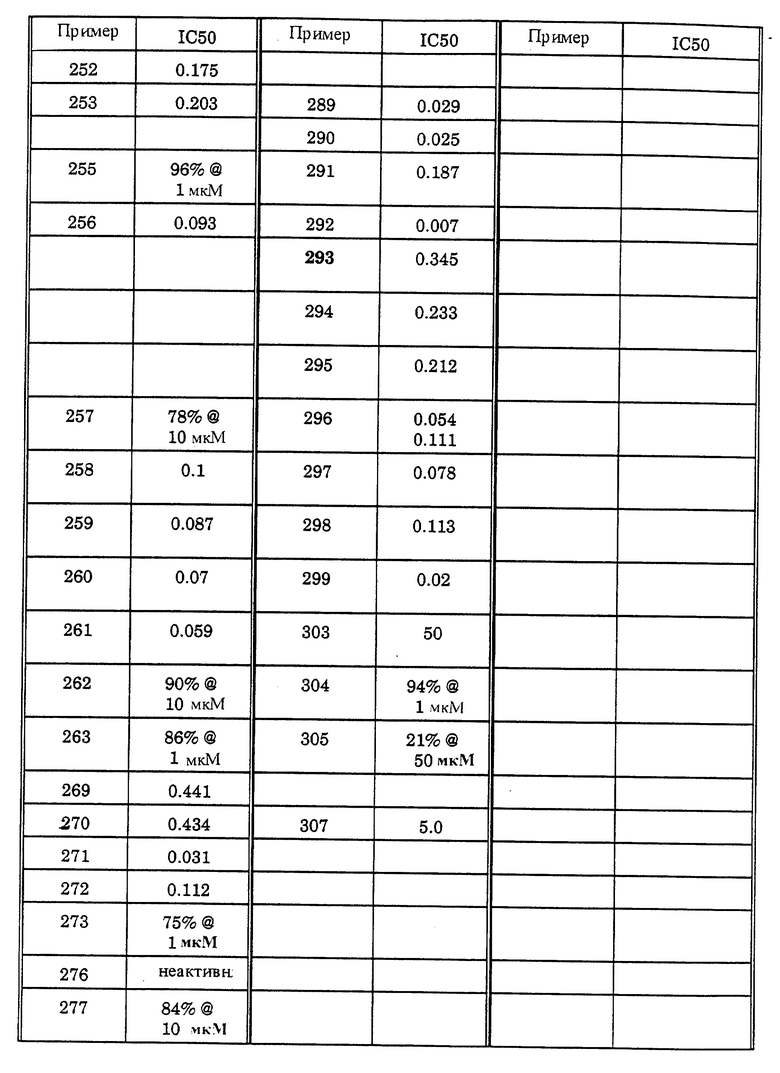
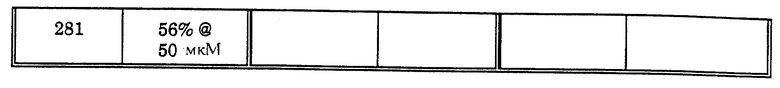
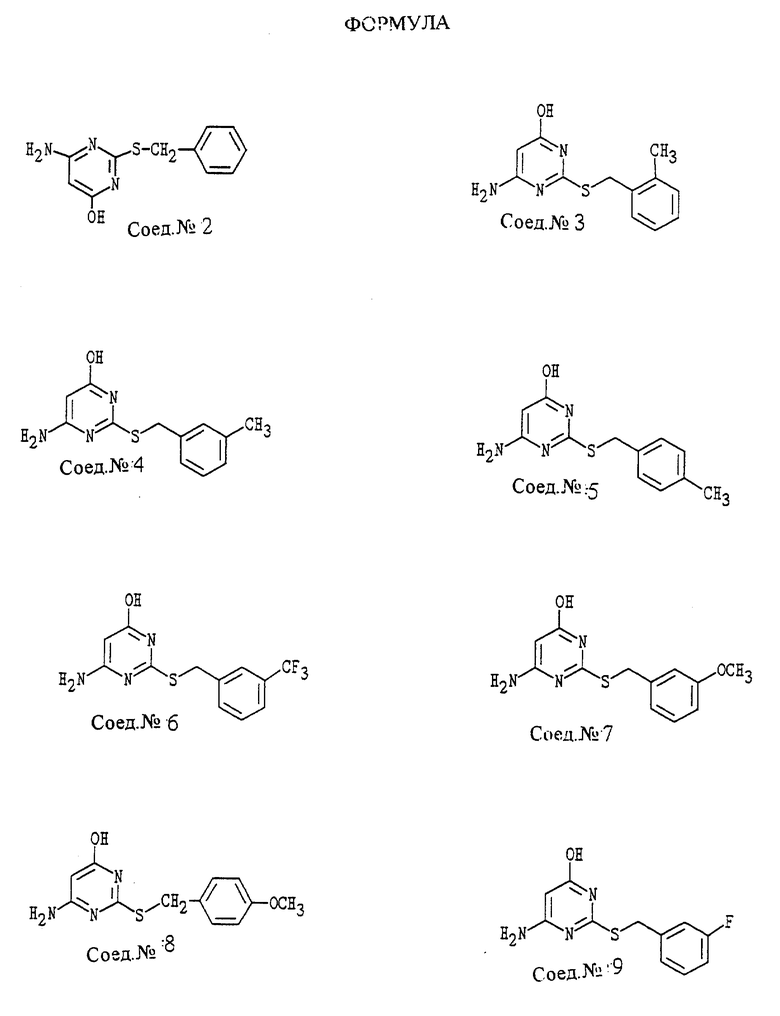
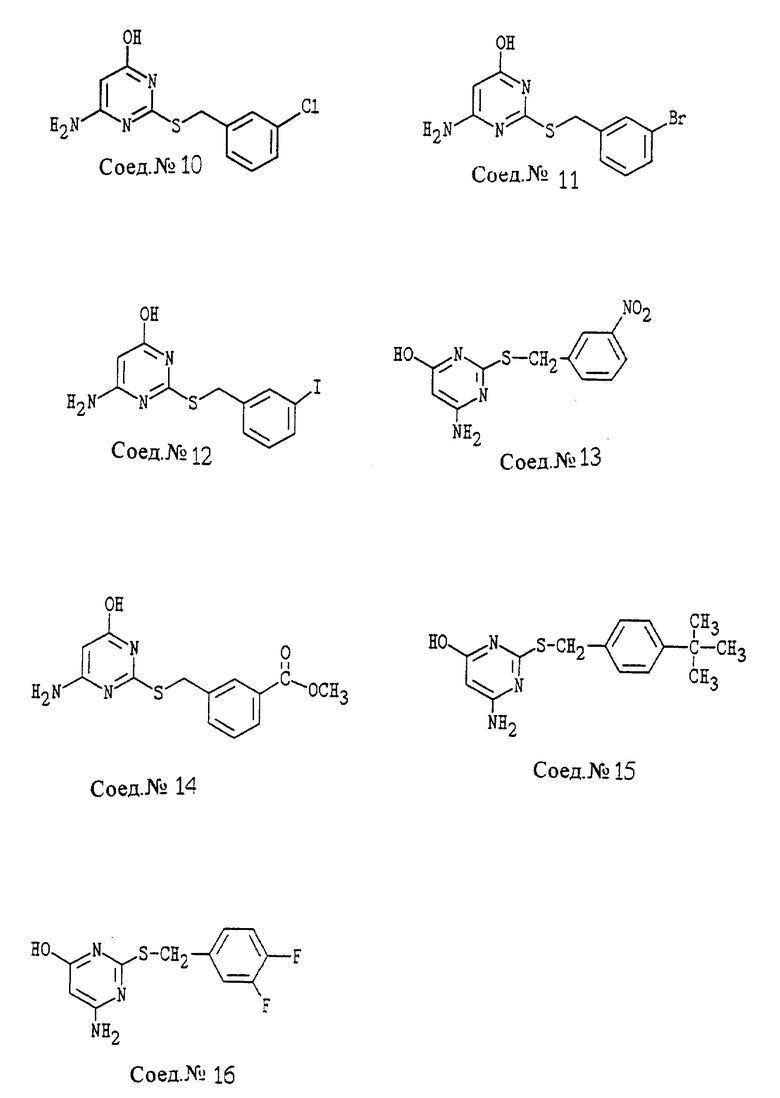
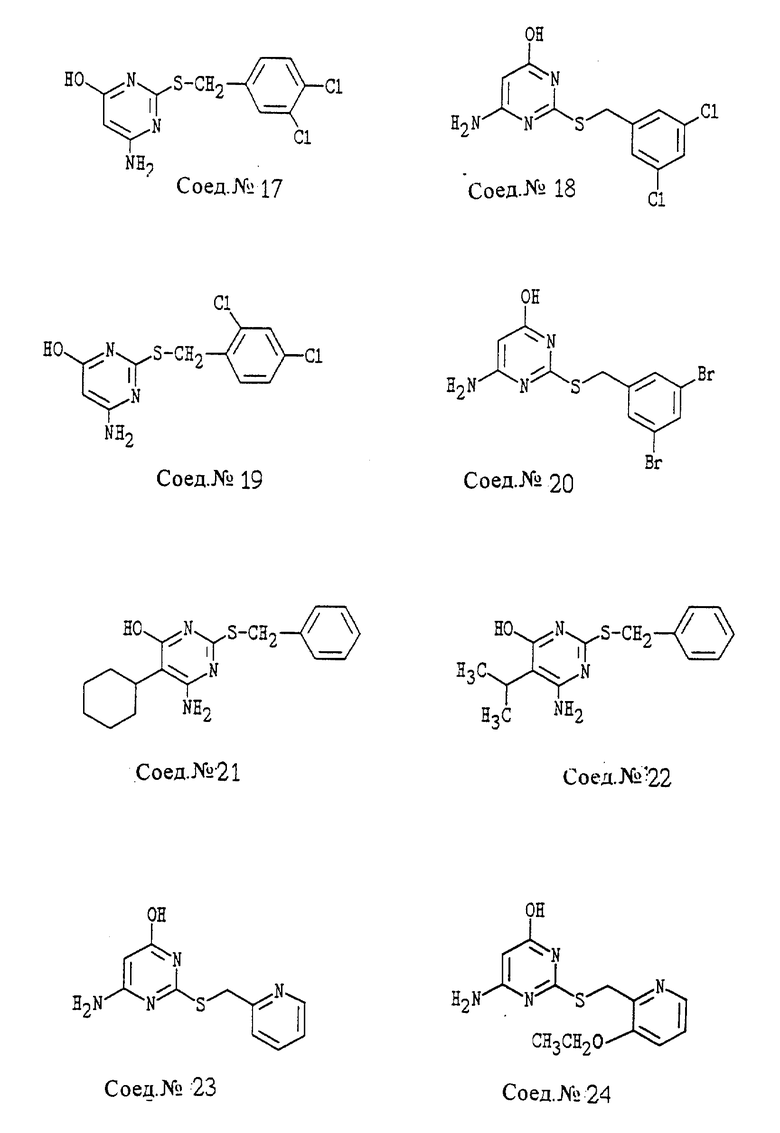


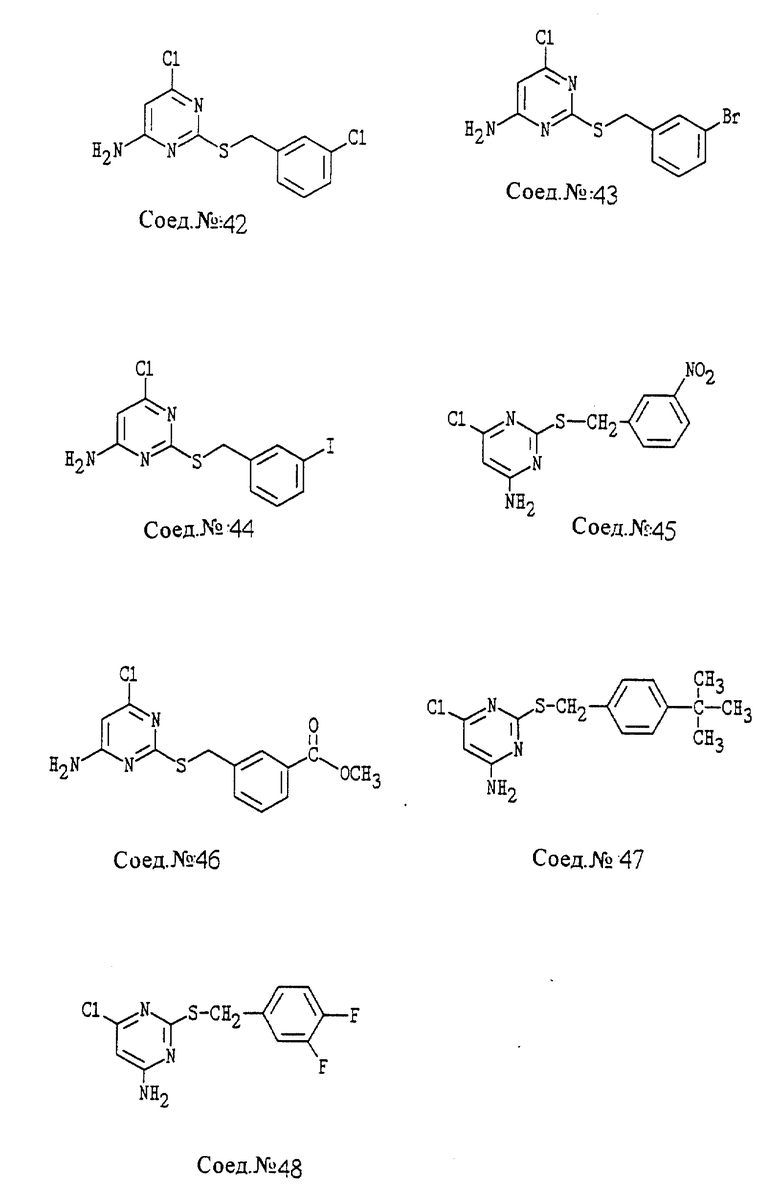
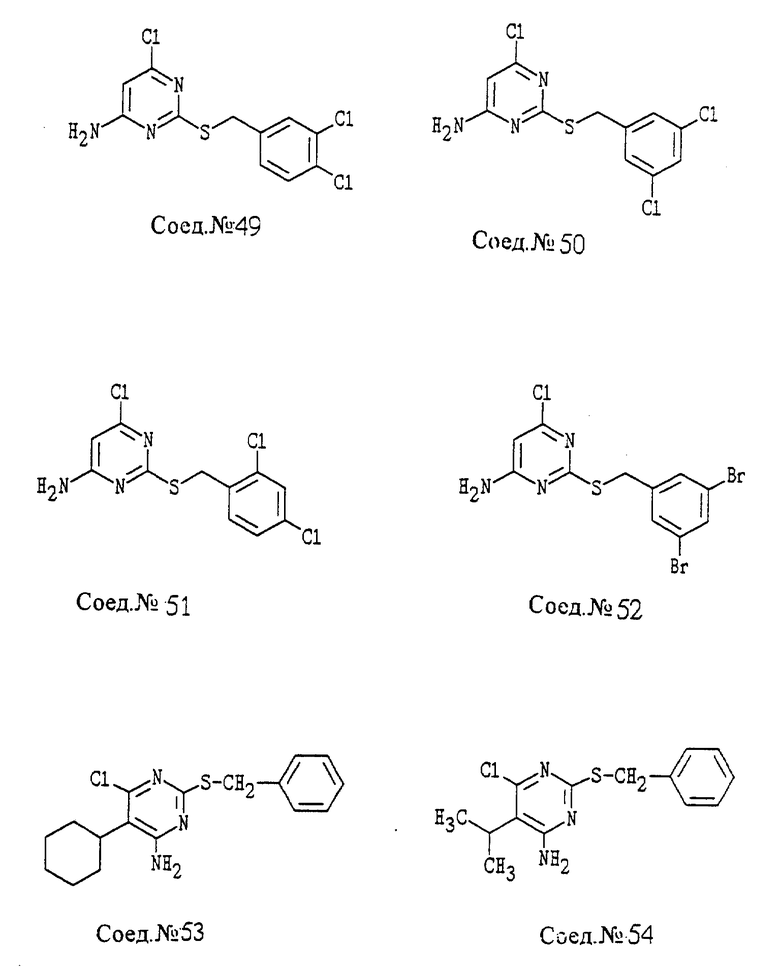

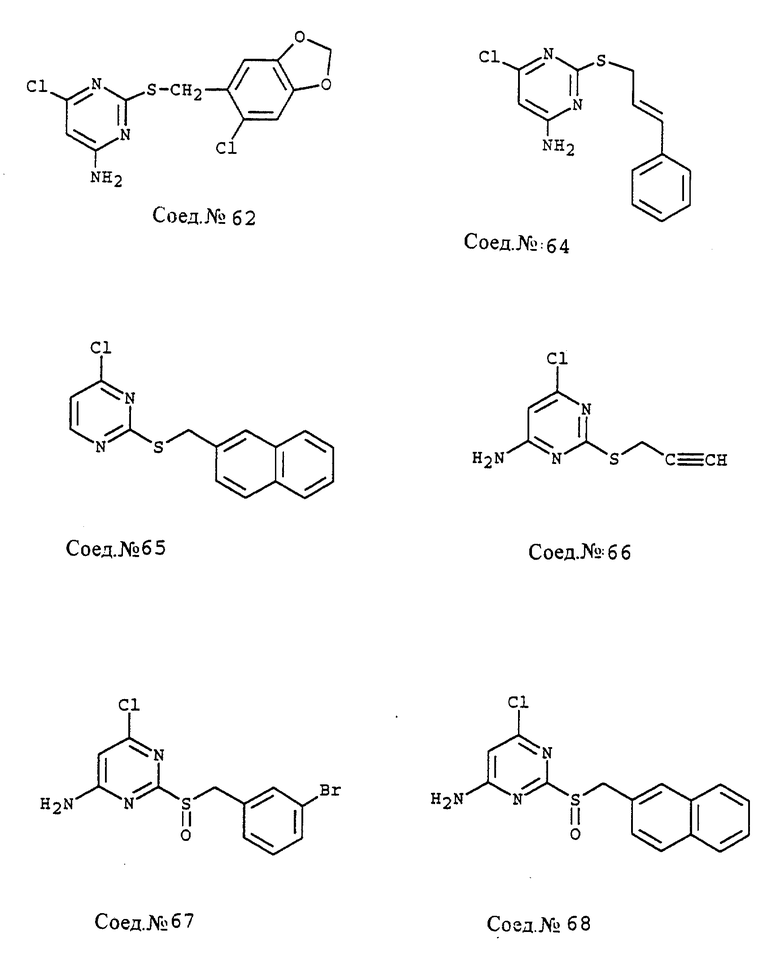
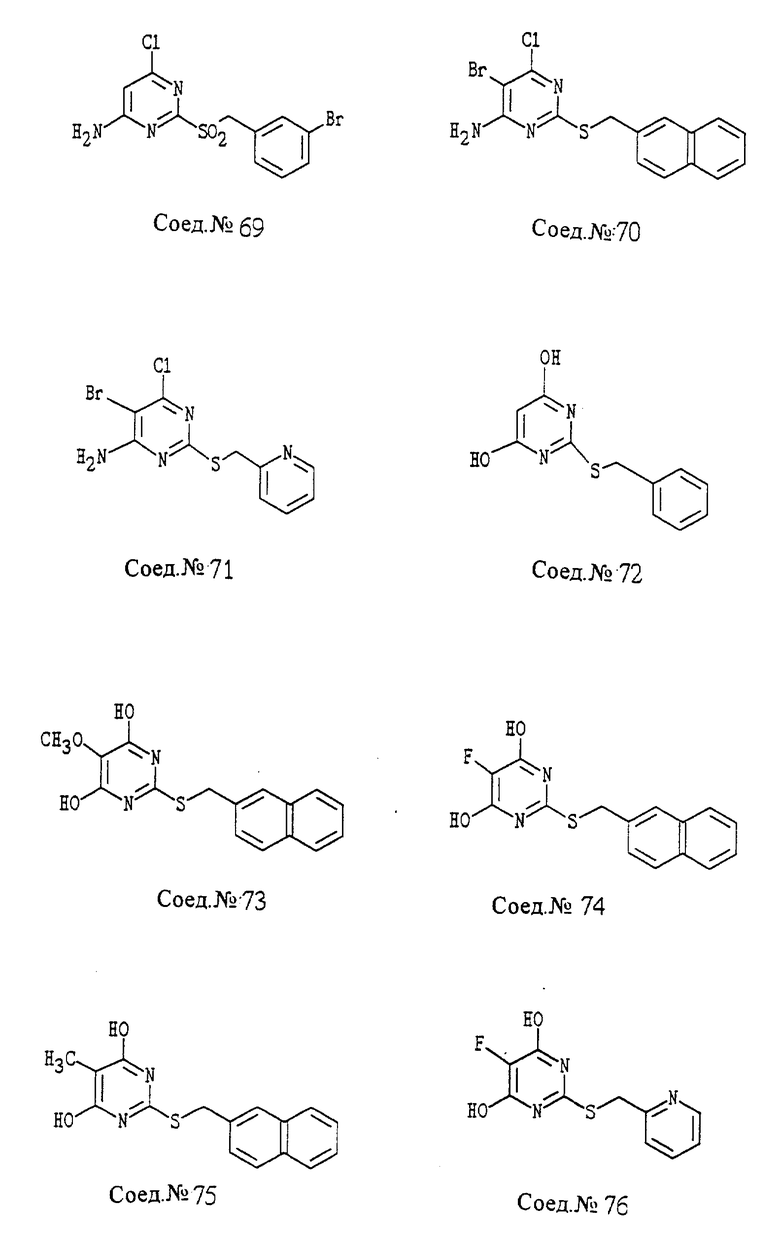

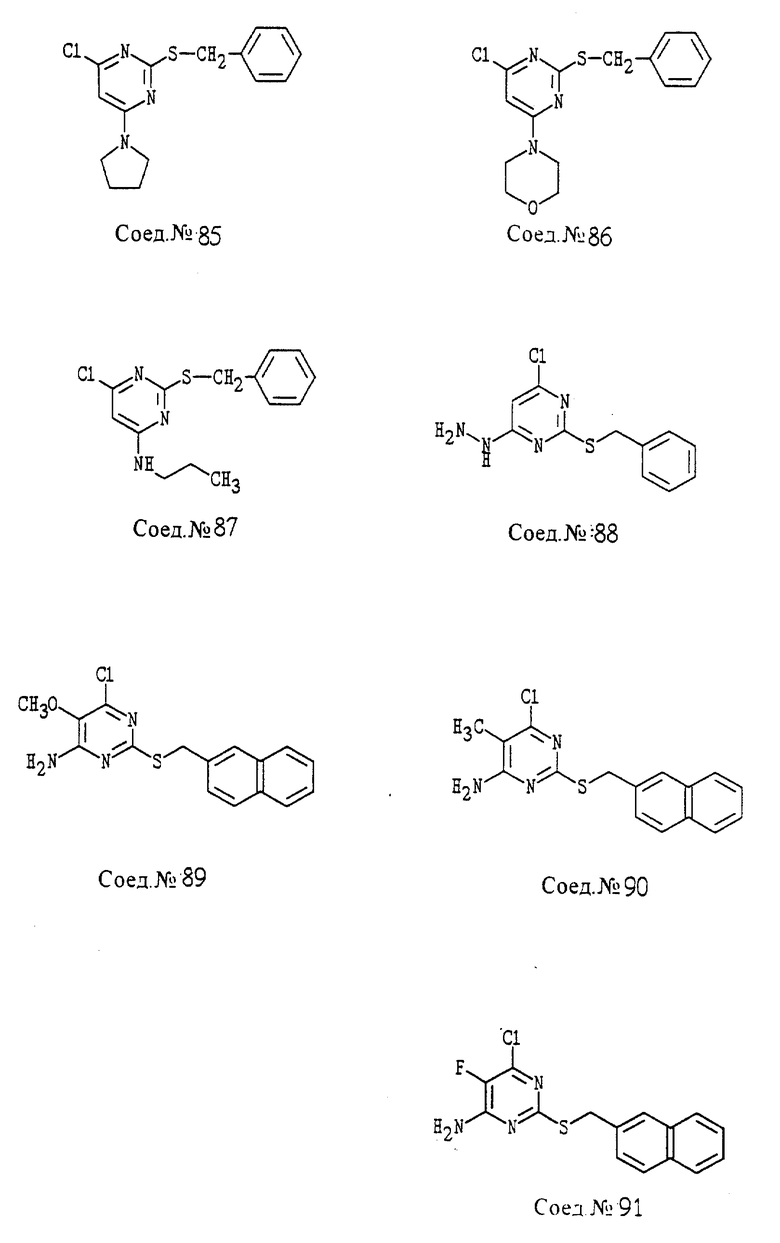
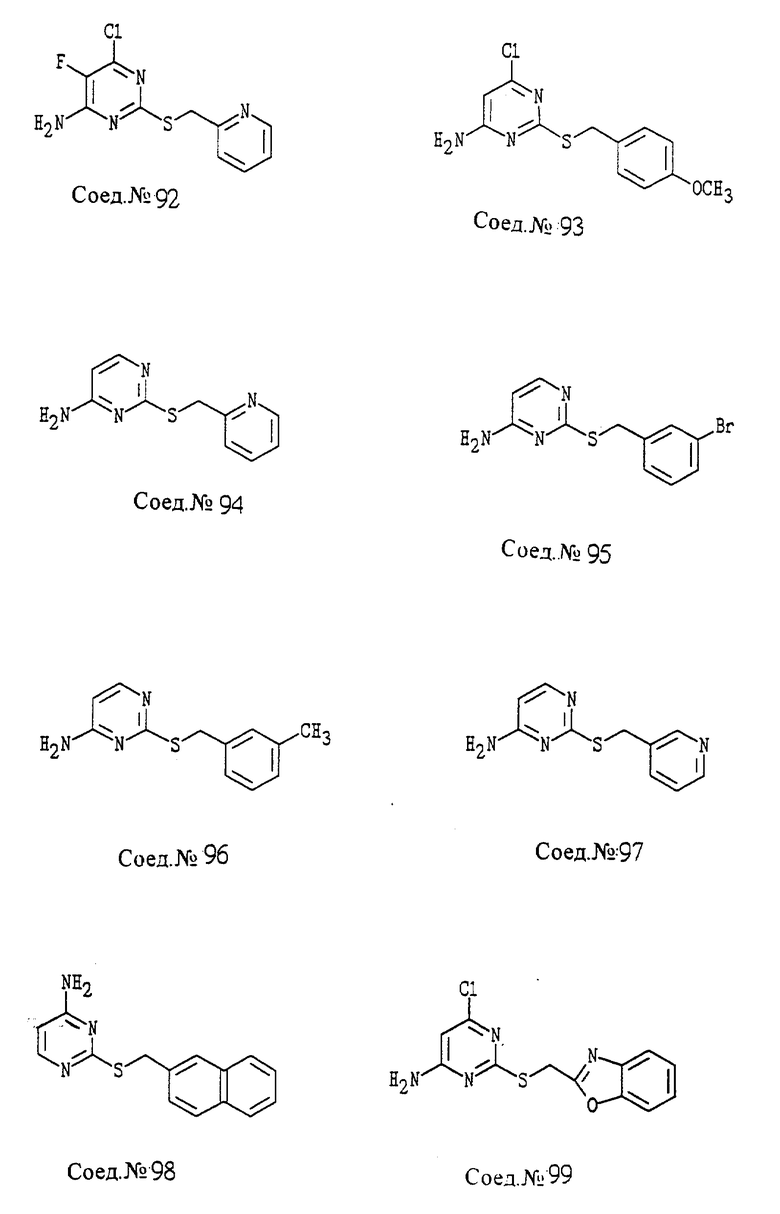
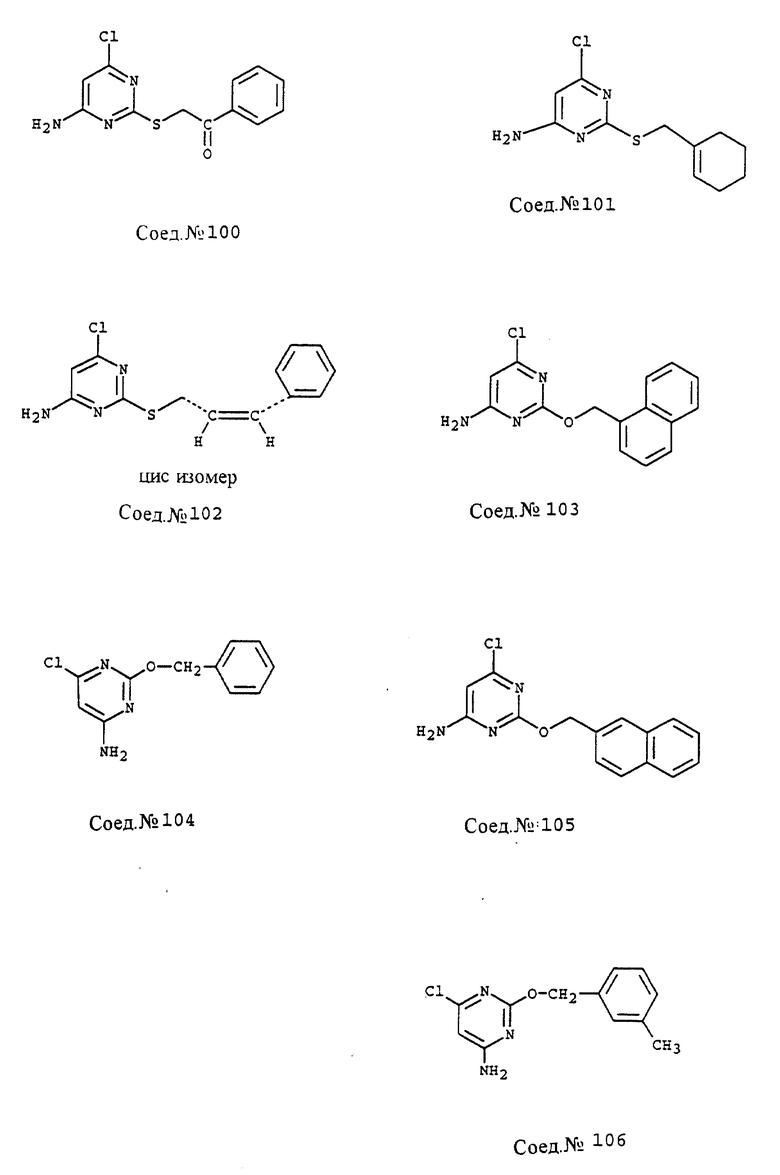
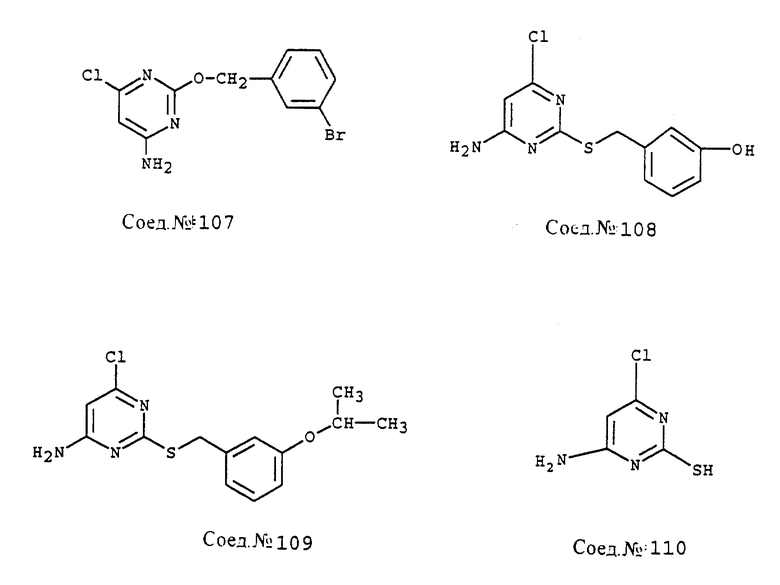
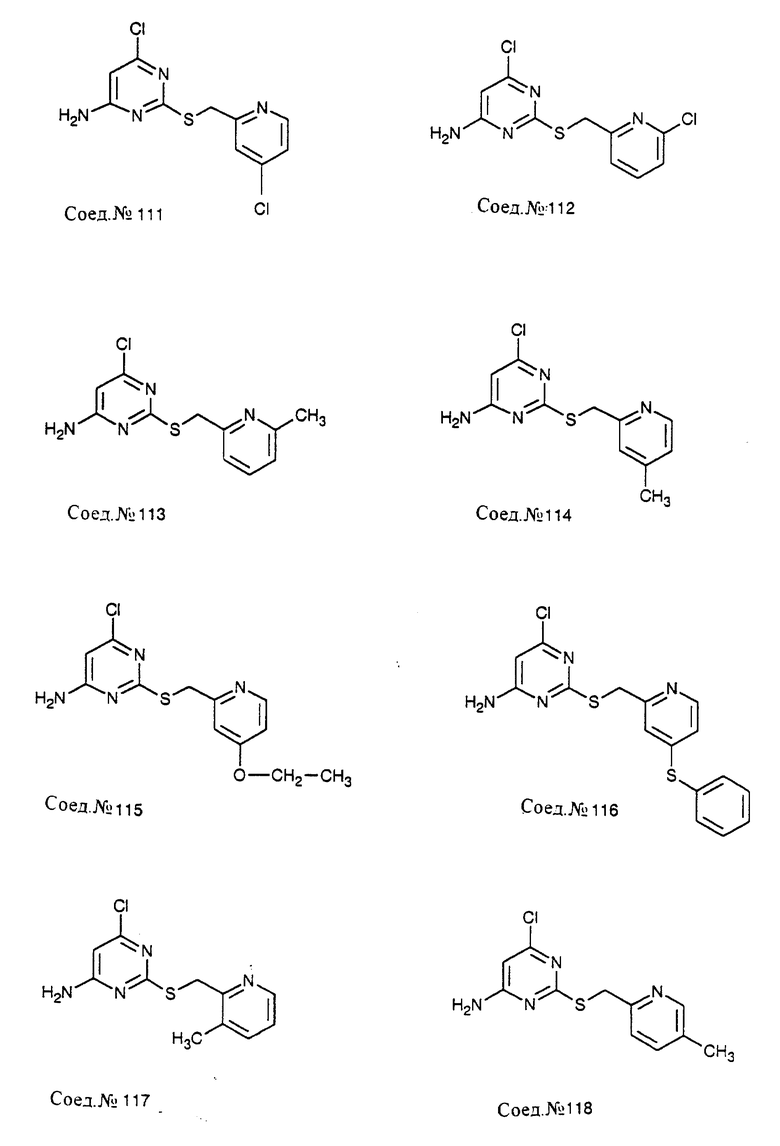
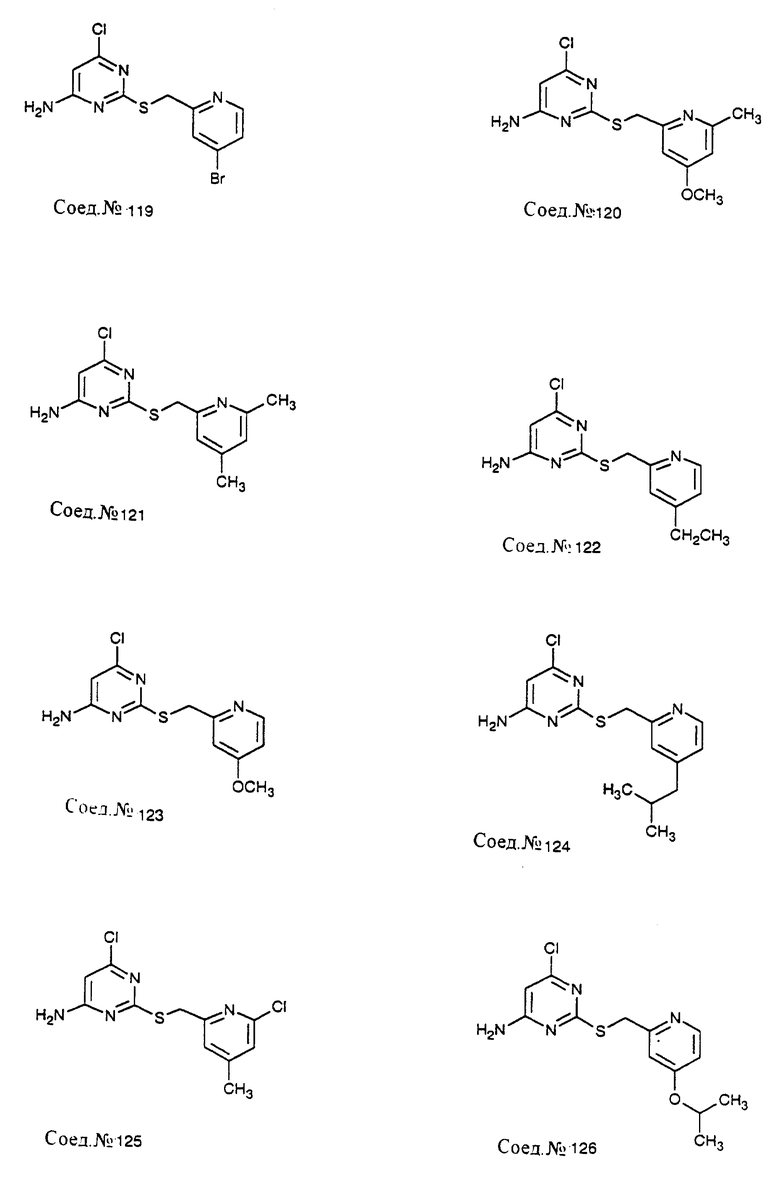
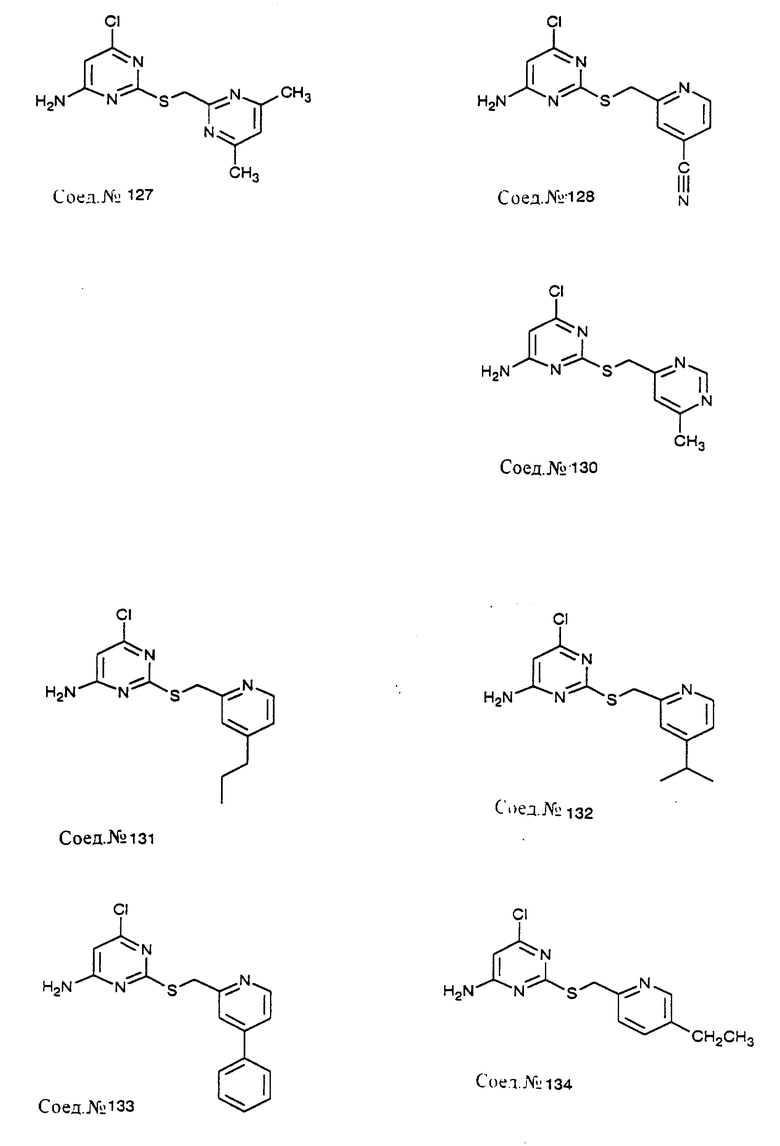
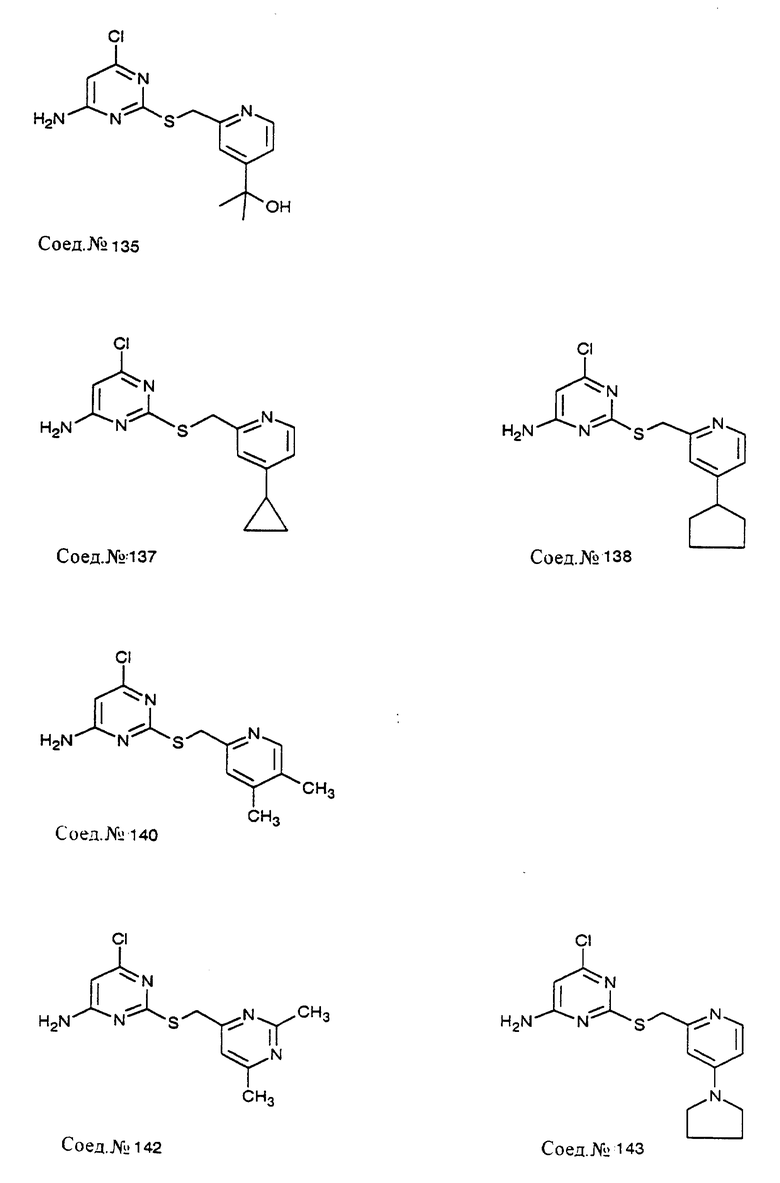
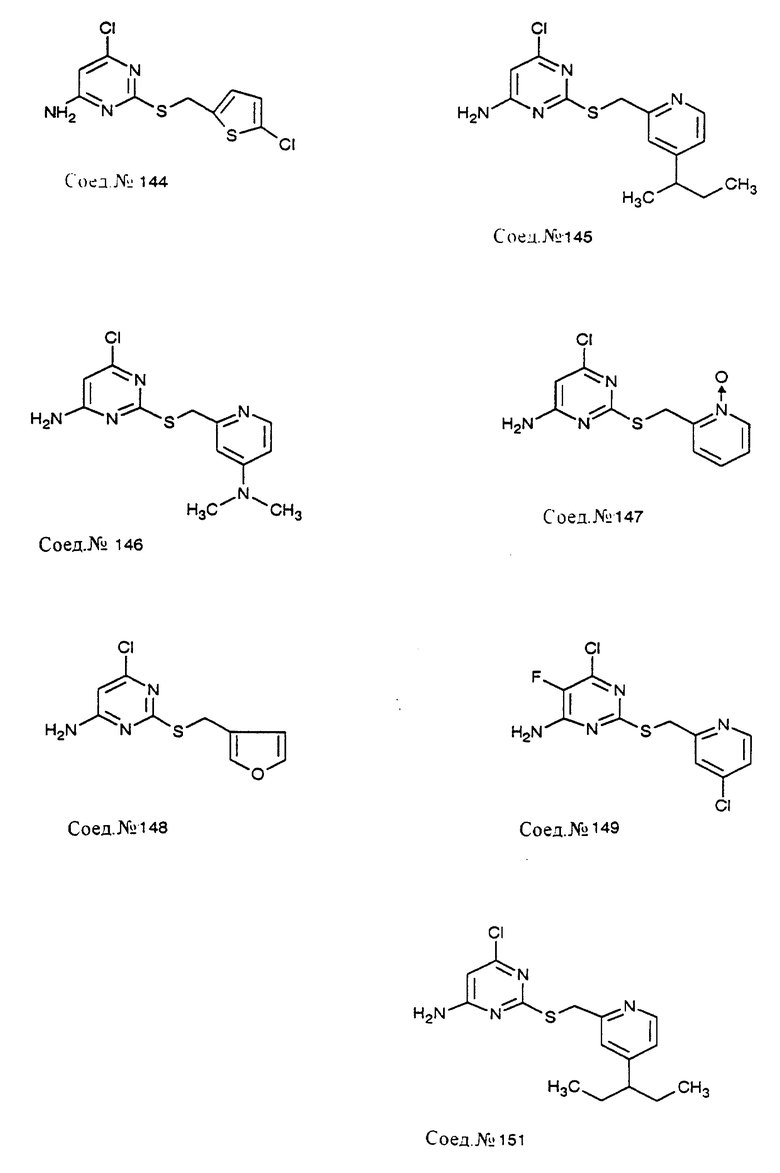
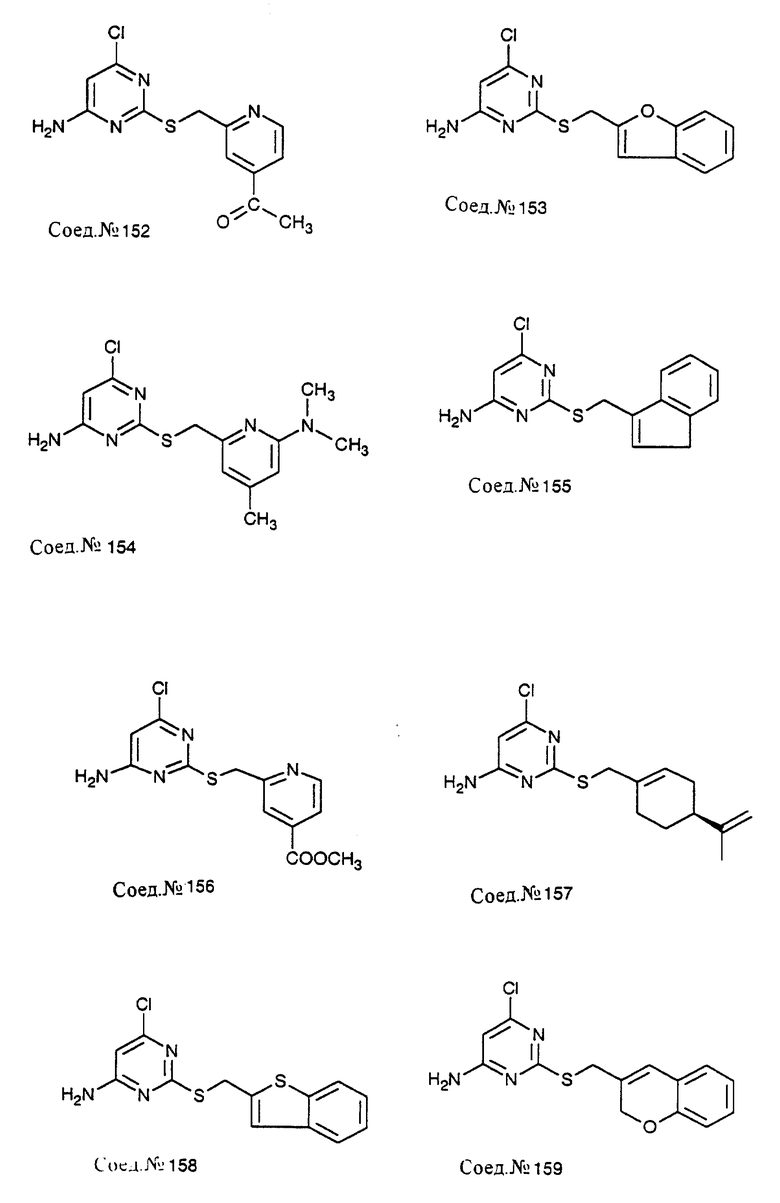
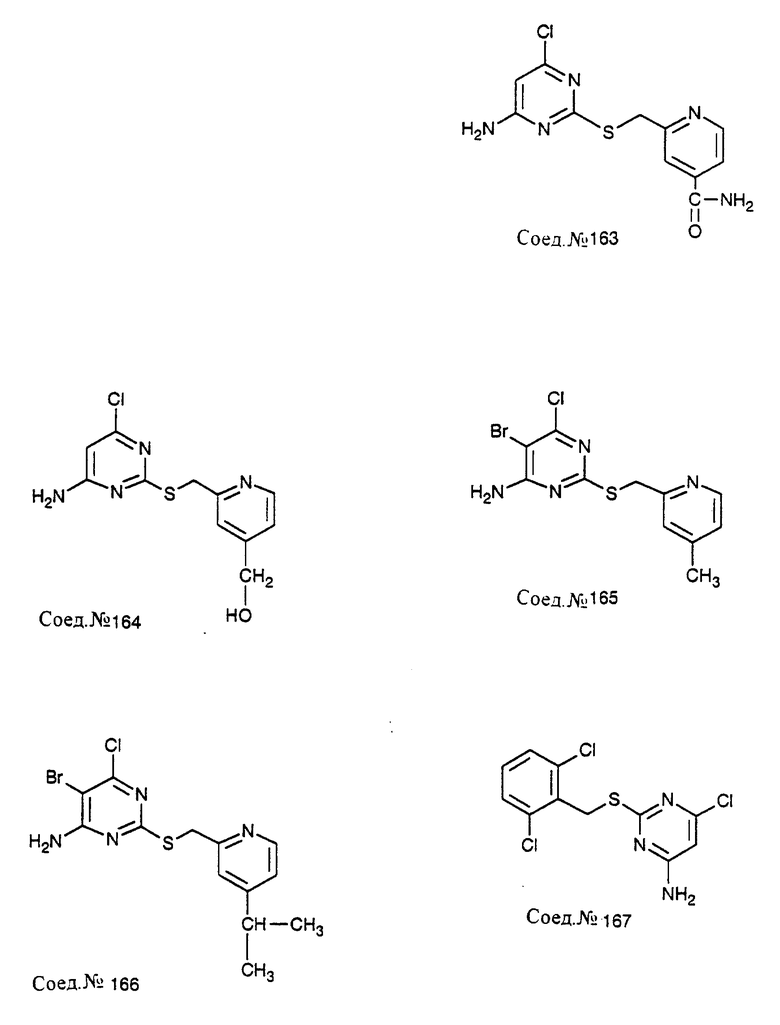
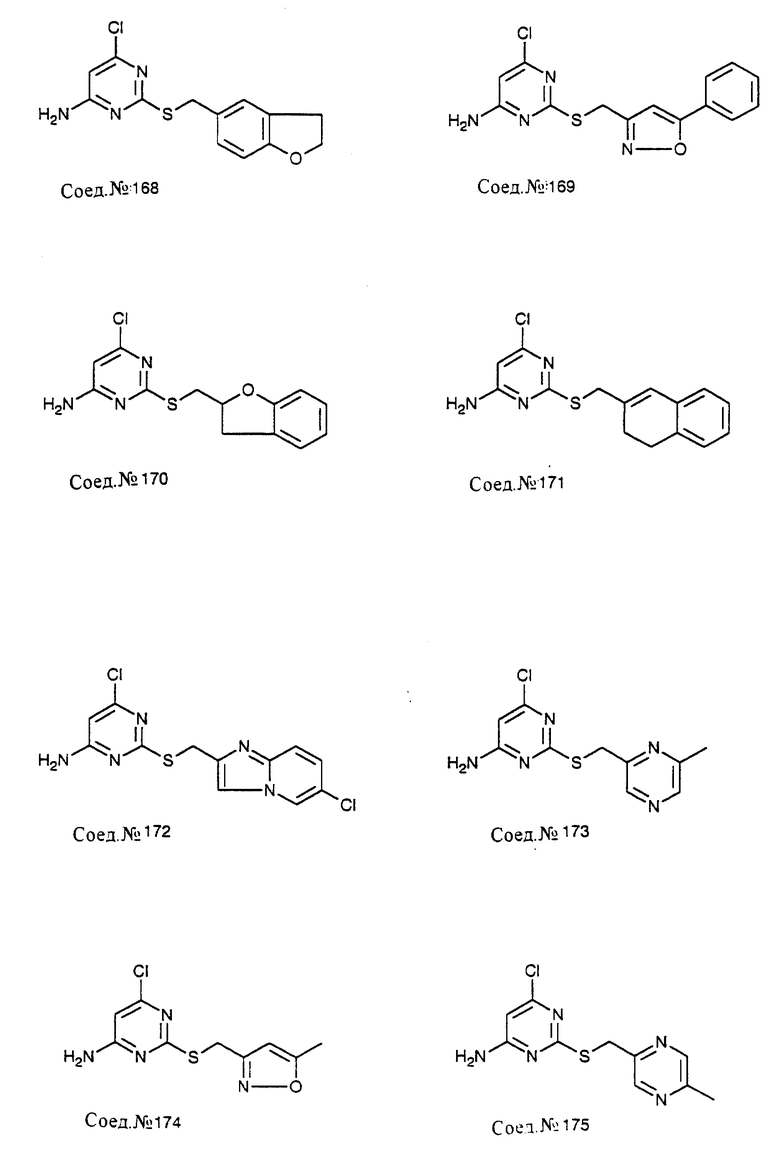
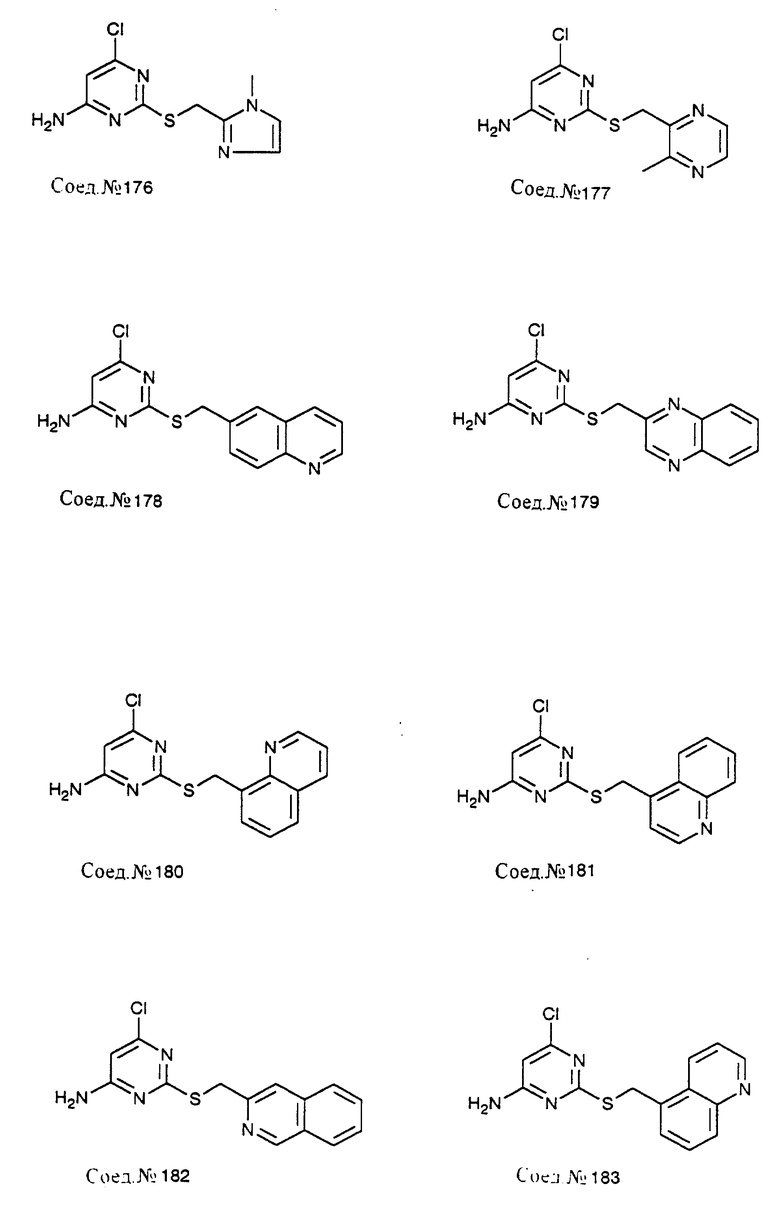
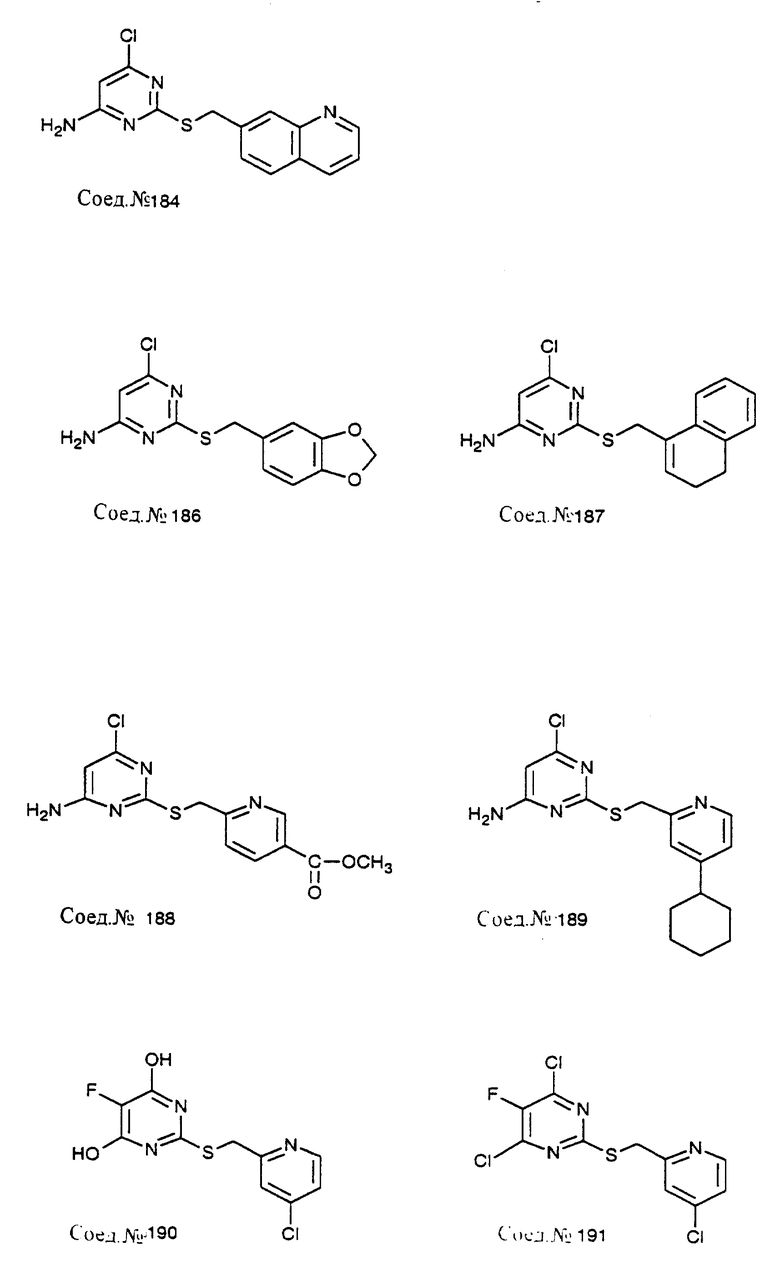

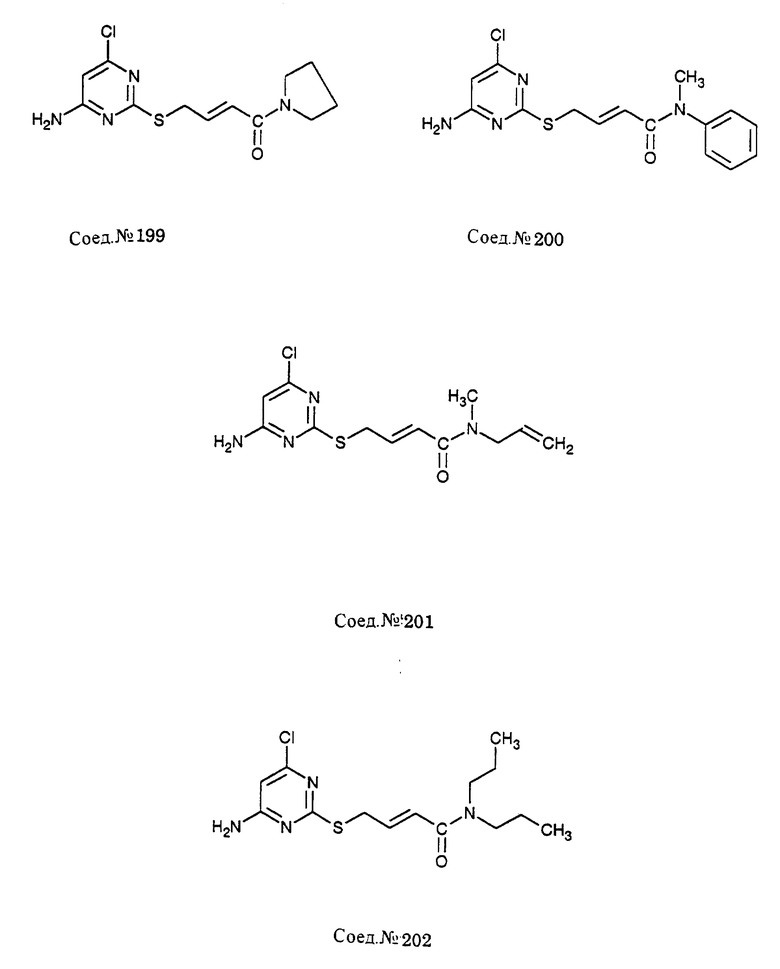
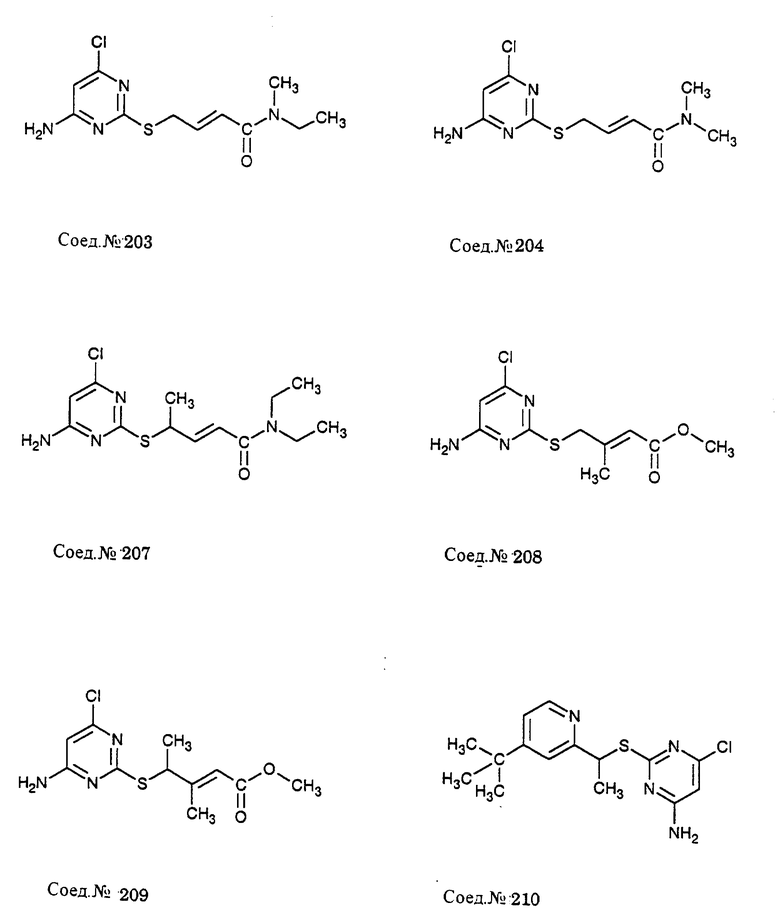
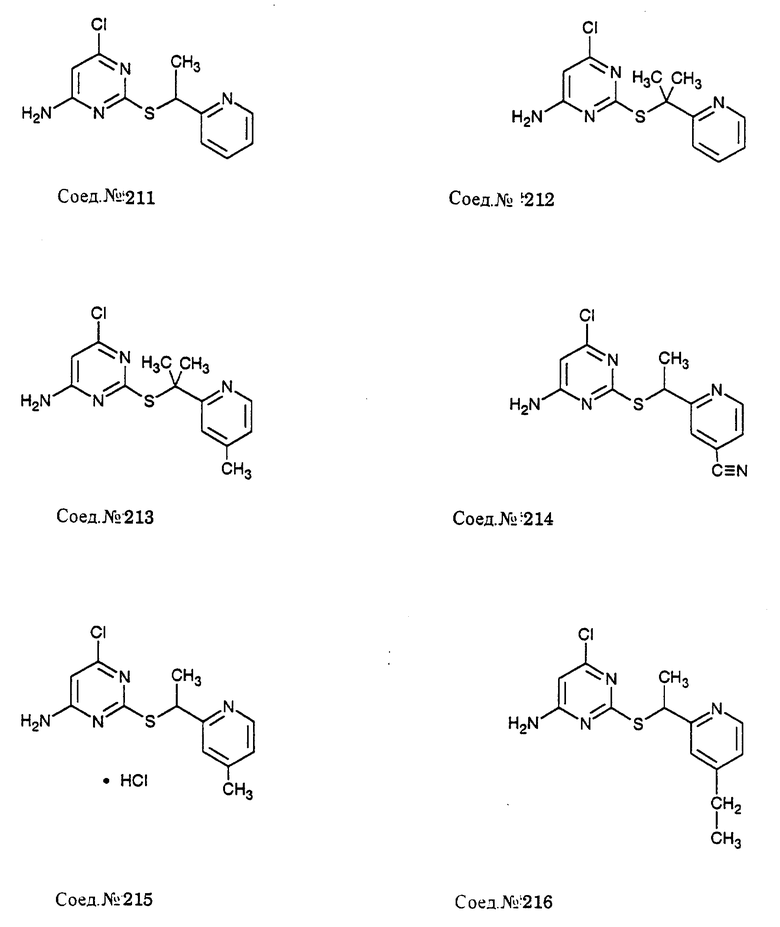


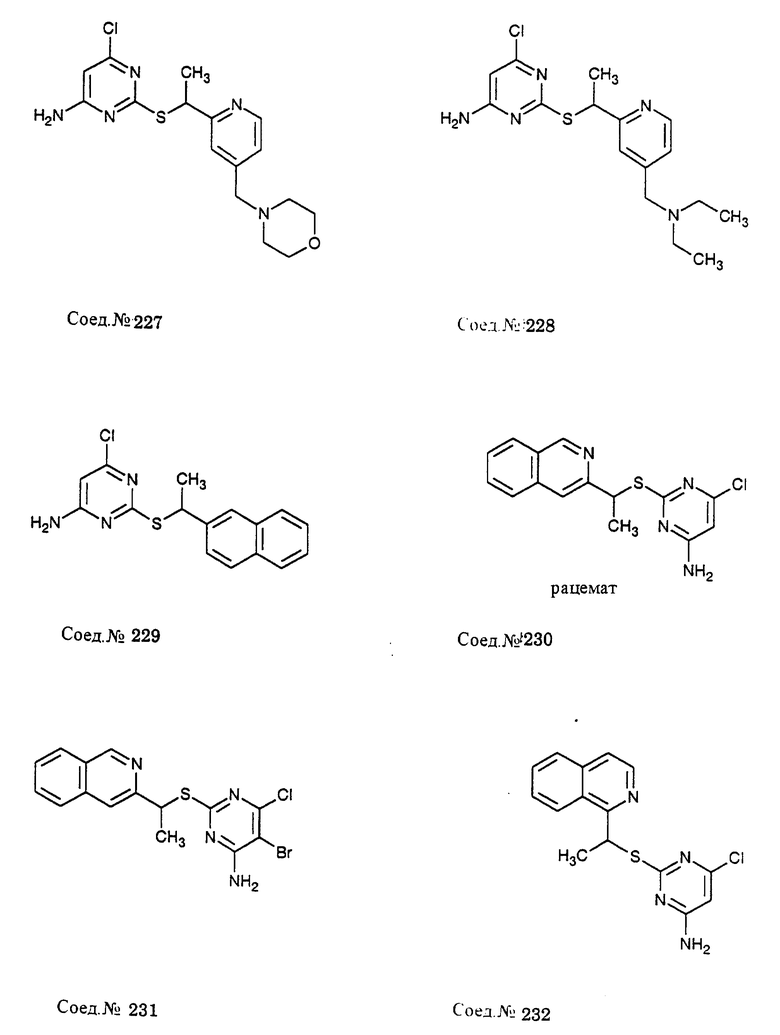
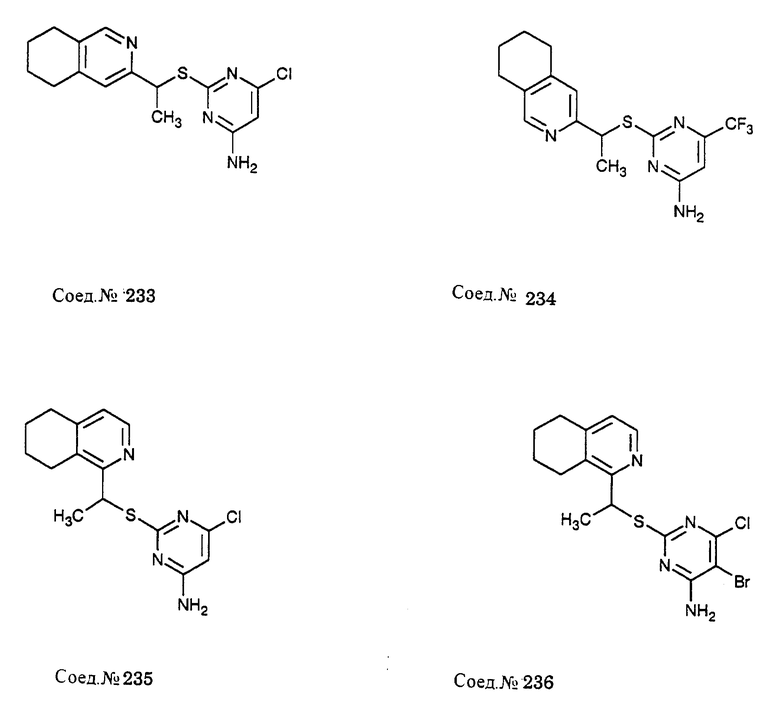
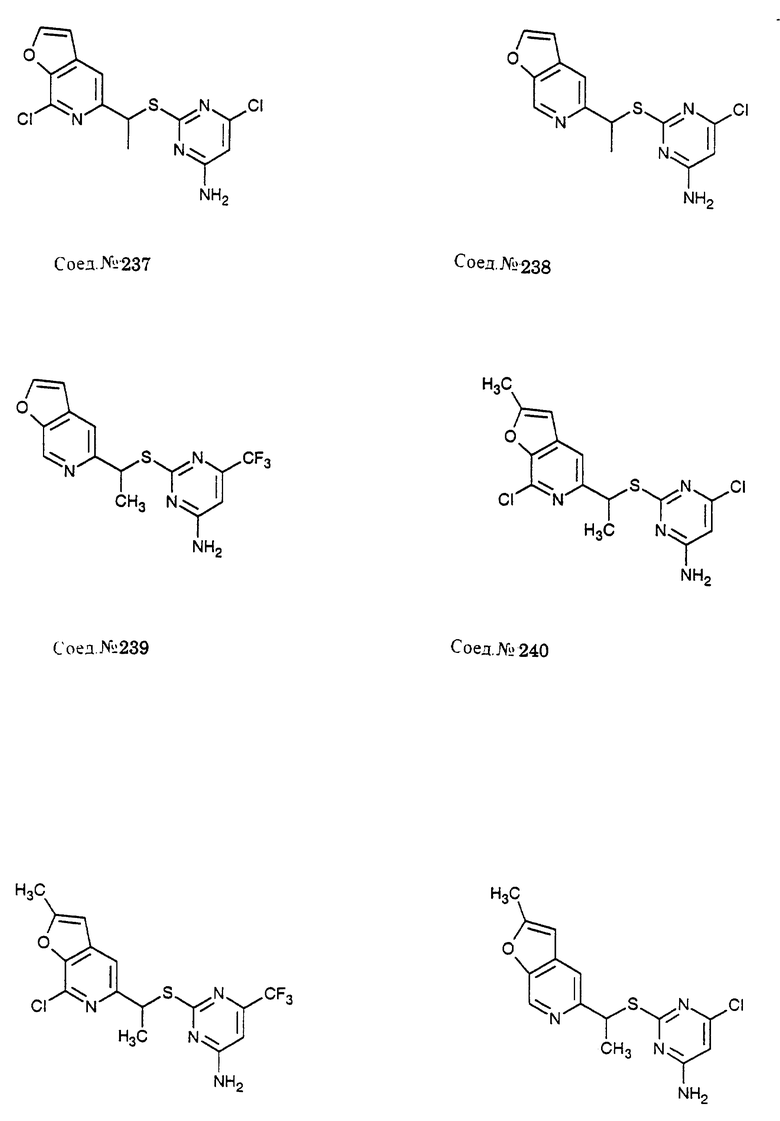
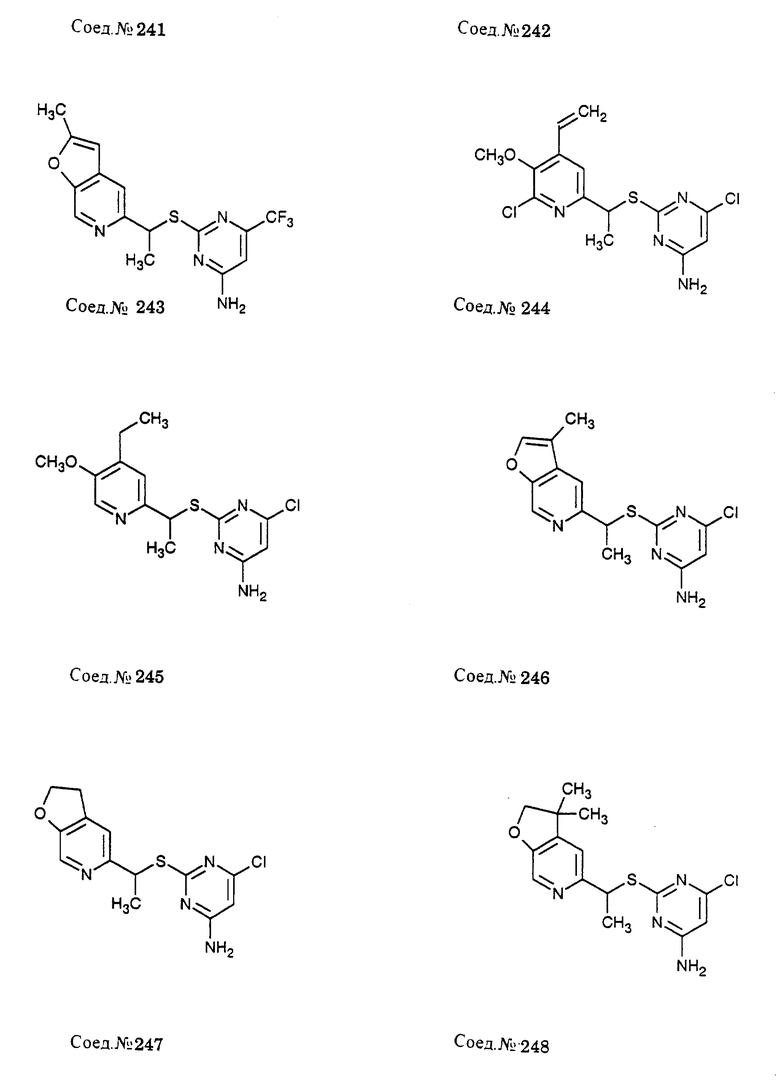
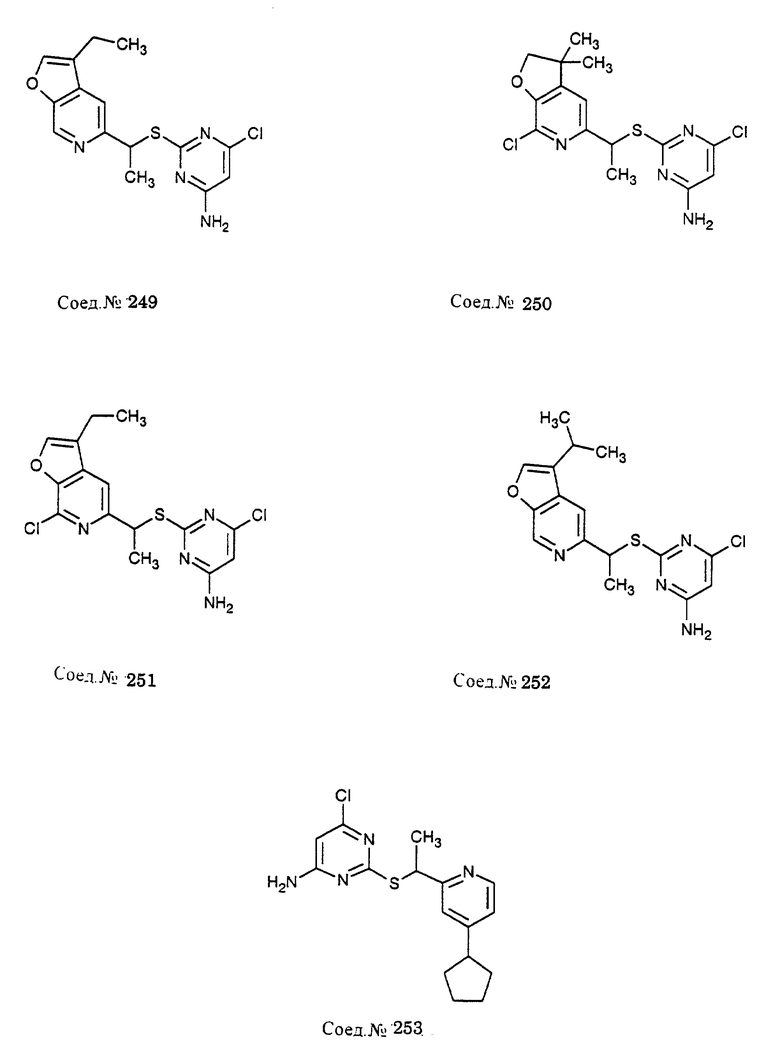
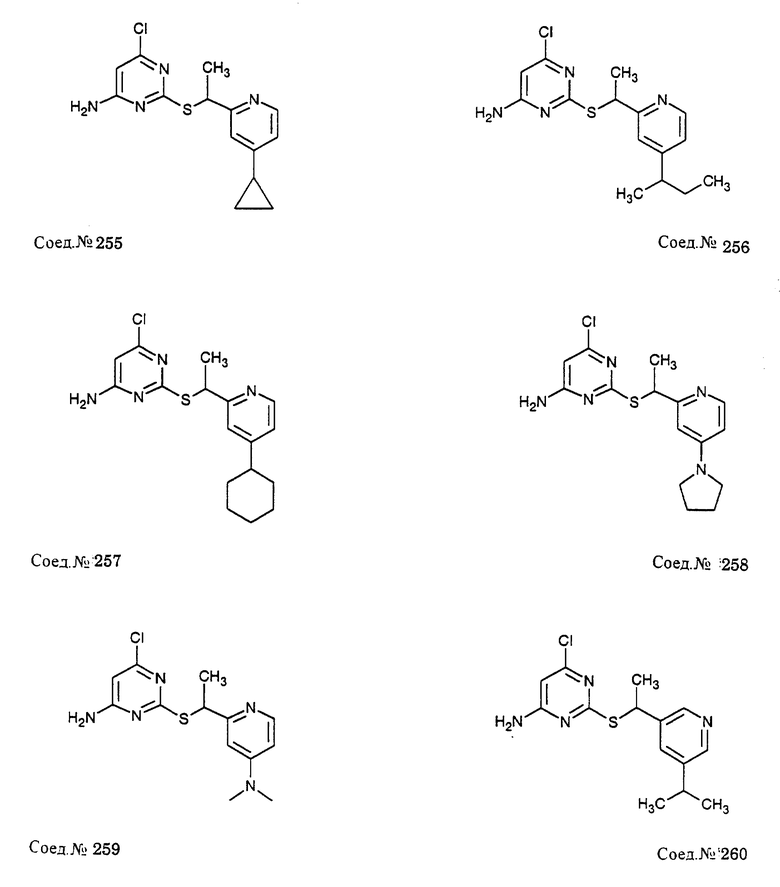
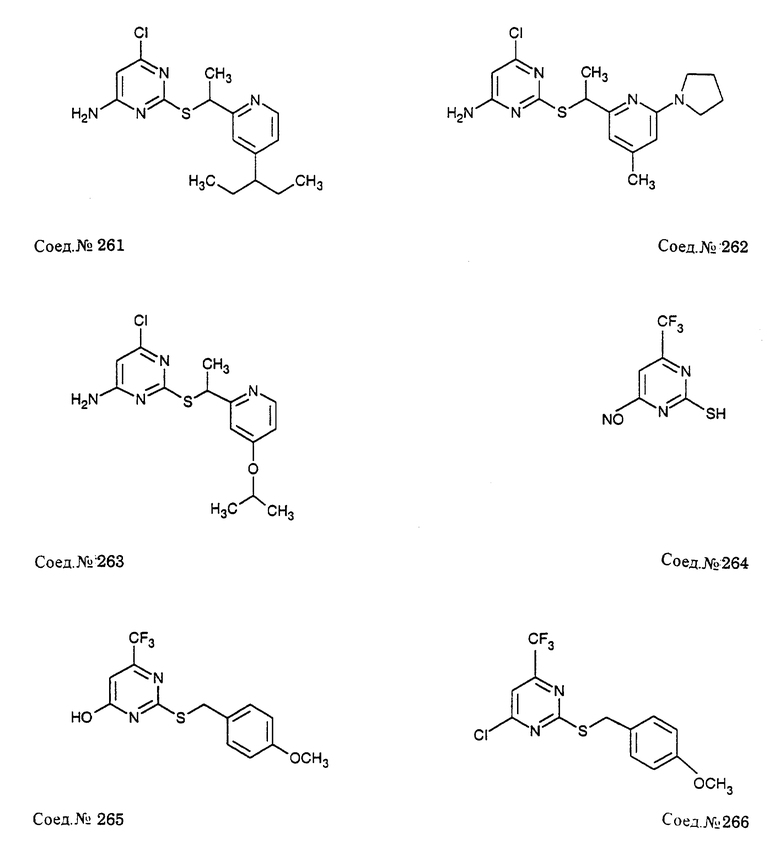

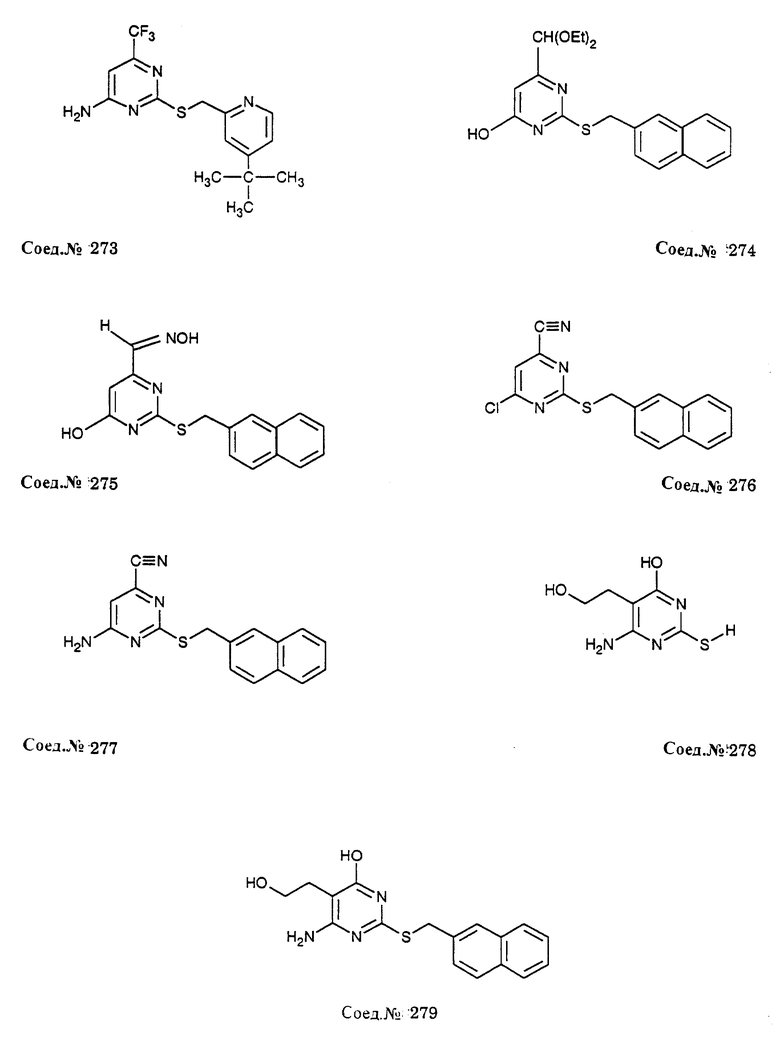
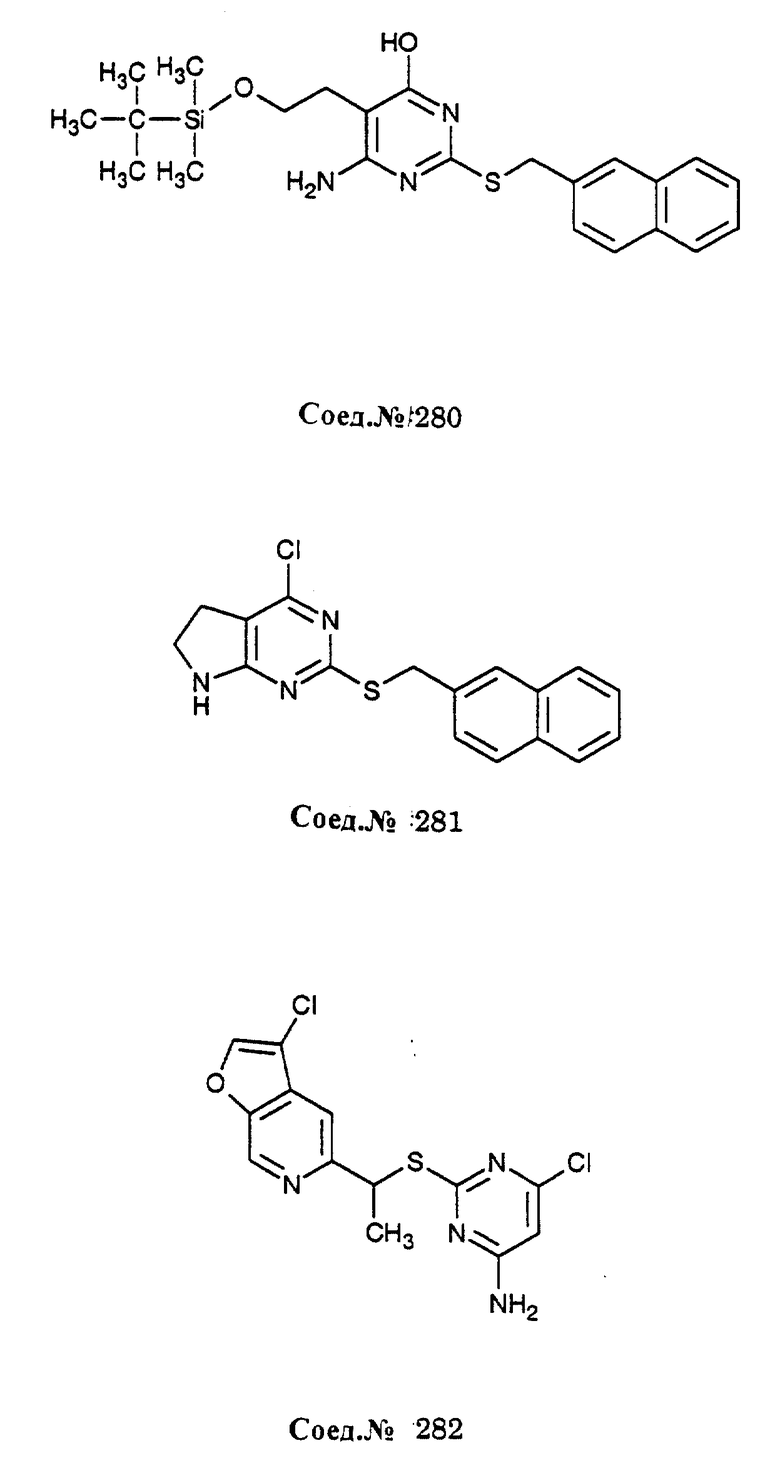
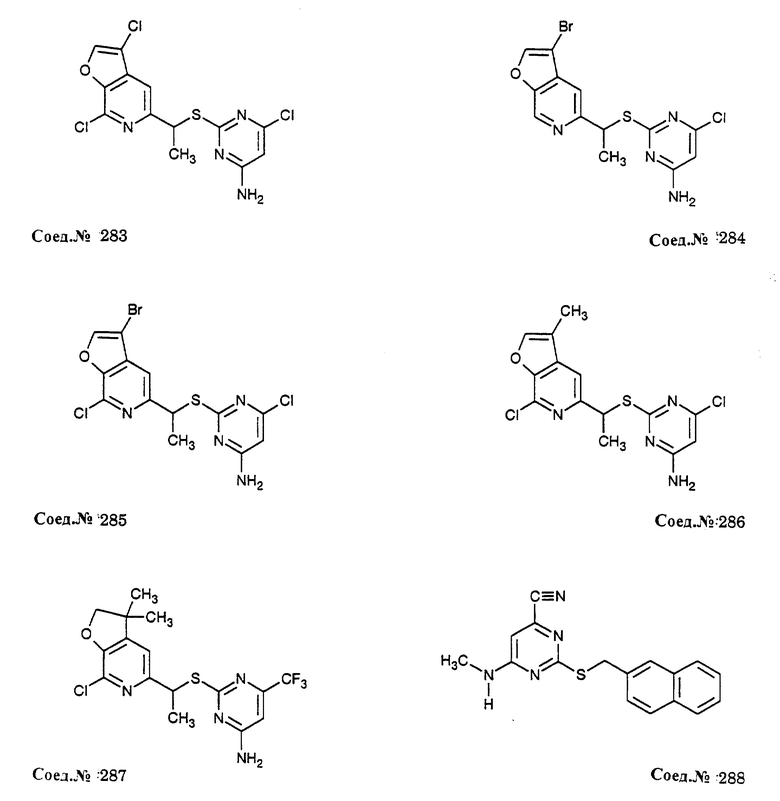
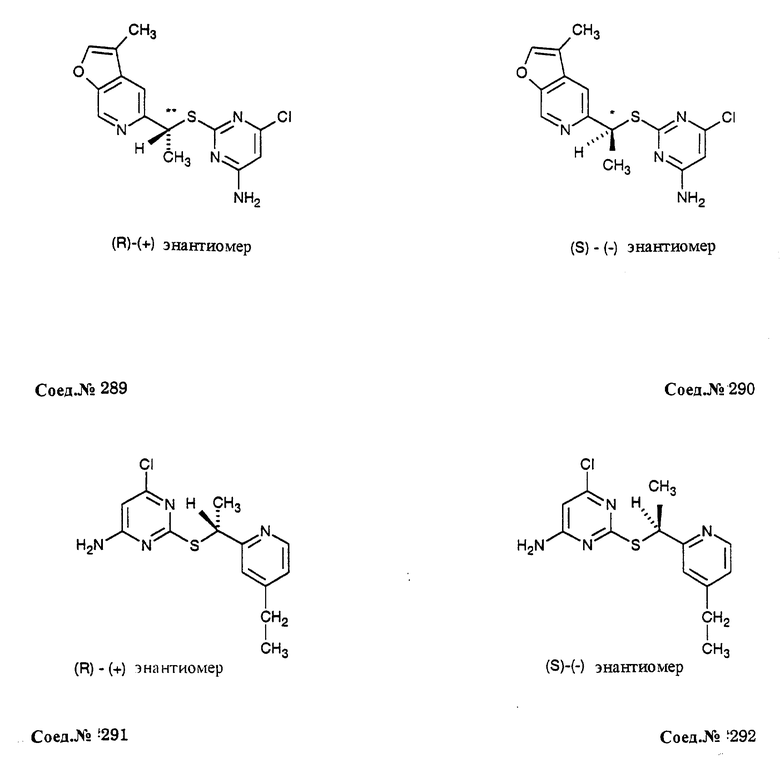
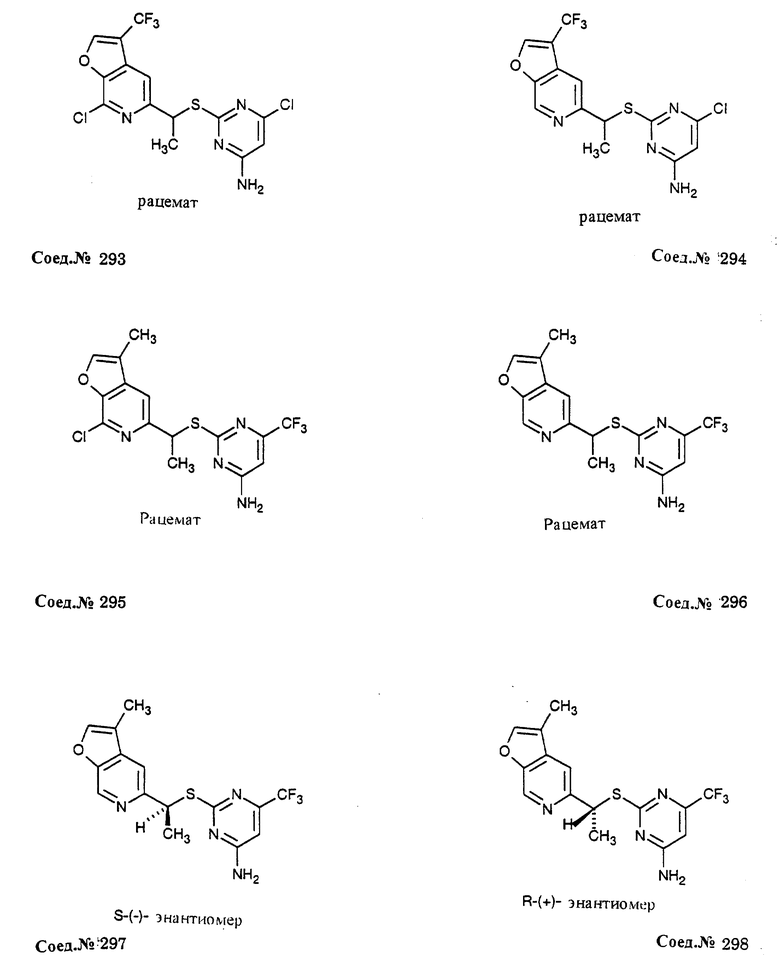
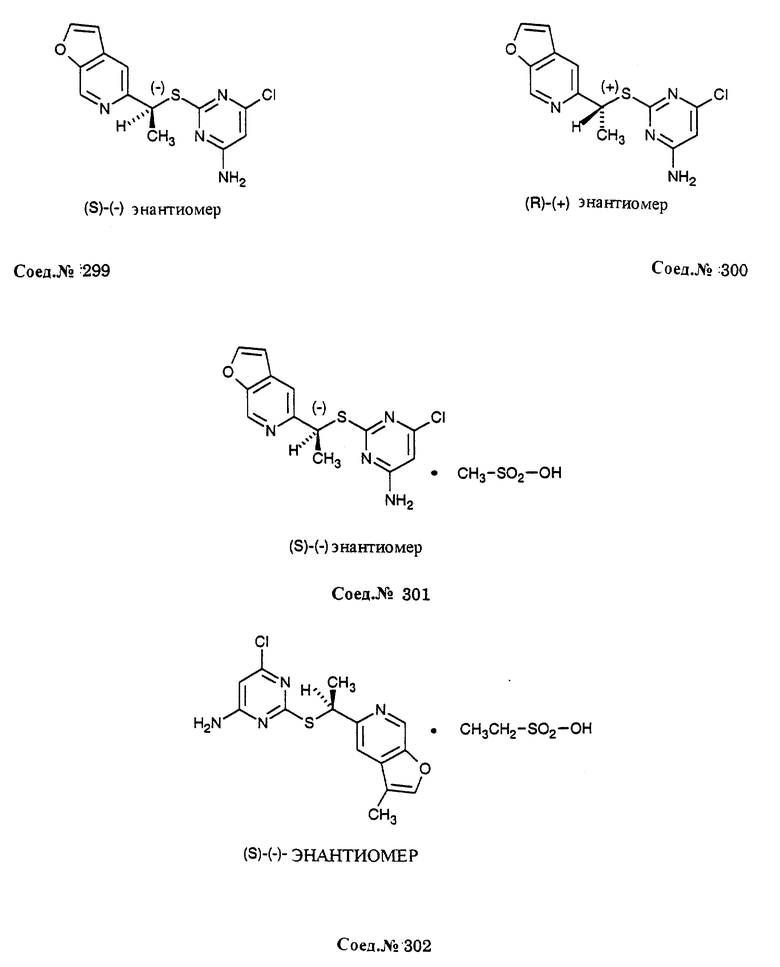

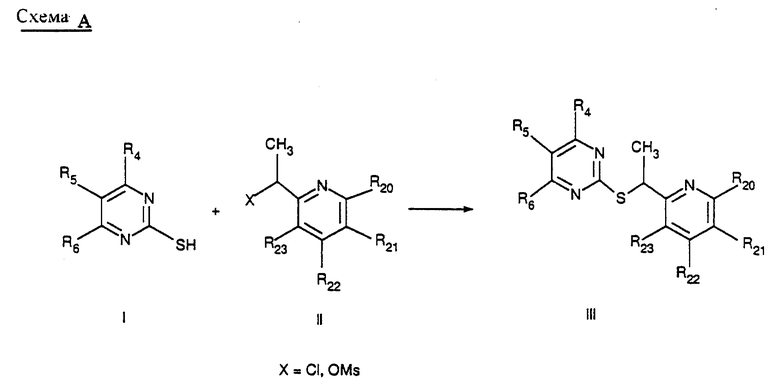
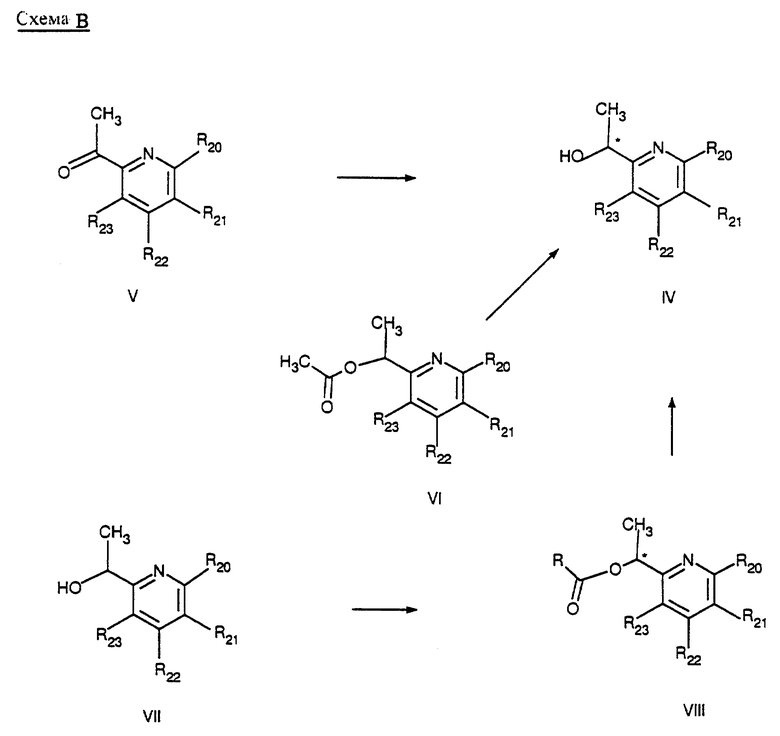
Изобретение относится к новым замещенным пиримидинтиоалкильным или алкилэфирным соединениям, их фармацевтически приемлемым солям, гидратам, N-оксидам и способу ингибирования обратной транскриптазы вирусов. Предлагаемые соединения могут быть использованы при лечении ВИЧ-инфицированных пациентов. Предлагаемые согласно изобретению соединения соответствуют общей структурной формуле I, где m = 0 или 1, R1 выбран из группы, состоящей из -C=CH,-CO2R53, -CONR54R55 или остатков формул А, В, С, значения радикалов в указанных группах приведены в формуле изобретения. Способ ингибирования обратной транскриптазы вирусов заключается во введении эффективного количества соединения формулы 1 по п.1. 2 c. и 18 з. п. ф-лы, 13 табл.
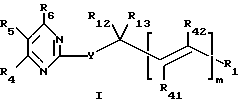
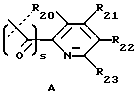
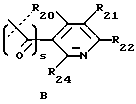

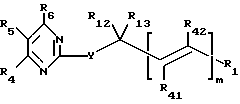
где m = 0 или 1;
R1 выбран из группы, состоящей из -C≡CH, -CO2R53, -CONR54R55,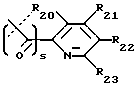
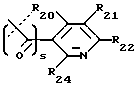
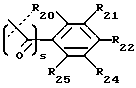
где s = 0 или 1;
R20, R21, R22, R23, R24 и R25 являются одинаковыми или различными и выбраны из -H, C1-C6 алкила, C1-C6 алкенила, C1-С6 алкокси, -С3-С6 циклоалкила, -СF3, -NO2, галогена, -ОН, -CN, фенила, фенилтио, стирила, -СО2(R31), -СОN(R31)(R32), -СО(R31), -(CH2)n-N(R31)(R32), -С(ОН)(R31)(R33), и R20 и R21, или R21 и R22, или R22 и R23, взятые вместе, образуют шести- или пятичленное насыщенное или ненасыщенное кольцо, содержащее 0 или 1 атом кислорода, азота или серы, где ненасыщенное кольцо может быть необязательно 1, 2 или 3 замещено C1-C6 алкилом, C1-C6 алкокси, -СН2OН, -СF3, галогеном, -СO2(R31), -CON(R31)(R32), -СО(R31), -(CH2)nN(R31)(CO(R33)), -(CH2)nN(R31)(SO2(R33)), -CN, -СН2СF3 или -СН(СF3)2 и насыщенное кольцо может быть необязательно 1, 2 или 3 замещено -C1-C6 алкилом, -C1-C6 алкокси, или - (CH2)n-N(R31)(R32), где n = 0 - 3, и R31, R32 и R33 являются одинаковыми или различными и выбраны из -H, C1-C6 алкила, или R31 и R32, взятые вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из пирролидинила, пиперидинила; или представителя группы, включающей: 1-циклогексенил, 2-пиримидинил, 4-пиримидини 5-пиримидинил, 2-имидазолил, 4-имидазолил, 2-бензотиазолил, 2-бензоксазолил, 2-бензимидазолил, 2-оксазолил, 4-оксазолил, 2-тиазолил, 3-изоксазолил, 5-изоксазолил, 5-метил-3-изоксазолил, 5-фенил-3-изоксазолил, 4-тиазолил, 3-метил-2-пиразинил, 5-метил-2-пиразинил, 6-метил-2-пиразинил, 5-хлор-2-тиенил, 3-фурил, бензофуран-2-ил, бензотиен-2-ил, 1-метилимидазол-2-ил, хиноксалин-2-ил, пиперон-5-ил, 4,7-дихлорбензоксазол-2-ил, 4,6-диметилпиримидин-2-ил, 4-метилпиримидин-2-ил, 2,4-диметилпиримидин-6-ил, 2-метилпиримидин-4-ил, 4-метилпиримидин-6-ил, 6-хлорпиперон-5-ил, 5-хлор-имидазо[1,2-а]пиридин-2-ил, 1-Н-инден-3-ил, 1-Н-2-метил-инден-2-ил, 3,4-дигидронафт-1-ил, S-4-изопропенил-циклогексен-1-ил- или 4-дигидронафт-2-ил;
R53 выбран из группы, включающей -H, C1-C6 алкил, алкокси;
R54 и R55 могут быть одинаковыми или различными и выбраны из -H, C1-C6 алкила, аллила или, взятые вместе с атомом азота, к которому они присоединены, образуют кольцо, выбранное из пирролидинила, пиперидинила;
R12 и R13 выбран из группы, состоящей из -H, C1-C6 алкила;
Y выбран из -S-, -S(O)-, -S(O)2;
R4 выбран из группы, состоящей из -H, -ОН, галогена или -NR15R16, где R15 является -H и R16 является -H, C1-C6 алкилом, -NH2, или R15 и R16, взятые вместе с -N, образуют 1-пирролидино, 4-морфолино или 1-пиперидино;
R5 выбран из группы, состоящей из -H, галогена, C3-C6 циклоалкила, C1-C4 алкила или C1-C3 алкокси;
или R4 и Rs, взятые вместе, образуют пяти- или шестичленное насыщенное или ненасыщенное кольцо, которое вместе с пиримидиновым кольцом образует группу, включающую: фуро[2,3-d]пиримидин, 5,6-дигидрофуро[2,3-d]-пиримидин, где ненасыщенное кольцо может быть необязательно 1, 2 или 3 замещено C1-C6 алкилом, -СF3, галогеном, -СO2(R31), -CON(R31)(R32), -(CH2)nN(R31)(SO2(R33)), и насыщенное кольцо может быть необязательно 1, 2 или 3 замещено C1-C6 алкилом, C1-C6 алкокси;
R6 выбран из группы, состоящей из -H, -OН, галогена, -CN, -СF3, при общем условии, что R4 и R6 не являются оба -H; и со следующим условием, что и R12 и R13 не являются оба -H, за исключением случая, когда R6 выбран из -CN, -СF3, или R1 выбран из -CO2R23 или -C(O)N(R54)(R55);
при общем условии, что, когда R1 не является 2- или 3-пиридинилом, необязательно замещенным C1-C4 алкилом, атомом галогена, -NH2 или -ОН, тогда m = 0, Y является S, R13 является -H, R12 является -H или C1-C4 алкилом, R4 является -H, -ОН, галогеном или NH2, R5 является -H, галогеном или C1-C4 алкилом, и R6 образует группу, содержащую -H, галоген или -ОН;
их фармацевтически приемлемые соли, гидраты, N-оксиды за исключением 4-амино-6-хлор-2-(1-(4-(4-морфолинилкарбинил)-2-пиридинил)этил)тиопиримидина и 4-амино-6-хлор-2-(1-(4-метил-2-пиридил)пентил)тиопиримидина.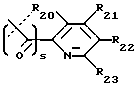
6. Соединение по п.5, где R4 является -NH2, R5 является -H, и R6 является -Сl, -СF3 или -CN.
и их фармацевтически приемлемые соли, гидраты, N-оксиды и сольваты.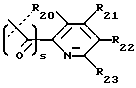
17. Способ по п.16, отличающийся тем, что R4 является -NH2, R5 является -H, и R6 является -Сl, -СF3 или -CN.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| БИБЛИОТЕКА \ | 0 |
|
SU391254A1 |
| 0 |
|
SU276825A1 | |
| Прибор для вычерчивания логарифмических спиралей | 1959 |
|
SU124630A1 |
| US 5025016 A, 18.06.1991 | |||
| US 3940394 A, 24.02.1976 | |||
| ТОРМОЗНАЯ ЖИДКОСТЬ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2004 |
|
RU2295560C2 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| WO 9507901 A1, 23.03.1995 | |||
| US 3940240 A, 24.06.1969 | |||
| СПОСОБ НАЛОЖЕНИЯ ПИЩЕВОДНО-ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА НА ШЕЕ ПРИ ЭЗОФАГОПЛАСТИКЕ | 2004 |
|
RU2266716C1 |
| SAIDA M | |||
| ET AL | |||
| Preparation of quinazolines for neoplasm inhibitor or skin preparation | |||
| CHEMICAL ABSTRACTS, Columbus Ohio, US, 1994 v.121, № 9 | |||
| OTA M | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| CHEMICAL ABSTRACTS, Columbus Ohio, US, l988, y.l08, №21 | |||
| SCHICKANEDER H | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J.MED.CHEM.Washmgton,1987,v.30, p.547-551 | |||
| MONTGOMERY J.A | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J.Am.Chem | |||
| Soc | |||
| Washington, 1959, v.81, p.3962-3969 | |||
| JIANG J.B | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J | |||
| .MED.CHEM | |||
| Washington, 1990, v.33, p.1721-1728 | |||
| SAARI W | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J.MED.CHEM | |||
| Washington, 1991, v.34, № 9, p.2922-2925 | |||
| GOLDMAN V.E | |||
| ET AL | |||
| Pyridinone Derivatives: Specific human immunodeficiency virus type reverse ingibitors with antiviral activity | |||
| PROC.NATL.ACAD.SCI.USA, Washington, 1991, v.88, p.6863-6867. | |||
Авторы
Даты
2001-05-20—Публикация
1996-05-03—Подача