Предлагаемое изобретение относится к способам получения новых непредельных циклоолигомерных углеводородов, конкретно к способу получения макроциклов с чередующимися алка-1Z,5Z-диеновыми фрагментами общей формулы (1):
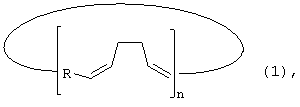 где R=(CH2)4, (CH2)5, (CH2)6; n=3-5
где R=(CH2)4, (CH2)5, (CH2)6; n=3-5
Предлагаемые соединения могут найти применение в синтезе биологически активных препаратов для медицины и животноводства, а также парфюмерной промышленности.
Известен способ (Г.А.Толстиков, У.М.Джемилев, С.С.Шаванов. К вопросу о получении циклотетрамеров бутадиена на комплексных никелевых катализаторах // Изв. АН СССР, Сер. хим., 1975, №11, С.2624) получения циклоолигомеров бутадиена (2-4) под действием низковалентных комплексов Ni, стабилизированных трифенилфосфитом в присутствии дизамещенного ацетилена по схеме:
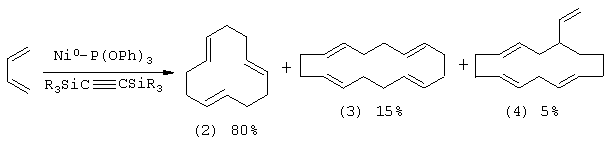
Известный способ не позволяет получать макроциклы (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами.
Известен способ (U.M.Dzhemilev, V.A.D'yakonov, L.O.Khaflzova, A.G.Ibragimov. Cyclo- and carbomagnesiation of 1,2-dienes catalyzed by Zr complexes // Tetrahedron, 2004, V.60, p.1287) получения линейных димеров 1,2-диенов (5) с цис-дизамещенными двойными связями реакцией терминальных алленов (R-=•=) с этилмагнийбромидом (EtMgBr) в присутствии магния (Mg, порошок) и катализатора титаноцендихлорида (Ср2TiCl2) с последующим гидролизом реакционной массы по схеме:

Известным способом не могут быть получены макроциклы (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами.
Таким образом, в литературе отсутствуют сведения по стереоселективному получению макроциклов (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами.
Предлагается новый способ получения макроциклов (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами.
Сущность способа заключается во взаимодействии α,ω-диалленов общей формулы =•=-R-=•=, где R=(CH2)4, (CH2)5, (СН2)6, с этилмагнийбромидом (EtMgBr) и магнием (Mg, порошок), взятыми в соотношении =•=-R-=•=:EtMgBrMg=10:(10-14):(5-7) ммолей, предпочтительно 10:12:6 ммолей, в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятого в количестве 0,3-0,7 ммолей по отношению к α,ω-диаллену, предпочтительно 0,5 ммолей, в атмосфере аргона при комнатной температуре (˜20°С) и нормальном давлении в тетрагидрофуране (ТГФ) с последуюнщм гидролизом реакционной массы. Время реакции 8-12 часов, предпочтительно 10 часов. Общий выход макроциклов (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами составляет 77-98%. Реакция протекает по схеме:
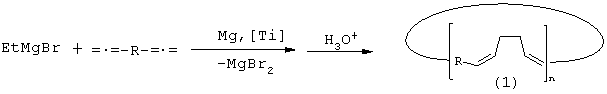
R=(CH2)4, (CH2)5, (CH2)6; n=3-5
Макроциклы (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами образуются только лишь с участием α,ω-диалленов (=•=-R-=•=), EtMgBr и катализатора Cp2TiCl2. В присутствии других магнийорганических соединений (например, амиды, алкоксиды, ацетилениды магния), других непредельных соединений (олефины, ацетилены) или другого катализатора (например, TiCl4, FeCl3, Fe(асас)3, CoCl2, PdCl2, Pd(acac)2, NiCl2, Ni(acac)2, ZrCl4) целевые продукты (1) не образуются.
Проведение указанной реакции в присутствии катализатора Cp2TiCl2 больше 7 мол.% по отношению к α,ω-диаллену не приводит к существенному увеличению выхода целевых продуктов (1). Использование катализатора Cp2TiCl2 менее 3 мол.% по отношению к α,ω-диаллену снижает выход макроциклов (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре ˜20°С. При более высокой температуре (например, 40°С) не наблюдается существенного увеличения выхода целевых продуктов (1), а при меньшей температуре (например, 0°С) снижается скорость реакции.
Изменение соотношения исходных реагентов в сторону увеличения содержания EtMgBr по отношению к исходному α,ω-диаллену не приводит к существенному повышению выхода целевых продуктов (1).
Реакции проводили с использованием тетрагидрофурана в качестве растворителя. В других растворителях (например, алифатические или ароматические) реакция не идет.
Существенные отличия предлагаемого способа:
1. В предлагаемом способе используются в качестве исходных соединений α,ω-диаллены (=•=-R-=•=), а в известном способе терминальные аллены (R-=•=).
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с высокой стереоселективностью макроциклы (1) с чередующимися алка-1Z,5Z- диеновыми фрагментами, синтез которых в литературе не описан.
Способ поясняется следующими примерами:
ПРИМЕР 1. В стеклянный реактор объемом 50 мл, установленный на магнитной мешалке, в атмосфере аргона помещают 12 ммолей свежеприготовленного EtMgBr в ТГФ, 6 мг-ат. Mg (порошок), при температуре -5°С 10 ммолей 1,2,9,10-ундекатетраена и 0,5 ммолей Ср2TiCl2, перемешивают 10 часов при комнатной температуре (˜20°С), реакционную массу гидролизуют 5-8% раствором HCl. Получают макроциклы с чередующимися ундека-1Z,5Z-диеновыми фрагментами (1) с выходом 88%.
Спектральные характеристики макроциклов с чередующимися ундека-1Z,5Z-диеновыми фрагментами (1):

Спектр ЯМР 1H (CDCl3, δ, м.д.) циклоолигомерного ундека-1,5-диена (6): 1.17-1.46 (м, СН2 при С8, С9, С10), 1.75-2.20 (м, СН2 при С3, С4, С7, С11), 5.20-5.40 (м, СН, олефиновые). Спектр ЯМР 13С (CDCl3, δ, м.д.): 130.30 (С1, С6), 129.20 (С2, С5), 27.18 (С3, С4), 27.34 (С7, С11), 29.66 (С8, С9, С10). ИК-спектр (ν, см-1): 730, 910, 1360, 1460, 1630, 2840, 2920.
Другие примеры, подтверждающие способ, приведены в табл.1.
=•=-R-=•=
=•=-R-=•=:EtMgBrMg:Cp2TiCl2
1,2,9,10-ундекатетраен
1,2,8,9-декатетраен
1,2,10,11-додекатетраен
Реакции проводили при комнатной температуре (˜20-21°С) в ТГФ. Число чередующихся алка-1Z,5Z-диеновых фрагментов во всех опытах составляет n=3-5.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛООЛИГОМЕРНЫХ 2-МЕТИЛИДЕН-5-АЛКИЛИДЕНМАГНЕЗАЦИКЛОПЕНТАНОВ | 2004 |
|
RU2268265C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСШИХ ЦИКЛОАЛКАНОВ | 2006 |
|
RU2307821C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,6-ДИАЛКИЛ-2,5-БИС(ЭТИЛМАГНЕЗА)-1,5-ГЕКСАДИЕНОВ | 2003 |
|
RU2238942C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4,7-ДИАЛКИЛ(БЕНЗИЛ)ИДЕН-1,9-ДЕКАДИЕНОВ | 2005 |
|
RU2283827C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4,7-ДИАЛКИЛ(БЕНЗИЛ)ИДЕН-2,10-ДОДЕКАДИЕНОВ | 2005 |
|
RU2286328C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,9-ДИМЕТИЛ-4,7-ДИАЛКИЛ(БЕНЗИЛ)-ИДЕН-1,9-ДЕКАДИЕНОВ | 2005 |
|
RU2283828C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,6-ДИМЕТИЛ-1,8-ДИАЛКИЛ(ФЕНИЛ)-2,6-ОКТАДИЕНОВ | 2005 |
|
RU2283826C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,6-ДИАЛКИЛ(БЕНЗИЛ)-2,5-ДИФЕНИЛ-1,5-ГЕКСАДИЕНОВ | 2005 |
|
RU2283296C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-5-АЛКИЛИДЕНМАГНЕЗАЦИКЛОПЕНТ-2-ЕНОВ | 2006 |
|
RU2374255C2 |
| СПОСОБ ПОЛУЧЕНИЯ 11-МАГНЕЗАТРИЦИКЛО[10.7.0.0]НОНАДЕКА-9,12-ДИЕНА | 2008 |
|
RU2375364C2 |
Изобретение относится к способу получения макроциклов с чередующимися алка-1Z,5Z-диеновыми фрагментами общей формулы (1):

где R=(СН2)4, (СН2)5, (СН2)6, n=3-5, который заключается в том, что α,ω-диаллены общей формулы =•=-R-=•=, где R=(СН2)4, (СН2)5, (СН2)6, взаимодействуют с этилмагнийбромидом (EtMgBr) и магнием (порошок) в мольном соотношении =•=-R-=•=:EtMgBr:Mg, равном 10:(10-14):(5-7) в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятого в количестве 0,3-07 ммолей по отношению к α,ω-диаллену, в тетрагидрофуране (ТГФ) в атмосфере аргона при комнатной температуре (˜20°С) в течение 8-12 часов. Технический результат - способ позволяет получать с высокой стереоселективностью макроциклы (1) с чередующимися алка-1Z,5Z-диеновыми фрагментами, синтез которых в литературе не описан. Эти соединения могут найти применение в синтезе биологически активных препаратов для медицины, а также в парфюмерной промышленности. 1 табл.
Способ получения макроциклов с чередующимися алка-1Z,5Z-диеновыми фрагментами общей формулы (1):
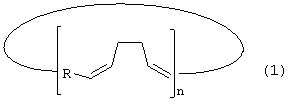 где R=(СН2)4, (СН2)5, (СН2)6,
где R=(СН2)4, (СН2)5, (СН2)6,
n=3-5
заключающийся в том, что α,ω-диаллены общей формулы =•=-R-=•=, где R=(СН2)4, (СН2)5, (СН2)6, взаимодействуют с этилмагнийбромидом (EtMgBr) и магнием (порошок) в мольном соотношении =•-R-=•=:EtMgBr:Mg, равном 10:(10-14):(5-7), в присутствии катализатора титанацендихлорида (Cp2TiCl2), взятого в количестве 0,3-0,7 ммолей по отношению к α,ω-диаллену, в ТГФ в атмосфере аргона при комнатной температуре (˜20°С) в течение 8-12 ч.
| Г.А.Толстиков и др | |||
| К вопросу о получении циклотримеров бутадиена на комплексных никелевых катализаторах | |||
| Изв | |||
| АН СССР | |||
| Сер | |||
| "Химия", 1975, №11, с.2624 | |||
| U.M.DZHMILEV et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Tetrahedron | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ совместного получения цис-транс1,5-циклодекадиена и цис-1,5-циклооктадиена | 1974 |
|
SU522165A1 |
Авторы
Даты
2006-02-10—Публикация
2004-07-05—Подача