Область техники
Настоящее изобретение относится к производным замещенного триазолдиамина и их применению в качестве селективных ингибиторов одной или двух разновидностей киназ. В частности, настоящее изобретение относится к производным замещенного 1,2,4-триазол-3,5-диамина и их применению в качестве селективных ингибиторов одной или двух киназ, а также к способу лечения или ослабления симптомов заболевания, опосредованного одной или двумя селективными киназами.
Предпосылки изобретения
В заявке на патент WO 99/21845 описаны (i) производные 4-аминотиазола нижеследующей формулы, предназначенные для применения в качестве ингибиторов циклинзависимых киназ:
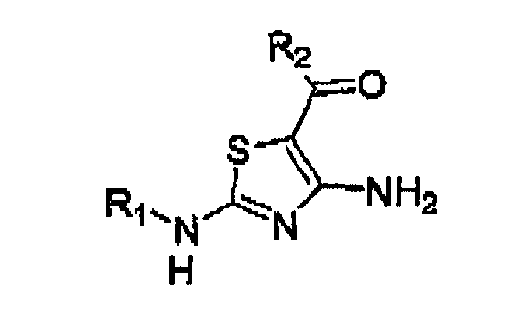
где:
R1 означает замещенную или незамещенную группу, представляющую C1-6 алкил (например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил); C1-6 алкенил; C1-6 алкинил; C1-6 алкоксил; C1-6 спирт; карбоциклический или гетероциклический циклоалкил, который может быть моноциклическим, конденсированным или неконденсированным полициклическим (например, циклопропил, циклобутил, циклопентил, циклогексил), или гетероциклоалкил, который может быть моноциклическим, конденсированным или неконденсированным полициклическим (например, пирролидинил, пиперидинил, морфолинил); карбоциклический или гетероциклический, моноциклический, конденсированный или неконденсированный полициклический арил (например, фенил, нафтил, пирролил, индолил, фуранил, тиофенил, имидазолил, оксазолил, изоксазолил, тиазолил, триазолил, тетразолил, пиразолил, пиридинил, хинолинил, изохинолинил, акридинил, пиразинил, пиридазинил, пиримидинил, бензимидазолил, бензотиофенил или бензофуранил); карбонил (например, карбоксил, сложный эфир, альдегид или кетон); простой эфир; (C1-6 алкил)карбонил; (C1-6 алкил)арил; (C1-6 алкил)циклоалкил; (C1-6 алкил)(C1-6 алкоксил); арил(C1-6 алкоксил); простой тиоэфир (например, арил-S-арил, циклоалкил-S-арил, циклоалкил-S-циклоалкил или диалкилсульфид); тиол и сульфонил; и R2 означает замещенную или незамещенную, карбоциклическую или гетероциклическую, моноциклическую, конденсированную или неконденсированную полициклическую кольцевую структуру; где каждый необязательный заместитель для R1 и R2 независимо представляет галоген (например, хлор, йод, бром или фтор); кислород (=О); галогеналкил (например, трифторметил); C1-6 алкил; C1-6 алкенил; C1-6 алкинил; гидроксил; C1-6 алкоксил; карбоциклический циклоалкил, который может быть моноциклическим, конденсированным или неконденсированным полициклическим (например, циклопропил, циклобутил, циклопентил или циклогексил), или гетероциклоалкил, который может быть моноциклическим, конденсированным или неконденсированным полициклическим (например, пирролидинил, пиперидинил, пиперазинил, морфолинил или тиазинил); карбоциклический или гетероциклический, моноциклический, конденсированный или неконденсированный полициклический арил (например, фенил, нафтил, пирролил, индолил, фуранил, тиофенил, имидазолил, оксазолил, изоксазолил, тиазолил, триазолил, тетразолил, пиразолил, пиридинил, хинолинил, изохинолинил, акридинил, пиразинил, пиридазинил, пиримидинил, бензимидазолил, бензотиофенил или бензофуранил); аминогруппу (первичную, вторичную или третичную); нитро; тиол; простой тиоэфир; имин; циано; амидо; фосфонато; фосфин; карбоксил, тиокарбонил; сульфонил; сульфонамид; кетон; альдегид или сложный эфир; (ii) фармацевтически приемлемые соли соединений вышеуказанной формулы и (iii) пролекарства и фармацевтически активные метаболиты соединений вышеуказанной формулы или их фармацевтически приемлемые соли; и (b) фармацевтически приемлемый носитель.
В заявке на патент WO 01/09106 описаны диамино-1,2,4-триазолкарбоновая кислота и ее производные формулы (I), предназначенные для применения в качестве ингибиторов GSK-3 (протеинкиназы):
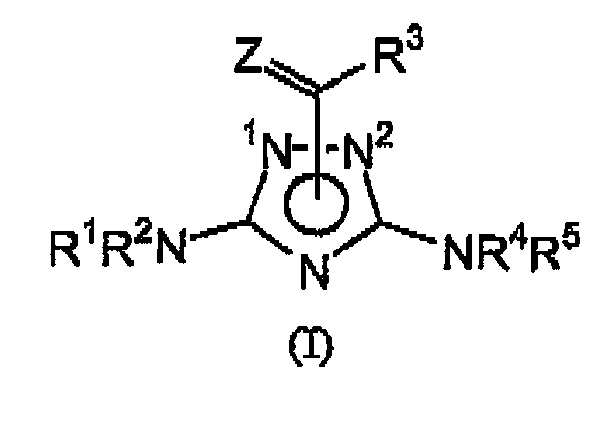
где:
R3CZ-часть может быть присоединена к атому азота в положении 1 или в положении 2;
R1 означает водород, алкил, арил, аралкил, аралкенил или алициклическую группу; R2 означает водород, алкил, арил, аралкил, аралкенил или алициклическую группу, либо R1 и R2 с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо, которое может быть не замещено или замещено; R3 означает алкил, арил, аралкил, арил(Q)алкил, где Q означает О или S, аралкенил, алициклическую группу, гетероарил, гетероаралкил, арилкарбонилалкил, алициклилалкил, диарилалкил или NR6R7; R4 означает водород, алкил, арил, аралкил, аралкенил или алициклическую группу; R5 означает водород, алкил, арил, аралкил, аралкенил или алициклическую группу, либо R4 и R5 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо, которое может быть не замещено или замещено; R6 означает водород, арил или алициклическую группу; R7 означает водород, арил или алициклическую группу, и Z означает кислород или серу. R1 может представлять водород, незамещенный или замещенный фенил, причем заместители для фенильной группы независимо выбирают из одной-трех групп, включающих C1-C6 алкил, C1-C6 алкокси, C1-C6 алкокси(C1-C6)алкил, арил, арилокси, галоген, гидрокси, карбокси, циано и нитро. R1 предпочтительно означает фенил, который может быть не замещен или замещен одной-тремя группами, такими как метил, метокси или хлор. R2 может представлять водород, незамещенный или замещенный фенил, причем заместители для фенильной группы независимо выбирают из одной-трех групп, включающих C1-C6 алкил, C1-C6 алкокси, C1-C6 алкокси(C1-C6)алкил, арил, арилокси, галоген, гидрокси, карбокси, циано и нитро. R2 предпочтительно означает водород. R3 может представлять незамещенный или замещенный фенил, незамещенный или замещенный нафтил, незамещенный или замещенный бензил, незамещенный или замещенный тиенилметил, незамещенный или замещенный фенилтиометил, незамещенный или замещенный нафтилметил, незамещенный или замещенный фурилэтенил, незамещенный или замещенный циклогексил, незамещенный или замещенный пиридил, незамещенный или замещенный индолилметил, незамещенный или замещенный фенилкарбонилэтил, незамещенный или замещенный циклопентенилметил, незамещенный или замещенный фенилпропил, незамещенный или замещенный дифенилэтил, причем заместители для арильных групп R3 выбирают из -О(СН2)nО-, где n равно 1-3, или из одной-трех групп, включающих галоген, арил, перфтор(C1-C6)алкил, нитро, арилкарбонил, арилокси, C1-C6 ацил; или R3 представляет NR6R7, где R6 и R7 независимо означают водород, незамещенный или замещенный арил, незамещенную или замещенную C1-C6 алициклическую группу, причем заместители для групп R6 и R7 независимо выбирают из одной-трех групп, включающих галоген, арил, арилокси, алкил, нитро и алкокси. R3 предпочтительно означает фенил, который может быть не замещен или замещен одной-тремя группами, включающими хлор, бром, фенил, трифторметил, нитро, бензоил, фенокси, ацетил или 3,4-ОСН2O-; нафтил; бензил, который может быть не замещен иили замещен одной-тремя группами, включающими фенил или фтор; 2-тиенилметил; фенилтиометил 2-нафтил-метил; циклогексил; 3-пиридил; 3-индолилметил; фенилкарбонилэтил; циклопент-2-енилметил; фенилпропил; 2,2-дифенилэтил; 2-фурилэтенил; или NR6R7, где R6 и R7 независимо означают водород, фенил, который может быть не замещен или замещен одной-тремя группами, включающими хлор, фенил, фенокси, метил, бром, нитро или метокси; циклогексил или 1-нафтил. В удобном случае R4 может представлять водород. В удобном случае R5 может представлять водород. В удобном случае R6 может представлять незамещенный или замещенный арил, незамещенную или замещенную алициклическую группу. R6 предпочтительно означает циклогексил, нафтил или фенил, который может быть не замещен или замещен одной-тремя группами, включающими хлор, бром, фенил, метил, фенокси, нитро или метокси. R7 может представлять водород.
В патенте США № 5750545 описаны производные триазола формулы (I) и формулы (III), предназначенные для применения в качестве лекарственных средств для профилактики и лечения иммунных заболеваний:
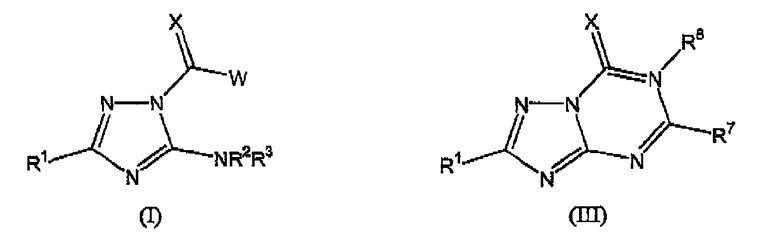
где:
Х означает атом кислорода или атом серы; W означает -NR4R5 или -SR6; R1 означает атом водорода, низший алкил, -NR10R11, -N=R13, или группу формулы (II)
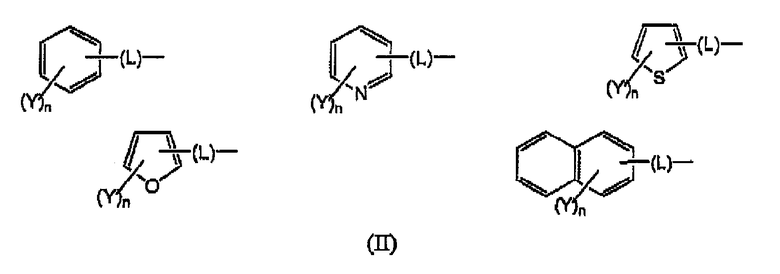
где:
Y означает атом водорода, низший алкил, низший алкокси, галоген, циано, нитро, низший алкил, замещенный галогеном, -NR14R15, тетразолил, необязательно замещенный фенил, гидрокси или карбоксил, L означает прямую (непосредственную) связь, атом кислорода, атом серы, алкилен, винилен или этинилен и n является целым числом от 1 до 3 при условии, что, когда n равно 2 или 3, Y может иметь одинаковые или разные значения; R2 и R3 имеют одинаковые или разные значения и представляют атом водорода или низший алкил; R4 и R5 имеют одинаковые или разные значения и представляют атом водорода, необязательно замещенный низший алкил, циклоалкил, фенил или -(СН2)mCOOR16, где R16 означает атом водорода или низший алкил, m является целым числом от 1 до 6, R6 означает низший алкил, R10 и R11 имеют одинаковые или разные значения и представляют атом водорода, необязательно замещенный бензоил, необязательно замещенный фенил, низший алкилкарбонил или -COCOOR17, где R17 означает низший алкил, R13 означает необязательно замещенный метилен, R14 и R15 имеют одинаковые или разные значения и представляют атом водорода, низший алкил, -COCOOR17 или -CSNHR18, где R18 означает низший алкил, или их фармацевтически приемлемые соли.
Объектом настоящего изобретения являются производные замещенного триазолдиамина и их применение в качестве селективных ингибиторов одной или двух киназ. В частности, объектом настоящего изобретения являются производные замещенного 1,2,4-триазол-3,5-диамина, их применение в качестве селективных ингибиторов одной или двух киназ и способ лечения или ослабления симптомов заболевания, опосредованного одной или двумя селективными киназами.
Краткое изложение существа изобретения
Настоящее изобретение относится к соединению формулы (I):
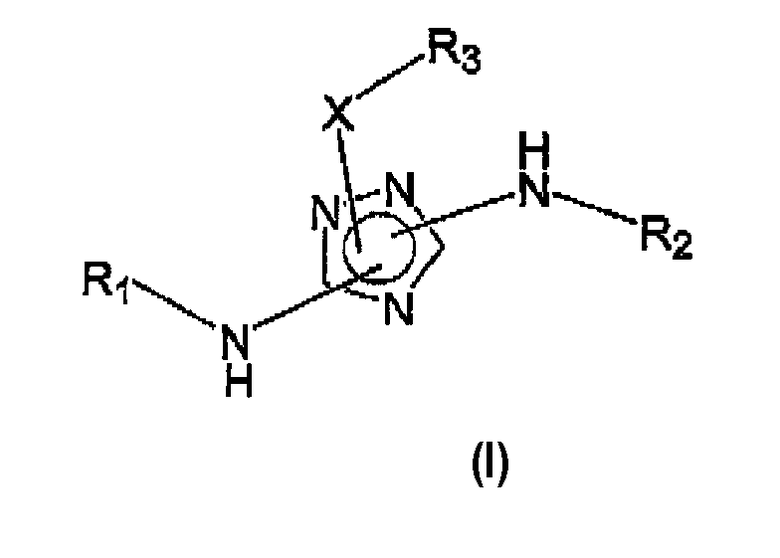
где:
R1 выбирают из группы, включающей C1-8 алкил, циклоалкил, гетероциклил, арил или гетероарил {причем гетероциклил необязательно замещен 1-2 оксозаместителями; и циклоалкил, гетероциклил, арил и гетероарил замещены заместителем, выбираемым из группы, включающей:
C1-8 алкил (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -CO2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил);
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2-(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; гетероциклил необязательно замещен 1-2 оксозаместителями; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены заместителем, выбираемым из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси и амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил)}};
R2 выбирают из группы, включающей водород, C1-8 алкил, C2-8 алкенил, C2-8 алкинил и гидрокси(C1-8)алкил;
Х выбирают из группы, включающей -С(О)-, -С(S)- и -SO2-; и
R3 выбирают из группы, включающей:
C1-8 алкил, C2-8 алкенил, C2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2H, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-8 алкил, C2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-8)алкил, C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -С(О)(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил))},
-NH-SO2-(C1-8)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)};
и его фармацевтически приемлемым солям.
Один из вариантов осуществления настоящего изобретения относится к способу лечения или ослабления симптомов заболевания, опосредованного одной или двумя селективными киназами.
Другой вариант осуществления настоящего изобретения относится к способу получения соединений по данному изобретению, фармацевтических композиций и лекарственных препаратов.
Подробное описание изобретения
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), в которой R1 предпочтительно выбирают из группы, включающей C1-4 алкил, циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил замещены заместителем, выбираемым из группы, включающей:
C1-4 алкил (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-4)алкил, -СО2H, -СО2(C1-4)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил);
C1-4 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-4)алкил, -СО2Н, -СО2(C1-4)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -SO2-(C1-4)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил, -C1-4 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; гетероциклил необязательно замещен 1-2 оксозаместителями; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены заместителем, выбираемым из группы, включающей C1-4 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-4 алкокси и амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил)}}.
Более предпочтительно R1 выбирают из группы, включающей C1-4 алкил и арил {причем арил замещен заместителем, выбираемым из группы, включающей:
C1-4 алкил (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано,
(галоген)1-3, гидрокси и нитро),
C1-4 алкокси,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -SO2-(C1-4)алкил);
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил, -C1-4 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил) и гетероарил)},
гетероциклил (причем гетероциклил необязательно замещенный 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил и оксо) и гетероарил}.
Наиболее предпочтительно R1 выбирают из группы, включающей C1-4 алкил и фенил (причем фенил замещен заместителем, выбираемым из группы, включающей:
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -SO2-(C1-4)алкил);
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей пиперидинил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил, -C1-4 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил) и пиридинил)}, и
пиперазинил (необязательно замещенный 1-2 заместителями, представляющими C1-4 алкил), имидазолидинил, изотиазолидинил (причем имидазолидинил и изотиазолидинил необязательно замещены 1-2 оксозаместителями), имидазолил и триазолил}.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), в которой R2 предпочтительно выбирают из группы, включающей водород,
C1-4 алкил, C2-4 алкенил, C2-4 алкинил и гидрокси(C1-4)алкил.
Более предпочтительно R2 выбирают из группы, включающей водород и C1-4 алкил.
Наиболее предпочтительно R2 представляет водород.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), в которой Х предпочтительно выбирают из группы, включающей -С(О)-, -C(S)- и -SO2-.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), в которой R3 предпочтительно выбирают из группы, включающей:
C1-4 алкил, C2-4 алкенил, C2-4 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-4)алкил, -СО2Н, -СО2(C1-4)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, (галоген)1-3(C1-4)алкил, (галоген)1-3 (C1-4)алкокси, гидрокси, гидрокси(C1-4)алкил, гидрокси(C1-4)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-4 алкил, C2-4 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-4)алкил, -СО2Н, -СО2(C1-4)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-4)алкил,
C1-4 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-4)алкил, -СО2Н, -СО2(C1-4)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -С(О)(C1-4)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -C1-4 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил))},
-NH-SO2-(C1-4)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, (галоген)1-3(C1-4)алкил, (галоген)1-3(C1-4)алкокси, гидрокси, гидрокси(C1-4)алкил, гидрокси(C1-4)алкокси и нитро)}.
Более предпочтительно R3 выбирают из группы, включающей:
C1-4 алкил, C2-4 алкенил, C2-4 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, (галоген)1-3(C1-4)алкил, (галоген)1-3(C1-4)алкокси, гидрокси, гидрокси(C1-4)алкил, гидрокси(C1-4)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-4 алкил, C2-4 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -СО2Н, -СО2(C1-4)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-4)алкил,
C1-4 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-4)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -С(О)-(C1-4)алкил),
арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и арил (причем арил необязательно замещен 1-5 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, (галоген)1-3(C1-4)алкил, (галоген)1-3(C1-4)алкокси, гидрокси, гидрокси(C1-4)алкил, гидрокси(C1-4)алкокси и нитро)}.
Наиболее предпочтительно R3 выбирают из группы, включающей:
C1-4 алкил, C2-4 алкенил, C2-4 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси, нитро, фенил и тиенил (причем фенил и тиенил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, гидрокси и нитро)},
циклопентил, циклогексил, циклогептил, бензо[b]тиенил, фенил, фурил, тиенил, тиазолил, изоксазолил, тиадиазолил, пиридинил {причем циклогексил и фенил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклогексил и фенил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-4 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси и нитро),
-СН(ОН)(C1-4)алкил,
C1-4 алкокси,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил),
тиенил и тиазолил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, тиенил и тиазолил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-4 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей -СО2Н, -СО2(C1-4)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси и нитро),
C1-4 алкокси,
-С(О)(C1-4)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -С(О)(C1-4)алкил),
пирролил и пиридинил;
и тиадиазолил необязательно замещен одним заместителем, выбираемым из группы, включающей C1-4 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей:
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-4 алкокси, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил),
циано, галоген, гидрокси и нитро} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и фенил (причем фенил необязательно замещен 1-5 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил, циано, галоген, гидрокси и нитро)}.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), представляющим соединение формулы (Ia):
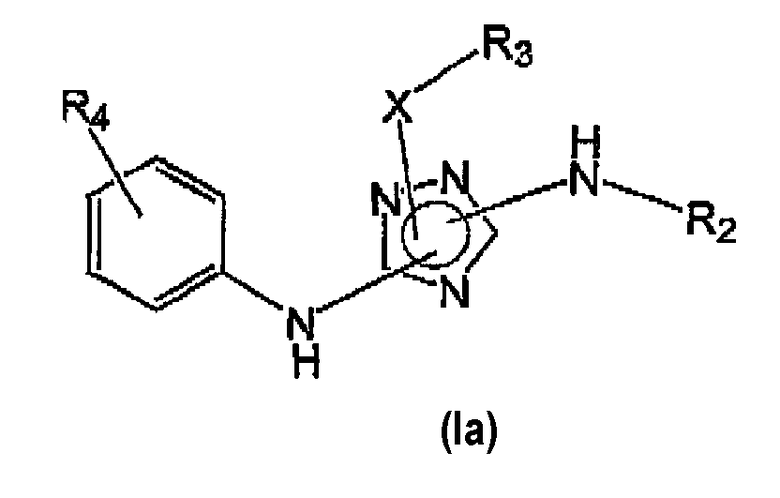
где:
R4 выбирают из группы, включающей:
C1-8 алкил {необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил};
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2-(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, галоген, гидрокси и нитро; и гетероциклил необязательно замещен 1-2 оксозаместителями)};
R2 выбирают из группы, включающей водород, C1-8 алкил, C2-8 алкенил, C2-8 алкинил и гидрокси(C1-8)алкил;
Х выбирают из группы, включающей -С(О)-, -С(S)- и -SO2-; и
R3 выбирают из группы, включающей:
C1-8 алкил, C2-8 алкенил, C2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-8 алкил, C2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-8)алкил,
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -С(О)(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил))},
-NH-SO2-(C1-8)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)};
и его фармацевтически приемлемые соли.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), представляющим соединение формулы (Ib):
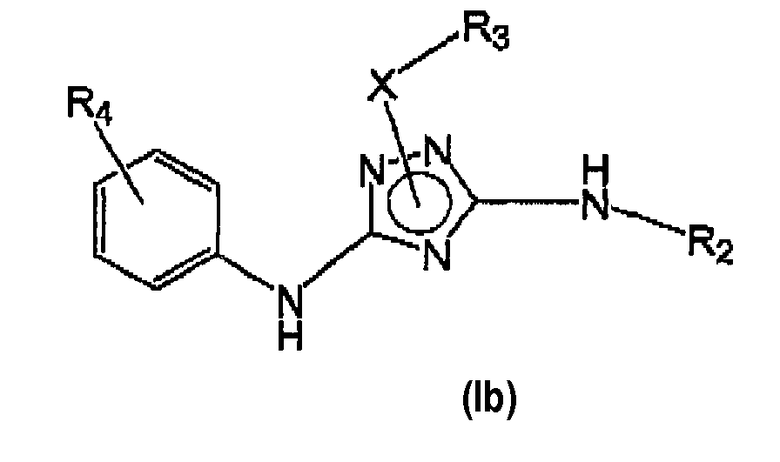
где:
R4 выбирают из группы, включающей:
C1-8 алкил {необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил};
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2- (C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, галоген, гидрокси и нитро; и гетероциклил необязательно замещен 1-2 оксозаместителями};
R2 выбирают из группы, включающей водород, C1-8 алкил, С2-8 алкенил, С2-8 алкинил и гидрокси(C1-8)алкил;
Х выбирают из группы, включающей -С(О)-, -С(S)- и -SO2-; и
R3 выбирают из группы, включающей:
C1-8 алкил, С2-8 алкенил, С2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-8 алкил, С2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(С1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-8)алкил,
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -С(О)(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), -SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил))},
-NH-SO2-(C1-8)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)};
и его фармацевтически приемлемые соли.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), представляющим соединение формулы (Ic):
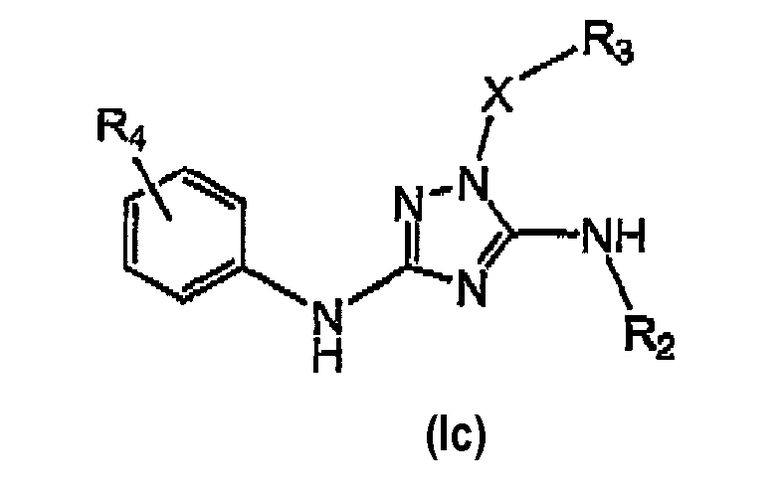
где:
R4 выбирают из группы, включающей:C1-8 алкил {необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил};
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2-(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, галоген, гидрокси и нитро; и гетероциклил необязательно замещен 1-2 оксозаместителями};
R2 выбирают из группы, включающей водород, C1-8 алкил, С2-8 алкенил, С2-8 алкинил и гидрокси(C1-8)алкил;
Х выбирают из группы, включающей -С(О)-, -С(S)- и -SO2-; и
R3 выбирают из группы, включающей:
C1-8 алкил, С2-8 алкенил, С2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
С1-8 алкил, С2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(С1-8)алкил, -СО2Н, -СО2(С1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и С1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(С1-8)алкил,
С1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(С1-8)алкил, -СО2Н, -СО2(С1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, С1-8 алкил, -С(О)(С1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и С1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, С1-8 алкил и -С1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и С1-8 алкил))},
-NH-SO2-(С1-8)алкил,циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, С1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей С1-8 алкил, циано, галоген, (галоген)1-3(С1-8)алкил, (галоген)1-3(С1-8)алкокси, гидрокси, гидрокси(С1-8)алкил, гидрокси(С1-8)алкокси и нитро)};
и его фармацевтически приемлемые соли.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (Ic), в которой R4 предпочтительно выбирают из группы, включающей:
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -SO2-(C1-4)алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-4 алкил и -C1-4 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-4 алкил) и гетероарил)},
гетероциклил (необязательно замещенный 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4 алкил и оксо) и гетероарил.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), представляющим соединение формулы (Id):
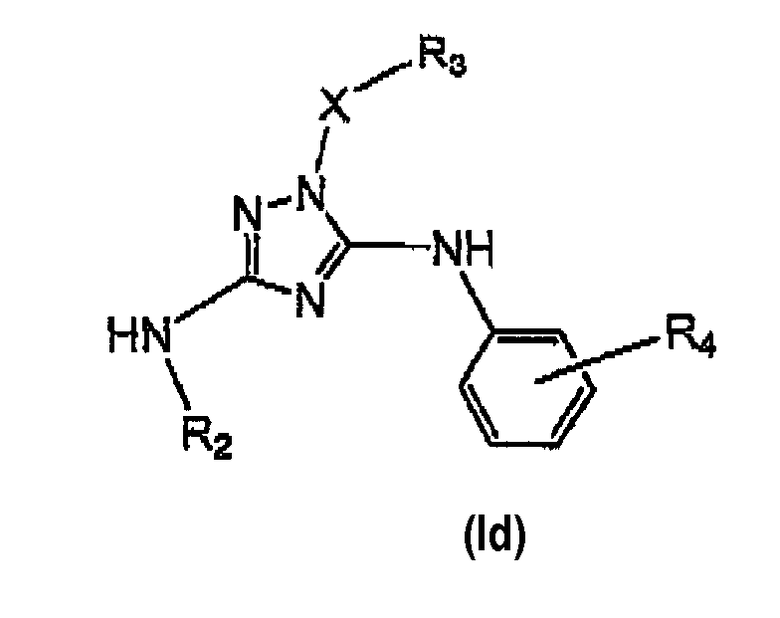
где:
R4 выбирают из группы, включающей:
C1-8 алкил {необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил};
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2-(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, галоген, гидрокси и нитро; и гетероциклил необязательно замещен 1-2 оксозаместителями};
R2 выбирают из группы, включающей водород, C1-8 алкил, С2-8 алкенил, C2-8 алкинил и гидрокси(C1-8)алкил;
Х выбирают из группы, включающей -С(О)-, -С(S)- и -SO2-; и
R3 выбирают из группы, включающей:
C1-8 алкил, C2-8 алкенил, C2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-8 алкил, C2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-8)алкил,
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -С(О)(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил))},
-NH-SO2-(C1-8)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)};
и его фармацевтически приемлемые соли.
Некоторые варианты осуществления настоящего изобретения относятся к соединениям формулы (I), представляющим соединение формулы (Ie):
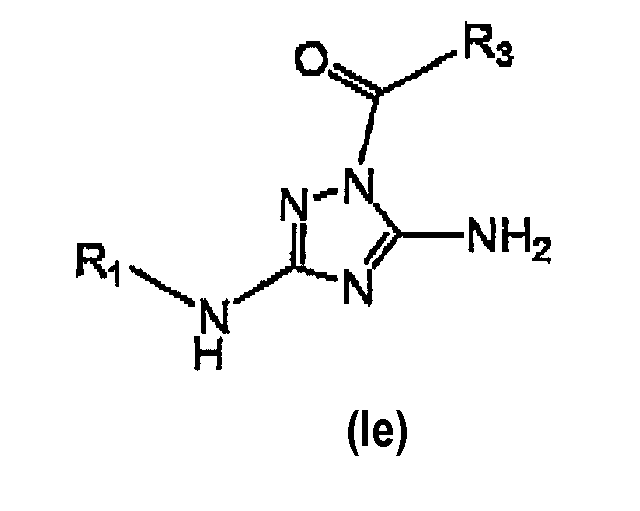
где:
R1 выбирают из группы, включающей C1-8 алкил, циклоалкил, гетероциклил, арил или гетероарил {причем гетероциклил необязательно замещен 1-2 оксозаместителями; и циклоалкил, гетероциклил, арил и гетероарил замещены заместителем, выбираемым из группы, включающей:
C1-8 алкил (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил);
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -SO2-(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил) и гетероарил)},
циклоалкил, гетероциклил, арил и гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; гетероциклил необязательно замещен 1-2 оксозаместителями и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены заместителем, выбираемым из группы, включающей C1-8 алкил (причем алкил необязательно замещен у концевого атома углерода заместителем, выбираемым из группы, включающей амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси и нитро), C1-8 алкокси и амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил)}}; и
R3 выбирают из группы, включающей:
C1-8 алкил, C2-8 алкенил, C2-8 алкинил {причем алкил, алкенил и алкинил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, арил и гетероарил (причем арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)},
циклоалкил, гетероциклил, арил, гетероарил {причем циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-3 заместителями, независимо выбираемыми из группы, включающей циано, галоген, гидрокси и нитро; и, кроме того, циклоалкил, гетероциклил, арил и гетероарил необязательно замещены 1-2 заместителями, независимо выбираемыми из группы, включающей:
C1-8 алкил, C2-8 алкенил (причем алкил и алкенил необязательно замещены у концевого атома углерода заместителем, выбираемым из группы, включающей -С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил, амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил), циано, (галоген)1-3, гидрокси, нитро, циклоалкил, гетероциклил, арил и гетероарил),
-СН(ОН)(C1-8)алкил,
C1-8 алкокси (необязательно замещенный у концевого атома углерода заместителем, выбираемым из группы, включающей (галоген)1-3 и гидрокси),
-С(О)Н, -С(О)(C1-8)алкил, -СО2Н, -СО2(C1-8)алкил,
амино (замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, -С(О)(C1-8)алкил),
-С(О)амино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил),
-SO2- {замещенный одним заместителем, выбираемым из группы, включающей гетероциклил и амино (причем амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил и -C1-8 алкиламино (где амино замещен двумя заместителями, независимо выбираемыми из группы, включающей водород и C1-8 алкил))},
-NH-SO2-(C1-8)алкил,
циклоалкил, гетероциклил (необязательно замещенный 1-2 оксозаместителями), арил и гетероарил} и
амино {замещенный двумя заместителями, независимо выбираемыми из группы, включающей водород, C1-8 алкил, циклоалкил, арил и гетероарил (причем циклоалкил, арил и гетероарил необязательно замещены 1-5 заместителями, независимо выбираемыми из группы, включающей C1-8 алкил, циано, галоген, (галоген)1-3(C1-8)алкил, (галоген)1-3(C1-8)алкокси, гидрокси, гидрокси(C1-8)алкил, гидрокси(C1-8)алкокси и нитро)};
и его фармацевтически приемлемые соли.
Иллюстративные соединения по настоящему изобретению включают соединение формулы (I), представляющее соединение формулы (Ic):

Соединение формулы (Ic), в которой Х, R2, R3 и R4 взаимозависимо выбирают из нижеследующих групп:
и его фармацевтически приемлемые соли.
Иллюстративные соединения по настоящему изобретению включают соединение формулы (I), представляющее соединение формулы (Id):
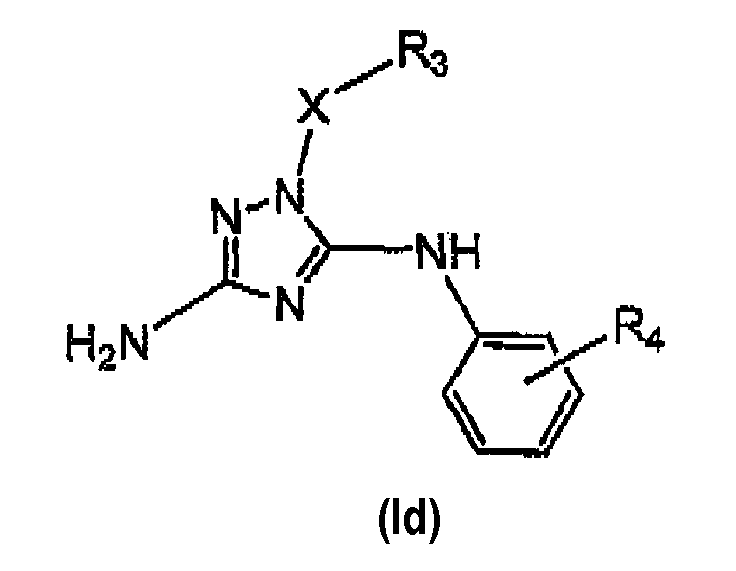
где Х, R3 и R4 взаимозависимо выбирают из нижеследующих групп:
и его фармацевтически приемлемые соли.
Иллюстративные соединения по настоящему изобретению включают соединение формулы (I), представляющее соединение формулы (Ie):

где R1 и R3 взаимозависимо выбирают из нижеследующих групп:
и его фармацевтически приемлемые соли.
Соединения по настоящему изобретению могут также быть в форме фармацевтически приемлемых солей. Для использования в медицине соли соединений по данному изобретению представляют нетоксичные "фармацевтически приемлемые соли" (Ref. International J. Pharm., 1986, 33, 201-217; J. Pharm. Sci., 1997 (Jan), 66, I, 1). Однако другие соли могут быть полезны для получения соединений по данному изобретению или их фармацевтически приемлемых солей. Типичные органические или неорганические кислоты включают, не ограничиваясь ими, хлористоводородную, бромистоводородную, иодистоводородную, перхлорную, серную, азотную, фосфорную, уксусную, пропионовую, гликолевую, молочную, янтарную, малеиновую, фумаровую, яблочную, винную, лимонную, бензойную, миндальную, метансульфоновую, гидроксиэтансульфоновую, бензолсульфоновую, щавелевую, памовую, 2-нафталинсульфоновую, п-толуолсульфоновую, циклогексансульфаминовую, салициловую, сахариновую или трифторуксусную кислоту. Типичные органические или неорганические основания включают, не ограничиваясь ими, основные или катионные соли, такие как бензатин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин, прокаин, соли алюминия, кальция, лития, магния, калия, натрия и цинка.
В объем настоящего изобретения входят пролекарства соединений по данному изобретению. Такие пролекарства обычно представляют собой содержащие функциональные группы производные указанных соединений, которые легко превращаются in vivo в требуемое соединение. Таким образом, в способах лечения по настоящему изобретению термин "введение" означает лечение разных заболеваний специально описанным или не описанным соединением, которое превращается в требуемое соединение in vivo после введения нуждающемуся субъекту. Обычные способы выбора и получения приемлемых производных пролекарств описаны, например, в издании "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985.
Соединения по данному изобретению, имеющие, по крайней мере, один хиральный центр, могут существовать в виде энантиомеров. Соединения, имеющие два или более хиральных центров, могут дополнительно существовать в виде диастереомеров. Если при осуществлении способов получения соединений по данному изобретению образуется смесь стереоизомеров, такие изомеры можно разделить обычными методами, в частности препаративной хроматографией. Указанные соединения можно получить в виде рацемической смеси, или отдельные энантиомеры можно получить стандартными методами, известными специалисту в данной области, например при помощи энантиоселективного синтеза или разделения, создания диастереомерных пар в результате образования соли с использованием оптически активной кислоты, последующего выполнения фракцонированной кристаллизации и восстановления свободного основания. Соединения можно также выделить путем образования диастереомерных сложных эфиров или амидов с последующим выполнением хроматографического разделения и удаления вспомогательного хирального центра. Альтернативно соединения можно разделить при помощи колонки для хиральной ВЭЖХ. Следует отметить, что все указанные изомеры и смеси входят в объем настоящего изобретения и, кроме того, термин "соединение формулы Х" означает энантиомеры, диастереомеры и подобные формы соединения.
За исключением особо оговоренных случаев термин "алкил" означает насыщенную группу с прямой или разветвленной цепью, состоящую только из 1-8 замещенных водородом атомов углерода, предпочтительно 1-6 замещенных водородом атомов углерода и наиболее предпочтительно 1-4 замещенных водородом атомов углерода. Термин "алкенил" означает частично ненасыщенную алкильную группу с прямой или разветвленной цепью, имеющую по крайней мере одну двойную связь. Термин "алкинил" означает частично ненасыщенную алкильную группу с прямой или разветвленной цепью, имеющую по крайней мере одну тройную связь. Термин "алкокси" означает -О-алкил, где алкил имеет указанные выше значения.
Термин "циклоалкил" означает насыщенное или частично ненасыщенное циклическое алкильное кольцо, имеющее 3-8 замещенных водородом атомов углерода. Примеры таких групп включают, не ограничиваясь ими, циклопропил, циклопентил, циклогексил или циклогептил.
Термин "гетероциклил" означает насыщенное или частично ненасыщенное пятичленное кольцо, в котором по крайней мере один член представляет атом N, O или S и которое необязательно содержит один дополнительный атом О или один, два или три дополнительных атома N; насыщенное или частично ненасыщенное шестичленное кольцо, в котором один, два или три члена представляют атом N; насыщенное или частично ненасыщенное бициклическое девятичленное кольцо, в котором по крайней мере один член представляет атом N, O или S и которое необязательно содержит один, два или три дополнительных атома N; и насыщенное или частично ненасыщенное бициклическое десятичленное кольцо, в котором один, два или три члена представляют атом N. Примеры таких групп включают, не ограничиваясь ими, пирролинил, пирролидинил, диоксоланил, имидазолинил, имидазолидинил, пиразолинил, пиразолидинил, пиперидинил, морфолинил или пиперазинил.
Термин "арил" означает ароматическую моноциклическую кольцевую систему, содержащую 6 замещенных водородом атомов углерода, ароматическую бициклическую кольцевую систему, содержащую 10 замещенных водородом атомов углерода или ароматическую трициклическую кольцевую систему, содержащую 14 замещенных водородом атомов углерода. Примеры таких групп включают, не ограничиваясь ими, фенил, нафталинил или антраценил.
Термин "гетероарил" означает ароматическую моноциклическую пятичленную кольцевую систему, в которой по крайней мере один член представляет атом N, O или S и которая необязательно содержит один, два или три дополнительных атома N, ароматическое моноциклическое шестичленное кольцо, в котором один, два или три члена представляют атом N, ароматическое бициклическое девятичленное кольцо, в котором по крайней мере один член представляет атом N, O или S и которое необязательно содержит один, два или три дополнительных атома N, и ароматическое бициклическое десятичленное кольцо, в котором один, два или три члена представляют атом N. Примеры таких групп включают, не ограничиваясь ими, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, пиридинил, пиридазинил, пиримидинил, пиразинил, индолил, индазолил, хинолинил или изохинолинил.
Термин "галоген" означает атом фтора, хлора, брома или иода.
Термин "независимо" означает, что, когда группа замещена более чем одним заместителем, указанные заместители могут иметь одинаковые или разные значения. Термин "взаимозависимо" означает, что заместители определены соответствующей комбинацией структурных элементов.
Одним из вариантов осуществления изобретения является фармацевтическая композиция или лекарственный препарат, содержащие фармацевтически приемлемый носитель и любое из вышеописанных соединений. В качестве примера осуществления изобретения можно привести фармацевтическую композицию или лекарственный препарат, полученный смешиванием любого из вышеописанных соединений и фармацевтически приемлемого носителя. В качестве другого примера осуществления изобретения можно привести способ получения фармацевтической композиции или лекарственного препарата, включающий смешивание любого из вышеописанных соединений и фармацевтически приемлемого носителя. В качестве еще одного примера осуществления настоящего изобретения можно привести фармацевтические композиции или лекарственные препараты, содержащие одно или несколько соединений по данному изобретению в сочетании с фармацевтически премлемым носителем.
В используемом здесь значении термин "композиция" означает продукт, содержащий соответствующие ингредиенты в определенных количествах, а также любой продукт, получаемый прямым или непрямым способом в результате объединения определенных ингредиентов в определенных количествах.
Соединения по настоящему изобретению представляют селективные ингибиторы одной или двух киназ, пригодные для применения в способе лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами. В частности, такая киназа представляет циклинзависимую киназу или тирозинкиназу. Более конкретно, киназа представляет циклинзависимую киназу-1, циклинзависимую киназу-2, циклинзависимую киназу-4, рецептор-2 эндотелиального фактора роста сосудов, рецептор эндотелиального фактора роста и рецептор-2 эпидермального фактора роста человека.
Ингибиторы циклинзависимых киназ играют важную роль в регуляции развития эукариотической клетки на протяжении всего жизненного цикла клетки благодаря тому, что они связываются с белковыми комплексами, образуемыми циклинами и циклинзависимыми киназами, и таким образом ослабляют активность циклинзависимых киназ. Пути метаболизма, в которые вовлечены ингибиторы циклинзависимых киназ, часто бывают разрушены в опухолевых клетках, что вызывает неправильную регуляцию жизненного цикла клетки. Сверхэкспрессия ингибиторов циклинзависимых киназ тормозит развитие клеток в одной из контрольных точек жизненного цикла клетки. Поэтому использование ингибиторов циклинзависимых киназ кажется весьма привлекательным для лечения опухолей, так как указанные киназы способствуют росту опухоли. Подавление или контроль нерегулируемой пролиферации клеток может дать положительные результаты в случае некоторых видов ангиопатии, роста доброкачественной опухоли, лейкозов и подобных заболеваний. Особенно хорошей мишенью для ингибитора циклинзависимых киназ (CDK) при создании противоопухолевых средств является рецептор CDK-1. Указанный белок контролирует последнюю контрольную точку в жизненном цикле клетки между фазой G2 и M.
Вторым белком-мишенью, который способен облегчить процесс уничтожения опухоли, является рецептор эндотелиального фактора роста сосудов (VEGF) тирозинкиназы. Указанный белок участвует как в нормальном, так и патологическом ангиогенезе. Рецепторы VEGF являются трехраздельными и включают внеклеточный лигандсвязывающий домен, трансмембранный домен и внутриклеточный домен тирозинкиназы. В настоящее время известны два рецептора VEGF: (1) VEGF-R2 (KDR/Flk1/VEGF-R2) - рецептор, опосредующий биологическую активность митогенеза и пролиферацию эндотелиальных клеток; и (2) VEGF-R1 (Flt1/VEGF-R1) - рецептор, опосредующий такие функции, как адгезия эндотелиальных клеток. Установлено, что ингибирование передачи сигналов VEGF-R2 подавляет процесс развития кровеносных сосудов. Ингибиторы указанного рецептора, по-видимому, полезны для регулирования или ограничения ангиогенеза.
Многие цитотоксические методы лечения рака вызывают разрушение быстро делящегося эпителия волосяного мешочка, что ведет к алопеции (выпадению волос). Ингибирование циклинзависимых киназ позволяет предотвратить вызываемую химиотерапией алопецию благодаря задержке жизненного цикла клетки и уменьшению чувствительности эпителиальных клеток к противоопухолевым средствам (Davis S.T., et al., Prevention of chemotherapy-induced alopecia in rats by CDK inhibitors, Science, 2001, (Jan 5), 291, 5501, 25-6). Местное применение не вызывающих апоптоз ингибиторов CDK представляет потенциально эффективный подход к предотвращению вызываемой химиотерапией алопеции у больных раком.
Хотя пластика коронарной артерии является весьма эффективным способом устранения окклюзии коронарной артерии, успех такого лечения в долговременной перспективе ограничен высокими показателями рестеноза. Рестеноз после пластической операции на сосудах в значительной степени обусловлен активацией, миграцией и пролиферацией клеток гладких мышц сосудов (Ross, R., Nature, 1993, 362, 801-809). Последние исследования показали, что CDK2 очень быстро активируется после денудации эндотелиальных клеток в модели рестеноза сонной артерии у крыс (Wei, G.L., et al., Circ. Res., 1997, 80, 418-426). Поэтому лечение, подавляющее пролиферацию клеток, которое целенаправленно воздействует на циклинзависимые киназы или другие компоненты механизма, определяющего жизненный цикл клеток, может быть перспективным подходом к лечению указанных заболеваний.
Некоторые варианты осуществления настоящего изобретения относятся к способу лечения или ослабления симптомов заболевания, опосредованного одной или двумя селективными киназами, который включает введение нуждающемуся субъекту терапевтически эффективного количества соединения или фармацевтической композиции по данному изобретению. Терапевтически эффективное количество соединений формулы (I), используемых при осуществлении указанного способа, составляет от около 0,001 мг/кг/сутки до около 300 мг/кг/сутки.
Некоторые варианты осуществления настоящего изобретения относятся к использованию соединения формулы (I) для получения лекарственного препарата для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами, у нуждающегося субъекта.
В соответствии со способами по настоящему изобретению соединения по настоящему изобретению или содержащие их фармацевтические композиции можно вводить отдельно в разное время на протяжении всего курса лечения или одновременно в виде раздельных или общих форм. Поэтому в объем настоящего изобретения входят все такие способы одновременного или поочередного лечения, и термин "введение" должен иметь соответствующее значение.
Некоторые варианты осуществления настоящего изобретения относятся к соединению или содержащей его фармацевтической композиции, вводимым в выгодной комбинации с другими лекарственными средствами, предназначенными для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами. Комбинированная терапия предполагает совместное введение соединения формулы (I) или содержащей его фармацевтической композиции и дополнительного лекарственного средства для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами, последовательное введение соединения формулы (I) или содержащей его фармацевтической композиции и дополнительного лекарственного средства для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами, введение фармацевтической композиции, включающей соединение формулы (I) или содержащую его фармацевтическую композицию и дополнительное средство, для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами, или по существу одновременное введение отдельной фармацевтической композиции, содержащей соединение формулы (I), и отдельной фармацевтической композиции, содержащей дополнительное лекарственное средство, для лечения или ослабления симптомов заболевания, опосредованного одной или двумя киназами.
Термин "другие лекарственные средства" означает, не ограничиваясь ими, средства, подавляющие развитие кровеносных сосудов, противоопухолевые средства, цитотоксические средства, ингибиторы пролиферации клеток и тому подобные. Термин "лечение или ослабление симптомов" означает, не ограничиваясь таким определением, уничтожение и подавление развития или активацию стаза злокачественной опухоли. Например, ингибитор двух киназ CDK1-VEGF-R по настоящему изобретению, подавляющий развитие кровеносных сосудов, можно вводить в соответствии со схемой лекарственного лечения вместе с другим цитотоксическим соединением, таким как ДНК-алкилирующее средство. Предпочтительные противоопухолевые средства выбирают из группы, включающей кладрибин (2-хлор-2'-дезокси(бета)-D-аденозин), хлорамбуцил (4-[бис(2-хлорэтил)амино]бензолбутановая кислота), DTIC-дом (5-(3,3-диметил-1-триазено)имидазол-4-карбоксамид), платиновые и неплатиновые химиотерапевтические средства. Содержащие платину противоопухолевые средства включают, не ограничиваясь ими, цисплатин (цис-дихлордиаминплатина). Не содержащие платины противоопухолевые средства включают, не ограничиваясь ими, циклофосфамид, фторурацил, эпирубицин, метотрексат, винкристин, доксорубицин, блеомицин и этопозид. Любое противоопухолевое средство вводят в терапевтически эффективном количестве, которое изменяется в зависимости от используемого средства, типа злокачественного заболевания, подлежащего лечению или ослаблению симптомов, и других условий, способами, хорошо известными в данной области.
Термин "субъект" в используемом здесь значении означает животное, предпочтительно млекопитающее, наиболее предпочтительно человека, являющееся объектом лечения, наблюдения или эксперимента.
Термин "терапевтически эффективное количество" в используемом здесь значении означает такое количество активного соединения или фармацевтического средства, которое вызывает биологическую или лечебную реакцию в тканевой системе, животном или человеке, которую желает получить исследователь, ветеринар, лечащий врач или другой клиницист и которая включает ослабление симптомов подлежащего лечению заболевания или нарушения.
Широко распространенный характер изоформ киназы и их важная роль в физиологии требуют создания в высшей степени селективных ингибиторов киназы. На основании данных, свидетельствующих о взаимосвязи определенных изоформ с конкретными заболеваниями, можно предположить, что ингибирующие соединения, избирательно воздействующие на одну или две изоформы (соединения, избирательно воздействующие по крайней мере на две изоформы циклинзависимой киназы или тирозинкиназы, именуются ингибиторами двух киназ) или только на одну изоформу, относительно других изоформ или других киназ, являются превосходными лечебными средствами. Такие соединения должны характеризоваться более высокой эффективностью и меньшей токсичностью благодаря своей специфичности. Поэтому специалист в данной области должен оценить то, что соединение формулы (I) является терапевтически эффективным для лечения заболеваний, опосредованных определенными, одной или двумя, киназами, благодаря селективному ингибированию одной или двух киназ. Соединения по данному изобретению обладают активностью селективных ингибиторов одной или двух киназ благодаря новой комбинации структурных элементов Х, R3 и R4, оптимально замещенных в области триазола. Пригодность соединения формулы (I) в качестве селективного ингибитора одной или двух киназ можно определить методами, приведенными в данном описании изобретения, при этом объем такой пригодности позволяет использовать указанное соединение для лечения одного или нескольких заболеваний, опосредованных одной или двумя киназами.
Поэтому термин "заболевания, опосредованные одной или двумя киназами" в используемом здесь значении включают, не ограничиваясь ими, соединения, способные ингибировать одну или несколько киназ, причем ингибирование киназы относится к раковым заболеваниям, аномальной пролиферации клеток, росту опухоли, васкуляризации опухоли, а также ангиопатии, ангиогенезу, вызванной химиотерапией алопеции и рестенозу.
Соединения по данному изобретению пригодны для использования в качестве вспомогательного средства для целого ряда химиотерапевтических средств, рекомендованных для схем лечения конкретных типов рака. Например, установлено, что соединения по данному изобретению можно использовать в комбинированной терапии по крайней мере с еще одним химиотерапевтическим средством для лечения целого ряда разных раковых заболеваний, благодаря чему можно сократить дозу химиотерапевтического средства, рекомендованного для лечения определенного типа рака или нарушения, связанного с пролиферацией клеток. Поэтому предполагается, что соединения по данному изобретению можно использовать в соответствии с лечебной схемой до введения определенного химиотерапевтического средства, рекомендованного для определенного типа рака, во время введения химиотерапевтического средства или после введения определенного химиотерапевтического средства.
Фармацевтические композиции по данному изобретению можно получить обычными методами, применяемыми в фармакологии. Композиция по данному изобретению может содержать фармацевтически приемлемый носитель. Указанную композицию можно получить в разных формах в зависимости от формы лекарственного препарата, включая, но не ограничиваясь ими, формы, предназначенные для внутривенного (в виде болюса и вливания), перорального, назального, чрескожного, местного (с окклюзией или без нее), внутрибрюшинного, подкожного, внутримышечного или парентерального введения, причем все указанные формы хорошо известны спецалистам в области фармакологии. При получении композиций в виде лекарственной формы для перорального введения можно использовать один или несколько обычных фармацевтических носителей, таких как вода, гликоли, масла, спирты, ароматизаторы, консерванты, красители, сиропы и тому подобные, в случае жидких препаратов для перорального введения (например, суспензий, эликсиров и растворов), или такие носители, как крахмалы, сахара, разбавители, гранулирующие средства, смазывающие вещества, связывающие вещества, разрыхлители и тому подобные, в случае получения твердых препаратов для перорального введения (например, порошков, капсул и таблеток).
Как известно в данной области, указанные соединения можно вводить парентерально в виде инъекции препарата, содержащего активный ингредиент, растворенный в инертном жидком носителе. Инъекционный препарат может содержать активный ингредиент в смеси с приемлемым инертным жидким носителем. Приемлемые жидкие носители включают растительные масла, такие как арахисовое масло, хлопковое масло, кунжутное масло и тому подобные, а также органические растворители, такие как солкеталь, глицерин, формаль и тому подобное. В качестве альтернативы можно также использовать водные препараты для парентерального введения. Например, приемлемые водные растворители включают воду, раствор Рингера и изотонический водный физиологический раствор. Кроме того, в качестве растворителя или суспендирующего агента в водном препарате обычно используют стерильное нелетучее масло. Указанные препараты получают растворяя или суспендируя активный ингредиент в жидком носителе в количестве, обеспечивающем содержание от 0,005 до 10 мас.% активного ингредиента в конечном препарате. Можно использовать другие добавки, включающие консервант, вещество для получения изотонического раствора, солюбилизатор, стабилизатор и болеутоляющее средство.
Кроме того, соединения по настоящему изобретению можно использовать в виде формы для введения в нос благодаря местному применению приемлемых назальных носителей или формы для чрескожного введения, представляющей чрескожные наклейки (патчи), хорошо известные специалистам в данной области. Использование системы для чрескожной доставки лекарственного средства обеспечивает схему лекарственного лечения с постоянным введением требуемой дозы, в отличие от прерывистого введения.
Благодаря простоте введения предпочтительной дозированной лекарственной формой для перорального введения являются таблетки и капсулы, в которых использованы твердые фармацевтические носители. При желании на таблетки стандартными методами может быть нанесено сахарное или энтеросолюбильное покрытие.
При получении жидких форм активный лекарственный компонент можно объединять с ароматизированными суспендирующими или диспергирующими веществами, такими как синтетические и природные камеди, включающие, например, трагакант, аравийскую камедь, метилцеллюлозу и тому подобные. Другие пригодные для использования диспергирующие вещества включают глицерин и подобные вещества.Соединения по настоящему изобретению можно также вводить в виде липосомных систем для доставки, таких как мелкие однослойные пузырьки, крупные однослойные пузырьки и многослойные пузырьки. Системы доставки, содержащие липосомы, хорошо известные в данной области, получают с использованием разных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Фармацевтические композиции по данному изобретению обычно содержат в одной дозированной лекарственной форме (такой как таблетка, капсула, порошок, инъекционный раствор, лекарственное средство, расфасованное в количестве чайной ложки, и тому подобные) от около 0,001 до около 100 мг/кг. В одном варианте осуществления изобретения фармацевтическая композиция содержит в одной дозированной лекарственной форме от около 0,01 до около 50 мг/кг соединения, предпочтительно от около 0,05 до около 20 мг/кг. В данной области известны методы определения терапевтически эффективных доз для конкретной фармацевтической композиции. Терапевтически эффективное количество, необходимое для введения человеку, можно определить, например, математически на основании результатов исследования животных.
Аббревиатуры
CSCl2 -тиофосген
DIC - диизопропилкарбодиимид
ДМФА - N,N-диметилформамид
EDCI - этилдиметиламинопропилкарбодиимид
HOBI - гидроксибензилтриазол
NH2NH2 -гидразин
Pd - палладий(II)
Ph - фенил
TBAF - фторид тетрабутиламмония
ТФУ - трифторуксусная кислота
ТГФ - тетрагидрофуран
Номенклатура
Названия, присвоенные соединениям, соответствуют номенклатуре, хорошо известной в данной области; пример названия соединения с использованием нумерации колец приведен ниже:
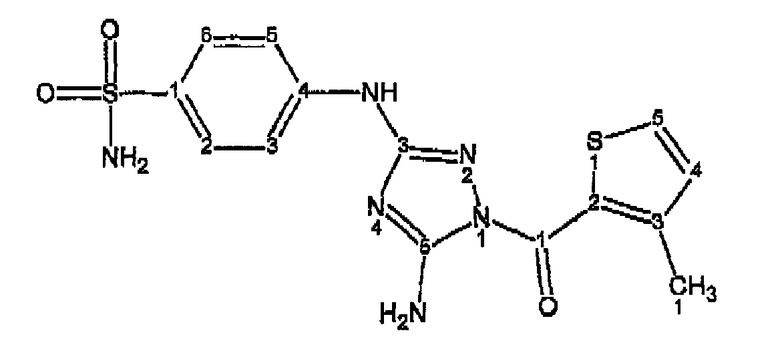
4-[[5-амино-1-[(3-метил-2-тиенил)карбонил]-1H-1,2,4-триазол-3-ил]амино]бензолсульфонамид
Названия могут быть присвоены при помощи номенклатурной системы на основании приведенного примера или могут быть созданы с использованием коммерческой программы присвоения химических названий, такой как ACD/Index Name (Advanced Chemistry Development, Inc., Toronto, Ontario).
Общие способы синтеза
Типичные соединения по настоящему изобретению могут быть синтезированы общими способами синтеза, которые описаны ниже и проиллюстрированы на схемах. Так как схемы приведены только для иллюстрации, объем изобретения не ограничен представленными химическими реакциями и условиями. Способы получения разных исходных веществ, используемых на указанных схемах, хорошо известны специалистам в данной области.
Схема А
Способ получения соединения А3 (описанный в статье Jenardanan, G.C., Francis, M., Deepa, S., and Rajaskekharan, N.R., Synthetic Communications, 1997, 27, 19, 3457-3462) заключается в том, что изоцианат, представляющий соединение А1 (полученное способом, описанным в статье R.L.McKee and R.W. Bost, J. Am. Chem. Soc., 1946, 68, 2506-2507) (где R1 имеет указанные выше значения) растворяют в приемлемом растворителе и объединяют с суспензией соединения А2 и гидроксида калия в растворителе. Смесь нагревают и перемешивают, после чего продукт, представляющий соединение А3, выделяют осаждением в холодной воде.
Способ получения соединения А5 (Reiter, J., Pongo, L. and Dvortsak, P., J. Heterocyclic Chemistry, 1987, 24, 127-142) заключается в том, что соединение А3 растворяют в приемлемом растворителе и подвергают взаимодействию с гидразином. Затем растворитель выпаривают и остаток соединения А3 нагревают с обратным холодильником в спиртовом растворителе с образованием твердого вещества, представляющего соединение А4. Соединение А4 растворяют в приемлемом растворителе и подвергают взаимодействию с R3CO2H или R3COCl (где R3 имеет указанные выше значения) и агентом сочетания, таким как DIC (диизопропилкарбодиимид) или EDCl (этилдиметиламинопропилкарбодиимид), получая при этом целевое соединение А5
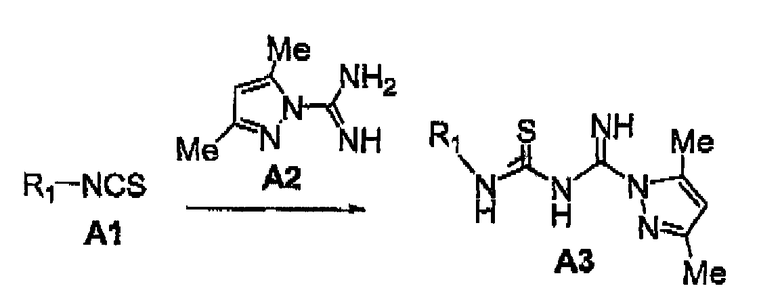
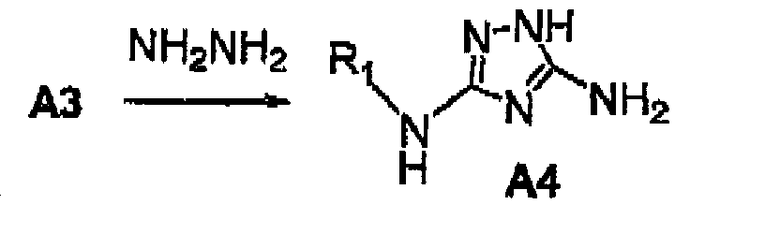
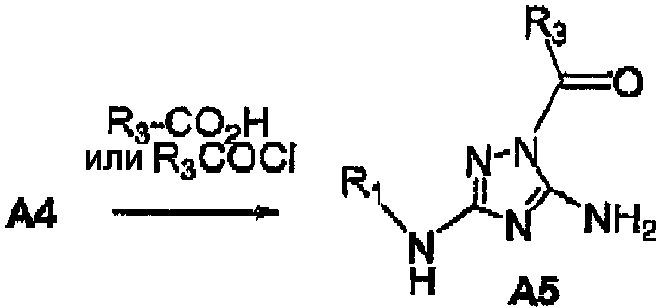
Схема В
Альтернативно соединение В3 получают способом, описанным в научной литературе (Webb, R.L., Eggleston, D.S. and Labaw, C.S., J. Heterocyclic Chemistry, 1987, 24, 275-278). В соответствии со способом, представленным на схеме А, соединение В3 подвергают взаимодействию с гидразином с образованием целевого промежуточного соединения А4.
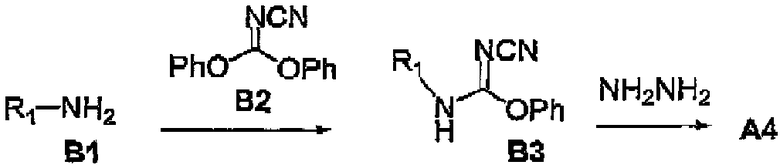
Схема С
Соединение С1 (CAS № 1455-77-2) растворяют в приемлемом растворителе и подвергают взаимодействию с R3СО2H или R3COCl (где R3 имеет указанные выше значения) и агентом сочетания, таким как DIC или EDCI, с образованием соединения С2. Соединение С2 очищают, растворяют в приемлемом растворителе и подвергают взаимодействию в инертной атмосфере с R1-галогеном (где R1 и галоген имеют указанные выше значения; помимо галогена R1 может быть связан с другой приемлемой удаляемой группой) в присутствии основания, такого как карбонат калия, и катализатора, такого как палладиевый комплекс. Продукт, представляющий соединение А5, выделяют обычными методами.
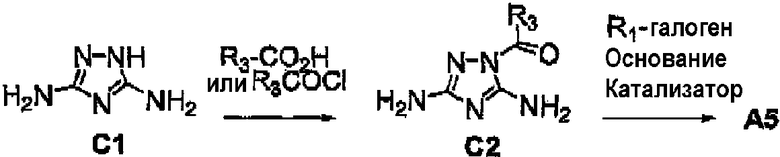
Схема D
Альтернативно соединение D1 (CAS № 24807-56-5) растворяют в приемлемом растворителе и подвергают взаимодействию с R1NH2 в присутствии основания, такого как карбонат калия, и катализатора, такого как палладиевый комплекс, с образованием соединения D2. Соединение D2 очищают, растворяют в приемлемом растворителе и подвергают каталитическому гидрированию, получая при этом соединение А4. Соединение А4 можно использовать для получения других целевых соединений по данному изобретению в соответствии со схемой А.
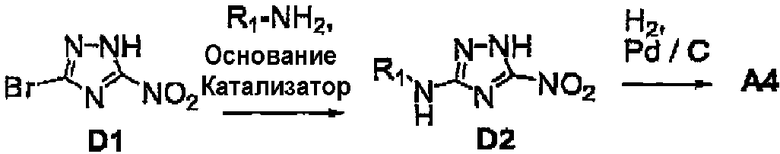
Схема Е
Соединение А3 растворяют в растворителе и подвергают взаимодействию с защитной группой, такой как замещенный бензилгалогенид (например, 4-метоксибензилбромид), в присутствии основания (такого как карбонат калия) с образованием соединения Е1. Соединение Е1 очищают, растворяют в приемлемом растворителе и подвергают взаимодействию с R2-галогеном (где R2 и галоген имеют указанные выше значения; помимо галогена R2 может быть связан с другой подходящей удаляемой группой) в присутствии основания (такого как карбонат калия), получая при этом соединение Е2. Соединение Е2 обрабатывают подходящим реагентом, таким как трифторуксусная кислота, и при нагревании получают соединение Е3. Соединение Е3 растворяют в подходящем растворителе и подвергают взаимодействию с R3CO2H или R3COCl (где R3 имеет указанные выше значения) и агентом сочетания, таким как DIC или EDCI, получая при этом целевое соединение Е4. Продукт, представляющий соединение Е4, очищают обычными методами.
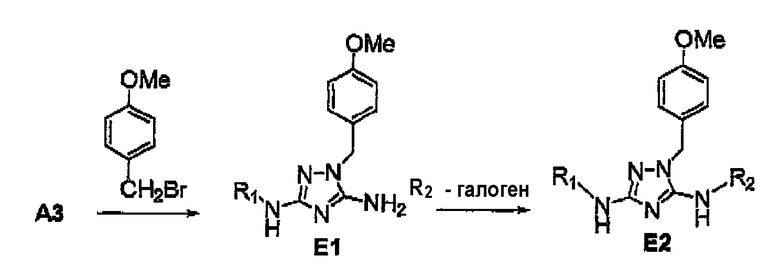
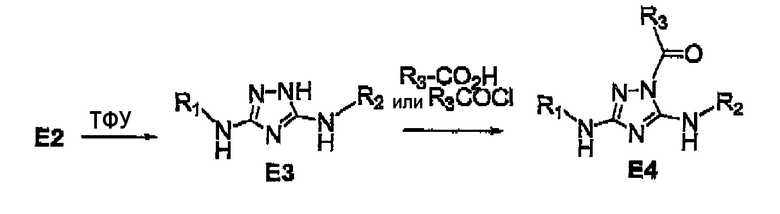
Альтернативно соединение Е4 получают растворяя соединение А5 в приемлемом растворителе и подвергая взаимодействию с R2-галогеном (где R2 и галоген имеют указанные выше значения; помимо галогена R2 может быть связан с другой подходящей удаляемой группой) в присутствии основания (такого как карбонат калия).
Специальные примеры синтеза
Конкретные характерные соединения по данному изобретению получают в соответствии с нижеследующими примерами и последовательностями реакций; примеры и схемы, отображающие последовательности реакций, приведены в качестве иллюстрации для лучшего понимания изобретения и не должны ограничивать объем изобретения, изложенного в прилагаемой формуле изобретения. Описанные промежуточные вещества могут быть также использованы в нижеследующих примерах для получения дополнительных соединений по настоящему изобретению. Выходы продуктов, получаемых при выполнении описанных реакций, не оптимизированы. Специалисту в данной области должно быть известно, как увеличить выходы продуктов в результате изменения времени реакций, температуры, растворителей и/или реагентов.
Спектры 1Н и 13С ЯМР получены в спектрометре Bruker AC-300 (300 МГц) с использованием в качестве внутренних эталонов соответственно тетраметилсилана и ДМСО. Элементные анализы выполнены в компании Quantitative Technologies Inc. (Whitehouse, New Jersey), причем полученные результаты отличаются от вычисленных значений в пределах 0,4% за исключением особо оговоренных случаев. Температуры плавления определены в открытых капиллярных трубках при помощи аппарата Mel-Temp II (Laboratory Devices Inc.) без коррекции полученных значений. Масс-спектры с электрораспылением (MS-ES) получены в спектрометре Hewlett Packard 59987A.
Пример 1
4-[[5-амино-1-(2,6-дифторбензоил)-1Н-1,2,4-триазол-
3-ил]амино]бензолсульфонамид (соединение 1)
Суспензию 1-амидино-3,5-диметилпиразолнитрата, представляющего соединение 1С (2,012 г, 10 ммоль), и порошкообразного гидроксида калия (0,561 г, 10 ммоль) в ДМФА (8 мл) при 0°С добавляют к раствору (3 мл) изоцианата, представляющего соединение 1В (полученного из сульфаниламида, представляющего соединение 1А, и тиофосгена способом, описанным в статье R.L McKee and R.W. Bost, J. Am. Chem. Soc., 1946, 68, 2506-2507), в ДМФА. Реакционную смесь нагревают до 50-60°С, перемешивают в течение 1 часа и выливают в 250 мл смеси воды со льдом. Образовавшееся желтое твердое вещество фильтруют, промывают водой и сушат в вакууме, получая при этом промежуточное соединение 1D в виде желтого порошка (2,5513 г); т.п. 69-80°С (разложение). 1H ЯМР (300 МГц, CD3OD) δ 7,90 (м, 4H), 6,05 (с, 1H), 2,22 (с, 3H), 2,20 (с, 3H); (CDCl3) δ 10,75 (с, шир, 1H), 8,35 (с, шир, 1H), 7,90 (кв, 4H), 7,65 (c, шир, 2H), 5,95 (с, 1H), 5,00 (c, шир, 2H); MS (ESI) m/z: 353 (М+H+).
Гидразин (1,845 г, 57,58 ммоль) добавляют к раствору промежуточного соединения 1D (1,88 г, 5,33 ммоль) в ТГФ (60 мл). Реакционную смесь интенсивно перемешивают при 50-60°С в течение 2-3 часов и упаривают в вакууме. Остаток нагревают с обратным холодильником в метаноле (60 мл) и охлаждают до комнатной температуры. Образовавшееся твердое вещество собирают фильтрованием и промывают метанолом, получая при этом промежуточное соединение 1Е в виде серого твердого вещества (0,8722 г, 64%); т.п. 291-296°С (разложение); 1H ЯМР (300 МГц, (CD3)2SO) δ 9,20 (с, 1H), 7,60 (м, 4H), 7,00 (с, 2H), 5,90 (с, 2H); MS (ESI) m/z: 255 (М+H+), 277 (М+Na+).
2,6-Дифторбензоилхлорид, представляющий соединение 1F (41,4 мкл, 0,33 ммоль), добавляют к раствору промежуточного соединения 1Е (63,6 мг, 0,25 ммоль) в безводном пиридине (2,5 мл) на бане со смесью воды со льдом. Полученную реакционную смесь перемешивают при комнатной температуре в течение 6 часов и упаривают в вакууме досуха. Остаток очищают хроматографией с использованием 10% метанола/метиленхлорида и перекристаллизовывают из ТГФ/метиленхлорида, получая при этом соединение 1 (50,2 мг, 51%) в виде белого порошка, т.п. 149-155°С (разложение); 1H ЯМР (300 МГц, CD3OD) δ 7,65 (м, 3Н), 7,55 (д, 2Н), 7,18 (т, 2Н); ((CD3)2SO) δ 9,86 (с, 1Н), 8,03 (с, 2Н), 7,72 (м, 1Н), 7,58 (д, J=8,9 Гц, 2Н), 7,46 (д, J=8,9 Гц, 2H), 7,35 (т, J=8,3 Гц, 2Ц), 7,11 (с, 2H); 13С ЯМР (300 МГц, (CD3)2SO) δ 160,4, 159,7, 158,9, 157,9, 157,1, 157,0, 156,6, 144,0, 135,6, 133,9, 127,0, 116,3, 112,9, 112,5, 112,3; MS (ESI) m/z: 395 (М+H+), 417 (М+Na+). Элементный анализ. Вычислено для С15Н12F2N6O3S: C 45,69; H 3,07; N 21,31. Найдено: С 45,29; H 3,04; N 20,89.
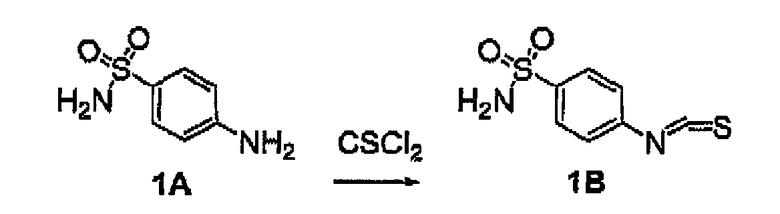
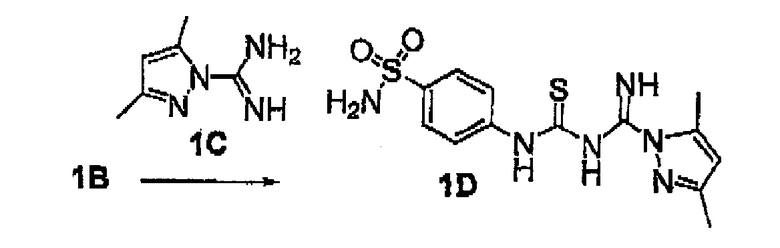
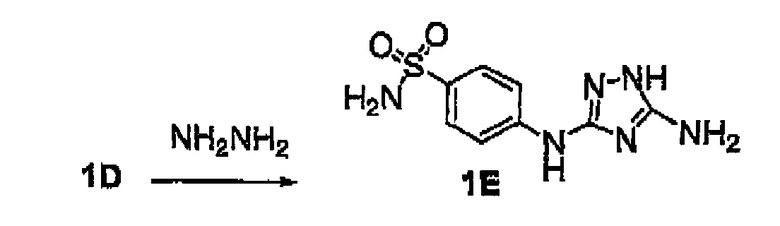
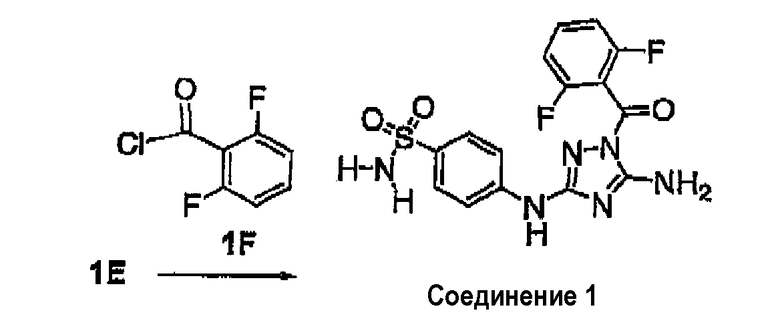
Нижеследующие соединения получают ацилированием промежуточного соеднения 1Е способом по примеру 1, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2CO) δ 8,80 (c, 1Н), 7,78-7,55 (м, 5H), 7,52 (с, 2H), 7,12 (т, 2H), 6,38 (с, 2H), 2,22 (с, 3Н); MS (ESI) m/z: 409 (М+H+), 431 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,85 (с, 1H), 7,78-7,50 (м, 7H), 7,32 (м, 1H), 6,38 (с, 2H); MS (ESI) m/z: 413 (М+H+), 435 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,90 (с, шир, 1H), 8,00 (с, шир, 2H), 7,82 (т, 1H), 7,78-7,20 (м, 7H), 6,35 (с, шир, 2H); MS (ESI) m/z: 377 (М+H+), 399 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,88 (с, 1H), 7,95 (с, 2H), 7,78-7,58 (м, 4H), 7,48 (с, 2H), 7,35-7,77 (м, 2H), 6,38 (с, 2H); MS (ESI) m/z: 395 (М+H+), 417 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,86 (с, 1H), 8,06 (с, 2H), 7,85 (м, 3H), 7,54 (д, J=8,9 Гц, 2H), 7,40 (д, J=8,9 Гц, 2H), 7,09 (с, 2H); MS (ESI m/z: 445 (M+H+), 467 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,82 (с, 1H), 7,68-7,45 (м, 9H), 6,35 (с, 2H); (CD3OD) 7,60 (д, 2H), 7,55 (м, 3H), 7,38 (д, 2H); MS (ESI) m/z: 428 (М+H+), 450 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,88 (с, 1H), 7,78 (с, 2H), 7,75-7,48 (м, 6H), 6,38 (с, 2H); MS (ESI) m/z: 462 (М+Н+), 484 (М+Na+)
1H ЯМР (300 МГц, CD3OD) δ 8,28 (д, 2H), 8,95-7,85 (м, 3Н), 7,62 (д, 2H), 7,35 (д, 2H); MS (ESI) m/z: 404 (М+Н+), 426 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,65 (с, шир, 1H), 7,68 (м, 4H), 7,50 (д, 1H), 7,30 (с, шир, 2H), 6,72 (д, 1H), 6,68 (дд, 1H), 6,35 (с, шир, 2H), 3,92 (с, 3H), 3,85 (с, 3H); MS (ESI) m/z: 419 (М+H+), 441 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,78 (с, 1H), 7,78 (с, 2H), 7,72-7,43 (м, 5H), 7,75-6,78 (м, 3H), 6,35 (с, 2H), 2,38-2,16 (м, 9H); MS (ESI) m/z 401 (М+H+), 423
(М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,80 (с, 1H), 8,28 (д, 2H), 7,80-7,58 (м, 7H), 7,52 (с, 2H), 6,38 (с, 2H); MS (ESI) m/z: 359 (М+H+), 381 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,92 (с, 1H), 8,40 (дд, 1H), 8,12 (дд, 1H), 7,88 (кв, 4H), 7,50 (с, 2H), 7,32 (т, 1H), 6,45 (с, 2H); MS (ESI) m/z: 365 (М+H+), 387 (М+Na+)
т.п. 280-284°С; 1H ЯМР (300 МГц, (CD3)2SO) δ 9,88 (с, 1H), 8,05 (д, 1H), 7,88 (c, 2H), 7,78 (кв, 4H), 7,15 (м, 3H), 2,62 (с, 3Н);
(CD3)2CO) δ 8,92 (с, 1H), 7,98 (д, 1H), 7,90 (кв, 4H), 7,45 (c, 2H), 7,15 (д, 1H), 6,42 (с, 2H), 2,68 (с, 3H);
13C ЯМР (300 МГц, (CD3)2SO) δ 160,6, 157,9, 157,4, 157,2, 150,9, 143,9, 136,0, 135,5, 131,8, 127,3, 124,3, 116,3, 18,1; MS (ESI) m/z: 379 (М+H+), 401 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,92 (с, шир, 1Н), 8,18 (т, 1Н), 7,92 (с, шир, 2H), 7,78 (кв, 4H), 7,25 (д, 1Н), 7,18 (с, шир, 2H); MS (ESI) m/z: 383 (М+H+), 405 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,92 (с, шир, 1H), 8,25 (д, 1H), 7,95 (с, шир, 2H), 7,78 (кв, 4H), 7,32 (д, 1H), 7,18 (с, шир, 2H); MS (ESI) m/z: 399 (М+H+), 421 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (с, шир, 1H), 8,08 (д, 1H), 7,85-7,75 (м, 6H), 7,28 (д, 1H), 7,15 (с, шир, 2H); MS (ESI) m/z: 409 (М+H+), 431 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 11,0 (с, шир, 1H), 9,92 (с, шир, 1H), 8,18 (кв, 2H), 7,85 (с, шир, 2H), 7,78 (кв, 4H), 7,15 (с, шир, 2H), 2,20 (с, 3H); MS (ESI) m/z: 421 (М+H+), 444 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,92 (с, шир, 1H), 8,15 (д, 1H), 7,85 (с, шир, 2H), 7,78 (кв, 4H), 7,20 (с, шир, 2H), 7,08 (д, 1H), 2,62 (c, 3H); MS (ESI) m/z: 379 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,98 (с, шир, 1H), 8,05 (д, 1H), 7,95 (c, шир, 2H), 7,78 (кв, 4H), 7,48 (д, 1H), 7,20 (с, шир, 2H); MS (ESI) m/z; 444 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,02 (c, шир, 1H), 8,28 (д, 1H), 8,02 (д, 1H), 7,95 (c, шир, 2H), 7,75 (кв, 4H), 7,20 (с, шир, 2H), 2,65 (c, 3H); MS (ESI) m/z: 407 (M+H+), 429 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,87 (с, 1H), 8,20 (д, 1H), 8,02 (дд, 1H), 7,85 (кв, 4H), 7,48 (c, 2H), 6,88 (дд, 1H), 6,42 (с, 2H); MS (ESI) m/z: 349 (М+H+), 371 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,95 (с, шир, 1H), 8,92 (д, 1H), 8,00 (c, шир, 2H), 7,78 (м, 2H), 7,68 (м, 3H), 7,15 (с, шир, 2H); MS (ESI) m/z: 350 (М+H+), 372 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,75 (с, 1H), 8,72 (д, 1H), 8,00 (м, 2H), 7,90 (с, шир, 2H), 7,68-7,48 (м, 5H), 7,10 (с, шир, 2H); MS (ESI) m/z: 360 (М+H+), 382 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,82 (с, 1H), 9,22 (д, 1H), 8,78 (дд, 1H), 8,45 (дд, 1H), 7,92 (c, шир, 2H), 77,62 (кв, 4H), 7,15 (с, шир, 2H); MS (ESI) m/z: 360 (М+H+), 382 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,80 (с, 1H), 8,82 (д, 2H), 8,00-7,90 (м, 4H), 7,60 (кв, 4H), 7,12 (с, шир, 2H); MS (ESI) m/z: 360 (М+H+), 382 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 9,08 (д, 1H), 8,85 (с, шир, 1H), 7,98 (дд, 1H), 7,82 (кв, 4H), 7,62 (дд, 1H), 7,48 (с, шир, 1H), 6,45 (с, шир, 2H); MS (ESI) m/z: 365 (М+H+), 387(М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,95 (с, шир, 1H), 8,85 (с, 1H), 8,15 (дд, 2H), 8,02 (с, шир, 2H), 7,85 (кв, 4H), 7,55 (м, 2H), 7,18 (с, шир, 2H); MS (ESI) m/z: 415 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,88 (с, шир, 1H), 7,90 (c, шир, 2H), 7,78 (кв, 4H), 7,15 (с, шир, 2H), 2,78 (c, 6Н); MS (ESI) m/z: 394 (М+H+), 416 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,95 (c, 1H), 8,23 (д, J=5,31H), 7,95 (с, 2H), 7,77 (с, 4H), 7,39 (д, J=5,3 1H), 7,16 (с, 2H); MS (ESI) m/z: 444,9 (М+H), 466,9 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,07 (с, 1H), 8,09 (с, 2H), 7,86 (д, J=8,8, 2H), 7,72 (д, J=8,9, 2H), 7,21 (с, 2H), 3,02 (c, 3Н); MS (ESI) m/z: 381,0 (М+H), 403,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,18 (с, 1H), 9,93 (с, 1H), 8,05 (с, 2H), 7,76 (д, J=8,8, 2H), 7,63 (д, J=8,8, 2H), 7,16 (с, 2H); MS (ESI) m/z: 367,0 (М+H), 389,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,73 (с, 1H), 7,69 (с, 4H), 7,65 (с, 2H), 7,13 (c, 2H), 1,78 (м, 3Н), 1,65 (м, 6H); MS (ESI) m/z: 351,0 (М+H), 373,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,76 (с, 1H), 7,69 (с, 4H), 7,66 (с, 2H), 7,13 (c, 2H), 1,98 (c, 2H), 1,80 (c, 2H), 1,69 (д, 1H), 1,36 (м, 6Н); MS (ESI) m/z: 365,0 (М+H), 387,1 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,80 (с, 1H), 7,73 (д, J=1,2, 4H), 7,69 (с, 2H), 7,45 (дд, J=1,5, 1H), 7,16 (с, 2H), 7,08 (д, J=2,7, 1H), 7,01 (т, J=5,1, 1H), 4,52 (с, 2H);
MS (ESI) m/z: 379,0 (М+H), 400,9 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,82 (с, 1H), 7,92 (д, J=8,3, 1H), 7,72 (с, 4H), 7,35 (д, J=15,8, 2H), 7,26 (д, J=19,5, 3Н), 7,15 (с, 2H), 6,26 (c, 1H); MS (ESI) m/z: 391,0 (М+H), 412,9 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,81 (с, 1H), 7,69 (с, 6H), 7,44 (т, J=16,6, 1H), 7,16 (с, 3Н), 4,37 (с, 2H); MS (ESI) m/z: 409,0 (М+H), 431,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,86 (с, 1H), 7,85 (д, J=4,7, 2H), 7,71 (с, 4H), 7,31 (м, 4H), 7,16 (с, 2H), 6,31 (с, 1H); MS (ESI) m/z: 421,0 (М+H), 442,9 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,75 (с, 1H), 7,69 (c, 4H), 7,66 (c, 2H), 7,12 (c, 2H), 2,00 (д, J=11,7, 2H), 1,77 (д, J=10,5, 2H), 1,40 (м, 3H), 1,07 (м, 2H), 0,91 (д, J=6,4, 4H); MS (ESI) m/z: 254, 379,0 (М+H), 401,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,75 (с, 1H), 7,69 (с, 4H), 7,66 (с, 2H), 7,12 (c, 2H), 2,00 (д, J=11,7, 2H), 1,77 (д, J=10,5, 2H), 1,40 (м, 3H), 1,07 (м, 2H), 0,91 (д, J=6,4, 4H); MS (ESI) m/z: 254, 379,0 (М+H), 401,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,75 (с, 1H), 7,68 (c, 4H), 7,66 (с, 2H), 7,13 (c, 2H), 1,55 (м, 9H), 0,85 (д, J=6,0, 4H); MS (ESI) m/z: 254, 379,0 (М+H), 401,0 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,75 (с, 1H), 7,68 (с, 4H), 7,66 (c, 2H), 7,12 (c, 2H), 2,02 (д, J=11,3, 2H), 1,82 (д, J=9,9, 2H), 1,40 (д, J=11,3, 2H), 1,25 (с, 7H), 1,02 (м, 4H), 0,87 (с, 4H); MS (ESI) m/z: 254, 435,1 (М+H), 457,1 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,98 (с, 1H), 8,65 (д, 1H), 8,25 (д, 1H), 8,08 (д, 1H), 8,02-7,75 (м, 8Н), 7,42 (дд, 1H), 7,20 (с, 2H); MS (ESI) m/z: 442 (М+H+), 464 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (c, 1Н), 8,18 (д, 1Н), 7,85-7,70 (м, 6H), 7,32 (д, 1H), 7,18 (с, 2H), 7,12 (т, 2H), 6,20 (т, 2H); MS (ESI) m/z: 430 (М+H+)
1H ЯМР (300 МГц, (CD3)2CO) δ
8,95 (с, 1H), 8,25 (д, 1H), 7,95 (д, 2H), 7,85 (д, 2H), 7,50 (с, 2H), 7,18 (д, 1H), 6,48 (с, 2H), 1,55 (с, 9H); MS (ESI) m/z: 421 (М+H+), 443 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,95 (с, 1H), 8,22 (д, 1H), 7,95 (с, 2H), 7,82-7,68 (м, 6H), 7,15 (с, 2H), 6,52 (д, 1H), 1,52 (с, 9H); MS (ESI) m/z: 491 (М+H+), 513 (М+Na+)
5-(2-трет-бутоксикарбонилвинил)тиофен-2-карбоновая кислота (промежуточное соединение) 1H ЯМР (300 МГц, (CD3)2CO) δ 7,80-70 (м, 2Н), 7,48 (д, 1Н), 7,32 (д, 1Н), 1,50 (с, 9Н), MS (ESI) m/z: 253 (M-H+), 209 (M-H+-CO2)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,98 (с, 1H), 8,20 (д, 1H), 7,95 (с, 2H), 7,78 (м, 4Н), 7,62 (м, 2H), 7,60 (д, 1H), 7,45 (м, 3H), 7,18 (с, 2H); MS (ESI) m/z: 465 (М+H+), 487 (М+Na+)
5-фенилэтинилтиофен-2-карбоновая кислота (промежуточное соединение)
1H ЯМР (300 МГц, (CD3)2CO) δ 7,98 (д, 1Н), 7,58 (м, 2Н), 7,45 (м, 3Н), 7,35 (д, 1Н); MS (ESI) m/z: 229 (М+H+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,90 (с, 1H), 8,55 (м, 1H), 7,75-7,50 (м, 7Н), 6,25 (с, 2H); MS (ESI) m/z: 440 (М+H+), 462 (М+Na+)
1H ЯМР (300 МГц, CD3OD) δ 7,68 (д, 2H), 7,45 (д, 2H), 6,95 (м, 1Н), 6,85 (м, 1Н); MS (ESI) m/z: 410 (М+H+), 432 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ
8,75 (с, 1Н), 7,65-7,28 (м, 7H), 7,15 (д, 2H), 6,32 (с, 2H), 2,25 (с, 6H); MS (ESI) m/z: 387 (М+H+), 409 (М+Na+).
1H ЯМР (300 МГц, (CD3)2CO) δ 8,75 (с, 1Н), 7,72-7,25 (м, 10Н), 6,35 (с, 2H), 2,45 (с, 3Н); MS (ESI) m/z: 373 (М+H+), 395 (М+Na+).
1H ЯМР (300 МГц, (CD3)2CO) δ 10,40 (с, 1H), 8,90 (с, 1Н), 8,15 (с, 2H), 7,85 (д, 2H), 7,75 (д, 2H), 7,40 (м, 1Н), 7,15 (м, 2H), 6,35 (с, 2H), 5,75 (с, 2H); MS (ESI) m/z: 426 (М+H+), 448 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 9,15 (с, 1Н), 8,80 (с, 1Н), 7,80 (д, 2H), 7,70 (д, 2H), 7,42 (м, 1Н), 7,15 (м, 2H), 7,00 (с, 2H), 6,35 (с, 2H); MS (ESI) m/z: 410 (М+H+), 432 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 8,80 (с, 1Н), 7,85 (м, 1Н), 7,75 (д, 2H), 7,65 (д, 2H), 7,30 (т, 2H), 6,95 (с, 2H), 6,35 (с, 2H); MS (ESI) m/z: 431 (М+H+), 453 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (с, 1Н), 8,05 (c, 2H), 7,64-7,55 (м, 3Н), 7,45-7,35 (м, 3Н), 7,10 (c, 2H), 2,38 (с, 3Н); MS (ESI) m/z: 425 (М+H+), 447 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,87 (с, 1H), 8,05 (с, 2H), 7,68-7,63 (м, 1H), 7,57-7,50 (м, 3H), 7,48-7,42 (м, 3H), 7,09 (c, 2H); MS (ESI) m/z; 411 (М+H+), 433 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,89 (c, 1H), 8,07 (c, 2H), 8,00-7,92 (т, 1Н), 7,59 (д, 2Н), 7,49-7,44 (м, 3H), 7,12 (с, 2Н); MS (ESI) m/z: 429 (М+H+)
(второстепенный изомер положения соединения 1)
1H ЯМР (300 МГц, CD3CN) δ 9,90 (с, 1H), 7,90 (кв, 4H), 7,60 (м, 1H), 7,15 (т, 2Н), 5,62 (с, 2Н), 4,85 (с, 2Н); MS (ESI) m/z: 395 (М+H+), 417 (М+Na+)
(второстепенный изомер положения соединения 2)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,0 (c, 1H), 8,00 (д, 2Н), 7,78 (д, 2Н), 7,50 (м, 1H), 7,20 (с, 2Н), 7,15 (т, 2Н), 6,25 (с, 2H), 2,28 (с, 3H); MS (ESI) m/z: 409 (М+H+), 431 (М+Na+)
(второстепенный изомер положения соединения 66)
1H ЯМР (300 МГц, (CD3)2CO) δ
12,10 (с, 1H), 10,28 (8,1H), 7,85 (м, 4Н), 7,45 (м, 1H), 7,20 (м, 2Н), 6,45 (с, 2Н), 5,75 (с, 2H);
MS (ESI) m/z: 426 (М+Н+), 448 (М+Na+)
Пример 2
1-(2,6-Дифторбензоил)-N3-[4-(1-пиперидинилсульфонил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 13)
1-Амидино-3,5-диметилпиразолнитрат, представляющий соединение 1С, подвергают взаимодействию с 1-(4-изотиоцианатофенилсульфонил)пиперидином, представляющим соединение 2В, способом по примеру 1, получая при этом соединение 2С. 1H ЯМР (300 МГц, CD3CN) δ 10,75 (c, шир, 1Н), 8,40 (с, шир, 1Н), 7,95 (с, шир, 1Н), 7,55 (кв, 4Н), 5,95 (с, 1Н), 3,00 (м, 4Н), 2,25 (с, 6Н), 1,68 (м, 4Н), 1,45 (м, 2Н); MS (ESI) m/z: 421 (M+H+).
Соединение 2С подвергают взаимодействию с гидразином, получая при этом соединение 2D. 1H ЯМР (300 МГц, CD3CN) δ 10,75 (c, шир, 1Н), 7,65 (с, шир, 1H), 7,55 (кв, 4H), 5,85 (с, шир, 2H), 2,82 (м, 4Н), 1,55 (м, 4H), 1,32 (м, 2H); MS (ESI) m/z: 323 (М+H+).
Соединение 2D ацилируют 2,6-дифтор-3-метилбензоилхлоридом, представляющим соединение 1F, в безводном пиридине, получая при этом соединение 13 (выход 85%). 1H ЯМР (300 МГц, CDCl3): δ 7,60-7,50 (м, 3H), 7,42 (д, 2H), 7,18 (т, 2H), 6,98 (с, шир, 1H), 6,55 (с, шир, 2H), 2,98 (м, 4H), 1,65 (м, 4H), 1,42 (м, 2H); MS (ESI) m/z: 363 (М+H+), 485 (М+Na+).
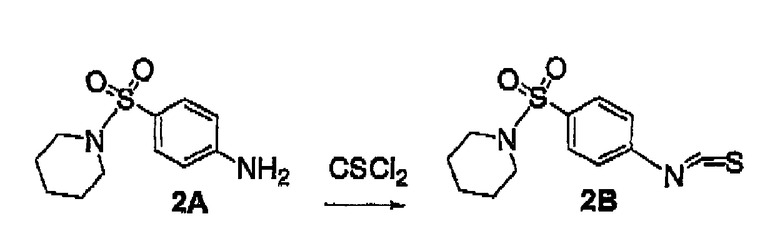
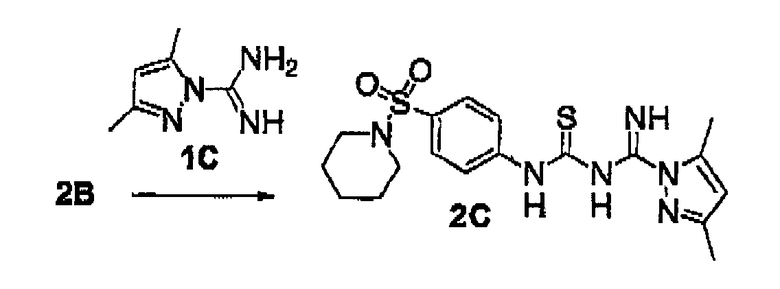
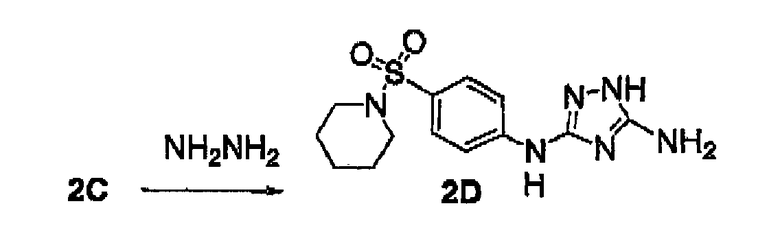
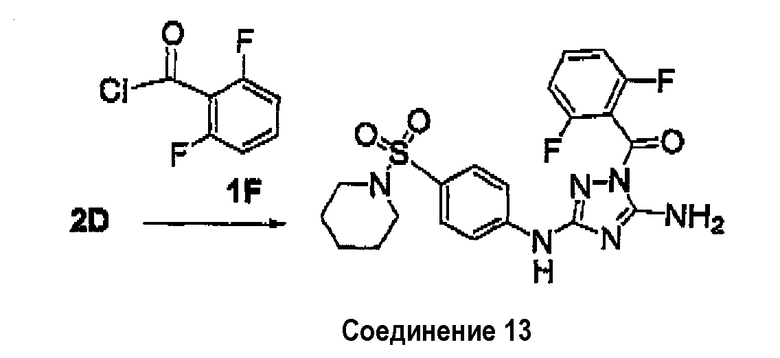
Нижеследующие соединения получают ацилированием промежуточного соединения 2D способом по примеру 3, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 10,02 (с, шир, 1H), 8,40 (дд, 1H), 8,18 (дд, 1H), 7,92 (c, шир, 2H), 7,88 (д, 2H), 7,58 (д, 2H), 7,32 (т, 1H), 2,88 (м, 4H), 1,55 (м, 4H), 1,35 (м, 2H); MS (ESI) m/z: 433 (М+H+), 455 (М+Na+)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,02 (с, шир, 1H), 8,02 (д, 1H), 7,95-7,80 (м, 4H), 7,68 (д, 2H), 7,18 (д, 1H), 2,88 (м, 4H), 2,68 (c, 3Н), 1,55 (м, 4H), 1,35 (м, 2H); MS (ESI) m/z: 447 (М+H+), 469 (М+Na+)
Пример 3
4-[[5-Амино-1-[(5-этил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]бензолсульфонамид (соединение 32)
Моногидрат гидразина (0,97 мл, 1,019 моль) и гидроксид калия (1,12 г, 20 ммоль) добавляют к раствору 5-ацетилтиофен-2-карбоновой кислоты (1,70 г, 10 ммоль) в диэтиленгликоле (20 мл) и воде (1 мл). Реакционную смесь перемешивают на масляной бане при 110°С в течение 16 часов, охлаждают до комнатной температуры, подкисляют 2 н. раствором HCl и экстрагируют метиленхлоридом (4×50 мл). Органические слои объединяют, сушат, концентрируют и разделяют хроматографией на силикагеле (производя элюирование смесью 10% метанол/метиленхлорид), получая при этом 3-этилтиофен-2-карбоновую кислоту, представляющую соединение 3А, в виде бледно-желтого твердого вещества (1,161 г, 74%). 1H ЯМР (300 МГц, CD3OD) δ 7,59 (д, J=3,7, 1H), 6,87 (д, J=3,7, 1H), 2,88 (кв, J=7,5, 1Н), 1,32 (т, J=7,5, 3Н); MS (ESI) m/z: 155 (M-H+).
Соединение 1Е ацилируют соединением 3А, при посредстве DIC/HOBt, в безводном ДМФА способом по примеру 1, получая при этом соединение 32 (выход 59%). 1H ЯМР (300 МГц, (CD3)2CO) δ 8,90 (с, шир, 1H), 8,25 (д, 1H), 7,88 (кв, 4H), 7,45 (с, шир, 2H), 7,10 (д, 1H), 6,45 (c, шир, 2H), 3,05 (кв, 2H), 1,42 (т, 3H); MS (ESI) m/z: 393 (М+H+), 415 (М+Na+).
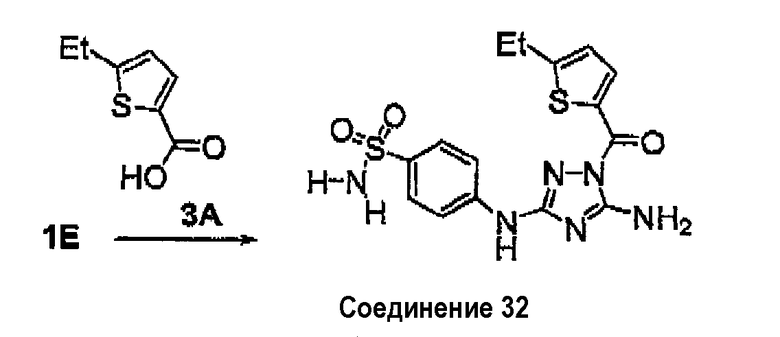
Пример 4
4-[[5-Амино-1-[(3,5-диметил-2-тиенил)карбонил]-1H-1,2,4-триазол-3-ил]амино]бензолсульфонамид (соединение 33)
2,2 эквивалента 2,0 М раствора LDA в гептане/ТГФ/этилбензоле (0,97 мл, 1,019 моль) добавляют к раствору 3-метилтиофен-2-карбоновой кислоты (1,42 г, 10 ммоль) в безводном ТГФ (20 мл) при 0°С. Реакционную смесь перемешивают при 0°С в течение 1,5 часов и затем добавляют метилиодид (1,4 мл, 22 ммоль). Полученную смесь перемешивают при 0°С еще 2 часа, подкисляют 2 н. раствором HCl и экстрагируют метиленхлоридом (4×50 мл). Органические слои объединяют, концентрируют и разделяют ВЭЖХ, получая при этом 3,5-диметилтиофен-2-карбоновую кислоту, представляющую соединение 4А, в виде белого порошка. 1H ЯМР (300 МГц, CD3OD) δ 6,72 (с, 1H), 2,43 (с, 3H), 2,46 (с, 3H); MS (ESI) m/z: 155 (М-H+).
Соединение 1Е ацилируют соединением 4А, при посредстве DIC/HOBt, в безводном ДМФА способом по примеру 1, получая при этом соединение 33 (выход 73%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,88 (с, шир, 1H), 7,85 (c, шир, 2H), 7,78 (кв, 4H), 7,18 (с, шир, 2H), 6,92 (с, 1H), 2,58 (c, 3Н), 2,55 (с, 3H); MS (ESI) m/z: 393 (М+H+), 415 (М+Na+).
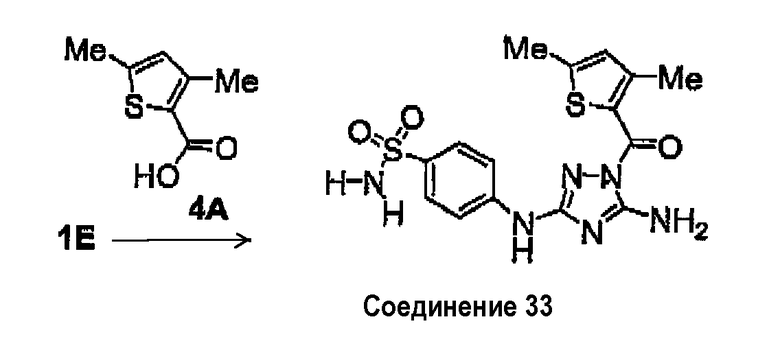
Пример 5
4-[[5-Амино-1-[2,6-дифтор-3-(1-гидроксиэтил)бензоил]-1Н-1,2,4-триазол-3-ил]амино]бензолсульфонамид (соединение 58)
2',4'-Дифторацетофенон (5 г, 32 ммоль) подвергают взаимодействию с борогидридом натрия (1,21 г) в ТГФ (20 мл) и метаноле (10 мл) в течение 1 часа. Полученную смесь упаривают досуха и распределяют между метиленхлоридом и водой. Органический слой отделяют, сушат и упаривают, получая при этом 1-(2',4'-дифторфенил)этанол в виде бесцветного масла (4,86 г, 96%). 1H ЯМР (300 МГц, CDCl3) δ 7,48 (м, 1Н), 6,85 (м, 1Н), 6,75 (м, 1Н), 5,15 (кв, 1Н), 2,0 (с, 1Н), 1,5 (д, 3Н).
1-(2',4'-Дифторфенил)этанол (5,384 г, 34 ммоль), трет-бутилтриметилсилилхлорид (6,148 г, 40,8 ммоль) и имидазол (5,567 г, 81,8 ммоль) в ДМФА (60 мл) объединяют и перемешивают при комнатной температуре в течение ночи. Полученную смесь упаривают досуха в вакууме и остаток распределяют между метиленхлоридом и водой. Органический слой отделяют, сушат и упаривают, получая при этом 1-(2',4'-дифторфенил)этил-трет-бутилтриметилсилиловый эфир в виде белого твердого вещества (6,88 г, 74%). 1H ЯМР (300 МГц, CDCl3) δ 7,45 (кв, 1H), 6,75 (м, 1H), 6,62 (м, 1H), 5,05 (кв, 1H), 1,32 (д, 3H), 0,88 (с, 9H), 0,05 и 0,01 (оба синглет, оба 3Н).
1,6 М раствор н-бутиллития в гексане (3,75 мл, 6 ммоль) по каплям добавляют к раствору 1-(2',4'-дифторфенил)этил-трет-бутилтриметилсилилового эфира (1,362 г, 5 ммоль) в ТГФ (60 мл) при -50°С и перемешивают при той же температуре в течение 3 часов. Реакционную смесь выливают на сухой лед и упаривают досуха. Остаток распределяют между метиленхлоридом и водой и подкисляют уксусной кислотой. Органический слой отделяют, сушат и упаривают, получая при этом 2,6-дифтор-3-(1-трет-бутилтриметилсилилоксиэтил)бензойную кислоту, представляющую соединение 5А, в виде белого твердого вещества (1,57 г, 99%). 1H ЯМР (300 МГц, CDCl3) δ 7,70 (кв, 1H), 7,00 (т, 1H), 6,00 (шир, 1Н), 5,15 (кв, 1H), 1,40 (д, 3H), 0,90 (с, 9H), 0,12 и 0,05 (оба синглет, оба 3H).
Соединение 1Е ацилируют соединением 5А, связанным DIC/HOBt, в безвводном ДМФА способом по примеру 1, получая при этом 4-[[5-амино-1-(2,6-дифтор-3-(1-трет-бутилтриметилсилилоксиэтил)бензоил)-1Н-1,2,4-триазол-3-ил]амино]бензолсульфонамид, представляющий соединение 5В (выход 46%). 1H ЯМР (300 МГц, CDCl3) δ 7,72 (м, 3H), 7,38 (д, 2H), 7,02 (т, 1H), 6,80 (с, 1H), 6,45 (с, 2H), 5,15 (кв, 1H), 4,68 (с, 2Н), 1,15 (д, 3H), 0,92 (с, 9H), 0,10 (с, 3H), 0,02 (с, 3H); MS (ESI) m/z: 553 (М+H+), 575 (M+Na+).
Из реакционной смеси выделяют также 4-[[5-амино-2-(2,6-дифтор-3-(1-трет-бутилтриметилсилилоксиэтил)бензоил)-2Н-1,2,4-триазол-3-ил]амино]бензолсульфонамид (второстепенный изомер положения) (192 мг, 34%). 1H ЯМР (300 МГц, CDCl3): δ 10,00 (с, 1H), 7,92 (д, 2H), 7,82 (д, 2H), 7,70 (кв, 1H), 7,02 (т, 1H), 5,18 (кв, 1H), 4,82 (с, 2H), 4,32 (c, 2H), 1,42 (д, 3H), 0,92 (с, 9H), 0,10 (с, 3H), 0,02 (c, 3H); MS (ESI) m/z: 553 (М+H+), 575 (М+Na+).
0,7 мл 1,0 М раствора TBAF в ТГФ добавляют к раствору 4-[[5-амино-1-(2,6-дифтор-3-(1-трет-бутилтриметилсилилоксиэтил)бензоил)-1Н-1,2,4-триазол-3-ил]амино]бензолсульфонамида, представляющего соединение 5В (193 мг, 0,35 моль), в ТГФ (10 мл). Реакционный раствор перемешивают при комнатной температуре в течение 1 часа и упаривают досуха. Образовавшийся остаток подвергают хроматографии на колонке с силикагелем, производя элюирование смесью 20% метанола/метиленхлорид, получая при этом продукт, представляющий соединение 58, в виде белой пены (90 мг, 59%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (с, 1H), 8,00 (с, 2H), 7,75 (м, 1H), 7,55 (м, 2H), 7,45 (м, 2H), 7,30 (т,1Н), 7,10 (с, 2H), 6,80 (с, 1H), 5,55 (д, 1H), 5,00 (м, 1H), 1,38 (д, 3H); MS (ESI) m/z: 421 (М+Н+-H2O), 439 (М+H+), 461 (М+Na+).
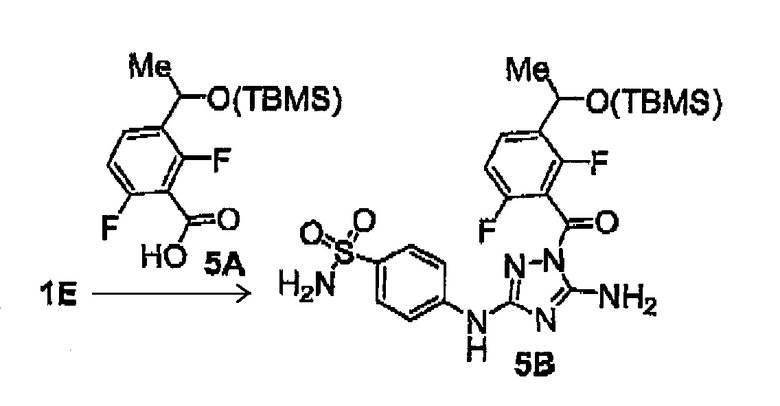
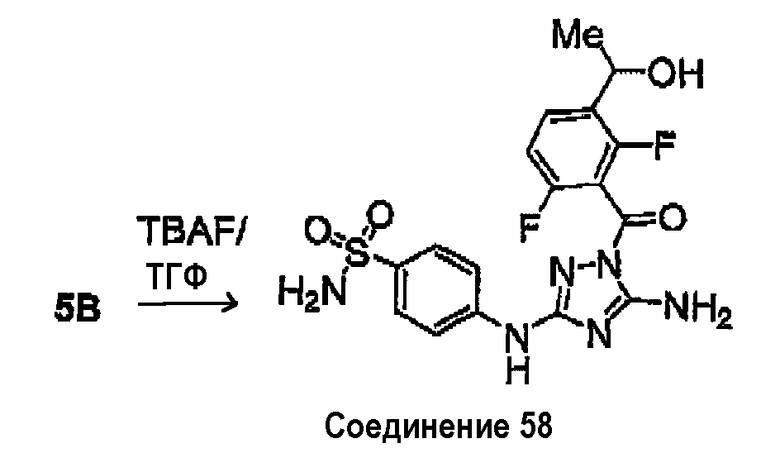
Пример 6
4-[[5-Амино-(2,6-дифторбензоил)-1Н-1,2,4-триазол-3-ил]амино]бензолсульфоновая кислота (соединение 59)
Натриевую соль 4-сульфофенилизотиоцианата, представляющего соединение 6В (полученного способом по примеру 1), подвергают взаимодействию с 1-амидино-3,5-диметилпиразолнитратом, представляющим соединение 1С, с образованием соединения 6С, которое подвергают взаимодействию с гидразином, получая при этом соеднение 6D. 1H ЯМР (300 МГц, (CD3)2SO) δ 11,1 (с, 1H), 8,75 (с, 1H), 7,3 (м, 4H), 5,85 (с, 2H); MS (ESI) m/z: 256 (М+H+).
Соединение 6D ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине, получая при этом соединение 59 (выход 4%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,35 (с, 1H), 7,95 (с, 2H), 7,82 (м, 2H), 7,45-7,25 (м, 5Н); MS (ESI) m/z: 396 (М+H+).
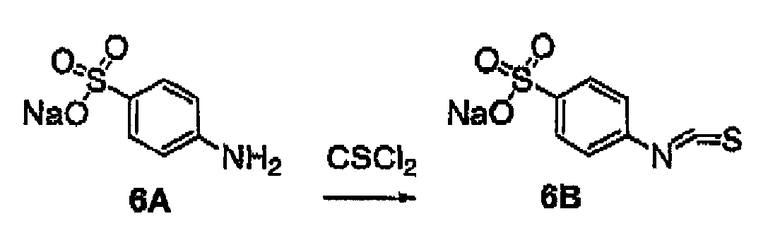
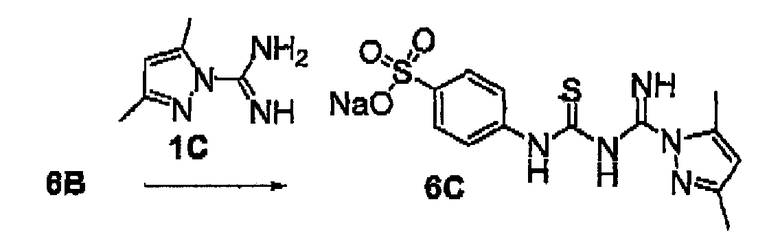
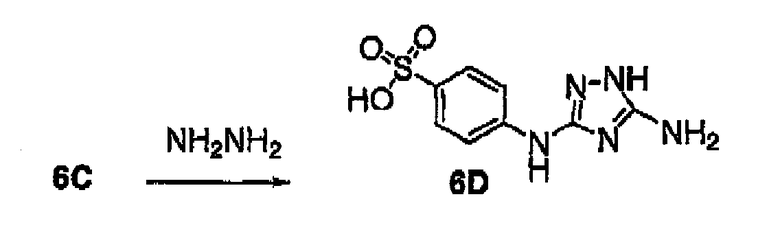
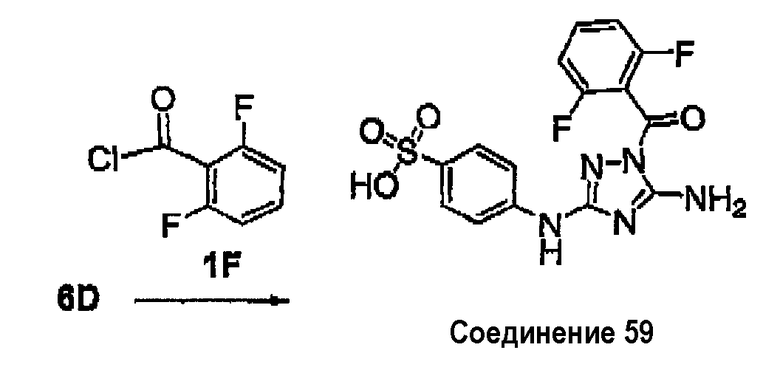
Нижеследующие соединения получают ацилированием промежуточного соеднения 6D способом по примеру 6, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, CD3OD) δ 7,62 (д, 2H), 7,50 (м, 1Н), 7,38 (д, 2H), 7,05 (м, 1H), 2,30 (с, 3H); MS (ESI) m/z: 410 (М+H+).
Пример 7
1-(2,6-Дифторбензоил)-N3-фенил-1Н-1,2,4-триазол-3,5-диамин (соединение 61)
3-Анилино-5-амино-1,2,4-триазол, представляющий соединение 7А (полученный способом по примеру 1), ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине, получая при этом соединение 61 в виде белого твердого вещества (выход 61%). 1H ЯМР (300 МГц, CDCl3) δ 7,80 (с, 1H), 7,45 (м, 1H), 7,30-7,15 (м, 4H), 7,05-6,85 (м, 5H), 6,70 (с, 2H); MS (ESI) m/z: 316 (М+H+), 338 (М+Na+).
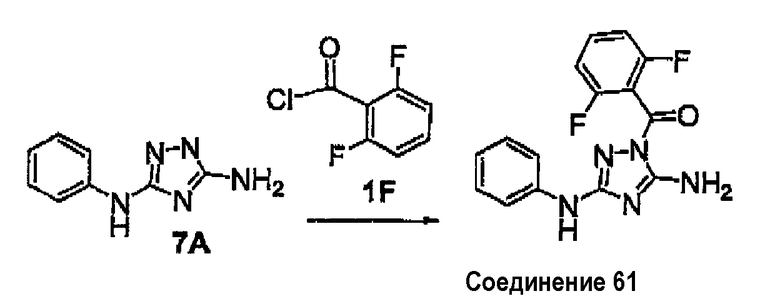
Нижеследующие соединения получают ацилированием соединения 7А способом по примеру 7, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, CDCl3) δ 8,30 (с, 2H), 7,65-7,40 (м, 5H), 7,28 (д, 2Н), 7,00 (т, 1H), 6,80 (с, 1H), 6,70 (с, 2H);
MS (ESI) m/z: 280 (М+H+), 302 (М+Na+)
1H ЯМР (300 МГц, (CD3)2CO) δ 9,20 (c, 1Н), 8,20 (с, 1Н), 7,70 (м, 4H), 7,35 (т, 2H), 7,25 (т, 2H), 7,15 (т, 1Н), 7,98 (с, 2H), 6,88 (т, 1Н); MS (ESI) m/z: 295 (М+H+), 317 (М+Na+).
(второстепенный изомер положения соединения 61)
1H ЯМР (300 МГц, CDCl3) δ 9,80 (c, 1H), 7,65 (д, 2H), 7,60-7,32 (м, 3H),
7,25-7,00 (м, 3H), 4,40 (с, 2H); MS (ESI) m/z: 316 (М+H+), 338 (М+Na+)
(второстепенный изомер положения соединения 62)
1H ЯМР (300 МГц, CDCl3) δ 10,20 (с, 1H), 8,18 (д, 2H), 7,72-7,30 (м, 7Н),
7,15 (т, 1H), 4,30 (с, 2H); MS (ESI) m/z: 280 (М+H+), 302 (М+Na+)
Пример 8
N3-(3-Хлорфенил)-1-(2,6-дифторбензоил)-1Н-1,2,4-триазол-
3,5-диамин (соединение 63)
3-(3-Хлоранилино)-5-амино-1,2,4-триазол, представляющий соединение 8А (полученный способом по примеру 1), ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине, получая при этом соединение 63 в виде бледно-желтого твердого вещества (выход 66%). 1H ЯМР (300 МГц, CDCl3) δ 7,6-7,50 (м, 2H), 7,15-6,80 (м, 6H), 6,60 (с, 2H); MS (ESI) m/z: 350 (М+H+), 372 (М+Na+).
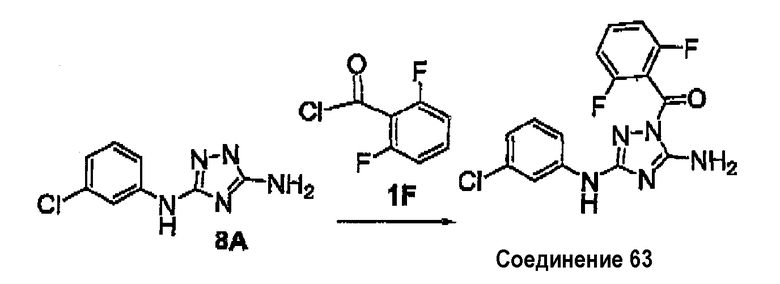
Нижеследующие соединения получают ацилированием промежуточного соединения 8А способом по примеру 8, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2CO) δ 8,58 (с, 1H), 8,30 (д, 2H), 8,00 (м, 1Н), 7,75-7,25 (м, 6H), 6,90 (д, 1H); MS (ESI) m/z: 314 (М+H+), 336 (М+Na+)
1H ЯМР (300 МГц, CDCl3) δ 9,90 (с, 1H), 7,90 (с, 1H), 7,58-6,95 (м, 7H), 4,35 (с, 2H); MS (ESI) m/z: 350 (М+H+), 472 (М+Na+)
(второстепенный изомер положения соединения 64)
1H ЯМР (300 МГц, (CD3)2CO) δ 10,30 (с, 1H), 8,20 (д, 2H), 8,15 (м, 1H), 7,70-7,60 (м, 2H),
7,55 (т, 2H), 7,35 (т, 1H), 7,10 (д, 1H), 5,60 (с, 2H); MS (ESI) m/z: 314 (М+H+), 336 (М+Na+)
Пример 9
1-(2,6-Дифторбензоил)-N3-[4-(4-метил-1-пиперазинил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 71)
4-(4-Метилпиперазино)фенилизотиоцианат подвергают взаимодействию с 1 эквивалентом нитрата 3,5-диметилпиразол-1-карбоксамидина и 1,1 эквивалента трет-бутоксида калия в ДМСО при 55°С в течение 4 часов. Добавляют 10 эквивалентов гидразина и перемешивают при 55°С в течение 4 часов. Реакцонную смесь концентрируют, растворяют в метаноле, отфильтровывают загрязняющие примеси и концентрируют, получая при этом 3-(4-метилпиперазино)анилино-5-амино-1,2,4-триазол, представляющий соединение 9А (выход 87%). 1H ЯМР (400 МГц, (CD3)2SO) δ 9,05 (c, 1H), 8,60 (c, 1H), 7,35 (д, 2H), 6,77 (д, 2H), 5,70 (с, 2H), 2,97 (м, 4H), 2,48 (м, 4H), 2,23 (с, 3H); MS (ESI) m/z: 274 (М+H+).
3-(4-Метилпиперазино)анилино-5-амино-1,2,4-триазол, представляющий соединение 9А, ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине, получая при этом соединение 71 (выход 30%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,07 (с, 1H), 7,88 (с, 1H), 7,72-7,66 (м, 1H), 7,32 (т, 1H), 7,25-7,17 (м, 2H), 6,97-6,92 (м, 1H), 6,71 (д, 1H), 3,39-3,35 (м, 2H), 3,17 (с, 3H), 3,00-2,97 (м, 4H), 2,51-2,46 (м, 4H); MS (ESI) m/z: 414 (М+H+).
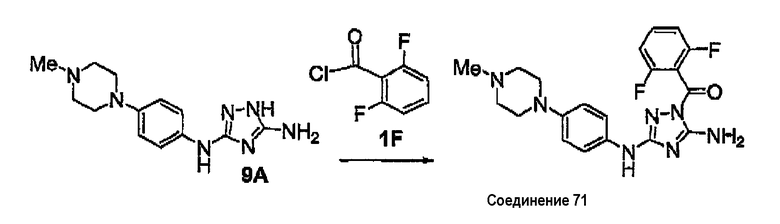
Нижеследующие соединения получают ацилированием промежуточного соединения 9А способом по примеру 9, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,05 (c, 1H), 7,87 (с, 1H), 7,59-7,51 (м, 1H), 7,24-7,18 (м, 2H), 6,72 (д, 2H), 3,35 (с, 2H), 2,99-2,96 (м, 4H), 2,45-2,42 (м, 4H), 2,28 (с, 3H); MS (ESI) m/z: 428 (М+Н+).
1H ЯМР (300 МГц, (CD3)2SO) δ 9,13 (с, 1H), 7,77 (c, 1H), 7,58-7,55 (м, 2Н), 7,38-7,26 (м, 1H), 6,92 (д, 2Н), 3,17 (c, 3Н), 3,09-3,07 (м, 4Н), 2,62 (с, 4Н), 2,35 (с, 3H); MS (ESI) m/z: 398 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,11 (с, 1H), 7,73 (с, 2Н), 7,59-7,54 (м, 2Н), 7,38-7,26 (м, 1H), 6,94 (д, 2Н), 3,16-3,13 (м, 4Н), 2,80-2,78 (м, 4Н), 2,56 (с, 3Н), 2,53 (c, 3Н), 2,46 (с, 3Н); MS (ESI) m/z: 412 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,17 (с, 1H), 7,78 (с, 1H), 7,51 (д, 2Н), 7,35-7,24 (м, 3Н), 7,08 (д, 2Н), 3,14-3,12 (м, 4H), 2,96 (кв, 2Н), 2,76-2,73 (м, 4Н), 2,43 (с, 3Н), 1,34 (т, 3Н); MS (ESI) m/z: 412 (М+H+)
Пример 10
4-[[5-Амино-1-(2,6-дифторбензоил)-1Н-1,2,4-триазол-3-ил]амино]-N-этилбензолсульфонамид (соединение 76)
Соединение 1 (100 мг, 0,254 ммоль) подвергают взаимодействию с 1,2 эквивалента этилтрифторметансульфоната (Et-TFMS) (40 мкл, 0,305 ммоль) и 1,5 эквивалента трет-бутоксида калия (K-t-BO) (0,38 ммоль, 381 мкл 1,0 М раствора в ТГФ) в ТГФ (5 мл) при 50°С, перемешивая смесь в течение 16 часов. Реакционную смесь очищают хроматографией на колонке, производя элюирование смесью 10% метанола/метиленхлорид, и получают продукт, представляющий соединение 76 (27,1 мг, выход 25%). 1H ЯМР (400 МГц, (CD3)2SO) δ 9,87 (с, 1H), 8,00 (с, 2H), 7,76-7,68 (м, 1H), 7,55-7,48 (м, 4H), 7,34 (т, 2H), 7,22 (т, 1H), 2,73-2,67 (м, 2H), 0,94 (т, 3H); MS (ESI) m/z: 423 (М+H+).
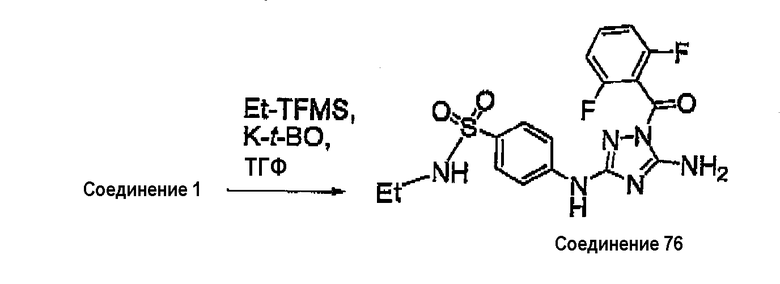
Пример 12
N3-Метил-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3,5-диамин (соединение 79)
3,5-Диамин-1,2,4-триазол, представляющий соединение 12А, ацилируют 3-метилтиофен-2-карбоновой кислотой, представляющей соединение 12В, связанной DIC/HOBt, в безводном ДМФА способом по примеру 1, получая при этом соединение 41 (выход 72%). 1H ЯМР (300 МГц, (CD3)2SO) δ 7,88 (д, J=4,5, 1H), 7,59 (с, 2H), 7,05 (д, J=4,8, 1H), 5,78 (с, 2H), 2,55 (с, 3H); MS (ESI) m/z: 224,1 (М+H+), 245,9 (М+Na+).
Соединение 41 (0,45 ммоль, 100 мг) подвергают взаимодействию с 3 эквивалентами иодметана (1,34 ммоль, 84 мкл) и 1,1 эквивалента трет-бутоксида калия (0,49 ммоль, 493 мкл 1,0 М раствора в ТГФ) в ТГФ (5 мл), перемешивая смесь в течение 16 часов при 25°С. Реакционную смесь очищают хроматографией на колонке (элюирование смесью 10% метанола/дихлорметан), получая при этом продукт, представляющий соединение 79 (7,7 мг, выход 7%). 1H ЯМР (400 МГц, (CD3)2SO) δ 9,80 (с, 1H), 7,60 (д, 1H), 6,96 (д, 1H), 6,17 (с, 2H), 3,47 (c, 3Н), 2,40 (с, 3H); MS (ESI) m/z: 238 (М+H+), 260 (М+Na+).
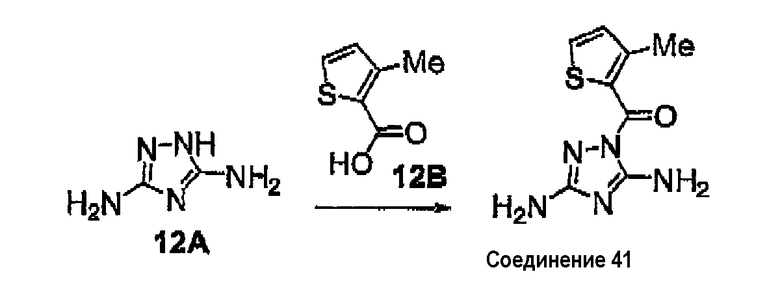
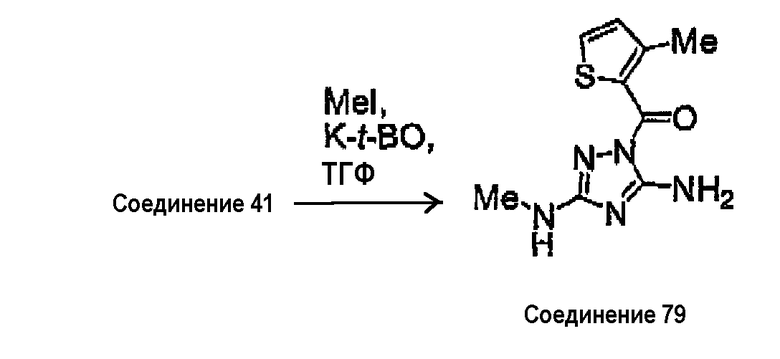
Пример 13
4-[[5-Амино-1-(2,6-дифторбензоил)-1Н-1,2,4-триазол-3-ил]амино]-N-метилбензолсульфонамид (соединение 80)
Трет-BuOK (23,1 мл, 1,0 М раствор в трет-BuOH, 23,1 ммоль) по каплям добавляют к раствору 4-изотиоцианато-N-метилбензолсульфонамида, представляющего соединение 13В (полученного способом по примеру 1) (4,8 г, 21,0 ммоль), и нитрата 2,5-диметилпиразол-1-карбоксимидина, представляющего соединение 1С (4,2 г, 21,0 ммоль), в ДМФА (20 мл). Смесь нагревают до 60°С в течение 2 часов и выливают на лед. Осадок собирают фильтрованием, промывают водой и подвергают воздушной сушке, получая при этом 4-[3-(3,5-диметилпиразол-1-илиминометил)тиоуреидо]-N-метилбензолсульфонамид, представляющий соединение 13С, в виде желтого твердого вещества (7,3 г, выход 95%). 1H ЯМР (300 МГц, (CD3)2SO) δ 8,01 (c, 1H), 7,71 (м, 4H), 6,15 (с, 1H), 2,40 (c, 3Н), 2,22 (с, 6H); MS (ESI) m/z: 367 (М+H+).
Гидразин (3,3 г, 110,0 ммоль) добавляют при 0°С к суспензии 4-[3-(3,5-диметилпиразол-1-илиминометил)тиоуреидо]-N-метилбензолсульфонамида, представляющего соединение 13С (2,0 г, 5,5 ммоль), в ТГФ (20 мл). Смесь нагревают до 60°С в течение 2 часов и выливают на лед. Осадок собирают фильтрованием, промывают водой и СН2Cl2 и подвергают воздушной сушке, получая при этом соединение 13D в виде белого твердого вещества (1,3 г, выход 87%). 1H ЯМР (300 МГц, (CD3)2SO) δ 11,36 (с, 1H), 9,31 (с, 1H), 7,63 (кв, 4H), 7,09 (кв, 1H), 6,05 (с, 2H), 2,39 (д, 3H); MS (ESI) m/z: 269 (М+H+).
Соединение 13D ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине способом по примеру 1, получая при этом соединение 80 (выход 80%). 1H ЯМР (300 МГц, CD3OD) δ 7,64 (м, 1H), 7,63 (д, 2H), 7,53 (д, 2H), 7,15 (т, 2H), 2,43 (с, 3H); MS (ESI) m/z: 409 (М+H+).
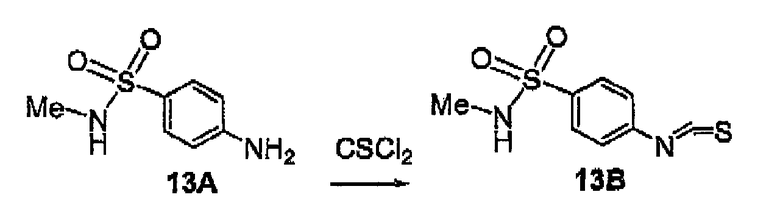
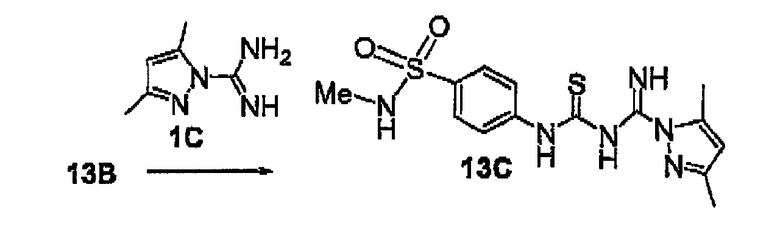
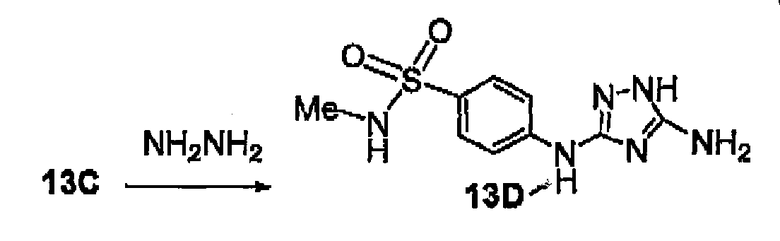
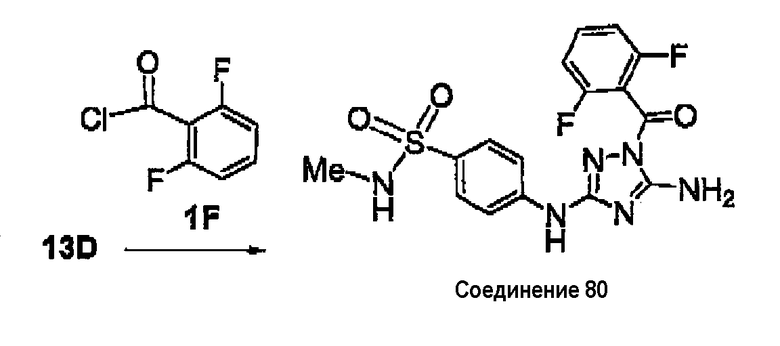
Нижеследующие соединения получают ацилированием промежуточного соединения 13D способом по примеру 13, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, CD3OD) δ 7,55 (д, 2H), 7,48-7,44 (м, 1Н), 7,46 (д, 2H), 2,42 (с, 3H), 2,25 (с, 3H); MS (ESI) m/z: 423 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,92 (с, 1H), 8,03 (д, 1H), 7,81 (д, 2H), 7,69 (д, 2H), 7,14 (м, 2H), 2,62 (c, 3H), 2,55 (с, 3H); MS (ESI) m/z: 393 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,89 (с, 1H), 8,09 (д, 1H), 7,74 (д, 2H), 7,63 (д, 2H), 7,02 (д, 1H), 2,94 (кв, 2H), 2,32 (с, 3H), 1,33 (т, 3H); MS (ESI) m/z: 407 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,65 (c, 1H), 7,64 (д, 1H), 7,50 (д, 2H), 7,69 (д, 2H), 6,66 (с, 1H), 2,36 (c, 3H), 2,34 (с, 3H), 2,12 (с, 3H); MS (ESI) m/z: 407
(М+H+)
Пример 14
1-[(3,5-Диметил-2-тиенил)карбонил]-N3-[4-(1Н-имидазол-1-ил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 85)
4-Изотиоцианат-N,N-диметилбензолсульфонамид, представляющий соединение 14В (полученное способом по примеру 1) (1,8 г, 7,4 ммоль), подвергают взаимодействию с нитратом 2,5-диметилпиразол-1-карбоксиимидина, представляющего соединение 1С (1,5 г, 7,4 ммоль), и трет-BuOK (7,4 мл, 1,0 М раствор в трет-BuOH, 7,4 ммоль), получая при этом 4-[3-(3,5-диметилпиразол-1-илиминометил)тиоуреидо]-N,N-диметилбензолсульфонамид, представляющий соединение 14С, в виде желтого твердого вещества (2,5 г, выход 89%). 1H ЯМР (300 МГц, (CD3)2SO) δ 10,05 (с, 1H), 8,91 (c, 1H), 7,67 (м, 4H), 6,15 (c, 1H), 2,57 (c, 6Н), 2,18 (c, 6Н); MS (ESI) m/z: 381 (М+Н+).
Соединение 14С (2,5 г, 6,6 ммоль) подвергают взаимодействию с гидразином (4,2 г, 132,0 ммоль), получая при этом 1,7 г (90%) соединения 14D в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 9,47 (с, 1H), 7,81 (д, 2H), 7,75 (д, 2H), 6,10 (c, 1H), 2,67 (с, 6Н); MS (ESI) m/z: 283 (М+H+).
Соединение 14D ацилируют 3,5-диметилтиофен-2-карбоновой кислотой, представляющей соединение 1F, связанной DIC/HOBt, в ДМФА, получая при этом соединение 85 (выход 52%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,93 (с, 1H), 7,88 (д, 2H), 7,85 (с, 1H), 7,65 (д, 2H), 6,90 (с, 1H), 2,60 (с, 6Н), 2,56 (с, 3H), 2,54 (с, 3H); MS (ESI) m/z: 421 (М+H+).
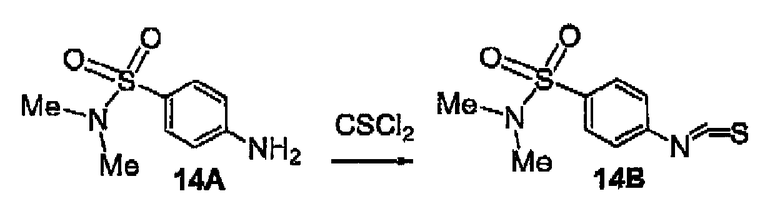
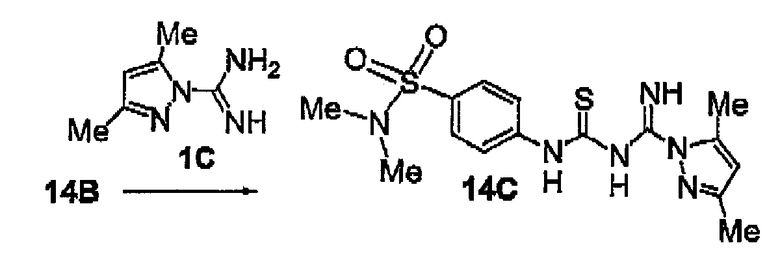
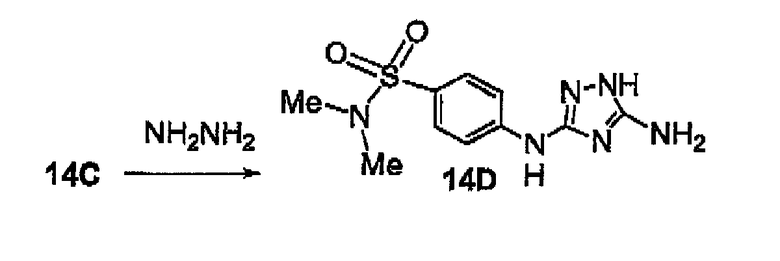
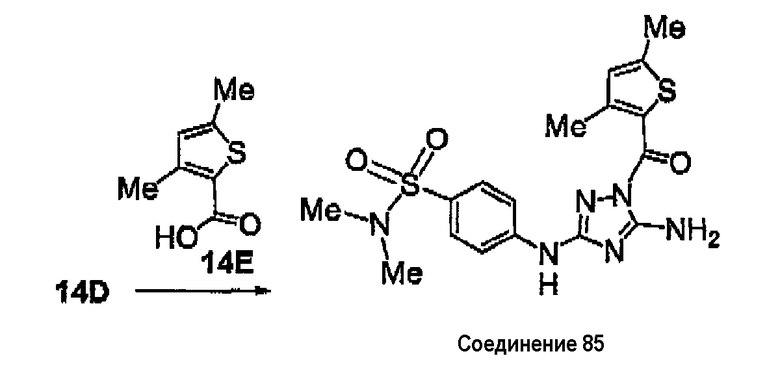
Нижеследующие соединения получают ацилированием промежуточного соединения 14D способом по примеру 14, используя указанное исходное вещество вместо соединения 14Е и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 10,03 (с, 1H), 8,13 (д, 1H), 7,91 (с, 1H), 7,86 (д, 2H), 7,66 (д, 2H), 7,10 (д, 2H), 2,95 (кв, 2H), 2,56 (с, 6H), 1,32 (т, 3H); MS (ESI) m/z: 421 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 10,01 (c, 1H), 8,05 (д, 1H), 7,86 (д, 3H), 7,69 (д, 2H), 7,13 (д, 1H), 2,63 (с, 3H), 2,55 (с, 6H); MS (ESI) m/z: 407 (М+H+)
1H ЯМР (300 МГц, CDCl3) δ 7,79 (с, 1Н), 7,55 (д, 2H), 7,40 (д, 2H), 7,35 (м, 1Н), 6,95 (с, 2H), 6,92 (м, 1Н), 2,65 (с, 6H), 2,27 (с, 3H); MS (ESI) m/z: 437 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,74 (с, 1H), 7,77 (c, 2H), 7,50-7,40 (м, 1Н), 7,30-7,20 (м, 4Н), 7,10 (м, 2H), 2,25 (с, 6H), MS (ESI) m/z: 423 (М+H+)
Пример 15
1-[(5-Этил-2-тиенил)карбонил]-N3-[4-(1Н-имидазол-1-ил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 90)
При помощи способа, описанного в научной литературе (Webb et al., J. Heterocyclic Chem., 1987, 24, 275-278), 4-имидазол-1-иланилин (0,50 г, 3,14 ммоль), дифенилцианокарбонимидат (0,75 г, 3,14 ммоль) и ТГФ (30 мл) объединяют в продуваемой азотом колбе. Смесь нагревают с обратным холодильником в течение 2 часов, охлаждают до температуры льда и по каплям добавляют гидразин (31,4 мл, 1,0 М раствор в ТГФ, 31,4 ммоль). Затем смесь снова нагревают с обратным холодильником в течение 2 часов. Осадок фильтруют, собирают, промывают этилацетатом и подвергают воздушной сушке, получая при этом промежуточное соединение 15А (0,60 г, 79%). 1H ЯМР (300 МГц, (CD3)2SO) δ 11,15 (с, 1H), 8,85 (с, 1H), 8,05 (c, 1H), 7,57 (с, 1H), 7,48 (д, 2H), 7,35 (д, 2H), 7,04 (с, 1H), 5,85 (c, 2H); MS (ESI) m/z: 242 (М+H+).
Соединение 15А ацилируют 5-этилтиофен-2-карбоновой кислотой, представляющей соединение 15В, связанной DIC/HOBt, в ДМФА способом по примеру 1, получая при этом соединение 90 (выход 59%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,63 (с, 1H), 8,14 (д, 1H), 7,85-7,70 (м, 7Н), 7,56-7,53 (м, 2H), 7,07 (д, 2H), 2,95 (кв, 2H), 1,33 (т, 3H); MS (ESI) m/z: 380 (М+H+).
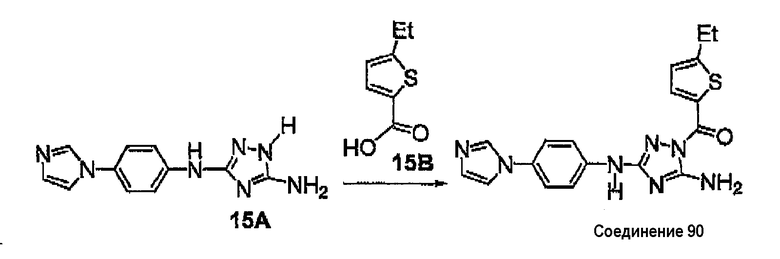
Нижеследующие соединения получают ацилированием промежуточного соединения 15А способом по примеру 15, используя указанное исходное вещество вместо соединения 15В и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,62 (с, 1H), 7,97 (д, 1H), 7,92 (c, 1H), 7,82-7,72 (м, 5Н), 7,56-7,53 (м, 2H), 7,11 (д, 1H), 2,61 (с, 3H); MS (ESI) m/z: 366 (М+H+).
1H ЯМР (300 МГц, (CD3)2CO) δ 9,51 (с, 1Н), 8,15 (с, 1Н), 7,75 (м, 4H), 7,61 (c, 1H), 7,53 (д, 2H), 7,05 (с, 1H), 6,85 (с, 1H), 2,53 (с, 3H), 2,52 (с, 3H); MS (ESI) m/z: 380 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,52 (с, 1H), 8,06 (с, 1H), 7,93 (с, 1H), 7,70 (п, 1H), 7,57 (с, 1H), 7,45 (д, 2H), 7,36 (д, 2H), 7,30 (т, 2H), 7,01 (с, 1H); MS (ESI) m/z: 382 (М+H+)
1H ЯМР (300 МГц, (CD3)2SO) δ
9,52 (с, 1H), 8,08 (с, 1H), 7,93 (с, 1H), 7,57 (с, 1H), 7,53 (т, 1H), 7,42 (д, 2H), 7,35 (д, 2H), 7,18 (т, 1H), 7,02 (с, 1H), 2,25 (с, 3H); MS (ESI) m/z: 396
Пример 16
1-(2,6-Дифтор-3-метилбензоил)-N3-[4-(1Н-1,2,4-триазол-1-ил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 95)
4-(1,2,4-Триазол-1-ил)анилин (0,35 г, 2,18 ммоль), дифенилцианокарбонимидат (0,52 г, 2,18 ммоль) и гидразин (21,8 мл, 1,0 М раствор в ТГФ, 21,8 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 16D (0,40 г, выход 78%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 11,21 (с, 1H), 9,06 (с, 1H), 8,92 (с, 1H), 8,13 (с, 1H), 7,61 (м, 4H), 5,87 (с, 2H); MS (ESI) m/z: 243 (М+H)+.
Соединение 16D ацилируют 2,6-дифтор-3-метилбензоилхлоридом, представляющим соединение 16В, в безводном пиридине способом по примеру 1, получая при этом соединение 95 (выход 51%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,62 (с, 1H), 9,11 (с, 1H), 8,12 (с, 1H), 7,91 (с, 1H), 7,56 (д, 2H), 7,60-7,50 (кв, 1H), 7,45 (д, 2H), 7,16 (т, 1H), 2,25 (с, 3H); MS (ESI) m/z: 397 (М+H+).
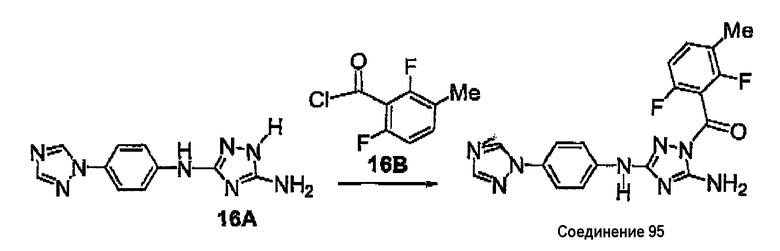
Нижеследующие соединения получают ацилированием промежуточного соединения 16А способом по примеру 16, используя указанное исходное вещество вместо соединения 16В и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,61 (с, 1H), 9,05 (с, 1H), 8,07 (с, 1H), 7,85 (с, 2H), 7,63 (п, 1H), 7,53 (д, 2H), 7,41 (д, 2H), 7,30 (т, 2H), 7,29 (т, 2H); MS (ESI) m/z: 383 (М+H+).
1H ЯМР (300 МГц, (CD3)2SO) δ 9,72 (с, 1H), 9,15 (с, 1Н), 8,17 (с, 1H), 8,16 (д, 1H), 7,78 (с, 2H), 7,77 (д, 2H), 7,72 (д, 2H), 7,04 (д, 1H), 2,96 (кв, 2H), 1,33 (т, 3H); MS (ESI) m/z: 381 (М+H+).
1H ЯМР (300 МГц, (CD3)2SO) δ 9,67 (с, 1H), 9,15 (с, 1H), 8,18 (c, 1H), 7,75 (м, 6H), 6,89 (с, 1H), 2,52 (с, 3Н), 2,51 (с, 3H); MS (ESI) m/z: 381 (М+H+).
1H ЯМР (300 МГц, (CD3)2SO) δ 9,68 (с, 1H), 9,13 (с, 1H), 8,16 (с, 1H), 7,99 (д, 1H), 7,77 (м, 6H), 7,12 (д, 1H); MS (ESI) m/z: 367 (М+H+).
Пример 17
1-(2,6-Дифторбензоил)-N3-[4-(4Н-1,2,4-триазол-4-ил)фенил]-1Н-1,2,4-триазол-3,5-диамин (соединение 100)
4-(1,3,4-Триазол-1-ил)анилин (1,35 г, 8,43 ммоль), дифенилцианокарбонимидат (2,00 г, 8,43 ммоль) и гидразин (84,3 мл, 1,0 М раствор в ТГФ, 84,3 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 17А (1,10 г, выход 77%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 8,90 (c, 2H), 7,62 (д, 2H), 7,36 (д, 2H), 5,82 (с, 2H); MS (ESI) m/z: 243 (М+H+).
Соединение 17А ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине способом по примеру 1, получая при этом соединение 100 (выход 36%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,61 (с, 1H), 8,98 (c, 2H), 7,96 (c, 2H), 7,67 (п, 1Н), 7,47 (д, 2H), 7,42 (д, 2H), 7,32 (т, 2H); MS (ESI) m/z: 383 (М+Н+).
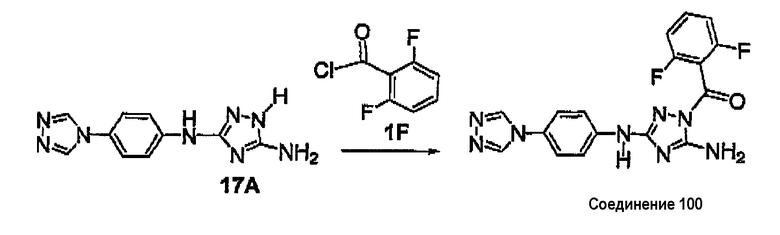
Нижеследующие соединения получают ацилированием промежуточного соединения 17D способом по примеру 17, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,61 (с, 1H), 8,94 (с, 2H), 7,91 (с, 2H), 7,55 (кв, 1H), 7,43 (кв, 4H), 7,18 (т, 1H); MS (ESI) m/z: 397 (М+Н+).
1H ЯМР (300 МГц, (CD3)2SO) δ 10,22 (с, 1H), 9,04 (с, 2Н), 7,95 (м, 3Н), 7,67 (д, 2H), 7,07 (д, 1H), 6,13 (с, 2H); MS (ESI) m/z: 367 (М+Н+)
Пример 18
4-[[5-Амино-1-[(5-этил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]-N-[2-(диметиламино)этил]бензолсульфонамид(соединение 103)
4-Амино-N-(2-диметиламиноэтил)бензолсульфонамид (2,00 г, 8,22 ммоль), дифенилцианокарбонимидат (2,00 г, 8,22 ммоль) и гидразин (82,3 мл, 1,0 М раствор в ТГФ, 82,3 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 18А (1,35 г, выход 50%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 9,22 (с, 1Н), 8,43 (с, 1H), 7,55 (м, 4H), 7,02 (с, 1H), 5,91 (с, 2Н), 2,71 (т, 2H), 2,15 (т, 2Н), 2,05 (с, 6H); MS (ESI) m/z: 326 (М+Н+).
Соединение 18А ацилируют 5-этилтиофен-2-карбоновой кислотой, представляющей соединение 15В, связанной DIC/HOBt, в ДМФА способом по примеру 1, получая при этом соединение 103 (выход 40%). 1H ЯМР (300 МГц, (CD3)2SO) δ 10,02 (с, 1H), 8,13 (д, 1H), 7,88 (с, 1H), 7,75 (д, 2Н), 7,71 (д, 2Н), 7,07 (д, 1H), 7,01 (с, 2Н), 2,95 (кв, 2Н), 2,75 (т, 2Н), 2,20 (т, 2Н), 2,04 (с, 6H), 1,35 (т, 3H); MS (ESI) m/z: 464 (М+Н+).
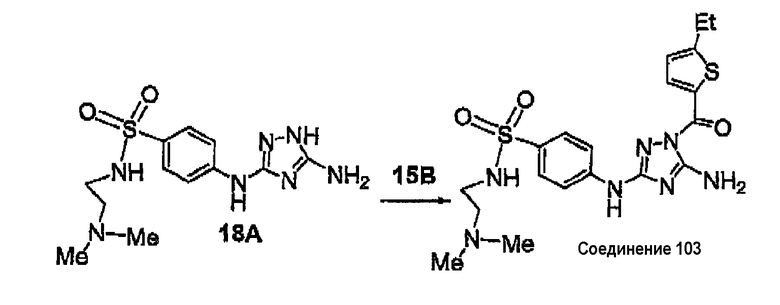
Нижеследующие соединения получают ацилированием промежуточного соединения 18А способом по примеру 18, используя указанное исходное вещество вместо соединения 15В и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,89 (с, 1H), 8,04 (д, 1H), 7,83 (с, 1H), 7,79 (д, 2H), 7,71 (д, 2H), 7,15 (с, 2H), 7,08 (д, 1H), 2,76 (т, 2H), 2,61 (с, 3H), 2,21 (т, 2H), 2,07 (с, 6H); MS (ESI) m/z: 450 (М+Н+).
1H ЯМР (300 МГц, CD3OD) δ 7,57 (д, 2H), 7,45 (м, 3H), 7,00 (т, 1H), 2,86 (т, 2H), 2,32 (т, 2H), 2,25 (с, 3H), 2,11 (с, 6H); MS (ESI) m/z: 480 (М+Н+)
этил]бензолсульфонамид
1H ЯМР (300 МГц, CD3OD) δ 7,60 (м, 1H), 7,55 (д, 2H), 7,45 (д, 2H), 7,11 (т, 1H), 2,87 (т, 2H), 2,32 (т, 2H), 2,12 (с, 6H); MS (ESI) m/z: 466 (М+Н+)
бензолсульфонамид
1H ЯМР (300 МГц, (CD3)2SO) δ 9,89 (с, 1H), 7,81 (м, 4Н), 7,71 (д, 2H), 7,22 (с, 1H), 6,86 (c, 1H), 2,79 (т, 2H), 2,63 (с, 3H), 2,61 (с, 3H), 2,21 (т, 6H), 2,06 (с, 6H); MS (ESI) m/z: 464 (М+Н+)
Пример 19
N-[4-[[5-Амино-1-[(3,5-диметил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]фенил]метансульфонамид (соединение 108)
N-(4-Аминофенил)метансульфонамид (2,00 г, 10,70 ммоль), дифенилцианокарбонимидат (2,60 г, 10,70 ммоль) и гидразин (107,0 мл, 1,0 М раствор в ТГФ, 107,0 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 19А (1,30 г, выход 45%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 8,80 (c, 1H), 8,55 (с, 1H), 7,43 (д, 2H), 6,96 (д, 2H), 5,75 (с, 2H), 2,82 (с, 3H); MS (ESI) m/z: 269 (М+Н+).
Соединение 19А ацилируют 3,5-диметилтиофен-2-карбоновой кислотой, представляющей соединение 19В, связанной DIC/HOBt, в ДМФА способом по примеру 1, получая при этом соединение 108 (выход 11%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,30 (с, 1H), 9,25 (с, 1H), 7,70 (с, 1H), 7,61 (д, 2H), 7,12 (д, 2H), 6,83 (с, 1H), 2,87 (с, 3H), 2,50 (с, 3H); MS (ESI) m/z: 407 (М+Н+).
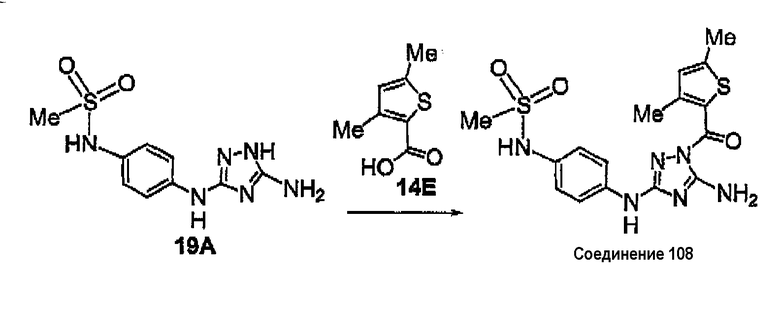
Нижеследующие соединения получают ацилированием промежуточного соединения 19А способом по примеру 19, используя указанное исходное вещество вместо соединения 14Е и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ
9,35 (c, 1Н), 9,30 (с, 1Н), 8,01 (д, 1Н), 7,75 (с, 1Н), 7,62 (д, 2H), 7,12 (м, 3Н), 6,83 (с, 1Н), 2,89 (с, 3Н), 2,59 (с, 3H); MS (ESI) m/z: 393 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,37 (с, 1Н), 9,30 (с, 1Н), 8,12 (д, 1Н), 7,74 (с, 1Н), 7,62 (д, 2H), 7,12 (д, 2H), 7,03 (д, 1Н), 2,95 (кв, 2H), 2,89 (с, 3Н), 1,35 (т, 3Н); MS (ESI) m/z: 407 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,32 (с, 1Н), 9,21 (с, 1Н), 7,88 (с, 2H), 7,64 (п, 1Н), 7,25 (м, 4Н), 6,92 (д, 2H), 2,82 (с, 3Н); MS (ESI) m/z: 409 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ
9,33 (с, 1H), 7,88 (с, 2H), 7,54 (кв, 1H), 7,25 (д, 2H), 7,16 (т, 1H), 6,92 (д, 2H), 2,82 (с, 3H), 2,25 (с, 3Н); MS (ESI) m/z: 423 (М+Н+)
Пример 20
1-[4-[[5-Амино-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]фенил]-2-имидазолидинон (соединение 113)
1-(4-Аминофенил)имидазолидин-2-он (0,24 г, 1,35 ммоль), дифенилцианокарбонимидат (0,32 г, 1,35 ммоль) и гидразин (13,5 мл, 1,0 М раствор в ТГФ, 13,5 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 20А (0,28 г, 80%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 11,05 (с, 1H), 8,42 (с, 1H), 7,35 (д, 2H), 7,24 (д, 2H), 6,65 (с, 1H), 5,78 (c, 2H), 3,74 (т, 2H), 3,32 (т, 2H); MS (ESI) m/z: 260 (М+Н+).
Соединение 20А ацилируют 3-метилтиофен-2-карбоновой кислотой, представляющей соединение 20В, связанной DIC/HOBt, в ДМФА способом по примеру 1, получая при этом соединение 113 (выход 41%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,21 (c, 1H), 8,01 (д, 1H), 7,68 (с, 1H), 7,55 (д, 2H), 7,43 (д, 2H), 7,11 (д, 1H), 6,71 (c, 1H), 3,83 (кв, т), 3,37 (кв, 2H), 2,63 (с, 3H); MS (ESI) m/z: 384 (М+Н+).
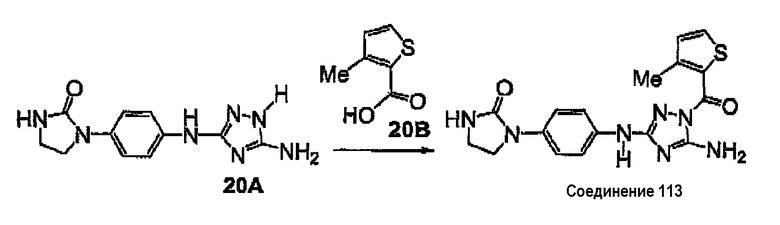
Нижеследующие соединения получают ацилированием промежуточного соединения 20А способом по примеру 20, используя указанное исходное вещество вместо соединения 20В и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,12 (с, 1H), 7,82 (с, 2H), 7,50 (м, 1H), 7,21 (м, 4H), 7,20 (м, 1H), 6,70 (с, 1H), 3,72 (т, 2H), 3,28 (т, 3H), 2,21 (с, 3H); MS (ESI) m/z: 414 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ
9,16 (c, 1H), 7,87 (с, 2H), 7,63 (м, 1H), 7,19 (м, 6H), 6,74 (с, 1H), 3,72 (т, 2H), 3,28 (т, 3H); MS (ESI) m/z: 400 (М+Н+)
Пример 21
N3-[4-(1,1-Диоксидо-2-изотиазолидинил)фенил]-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3,5-диамин (соединение 116)
4-(1,1-Диоксоизотиазолидин-2-ил)фениламин (0,92 г, 4,36 ммоль), дифенилцианокарбонимидат (1,10 г, 4,36 ммоль) и гидразин (43,6 мл, 1,0 М раствор в ТГФ, 43,6 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 21А (1,2 г, 95%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 11,05 (с, 1H), 8,58 (c, 1H), 7,47 (д, 2H), 7,05 (д, 2H), 5,78 (с, 1H), 3,55 (т, 2H), 3,32 (т, 2H), 2,30 (п, 2H); MS (ESI) m/z: 295 (М+Н+).
Соединение 21А ацилируют 3-метилтиофен-2-карбоновой кислотой, представляющей соединение 20В, связанной DIC/HOBt, в ДМФА способом по примеру 1, получая при этом соединение 116 (выход 48%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,38 (с, 1H), 8,01 (д, 1H), 7,73 (с, 2H), 7,62 (д, 2H), 7,15 (д, 2H), 7,08 (д, 1H), 3,67 (т, 2H), 3,42 (т, 2H), 2,58 (с, 3H), 2,35 (п, 2H); MS (ESI) m/z: 419 (М+Н+).
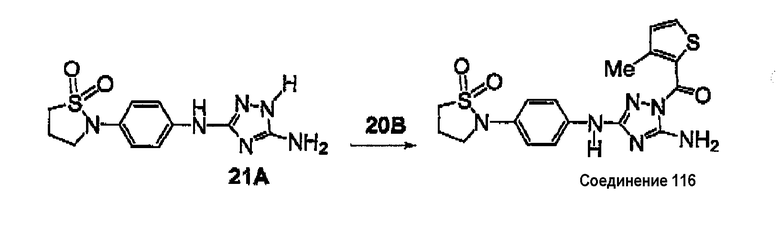
Нижеследующие соединения получают ацилированием промежуточного соединения 21А способом по примеру 21, используя указанное исходное вещество вместо соединения 20В и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,31 (с, 1H), 7,80 (с, 2H), 7,62 (т, 2H), 7,28 (м, 3H), 7,01 (д, 2H), 3,63 (т, 2H), 3,35 (т, 2H), 2,32 (п, 2H); MS (ESI) m/z: 435 (М+Н+).
Пример 22
4-[[5-Амино-1-(2,6-дифторбензоил)-1Н-1,2,4-триазол-3-ил]амино]-N-(2-пиридинил)бензолсульфонамид (соединение 118)
4-Амино-N-пиридин-2-ил-бензолсульфонамид (1,48 г, 5,96 ммоль), дифенилцианокарбонимидат (1,42 г, 5,96 ммоль) и гидразин (59,6 мл, 1,0 М раствор в ТГФ, 59,6 ммоль) подвергают взаимодействию способом по примеру 15, получая при этом соединение 22А (0,98 г, 50%) в виде белого твердого вещества. 1H ЯМР (300 МГц, (CD3)2SO) δ 9,22 (с, 1Н), 8,05 (с, 1Н), 7,73 (м, 3Н), 7,53 (д, 2H), 7,04 (д, 1H), 6,85 (м, 2H), 5,85 (с, 2H); MS (ESI) m/z: 332 (М+Н+).
Соединение 22А ацилируют 2,6-дифторбензоилхлоридом, представляющим соединение 1F, в безводном пиридине способом по примеру 1, получая при этом соединение 118 (выход 61%). 1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (с, 1H), 8,00-7,90 (м, 2H), 7,65 (м, 1H), 7,59 (д, 2H), 7,35 (д, 2H), 7,25 (т, 2H), 7,04 (д, 1H), 6,81 (т, 1H), 3,31 (с, 2H); MS (ESI) m/z: 472 (М+Н+).
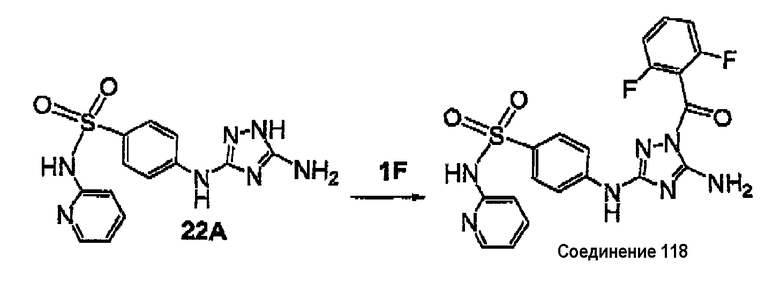
Нижеследующие соединения получают ацилированием промежуточного соединения 22А способом по примеру 22, используя указанное исходное вещество вместо соединения 1F и соответствующий реагент (реагенты):
1H ЯМР (300 МГц, (CD3)2SO) δ 9,87 (с, 1H), 8,11 (д, 1H), 8,01 (с, 1H), 7,90 (с, 1H), 7,75 (м, 4H), 7,68 (д, 2H), 7,63 (т, 1H), 7,07 (м, 2H), 6,85 (м, 1H), 2,95 (кв, 2H), 1,32 (т, 3H); MS (ESI) m/z: 470 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ
9,84 (с, 1H), 7,98 (с, 1H), 7,91 (с, 1H), 7,74 (м, 4H), 7,71 (д, 2H), 7,63 (т, 1H), 7,07 (м, 1H), 6,85 (м, 2H), 2,53 (с, 3H), 2,52 (с, 3H); MS (ESI) m/z: 470 (М+Н+)
1H ЯМР (300 МГц, (CD3)2SO) δ 9,85 (с, 1H), 8,02 (м, 2H), 7,79 (м, 4H), 7,73 (д, 2H), 7,63 (т, 1H), 7,13 (д, 1H), 7,07 (м, 1H), 6,81 (м, 1H), 2,61 (с, 3H); MS (ESI) m/z: 456 (М+Н+)
Биологические примеры
Пригодность соединений для лечения или облегчения симптомов заболеваний, опосредованных циклинзависимой киназой и тирозинкиназой, определяют описанными ниже способами.
Пример 1
Скрининг CDK1
Для скрининга киназы используют реакционную смесь, содержащую 50 мМ трис-HCl с рН 8, 10 мМ MgCl2, 0,1 мМ Na3PO4, 1 мМ дитиотреитол (DTT), 10 мкМ АТФ, 0,025 мкМ биотинилированного гистоном-Н1 пептидного субстрата, и 0,2 мкКи на лунку 33Р-γ-АТФ [2000-3000 Ки/ммоль]. В каждую лунку покрытого стрептавидином планшета FlashPlate™ (№ по каталогу SMP103, NEN, Boston, MA) пипеткой-дозатором вводят 70 мкл реакционной смеси для скрининга киназы. Затем в лунки добавляют 1 мкл исходного раствора испытуемого соединения в 100% ДМСО до достижения конечной концентрации, равной 1% ДМСО в реакционной смеси с конечным объемом 100 мкл. Белок CDK1:циклин-В разводят в 50 мМ трис-HCl с рН 8,0, содержащего 0,1% альбумин бычьей сыворотки (BSA), в концентрации 1 нг на 1 мкл и для инициации реакции в каждую лунку добавляют 30 мкл смеси (30 нг фермента/лунку). Реакционную смесь инкубируют в течение одного часа при 30°С. По окончании инкубационного периода, равного 1 часу, реакцию прекращают, для чего реакционную смесь отсасывают с планшета и лунки дважды промывают ЗФР, содержащим 100 мМ ЭДТК. Пептидный субстрат, биотинилированный гистоном-Н1, иммобилизуют на планшете Flashplate™ и измеряют содержание 33Р-γ-АТР, считывая планшет при помощи сцинтилляционного счетчика. Ингибирование ферментативной активности CDK1 измеряют по уменьшению количества 33Р-γ-АТР, содержащегося в иммобилизованном пептиде.
Скрининг VEGF-R
Для скрининга киназы используют реакционную смесь, содержащую 50 мМ трис-HCl с рН 8, 10 мМ MgCl2, 0,1 мМ Na3PO4, 1 мМ DTT, 10 мкМ АТФ, 0,025 мкМ биотинилированного пептидного субстрата и 0,8 мкКи на лунку 33Р-γ-АТР [2000-3000 Ки/ммоль]. В каждую лунку покрытого стрептавидином планшета FlashPlate™ (№ по каталогу SMP103, NEN, Boston, MA) пипеткой-дозатором вводят 70 мкл реакционной смеси для скрининга киназы. Затем в лунки добавляют 1 мкл исходного раствора испытуемого соединения в 100% ДМСО до достижения конечной концентрации, равной 1% ДМСО в реакционной смеси с конечным объемом 100 мкл. Растворимую тирозинкиназу крысы, содержащую метку 6ХHIS у N-конца, разводят в 50 мМ трис-HCl с рН 8,0, содержащего 0,1% BSA, до концентрации 5 нг на мкл раствора, и для инициации реакции в каждую лунку добавляют 30 мкл смеси (150 нг фермента/лунку). Реакционную смесь инкубируют в течение одного часа при 30°С. По окончании инкубационного периода, равного 1 часу, реакцию прекращают, для чего реакционную смесь отсасывают с планшета и лунки дважды промывают ЗФР, содержащим 100 мМ ЭДТК. Пептидный субстрат, биотинилированный PLC1, иммобилизуют на планшете FlashPlate™ и измеряют содержание 33Р-γ-АТР, считывая планшет при помощи сцинтилляционного счетчика. Ингибирование ферментативной активности VEGF-R измеряют по уменьшению количества 33Р-γ-АТР, содержащегося в иммобилизованном пептиде.
Данные IC50 для VEGF-R и CDK приведены в таблице 1. Значения IC50, указанные как >10 или >100, свидетельствуют о том, что при наибольшей испытанной дозе не обнаружено как 50% ингибирование, так и максимальное ингибирование.
Пример 2
Испытание на селективность в отношении киназы
Испытания на ингибирование испытуемыми соединениями разных киназ выполняют методами, позволяющими измерить величину фосфорилирования биотинилированного пептидного субстрата. При выполнении анализов использованы описанные в научной литературе биотинилированные пептидные субстраты, соответствующие каждому оцениваемому ферменту. Активность киназы анализируют следующим образом: получают реакционную смесь, содержащую 50 мМ трис-HCl с рН 8, 10 мМ MgCl2, 0,1 мМ Na3VO4, 1 мМ DTT, 10 мкМ АТФ, 0,25-1 мкМ биотинилированного пептидного субстрата и 0,2-0,8 мкКи на лунку 33Р-γ-АТР [2000-3000 Ки/ммоль]. Условия проведения испытаний несколько отличаются для каждой протеинкиназы, например, для измерения активности киназы рецептора инсулина необходимо 10 мМ MnCl2, а для измерения активности кальмодулинзависимой протеинкиназы необходим кальмодулин и 10 мМ CaCl2. Такие условия проведения испытаний известны в данной области. Реакционную смесь вводят пипеткой-дозатором в лунки покрытого стрептавидином планшета FlashPlate и добавляют 1 мкл исходного раствора лекарственного средства в 100% ДМСО до достижения конечной концентрации, равной 1% ДМСО в реакционной смеси с конечным объемом 100 мкл. Фермент разводят в 50 мМ трис-HCl с рН 8,0, содержащего 0,1% BSA, и добавляют в каждую лунку. Реакционную смесь инкубируют в течение одного часа при 30°С. Через один час реакционную смесь отсасывают с планшета и планшет промывают ЗФР, содержащим 100 мМ ЭДТК. Планшет считывают при помощи сцинтилляционного счетчика для определения количества 33Р-γ-АТР, содержащегося в иммобилизованном пептиде. Испытуемые соединения анализируют дважды в 8 концентрациях [100 мкМ, 10 мкМ, 1 мкМ, 100 нМ, 10 нМ, 1 нМ, 100 пМ, 10 пМ]. При выполнении анализа определяют максимальный и минимальный сигналы на каждом планшете. Значение IC50 вычисляют на основании кривой зависимости от дозы в процентах подавления максимального сигнала по формуле [максимальный сигнал - фоновый сигнал/сигнал испытуемого соединения - фоновый сигнал (100)=% ингибирования], строя график зависимости процентного значения ингибирования от логарифмической концентрации испытуемого соединения. На каждый планшет помещают также известные ингибирующие соединения для данной киназы.
Определение ферментов киназы и источники их получения
VEGF-R (рецептор-2 фактора роста сосудистого эндотелия) представляет слитый белок, содержащий полигистидиновую метку у N-конца, за которой следуют аминокислоты 786-1343 домена киназы VEGF-R2 крысы (№ доступа U93306 в банке генов GenBank). CDK1 (циклинзависимая киназа 1) выделяют из клеток насекомых, экспрессирующих каталитическую субъединицу CDK1 человека и ее положительную регуляторную субъединицу циклин В (New England Biolabs, Beverly, MA, № по каталогу 6020). Комплекс CDK1 с циклином А имеется в продаже (Upstate Biotech, Lake Placid, NY). Комплекс CDK4 состоит из белка CDK4 мыши и белка циклина D1 мыши (белок CDK4 мыши получают в результате генетического слияния с N-концевой меткой в виде эпитопа Flag, а белок циклина D1 мыши получают в результате слияния с N-концевой меткой в виде эпитопа AU-1. Гены, кодирующие указанные белки, переносят в векторы на основе бакуловируса, имеющиеся в продаже. Рекомбинантный комплекс CDK4/D1 получают коинфицируя имеющиеся в продаже клетки насекомых вирусами, несущими две указанные конструкции). Киназа рецептора инсулина состоит из остатков 941-1313 цитоплазматического домена бета-субъединицы рецептора инсулина человека (BIOMOL, Plymouth Meeting, PA, № по каталогу SE-195). Протеинкиназа А представляет каталитическую субъединицу цАМФ-зависимой протеинкиназы-А, выделенной из бычьего сердца (Upstate Biotech, Lake Placid, NY, № по каталогу 14-114). РКС (протеинкиназа-С) представляет гамма- или бета-изоформу белка человека, продуцируемую в клетках насекомых (BIOMOL, Plymouth Meeting, PA, № по каталогу SE-143). Казеинкиназа 1 представляет усечение у аминокислоты 318 С-концевой части дельта-изоформы СК1 крысы, продуцированной в E. coli (New England Biolabs, Beverly, MA, № по каталогу 6030). Казеинкиназа 2 включает альфа- и бета-субъединицы белка СК2 человека, продуцированного в E. coli (New England Biolabs, Beverly, MA, № по каталогу 6010). Кальмодулинкиназа (кальмодулинзависимая протеинкиназа 2) представляет усеченный вариант альфа-субъединицы белка крысы, продуцированного в клетках насекомых (New England Biolabs, Beverly, MA, № по каталогу 6060). Гликогенсинтаза-киназа-3 представляет бета-изоформу фермента кролика, продуцированного в E. coli (New England Biolabs, Beverly, MA, № по каталогу 6040). МАР-киназа представляет изоформу ERK-2 кролика, содержащую полигистидиновую метку у N-конца, продуцированную в E. coli и активированную фосфорилированием МЕК1 до очистки (BIOMOL, Plymouth Meeting, PA, № по каталогу SE-137). Белок ERK-1 (расщепленный в компании Calbiochem), EGFR (рецептор эпидермального фактора роста) выделяют из мембран клеток А431 человека (Sigma, St. Louis, MO, № по каталогу Е3641). PDGF-R (рецептор фактора роста, выделенный из тромбоцитов) представляет слитый белок, содержащий полигистидиновую метку у N-конца, за которой следуют нуклеотиды 1874-3507 домена киназы бета-субъединицы PDGF-R человека (№ доступа М21616). HER2 (рецептор-2 эпидермального фактора роста человека) содержит полигистидиновую метку у N-конца, за которой следуют 24 дополнительные аминокислоты, и начинается у аминокислоты 676, за которой следует остальная часть цитоплазматического домена HER2.
Пептидные субстраты
Данные IC50 для разных киназ приведены в таблицах 2а-2k. Значения IC50, указанные как >10 или >100, свидетельствуют о том, что при наибольшей испытанной дозе в данном анализе не обнаружено как 50% ингибирование, так и максимальное ингибирование. Величины, указанные как ˜10, представляют приблизительное значение, полученное на основании обнаруженного 50% ингибирования.
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Селективность в отношении киназы
Пример 3
Измерение ингибирования пролиферации клеток
Способность испытуемого соединения ингибировать пролиферацию клеток определяют измеряя содержание 14С-меченого тимидина во вновь синтезированной ДНК клеток. При выполнении данного метода используют линии клеток, выделенные из карцином нескольких тканей, таких как аденокарцинома шейки матки HeLa (Американская коллекция типовых культур (АТСС), Виргиния, № по каталогу CCL-2), злокачественная меланома А375 (АТСС CRL-1619), аденокарцинома яичника SK-OV-3 (ATCC HTB-77), карцинома ободочной кишки НСТ-116 (CCL-247), аденокарцинома предстательной железы РС-3 (АТСС CRL-1435) и MDA-MB-231 (Xenogen Corp.). Подобным образом можно определить воздействие соединения на рост клеток многих фенотипов. Клетки обрабатывают трипсином и подсчитывают, затем в каждую лунку 96-луночного сцинтилляционного микропланшета CytoStar, обработанного под культуры тканей (Amersham № RPNQ0160), добавляют 3000-8000 клеток в полной среде в объеме, равном 100 мкл. Клетки инкубируют в течение 24 часов в полной среде при 37°С в атмосфере, содержащей 5% СО2. Затем в лунки планшета добавляют 1 мкл испытуемого соединения в 100% ДМСО. В контрольные лунки добавляют только ДМСО. Клетки инкубируют в течение 24 часов в полной среде при 37°С в атмосфере, содержащей 5% СО2. Метил-14С-тимидин в количестве 56 мКи/ммоль (NEN № NEC568 или Amersham № CFA532) разводят в полной среде и в каждую лунку планшета CytoStar добавляют 0,2 мкКи/лунку в объеме, равном 20 мкл. Планшет инкубируют с лекарственным средством и 14С-тимидином в течение 24 часов при 37°С с 5% СО2. Затем планшет переворачивают и его содержимое удаляют в контейнер для 14С-радиоактивных отходов, после чего планшет дважды промывают 200 мкл ЗФР. В каждую лунку добавляют 200 мкл ЗФР. Верхнюю часть планшета заклеивают прозрачным приспособлением для герметизации планшетов и на основание планшета накладывают белое приспособление для герметизации нижней части планшета (Packard № 6005199). Количественное определение содержания метил-14С-тимидина производят при помощи счетчика Packard Top.
Ингибирование пролиферации клеток (IC50, нМ)
данных
Пример 4
Модели in vivo - подавление роста опухоли
Воздействие соединения на рост опухолевых клеток человека in vivo можно определить имплантируя опухолевые клетки человека в задний пах безтимусных мышей с последующим введением мышам испытуемого соединения. Опухолевые клетки человека, выделенные из опухолей разных типов, таких как клетки меланомы человека А375, имплантируют подкожно в задний пах самцам безтимусных мышей (Charles River) и наблюдают за ростом опухоли у мышей в течение 6-10 дней, измеряя опухоль штангенциркулем. Затем вводят испытуемое соединение вместе с приемлемым носителем в виде внутрибрюшинной инъекции один раз в сутки в течение 30 дней. Испытуемое соединение можно вводить другими способами, например перорально, подкожно или в виде внутривенного вливания. При выполнении данного исследования величину опухоли измеряют через каждые четыре дня и определяют степень ингибирования, сравнивая состояние животных, которым вводят лекарственное средство, с животными, которым вводят только носитель.
При помощи указанной модели можно также определить синергизм или усиление действия обычного химиотерапевтического средства испытуемым соединением, сравнивая животных, подвергаемых обычному лечению, с животными, которым наряду с обычным лечением вводят испытуемое соединение. В случае синергичного действия, вызываемого испытуемым соединением, рост опухоли должен замедляться в большей степени.
Хотя в приведенном выше описании изобретения изложены основные принципы настоящего изобретения, проиллюстрированные примерами, совершенно очевидно, что практика применения изобретения включает все возможные варианты, адаптации и модификации, которые входят в объем нижеследующей формулы изобретения и ее эквивалентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ ФЕРМЕНТА ДИАЦИЛГЛИЦЕРИН-О-АЦИЛТРАНСФЕРАЗЫ ТИПА 1 | 2008 |
|
RU2486186C2 |
| ИНГИБИТОР, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ ПРОИЗВОДНОЕ ПИРИДАЗИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2807611C2 |
| НОВОЕ ФОСФОРАМИДАТНОЕ ПРОИЗВОДНОЕ НУКЛЕОЗИДА И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2621709C2 |
| Соединения формул (I) и (A), фармацевтическая композиция, лекарственное средство, применение и способ получения соединения формулы (I) | 2018 |
|
RU2822758C2 |
| ПРОИЗВОДНОЕ 1,2,4-ТРИАЗОЛОНА | 2011 |
|
RU2566754C2 |
| НОВОЕ ПРОИЗВОДНОЕ НИКОТИНАМИДА ИЛИ ЕГО СОЛЬ | 2011 |
|
RU2560163C2 |
| ТРИАЗОЛОПИРИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2561104C2 |
| ПРОИЗВОДНЫЕ 1H-1,2,4-ТРИАЗОЛ-3-КАРБОКСАМИДА В КАЧЕСТВЕ ЛИГАНДОВ РЕЦЕПТОРА КАННАБИНОИДОВ | 2003 |
|
RU2325382C2 |
| КЛАСС КОНДЕНСИРОВАННЫХ КОЛЬЦЕВЫХ СОЕДИНЕНИЙ И ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2021 |
|
RU2831125C1 |
| ДИГИДРОПИРИДОФТАЛАЗИНОНОВЫЕ ИНГИБИТОРЫ ПОЛИ(АДФ-РИБОЗА)ПОЛИМЕРАЗЫ | 2009 |
|
RU2514937C2 |
Описываются производные замещенного триазолдиамина формулы (I):

где: R1 - С1-4алкил, фенил, возможно замещенный галогеном, замещенной -SO2-(С1-4)алкилом аминогруппой, имидазолилом, 1,2,4-триазолилом, имидазолидиноном, диоксидоизотиазолидинилом, C1-4алкилпиперазинилом, остатком -SO2-, замещенным, аминогруппой, С1-4алкиламиногруппой, С1-4диалкиламиногруппой, пиридиниламиногруппой, пиперидинилом, гидроксилом или С1-4диалкиламино-С1-3алкиламиногруппой, a R2 - Н, или
R1 - Н, a R2 - фенил, возможно замещенный галоидом или -SO2-NH2;
Х - -С(O)-, -C(S)- или -SO2-; и
R3 - фенил, необязательно замещенный 1-3 заместителями, включающими галоген и нитро, или 1-2 заместителями, включающими C1-4алкокси, гидрокси-C1-4-алкил, амино или C1-4алкил, возможно замещенный 1-3 галоидом при концевом атоме углерода;
C3-7циклоалкил, возможно 1-2 замещенный C1-4алкилом;
тиенил, возможно замещенный галоидом, C1-4алкилом (который, возможно, замещен -CO2(C1-4)алкилом), С2-4алкенилом (который, возможно, замещен -СО2(C1-4)алкилом, C1-4-алкокси, пирролилом, пиридинилом или амино, замещенным -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, замещенным галогеном;
С2-8алкинил, замещенный фенилом;
амино, замещенный галоидзамещенным фенилом;
фурил, изоксазолил, пиридинил, дегидробензотиенил, тиазолил или тиадиазолил, причем тиазолил и тиадиазолил, возможно, замещены C1-4алкилом;
их фармацевтически приемлемые соли, фармацевтическая композиция на их основе и способ ее получения. Новые соединения обладают селективной ингибирующей активностью в отношении циклинзависимых киназ и могут быть использованы при лечении опухолевых болезней. 3 и 13 з.п. ф-лы, 3 табл.
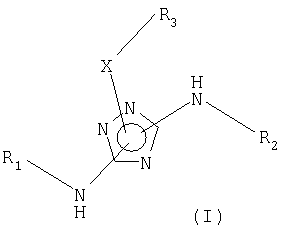
где R1 означает C1-4алкил, фенил, который не замещен или замещен галогеном, замещенной -SO2-(C1-4)алкилом аминогруппой, имидазолилом, 1,2,4-триазолилом, имидазолидиноном, диоксидоизотиазолидинилом, C1-4алкилпиперазинилом, остатком -SO2-, замещенным, в свою очередь, аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой, пиридиниламиногруппой, пиперидинилом, гидроксилом или C1-4диалкиламино-C1-3алкиламиногруппой, a R2 означает водород, или
R1 означает водород, a R2 означает фенил, который не замещен или замещен галоидом или группой -SO2-NH2;
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 означает фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
C3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4алкил;
тиенил, не замещенный или замещенный галогеном, C1-4алкилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C2-4алкенилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C1-4алкокси, пирролилом, пиридинилом или амино, который сам замещен -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
C2-8алкинил, замещенный фенилом;
амино, замещенный фенилом, который, в свою очередь, может быть замещен галогеном;
фурил, изоксазолил, пиридинил, дигидробензотиенил, тиазолил или тиадиазолил, причем тиазолил и тиадиазолил могут быть замещены C1-4алкилом;
или их фармацевтически приемлемые соли.
фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
C3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4алкил;
тиенил, не замещенный или замещенный галогеном, С1-4алкилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C2-4алкенилом (который, в свою очередь, может быть замещен -СО2(C1-4)алкилом), C1-4алкокси, пирролилом, пиридинилом или амино, который сам замещен -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
C2-4алкинил, замещенный фенилом;
амино, замещенный фенилом, который, в свою очередь, может быть замещен галогеном;
фурил, изоксазолил, пиридинил, дигидробензотиенил, тиазолил или тиадиазолил, причем тиазолил и тиадиазолил могут быть замещены C1-4алкилом.
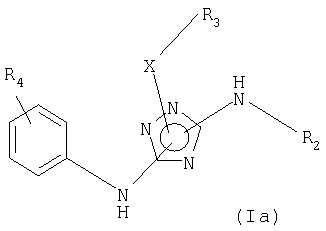
где
R4 выбирают из группы, включающей замещенную -SO2-(C1-4)алкилом аминогруппу, имидазолил, 1,2,4-триазолил, имидазолидинон, диоксидоизотиазолидинил, C1-4алкилпиперазинил, остаток -SO2-, замещенный, в свою очередь, аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой, пиридиниламиногруппой, пиперидинилом или C1-4диалкиламино-C1-4алкиламиногруппой;
R2 означает водород;
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 означает фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
C3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4алкил;
тиенил, не замещенный или замещенный галогеном, C1-4алкилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C2-4алкенилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C1-4алкокси, пирролилом, пиридинилом или амино, который сам замещен -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
C2-8алкинил, замещенный фенилом;
амино, замещенный фенилом, который, в свою очередь, может быть замещен галогеном;
фурил, изоксазолил, пиридинил, дигидробензотиенил, тиазолил или тиадиазолил, причем тиазолил и тиадиазолил могут быть замещены C1-4алкилом;
или его фармацевтически приемлемые соли.
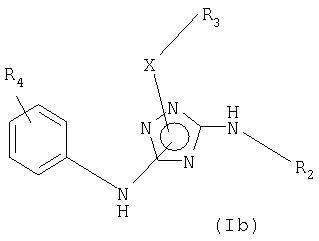
где
R4 выбирают из группы, включающей замещенную -SO2-(C1-4)алкилом аминогруппу, имидазолил, 1,2,4-триазолил, имидазолидинон, диоксидоизотиазолидинил, C1-4алкилпиперазинил, остаток -SO2-, замещенный, в свою очередь, аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой, пиридиниламиногруппой, пиперидинилом или C1-4диалкиламино-C1-3алкиламино группой;
R2 означает водород;
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 означает фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
C3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4-алкил;
тиенил, незамещенный или замещенный галогеном, C1-4алкилом (который, в свою очередь, может быть замещен -СО2(C1-4алкилом), C2-4алкенилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом), C1-4-алкокси, пирролилом, пиридинилом или амино, который сам замещен -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
C2-8алкинил, замещенный фенилом;
амино, замещенный фенилом, который, в свою очередь, может быть замещен галогеном;
фурил, изоксазолил, пиридинил, дигидробензотиенил, тиазолил или тиадиазолил, причем тиазолил и тиадиазолил могут быть замещены C1-4алкилом;
или его фармацевтически приемлемые соли.
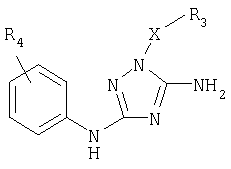
где
R4 выбирают из группы, включающей замещенную -SO2-(C1-4)алкилом аминогруппу, 1,2,4-триазолил, имидазолидинон, остаток -SO2-, замещенный, в свою очередь, аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой или C1-4диалкиламино-C1-3алкиламиногруппой; и
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 означает фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4-алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
С3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4алкил;
тиенил, не замещенный или замещенный галогеном; C1-4алкилом (который, в свою очередь, может быть замещен -СО2(C1-4)алкилом), C2-4алкенилом (который, в свою очередь, может быть замещен -СО2(C1-4)алкилом), C1-4алкокси, или амино, который сам замещен -C(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
С3-8алкинил, замещенный фенилом;
или его фармацевтически приемлемые соли.

где
R4 выбирают из группы, включающей
замещенную -SO2-(C1-4)алкилом аминогруппу
-SO2-, замещенный, в свою очередь, аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой или C1-4диалкиламино-C1-3алкиламиногруппой;
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 выбирают из группы, включающей
фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, гидрокси-C1-4-алкил, амино или C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
C3-7циклоалкил, не замещенный или замещенный 1-2 группами C1-4-алкил;
тиенил, не замещенный или замещенный галогеном; C1-4алкилом (который, в свою очередь, может быть замещен -СО2(C1-4)алкилом), С2-4алкенилом (который, в свою очередь, может быть замещен -CO2(C1-4)алкилом); C1-4алкокси; или амино, который сам замещен -С(O)(C1-4)алкилом;
C1-4алкил, замещенный тиенилом или фенилом, который, в свою очередь, замещен галогеном;
С2-8алкинил, замещенный фенилом;
или его фармацевтически приемлемые соли.

где
R4 означает остаток -SO2-, замещенный аминогруппой, C1-4алкиламиногруппой, C1-4диалкиламиногруппой, или C1-4-диалкиламино-C1-3-алкиламиногруппой;
Х выбирают из группы, включающей -С(O)-, -C(S)- и -SO2-; и
R3 означает фенил, необязательно замещенный 1-3 заместителями, независимо выбираемыми из группы, включающей галоген и нитро, или 1-2 заместителями, независимо выбираемыми из группы, включающей C1-4алкокси, -СН(ОН) (C1-3)алкил и C1-4алкил, не замещенный или замещенный 1-3 атомами галогена при концевом атоме углерода;
С3-7 циклоалкил, не замещенный или замещенный 1-2 группами C1-4-алкил;
тиенил, не замещенный или замещенный галогеном, C1-4алкокси или C1-4алкилом;
или их фармацевтически приемлемые соли.
5-амино-3-[[4-(аминосульфонил)фенил]амино]-N-(2,6-дифторфенил)-1Н-1,2,4-триазол-1-карботиоамид;
5-амино-3-[[4-(аминосульфонил)фенил]амино]-N-(2,6-дифторфенил)-1Н-1,2,4-триазол-1-карбоксамид;
4-[[5-амино-1-(2-хлор-6-фторбензоил)-1Н-1,2,4-триазол-3-ил]амино]бензолсульфонамид;
4-[[5-амино-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]-N-метилбензолсульфонамид;
4-[[5-амино-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]-N-[2-(диметиламино)этил]бензолсульфонамид;
1-[4-[[5-амино-1-[(3-метил-2-тиенил)карбонил]-1Н-1,2,4-триазол-3-ил]амино]фенил]-2-имидазолидинон.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Устройство для нанесения клея | 1978 |
|
SU710654A1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛИЛГИДРАЗИДА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИГОДНЫЕ СОЛИ | 1990 |
|
RU2039051C1 |
| ПРОИЗВОДНЫЕ 1,2,4-ТРИАЗОЛИЛТИОАМИДОВ | 1990 |
|
RU2045521C1 |
Авторы
Даты
2006-04-20—Публикация
2001-12-21—Подача