Изобретение относится к медицине, в частности к фармации, хирургии и оториноларингологии.
Наиболее близкой лекарственной формой является порошок цефазолина для приготовления инъекционного раствора, который применяют внутримышечно или внутривенно (струйно или капельно). Для профилактики послеоперационных инфекционных осложнений цефазолин назначают 1,0 г за 30 мин до операции, 0,5-1,0 г во время операции и по 0,5-1,0 г каждые 6-8 ч в течение суток после операции. Продолжительность лечения составляет 7-10 дней. Расход цефазолина от 3,5 до 42 г [Пискунов Г.З., Пискунов С.З. Лекарственные средства, применяемые в оториноларингологии. - М.: ЗАО "Финстатинформ", 2000. - С.33-34; Машковский М.Д. Лекарственные средства: Пособие для врачей: В 2 т. - Т.2. - Изд. 14-е, перераб. и доп. - М.: Новая волна, 2000. - 608 с.; Белоусов Ю.Б., Ушкалова Е.А. Формулярная система в антибиотикотерапии // Антибиотики и химиотерапия. - 2001. - Т.46. - №11. - С.23-35].
Указанная лекарственная форма цефазолина имеет недостатки: побочные явления со стороны жизненно важных систем организма, тошнота, рвота, диарея, боли в эпигастральной области, псевдомембранозный колит, кандидомикоз, нарушение функции почек, повышение концентрации печеночных ферментов (ACT, АЛТ, щелочная фосфатаза, ЛДГ) в крови, изменения картины периферической крови (обратимая лейкопения, нейтропения, тромбоцитопения, агранулоцитоз, лимфоцитоз, гемолитическая анемия), аллергические проявления (кожные высыпания, зуд, токсический эпидермальный некроз, многоформная эритема, лихорадка; отек Квинке, артралгии, анафилактический шок). Возможна болезненность в месте внутримышечного введения, образование инфильтратов, абсцессов, флебитов и тромбофлебитов [Пискунов Г.З., Пискунов С.З. Лекарственные средства, применяемые в оториноларингологии. - М.: ЗАО "Финстатинформ", 2000. - С.33-34; Машковский М.Д. Лекарственные средства: Пособие для врачей: В 2 т. - Т.2. - Изд. 14-е, перераб. и доп. - М.: Новая волна, 2000. - 608 с.; Регистр лекарственных средств России. 8-е изд., перераб. и доп. / Гл. ред. Ю.Ф.Крылов. - М.: РЛС-2001, 2001. - 1503 с.].
Таким образом, основными недостатками раствора цефазолина, вводимого внутривенно или внутримышечно, является побочное действие и значительный расход антибиотика.
Задачей изобретения является расширение ассортимента лекарственных форм цефазолина для профилактики послеоперационных инфекционных осложнений в оториноларингологии.
Поставленная задача достигается тем, что иммобилизованная форма, кроме цефазолина, содержит натрий-карбоксиметилцеллюлозу и глицерин при следующем соотношении компонентов, мас.%:
Изобретение поясняется следующими таблицами и чертежом.
Таблица 1. Влияние цефазолина в полимерных матрицах на транспортную функцию мерцательного эпителия слизистой оболочки полости носа.
Таблица 2. Антимикробная активность полимерных матриц с цефазолином.
Таблица 3. Влияние температуры сушки на стабильность полимерных матриц с цефазолином.
Таблица 4. Стабильность иммобилизованной формы цефазолина в процессе хранения при (4±2)°С.
Таблица 5. Влияние иммобилизованной формы цефазолина на регрессию симптомов воспаления слизистой оболочки носа в послеоперационном периоде.
Чертеж. Высвобождение цефазолина из полимерных матриц.
Введение в состав иммобилизованной формы цефазолина натрий-карбоксиметилцеллюлозы позволяет снизить токсичность цефазолина, увеличить время и степень его высвобождения из лекарственной формы и, следовательно, повысить эффективность.
Для увеличения эластичности полимерных матриц в их состав введен глицерин.
Характеристика объектов:
Цефазолин* (Cefazolin*)-(6R-транс)-3-[(5-метил-1,3,4-тиадиазол-2-ил)-тиометил]-8-оксо-7-[(1Н-тетразол-1-ил-ацетил)амино]-5-тио-1-азабицикло[4.2.0.]окт-2-ен-2-карбоновая кислота (и в виде натриевой соли). Синонимы: Цефазолина натриевая соль, Цефазолин натрия (Cefazolinum-natrium) АБОЛмед (Россия) (ФС 42-3477-98), Анцеф (Ancef), Вулмизолин (Vulmizolin), Кефзол (Kefzol), Интразолин (Intrazoline) и др. Лиофилизированный порошок белого или белого с желтоватым оттенком цвета. Растворим в воде, в изотоническом растворе натрия хлорида и 5% растворе глюкозы, очень мало растворим в спирте этиловом. Фармакологическое действие - антибактериальное, бактерицидное. Имеет широкий спектр антимикробного действия: активен в отношении как грамположительных (стафилококки, не продуцирующие и продуцирующие пенициллиназу; зеленящие и гемолитические стрептококки группы А, пневмококки, палочки дифтерии, сибирской язвы), так и грамотрицательных микроорганизмов (менингококки, гонококки, шигеллы, сальмонеллы, кишечная палочка, клебсиеллы, протей и др.). Цефазолин препятствует образованию бактериальной стенки путем конкурентного блокирования ферментов, участвующих в синтезе мукопептида, входящего в состав клеточной мембраны. Период полувыведения 1,8 ч при внутривенном и 2 ч после внутримышечного введения, максимальная концентрация в крови достигается через 1 ч. Связывается с белками плазмы на 80%, не биотрансформируется, экскретируется почками [Регистр лекарственных средств России. Энциклопедия лекарств. 8-е изд., переработанное и дополненное. / Гл. ред. Ю.Ф.Крылов / М.: "РЛС-2001". - 2001. - 1504 с.; Государственный реестр лекарственных средств / МЗ РФ. - М., 1998. - 1004 с.]. Выбранное количество цефазолина обусловлено отсутствием негативного влияния на транспортную активность мерцательного эпителия слизистой оболочки полости носа и оптимальной антимикробной активностью при местном введении (табл.1 и 2).
Натрий-карбоксиметилцеллюлоза (Na-КМЦ) представляет собой натриевую соль простого эфира целлюлозы и гликолевой кислоты. Это белый или слегка желтоватый порошкообразный продукт без запаха. Кроме Na-КМЦ отечественного производства в настоящее время применяется Na-КМЦ производства голландской фирмы Hercules Blanose Cellulose Gum Type 7M31CF (Blanose), представляющая собой гранулированный продукт. Na-КМЦ растворима в горячей и холодной воде, 50% водном растворе этанола, образует высоковязкие водные растворы. Na-КМЦ физиологически инертна и не оказывает раздражающего действия. Na-КМЦ в фармацевтической практике применяют в качестве пролонгатора действия лекарственных веществ в глазных каплях и инъекционных растворах, эмульгатора, связывающего и разрыхляющего средства в производстве таблеток, основы лекарственных пленок [Полимеры в фармации / А.И.Тенцова, М.Т.Алюшин. - М.: Медицина, 1985. - С.10-20]. Na-КМЦ и Blanose обеспечивают максимальное, равномерное растворение и высвобождение цефазолина из полимерной матрицы по сравнению с метилцеллюлозой (МЦ) и оксипропилметилцеллюлозой (ОПМЦ) (см.чертеж), стабильность в процессе хранения (табл.4) и, следовательно, повышают терапевтический эффект. В полимерных композициях цефазолина с ОПМЦ и МЦ в процессе сушки происходит деструкция антибиотика, о чем свидетельствуют изменение цвета, сдвиг максимума поглощения, значительное снижение зон угнетения роста тест-микроорганизма и количественного содержания (табл.3). Выбранные количества Na-КМЦ и Blanose обусловлены тем, что при концентрации ниже 2 мас.% снижается прочность полимерной матрицы и время контакта со слизистой оболочкой, а при содержании более 4 мас.% образующийся при растворении матрицы гель снижает транспортную активность мерцательного эпителия слизистой оболочки полости носа.
Введение в полимерную матрицу 1,5-2,5 мас.% глицерина (ФС 42-2202-99) обеспечивает эластичность и прочность матриц (табл.4).
Таким образом, оптимальной иммобилизованной формой цефазолина является полимерная матрица из 2-4 мас.% натрий-карбоксиметилцеллюлозы, содержащая 0,5-2,0 мас.% цефазолина и 1,5-2,5 мас.% глицерина.
Для предлагаемого состава с учетом свойств входящих ингредиентов установлена оптимальная температура сушки полимерной композиции (30°С), которая позволяет сохранить антимикробную активность, количественное содержание антибиотика в пределах нормы, и разработана технология изготовления (с постадийным контролем качества), которая состоит из следующих этапов.
1. Санитарная обработка производства. Подготовка помещения, персонала, вспомогательных материалов, оборудования, сырья.
2. Получение лекарственной композиции.
2.1. Приготовление раствора натрий-карбоксиметилцеллюлозы и глицерина в части воды очищенной.
2.2. Растворение цефазолина в оставшейся части воды очищенной.
2.3. Смешивание раствора полимера с раствором антибиотика.
2.4. Деаэрация.
3. Получение полимерной матрицы.
3.1. Розлив лекарственной композиции на подложки.
3.2. Сушка.
3.3. Дозирование.
4. Фасовка и упаковка полимерных матриц.
Пример по способу получения.
С целью повышения стабильности полимерные матрицы готовят в асептических условиях в соответствии с требованиями нормативной документации с использованием стерильной посуды. Навеску Na-КМЦ (или Blanose) заливают частью стерильной воды очищенной, нагретой до 50-70°С, и периодически перемешивают до растворения полимера, добавляют глицерин. Цефазолин растворяют в оставшемся количестве стерильной воды и тщательно смешивают с охлажденным до (20±2)°С раствором полимера до однородности. После деаэрации однородную полимерную лекарственную композицию разливают на подложки и сушат при температуре (30±3)°С в течение 5-6 часов. Высушенные полимерные матрицы снимают с подложек, дозируют и упаковывают в стерильные стеклянные флаконы из дрота для лекарственных средств (ТУ 62-2-1077) (стекло НС-1), укупоривают резиновыми пробками марки ИР-119 (ТУ 38-006108-90) и металлическими колпачками "под обкатку". Флаконы помещают в картонные коробки. Хранят при температуре (4±2)°С в защищенном от света месте (в холодильнике) в течение 12 (24) месяцев (табл.4).
Снижение токсичности и повышение эффективности цефазолина в иммобилизованной форме при профилактике послеоперационных инфекционных осложнений подтверждено результатами применения (таблица 5).
Методика применения иммобилизованной формы цефазолина.
На поверхность слизистой оболочки нижней носовой раковины и перегородки носа укладывали полимерные матрицы с цефазолином размером 2×1 см, на среднюю носовую раковину - матрицы размером 1,5×1 см. Первое введение полимерных матриц с цефазолином осуществляли за 2 часа до операции. После удаления тампонов через сутки после операции введение иммобилизованной формы цефазолина производили ежедневно один раз в сутки в течение 5-6 дней. Не выявлено аллергических реакций, воспаления и изъязвления слизистых оболочек полости носа.
Пример по способу использования.
Больному М., 25 лет, история болезни №1348 18.02.04 г., выполнена подслизистая резекция перегородки носа, двухсторонняя подслизистая вазотомия. После удаления тампонов из полости носа на следующие сутки введена иммобилизованная форма цефазолина по изложенной выше методике. Введение цефазолина осуществлялось в течение 4 дней. Уже через сутки у пациента при риноманометрии отмечалась достаточная степень носового дыхания, отсутствовали воспалительные явления, не отмечалось избыточной продукции носового секрета, поверхностная температура слизистой оболочки приближалась к контрольным показателям, отсутствовала необходимость использования деконгенсантов.
Для выявления влияния полимера-носителя на терапевтическую активность иммобилизованной формы цефазолина группе пациентов после операции в левую половину носа вводили полимерные матрицы цефазолина из Blanose, в правую - из Na-КМЦ. Различий в течении послеоперационного периода не установлено. Регрессия симптомов воспаления была одинакова в обеих половинах носа, что свидетельствует об одинаковой активности полимерных матриц из Na-КМЦ и Blanose.
Таким образом, предлагаемая иммобилизованная форма цефазолина обладает высокой терапевтической эффективностью, низкой токсичностью в отношении тканей слизистой оболочки полости носа и экономичностью. Расход антибиотика на курс лечения 0,2-0,8 г. Разработан оптимальный способ изготовления иммобилизованной формы цефазолина, исключающий изменения структуры и физико-химических свойств лекарственного вещества.
Предлагаемая иммобилизованная форма цефазолина позволяет расширить ассортимент имеющихся лекарственных средств для профилактики послеоперационных инфекционных осложнений.
в полимерной матрице, мас.%
слизистой оболочки полости носа
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАГИНАЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2347568C1 |
| ИММОБИЛИЗОВАННАЯ ФОРМА ДОКСОРУБИЦИНА | 2003 |
|
RU2262923C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОЖОГОВ (ВАРИАНТЫ) И СПОСОБ ЕЕ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2006 |
|
RU2317811C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОСТРЫХ ЖЕЛУДОЧНО-КИШЕЧНЫХ БОЛЕЗНЕЙ НОВОРОЖДЕННЫХ ТЕЛЯТ | 2020 |
|
RU2740602C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БОЛЕЗНЕЙ ОРГАНОВ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2000 |
|
RU2181583C1 |
| КОМПОЗИЦИЯ ДЛЯ ИЗОЛИРОВАНИЯ КИШЕЧНОГО АНАСТАМОЗА И ПРЕДОТВРАЩЕНИЯ ПОСЛЕОПЕРАЦИОННОГО СПАЕЧНОГО ПРОЦЕССА | 2022 |
|
RU2796007C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ МЕСТНЫХ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ КОЖИ И СЛИЗИСТЫХ ОБОЛОЧЕК | 2001 |
|
RU2235535C2 |
| ЛЕКАРСТВЕННАЯ КОМПОЗИЦИЯ С РЕГЕНЕРАТИВНЫМИ И АНТИБАКТЕРИАЛЬНЫМИ СВОЙСТВАМИ ДЛЯ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ В РИНОЛОГИИ | 2022 |
|
RU2792597C1 |
| ПЛЕНКООБРАЗУЮЩЕЕ АНТИСЕПТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ | 2009 |
|
RU2410092C1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ | 2011 |
|
RU2481835C2 |
Изобретение относится к фармацевтике, в частности к иммобилизованной форме цефазолина. Изобретение заключается в том, что иммобилизованная форма цефазолина представляет собой цефазолин, заключенный в полимерную матрицу из натрий-карбоксиметилцеллюлозы. Изобретение обеспечивает сокращение срока лечения на три дня. 5 табл., 1 ил.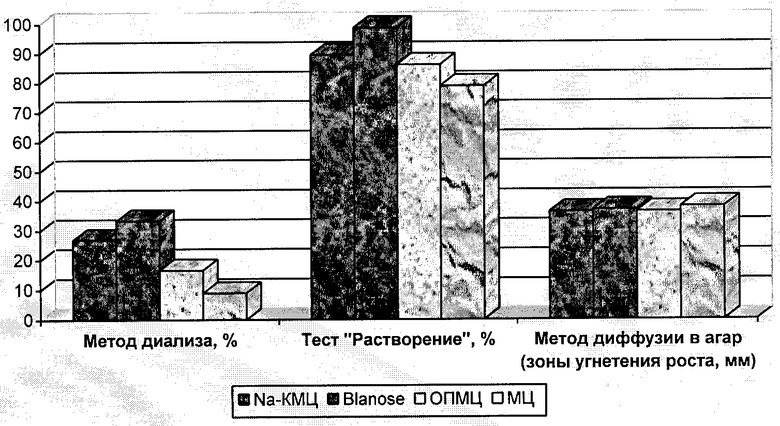
Средство для профилактики послеоперационных инфекционных осложнений в оториноларингологии, содержащая цефазолин, полимер и глицерин, отличающееся тем, что цефазолин заключен в полимерную матрицу из натрий-карбоксиметилцеллюлозы при следующем соотношении компонентов, мас.%:
| БИОАДГЕЗИВНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ (ВАРИАНТЫ), УСТРОЙСТВО ДЛЯ ДОСТАВКИ ЧЕРЕЗ СЛИЗИСТУЮ ОБОЛОЧКУ АКТИВНОГО АГЕНТА, СПОСОБ ПРОЛОНГИРОВАННОГО МЕСТНОГО ВВЕДЕНИЯ ОДНОГО ИЛИ БОЛЕЕ АКТИВНЫХ АГЕНТОВ СУБЪЕКТУ (ВАРИАНТЫ) И СПОСОБ СОКРАЩЕНИЯ ВРЕМЕНИ, ТРЕБУЕМОГО ДЛЯ ПРИКЛЕИВАНИЯ КОМПОЗИЦИИ К СЛИЗИСТОЙ ТКАНИ | 1998 |
|
RU2234337C2 |
| КОМПОЗИЦИИ МАТРИКСНЫХ ПРОТЕИНОВ ДЛЯ ЗАЛЕЧИВАНИЯ РАН | 1999 |
|
RU2241489C2 |
| СПОСОБ УЛУЧШЕНИЯ СЛУХА ПРИ ТИМПАНОСКЛЕРОЗЕ | 2002 |
|
RU2223084C1 |
| ПИСКУНОВ Г.З., ПИСКУНОВ С.З., ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ В ОТОРИНОЛАРИНГОЛОГИИ, МОСКВА, ЗАО "ФИНСТАТИНФОРМ", 2000, с.33-34. | |||
Авторы
Даты
2006-06-20—Публикация
2004-09-21—Подача