Описание
Предпосылки изобретения
Настоящее изобретение относится к способу удаления примесей из рацемической смеси цис-изомеров соединения формулы I - цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, (далее "рацемический лазофоксифен" или "рацемат")
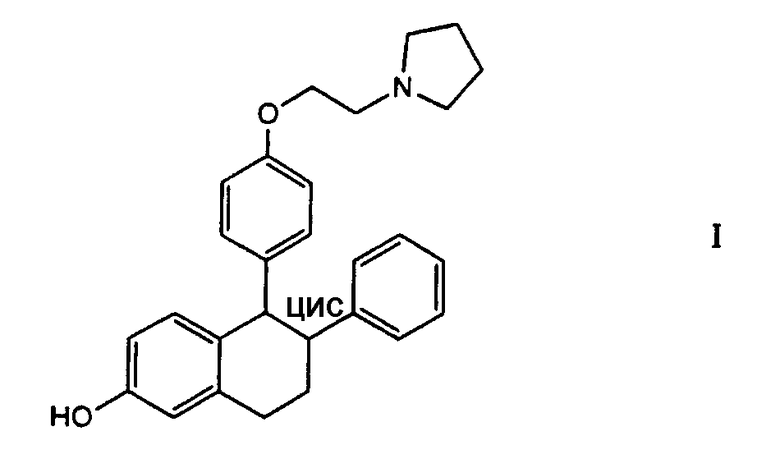
Данное изобретение относится также к очищенному рацемическому лазофоксифену, т.е. цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-олу, (далее "очищенный рацемический лазофоксифен" или "очищенный рацемат"), и очищенному D-тартрату лазофоксифена, или D-тартрату (-)цис-6(S)-фенил-5(R)-[4-(2-пирролидин-1-ил-этокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, который полезен как агонист/антагонист эстрогена, известный так же как селективный модулятор рецепторов эстрогена, ("SERM"). Рацемический лазофоксифен является промежуточным соединением в синтезе D-тартрата лазофоксифена, имеющего следующую структуру:
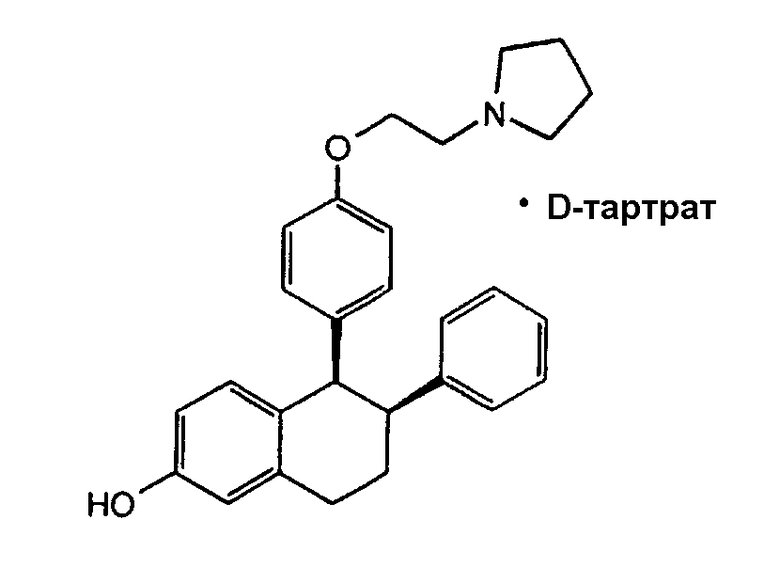
Лазофоксифен, D-тартрат лазофоксифена, его рацемат и способы их получения раскрыты в общедоступном патенте США № 5552412, опубликованном 3 сентября 1996, и патенте США № 5948809, опубликованном 7 сентября 1999. Текст этих патентов и всех других ссылок, указанных в этом описании, включен сюда посредством ссылки во всей их полноте.
Обычно лекарственные субстанции предпочтительно содержат менее 0,2% примесей, наиболее предпочтительно менее 0,1% примеси. Однако при переходе на промышленное производство D-тартрата лазофоксифена было определено, что получающееся соединение D-тартрат лазофоксифена содержит нежелательные примеси в количестве более 0,2%. Было также определено, что очистка D-тартрата лазофоксифена до менее чем 0,1% примесей в таком масштабе была технически неосуществимой.
Следовательно, имелась потребность в получении соединения, являющегося промежуточным для D-тартрата лазофоксифена, имеющего чистоту менее 0,1% примесей. Эту проблему разрешает способ, описанный в рамках настоящего изобретения.
Краткое содержание изобретения
Данное изобретение направлено на способ очистки рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, который включает:
a) внесение рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола в смесь этанола и тетрагидрофурана с образованием суспензии;
b) перемешивание и нагрев указанной суспензии;
c) охлаждение указанной суспензии со стадии (b); и
d) сбор твердого очищенного рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола.
В предпочтительном варианте исполнения указанная смесь этанола и тетрагидрофурана имеет объемное отношение примерно 4:1.
В другом предпочтительном варианте исполнения указанная смесь этанола и тетрагидрофурана имеет объемное отношение примерно 3:1.
В более предпочтительном варианте исполнения указанная смесь этанола и тетрагидрофурана имеет объемное отношение примерно 2:1.
В более предпочтительном варианте исполнения указанная смесь этанола и тетрагидрофурана имеет объемное отношение примерно 1:1.
В предпочтительном варианте исполнения указанную суспензию, образованную на стадии (a), на стадии (b) перемешивают и нагревают от комнатной температуры до приблизительно 70°C.
В другом предпочтительном варианте исполнения указанную суспензию, образованную на стадии (a), перемешивают и нагревают от комнатной температуры до приблизительно 65°C в течение от примерно 30 минут до примерно 12 часов (b).
В предпочтительном варианте исполнения суспензию, образованную таким образом на стадии (b), на стадии (c) охлаждают и перемешивают в течение от примерно 30 минут до примерно 18 часов.
В другом предпочтительном варианте исполнения указанную суспензию, полученную таким образом на стадии (c), собирают путем фильтрации, получая очищенный рацемический цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол, содержащий менее 0,1% примесей.
В другом аспекте изобретение направлено на очищенный рацемический цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол.
Используемый здесь термин "комнатная температура" означает температуру 15-25°C.
Используемые здесь термины "неочищенный рацемический лазофоксифен" или "рацемат" означают рацемическую смесь цис-изомеров цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола до проведения процесса очистки (т.е. сболее 0,1 % примесей).
Используемые здесь термины "очищенный рацемат лазофоксифена" или "очищенный рацемат" означают рацемический цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол, содержащий менее 0,1% примесей.
Используемый здесь термин "очищенный D-тартрат лазофоксифена" означает D-тартрат (-)цис-6(S)-фенил-5(R)-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол, содержащий менее 0,2% примесей.
Подробное описание схемы I изобретения
Лазофоксифен является ценным антагонистом эстрогена и полезен, помимо прочего, для оральной контрацепции; для облегчения симптомов менопаузы; для предотвращения угрожающего или привычного выкидыша; для облегчения дисменореи, для облегчения дисфункционального маточного кровотечения; для облегчения эндометриоза; для содействия развитию; для лечения прыщей (акне); для уменьшения чрезмерного роста волос на теле у женщин (гирсутизм); для предупреждения и лечения сердечно-сосудистых заболеваний; для предупреждения и лечения артериосклероза; для предупреждения и лечения остеопороза; для лечения доброкачественной аденомы предстательной железы и ожирения при раке простаты и для подавления послеродовой лактации.
Лазофоксифен также оказывает благоприятное влияние на уровень липидов в плазме и поэтому полезен для лечения и профилактики гиперхолестеринемии. Хотя лазофоксифен является агонистом эстрогена в костях, он является антиэстрогеном в тканях молочной железы и поэтому может быть полезным при лечении и предупреждении рака молочной железы.
Рацемический лазофоксифен является цис-рацематом лазофоксифена, содержащим два асимметричных атома углерода, соответствующих двум оптически активным соединениям. Разрешение рацемата было проведено путем кристаллизации соли с гидрофосфатом R-(-)-1,1'-бинафтил-2,2'-диила ("R-бинафт"), как описано в общедоступном патенте США № 5552412. Разрешение рацемата было также выполнено путем добавления D-винной кислоты в рацемический или частично оптически обогащенный цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)-5,6,7,8-тетрагидронафталин-2-ол с образованием соли в соотношении 1:1 в водном растворе этанола, как описано в патенте США № 5948809. После охлаждения (-) изомер отделяли в виде твердого вещества и собирали, получая желаемую фармацевтически приемлемую соль изомера (-)цис-D-тартрата с высоким выходом.
Для снижения количества примесей в D-тартрате лазофоксифена до менее чем 0,2% было исследовано несколько методов очистки, включая рекристаллизацию и хроматографию. Эти методы были неудовлетворительными либо из-за низкого выхода, либо из-за недостаточной чистоты D-тартрата лазофоксифена. Было определено, что желаемый уровень очистки (менее 0,1%) и оптимальный выход получаются способами очистки, описанными в данной заявке.
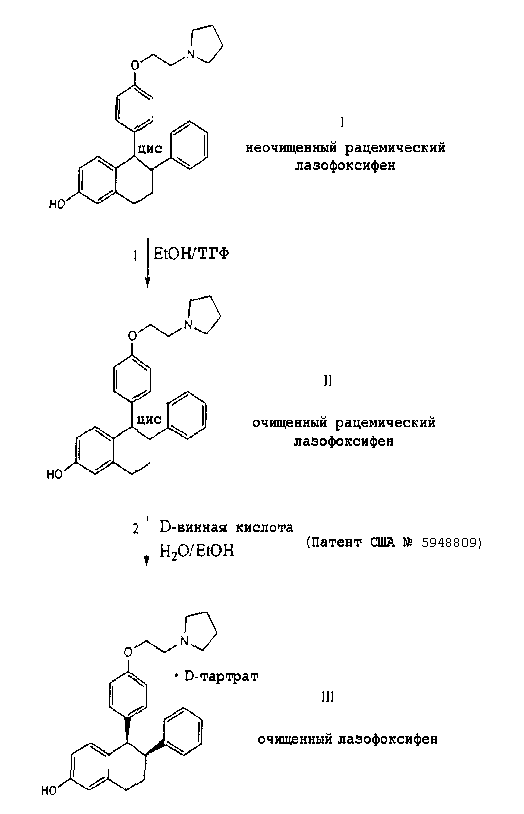
Как показано на схеме I и в примерах, на стадии 1(a) неочищенный рацемический лазофоксифен соединяют со смесью этанола и тетрагидрофурана. Специалисты, обладающие обычными познаниями в данной области техники, поймут, что отношение этанола к тетрагидрофурану можно менять. Предпочтительно, однако, чтобы объемное отношение составляло от 1:1 до 4:1.
На стадии 1(b) полученную суспензию нагревают от комнатной температуры до примерно 70°C и перемешивают в течение от примерно 30 минут до примерно 12 часов. Предпочтительно, однако, суспензию перемешивают от примерно 8 до примерно 12 часов. Специалист средних знаний в данной области техники поймет, что длительность перемешивания данной суспензии может быть более 12 часов. На стадии 1(c) нагретую суспензию охлаждают затем до примерно комнатной температуры при перемешивании в течение от примерно 30 минут до примерно 18 часов. Наконец, на стадии 1(d) твердое вещество может быть собрано средствами, известными специалисту в данной области (например, фильтрацией), промыто подходящим растворителем (например, этанолом) и высушено (например, в вакууме), давая в результате очищенный рацемический лазофоксифен.
Очищенный рацемический лазофоксифен может быть растворен, как показано на стадии II и описано в патенте США № 5948809, с получением очищенного D-тартрата лазофоксифена.
Специалист средней квалификации в данной области техники поймет, что отношения этанола к тетрагидрофурану, температура, длительность нагревания и перемешивания могут меняться. Эти изменения находятся в рамках данного изобретения.
Примеры
Примеры ниже предназначены для иллюстрации частных вариантов исполнения изобретения и не имеют целью каким-либо образом ограничить подробное описание, в том числе формулу изобретения.
Пример 1
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 2:1
60 граммов неочищенного рацемического лазофоксифена соединяли со 150 мл этанола и 76,8 мл тетрагидрофурана. Полученную суспензию нагревали до примерно 65-70°C и перемешивали в течение примерно 3 часов, охлаждали до комнатной температуры и дополнительно перемешивали около 18 часов. Твердое вещество собирали фильтрованием, дважды промывали 25 мл этанола и сушили в вакуумепри 45°C с получением 49,36 граммов очищенного рацемического лазофоксифена (выход 82,3%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью высокоэффективной жидкостной хроматографии (далее "ВЭЖХ") с обращенной фазой, используя ВЭЖХ-систему с ультрафиолетовым ("УФ") детектором, установленным на 230 нм, и колонку Symmetry c картриджем C18 (длиной 50 мм и внутренним диаметром 3,9 мм при 40°C). Подвижная фаза состояла из следующих компонентов в объемных отношениях 1400:600:5:4 вода: ацетонитрил: трифторуксусная кислота: гидроксид аммония, и имела pH 3,0 при скорости потока 2,0 мл/мин. Время удержания рацемического лазофоксифена составляет 5,7 минут. Результаты сведены в таблицу 1 и даны в процентах (%) площади пиков.
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 2
Крупномасштабная очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 2:1
24,9 килограммов неочищенного рацемического лазофоксифена соединяли с 62 литрами этанола и 31 литром тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 12 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 22 литрами этанола и сушили в вакууме при температуре около 45°C с получением 20,5 кг очищенного рацемического лазофоксифена (выход 82,3%).
Профиль распределения примесей неочищенного и очищенного лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 2 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 3
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 2:1
8,14 граммов неочищенного рацемического лазофоксифена соединяли с 20 мл этанола и 10 мл тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали в течение примерно двух часов. Твердое вещество собирали фильтрованием, промывали 2 мл этанола и сушили в вакууме при температуре около 40°C с получением 6,81 граммов очищенного рацемического лазофоксифена (выход 83,7%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 3 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 4
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 2:1
8,2 граммов неочищенного рацемического лазофоксифена соединяли с 41,1 мл этанола и 20,6 мл тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 2 мл этанола и сушили в вакууме при температуре около 40°C с получением 6,76 граммов очищенного рацемического лазофоксифена (выход 82,5%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 4 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 5
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-
5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 2:1
8,2 граммов неочищенного рацемического лазофоксифена соединяли с 13,7 мл этанола и 6,8 мл тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 2 мл этанола и сушили в вакууме при температуре около 40°C с получением 7,65 граммов очищенного рацемического лазофоксифена (выход 93,3%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 5 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 6
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 1:1
4,0 грамма неочищенного рацемического лазофоксифена соединяли с 7,5 мл этанола и 7,5 мл тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 0,5 мл этанола и сушили в вакууме при температуре около 40°C с получением 3,31 граммов очищенного рацемического лазофоксифена (выход 82,8%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 6 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 7
Очистка цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола смесью этанол:тетрагидрофуран 5:1
4,0 грамма неочищенного рацемического лазофоксифена соединяли с 12,5 мл этанола и 2,5 мл тетрагидрофурана. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 0,5 мл этанола и сушили в вакууме при температуре около 40°C с получением 3,69 граммов очищенного рацемического лазофоксифена (выход 92,3%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 7 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 8
Попытка очистки цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола этанолом
4,0 грамма неочищенного рацемического лазофоксифена соединяли с 15 мл этанола. Полученную суспензию нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около двух часов. Твердое вещество собирали фильтрованием, промывали 0,5 мл этанола и сушили в вакууме при температуре около 40°C с получением 3,31 грамма очищенного рацемического лазофоксифена (выход 82,8%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 8 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 9
Рекристаллизация цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола тетрагидрофураном
4,0 грамма неочищенного рацемического лазофоксифена соединяли с 15 мл тетрагидрофурана. Полученный раствор нагревали до 60-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры, при которой кристаллизация не происходила. Кристаллизация начиналась после использования затравки. Суспензию перемешивали при комнатной температуре в течение примерно двух часов. Твердое вещество собирали фильтрованием, промывали 0,5 мл этанола и сушили в вакууме при температуре около 40°C с получением 2,65 г продукта (выход 66,3%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена определяли по ВЭЖХ, как описано выше. Результаты сведены в таблицу 9 и даны в процентах (%).
Процент примесей в неочищенном и очищенном рацемическом лазофоксифене
Пример 10
Попытка очистки D-тартрата лазофоксифена, т.е. D-тартрата (-)цис-6(S)-фенил-5(R)-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, рекристаллизацией из смеси этанол/вода
8,28 граммов неочищенного D-тартрата лазофоксифена растворяли в 166 мл смеси этанола и воды 1:1 путем нагревания до примерно 50°C. После фильтрования раствор медленно охлаждали до температуры примерно 0°C, при которой начинается кристаллизация. Смесь перемешивали при комнатной температуре около 48 часов. Твердое вещество собирали фильтрованием и дважды промывали 10 мл этанола. Затем его сушили в вакууме при температуре около 45°C с получением 6,37 граммов очищенного D-тартрата лазофоксифена (выход 76,9%).
Профиль распределения примесей неочищенного и очищенного D-тартрата лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 10 и даны в процентах (%).
Процент примесей в неочищенном и очищенном D-тартрате лазофоксифена
Пример 11
Крупномасштабная очистка неочищенного рацемического лазофоксифена, т.е цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, смесью этанол/тетрагидрофуран
20,4 килограммов неочищенного рацемического лазофоксифена соединяли с 50 литрами этанола и 25 литрами тетрагидрофурана. Полученную суспензию нагревали до 55-65°C и перемешивали в течение примерно 8 часов, охлаждали до комнатной температуры и дополнительно перемешивали около четырех часов. Твердое вещество собирали фильтрованием, дважды промывали 40 литрами этанола и сушили в вакууме при температуре около 40°C с получением 16,8 килограммов очищенного рацемического лазофоксифена (выход 82,3%).
Профиль распределения примесей неочищенного и очищенного рацемического лазофоксифена анализировали с помощью ВЭЖХ, как описано выше. Результаты сведены в таблицу 11 и даны в процентах (%).
Процент примесей в неочищенном и очищенном лазофоксифене
| название | год | авторы | номер документа |
|---|---|---|---|
| D-ТАРТРАТ(-)ЦИС-6(S)-ФЕНИЛ-5(R)-[4-(2-ПИРРОЛИДИН-1-ИЛЭТОКСИ)ФЕНИЛ]-5,6,7,8 -ТЕТРАГИДРОНАФТАЛИН-2-ОЛА, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ ПРЕДОТВРАЩЕНИЯ СОСТОЯНИЙ, ПОДДАЮЩИХСЯ ВОЗДЕЙСТВИЮ АГОНИСТОВ ЭСТРОГЕНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2162465C2 |
| СОЕДИНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ЭНДОМЕТРИОЗА И ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ | 1996 |
|
RU2130454C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-1-{2-[4-(6-МЕТОКСИ-2-ФЕНИЛ-1,2,3,4-ТЕТРАГИДРОНАФТАЛИН-1-ИЛ)ФЕНОКСИ]ЭТИ Л}ПИРРОЛИДИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2000 |
|
RU2195445C2 |
| СТИМУЛЯТОРЫ СЕКРЕЦИИ ГОРМОНА РОСТА | 1996 |
|
RU2172742C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И НАБОР ДЛЯ ЛЕЧЕНИЯ ПОНИЖЕННОЙ КОСТНОЙ МАССЫ (ВАРИАНТЫ) | 1996 |
|
RU2190395C2 |
| 8-ЗАМЕЩЕННЫЕ-2-АМИНОТЕТРАЛИНОВЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ИЗ ПОЛУЧЕНИЯ | 1990 |
|
RU2093507C1 |
| ИНГИБИТОРЫ БЕЛКОВЫХ ТИРОЗИНФОСФАТАЗ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2833220C2 |
| НОВЫЕ СОЛИ МОРФОЛИНОБЕНЗАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 2000 |
|
RU2237668C2 |
| ЗАМЕЩЕННЫЕ АМИНОИНДАНЫ И ИХ АНАЛОГИ, И ИХ ПРИМЕНЕНИЕ В ФАРМАЦЕВТИКЕ | 2009 |
|
RU2522586C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗОПИРАН-2-ОЛА | 2007 |
|
RU2397163C2 |
Изобретение относится к способу очистки рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола, который включает:
(a) суспендирование рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола в смеси этанола и тетрагидрофурана с образованием суспензии, где указанная смесь этанола и тетрагидрофурана имеет объемное отношение от 4:1 до 1:1;
(b) перемешивание и нагрев указанной суспензии;
(c) охлаждение указанной суспензии со стадии (b); и
(d) сбор твердого очищенного рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола. Способ обеспечивает получение продукта с примесями менее 0,1%. 2 н. и 9 з.п. ф-лы, 11 табл.
(a) суспендирование рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола в смеси этанола и тетрагидрофурана с образованием суспензии, где указанная смесь этанола и тетрагидрофурана имеет объемное соотношение от 4:1 до 1:1;
(b) перемешивание и нагрев указанной суспензии;
(с) охлаждение указанной суспензии со стадии (b) и
(d) сбор твердого очищенного рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола.
(a) суспендирование рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола в смеси этанола и тетрагидрофурана в объемном соотношении 2:1 с образованием суспензии;
(b) перемешивание и нагрев указанной суспензии от комнатной температуры до температуры, не превышающей 65°С, в течение до 12 ч;
(с) охлаждение полученной таким образом указанной суспензии при перемешивании до 18 ч и
(d) сбор твердого рацемического цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола путем фильтрования.
| US 5552412, 13.09.1996 | |||
| EP 1086692 A2, 28.03.2001 | |||
| US 5948809, 07.09.1999 | |||
| Способ получения производных бутирофенонпирролидина или их солей | 1973 |
|
SU548206A3 |
Авторы
Даты
2006-06-27—Публикация
2003-03-17—Подача